视网膜下切向针导管引导件和引入器的制作方法
优先权
本专利申请要求2014年6月6日提交的名称为“sub-retinaltangentialneedlecatheterguidewithintroducermechanism,andmethodofusingfordeliveryofbioactiveagents”的美国临时专利申请号62/008,756的优先权,该临时专利申请的公开内容以引用方式并入本文。
联合研究声明
本专利申请所公开的主题由联合研究合约的一方或多方开发或者代表联合研究合约的一方或多方,并且受权利要求书保护的发明由联合研究合约的一方或多方完成或者代表联合研究合约的一方或多方,所述联合研究合约在受权利要求书保护的发明的有效申请日或之前有效。受权利要求书保护的发明源自在联合研究合约的范围内从事的活动。联合研究合约的各方包括ethiconendo-surgery,inc.和janssenresearch&development,llc.。
背景技术:
人眼包括若干层。白色外层为巩膜,所述巩膜围绕脉络膜层。视网膜位于脉络膜层内部。巩膜包含为脉络膜和视网膜提供保护的胶原纤维和弹性纤维。脉络膜层包括为视网膜提供氧气和营养的脉管系统。视网膜包括光敏组织,所述光敏组织包括视杆和视锥。黄斑位于眼后部的视网膜的中心处,通常对中在穿过眼的晶状体和角膜的中心的轴线(即,视轴)上。黄斑提供中心视力,具体地讲通过视锥细胞。
黄斑变性为影响黄斑的医学病症,使得患有黄斑变性的人可经历丧失的或下降的中心视力同时保留一定程度的周边视力。黄斑变性可由多个因素引起,例如年龄(也称为“amd”)和遗传学因素。黄斑变性可以“干性”(非渗出性)形式产生,其中称为玻璃疣的细胞碎屑聚积在视网膜和脉络膜之间,从而导致地图状萎缩区域。黄斑变性也可以“湿性”(渗出性)形式产生,其中血管从视网膜后的脉络膜生长。尽管患有黄斑变性的人可保留一定程度的周边视力,但中心视力的丧失可对生活质量产生显著的负面影响。此外,保留的周边视力的质量可下降并且在一些情况下也可消失。因此,期望提供对黄斑变性的治疗以便阻止或消除由黄斑变性引起的视力丧失。在一些情况下,期望以高度集中方式提供此类治疗,例如通过将治疗物质递送到紧邻黄斑附近的地图萎缩区域的视网膜下层(视网膜的感觉神经层之上和视网膜色素上皮细胞之下)中。然而,由于黄斑位于眼的后部和视网膜的灵敏层下面,因此可难以通过实用方式触及黄斑。
尽管已研制和使用了治疗眼的多种外科方法和器械,但据信在本发明人之前还无人研制出或使用所附权利要求中描述的发明。
附图说明
尽管本说明书得出了具体地指出和明确地声明这种技术的权利要求,但是据信从下述的结合附图描述的某些示例将更好地理解这种技术,其中相似的参考数字指示相同的元件,并且其中:
图1示出了用于从脉络膜上途径进行治疗剂的视网膜下给药的示例性器械的透视图;
图2示出了图1器械的侧正视图;
图3示出了图1的器械的另一个侧正视图,其中锁定构件被移除;
图4示出了图1的器械的另一个侧正视图,其中致动构件朝远侧推进以使针从插管朝远侧延伸;
图5示出了可结合到图1的器械中的示例性插管的远侧端部的透视图;
图6示出了图5的插管的横截面视图,其中该横截面为沿图5的线6-6截取的;
图7示出了用于从脉络膜上途径进行治疗剂的视网膜下给药的另一个示例性另选器械的透视图;
图8示出了示例性缝合线测量模板的透视图,所述缝合线测量模板可用于从脉络膜上途径给药治疗剂的示例性方法中;
图9a示出了患者的眼的顶部平面图,其中眼的周围结构被固定并且枝形吊灯被安装;
图9b示出了图9a的眼的顶部平面图,其中图8的模板设置在眼上;
图9c示出了图9a的眼的顶部平面图,其中多个标记物设置在眼上;
图9d示出了图9a的眼的顶部平面图,其中缝合线套环附接到眼;
图9e示出了图9a的眼的顶部平面图,其中巩膜切开术正在被执行;
图9f示出了图9a的眼的顶部平面图,其中图1的器械正穿过巩膜切开术开口插入到眼的巩膜和脉络膜之间;
图9g示出了图9a的眼的顶部平面图,其中图1的器械在眼后部处的直接可视化下设置在巩膜和脉络膜之间;
图9h示出了图9a的眼的顶部平面图,其中图1的器械的针在眼后部处的直接可视化下被推进,由此压贴脉络膜的外表面以使得脉络膜“呈帐篷状”;
图9i示出了图9a的眼的顶部平面图,其中针在眼后部处的直接可视化下分配先导水泡,针位于巩膜和脉络膜之间,并且先导水泡位于脉络膜和视网膜之间的视网膜下腔中;
图9j示出了图9a的眼的顶部平面图,其中针将治疗剂在巩膜和脉络膜之间的眼的后部处分配到眼;
图10a示出了图9a的眼的横截面视图,其中该横截面为围绕图9a的线10a-10a截取的;
图10b示出了图9a的眼的横截面视图,其中该横截面为围绕图9e的线10b-10b截取的;
图10c示出了图9a的眼的横截面视图,其中该横截面为围绕图9f的线10c-10c截取的;
图10d示出了图9a的眼的横截面视图,其中该横截面为围绕图9g的线10d-10d截取的;
图10e示出了图9a的眼的横截面视图,其中该横截面为围绕图9h的线10e-10e截取的;
图10f示出了图9a的眼的横截面视图,其中该横截面为围绕图9i的线10f-10f截取的;
图10g示出了图9a的眼的横截面视图,其中该横截面为围绕图9j的线10g-10g截取的;
图11a示出了图9a的眼的详细横截面视图,其被示为处于图10e所示的状态;
图11b示出了图9a的眼的详细横截面视图,其被示为处于图10f所示的状态;
图11c示出了图9a的眼的详细横截面视图,其被示为处于图10g所示的状态;
图12示出了用于治疗剂的视网膜下给药的另一个示例性器械的侧正视图;
图13示出了用于治疗剂的视网膜下给药的另一个示例性器械的透视图;
图14示出了图13的器械的侧正视图;
图15示出了图13的器械的另一个透视图;
图16示出了图13的器械的局部分解透视图;
图17示出了沿图13的线17-17截取的图13的器械的局部横截面透视图;
图18示出了图13的器械的滑动件的透视图;
图19示出了图18的滑动件的另一个透视图;
图20a示出了沿图13的线17-17截取的图13的器械的横截面侧视图,其中图18的滑动件处于近侧纵向位置;
图20b示出了沿图13的线17-17截取的图13的器械的横截面侧视图,其中图18的滑动件运动到远侧纵向位置;
图21示出了用于治疗剂的视网膜下给药的另一个示例性器械的透视图;
图22示出了图21的器械的侧正视图;
图23示出了图21的器械的另一个透视图;
图24a示出了图21的器械的详细透视图,其中器械的微导管回缩到器械的针中的近侧纵向位置;
图24b示出了图21的器械的详细透视图,其中微导管从图24a的针朝远侧推进;
图25示出了图21的器械的详细横截面侧视图;
图26a示出了图21的器械的详细透视图,其中器械中的导管致动器处于近侧纵向位置;
图26b示出了图21的器械的详细透视图,其中图26a的导管致动器运动到远侧纵向位置;
图27a示出了图21的器械的详细横截面侧视图,其中图26a的导管致动器处于图26a的近侧纵向位置;
图27b示出了图21的器械的详细横截面侧视图,其中图26a的导管致动器运动到图26b的远侧纵向位置;
图28示出了示例性针引导装置的透视图;
图29示出了图28的引导装置的另一个透视图;
图30示出了图28的引导装置的另一个透视图;
图31示出了图28的引导装置的侧正视图;
图32示出了图28的引导装置的另一个侧正视图;
图33示出了沿图29的线33-33截取的图28的引导装置的横截面侧正视图;
图34示出了图28的引导装置的引导锚定件的详细透视图;
图35示出了图34的引导锚定件的另一个详细透视图;
图36示出了沿图34的线36-36截取的图34的引导锚定件的详细横截面侧视图;
图37示出了图28的引导装置的透视图,其中观察透镜联接在引导装置内;
图38示出了图28的引导装置的侧正视图,其中图37的观察透镜联接在引导装置内;
图39示出了附接到眼的图28的引导装置的透视图,并且其中图37的观察透镜联接在引导装置内;
图40示出了另一个示例性引导装置的透视图;
图41示出了图40的引导装置的另一个透视图;
图42示出了沿图40的线42-42截取的图40的引导装置的横截面侧正视图;
图43示出了图40的引导装置的透视图,其中观察透镜联接在引导装置内;
图44示出了图40的引导装置的侧正视图,其中图43的观察透镜联接在引导装置内;
图45示出了另一个示例性引导装置的透视图;
图46示出了图45的引导装置的另一个透视图;
图47示出了沿图45的线47-47截取的图45的引导装置的横截面侧正视图;
图48示出了图45的引导装置的透视图,其中观察透镜联接在引导装置内;
图49示出了图45的引导装置的侧正视图,其中图43的观察透镜联接在引导装置内;
图50示出了附接到眼的另一个示例性引导装置的透视图,并且其中观察透镜联接在引导装置内;
图51示出了附接到眼的图50的引导装置的横截面侧视图,其中图50的观察透镜联接在引导装置内;
图52a示出了图39的眼的横截面侧视图,其中图12的器械的针穿过图28的引导装置的开口并且定位在眼附近;
图52b示出了图39的眼的横截面侧视图,其中图52a的针穿过图28的引导装置的开口并且插入到眼内以便刺穿巩膜和脉络膜;
图52c示出了图39的眼的横截面侧视图,其中图52a的针穿过图28的引导装置的开口并且插入到眼内以便刺穿巩膜和脉络膜,其中针在眼侧部处的直接可视化下分配先导水泡;
图53a示出了图39的眼的详细横截面侧视图,其中图52a的针插入到眼内以便刺穿巩膜和脉络膜,其中针在眼侧部处的直接可视化下分配先导水泡;
图53b示出了图39的眼的详细横截面侧视图,其中微导管从图52a的针延伸到先导水泡中;
图53c示出了图39的眼的详细横截面侧视图,其中图53b的微导管在脉络膜和视网膜之间的视网膜下腔内进一步延伸到眼的后部;并且
图53d示出了图39的眼的详细横截面侧视图,其中图53b的微导管将治疗剂在眼后部处的视网膜下腔中分配到眼。
附图并非旨在以任何方式进行限制,并且可以预期本技术的各种实施方案能够以多种其他方式来执行,包括那些未必在附图中示出的方式。并入本说明书并构成其一部分的附图示出了本技术的若干方面,并且与说明书一起用于解释本技术的原理;然而,应当理解,这种技术不局限于所示的精确布置方式。
具体实施方式
下面描述的本技术的某些示例不应用于限制本技术的范围。从下面的描述而言,本技术的其他示例、特征、方面、实施方案和优点对本领域的技术人员而言将显而易见,下面的描述以举例的方式进行,这是为实现本技术所设想的最好的方式之一。正如将意识到的,本文所述技术能够包括其他不同的和明显的方面,这些均不脱离本发明技术。因此,附图和具体实施方式应被视为实质上是说明性的而非限制性的。
还应当理解,本文所述的教导内容、表达方式、实施方案、示例等中的任何一者或多者可与本文所述的其他教导内容、表达方式、实施方案、示例等中的任何一者或多者进行组合。下述教导内容、表达方式、实施方案、示例等因此不应视为彼此孤立。参考本文的教导内容,本文的教导内容可进行组合的各种合适方式对于本领域的普通技术人员而言将显而易见。此类修改和变型旨在包括在权利要求书的范围内。
为公开的清楚起见,术语“近侧”和“远侧”在本文中是相对于抓持具有远侧外科端部执行器的外科器械的外科医生或其他操作者定义的。术语“近侧”是指元件的更靠近外科医生或其他操作者的位置,并且术语“远侧”是指元件的更靠近外科器械的外科端部执行器并且更远离外科医生或其他操作者的位置。
i.具有滑块关节运动特征结构的示例性器械
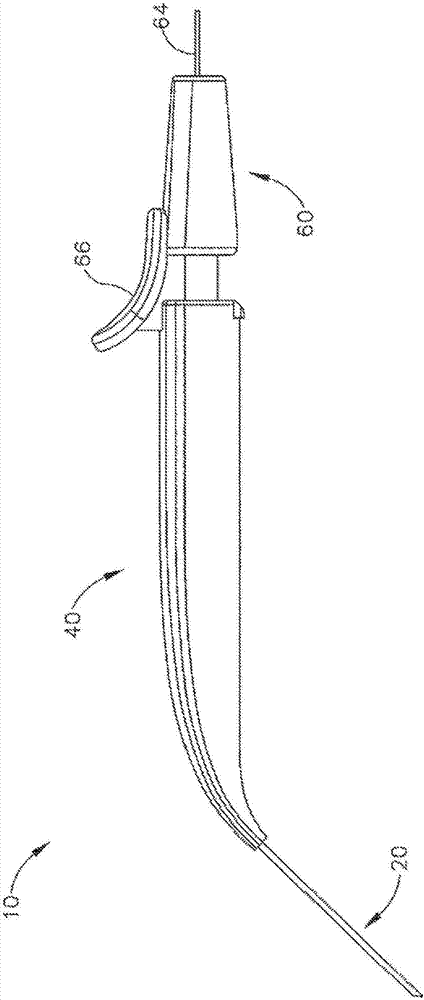
图1-图4示出了示例性器械10,其被构造成能够用于从脉络膜上途径对患者的眼进行治疗剂的视网膜下给药的过程中。器械10包括柔性插管20、主体40、和滑块60。插管20从主体40朝远侧延伸并且具有大体矩形的横截面。插管20通常被构造成能够支撑可在插管20内滑动的针30,如将在下文更详细所述。
在本示例中,插管20包括柔性材料,例如可以商品名pebax制造的聚醚嵌段酰胺(peba)。当然,可使用任何其他合适的材料或材料组合。另外在本示例中,插管20具有约2.0mm×0.8mm的横截面轮廓尺寸以及约80mm的长度。另选地,可使用任何其他合适的尺寸。
如将在下文更详细所述,插管20为足够柔性的以适形于患者的眼的特定结构和轮廓,然而插管20具有足够的柱强度以允许插管20推进到患者的眼的巩膜和脉络膜之间而不屈曲。若干因素可有助于插管20的合适柔性。例如,用于构造插管20的材料的硬度计至少部分地表征插管20的柔性。仅以举例的方式,用于形成插管20的材料可具有约27d、约33d、约42d、约46d的肖氏硬度、或任何其他合适的肖氏硬度。应当理解,肖氏硬度可位于约27d至约46d的范围内;或者更具体地讲约33d至约46d的范围内;或者更具体地讲约40d至约45d的范围内。插管20的特定横截面形状也可至少部分地表征插管20的柔性。另外,设置在插管20内的针30的刚度可至少部分地表征插管20的柔性。
在本示例中,插管20的柔性可通过计算插管20的抗弯刚度来量化。抗弯刚度通过弹性模量和面积惯性矩的乘积来计算。仅以举例的方式,可用于形成插管20的一种示例性材料可具有d27的肖氏硬度、1.2×107n/m2的弹性模量(e)、和5.52×10-14m4的面积惯性矩(ix),从而提供0.7×10-6nm2的围绕x轴的经计算抗弯刚度。可用于形成插管20的另一种示例性材料可具有d33的肖氏硬度、2.1×107n/m2的弹性模量(e)、和5.52×10-14m4的面积惯性矩(ix),从而提供1.2×10-6nm2的围绕x轴的经计算抗弯刚度。可用于形成插管20的另一种示例性材料可具有d42的肖氏硬度、7.7×107n/m2的弹性模量(e)、和5.52×10-14m4的面积惯性矩(ix),从而提供4.3×10-6nm2的围绕x轴的经计算抗弯刚度。可用于形成插管20的另一种示例性材料可具有d46的肖氏硬度、17.0×107n/m2的弹性模量(e)、和5.52×10-14m4的面积惯性矩(ix),从而提供9.4×10-6nm2的围绕x轴的经计算抗弯刚度。因此,仅以举例的方式,插管20的抗弯刚度可位于约0.7×10-6nm2至约9.4×10-6nm2的范围内;或更具体地讲约1.2×10-6nm2至约9.4×10-6nm2范围内;或更具体地讲约2.0×10-6nm2至约7.5×10-6nm2的范围内;或更具体地讲约2.0×10-6nm2至约6.0×10-6nm2的范围内;或更具体地讲约3.0×10-6nm2至约5.0×10-6nm2的范围内;或更具体地讲约4.0×10-6nm2至约5.0×10-6nm2的范围内。
在本示例中,插管20的柔性还可通过以下公式来量化:
(1)
在上述方程中,抗弯刚度(ei)通过将具有固定跨度(l)的插管20挠曲设定距离以产生预定的挠曲量(δ)来实验性地计算。然后可记录这种挠曲所需的力(f)的量。例如,当使用此方法时,插管20可具有0.06m的跨度并且可被挠曲给定的距离。仅以举例的方式,可用于形成插管20的一种示例性材料可需要0.0188n的力来实现0.0155m的挠曲,从而提供5.5×10-6nm2的围绕x轴的经计算抗弯刚度。可用于形成插管20的另一种示例性材料可需要0.0205n的力来实现0.0135m的挠曲,从而提供6.8×10-6nm2的围绕x轴的经计算抗弯刚度。可用于形成插管20的另一种示例性材料可需要0.0199n的力来实现0.0099m的挠曲,从而提供9.1×10-6nm2的围绕x轴的经计算抗弯刚度。可用于形成插管20的另一种示例性材料可需要0.0241n的力来实现0.0061m的挠曲,从而提供1.8×10-6nm2的围绕x轴的经计算抗弯刚度。可用于形成插管20的另一种示例性材料可需要0.0190n的力来实现0.0081m的挠曲,从而提供1.0×10-6nm2的围绕x轴的经计算抗弯刚度。可用于形成插管20的另一种示例性材料可需要0.0215n的力来实现0.0114m的挠曲,从而提供8.4×10-6nm2的围绕x轴的经计算抗弯刚度。可用于形成插管20的另一种示例性材料可需要0.0193n的力来实现0.0170m的挠曲,从而提供5.1×10-6nm2的围绕x轴的经计算抗弯刚度。可用于形成插管20的另一种示例性材料可需要0.0224n的力来实现0.0152m的挠曲,从而提供6.6×10-6nm2的围绕x轴的经计算抗弯刚度。可用于形成插管20的另一种示例性材料可需要0.0183n的力来实现0.0119m的挠曲,从而提供6.9×10-6nm2的围绕x轴的经计算抗弯刚度。可用于形成插管20的另一种示例性材料可需要0.0233n的力来实现0.0147m的挠曲,从而提供7.1×10-6nm2的围绕x轴的经计算抗弯刚度。可用于形成插管20的另一种示例性材料可需要0.0192n的力来实现0.0122的挠曲,从而提供7.1×10-6nm2的围绕x轴的经计算抗弯刚度。可用于形成插管20的另一种示例性材料可需要0.0201n的力来实现0.0201的挠曲,从而提供4.5×10-6nm2的围绕x轴的经计算抗弯刚度。因此,仅以举例的方式,插管20的抗弯刚度可位于约1.0×10-6nm2至约9.1×10-6nm2的范围内。应当理解,在其他示例中,插管的抗弯刚度可位于约0.7×10-6nm2至约11.1×10-6nm2的范围内;或更具体地讲约2.0×10-6nm2至约6.0×10-6nm2的范围内。
针30可具有与插管20的抗弯刚度不同的抗弯刚度。仅以举例的方式,针30可由镍钛诺材料形成,所述镍钛诺材料具有7.9×1010n/m2的弹性模量(e)、和2.12×10-17m4的面积惯性矩(ix),从而提供1.7×10-6nm2的围绕x轴的经计算抗弯刚度。仅以另一个示例的方式,针30的抗弯刚度可位于约0.5×10-6nm2至约2.5×10-6nm2的范围内;或更具体地讲约0.75×10-6nm2至约2.0×10-6nm2的范围内;或更具体地讲约1.25×10-6nm2至约1.75×10-6nm2的范围内。
如在图5和图6中可见,插管20包括纵向延伸穿过插管20并且终止于无创斜面远侧端部26处的两个侧管腔22和单个中心管腔24。斜面侧向开口28位于斜面远侧端部26的近侧。侧管腔22有助于插管20的柔性。尽管管腔22,24被示为在斜面远侧端部26处开口,但应当理解,在一些示例中,侧管腔22,24可任选地在斜面远侧端部26处封闭。如将在下文更详细所述,中心管腔24被构造成能够接收针30和针引导件80。在一些型式中,光纤(未示出)也横靠针30设置在中心管腔24中。此类光纤可用于提供照明和/或光学反馈。
斜面远侧端部26为大体倾斜的,以提供巩膜和脉络膜层之间的分离,从而使得插管20能够在这些层之间推进,同时不会使巩膜或脉络膜层受到创伤。在本示例中,斜面远侧端部26相对于本示例中的插管20的纵向轴线倾斜成约15°的角度。在其他示例中,斜面远侧端部26的斜面角度可位于约5°至约50°的范围内;或更具体地讲约5°至约40°的范围内;或更具体地讲约10°至约30°的范围内;或更具体地讲约10°至约20°的范围内。
针引导件80设置在管腔24内,使得针引导件80的远侧端部邻接斜面侧向开口28。针引导件80通常被构造成能够沿着相对于插管20的纵向轴线(la)倾斜取向的出口轴线(ea)来向上引导针30穿过插管20的斜面开口28。针引导件80可由塑料、不锈钢和/或任何其他一种或多种合适的生物相容性材料形成。针引导件80的形状被构造成能够用于插入到中心管腔24内。在本示例中,针引导件80通过压力或过盈配合被固定在中心管腔24内,但在其他示例中,可使用粘合剂和/或机械锁定机构来固定针引导件80。
如在图6中最佳可见,针引导件80限定被构造成能够可滑动地接收针30的内部管腔84。具体地讲,内部管腔84包括大体直形近侧部分86和弯曲远侧部分88。直形近侧部分86对应于插管20的纵向轴线(la),而弯曲远侧部分88远离插管20的纵向轴线向上弯曲。本示例的弯曲远侧部分88为弯曲的,以沿着出口轴线(ea)引导针30,所述出口轴线(ea)以相对于插管20的纵向轴线(la)成约7°至约9°的角度的方式从插管20朝远侧延伸。应当理解,此角度可有利于使针30沿着某个方向挠曲,以确保针穿透到脉络膜306内并且最小化针30一直在脉络膜306下面穿过脉络膜上腔的可能性(形成对照的是穿透脉络膜306)以及视网膜穿孔的可能性。仅以另一个示例的方式,弯曲远侧部分88可迫使针30沿着出口轴线(ea)离开插管20,所述出口轴线(ea)相对于插管20的纵向轴线(la)被取向成约5°至约30°的范围内的角度;或更具体地讲相对于插管20的纵向轴线(la)被取向成约5°至约20°的范围内的角度;或更具体地讲相对于插管20的纵向轴线(la)被取向成约5°至约10°的范围内的角度。
针30呈内部插管的形式,所述内部插管具有尖型远侧端部32并且限定内部管腔34。本示例的远侧端部32具有刺血针构型。在一些其他型式中,远侧端部32具有三斜面构型或任何其他构型,如在2015年2月11日提交的名称为“methodandapparatusforsuprachoroidaladministrationoftherapeuticagent”的美国专利申请号14/619,256中所述,该专利申请的公开内容以引用方式并入本文。参考本文的教导内容,远侧端部32可采用的其他合适形式对于本领域的普通技术人员而言将显而易见。本示例的针30包括镍钛诺皮下注射针,所述镍钛诺皮下注射针的尺寸被设定成递送治疗剂,同时足够小以在针30穿透患者的眼的组织结构时产生自密封伤口,如将在下文更详细所述。仅以举例的方式,针30可为具有100μm内径的35规格,但可使用其他合适的尺寸。例如,针30的外径可位于27规格至45规格的范围内;或更具体地讲30规格至42规格的范围内;或更具体地讲32规格至39规格的范围内。作为另一个仅示例性例子,针30的内径可位于约50μm至约200μm的范围内;或更具体地讲约50μm至约150μm的范围内;或更具体地讲约75μm至约125μm的范围内。
重新参照图1-图2,主体40通常成形为具有弯曲远侧端部的细长矩形。示出的主体40的特定形状被构造成能够被操作者抓持。另选地,主体40可安装在支撑装置或机械臂上以便于定位器械10,如在2015年2月11日提交的名称为“methodandapparatusforsuprachoroidaladministrationoftherapeuticagent”的美国专利申请号14/619,256中所述,该专利申请的公开内容以引用方式并入本文。
致动组件60包括致动构件62和锁定构件66。锁定构件66能够在主体40和致动构件62之间可移除地附接到主体接合部分50。如将在下文更详细所述,锁定构件66填充主体40和致动构件62之间的空间,以阻止致动构件62相对于主体40朝远侧推进。然而,锁定构件66可被移除以选择性地允许致动构件62相对于主体40朝远侧推进。
图2-图4示出了器械10的示例性致动。具体地讲,如在图2中可见,针30初始回缩到插管20内并且锁定构件66被定位在主体40和致动构件62之间,由此阻止致动构件62的推进。在器械10处于此构型的情况下,插管20可被定位在患者的眼内,如将在下文更详细所述。
一旦插管20被定位在患者的眼内,操作者就可期望相对于插管20推进针30。为了推进针30,操作者可首先通过牵拉锁定构件66远离器械10来移除锁定构件66,如在图3中可见。一旦锁定构件66被移除,致动构件62就可相对于主体40运动或平移以相对于插管20推进针30,如在2015年2月11日提交的名称为“methodandapparatusforsuprachoroidaladministrationoftherapeuticagent”的美国专利申请号14/619,256中所述,该专利申请的公开内容以引用方式并入本文。本示例的致动构件62仅被构造成能够平移针30并且不能旋转针30。在其他示例中,可期望旋转针30。因此,另选示例可在致动构件62中包括用以旋转和平移针30的特征结构。
在本示例中,如图4所示,致动构件62推进到接触主体40对应于将针30推进到相对于插管20的某个位置以到达患者的眼内的预定穿透量。换句话讲,器械10被构造成能够使得操作者将致动构件62推进到接触主体40,以将针30正确地定位在患者的眼内。在一些示例中,针30相对于插管20的预定推进量介于约0.25mm至约10mm之间;或更具体地讲在约0.1mm至约10mm的范围内;或更具体地讲在约2mm至约6mm的范围内;或更具体地讲约4mm。在其他示例中,除了针30相对于插管20的最大推进之外,致动构件62和主体40之间的接触可不具有特定意义。相反,器械10可配备有某些触觉反馈特征结构,以向操作者指示针30何时已相对于插管20推进到某些预定距离。因此,操作者可基于器械上的标记的直接可视化和/或基于来自器械10的触觉反馈来确定针30穿透到患者的眼内的期望深度。当然,此类触觉反馈特征结构可与本示例相结合,这参考本文的教导内容对于本领域的普通技术人员而言将显而易见。
ii.示例性的另选器械和特征结构
在一些示例中,可期望改变本文所述的器械的某些部件或特征结构。例如,可期望使用类似于器械10的具有用以致动针30的另选机构的器械。然而在其他示例中,可期望使用类似于器械10的配备有不同的插管20或针30几何形状的器械。具有上文所述的变型形式的器械可有利于用于不同的外科手术或者类似于上文讨论的手术的外科手术,以接合具有不同物理特性的组织结构。尽管本文描述了某些示例的变型形式,但应当理解,本文所述的器械可包括任何其他另选的特征结构,这参考本文的教导内容对于本领域的普通技术人员而言将显而易见。
图7示出了类似于上文所述的器械10的示例性另选器械2010。尽管下文描述了器械2010的某些特征结构和可操作性,但应当理解,除了下文所述之外或替代下文所述,器械2010可根据2015年2月11日提交的名称为“methodandapparatusforsuprachoroidaladministrationoftherapeuticagent”的美国专利申请号14/619,256的教导内容中的任一个来构造和/或操作,该专利申请的公开内容以引用方式并入本文。如同器械10,本示例的器械2010通常可用于本文所述的过程中,以从脉络膜上途径将治疗流体在视网膜下递送到患者的眼。因此应当理解,器械2010可易于取代器械10来使用以执行本文所述的医疗过程。类似于器械10,本示例的器械2010包括插管2020、主体2040、和致动组件2100。插管2020包括贯穿延伸的镍钛诺针2030并且与上文所述的插管20基本上相同。在本示例中,插管2020和针2030与上文所述的插管20和针30基本上相同。
器械10和器械2010之间的主要差异在于器械2010的致动组件2100为可旋转的而非可滑动的。另外,器械2010包括阀组件(未示出),所述阀组件能够操作以改变针2030的流体状态。致动组件2100通常能够操作以通过旋钮构件2110的旋转来纵向地平移阀组件,由此相对于插管2020纵向地平移针2030。
当致动组件2100处于近侧位置时,操作者可沿逆时针或顺时针方向旋转所述旋钮构件2110。如果旋钮构件2110沿逆时针方向旋转,则旋转构件2110将仅自由地旋转。为了开始致动组件2100、阀组件、和针2030的推进,操作者可沿顺时针方向旋转所述旋钮构件2110。旋钮构件2110的顺时针旋转将用于朝远侧平移旋钮构件2110并且还将用于朝远侧平移阀组件和针2030。操作者可继续旋钮构件2110的顺时针旋转以驱动针2030穿出插管2020的远侧端部。一旦针2030已相对于插管2020的远侧端部推进到其最远侧位置,旋钮构件2110的进一步顺时针旋转将因结合到致动组件2100内的离合器特征结构的滑移而仅导致旋钮构件2110的自由旋转。在针2030处于远侧位置的情况下,操作者可致动阀组件以允许经由针2030递送治疗剂,如下文更详细所述。
在治疗剂被递送之后,操作者可随后希望回缩针2030。旋钮构件2110的逆时针旋转将导致致动组件2100、阀组件、和针2030相对于主体2040的近侧平移。应当理解,当致动组件2100被旋转以致动阀组件和针2030时,阀组件和针2030相对于主体2040保持基本上旋转固定。另外应当理解,尽管本示例的旋转构件2110被描述为手动旋转,但旋转构件2110可经由马达和/或一些其他动力源进行旋转。因此,应当理解,针2030的平移可经由伺服马达来机械地/电力地驱动。伺服马达的致动可由伺服控制器来控制,如将在下文更详细所述。此类伺服控制器可手动地操作。除此之外或另选地,此类伺服控制器可经由计算机来操作,所述计算机基于来自器械2010或本文所述的任何其他部件的反馈采取动作。
iii.示例性缝合线测量模板
图8示出了可用于从脉络膜上途径提供治疗剂的视网膜下递送的过程中的示例性缝合线测量模板210,如将在下文更详细所述。一般来讲,模板210被构造成能够压贴患者的眼以将特定的色素图案压印到患者的眼上。应当理解,本文中使模板210压贴患者的眼的参考内容可包括但不必限于使模板210直接压贴巩膜304表面(例如,在结膜已被取出或以其他方式移位)。模板210包括刚性主体220和刚性轴240。如将在下文更详细所述,主体220为大体成轮廓的以对应于患者的眼的曲率,使得主体220可被按压或放置到患者的眼的至少一部分上。主体220包括上引导部分222和从主体220的眼面224朝远侧延伸的多个突起230。
上引导部分222为大体半圆形形状并且设置在主体220的顶部。上引导部分222的半圆形形状具有对应于患者的眼的角巩膜缘的曲率的半径。换句话讲,上引导部分222沿着对应于患者的眼球的曲率半径的第一半径朝近侧弯曲;并且沿着对应于患者的眼的角巩膜缘的曲率半径的第二半径向下(朝轴240的纵向轴线)弯曲。如将在下文更详细所述,上引导部分222可用于相对于患者的眼的角巩膜缘来正确地定位模板210。因此,可相对于患者的眼的角巩膜缘来定位可通过模板沉积到患者的眼上的任何着色。
突起230与上引导部分222间隔开预定距离。具体地讲,突起230形成图案,所述图案可对应于在下述方法期间使用的有关标记。本示例的突起230包括四个缝合线套环突起230a-230h和两个巩膜切开术突起230i,230j。缝合线套环突起230a-320h和巩膜切开术突起230i,230j从主体220向外延伸相等的距离,使得突起230共同保持由主体220限定的曲率。换句话讲,突起230a-230j的末端全部位于由下述曲率半径限定的弯曲平面上,所述曲率半径与患者的眼球的曲率半径互补。突起230a-230j的末端为圆形的和无创的,使得突起230a-230j可压贴眼而不损害患者的眼的巩膜或其他部分。
轴240从主体220朝近侧延伸。轴240被构造成能够允许操作者抓持模板210和操纵主体220。在本示例中,轴240与主体220形成一体。在其他示例中,轴240可通过机械紧固装置(例如螺纹联接件或机械扣合件等)选择性地附接到主体。在一些型式中,可向操作者提供包括轴240和多个主体220的套件。主体220可具有不同的曲率以对应于具有不同曲率半径的不同眼球。操作者可因此基于操作者前面的特定患者的解剖结构来从套件中选择适当的主体220;并且操作者可随后将所选择的主体220固定到轴240。尽管未示出,但应当理解,轴240的近侧端部可附加包括t形握把、旋钮、或其他抓持特征结构以允许操作者更容易地抓持轴240。
在示例性使用中,缝合线套环突起232和巩膜切开术突起234各自对应于下文所述的方法的特定部分。具体地讲,在下文所述的方法之前或期间,操作者可通过以下方式利用生物相容性色素或墨水来涂覆突起230:将突起230按压到色素或墨水垫250上、将色素或墨水刷涂到突起230上、或者以其他方式将色素或墨水施用到突起230。一旦突起230已接收色素或墨水,操作者就可通过将模板210的突起230按压到患者的眼上来标记患者的眼,如将在下文更详细所述。一旦模板210从患者的眼移除,来自突起的色素就可保持附着到眼以标记特定的感兴趣点,如将在下文更详细所述。
iv.用于从脉络膜上途径进行治疗剂的视网膜下递送的示例性方法
图9a-图11c示出了利用上文所述的器械10从脉络膜上途径进行治疗剂的视网膜下递送的示例性过程。然而应当理解,器械2010可易于结合或取代器械10来用于下文所述的过程中。仅以举例的方式,本文所述的方法可用于治疗黄斑变性和/或其他眼睛病症。尽管本文所述的过程在年龄相关性黄斑变性的治疗的背景中进行讨论,但应当理解,并非旨在或隐含具有此类限制。例如,在一些仅示例性另选过程中,可使用本文所述的相同技术来治疗色素性视网膜炎、糖尿病性视网膜病、和/或其他眼睛病症。另外,应当理解,可使用本文所述的过程来治疗干性或湿性年龄相关性黄斑变性。
如在图9a中可见,该过程开始于操作者利用窥器312和/或适用于固定的任何其他器械来固定围绕患者的眼301的组织(例如,眼睑)。尽管本文参照围绕眼301的组织来描述固定,但应当理解,眼301本身可保持自由地运动。一旦围绕眼301的组织已被固定,就将眼枝形吊灯端口314插入眼301内,以在穿过瞳孔观察眼301的内部时提供眼内照明。在本示例中,眼枝形吊灯端口314被定位在下内侧象限中,使得可执行上颞侧象限巩膜切开术。如在图10a中可见,眼枝形吊灯端口314被定位成将光引导到眼314的内部,以照亮视网膜的至少一部分(例如,包括黄斑的至少一部分)。应当理解,这种照明对应于旨在被递送治疗剂的眼301的区域。在本示例中,在此阶段插入仅枝形吊灯端口314,而不将光纤315插入端口314内。在一些其他型式中,在此阶段可将光纤315插入枝形吊灯端口314内。在任一种情况下,可任选地使用显微镜来目视检查眼以确认眼枝形吊灯端口314相对于目标部位的正确定位。在一些示例中,可通过视网膜着色的相对不足来识别目标区域。尽管图9a示出了眼枝形吊灯端口314的特定定位,但应当理解,眼枝形吊灯端口314可具有任何其他定位,这参考本文的教导内容对于本领域的普通技术人员而言将显而易见。
一旦眼枝形吊灯端口314已被定位,就可通过切开结膜中的皮瓣并且向后牵拉皮瓣来剥离结膜,由此触及巩膜304。在这种剥离完成之后,可任选地利用烧灼工具来漂白巩膜304的暴露表面305以最小化出血。一旦结膜剥离完成,就可利用weck-cel或其他合适的吸收装置来任选地干燥巩膜304的暴露表面305。然后可使用上文所述的模板210标记眼301。如在图9b中可见,模板210被定位成与眼301的角巩膜缘对准。操作者可将轻力施加到模板210以将色素施用到眼301。然后移除模板210,由此留下附着到巩膜304的暴露表面305的色素,从而为操作者提供视觉引导件320,如在图9c中可见。操作者随后可利用视觉引导件320来附接缝合线套环组件330并且执行巩膜切开术。视觉引导件320包括一组缝合线套环标记物(321,322,323,324,325,326,327)和一对巩膜切开术标记物329。
图9d示出了已完成的缝合线套环组件330。如将在下文更详细所述,缝合线套环组件330通常被构造成能够引导器械10的插管20穿过巩膜切开术并且进入眼301内。可用于产生图9d所示的缝合线套环组件330的示例性过程在2015年2月11日提交的名称为“methodandapparatusforsuprachoroidaladministrationoftherapeuticagent”的美国专利申请号14/619,256中有所描述,该专利申请的公开内容以引用方式并入本文。一旦缝合线套环组件330已附接到眼301,就可对眼301执行巩膜切开术。如在图9e中可见,利用常规外科手术刀313或其他合适的切割器械在巩膜切开术标记物329之间切割眼301。尽管巩膜切开术标记物329被示为包括两个分立的点,但应当理解,在其他示例中,标记物329可包括任何其他类型的标记物,例如实线、点线、或虚线。巩膜切开术过程形成穿过眼301的巩膜304的小切口316。如在图10b中最佳可见,特别谨慎地执行巩膜切开术以避免脉络膜306的穿透。因此,巩膜切开术过程提供到达巩膜304和脉络膜306之间的空间的入口。一旦在眼301中制备切口316,就可任选地执行钝性剥离以局部地分离巩膜304与脉络膜306。可利用小钝型细长器械来执行这种剥离,这参考本文的教导内容对于本领域的普通技术人员而言将显而易见。
在巩膜切开术过程已被执行的情况下,操作者可将器械10的插管20穿过切口316插入到巩膜304和脉络膜306之间的空间内。如在图9f中可见,引导插管20穿过缝合线套环组件330的引导套环336并且进入切口316内。如上所述,引导套环336可稳定插管20。另外,引导套环336保持插管20相对于切口316处于大体切向取向。这种切向取向可在插管20被引导穿过切口316时降低创伤,以稳定插管20并且避免损害周围组织。当插管20穿过引导套环336插入切口316内时,操作者可利用夹钳或其他器械来沿着无创路径进一步引导插管20。当然,夹钳或其他器械的使用仅为任选的并且在一些示例中可被省去。尽管未示出,但应当理解,在一些示例中,插管20可包括位于插管20的表面上的一个或多个标记物以指示各种插入深度。尽管仅为任选的,但此类标记物可为有利的,以有助于在沿着无创路径引导插管20时标识正确的插入深度。例如,操作者可目视观察此类标记物相对于引导套环336和/或相对于切口316的位置以作为插管20插入到眼301中的深度的指示。仅以举例的方式,一个此类标记物可对应于插管20的约6mm插入深度。
一旦插管20至少部分地插入到眼301内,操作者就可将光纤315插入到眼枝形吊灯端口314内,但在此阶段光纤315还未被插入。在眼枝形吊灯端口314保持在适当的位置并且装配有光纤315的情况下,操作者可通过引导光穿过光纤315来激活眼枝形吊灯端口314,以提供眼301的照明并且由此可视化眼301的内部。此时可任选地对插管20的定位作出进一步的调整,以确保相对于视网膜308的地图状萎缩区域的正确定位。在一些情况下,操作者可希望例如通过牵拉缝合线(334,339)来旋转眼301,以引导眼301的瞳孔朝向操作者,以便优化经由瞳孔的眼301内部的可视化。
图9g和图10c-图10d示出了在巩膜304和脉络膜306之间被引导到治疗剂的递送部位的插管20。在本示例中,递送部位对应于视网膜308的地图状萎缩区域附近的眼301的大体后部区域。具体地讲,本示例的递送部位位于黄斑的上侧、感觉神经性视网膜与视网膜色素上皮细胞层之间的潜在空间中。图9g示出了处于通过引导穿过眼301的瞳孔的显微镜的直接可视化下的眼301,其中通过光纤315和端口314提供照明。如图可见,插管20为穿过眼301的视网膜308和脉络膜306至少部分地可见的。因此,操作者可在插管20从图10c所示的位置穿过眼301推进到图10d所示的位置时跟踪该插管。在其中使用光纤34发射可见光穿过插管20的远侧端部的型式中,这种跟踪可得到增强。
一旦插管20已推进到如图10d所示的递送部位,操作者就可推进器械10的针30,如上文相对于图3-图4所述。如在图9h-图9i、10e和11a中可见,相对于插管20推进针30,使得针30刺穿脉络膜306而不穿透视网膜308。在即将穿透脉络膜306之前,针30可在直接可视化下显示为使脉络膜306的表面“呈帐篷状”,如在图9h中可见。换句话讲,针30可通过向上推压脉络膜使脉络膜306变形,由此提供以下外观,所述外观类似于使帐篷顶变形的帐篷杆。操作者可使用这种视觉现象来识别脉络膜306是否即将被刺穿以及任何最终刺穿的位置。足以引起脉络膜306的“呈帐篷状”和后续刺穿的特定的针30推进量可具有任何合适的数值,所述数值可取决于多个因素,例如但不限于总体患者解剖结构、局部患者解剖结构、操作者偏好、和/或其他因素。如上所述,针30推进的仅示例性范围可介于约0.25mm和约10mm之间;或更具体地讲介于约2mm和约6mm之间。
在本示例中,在操作者已通过观察到上文所述的帐篷状效果确认针30已被正确推进之后,操作者在针30相对插管20推进时注入平衡盐溶液(bss)或其他类似溶液。这种bss溶液可在针30推进穿过脉络膜306时在针30之前形成先导水泡340。先导水泡340可出于两个原因而为有利的。第一,如图9i、图10f和图11b所示,先导水泡340可向操作者提供另一个视觉指示器以指示针30何时被正确地定位在递送部位处。第二,先导水泡340可在针30一旦穿透脉络膜306时在针30与视网膜308之间提供屏障。这种屏障可向外推压视网膜壁(如在图10f和图11b中最佳所见),由此最小化针30推进到递送部位时的视网膜穿孔的风险。在一些型式中,致动脚踏开关以便从针30驱动出先导水泡340。另选地,参考本文的教导内容,可用于从针30驱动出先导水泡340的其他合适的特征结构对于本领域的普通技术人员而言将显而易见。
一旦操作者观察到先导水泡340,操作者就可停止bss的注入,由此留下流体袋,如在图9i、图10f、和图11b中可见。接下来,可通过致动注射器或其他流体递送装置来注入治疗剂341,如上文相对于器械10所述。所递送的具体治疗剂341可为被构造成能够治疗眼睛病症的任何合适的治疗剂。一些仅示例性的合适治疗剂可包括但不必限于具有较小分子或大分子的药物、治疗细胞溶液、某些基因治疗溶液、和/或任何其他合适的治疗剂,这参考本文的教导内容对于本领域的普通技术人员而言将显而易见。仅以举例的方式,治疗剂341可根据2008年8月19日公布的名称为“treatmentofretinitispigmentosawithhumanumbilicalcordcells”的美国专利号7,413,734的教导内容中的至少一些来提供,该专利的公开内容以引用方式并入本文。
在本示例中,最终递送到递送部位的治疗剂341的量为约50μl,但可递送任何其他合适的量。在一些型式中,致动脚踏开关以便从针30驱动出试剂341。另选地,参考本文的教导内容,可用于从针30驱动出试剂341的其他合适的特征结构对于本领域的普通技术人员而言将显而易见。可通过流体袋的膨胀来可视化治疗剂的递送,如在图9j、图10g、和图11c中可见。如图所示,当治疗剂341注射到脉络膜上腔内时,治疗剂341与先导水泡340的流体基本上混合。
一旦递送完成,就可通过相对于主体40朝近侧滑动致动组件60来回缩针20;并且随后可从眼301抽出插管30。应当理解,由于针20的尺寸,针20穿透脉络膜306的部位为自密封的,使得无需采取其他步骤来密封穿过脉络膜306的递送部位。可移除缝合线套环组件330和枝形吊灯314,并且可利用任何合适的常规技术来闭合巩膜304中的切口316。
如上所述,可执行上文所述的过程来治疗具有黄斑变性的患者。在一些此类情况下,通过针20递送的治疗剂341可包括源于产后脐和胎盘的细胞。如上所述并且仅以举例的方式,治疗剂341可根据2008年8月19日公布的名称为“treatmentofretinitispigmentosawithhumanumbilicalcordcells”的美国专利号7,413,734的教导内容中的至少一些来提供,该专利的公开内容以引用方式并入本文。另选地,除了或取代美国专利号7,413,734中和/或本文在别处描述的物质,针20可用于递送任何其他一种或多种合适的物质。仅以举例的方式,治疗剂341可包括各种药物,所述药物包括但不限于小分子、大分子、细胞、和/或基因治疗物。还应当理解,黄斑变性仅为可通过本文所述的过程治疗的病症的一种仅示例性例子。可利用本文所述的器械和过程解决的其他生物学病症对于本领域的普通技术人员而言将显而易见。
v.具有微导管的示例性器械
在一些情况下,可希望改变本文所述的器械的某些部件或特征结构以便改变用于将治疗剂递送到眼的视网膜下腔的技术。在一些示例中,还可希望改变本文所述的外科过程的某些步骤或特征结构。例如,可希望利用类似于器械(10,2010)的具有以下特征结构的器械来改变本文所述的外科过程,所述特征结构被构造成能够较少限度地需要利用如上所述的外科手术刀或其他切割器械来切割眼。具有上文所述的变型形式的器械可有利于用于不同的外科手术或者类似于上文讨论的手术的外科手术,以接合具有不同物理特性的组织结构。尽管本文描述了某些示例的变型形式,但应当理解,本文所述的器械可包括任何其他另选的特征结构,这参考本文的教导内容对于本领域的普通技术人员而言将显而易见。
a.具有手动滑动式微导管的示例性器械
图12示出了示例性器械400,其被构造成能够用于将治疗剂在视网膜下给药到患者的眼的过程中。器械400包括针420、主体440、和微导管460。针420从主体440朝远侧延伸。针420通常被构造成能够支撑微导管460,如将在下文更详细所述。另外将在下文更详细所述,针420具有足够的柱强度以允许针420穿过巩膜和脉络膜刺穿并推进到患者的眼的视网膜下腔而不屈曲。针420具有尖型远侧端部422并且限定纵向延伸穿过针420的内部管腔(未示出)。如将在下文更详细所述,针420的管腔被构造成能够可滑动地接收微导管460。
尖型远侧端部422被构造成能够刺穿和穿透巩膜和脉络膜层,以使得针420能够穿过这些层推进到视网膜下腔,同时不会使巩膜或脉络膜层受到其他附带创伤。本示例的远侧端部422具有刺血针构型。在一些其他型式中,远侧端部422具有三斜面构型或任何其他构型,如在2015年2月11日提交的名称为“methodandapparatusforsuprachoroidaladministrationoftherapeuticagent”的美国专利申请号14/619,256中所述,该专利申请的公开内容以引用方式并入本文。参考本文的教导内容,远侧端部422可采用的其他合适形式对于本领域的普通技术人员而言将显而易见。本示例的针420包括不锈钢皮下注射针,所述不锈钢皮下注射针的尺寸被设定成接收微导管460,同时足够小以最小化针420穿透患者的眼的组织结构时的附带伤口,如将在下文更详细所述。仅以举例的方式,针420可为23规格,但可使用其他合适的尺寸。
主体440为大体t形的,具有向外伸出的流体端口442。示出的主体440的特定形状被构造成能够被操作者抓持。另选地,主体440可安装在支撑装置或臂上以便于定位器械400,如在2015年2月11日提交的名称为“methodandapparatusforsuprachoroidaladministrationoftherapeuticagent”的美国专利申请号14/619,256中所述,该专利申请的公开内容以引用方式并入本文。流体端口442提供到达主体440的内部的流体入口。在本示例中,流体供给管线444与流体端口442联接并且被构造成能够将流体提供到主体440的内部。如将在下文更详细所述,针420与主体440的内部流体连通,使得经由流体供给管线444提供的流体(例如,由abbottmedicaloptics制造的
主体440的近侧部分包括套圈446。套圈446提供到达主体440的内部的入口。套圈446被构造成能够可滑动地接收微导管460,使得微导管460可穿过套圈446进入主体440的内部。微导管460的一部分相对于套圈446为暴露的,使得操作者可接合并且手动地平移微导管460。套圈446包括密封元件(例如,刮拭密封件或o形环)(未示出),所述密封元件允许微导管460在套圈446内并且相对于套圈446平移同时避免流体从主体440内部的意外渗漏。针420被构造成能够可滑动地接收微导管460。微导管460因而被构造成能够穿过套圈446、穿过主体440的内部、并且进入针420的管腔。本示例的针420的尺寸被设定成使得甚至在微导管460定位在针420的管腔内的情况下,流体仍可围绕微导管460穿过针420。微导管460可在针420内并且相对于针420手动地平移。例如,微导管460可相对于针420朝远侧平移,直到微导管460从针420的远侧端部朝远侧延伸。
如将在下文更详细所述,在针420被定位成使得针420的远侧端部位于视网膜下腔内的情况下,微导管460可从针420的远侧端部在患者的眼的脉络膜与视网膜之间朝远侧推进到患者的眼的后部处的位置。微导管460的这种推进可通过操作者手动地平移微导管460来执行。微导管460为足够柔性的以适形于患者的眼的特定结构和轮廓,然而微导管460具有足够的柱强度以允许微导管460在患者的眼的脉络膜与视网膜之间推进而不屈曲。针420通常被构造成能够沿着相对于针420的纵向轴线成角度地倾斜取向的出口轴线来引导微导管460。应当理解,此类角度可有利于使微导管460沿着某个方向挠曲,以确保微导管460一直在视网膜308下面穿过视网膜下腔(形成对照的是穿透视网膜308)并且避免微导管460穿透到视网膜308内。
如将在下文更详细所述,微导管460限定内部管腔(未示出)。在微导管460被定位在患者的眼的后部处的情况下,微导管460的管腔被构造成能够允许流体(例如,治疗剂)穿过微导管460流到微导管460的远侧端部,以便将流体递送到患者的眼的后部。一旦流体已递送到患者的眼的后部,就可将微导管460朝近侧牵拉回到针420的远侧端部内。微导管460的这种近侧平移可通过操作者手动地平移微导管460来执行。另外如将在下文参照图图53b-图53d更详细所述,微导管460包括照明元件462,所述照明元件462被构造成能够有助于跟踪或定位患者的眼内的微导管460。
b.具有用以驱动微导管的齿轮组件驱动器的示例性器械
图13-图20b示出了类似于上文所述的器械400的示例性另选器械500。尽管下文描述了器械500的某些特征结构和可操作性,但应当理解,除了下文所述之外或替代下文所述,器械500可根据2015年2月11日提交的名称为“methodandapparatusforsuprachoroidaladministrationoftherapeuticagent”的美国专利申请号14/619,256的教导内容中的任一个来构造和/或操作,该专利申请的公开内容以引用方式并入本文。如同器械400,本示例的器械500通常可用于本文所述的过程中,以将治疗流体在视网膜下递送到患者的眼。因此应当理解,器械500可易于取代器械400来使用以执行本文所述的医疗过程。类似于器械400,本示例的器械500包括针520、主体540、和微导管560。针520包括与上文所述的针420基本上相同的不锈钢皮下注射针。在本示例中,针520和微导管560与上文所述的针420和微导管460基本上相同。
针520从主体540朝远侧延伸。针520通常被构造成能够支撑微导管560,如将在下文更详细所述。另外将在下文更详细所述,针520具有足够的柱强度以允许针520穿过巩膜和脉络膜推进到患者的眼的视网膜下腔而不屈曲。针520包括大体直形近侧部分520a和弯曲远侧部分520b。本示例的弯曲远侧部分520b为弯曲的,以改善器械500的人体工程学,由此允许操作者将针520相对于眼以适当的角度插入而不必将器械保持在相对于操作者而言不好处理的角度下。应当理解,此类角度可有利于使微导管560沿着某个方向挠曲,以确保微导管560一直在视网膜308下面穿过视网膜下腔并且避免微导管560穿透视网膜308。
如图20a-图20b最佳可见,针520具有尖型远侧端部522并且限定延伸穿过针520的内部管腔524。如将在下文更详细所述,针520的管腔524被构造成能够可滑动地接收微导管560。尖型远侧端部522被构造成能够刺穿巩膜和脉络膜层,以使得针520能够穿过这些层推进到视网膜下腔,同时不会使巩膜或脉络膜层受到其他附带创伤。本示例的远侧端部522具有刺血针构型。在一些其他型式中,远侧端部522具有三斜面构型或任何其他构型,如在2015年2月11日提交的名称为“methodandapparatusforsuprachoroidaladministrationoftherapeuticagent”的美国专利申请号14/619,256中所述,该专利申请的公开内容以引用方式并入本文。参考本文的教导内容,远侧端部522可采用的其他合适形式对于本领域的普通技术人员而言将显而易见。本示例的针520包括不锈钢皮下注射针,所述不锈钢皮下注射针的尺寸被设定成接收微导管560,同时足够小以最小化针520穿透患者的眼的组织结构时的附带伤口,如将在下文更详细所述。仅以举例的方式,针520可为23规格,但可使用其他合适的尺寸。
主体540为大体细长形状并且包括从主体540的远侧部分延伸的向外伸出的流体端口542。示出的主体540的特定形状被构造成能够被操作者抓持。另选地,主体540可安装在支撑装置或臂上以便于定位器械500,如在2015年2月11日提交的名称为“methodandapparatusforsuprachoroidaladministrationoftherapeuticagent”的美国专利申请号14/619,256中所述,该专利申请的公开内容以引用方式并入本文。如图17和图20a-图20b最佳可见,流体端口542提供主体540的内部541的流体入口。在本示例中,流体供给管线(未示出)与流体端口542联接并且被构造成能够将流体提供到主体540的内部541。如将在下文更详细所述,针520与主体540的内部541流体连通,使得经由流体供给管线提供的流体(例如,由abbottmedicaloptics制造的
器械400与器械500之间的主要差异在于器械500包括齿轮组件580,所述齿轮组件580被构造成能够驱动微导管560相对于针520的平移。主体540包括滑动件550,所述滑动件550可滑动地设置在形成于主体540的近侧部分中的圆柱形镗孔546内。滑动件550能够操作以在圆柱形镗孔546内在近侧纵向位置(图20a)与远侧纵向位置(图20b)之间纵向地平移。主体540包括销548,所述销548定位在形成于滑动件550的底部表面中的细长狭槽552(图19)内。销548能够操作以基于狭槽552的纵向长度来限制滑动件550的纵向平移。
齿轮组件580包括一对可旋转构件582,584。可旋转构件582包括定位在可旋转构件582的相对端部处的一对齿轮586,588。可旋转构件582相对于主体540为部分暴露的,使得操作者可利用其手指或拇指接合可旋转构件582,从而导致可旋转构件582的旋转。可旋转构件584包括细长齿轮583,所述细长齿轮583延伸基本上可旋转构件584的长度。可旋转构件582的齿轮586,588的齿接合可旋转构件584的齿轮583的齿,使得可旋转构件582的旋转导致可旋转构件584的同时旋转。可旋转构件582能够围绕垂直于主体540的纵向轴线的轴线旋转。
如图18中最佳可见,滑动件550包括沿着滑动件550的长度纵向延伸的多个齿轮齿558。滑动件550的齿558以齿轮齿条式关系接合可旋转构件584的齿轮583的齿。因此,可旋转构件584的旋转导致滑动件550在近侧纵向位置(图20a)与远侧纵向位置(图20b)之间的纵向平移。应当理解,可旋转构件582沿第一方向的旋转将导致滑动件550相对于主体540的远侧纵向平移,并且可旋转构件582沿第二方向的旋转将导致滑动件550相对于主体540的近侧纵向平移。
如图17中最佳可见,微导管560与滑动件550联接,使得滑动件550的平移导致微导管560的同时平移。微导管560朝远侧延伸穿过形成于滑动件550中的镗孔554并且从其朝远侧延伸。因此应当理解,可旋转构件582沿第一方向的旋转将导致微导管560相对于针520的远侧纵向平移,并且可旋转构件582沿第二方向的旋转将导致微导管560相对于针520的近侧纵向平移。
微导管560穿过形成于主体540中的镗孔549、穿过主体540的内部541、进入针520的管腔524。主体540的镗孔549可包括密封元件(例如,刮拭密封件或o形环)(未示出),所述密封元件允许微导管560在镗孔549内并且相对于镗孔549平移同时避免流体从主体540的内部541的意外渗漏。本示例的针520的尺寸被设定成使得甚至在微导管560定位在针520的管腔内的情况下,流体仍可围绕微导管560穿过针520。微导管560可经由滑动件550的平移在针520内并且相对于针520进行平移。例如,微导管560可相对于针520朝远侧平移,直到微导管560从针520的远侧端部朝远侧延伸。
如将在下文更详细所述,在针520被定位成使得针520的远侧端部位于视网膜下腔内的情况下,微导管560可从针520的远侧端部在患者的眼的脉络膜与视网膜之间朝远侧推进到患者的眼的后部处的位置。微导管560的这种推进通过可旋转构件582沿图20a和图20b所示的第一方向的旋转来执行。微导管560为足够柔性的以适形于患者的眼的特定结构和轮廓,然而微导管560具有足够的柱强度以允许微导管560在患者的眼的脉络膜与视网膜之间推进而不屈曲。针520通常被构造成能够沿着相对于针520的纵向轴线成角度地倾斜取向的出口轴线来引导微导管560。应当理解,此类角度可有利于使微导管560沿着某个方向挠曲,以确保微导管560一直在视网膜308下面穿过视网膜下腔并且避免微导管560穿透视网膜308。
如将在下文更详细所述,微导管560限定内部管腔。在微导管560被定位在患者的眼的后部处的情况下,微导管560的管腔被构造成能够允许流体(例如,治疗剂)穿过微导管560流到微导管560的远侧端部,以便将流体递送到患者的眼的后部。一旦流体已递送到患者的眼的后部,就可将微导管560朝近侧牵拉回到针520的远侧端部内。微导管560的这种近侧平移通过可旋转构件582沿第二方向的旋转来执行。另外如将在下文更详细所述,微导管560可包括照明元件,所述照明元件被构造成能够有助于跟踪或定位患者的眼内的微导管560。
c.具有用以驱动微导管的螺纹组件致动器的示例性器械
图21-图27b示出了类似于上文所述的器械400,500的示例性另选器械600。尽管下文描述了器械600的某些特征结构和可操作性,但应当理解,除了下文所述之外或替代下文所述,器械600可根据2015年2月11日提交的名称为“methodandapparatusforsuprachoroidaladministrationoftherapeuticagent”的美国专利申请号14/619,256的教导内容中的任一个来构造和/或操作,该专利申请的公开内容以引用方式并入本文。如同器械400,500,本示例的器械600通常可用于本文所述的过程中,以将治疗流体在视网膜下递送到患者的眼。因此应当理解,器械600可易于取代器械400,500来使用以执行本文所述的医疗过程。类似于器械400,500,本示例的器械600包括针620、主体640、和微导管660。针620包括与上文所述的针420,520基本上相同的不锈钢皮下注射针。在本示例中,针620和微导管660与上文所述的针420,520和微导管460,560基本上相同。
针620从主体640朝远侧延伸。针620通常被构造成能够支撑微导管660,如将在下文更详细所述。另外将在下文更详细所述,针620具有足够的柱强度以允许针620穿过巩膜和脉络膜推进到患者的眼的视网膜下腔而不屈曲。针620具有尖型远侧端部622并且限定延伸穿过针620的内部管腔624。如将在下文更详细所述,针620的管腔624被构造成能够可滑动地接收微导管660。尖型远侧端部622被构造成能够刺穿巩膜和脉络膜层,以使得针620能够穿过这些层推进到视网膜下腔,同时不会使巩膜或脉络膜层受到其他附带创伤。本示例的远侧端部622具有刺血针构型。在一些其他型式中,远侧端部622具有三斜面构型或任何其他构型,如在2015年2月11日提交的名称为“methodandapparatusforsuprachoroidaladministrationoftherapeuticagent”的美国专利申请号14/619,256中所述,该专利申请的公开内容以引用方式并入本文。参考本文的教导内容,远侧端部622可采用的其他合适形式对于本领域的普通技术人员而言将显而易见。本示例的针620包括不锈钢皮下注射针,所述不锈钢皮下注射针的尺寸被设定成接收微导管660,同时足够小以最小化针620穿透患者的眼的组织结构时的附带伤口,如将在下文更详细所述。仅以举例的方式,针620可为23规格,但可使用其他合适的尺寸。
主体640为大体细长形状并且包括向外延伸的流体供给管线642。示出的主体640的特定形状被构造成能够被操作者抓持。另选地,主体640可安装在支撑装置或臂上以便于定位器械600,如在2015年2月11日提交的名称为“methodandapparatusforsuprachoroidaladministrationoftherapeuticagent”的美国专利申请号14/619,256中所述,该专利申请的公开内容以引用方式并入本文。
器械400,500与器械600之间的主要差异在于器械600包括能够操作以控制tuohy-borst阀的哑铃形可旋转构件652;和被构造成能够导致微导管660的平移的柱塞组件690。如图25所示,可旋转构件652可旋转地设置在形成于主体640中的类似形状的镗孔646内。可旋转构件652能够操作以在镗孔646内旋转。可旋转构件652的近侧部分通过形成于主体640的顶部表面中的开口644而相对于主体640为暴露的,使得操作者可利用其手指或拇指接合可旋转构件652,从而导致可旋转构件652的旋转。可旋转构件652的远侧部分654包括形成于远侧部分654的圆柱形镗孔656中的内部螺纹655。针620的近侧端部与锥形针座623联接,所述锥形针座623包括向外延伸的凸缘651。凸缘651与螺纹655联接以形成鲁尔接头,由此相对于可旋转构件652以不透流体的方式牢固地固定针620。当然,针620可以任何其他合适的方式固定到可旋转构件652。
管659延伸穿过可旋转构件650的圆柱形镗孔656并且终止于套圈构件645中,所述套圈构件645包括o形环形式的内部密封件657。密封件657允许微导管660在管659内并且相对于管659的平移,同时选择性地避免流体从管659的内部的渗漏。具体地讲,可旋转构件652、套圈构件645、和密封件657配合以按照某个方式形成tuohy-borst阀,这参考本文的教导内容对于本领域的普通技术人员而言将显而易见。即,可旋转构件652能够操作以抓扣管659、套圈构件645、和密封件657的组件,从而避免经由管659、套圈构件645、和密封件657的组件的近侧端部进入/离开管659的内部的流体连通。
可旋转构件652可相对于主体640旋转。由于针620牢固地固定到可旋转构件652,因此针620也可相对于主体640旋转。换句话讲,操作者可相对于主体640旋转可旋转构件652,从而相对于主体640旋转针620。针的此类旋转可为有利的,以便将远侧端部622相对于患者的眼定位在围绕针620的纵向轴线的期望角度位置处。除此之外或者另选地,操作者可希望在驱动针620穿过巩膜304时相对于主体640旋转针620,因为针620的此类旋转可降低利用针620穿透巩膜304所需的纵向力。
流体供给管线642提供到达可旋转构件652的圆柱形镗孔656的流体入口。如将在下文更详细所述,针620经由针座623与可旋转构件652的圆柱形镗孔656流体连通,使得经由流体供给管线642提供的流体(例如,由abbottmedicaloptics制造的
柱塞组件690包括可滑动地设置在主体640的近侧部分内的柱塞692。滑动件692能够操作以相对于主体640在近侧纵向位置(图26a)与远侧纵向位置(图26b)之间纵向地平移。主体692包括销694,所述销694定位在形成于主体640的顶部表面中的细长狭槽646内。销694能够操作以基于狭槽646的纵向长度来限制柱塞692的纵向平移。如图23最佳可见,柱塞692包括设置在柱塞692的外表面的相对侧并且从其延伸的一对细长突起696。突起696可滑动地设置在形成于主体640的内表面中的一对配合细长狭槽648内,以便阻止柱塞692的旋转同时允许柱塞692相对于主体640的平移。
如图27a和图27b最佳可见,微导管660与柱塞692联接,使得柱塞692相对于主体640的平移导致微导管660相对于主体640的同时平移。微导管660朝远侧延伸穿过形成于柱塞692中的镗孔698并且从其朝远侧延伸。微导管660随后穿过管659并且进入针620的管腔624。密封件657允许微导管660在管659内并且相对于管659的平移,同时避免流体从管659的内部的渗漏。
本示例的针620的尺寸被设定成使得甚至在微导管660定位在针620的管腔624内的情况下,流体仍可围绕微导管660穿过针620。微导管660可经由柱塞692的平移在针620内并且相对于针620进行平移。例如,微导管660可相对于针620朝远侧平移,直到微导管660从针620的远侧端部朝远侧延伸。
如将在下文更详细所述,在针620插入到眼内的位置以使得针620的远侧端部622位于视网膜下腔内的情况下,微导管660可从针620的远侧端部622在患者的眼的脉络膜306与视网膜308之间朝远侧推进到患者的眼的后部处的位置。针620的插入通过朝远侧推进整个器械600来执行;同时微导管660的推进通过柱塞692相对于主体640的远侧平移来执行。微导管660为足够柔性的以适形于患者的眼的特定结构和轮廓,然而微导管660具有足够的柱强度以允许微导管660在患者的眼的脉络膜与视网膜之间推进而不屈曲。针620通常被构造成能够沿着相对于针620的纵向轴线成角度地倾斜取向的出口轴线来引导微导管660。应当理解,此类角度可有利于使微导管660沿着某个方向挠曲,以确保微导管660一直在视网膜308下面穿过视网膜下腔(形成对照的是穿透视网膜308)并且最大程度地降低微导管660穿透到视网膜308内。
另外如将在下文更详细所述,微导管660限定内部管腔。在微导管660被定位在患者的眼的后部处的情况下,微导管660的管腔被构造成能够允许流体(例如,治疗剂)穿过微导管660流到微导管660的远侧端部,以便将流体递送到患者的眼的后部。一旦流体已递送到患者的眼的后部,就可将微导管660朝近侧牵拉回到针620的远侧端部内。微导管660的这种近侧平移通过柱塞692的近侧平移来执行。然后通过朝近侧牵拉整个器械600来从患者的眼内抽出针620。另外如将在下文更详细所述,微导管660可包括照明元件,所述照明元件被构造成能够有助于跟踪或定位患者的眼内的微导管660。
d.示例性针引导装置
在一些情况下,可期望提供引导装置,所述引导装置能够操作以有助于操作者相对于患者的眼301适当地对准器械400,500,600的针420,520,620。例如,此类引导装置可被构造成能够将针420,520,620沿着切向于视网膜308的路径引导到患者的眼301内,使得在穿透患者的眼301时,针420,520,620沿着路径推进,由此针420,520,620的远侧端部穿过巩膜304和脉络膜306推进到眼301的视网膜下腔。此类引导装置可呈现不同的尺寸和维度并且可提供不同的推进路径以适应每个患者的眼301的解剖差异。尽管本文描述了某些示例的变型形式,但应当理解,本文所述的器械可包括任何其他另选的特征结构,这参考本文的教导内容对于本领域的普通技术人员而言将显而易见。
图28-图39示出了示例性引导装置700。引导装置700包括环形基座710,所述环形基座710的底部表面712被构造成能够与患者的眼301的边缘区域的轮廓互补。环形基座710包括多个缝合线套环714,使得引导装置700可经由穿过缝合线套环714的缝合线715固定到患者的眼301,如图39所示。除此之外或另选地,引导装置700可经由粘合剂、吸力、微倒钩、纹理化表面、或通过操作者的接触压力和稳定作用来固定到患者的眼301。环形基座710还包括引导锚定件716,所述引导锚定件716的底部表面717也被构造成能够与患者的眼301的轮廓互补。在引导装置700固定到患者的眼301的情况下,引导锚定件716被成形为沿着患者的眼301的侧面区域延伸,如图39-图40c最佳可见。引导锚定件716包括一对缝合线套环718,使得引导锚定件716可经由穿过缝合线套环718的缝合线715固定到患者的眼301,如图39所示。除此之外或另选地,引导锚定件716可经由粘合剂、吸力、微倒钩、纹理化表面、或通过操作者的接触压力和稳定作用来固定到患者的眼301。
如图34-图36最佳可见,引导锚定件716包括完全延伸穿过引导锚定件716的多个通孔740a,740b,740c,740d。通孔740a,740b,740c,740d被构造成能够接收器械400,500,600的针420,520,620,以便引导针420,520,620以预定角度接触患者的眼301。如图34最佳可见,每个通孔740a,740b,740c,740d包括形成于引导锚定件716的顶部表面719中的倒圆开口742。倒圆开口742被构造成能够有助于操作者将针420,520,620引导到通孔740a,740b,740c,740d内。如图36最佳可见,每个通孔740a,740b,740c,740d基于由每个通孔740a,740b,740c,740d提供的进入位置和角度来限定独特的引导路径。因此,应当理解,每个通孔740a,740b,740c,740d将通过通孔740a,740b,740c,740d的内表面与针420,520,620的外表面之间的接触来沿着独特路径引导针420,520,620以接触患者的眼301。操作者可基于每个患者的眼301的个体特征(轮廓、曲率、厚度、韧度等)来确定哪条独特路径为最适当的。例如,如将在下文更详细所述,操作者可确定用于将针(420,520,620)穿过巩膜304和脉络膜306引导到患者的眼301的视网膜下腔的最适当路径。
引导装置700还包括从环形基座710向上延伸的截头圆锥形突起720。如将在下文更详细所述,截头圆锥形突起720被构造成能够接收观察透镜750,所述观察透镜750能够操作以经由穿过截头圆锥形突起720和环形基座710形成的开口722并透过眼301的瞳孔来观察患者的眼301的内部,如图33最佳可见。支撑框架730从截头圆锥形突起720向上延伸。如将在下文更详细所述,支撑框架730被构造成能够将观察透镜750选择性地固定到引导装置700并且还在使用期间对观察透镜750提供支撑和稳定性。支撑框架730包括半圆形支撑构件732。支撑构件732被弹性地偏置成图28和图29最佳可见的形状。支撑构件732包括一对弯曲凸缘734,所述弯曲凸缘734为支撑构件732提供能够操作以接收观察透镜750的喇叭形开口。
如图37和图38所示,观察透镜750可固定在引导装置700内。观察透镜750可为例如由
在观察透镜750固定在引导装置700内并且引导装置700固定到患者的眼301的情况下,操作者可使用观察透镜750来经由穿过截头圆锥形突起720和环形基座710形成的开口722并透过眼的瞳孔来观察患者的眼301的内部。如将在下文更详细所述,观察透镜750的使用可有助于操作者跟踪或定位患者的眼301内的针420,520,620和/或微导管460,560,660。应当理解,在外科手术之前或期间,观察透镜750可被移除并且可能由其他观察透镜替换,这取决于操作者的需要。
如图40-图44所示,在引导装置700的一些型式中,支撑框架730可从引导装置700省去。在引导装置700的此类型式中,观察透镜750可经由与截头圆锥形突起720的接合而固定在引导装置700内,如图43和图44所示。具体地讲,观察透镜750经由过盈或摩擦配合来接合并且固定在截头圆锥形突起720内。除此之外或者另选地,观察透镜750可经由粘合剂或通过任何其他适当的方式固定在截头圆锥形突起720内。另外,观察透镜750可由操作者固定。
如图45-图49所示,在引导装置700的一些其他型式中,除了支撑框架730之外,截头圆锥形突起720也可从引导装置700省去。在引导装置700的此类型式中,观察透镜750可经由与环形基座710的接合而固定到引导装置700,如图48和图49所示。具体地讲,观察透镜750经由过盈或摩擦配合来接合并且固定到环形基座710。除此之外或者另选地,观察透镜750可经由粘合剂或通过任何其他适当的方式固定在环形基座710内。另外,观察透镜750可由操作者固定。
如图50和图51所示,在引导装置700的另外一些其他型式中,引导锚定件716可包括从引导锚定件716向上延伸的引导管760。沿着引导管760的长度延伸的管腔762用作一个或多个通孔740a,740b,740c,740d的延伸部。一个或多个通孔740a,740b,740c,740d的这种延伸长度提供通孔740a,740b,740c,740d的内表面与针420,520,620的外表面之间的额外接触。这种增加的接触在针(420,520,620)穿过巩膜304和脉络膜306推进到患者的眼301的视网膜下腔时提供针(420,520,620)的更精确引导。
vi.用于治疗剂的视网膜下递送的示例性另选方法
图52a-图53d示出了利用上文所述的器械400进行治疗剂的视网膜下递送的示例性过程。然而应当理解,器械500,600可易于结合或取代器械400来用于下文所述的过程中。器械10,2010也可进行修改以执行下文所述的过程。另外应当理解,器械10,2010可易于进行修改以包括器械400,500,600的上述特征结构中的至少一些,即使是器械10,2010仅用于如上文参照图9a-图11c所述的从脉络膜上途径进行治疗剂的视网膜下给药的过程中。本文的教导内容可进行互换和组合的其他合适方式对于本领域的普通技术人员而言将显而易见。
仅以举例的方式,本文所述的方法可用于治疗黄斑变性和/或其他眼睛病症。尽管本文所述的过程在年龄相关性黄斑变性的治疗的背景中进行讨论,但应当理解,并非旨在或隐含具有此类限制。例如,在一些仅示例性另选过程中,可使用本文所述的相同技术来治疗色素性视网膜炎、糖尿病性视网膜病、和/或其他眼睛病症。另外,应当理解,可使用本文所述的过程来治疗干性或湿性年龄相关性黄斑变性。
尽管未示于图52a-图53d中,但该过程开始于操作者利用窥器312和/或适用于固定的任何其他器械来固定围绕患者的眼301的组织(例如,眼睑)。在操作者已选择适当的引导装置700和观察透镜750之后,将观察透镜750按照上文所述的方式固定在引导装置700内。然后将引导装置700和观察透镜750定位在患者的眼301的边缘区域上并且经由环形基座710的缝合线套环714和缝合线715固定到该边缘区域。在一些型式中,操作者首先利用缝合线715将引导装置700固定到患者的眼301;随后在引导装置700已固定到患者的眼301之后将透镜750固定到引导装置700。
在操作者已确定适当的通孔740a,740b,740c,740d之后,将针420插入到通孔(740a,740b,740c,740d)内,如图52a所示。如图52b所示,利用针420的尖型远侧端部422,操作者随后刺穿巩膜304并且相对于引导装置700推进针420,使得针420刺穿脉络膜306而不穿透视网膜308。在即将穿透脉络膜306之前,针420可在直接可视化下显示为使脉络膜306的表面“呈帐篷状”。换句话讲,针420可通过向上推压脉络膜306使脉络膜306变形,由此提供以下外观,所述外观类似于使帐篷顶变形的帐篷杆,如上文所述。操作者可使用这种视觉现象来识别脉络膜306是否即将被刺穿以及任何最终刺穿的位置。足以引起脉络膜306的“呈帐篷状”和后续刺穿的针420推进的特定量可具有任何合适的数值,所述数值可取决于多个因素,例如但不限于总体患者解剖结构、局部患者解剖结构、操作者偏好、和/或其他因素。如上所述,针420推进的仅示例性范围可介于约0.25mm和约10mm之间;或更具体地讲介于约2mm和约6mm之间。
尽管未示出,但应当理解,在一些示例中,针400,500,600可包括位于针400,500,600的外表面上的一个或多个标记物以指示各种插入深度。尽管仅为任选的,但此类标记物可为有利的,以有助于在将针400,500,600引导到患者的眼301内时标识正确的插入深度。例如,操作者可目视观察此类标记物相对于引导锚定件716和/或相对于引导管760的位置以作为针400,500,600插入到眼301内的深度的指示。仅以举例的方式,一个此类标记物可对应于针400,500,600的约6mm插入深度。
在本示例中,在操作者已通过观察到上文所述的帐篷状效果确认针420已被正确推进之后,操作者经由针420将
图53a-图53d示出了在脉络膜306和视网膜308之间被引导到治疗剂774的递送部位的微导管460。在本示例中,递送部位对应于视网膜308的地图状萎缩区域附近的眼301的大体后部区域。具体地讲,本示例的递送部位位于黄斑的上侧、感觉神经性视网膜与视网膜色素上皮细胞层之间的潜在空间中。如图53b所示,微导管460从针420的远侧端部朝远侧推进到由先导水泡770提供的空间内。微导管460为穿过眼301的视网膜308至少部分地可见的。为了增加微导管460的可见度,微导管460可包括照明元件462,所述照明元件462可通过观察透镜750进行查看。微导管460随后在脉络膜306和视网膜308之间朝远侧进一步地推进到递送部位,如图53c所示。当微导管460在患者的眼301内推进时,微导管460可在直接可视化下显示为使视网膜308的表面“呈帐篷状”。此类视觉现象可供操作者使用以识别微导管460是否已推进到递送部位。此外,照明元件462可用于增加微导管460的可见度以识别微导管460是否已推进到递送部位。
在操作者已确认微导管460已正确地推进到递送部位之后,可通过致动注射器或其他流体递送装置经由微导管460注入治疗剂774。所递送的具体治疗剂774可为被构造成能够治疗眼睛病症的任何合适的治疗剂。一些仅示例性的合适治疗剂可包括但不必限于具有较小分子或大分子的药物、治疗细胞溶液、某些基因治疗溶液、和/或任何其他合适的治疗剂,这参考本文的教导内容对于本领域的普通技术人员而言将显而易见。仅以举例的方式,治疗剂774可根据2008年8月19日公布的名称为“treatmentofretinitispigmentosawithhumanumbilicalcordcells”的美国专利号7,413,734的教导内容中的至少一些来提供,该专利的公开内容以引用方式并入本文。
在本示例中,最终递送到递送部位的治疗剂774的量为约50μl,但可递送任何其他合适的量。在一些型式中,致动脚踏开关以便从微导管460驱动出试剂774。另选地,参考本文的教导内容,可用于从微导管460驱动出试剂774的其他合适的特征结构对于本领域的普通技术人员而言将显而易见。治疗剂的递送可被观察为另一个水泡。一旦递送完成,就可通过将微导管460滑动回到针420内来回缩微导管460;并且随后可从眼301抽出针420。应当理解,由于针420的尺寸,针420穿透巩膜304和脉络膜306的部位为自密封的,使得无需采取其他步骤来密封穿过脉络膜306的递送部位。可进一步地移除缝合线715。
如上所述,可执行上文所述的过程来治疗具有黄斑变性的患者。在一些此类情况下,通过微导管460递送的治疗剂774可包括源于产后脐和胎盘的细胞。如上所述并且仅以举例的方式,治疗剂774可根据2008年8月19日公布的名称为“treatmentofretinitispigmentosawithhumanumbilicalcordcells”的美国专利号7,413,734的教导内容中的至少一些来提供,该专利的公开内容以引用方式并入本文。另选地,除了或取代美国专利号7,413,734中和/或本文在别处描述的物质,微导管460可用于递送任何其他一种或多种合适的物质。仅以举例的方式,治疗剂774可包括各种药物,所述药物包括但不限于小分子、大分子、细胞、和/或基因治疗物。还应当理解,黄斑变性仅为可通过本文所述的过程治疗的病症的一种仅示例性例子。可利用本文所述的器械和过程解决的其他生物学病症对于本领域的普通技术人员而言将显而易见。
vii.示例性组合
下述示例涉及本文的教导内容可被组合或应用的各种非穷尽性方式。应当理解,下述实施例并非旨在限制可在本专利申请或本专利申请的后续提交文件中的任何时间提供的任何权利要求的覆盖范围。不旨在进行免责声明。提供下述实施例以仅仅用于示例性目的。可设想到,本文的各种教导内容可按多种其他方式进行排列和应用。还可设想到,某些变型可省去下述实施例提及的某些特征结构。因此,下文提及的方面或特征结构中的任一个均不应被视为决定性的,除非另外例如由发明人或关注发明人的继承者在稍后日期明确指明。如果本专利申请或与本专利申请相关的后续提交文件中提供的任何权利要求包括下文提及的那些之外的附加特征结构,则这些附加特征结构不应被假定为因与专利性相关的任何原因而被添加。
实施例1
一种设备,包括:(a)主体,其中所述主体包括:(i)主体远侧端部,(ii)主体近侧端部,和(iii)流体端口;(b)针,其中所述针从所述主体远侧端部朝远侧伸出,其中所述针包括:(i)针远侧端部,(ii)针近侧端部,和(iii)限定针管腔的内壁,其中所述针管腔与所述流体端口流体连通;(c)以能够滑动的方式设置在所述针管腔中的导管,其中所述导管包括:(i)导管远侧端部,(ii)导管近侧端部,和(iii)导管管腔;以及(d)第一致动器组件,其中所述第一致动器组件被构造成能够使所述导管在所述针内并且相对于所述针平移。
实施例2
根据实施例1所述的设备,其中所述流体端口位于所述主体远侧端部与所述主体近侧端部之间的所述主体的中间区域中。
实施例3
根据实施例2所述的设备,其中所述主体限定腔室,其中所述流体端口终止于所述腔室处,其中所述针近侧端部终止于所述腔室处。
实施例4
根据实施例3所述的设备,其中所述导管穿过所述腔室。
实施例5
根据实施例1至4中任一项所述的设备,其中所述针管腔和导管的尺寸被设定成在所述针的内壁与所述导管的外表面之间限定间隙,其中所述间隙被构造成能够提供路径以用于从所述流体端口到所述针远侧端部的流体连通。
实施例6
根据实施例1至5中任一项所述的设备,其中所述针具有预成形的弯曲部。
实施例7
根据实施例1至6中任一项所述的设备,其中所述导管为柔性的。
实施例8
根据实施例1至7中任一项所述的设备,其中所述第一致动器组件包括由所述主体以能够旋转的方式支撑的控制轮,其中所述第一致动器组件能够操作以响应于所述控制轮相对于所述主体的旋转而使所述导管在所述针内并且相对于所述针纵向地平移。
实施例9
根据实施例8所述的设备,其中所述主体限定纵向轴线,其中所述控制轮能够相对于所述主体围绕垂直于所述主体的纵向轴线的轴线旋转。
实施例10
根据实施例8所述的设备,其中所述第一致动器组件包括:(i)与所述控制轮联接的小齿轮,其中所述小齿轮被构造成能够响应于所述控制轮的旋转而旋转,以及(ii)与所述导管联接的齿条,其中所述齿条与所述小齿轮接合,使得所述齿条被构造成能够响应于所述小齿轮的旋转而平移。
实施例11
根据实施例1至10中任一项所述的设备,其中所述第一致动器组件包括以能够滑动的方式设置在所述主体内的柱塞,其中所述柱塞固定到所述导管,使得所述导管被构造成能够响应于所述柱塞相对于所述主体的平移而相对于所述主体平移。
实施例12
根据实施例1至11所述的设备,其中所述针被构造成能够相对于所述主体旋转。
实施例13
根据实施例12所述的设备,还包括第二致动器组件,其中所述第二致动器组件能够操作以使所述针相对于所述主体纵向地旋转。
实施例14
根据实施例13所述的设备,其中所述第二致动器组件包括可旋转构件,其中所述可旋转构件能够相对于所述主体旋转,其中所述针被构造成能够响应于所述可旋转构件相对于所述主体的旋转而相对于所述主体旋转。
实施例15
根据实施例14所述的设备,其中所述可旋转构件被构造成能够形成tuohy-borst阀。
实施例16
根据实施例1至15中任一项所述的设备,还包括引导装置,其中所述引导装置包括:(i)被构造成能够接合患者的眼的基座,和(ii)被构造成能够接收所述针并且相对于所述患者的眼引导所述针的至少一个引导通道。
实施例17
根据实施例16所述的设备,其中所述引导装置还包括透镜接合特征结构,该透镜接合特征结构被构造成能够与观察透镜以能够移除的方式联接。
实施例18
一种治疗剂的视网膜下给药的方法,所述方法包括以下步骤:(a)使针穿过患者的眼的所述巩膜和所述脉络膜插入到所述脉络膜与所述视网膜之间的、位于所述眼的第一区域处的位置;(b)将第一流体注入到所述脉络膜与所述视网膜之间以在所述脉络膜与所述视网膜之间形成先导水泡,其中所述第一流体经由所述针注入;(c)使导管从所述针的远侧端部延伸到所述先导水泡中;(d)使所述导管在所述脉络膜与所述视网膜之间进一步延伸到所述眼的第二区域;以及(e)将第二流体注入到所述患者的眼的所述脉络膜与所述视网膜之间以在所述脉络膜与所述视网膜之间形成另一个水泡,其中所述第二流体经由所述导管注入。
实施例19
根据实施例18所述的方法,还包括将引导装置固定到所述眼,其中所述引导装置限定引导通道,其中穿过所述巩膜和所述脉络膜插入所述针的动作还包括穿过所述引导装置的引导通道插入所述针,其中所述引导通道沿着路径引导所述针以定位穿过所述巩膜和所述脉络膜的所述针。
实施例20
一种设备,包括:(a)环形基座,其中所述环形基座具有被构造成能够与患者的眼的轮廓互补的底部表面;(b)与所述环形基座相关联的多个缝合线开口,其中所述缝合线开口被构造成能够接收缝合线以由此将所述环形基座固定到所述患者的眼;(c)从所述环形基座向下延伸的引导构件,其中所述引导构件限定至少一个引导通道,其中所述引导通道被构造成能够接收针并且沿着预定义路径相对于所述患者的眼引导所述针;以及(d)透镜联接特征结构,其中所述透镜联接特征结构被构造成能够相对于所述环形基座以能够移除的方式固定透镜。
实施例21
一种治疗剂的视网膜下给药的方法,所述方法包括以下步骤:使针穿过患者的眼的所述巩膜和所述脉络膜插入到所述脉络膜与所述视网膜之间的、位于所述眼的第一区域处的位置;将第一流体注入到所述脉络膜与所述视网膜之间以在所述脉络膜与所述视网膜之间形成先导水泡;使导管从所述针的远侧端部延伸到所述先导水泡中;使所述导管在所述脉络膜与所述视网膜之间延伸到所述眼的第二区域;以及将第二流体注入到所述患者的眼的所述脉络膜与所述视网膜之间以在所述脉络膜与所述视网膜之间形成另一个水泡。
实施例22
根据实施例21所述的方法,其中所述眼的第二区域位于所述眼的第一区域的后侧。
实施例23
根据实施例21至22中任一项所述的方法,其中所述第二流体为治疗剂。
实施例24
根据实施例21至23中任一项所述的方法,其中所述方法还包括监测所述眼的内部以观察所述脉络膜的帐篷状效果的步骤。
实施例25
根据实施例21至24中任一项所述的方法,其中所述方法还包括监测所述眼的内部以观察所述视网膜的帐篷状效果的步骤。
实施例26
根据实施例21至25中任一项所述的方法,其中导管包括照明节段。
实施例27
根据实施例21至26中任一项所述的方法,其中所述方法还包括将引导装置固定到所述眼的步骤。
实施例28
根据实施例27所述的方法,其中将所述引导装置固定到所述眼的所述步骤是利用缝合线实现的。
实施例29
根据实施例27至28中任一项所述的方法,其中所述引导装置包括至少一个引导镗孔。
实施例30
根据实施例29所述的方法,其中所述方法还包括穿过所述引导装置的至少一个引导镗孔插入所述针的步骤。
实施例31
根据实施例29至30中任一项所述的方法,其中所述至少一个引导镗孔包括多个引导镗孔,其中所述多个引导镗孔中的每个引导镗孔限定独特的路径。
实施例32
根据实施例27至31中任一项所述的方法,其中所述引导装置被构造成能够与观察透镜选择性地固定在一起。
实施例33
根据实施例32所述的方法,其中所述方法还包括通过所述观察透镜监测所述眼的内部的步骤。
实施例34
根据实施例32至33中任一项所述的方法,其中所述引导装置包括与所述观察透镜选择性地兼容的支撑框架。
实施例35
根据实施例21至34中任一项所述的方法,其中所述第一流体为
实施例36
一种在治疗剂的视网膜下给药期间使用的引导装置,所述引导装置包括:基座,其中所述基座的底部表面为患者的眼的轮廓的镜像,其中所述基座被构造成能够固定到患者的眼;和引导锚定件,其中所述引导锚定件从所述基座延伸,其中所述引导锚定件的底部表面为患者的眼的轮廓的镜像,其中所述引导锚定件包括延伸穿过所述引导锚定件的至少一个引导镗孔,其中所述引导镗孔被构造成能够接收针以便沿着相对于患者的眼的路径引导所述针,其中所述路径将所述针引导到患者的眼的内部。
实施例37
根据实施例36或下述实施例中任一项所述的引导装置,其中所述基座包括至少一个缝合线套环。
实施例38
根据实施例36或下述实施例中任一项所述的引导装置,其中所述至少一个引导镗孔包括多个引导镗孔,其中所述多个引导镗孔中的每个引导镗孔限定可引导针的独特路径。
实施例39
一种在治疗剂的视网膜下给药期间使用的器械,所述器械装置包括:主体,其中所述主体包括远侧端部和近侧端部;针,其中所述针包括远侧端部和近侧端部,其中所述针从所述主体朝远侧延伸,其中所述针限定管腔,其中所述针与流体源流体联接,其中所述流体源被构造成能够将流体提供到所述针的远侧端部;导管,其中所述导管包括远侧端部和近侧端部,其中所述导管以能够滑动的方式设置在所述针的管腔内,其中所述导管能够在所述针内并且相对于所述针平移,其中所述导管限定管腔,其中所述导管与流体源流体联接,其中所述流体源被构造成能够将流体提供到所述导管的远侧端部;以及第一致动器组件,其中所述第一致动器组件被构造成能够在所述针内并且相对于所述针平移所述导管。
实施例40
根据实施例39所述的引导装置,其中所述针被构造成能够相对于所述主体平移,其中所述器械还包括第二致动器组件,其中所述第二致动器组件被构造成能够相对于所述主体平移所述针。
viii.杂项
应当理解,本文所述的任何型式的器械还可包括除上述那些之外或作为上述那些的替代的各种其他特征结构。仅以举例的方式,本文的任何装置还可包括以引用方式并入本文的各种参考文献中的任何一者内公开的各种特征结构中的一种或多种。
应当理解,本文所述的教导内容、表达、实施方案、示例等中的任何一者或多者可与本文所述的其他教导内容、表达、实施方案、示例等中的任何一者或多者进行组合。因此,上述教导内容、表达、实施方案、示例等不应视为彼此独立。参考本文的教导内容,本文的教导内容可进行组合的各种合适方式对于本领域的普通技术人员而言将显而易见。此类修改和变型旨在包括在权利要求书的范围内。
应当理解,据称以引用方式并入本文中的任何专利、出版物或其他公开材料,无论是全文或部分,仅在所并入的材料与本公开中给出的定义、陈述或者其他公开材料不冲突的范围内并入本文。同样地并且在必要的程度下,本文明确阐述的公开内容取代以引用方式并入本文的任何冲突材料。任何据称以引用方式并入本文但与本文所述的现有定义、陈述或其他公开材料相冲突的任何材料或其部分,仅在所并入的材料和现有的公开材料之间不产生冲突的程度下并入本文。
上文所述型式可被设计成在单次使用后废弃,或者其可被设计成多次使用。在任一种情况下或两种情况下,可修复型式以在至少一次使用之后重复使用。修复可包括以下步骤的任意组合:拆卸装置,然后清洁或替换特定零件以及随后进行重新组装。具体地,可拆卸一些型式的所述装置,并且可选择性地以任何组合型式来替换或移除所述装置的任意数量的特定零件或部分。在清洁和/或替换特定部分时,所述装置的一些型式可在修复设施处重新组装或者在即将进行手术前由操作者重新组装以供随后使用。本领域的技术人员将会了解,装置的修复可以利用多种技术来进行拆卸、清洁/替换以及重新组装。这些技术的使用和所得修复装置均在本申请的范围内。
仅以举例的方式,本文描述的型式可在手术之前和/或之后消毒。在一种消毒技术中,将该装置放置在闭合且密封的容器中,诸如塑料袋或tyvek袋。然后可将容器和装置放置在可穿透所述容器的辐射场中,诸如γ辐射、x射线或高能电子。辐射可杀死装置上和容器中的细菌。经消毒的装置随后可储存在无菌容器中,以供以后使用。还可使用本领域已知的任何其他技术对装置进行消毒,所述技术包括但不限于β辐射或γ辐射、环氧乙烷或蒸汽。
已经示出和描述了本发明的各种实施方案,可在不脱离本发明的范围的情况下由本领域的普通技术人员进行适当修改来实现本文所述的方法和系统的进一步改进。已经提及了若干此类潜在修改,并且其他修改对于本领域的技术人员而言将显而易见。例如,上文所述的示例、实施方案、几何形状、材料、尺寸、比率、步骤等均为例示的而非所要求的。因此,本发明的范围应根据以下权利要求书来考虑,并且应理解为不限于说明书和附图中示出和描述的结构和操作细节。
- 还没有人留言评论。精彩留言会获得点赞!