用于预测机械通气对象中流体响应性的方法和设备与流程
本发明涉及用于预测经历机械通气的对象的流体响应性的方法、呼吸设备和计算机程序。
背景技术:
血流动力学监测(即通过特定装置连续显示和记录血流动力学参数以通报心血管系统的状态)是危重疾病患者护理的基石。血流动力学监测的主要目标是评估心血管系统的功能以诊断和指导治疗任何危险的急性心血管事件。临床医生之间有一个普遍的共识,即通过保持正常的心血管状态来保持器官功能,其中向组织的氧递送很大程度上与其氧消耗相匹配。心血管不稳定性损害外周的氧递送,并且如果持续未检测到或不适当地治疗,则可影响正常的组织功能并导致器官衰竭。在血流动力学监测帮助在器官功能障碍发生之前检测任何血流动力学不稳定性,并监测旨在预防它的主动治疗干预的幅度和时间的情况中,血流动力学监测是尤其成功的。因此,血流动力学监测必须被视为在急诊、手术室和重症监护病房中接受治疗的所有危重疾病患者的初始和持续管理中的重要组成部分。一旦发生器官功能障碍,单独的血流动力学监测和治疗对改善患者的结果几乎没有帮助1-4。
心血管系统状态的最重要决定因素之一是其有效体积的血液或其血容量(volemia)。在处于健康状态的这种系统内有一定量的血液(称为正常血容量),其与正常心血管功能相关,并因此与含氧血液充分递送到所有身体组织相关。相比之下,由于例如出血、脱水、微循环衰竭、第三空间流体隔离或过度血管舒张引起的血管内容量降低或血容量不足可导致缺乏氧气向组织中的递送,并且如果严重和/或时间足够长则可导致器官衰竭。血容量固有的概念是前负荷。前负荷定义为舒张结束时心室内血液的容量,其将心肌纤维拉伸至某肌节长度,这样的长度是收缩期期间正常有效且高效的心肌收缩所必需的。心脏前负荷的任何降低将导致心脏效率的降低和不同程度的全身性低灌注,其可频繁地与正常标准血流动力学参数(例如平均动脉或中心静脉压)共存。
标准血流动力学监测系统可以容易地检测严重的血容量不足状态,但通常无法诊断中度至轻度血容量不足。这是监测重症监护患者的重要限制,因为当这样的隐匿性血容量不足保持许多小时时,其可以与若干并发症相关,例如急性肾衰竭、心脏缺血、脑卒中或伤口感染等。这种隐匿性血容量不足表现为“前负荷依赖性”,这在医学术语中意指心血管系统在Frank-Starling关系的陡峭部分中工作,如图1所示。根据这种关系,响应于血管内容量施用,心室将以心输出量的提高作为响应(更经常地表示为每搏输出量(stroke volume)SV或每个心缩期中的心室射血体积)。换句话说,患者是“流体响应性的”。
参考图1,Frank-Starling关系描述了血容量(前负荷)和心输出量(cardiac output,CO)或者每搏输出量(SV)之间的关系。在由附图标记(a)表示的容量响应性部分中,血容量提高将导致每搏输出量的相应提高。在正常血容量患者中,相同的容量增量将仅导致SV中的非常适度的提高或根本没有提高,如由附图标记(b)表示的情况所示。在容量超负荷状态(Frank-Starling关系的平坦部分)中,任何给定容量不会影响SV,但可能导致肺和身体的流体超负荷。
这里要做的重要区分是,流体响应性并不一定意指患者为低血容量,由于静脉系统的高容纳量,流体响应性是正常的生理状态。这只是告诉我们,心血管系统将以一定的CO的提高来响应于静脉内流体施用。
静脉内流体施用被认为是对血流动力学不稳定的患者恢复正常血容量(或换句话说,优化前负荷)的一线干预。已有证据表明,通过容量加载来优化高风险手术患者改善了血流动力学并降低了术后并发症的发生率和住院死亡率5-7。然而,只有50%的血流动力学不稳定的患者是流体响应性的,并且已经清楚地确定,过量的静脉内流体(即过度复苏)与死亡率的提高相关,因为其可导致肺水肿、肺源性心脏病恶化或诱导左心衰竭,如所附参考文献列表的参考文献8中所讨论的。
因此,流体响应性的常规评估(即对其中静脉内流体施用将改善血流动力学的患者的预期鉴定)正成为目标导向流体治疗方案的重要组成部分,其目的在于优化血管内容量状态和避免流体超负荷的有害后果9,10。
用于流体响应性评估的现有技术
对有效的血管内血容量和流体响应性状态的正确评估仍是ICU医生和麻醉医师处理血流动力学不稳定的患者的主要挑战之一。然而,关于流体治疗的类型、量和时间安排的决定具有很大的临床相关性,因为血容量不足和血容量过高均与提高的发病率和死亡率相关。然而,没有例如金标准参数这样的事情,因此前负荷仍然难以临床评估。
为了以可接受的准确度确定患者的心血管状态和流体响应性的状态,临床医生必须评估可用血流动力学变量对产生足够幅度的扰动的限定干预的动态响应。这是功能性血流动力学监测概念背后的核心原则之一,其是使用主动干预来内插生理数据的多能方法,从而鉴定具有稳健的灵敏度和特异性的临床参数,进而鉴定心血管不稳定性和容量响应性11。两种最完善的干预措施是流体激发(fluid challenge)和被动腿部抬升(passive leg raising,PLR)操作。在流体激发期间,在短时间内静脉内输注指定量的体积。PLR是前负荷再分配操作(即一种自体输注),在该操作期间,将仰卧位躺着的患者的腿相对于水平面升高45°,而躯干保持在水平位置20-30秒。在这两种操作中,评价其响应的参考方法是测量心输出量或者说每搏输出量的变化。根据大多数公开文献的阳性响应是提高10至15%。
由于SV的测量的困难和侵入性,有数种临床血流动力学指标可用于评价或更好地预测容量响应性(参见表1)。静态指标包括经典的侵入性和非侵入性压力和容积测定参数。动态指标主要包括来自于机械通气期间心肺相互作用的指标。在具体情况中,静态指标可以与例如通过心脏充盈压测量的患者容量状态相关,但是已经反复证明这是非常差的容量响应性预测因子,因此对于指导流体治疗几乎没有用处。动态指标(例如脉搏压或每搏输出量变化)由于其简单性和健全的生理基础而引起了极大的兴趣。它们已在不同的患者人群中被证明是比静态指标更好的流体响应性的预测因子10-12。然而,目前公认的是,它们在ICU患者中的预测值比先前认为的差得多,并且只有2%的患者满足有效性标准以通过这些指标的方式适当地预测流体响应性13。下表说明了一些用于评估心脏前负荷和流体响应性的临床使用的静态和动态指标:
其中CVC=中心静脉导管(central venous catheter),PAC=肺动脉导管(pulmonary artery catheter),SVC=上腔静脉(superior vena cava),IVC=下腔静脉(inferior vena cava),以及EchoC=超声心动描记术(echo cardiography)。
现在,将更详细地讨论根据现有技术的用于评估流体响应性的干预的两个实例。
流体激发:
流体激发由在确定的短时间内迅速静脉内输注一定量的流体(类晶体或胶体)组成,以寻找对血流动力学参数的改善,其通常是收缩压或更常见的是每搏输出量的提高(即通过将心输出量除以心率而获得的心脏每次收缩期收缩所射出血液的体积)。对于限定充分流体激发的绝对量、流体类型和输注速率应该如何,尚缺乏共识。此外,如上所述,只有50%的危重疾病患者对流体激发有响应(响应者),并且这种不可逆的干预将总是在其余的50%的患者(无响应者)中引起不希望的、不必要的并且经常有害的流体超负荷。
被动腿部抬升操作:
被动腿部抬升(PLR)操作是可逆和动态的策略,其用于通过将腿抬高20-30秒并观察血流动力学响应来评估前负荷,所述血流动力学响应在临床上评估为心输出量、每搏输出量或收缩期动脉压的提高。由于从腿部向心脏的血液的自体输注,前负荷依赖性患者的心输出量提高。优点是没有额外的流体被注入,从而使潜在有害的流体超负荷的风险最小化。因此,可以反复执行PLR操作。然而,在该干预中还存在限制。首先,其通常不能在手术室中执行,并且不是所有ICU患者都可以经受这种操作。此外,在具有提高的腹内压的患者中的准确度较差。最后,其取决于患者的实际血容量状态(循环血液容量的量),使得预期的效果降低,并且在患有严重降低的血容量的患者中更难以解释。
现在,将更详细地描述用于根据现有技术评估流体响应性的评估和指标的一些实例。
临床评价
皮肤肿胀、患者的活力和认知状态、尿排出量、血压和心率、外周灌注和毛细血管再充盈时间是用于测定流体响应性的非特异性、主观和不可靠的临床体征14-16。这对于那些不明确的血容量不足并且具有轻度至中度前负荷依赖性的患者尤其如此。
血流动力学指标
上表中列出的基于压力的参数在临床上经常用于估计患者的前负荷状态。然而,它们对流体响应性的预测值非常有限,因为在大多数临床情况下心室或血管顺应性不是线性的,并且因此使得压力相关参数是血管内容量的不良替代。因此,那些血管内压力的增量/减量通常与血管内容量或心室前负荷的相应变化不匹配。另外,例如在心肌梗死后所见或由于高胸内压力造成的心脏跨壁压的变化可能在使用这些静态参数时被误解为血容量不足患者的过度血容量。静态参数一般是更准确的前负荷估计,但其或是侵入性的(RVEDV,GEDV)、主观的(LVEDA)或仅是间歇性评估的(GEDV,LVEDA)。
动态血流动力学指标:
脉搏压变化(pulse pressure variation,PPV)和每搏输出量变化(SVV)分别指在机械呼吸周期期间脉搏压波形的幅度和左心室喷射的血液体积的变化。在吸气正压呼吸循环期间看到的前负荷的减小和后负荷的提高表现为在呼气阶段期间脉搏压波形或每搏输出量的幅度的减小(作为全身动脉压波形的收缩部分下的面积测量)。这些参数的吸气和呼气值之间的相对差异定义了PPV和SSV。在前负荷依赖患者中,正压机械吸气期间胸内压力的吸气提高对于脉搏压幅度和每搏输出量比在正常血容量患者中具有大得多的影响。一般来说,确定的是高于13%的PPV和/或SSV即鉴定为容量响应者或前负荷依赖性患者。这些参数的优点是在理论上它们连续地指示患者的容量响应性的状态,而不需要测量心输出量或探测性流体激发。然而,这些指标有几个重要的限制。它们的性能受所应用的呼吸机设置的影响(一般需要比推荐用于肺保护性通气的更大的潮气量),并且它们仅在被动通气条件下,而没有患者的任何自主呼吸活动的情况下是可靠的。此外,它们受许多混杂因素的影响,并因此在ICU患者中观察到的数种常见病症(例如心律不齐或肺动脉高压)中不可靠。毫不奇怪,在最近的临床前瞻性评价中,只有3%的ICU患者符合使用PPV和SVV来预测容量响应性的有效性标准。
其他动态指标
通过多普勒超声心动描记术评估的主动脉流速的呼吸变化预测了机械通气患者的流体响应性17。类似地,通过回波描记术测量的上腔静脉和下腔静脉直径的循环变化已被用于检测机械通气患者中的前负荷依赖性。建议用扩张指标反映这种变化18。这些技术的限制是适当的超声设备的可用性、测量的间歇和主观性质以及对本领域的专家的需要。呼气末闭塞试验由通过呼气末闭塞的机械充气中断组成,其可以充分提高心脏前负荷以用于预测流体响应性。如果所述操作将心输出量提高超过15%,则认为该患者是流体响应者。
从上述讨论可以看出,希望有用于预测流体响应性的新技术,其满足以下目标:
-可逆性,意指临床测试不应对心血管系统或全身器官造成任何持久的潜在有害影响。例如上述讨论的流体激发的技术可与无响应患者中的严重并发症相关,导致不期望的和潜在的有害流体超负荷。
-动态性,意指新型技术导致心血管系统在一定程度上短时间地受到压力,以暴露前负荷依赖性。这样的动态操作已经反复地表现出比用于确定流体响应性的静态指标更精确。
-没有或最小化的侵入性,意指在流体响应性的评估中使用的任何血流动力学参数应理想地获得,而不穿透皮肤屏障或用导管或其他装置侵入心血管系统,从而避免严重的并发症,例如出血或感染。
-基于实时,意指在流体响应性的评估中使用的任何所监测参数必须具有这样的时间分辨率,其允许在连续或接近连续的基础上检测任何血流动力学变化,例如以逐次心跳或逐次呼吸为基础。
技术实现要素:
本发明的目的是提供用于预测经历机械通气的对象的流体响应性的方式。
本发明的另一个目的是提供清除或至少减轻与上述现有技术相关的一个或更多个缺点的这种方式。
本发明的另一个目的是提供能够容易和可靠地预测临床实践中在对象床边的机械通气对象的流体响应性的方式。
本发明的另一个目的是提供能够非侵入性地预测机械通气对象的流体响应性的方式。
从下文中的详细描述中将显而易见的是,这些和其他目的通过独立权利要求1所定义的用于预测对象的流体响应性的方法、独立权利要求10所定义的用于预测对象的流体响应性的计算机程序、以及独立权利要求12所定义的用于预测对象的流体响应性的呼吸设备来实现。
根据本公开内容的一个方面,提供了用于预测与能够向其提供机械通气的呼吸设备相连接的对象的流体响应性的方法。所述方法包括以下步骤:
-监测指示所述对象中二氧化碳清除程度(VCO2)的至少一个参数;
-应用呼气末正压(positive end-expiratory pressure,PEEP)操作,其中施加于所述对象的PEEP从第一PEEP水平改变为第二PEEP水平,以及
-基于PEEP的所述改变之后的所述至少一个所监测参数的变化来预测所述对象的流体响应性。
所提出的方法是非侵入性的,无血管内导管,完全可逆而不需要任何流体输注,动态(PEEP的变化)且实时监测对于PEEP变化的VCO2响应(VCO2的变化)。这种与CO2动力学有关的事件的特定组合允许容易地在床边诊断前负荷依赖性,而不需要在根据现有技术的系统中使用的高级的侵入性且昂贵的血流动力学监测。
此外,所提出的方法区分了由前负荷的变化引起的肺灌注的改变和由右心室收缩性的改变引起的肺灌注的改变。这是因为PEEP对心肌收缩本身没有任何影响,但它在正常血容量患者中最低限度地影响右心室每搏输出量和肺灌注,但在低血容量患者中有高度影响。换句话说,PEEP的变化(例如PEEP的逐步提高)将仅改变那些前负荷依赖的患者的血流动力学。
根据该方法的一个实施方案,作为在PEEP的所述改变之前的所述参数的基本上稳态水平(即基线水平)和在PEEP的所述改变之后的所述参数的新的基本上稳态水平之差异来确定所述至少一个所监测参数的变化。
根据该方法的一个实施方案,基于在PEEP的所述改变之前获得的所述至少一个所监测参数的至少一个前PEEP调整值与PEEP的所述改变之后获得的所述至少一个所监测参数的至少一个后PEEP调整值之差异来确定所述变化。
根据该方法的一个实施方案,在PEEP的所述改变之后10-120秒、优选30-90并且最优选45-75秒获得所监测参数的所述至少一个后PEEP调整值。在一个优选实施方案中,在PEEP的所述改变之后约1分钟获得至少一个后PEEP调整值。这是因为在大约5cmH2O的PEEP的适当变化之后,大多数通气对象中的VCO2在变化后约1分钟已经达到基本上稳定的状态。
根据该方法的一个实施方案,所述所监测参数是对象的实际VCO2,因此所述预测基于对象在PEEP的所述改变之后的CO2清除的变化(ΔVCO2)。可以根据对象呼出的呼出气体的所测量流量或体积以及指示所述呼出气体中存在CO2的所测量参数(例如呼出气体中CO2的分压、浓度或体积)来确定对象的VCO2。在一个优选实施方案中,通过体积二氧化碳图(volumetric capnography)确定对象的VCO2。
根据该方法的一个实施方案,所述预测包括以下步骤:如果CO2清除的变化(ΔVCO2)超过预定阈值,则判断通气对象是流体响应性的。所述阈值应优选为基线VCO2(即在PEEP变化之前VCO2的稳态水平)的至少5%、更优选至少10%并且甚至更优选至少11%。
优选地,经由至少5cmH2O的PEEP变化来进行PEEP操作。在一个实施方案中,所述PEEP变化是5或10cmH2O的PEEP逐步提高或降低。在一个优选的实施方案中,所述PEEP变化是5或10cmH2O的PEEP的逐步提高。
根据该方法的一个实施方案,在改变PEEP以便确定至少一个所监测的VCO2相关参数之变化的步骤之前进行预调节操作(preconditioning maneuver),其中向对象提供提高压力和提高PEEP的呼吸序列(sequence ofbreaths)。这具有使在PEEP激发期间(即在改变的PEEP水平下的通气期间)的任何显著的肺再扩张作用最小化的作用,并且因此用于提高流体响应性预测的准确性。
该方法还可以包括以下步骤:基于所述预测的结果向进行所述方法的呼吸设备的操作者以视觉和/或听觉的方式发信号通知(signaling)是否判断所述对象是流体响应性的。这可以例如通过在所述呼吸设备的显示单元上显示指示符来实现,所述指示符指示是否判断对象为流体响应性的。
在一些实施方案中,该方法可以包括以下步骤:基于在PEEP的所述改变之后的所述至少一个所监测参数的变化计算对象的流体响应性指标,以及将所述流体响应性指标以视觉和/或听觉的方式传达给所述呼吸设备的操作者。该流体响应性指标可以是在多级量表(例如1-5或1-10之间的量表)上指示对象的流体响应性程度的多级指标。
在一个实施方案中(以下中称为剂量响应实施方案),所述方法包括以下步骤:基于使所述至少一个所监测参数超过某一预定阈值所需的PEEP的变化来预测所述对象的流体响应性程度。剂量响应实施方案可以包括以下步骤:逐步改变施加于对象的PEEP直到至少一个所监测参数超过所述阈值(例如基线VCO2的11%),以及基于使所述至少一个所监测参数超过所述阈值所需的PEEP的变化来预测所述对象的流体响应性程度,也就是说基于在所监测参数中获得特定响应所需的“剂量”。例如,在5cmH2O的PEEP变化(例如从5变化至10cmH2O)后,所监测的VCO2值的变化超过例如基线VCO2的11%的阈值的患者可以被鉴定为严重血容量不足的患者,而除非PEEP的变化为至少10cmH2O,否则所监视的VCO2的变化不超过所述阈值的患者可以被鉴定为中度血容量不足的患者。对于其中所监测的VCO2值响应于例如10cmH2O的PEEP的变化仅轻微变化(即,VCO2<阈值的变化)的患者可以被鉴定为轻度血容量不足的患者。提供给使用上述原理判断为流体响应性之患者的血管内流体量可有利地根据使用所提出的剂量响应程序所预测的患者流体响应性程度来选择。因此,可以基于指示通气患者是否患有轻度、中度或严重血容量不足的非侵入性测试来选择流体的量。
因此,上述基于在PEEP的所述改变之后的所述至少一个所监测参数的变化来预测对象的流体响应性的步骤可以包括基于以下任一项或两者来预测对象的流体响应性程度的步骤:i)在施加到对象的PEEP中的某种预定变化之后的至少一个所监测参数的变化,以及ii)使得在所述至少一个所监视参数中的变化(在幅度上)超过特定阈值所需的PEEP变化。
根据本公开内容的另一方面,提供了用于预测与向其提供机械通气的呼吸设备相连接的对象的流体响应性的计算机程序。所述计算机程序包含计算机可读代码,当由呼吸设备的处理单元执行时,该计算机可读代码使呼吸设备执行根据上述实施方案中的任一项的方法。
因此,根据一个实施方案,当由处理单元执行时,计算机程序使呼吸设备:
-监测指示对象的VCO2的程度的至少一个参数;
-将施加于对象的PEEP从第一PEEP水平改变为第二PEEP水平,以及
-基于PEEP的所述改变之后的所述至少一个所监测参数的变化来预测对象的流体响应性。
根据本公开内容的另一方面,提供了用于预测与呼吸设备相连接的对象的流体响应性的呼吸设备。所述呼吸设备包含:
-PEEP调节装置,例如用于调节由对象呼出的呼出气体流的呼气阀,其配置成调节施加于所述对象的PEEP;
-控制单元,其用于控制所述PEEP调节装置并用于监测指示对象的VCO2程度的至少一个参数,
其中所述控制单元配置成控制所述PEEP调节装置以将施加于所述对象的PEEP从第一PEEP水平改变为第二PEEP水平,并且基于PEEP的所述改变之后的所述至少一个所监测参数的变化来预测对象的流体响应性。
呼吸设备还包含传感器装置(例如二氧化碳分析仪并且优选体积二氧化碳分析仪),其配置成测量由对象呼出的呼出气体的流量或体积,以及指示所述呼出气体中存在CO2的参数,例如呼出气体中CO2的分压、浓度或体积。在一个实施方案中,控制单元配置成从所述测量参数中计算对象的VCO2,其中对象的VCO2是由控制单元在流体响应性的预测中监测和使用的参数。
在一个实施方案中,控制单元配置成作为在PEEP所述变化之前的所述参数的基本稳定状态水平与在PEEP所述变化之后的所述参数的新的基本上稳态水平之差异来确定至少一个所监测参数中的所述变化。
在一个实施方案中,控制单元配置成基于在PEEP的所述改变之前获得的所述至少一个所监测参数的至少一个前PEEP调整值与PEEP的所述改变之后获得的所述至少一个所监测参数的至少一个后PEEP调整值之差异来确定所述至少一个所监测参数的变化,其中在PEEP的所述改变之后10-120秒获得所监测参数的所述至少一个后PEEP调整值。
根据一个实施方案,指示对象的二氧化碳清除的所监测参数可以是实际的二氧化碳清除本身,并且控制单元可以配置成基于PEEP变化之后对象的二氧化碳清除的变化(ΔVCO2)来预测对象的流体响应性。
在一个实施方案中,控制单元配置成如果所述CO2清除的变化(ΔVCO2)超过预定阈值,则判断对象是流体响应性的。
在一个实施方案中,控制单元配置成通过在改变PEEP之前向对象提供提高压力和提高PEEP的呼吸序列以执行预调节操作,以便确定所述至少一个所监测参数的变化。
在一个实施方案中,控制单元配置成基于所述预测的结果以视觉和/或听觉的方式向呼吸设备的操作者发信号通知是否认为对象(3)是流体响应性的。
在一个实施方案中,控制单元配置成基于PEEP所述变化之后的所述至少一个所监测参数的变化计算所述对象的流体响应性指标,并且将所述流体响应性指标以视觉和/或听觉的方式传达给呼吸设备的操作者。
在下文中的详细描述中将描述本发明的另一些有利方面。
附图说明
从下文中提供的详细描述和仅通过举例说明的方式给出的附图中将更充分地理解本发明,其中:
图1示出了Frank-Starling曲线,其为通过施用血管内容量的流体而获得的响应于前负荷变化的心输出量或每搏输出量的提高;
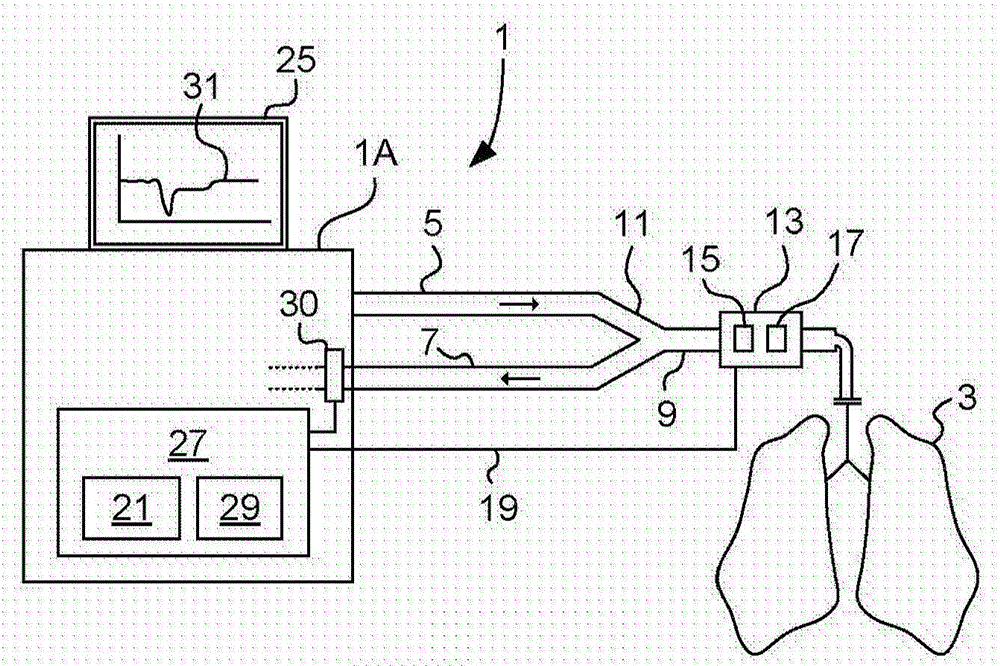
图2示意性地示出了根据本公开内容的实施方案的呼吸设备,其配置成用于预测通气对象的流体响应性;
图3示意性地示出了在对象的肺的肺泡中发生的肺气体交换的模型;
图4示出了举例说明在经受呼气末正压的变化之前、期间和之后的通气患者的二氧化碳清除之变化的图;
图5示出了图4中举例说明的通气患者的二氧化碳清除变化的图的一部分。
图6示出了举例说明根据本公开内容的一个实施方案用于预测流体响应性的方法的流程图。
具体实施方案
图2示出了根据本发明的一个示例性实施方案的呼吸设备1。在该实施方案中,呼吸设备是用于向与通气机相连接的患者3提供通气治疗的通气机。通气机经由用于向患者3供应呼吸气体的吸气管线(inspiratory line)5和用于将呼出气体从患者3递送离开的呼气管线(expiratory line)7与患者3相连接。吸气管线5和呼气管线7通过所谓的Y形件(Y-piece)11与公共管线(common line)9相连接,所述公共管线通过患者连接器例如气管内管与患者3相连接。
配置成用于体积二氧化碳测量的二氧化碳探测仪13布置在患者3的气道开口附近。在该示例性实施方案中,所述二氧化碳探测仪13布置在公共管线9中并暴露于患者3呼出和吸入的所有气体。二氧化碳分析仪13包含用于至少测量患者3呼出的呼出气体的流量或体积的流量或体积传感器15,以及用于检测在至少所述呼出气体中存在CO2的CO2传感器17。为此,二氧化碳分析仪13可以配置成测量指示肺泡CO2的任何合适的参数,例如呼出气体中CO2的分压(PACO2)、CO2浓度或CO2的体积。通常但不一定的是,二氧化碳分析仪13配置成还测量由患者3吸入的吸入气体的流量或体积以及指示吸入气体中存在CO2的参数。
二氧化碳分析仪13经由有线或无线连接19与通气机相连接,并且配置成将流量或体积和CO2测量值传送到通气机,以由通气机的处理单元21进一步处理。通气机优选地配置成从二氧化碳分析仪13接收的流量和二氧化碳测量值中产生体积二氧化碳描记图,并且另外地在通气机的显示器25上显示体积二氧化碳描记图。
处理单元21通常是通气机的控制单元27的一部分,所述控制单元27还包含存储计算机程序的非易失性存储器或数据载体29,所述计算机程序使得处理单元21根据本发明的原理预测患者3的流体相应性,这通常基于从二氧化碳分析仪13接收的流量或体积和CO2测量值,如将在下文中更详细地描述的。
控制单元27还配置成根据所述计算机程序的指令控制呼吸设备的呼气阀30,以便根据需要调节施加到通气对象3的呼气末正压(PEEP),从而根据本公开内容的原理预测对象3的流体响应性。
通气机还配置成在显示器25上显示与所预测的患者3的流体响应性相关的信息。优选地,所述信息包含指示符,其指示是否认为患者3是流体响应性的(即,流体响应者)或者认为患者3不是流体响应性的(即不是流体响应者)。通气机还可以配置成在显示器29上显示CO2清除(VCO2)趋势曲线31,其示出了患者3随着时间的CO2清除的变化。下面将参照图4更详细地描述VCO2趋势曲线31。
通气机1还包含用户界面(user interface),通气机的操作者可以通过所述用户界面控制通气机1的操作。用户界面可以包含显示器25,其可以包含允许操作者经由显示器25向通气机输入控制命令的触摸屏,和/或包含一个或更多个机电致动器的控制面板(未示出),操作者可以通过所述控制面板控制通气机1的操作。在一个实施方案中,通气机1配置成允许通气机操作者经由所述用户界面输入指示通气机1执行流体响应性检查的命令,其中根据本发明的原理预测当前连接到通气机1的患者3的流体响应性,现在将参考图2-5来描述所述原理。
所提出的用于评估流体响应性的技术背后的基本原理将正压通气并且特别是呼气末压力(PEEP)对于血流动力学和肺灌注的作用与它们如何影响CO2的身体动力学相组合。
正压通气和PEEP
在正压机械通气患者中的前负荷依赖性的发生率较高5。这与在整个呼吸周期中保持正气道压力的事实有关。这是对正常呼吸的极大对抗,其中经肺压力在吸气阶段期间保持为负,实际上将血液从体循环吸入胸部和右心。这种在正压通气过程中改变了的生理学显著地改变了呼吸对血流动力学的循环效应。它干扰静脉回流,因为主要静脉(进入胸腔的上和下腔静脉)被正胸内压压缩。这继而是RV每搏输出量减小的原因,由于心血管系统的串联构造,RV每搏输出量对LV每搏输出量具有即时影响。这种效应在临床上被认为是心输出量和主要是收缩期血压的降低。这是几乎所有新插管和机械通气患者的流体依赖性的首要的主要决定因素,所述患者需要可变量的静脉内流体来补偿这种效应。然而,存在控制心肺相互作用的其他机制,其降低前负荷或提高后负荷,从而损害RV功能,并因此损害通气患者的血流动力学。在机械通气期间施加的压力越高并且患者的血容量越低,这些负面影响可理解地将越大。它们一般可以总结如下:
-静脉回流降低:
a.压缩进入胸腔处的大静脉(上腔静脉和下腔静脉)
b.低右心房顺应性,其导致提高的右心房压力,这降低静脉回流压力梯度
-提高RV后负荷:
a.在正压通气期间的肺泡压力和PEEP提高,其压缩肺泡毛细血管从而提高肺血管阻力
b.肺塌陷,其降低肺毛细血管的横截面积并降低总肺容积,这两者都导致肺血管阻力提高
PEEP对血流动力学的影响
特别感兴趣的和广泛研究的主题是PEEP对血流动力学的影响。PEEP的使用提高了呼吸系统的“工作压力”,其将从在呼吸静止条件期间(即,在呼气末期)生理上保持的“正常”大气压改变到由PEEP确定的水平。这直接影响在机械递送周期期间所观察到的所有其他变化,并且将导致额外的心血管应激,其在呼气期间不从正压释放。总之,上述负血流动力学效应将通过添加PEEP而增强。
由于其已知的血流动力学效应,PEEP激发可以是一种有价值的替代性干预,以评估这种施加的应激对心血管系统和不同血流动力学或灌注变量的动态相互作用。PEEP激发可以定义为在PEEP水平上受控的阶跃变化(step change)(例如提高),所述阶跃变化是在限定的通气条件下足够大的变化。阶跃变化的大小取决于用于评估它的变量、肺的状态,并且取决于血容量,如在严重血容量不足患者中,PEEP的过度提高可导致心输出量的危险的降低。
作为肺灌注标志物的CO2
CO2遵循公知的身体动力学,其由以下四个步骤组成:
步骤I)代谢:体细胞代谢产生CO2;
步骤II)通过循环输送:CO2通过静脉血向右心脏和肺循环输送;
步骤III)扩散:CO2从肺毛细血管扩散到肺泡,以及
步骤IV)肺泡通气:通过肺泡通气清除CO2。
可以通过体积二氧化碳分析实时地非侵入性地监测这样的CO2动力学;即一次呼吸中的呼气体积的CO2的图形记录。这在图3中示出,其示意性地示出了在第一步骤I中发生的体细胞的CO2的代谢产生,在第二步骤II中发生通过静脉血向肺运输CO2,在第三步骤III中进行从肺毛细血管扩散到肺泡中的CO2扩散,以及在第四步骤IV中通过肺泡通气进行的CO2清除。在图3中,附图标记A表示代表其中发生扩散的肺泡和肺毛细血管的要素,而附图标记13表示图1中的二氧化碳分析仪,其与显示体积二氧化碳描记图33的显示器25相连接,其中为患者3的最后一次呼气将PACO2(y轴)相对于呼出气体体积(x轴)作图。体积二氧化碳描记图的主要变量是曲线下面积,其代表在单次呼吸中清除的CO2量。当将该值乘以呼吸速率(respiratory rate,RR)时,其产生每单位时间的CO2的肺清除,例如一分钟(VCO2)。
从体内清除CO2的唯一方式是通过遵循上述顺序和单向动力学。因此,如在机械通气患者中通常所观察到的,如果代谢(步骤1)和肺泡通气(步骤4)保持恒定,则VCO2是肺血流量的良好标志物。这个事实构成了使用Fick原理和部分再呼吸CO2技术的非侵入性确定有效肺血流量的基础。由于肺血流量取决于血容量(或前负荷)和右心室收缩力两者,因此任何血容量不足或收缩性的降低将减弱CO2的清除,反之亦然19-21。
一些出版物已经描述了潮气末CO2(PETCO2)的使用,即将一次呼吸中CO2的终末浓度/分压作为评估响应于不同干预的动态血流动力学变化的非侵入性参数20,21。这些研究基于上述的体内CO2动力学,并且用标准的基于时间的二氧化碳描记图而非所提出的体积二氧化碳描记图来进行。因此,Monge等人和Monnet等人表明,PETCO2可用于检测机械通气患者中的前负荷依赖性22,23。他们应用PLR操作来向心血管系统施压,并比较在PETCO2中所观察到的相比于标准侵入性心脏指标测量的血流动力学响应。在这些参数之间发现的良好的相关性证实了CO2对于血流动力学评估的临床作用。
然而,VCO2被认为是比PETCO2更好地确定肺血流量变化的参数,因为VCO2还包括了取决于通气和与肺泡毛细血管膜接触的血液量的“流量”(即依照时间的体积)的尺度。这意指VCO2与肺灌注和通气二者成正比。因此,由前负荷修正引起的肺血流量的任何变化将通过VCO2的变化来检测。相反,PETCO2是主要取决于来自静脉血的CO2的被动扩散的“分压”,并且与肺泡通气成反比。这些特征使得PETCO2对于检测由前负荷修正所引起的肺血流量的变化比VCO2更不敏感。
基于受PEEP调整诱导的CO2清除变化预测流体响应性
本公开内容提出了用于基于对VCO2的分析(优选地通过体积二氧化碳描记图)来检测前负荷依赖性患者的新技术。这种技术将向心血管系统施压的完全可逆和动态操作(逐步和短暂提高/降低PEEP)与非侵入性且实时监测血流动力学响应(通过体积二氧化碳描记图评估VCO2)相组合。
因此,所提出的用于检测流体响应性的方法的一些关键特征是引入通气患者的PEEP变化以及确定在PEEP的所述改变之后CO2清除变化的步骤。
如上所述,所提出的技术区分了由前负荷变化导致的和由于右心室收缩力变化而引起的肺灌注改变,因为PEEP对正常血容量患者的心肌收缩性没有影响,但对血容量不足患者的血流动力学有很高的影响。因此,PEEP的变化(例如PEEP的逐步提高)将仅改变那些前负荷依赖性患者的血流动力学。
然而,PEEP的效果并不总是容易预测,这取决于肺的基础状态。PEEP的提高伴随地提高吸气压力,并且这可以导致部分塌缩单元的复张(recruitment)。这将具有两个主要结果:1)它将提高毛细管横截面面积,因为它还将使灌注这些区域的毛细血管复张,以及2)将改善这些新复张单元的氧的区域肺泡张力,恢复缺氧性肺血管收缩效应。这两种效应将倾向于改善RV功能,因为它们将降低肺血管阻力并且因此减轻RV后负荷。这继而将模糊PEEP的阶跃提高的血流动力学响应,因为它将抵抗心输出量的预期降低。只要这种非故意复张效应的程度不可预测,则PEEP激发来评估血流动力学状态的特异性和敏感性将不可避免地降低。克服这种限制的一种可能的方式是执行在先的肺预调节操作以再次扩张塌缩的气道和容易再扩张的肺部区域一一肺容积的一种均一化。该预调节操作由在较高压力下的几次呼吸的序列组成,即与基线通气相比的提高压力的呼吸序列。优选但不必需的是,所述提高压力的呼吸也在较高的PEEP下递送,即在与基线通气相比提高的PEEP水平下递送。目的是在PEEP激发期间使任何显著的肺再扩张效应最小化。
优选地,动态操作由以下组成:首先是短预调节操作,以及在短稳定期之后的持续一分钟的在基线PEEP之上的PEEP的阶跃提高,之后再次将其减小到基线值。
应当注意的是,上述预调节操作不是该术语的常规含义中的肺复张操作,而是用于使患者的肺容积均一化的预调节操作。例如,在一些情况下,预调节操作可以由在大约10ml/kg的提高的潮气量的情况下施加10次呼吸(例如对应于与基线通气相比的20-30%的压力提高)和与基线通气相比提高5cmH2O的PEEP水平组成。
图4示出了根据本公开内容的原理在所提出的用于预测患者流体响应性的操作期间的PEEP和VCO2的记录(不与上面讨论的预调节操作混淆,其有利地在所提出的用于预测对象流体响应性的操作之前执行)。
最初,在操作之前确定基线VCO2(A),即在基线PEEP通气期间的VCO2水平。之后,PEEP突然提高5cmH2O使肺内保持一定体积的气体,因此VCO2由于存储在肺内的CO2被无CO2的吸入气体(B)暂时稀释而降低。一段时间后,在呼出的CO2中达到新平衡的阶段(C)(在图中的第二分钟结束时),并且分析该阶段中的最后四次呼吸。然后PEEP值返回到基线PEEP,使VCO2返回到基线VCO2(D)。
图5示出了由图4中的参考标号E表示的VCO2曲线的部分,即VCO2曲线的示出了在PEEP变化之后VCO2变化的部分。根据本发明的一个实施方案,在基线VCO2(A)与PEEP变化之后的VCO2的新稳态期间的VCO2水平(C)之间的VCO2差或变化(下文中称为ΔVCO2),是用于预测通气患者的流体响应性的参数。因此,参数ΔVCO2表示图4中点(A)与点(C)之间的VCO2差,并且ΔVCO2的幅度是PEEP变化后VCO2的(正或负)变化。
如果ΔVCO2的幅度超过预定阈值,则通气患者被判断为“响应者”,即为前负荷依赖性的并因此是流体响应性的患者。另一方面,如果ΔVCO2的幅度不超过所述预定阈值,则认为患者是“无响应者”,其被判断为不是流体响应性的。
优选地,ΔVCO2的幅度的阈值设置为基线VCO2的大约10%,并且甚至更优选设置为基线VCO2的大约11%。因此,根据本发明的一个实施方案,如果ΔVCO2≥基线VCO2的11%,则通气患者被判断为是流体响应性的。临床数据显示,以基线的11%为阈值来预测流体响应性,具有97%的灵敏度和95%的特异性。
应当注意的是,尽管图4和图5示出了这样的一个实施方案,其中所提出的PEEP操作包括施加于患者的PEEP的提高(导致VCO2的减小并且因此导致负的ΔVCO2),但是PEEP操作也可包括PEEP的降低(导致VCO2的提高,并因此导致正的ΔVCO2)。
所提出的操作优选地以受控机械通气的条件(优选以体积、恒流模式)进行,并且假定在大约一分钟的测量期间患者的通气(恒定潮气量和呼吸率)和代谢条件没有变化。因此,与其中患者的潮气量可在呼吸之间变化的压力控制的通气模式相反,在操作期间以体积控制的通气模式对患者进行通气可能是有利的。因此,在执行所提出的用于预测流体响应性的方法之前,将呼吸设备1的操作模式从当前非体积控制的通气模式切换到体积控制的通气模式可以是有利的。
图6示出了举例说明根据本公开内容的一个实施方案的用于预测流体响应性的方法的流程图。
该方法通常由呼吸设备(例如图2中的呼吸机)通过执行使得呼吸设备进行该方法的多个步骤的计算机程序来进行。
在第一步骤S1中,监测指示机械通气对象的CO2清除程度(VCO2)的至少一个参数。如上所述,这优选通过监测对象呼出的呼出气体的流量或体积和指示所述呼出气体中存在CO2的一个或更多个参数来进行,例如所述呼出气体中的PACO2、CO2浓度或CO2体积。优选地,所述至少一个参数通过二氧化碳绘图仪监测并且最优选通过能够从所测量的呼气流量和呼出的PACO2导出对象的VCO2的体积二氧化碳绘图仪监测。在通气的第一阶段期间首先监测所述至少一个参数,其中使用导致VCO2的基线水平的基线PEEP对对象进行通气,如图4所示,其中在该第一通气阶段期间的VCO2水平由附图标记(A)指示。
在第二步骤S2中,将PEEP的突然变化施加到对象。PEEP的变化限定了从第一阶段的通气到第二阶段的通气的转变,其间PEEP维持在新的(改变的)PEEP水平。在通气的第二阶段期间也监测指示对象的VCO2的程度的至少一个参数。在VCO2水平稳定在新的稳态水平(由图4中的附图标记(C)指示)之前,PEEP的突然变化通过引起VCO2的迅速波动而引起对象的VCO2的变化(由图4中的附图标记(B)指示)。具有改变的PEEP水平的通气第二阶段应该至少持续直到达到VCO2的所述新的稳定状态(平衡)。通常来说,改变的PEEP的第二通气阶段应持续至少30秒并且优选约1分钟。优选地,PEEP的变化是提高,例如5或10cmH2O的逐步提高或递增提高。然而,预期PEEP的突然降低也可以以类似的方式用于根据所提出的原理来预测对象的流体响应性。
在第三步骤S3中,基于指示随步骤S2中的PEEP的变化之后的VCO2程度的至少一个所监测参数的变化,并且通常基于在PEEP的所述改变之前和之后的至少一个所监测参数的值之间的比较,来预测对象的流体响应性。如上所述,如果基线PEEP通气期间(即在通气的第一阶段期间)VCO2的基线水平与在改变的PEEP通气期间(即在通气的第二阶段期间)VCO2的新的稳态水平之间的由PEEP诱导的CO2清除的差(ΔVCO2)超过特定阈值(根据一个实施方案可对应于基线VCO2水平的10%或甚至11%),则可以判断对象为应答者。
如图4所示,一旦在通气的第二阶段期间VCO2水平已经达到其新的稳态水平,则可以再次去除PEEP的变化。因此,步骤S3之后优选地进行这样的步骤,其中去除PEEP的变化,使得PEEP返回到其基线水平,即变化之前的PEEP水平。PEEP的变化的清除限定了从第二通气阶段向第三通气阶段的转变,其中对象的VCO2被允许返回到VCO2的基线水平(由图4中的附图标记(D)指示)。因此,所提出的基于PEEP诱导或后PEEP调节的CO2清除的改变来预测流体响应性的方法是完全可逆的方法,其可以频繁重复,而不影响患者的血流动力学或容量状态。
如上所述,优选在该方法之前进行预调节操作,以再次扩张塌缩的气道和容易再扩张的肺部区域。因此,根据一个实施方案,在第一步骤S1之前进行向对象提供提高的压力和优选地还提高的PEEP的呼吸序列的步骤,以使由后续PEEP激发潜在地引起的任何显著的肺再扩张效应最小化。在所述预调节操作之后,当对象的VCO2已经处于稳定状态时,可以进行步骤S2中的PEEP的改变。
因此,根据本公开内容的原理,基于指示由PEEP的变化引起的对象的VCO2的至少一个所监测参数的变化来预测通气对象的流体响应性。在上述实施方案中,根据所监测参数的变化是否超过预定阈值,认为通气对象是流体响应性的或非流体响应性的。因此,在该示例性实施方案中,预测是二元预测,据此,认为对象对血管内流体的施用是响应性的或非响应性的。图2中所示的呼吸设备1可以配置成例如通过在显示器25上显示指示符来将预测的结果传达给装置的操作者,所述指示符指示是否认为通气对象是的响应者或非响应者。
在另一些实施方案中,所述预测可以包括确定指示对象响应于施用血管内流体的可能性的多水平(多于两个)流体反应性指标。这样的流体响应性指标可以基于至少一个所监测参数的变化幅度来确定。例如,可以将所监测参数的变化幅度与存储在呼吸设备1的存储器29(参见图2)中的查找表中的参考值进行比较,由此呼吸设备1可以配置成基于所述比较来确定对象的流体响应性指标,并且在显示器25上显示流体响应性指标。流体响应指标可以例如是1-5或1-10规模之间的值,其中高值表示认为通气对象可能对施用血管内流体有响应。
确定心输出量或EPBF的变化
通常来说,假定二氧化碳清除的变化(VCO2[ml/分钟])与心输出量(CO[l/分钟])的变化成比例。然而,仅当对象的肺中的二氧化碳水平和对象的肺容积在所分析的呼吸之间恒定时,二氧化碳清除的变化才与心输出量的变化成比例。如果是这样,则对象的肺中的CO2含量保持恒定,因为通过肺血流添加至肺中的CO2的量等于通过通气而清除的CO2的量。此外,仅当静脉血中的分流分数(shunt fraction)和CO2含量在所分析的呼吸之间恒定时,二氧化碳清除的变化才与心输出量的变化成比例。
当进行PEEP操作时,将发生通气对象的有效肺容积的瞬时变化。在所述瞬时变化之后,出现基本上稳定的状态,该稳定状态持续大约一分钟的时间。根据本公开内容的原理,分析PEEP操作之前对象的CO2清除与对象在所述稳态期间的CO2清除之间的关系,以预测对象的流体响应性。
在一个实施方案中,可以实施所提出的用于预测流体响应性的方法以假设在所分析的呼吸之间在对象的肺中CO2的水平恒定。如果该假设是正确的,并且如果对象的静脉血中的分流分数和CO2含量在所分析的呼吸序列期间基本上恒定,则不同水平的CO2清除之间的关系是对象的流体响应性的可靠量度。
然而,PEEP操作改变对象的肺血流,导致在呈现新的基本稳定状态之前,对象的肺中CO2水平逐渐变化。此外,PEEP诱导的对象有效肺容积的变化有时非常快(仅在几次呼吸后即呈现新的稳定状态),而有时非常缓慢(在超过十次呼吸之后才呈现新的稳定状态)。最近的研究表明,这些现象的组合效应不容易预见,并且在PEEP操作之后期间对象的肺中CO2水平恒定的假设通常是不正确的。
因此,在一个优选实施方案中,所提出的用于预测通气对象的流体响应性的方法以考虑对象的肺中CO2水平的可能变化的方式,通过测量和使用它们来计算流体响应性和/或通过主动防止它们来实施。为此,如下面将更详细讨论的,所提出的方法可以包括测量呼出CO2水平的变化(其指示对象的肺中CO2水平的变化),并且在对象的流体响应性预测中使用所述测量值的步骤,和/或例如通过调整通气机呼吸循环的持续时间和/或由通气机递送的呼吸潮气量来调整对象的通气的步骤,以保持对象肺中的CO2水平在所分析的呼吸之间(即在测量用于计算的参数的呼吸之间)基本上恒定。后者可以通过使用呼出CO2的测量值作为控制参数对通气机进行的自动反馈控制来实现。
下面,将讨论描述单室肺模型的CO2动力学的一些方程,以及它们可如何用于分析PEEP操作影响机械通气患者的灌注的方式。
肺模型的二氧化碳动力学方程(假定恒定的ELV和Δt)可以写成:
ELV·(FACO2n-FACO2n-1)=Δt·EPBFn·(CvCO2-CACO2n)-VTCO 2n (方程1)
在这个方程中,ELV是含有CO2的呼气末肺容积,FACO2是肺泡CO2的分数,EPBF是有效的肺血流量;CvCO2是静脉血的CO2含量,CACO2是参与肺泡气体交换的肺毛细血管血液的CO2含量,而VTCO2是CO2的潮气清除。
在平衡(稳态)下,在PEEP操作(上标0)之前,我们具有以下关系:
0=Δt·EPBF0·(CvCO2-CACO20)-VTCO 20 (方程2)
通过引入血液中CO2溶解度系数(SCO2)以将血液中的CO2含量(CxCO2)表示为CO2的分数,方程1和2可重写以针对二氧化碳清除VCO2和FACO2表示EPBF:
通过形成方程3和4的商,获得以下关系:
从方程5开始并且假定在所分析的呼吸序列期间对象的肺中恒定CO2水平,我们以这样的关系结束(假定呼吸周期的恒定持续时间Δt)
该关系可以用于根据本公开内容的一些实施方案来评估对象的流体响应性。然而,如果对象肺中的CO2水平在所分析的呼吸之间变化,这意指项FACO2n-FACO2n-1和/或项FACO2n-FACO20是非零的,则方程6没有正确地反映方程5表达的相当复杂的关系。
此外,如上所述,在所分析的呼吸之间ELV恒定的假设并不总是正确的。如果ELV在呼吸之间不同,则肺模型的二氧化碳动力学方程表示为:
(ELVn·FACO2n-ELVn-1·FACO2n-1)=Δt·EPBFn·(CvCO2-CACO2n)-VTCO 2n
(方程7)
其中通过考虑ELVn=ELVn-1+ΔELVn,其中ΔELVn是呼吸n的吸气潮气量减去呼气潮气量(VTin-VTen),可以表示为:
ELVn·(FACO2n-FACO2n-1)=Δt·EPBFn·(CvCO2-CACO2n)-VTCO 2n-ΔELVn·FACO2n-1
(方程8)
从方程8开始,EPBF商可以表示为:
通过研究方程9,可以认识到如果FACO2在所分析的呼吸之间是恒定的(FACO20=FACO2n-1=FACO2n),其意指患者肺中的CO2水平保持恒定,则因子A和B被消除,并且方程9与方程6的不同仅在于易于测量的项ΔELVn·FACO2n-1,其被添加至商VTCO2n/VTCO20的分子中。然而,如果FACO2在所分析的呼吸之间不恒定,则剩余的因子A和B需要以某种方式处理。
上述讨论涉及通气对象的EPBF。为了了解对象的心输出量(CO)如何受到PEEP操作的影响,我们引入分流分数fs,根据公式将EPBF与心输出量相联系:
CO·(1-fs)=EPBF (方程10)
在方程9中引入该关系式得到:
显然,如果分流分数在所分析的呼吸序列期间变化,则PEEP诱导的心输出量变化,从而对象的流体响应性变得更难以量化。
考虑到上述算法,变得清楚的是,由PEEP操作引起的二氧化碳清除的变化不一定是对象的心输出量变化的真实指示。还需要考虑在所分析的呼吸之间的对象的分流分数的变化、对象的肺中CO2水平的变化和对象有效肺容积的变化,以便更准确地量化心输出量的变化。
为了使PEEP操作之后通气对象的分流分数的变化最小化,用于预测流体反应性的方法可包括以下步骤:在应用PEEP操作之前对对象施加预调节操作,所述预调节操作用于使在PEEP操作之后的分流分数fs变化的风险和任何显著的肺再扩张效应最小化。预调节操作包括递送高压呼吸序列,即与基线通气相比具有提高的压力的呼吸序列。优选地,所述呼吸序列以提高的PEEP(即与在基线通气时的PEEP水平相比提高的PEEP水平)递送。
此外,该方法可包括确定可直接测量的参数FACO2、VTCO2和ΔELV的步骤。优选地但不是必需地,针对呼吸序列0至n中的每次呼吸测量这些参数,即针对发生在施加PEEP操作(呼吸数0)时或之前的第一时间点,以及发生在PEEP操作之后的在二氧化碳清除已经达到新的基本上稳定状态(呼吸数n)时的第二时间点(通常在施加PEEP操作之后约一分钟)之间的每次呼吸。
对象的二氧化碳清除(VCO2)可以从对象呼出的呼出气体的呼气流量和CO2含量确定,而潮气CO2清除(VTCO2)可以从VCO2和呼吸周期的持续时间(Δt)确定。ΔELV可以从对象的吸气和呼气潮气量确定。FACO2也可以从对象呼出的呼出气体的呼出流量和CO2含量确定。例如,FACO2可以从由测量呼气流量或体积的体积二氧化碳分析所捕获的二氧化碳描记图,以及呼出气体中CO2的分数(或分压)来确定。FACO2可以作为由体积二氧化碳描记图给出的呼出CO2的潮气末级分(FetCO2)来评估,但优选作为在体积二氧化碳描记图的肺泡斜率(阶段III)的中点处或附近实测的CO2值来评估,已经发现该CO2值最好地代表CO2的肺泡分数或分压。
关于在所分析的呼吸之间对象的肺中CO2水平的可能变化(表现为测量的FACO2的变化),这样的变化可以以下方式中的任一种或两种来处理:
1)它们可用于通过在计算PEEP诱导的心输出量或EPBF变化时使用所测量的FACO2值来确定对象的流体响应性,例如使用针对呼吸0、n-1和n所确定的FACO2值,根据方程9或11所计算的。然而,该方法需要评估ELV和FVCO2,这不期望地提高了确定心输出量变化的不确定性。例如,可以使用WO WO2013/141766 A1中公开的方法评估ELV和FVCO2,所述方法允许对ELV和FVCO2两者(在使用血液中CO2溶解度系数SCO2将CvCO2转化为FvCO2之后)通过三维相关分析同时且非侵入性地确定。
2)可以通过主动控制通气机以保持对象肺中的CO2水平在所分析的呼吸之间基本上恒定来防止它们。这可以通过控制通气机以在呼吸之间保持所测量的FACO2水平基本恒定来实现,即在施加PEEP操作之后保持FACO2水平基本上等于在PEEP操作之前的FACO2水平(即,基本上等于FACO20)。为此,通气机的控制单元可以配置成基于所测量的FACO2值来调整患者的通气,优选地其基于逐呼吸测量(measured on breath-by-breath basis)。通过在所分析的呼吸之间保持FACO2水平基本上恒定,可以忽略方程9和11中的因子A和B,并且EPBF或心输出量的变化可以由控制单元从所测量的VTCO2、ΔELV和FACO2值中可靠地确定。更详细地,EPBF或心输出量的变化可以从VTCO20、VTCO2n、ΔELVn和FACO2n-1(或对于呼吸序列0至n中的任何呼吸获得的FACO2值,因为FACO2在所述呼吸序列期间保持恒定)确定。虽然使用这种方法,仅需要针对呼吸0和n确定VTCO2,但是优选地针对呼吸序列0至n中的每次呼吸测量对象的二氧化碳清除,以便确定在PEEP变化之后何时已经达到新的稳态水平。同样地,优选地针对呼吸序列0至n中的每次呼吸测量FACO2并且用作控制参数,以便使控制单元调整通气以保持FACO2在呼吸之间基本上恒定。所测量的FACO2值也可以用于验证FACO2在所分析的呼吸之间确实保持基本上恒定。如果尽管主动控制通气机以保持FACO2恒定,但是发现FACO2变化太大(例如大于某个阈值),则通风机可以配置成将变化的FACO2值用在如上所述的心输出量或EPBF的变化的计算中。
在一个示例性实施方案中,通过对由通气机提供给对象的通气的自动控制来防止对象肺中CO2水平变化的第二选择可以包括控制由通气机递送的呼吸的潮气量(VTn)。通过基于在一个或更多个先前呼吸期间测量的FACO2值逐呼吸地调整潮气量,可以使潮气量改变以保持FACO2基本恒定。然而,递送的潮气量的变化可能不期望地影响通气对象的肺动力学,例如通过重新打开封闭的肺泡。因此,根据一个优选实施方案,通过控制由通气机提供的呼吸循环的持续时间,即通过调整由通气机递送的呼吸的持续时间,可以代替地防止对象肺中CO2水平的变化。优选地,呼吸周期的持续时间通过调整前一呼吸的呼气结束和下一呼吸的吸气开始之间的暂停来调整(即,通过调整“呼气暂停”)。如果对象肺中的CO2水平(如通过所测量的FACO2值所显示的)开始降低,则可以延长呼气暂停,并且如果对象肺中的CO2水平开始提高,则可以缩短呼气暂停。如果修改方程11以考虑所分析的呼吸序列中的相应呼吸的持续时间的变化(Δtn),则商COn/CO0由以下方程给出:
假定分流分数(fs)恒定,则消除方程12中的因子(1-fs0)/(1-fsn),并且商COn/CO0和EPBFn/EPBF0由下式给出:
通过例如基于逐次呼吸调整Δt,使FACO2在呼吸序列0至n期间保持基本上恒定并等于FACO20,则因子A和B被消除,并且商COn/CO0和EPBFn/EPBF0由下式给出:
其中FACO2n-1可以替代为FACO2x,因为FACO2在呼吸之间保持基本上恒定。
因此,如果FACO2在所分析的呼吸(即呼吸数0、n-1和n)之间保持基本上恒定,则指示由所施加的PEEP操作引起的通气对象心输出量和EPBF的变化,并因此指示对象的流体响应性的商COn/CO0和EPBFn/EPBF0可以仅从所测量的VTCO2、ΔELV和FACO2值确定。然而,如果FACO2在所分析的呼吸之间不是或不能(例如通过自动调整所递送呼吸的持续时间(Δt))保持恒定,则应优选评估对象的有效肺容积和/或对象的静脉CO2,并在根据方程13测定COn/CO0或EPBFn/EPBF0商中与VTCO2、ΔELV和FACO2组合使用。
以上,已经在前述关于确定通气对象的流体响应性的描述的情况中描述了心输出量或EPBF的变化的计算。然而,应当认识到,计算背后的基本原理不限于对对象流体响应性的评估。响应于潜在地改变对象的心输出量或EPBF的任何激发的心输出量或EPBF的变化幅度,在评估通气对象的其他生理状态时也可以是可用的参数。因此,应当理解,用于确定上述通气对象的心输出量或EPBF的变化的方法还可有利地用于除了评估流体响应性之外的其他目的。
在前述描述中,心输出量的变化通过导致对象CO2清除变化的PEEP操作来实现。然而,关于确定心输出量或EPBF的变化的上述讨论不限于任何特定的操作或激发,并且可以使用潜在地导致对象的心输出量和/或EPBF改变的任何操作或激发。潜在地导致通气对象的心输出量和/或EPBF改变的激发或操作在下文中将称为心输出量激发(cardiac output challenge)。心输出量激发的非排他性实例是PEEP操作、流体激发和被动腿部抬升操作。
此外,上述计算依赖于肺泡CO2的分数(FACO2)作为对象肺中CO2水平的任何变化的指示。然而,可以使用指示对象肺中CO2水平的任何参数代替FACO2。例如,可以将FACO2替代为呼出CO2的分数或分压的测量值(FECO2或PECO2),例如呼出CO2的潮气末分数或分压(FetCO2或PetCO2)。
因此,根据本公开内容的一个方面,提供了用于确定与例如通气机的呼吸设备相连接的对象的心输出量或有效肺血流量(effective pulmonary blood flow,EPBF)变化的方法,其包括以下步骤:
-向对象施加心输出量激发;
-在发生在施加所述心输出量激发时或之前的第一时间点时确定对象的第一二氧化碳清除水平;
-在发生在施加所述心输出量激发之后的第二时间点时确定对象的第二二氧化碳清除水平,以及
-基于所述第一和第二二氧化碳清除水平来计算对象的心输出量或有效肺血流量(EPBF)的变化;
-确定指示对象肺中CO2水平的参数,以及
-在计算心输出量或有效肺血流量的变化时使用所述参数。
所述参数可以是FACO2、PACO2或对象的肺泡CO2的任何替代量度,例如FetCO2或PetCO2,或指示对象肺中CO2水平的任何其他参数。
如上所言明,该方法通常包括在确定心输出量或EPBF变化期间将所述参数的可能的变化考虑在内的步骤。可以通过测量并在心输出量或EPBF的计算中使用可能的变化和/或通过调整由呼吸设备提供的通气来主动地防止它们来考虑可能的变化,以至少在所分析的呼吸之间并且优选地在所述第一与第二时间点之间保持参数基本上恒定。
测量和使用所述参数中的变化通常意指反复地确定参数,优选地以逐次呼吸为基础确定参数,并且意指例如基于由方程13表示的关系,使用至少一些变化的参数值来计算心输出量或EPBF的变化。
通过调整由呼吸设备提供的通气来主动地防止它们通常意指调整由呼吸设备递送的呼吸的潮气量和/或持续时间,以保持参数至少在所分析的呼吸之间并且优选地在所述第一与第二时间点之间基本上恒定。在这种情况下,如上文所讨论,可以基于由方程14表示的关系来计算心输出量或EPBF的变化。
调整由呼吸设备提供的通气以保持参数基本上恒定的步骤通常包括调整由呼吸设备递送的呼吸的潮气量和/或持续时间。
优选地,例如以逐次呼吸为基础,反复地进行对指示对象肺中二氧化碳水平的参数的确定。反复确定的参数值可以由呼吸设备的控制单元用作控制参数,以便自动地调整对象的通气量,以保持参数基本上恒定。
此外,反复确定的参数值可以用于确定参数是否基本上恒定或者参数是否在呼吸之间变化。如果参数基本上恒定,则可以根据第一原理来计算心输出量或EPBF的变化,并且如果参数变化,则可以根据第二且不同的原理来计算心输出量或EPBF的变化。第一原理可包括基于由方程14表示的关系计算心输出量或EPBF的变化,而第二原理可包括基于由方程13表示的关系计算心输出量或EPBF的变化。呼吸设备的控制单元可以配置成根据第一或第二原理,依据所反复确定的参数是否基本上恒定,来计算心输出量或EPBF的变化。
如前所讨论,所计算的心输出量或EPBF的变化可用于评估通气对象的流体响应性,但也可用于评估对象的其他生理状态。
还如前所讨论,心输出量激发可以是PEEP操作,但也可以是潜在地改变对象的心输出量或EPBF的任何其他类型的激发,例如流体激发或被动腿部抬高操作。
应当理解,当对象与所述呼吸设备相连接并由所述呼吸设备通气时,用于确定通气对象的心输出量或EPBF的变化的方法通常由图1所示的呼吸设备1的控制单元27进行。
因此,根据本公开内容的另一方面,提供了呼吸设备1,例如呼吸机,其用于确定与所述呼吸设备1相连接的对象3的心输出量或有效肺血流的变化。呼吸设备1包含控制单元27,其配置成:
-在发生在向对象3施加心输出量激发时或之前的第一时间点时确定对象的第一二氧化碳清除水平;
-在发生在施加所述心输出量激发之后的第二时间点时确定对象的第二二氧化碳清除水平,以及
-基于所述第一和第二二氧化碳清除水平来计算对象3的心输出量或有效肺血流量的变化;
-确定指示对象3肺中的二氧化碳水平的参数,以及
-在计算心输出量或有效肺血流量(EPBF)的变化时使用所述参数。
控制单元27还可配置成执行与用于确定与呼吸设备1相连接的对象的心输出量或EPBF的变化的方法相关的上述方法步骤中的任一个或任意组合。
控制单元27通常配置成通过执行计算机程序来执行方法步骤,所述计算机程序可以存储在呼吸设备1的非易失性存储器29中。因此,根据本公开内容的另一方面,提供了用于确定与呼吸设备1相连接的对象3的心输出量或有效肺血流之变化的计算机程序。所述计算机程序包含计算机可读代码,其在由呼吸设备1的处理单元21执行时使呼吸设备1进行以下步骤:
-在发生在向对象3施加心输出量激发时或之前的第一时间点时确定对象的第一二氧化碳清除水平;
-在发生在施加所述心输出量激发之后的第二时间点时确定对象的第二二氧化碳清除水平,以及
-基于所述第一和第二二氧化碳清除水平来计算对象的心输出量或有效肺血流量(EPBF)的变化;
-确定指示对象肺中CO2水平的参数,以及
-在计算心输出量或有效肺血流量的变化时使用所述参数。
计算机程序还可以包含当这样的代码,当其由所述处理单元21执行时,使得呼吸设备1执行上述涉及用于确定与呼吸设备1相连接的对象的心输出量或EPBF变化的方法的方法步骤中的任一个或任意组合。
在本公开内容中,先前已经提出了用于预测与能够向其提供机械通气的呼吸设备1相连接的对象3的流体响应性的方法,其包括以下步骤:
-监测指示对象二氧化碳清除程度的至少一个参数;
-施加PEEP操作,其中施加于对象的PEEP从第一PEEP水平改变为第二PEEP水平,以及
-基于PEEP的所述改变之后的所述至少一个所监测参数的变化来预测对象的流体响应性。
根据上述讨论的发现,即二氧化碳清除的变化并不总是对于对象心输出量和EPBF的变化的非常精确的量度,因此流体响应性的预测优选地还基于指示对象肺中二氧化碳水平的参数。为此,所述用于预测流体响应性的方法可以包括以下附加步骤:
-确定指示对象肺中二氧化碳水平的参数;
-基于指示在PEEP的所述改变之后的对象二氧化碳清除程度的至少一个所监测参数和指示对象肺中的二氧化碳水平的所述参数两者的变化,来计算心输出量或EPBF的变化,以及
-基于所计算的心输出量或EPBF的变化来预测对象3的流体响应性。
此外,用于预测流体响应性的所述方法可以包括涉及用于确定对象的心输出量或EPBF的变化的方法的上述方法步骤中的任一个或任意组合,以便更准确地确定心输出量或EPBF的变化,从而更准确地预测对象的流体响应性。例如,其可以包括在确定心输出量或EPBF的变化期间考虑指示对象肺中二氧化碳水平的所述参数的可能变化的步骤,例如通过测量它们并且将他们用于心输出量或EPBF的计算,和/或通过调整由呼吸设备1提供的通气来主动防止它们以保持所述参数基本恒定。这里,取决于指示对象肺中的二氧化碳水平的参数是否在呼吸之间变化,所计算的心输出量或EPBF的变化也优选地基于方程13或方程14所表示的关系来计算。
缩写、首字母缩略词和定义
CO 心输出量(cardiac output)
CO2 二氧化碳(carbon dioxide)
CVC 中心静脉导管(central venous catheter)
CVP 中心静脉压(central venous pressure)
EchoC 超声心动描记术(echocardiography)
GEDV 整体舒张末期容积(global end-diastolic volume)
ICU 重症监护病房(intensive care unit)
IVC 下腔静脉(inferior vena cava)
LV 左心室(left ventricle)
LVEDA 左室舒张末期面积(left ventricular end-diastolic area)
MAP 平均动脉压(mean arterial pressure)
PAC 肺动脉导管(pulmonary artery catheter)
PACO2 CO2分压(partial pressure of CO2)
PAOP 肺动脉闭塞压(pulmonary artery occlusion pressure)
PEEP 呼气末正压(positive end-expiratory pressure)
PLR 被动腿部抬升操作(passive leg raising maneuver)
PPV 脉压变化(pulse pressure variation)
RAP 右心房压(right atrial pressure)
RV 右心室(right ventricle)
RVEDV 右室舒张末容积(right ventricular end-diastolic volume)
RVSP 收缩压呼吸变化(respiratory variations in systolic pressure)
SPV 收缩压变化(systolic pressure variation)
SV 每搏输出量(stroke volume)
SVC 上腔静脉(superior vena cava)
SVV 每搏输出量变化(stroke volume variation)
参考文献
1.Vincent J-L,Rhodes A,Perel A,Martin GS,Rocca Della G,Vallet B,Pinsky MR,Hofer CK,Teboul J-L,de Boode W-P,et al.:Clinical review:Update on hemodynamic monitoring--a consensus of 16.Crit Care 2011,15:229.
2.Rivers E,et al.Early goal-directed therapy in the treatment of severe sepsis and septic shock.N Engl Med J 2001;345:1368-1377.
3.Bland RD,et al.Hemodynamic and oxygen transport patterns in surviving and nonsurviving postoperative patients.Crit Care Med 1985;13:85-90.
4.Connors AF,et al.The effectiveness of right heart catheterization in the initial care of critically ill patients.JAMA 1996;276:889-897.
5.Kim IB,Bellomo R,Fealy N,et al.A pilot study of the epidemiology and association of pulse pressure variation in cardiac surgery patients.Crit Care Resusc 2011;13:17-23
6.Gan TJ,Soppitt A,Maroof M,et al.Goal-directed intraoperative fluid administration reduces length of hospital stay after major surgery.Anesthesiology 2002;97:820-6
7.Lopes MR,Oliveira MA,Lemos IP,et al.Goal-directed fluid management based on pulse pressure variation monitoring during high-risk surgery:a pilot randomized controlled trial.Crit Care 2007;11:R100
8.Bellamy MC:Wet,dry or something else?British Journal of Anaesthesia 2006,97:755-757.
9.Salzwedel C,Puig J,Carstens A,Bein B,Molnar Z,Kiss K,Hussain A,Belda J,Kirov MY,Sakka SG,Reuter DA.Perioperative goal-directed hemodynamic therapy based on radial arterial pulse pressure variation and continuous cardiac index trending reduces postoperative complications after major abdominal surgery:a multi-center,prospective,randomized study.Crit Care 2013;17:R191
10.Brandstrup B,Tonnesen H,Beier-Holgersen R,et al.Effects of intravenous fluid restriction on postoperative pulmonary complications:comparison of two perioperative fluid regiments:a randomized assessor-blinded multicenter trial Ann Surg 2003;238:641-8
11.Pinsky MR.Functional hemodynamic monitoring.Intensive Care Med 2002;28:386-8
12.Rosenberg AL,Dechert RE,Park PK,et al.Review of a large clinical series:association of cumulative fluid balance on outcome in acute lung injury;a retrospective review of the ARDSnet tidal volume study cohort.J Intensive Care Med 2009;24:35-46
13.Mahjoub Y,Lejeune V,Muller L,Perbet S,Zieleskiewicz L,Bart F,Veber B,Paugam-Burtz C,Jaber S,Ayham A,et al.:Evaluation of pulse pressure variation validity criteria in critically ill patients:a prospective observational multicentre point-prevalence study.British Journal of Anaesthesia 2014,112:681-685.
14.Marik PE,Monnet X,Teboul JL.Hemodynamic parameters to guide fluid theraphy.Ann Intensive Care 2011;1:1.
15.Cavallaro et al.Functional hemodynamic monitoring and dynamic indices of fluid responsiveness.Minerva Anestesiol 2008;74:123-135.
16.Vincent JL,et al.Fluid challenge revisited.Crit Care Med 2006;34:1333-1337.
17.Feissel M,et al.Respiratory changes in aortic blood velocity as an indicator of fluid responsiveness in ventilated patients with septic shock.Chest 2001;119:867-873.
18.Barbier C,et al.Respiratory changes in inferior vena cava diameter are helpful in predicting fluid responsiveness in ventilated septic patients.Intensive Care Med 2004;30:1740-1746.
19.Michard F,Chemla D,Richard C,et al.Clinical use of respiratory changes in arterial pulse pressure to monitor the hemodynamic effects of PEEP.Am J Respir Crit Care Med 1999;159:935-9
20.Lambert P,Sloth E,Smith B,Hansen LK,Koefoed-Nielsen J,Tonnesen E,Larsson A.Does a positive end-expiratory pressure-induced reduction in stroke volume indicate preload responsiveness?An experimental study.Acta Anaesthesiol Scand 2007;51:415-25
21.Tusman G,Areta M,Climente C,et al.Effect of pulmonary perfusion on the slopes of single-breath test of CO2.J Appl Physiol2005;99:650-5
22.Guzman JA,Lacoma FJ,Najar A,et al.End-tidal partial pressure of carbon dioxide as a non-invasive indicator of systemic oxygen supply dependency during hemorragic shock and resuscitation.Shock 1997;8:427-31
23.Gudipati CV,Weil MH,Bisera J,Deshmukh HG,Rackow EC.Expired carbon dioxide:a non-invasive monitor of cardiopulmonary resuscitation.Circulation 1988;77:234-239.
- 还没有人留言评论。精彩留言会获得点赞!