高剂量率近距离放射治疗的自适应规划和递送的制作方法
本公开涉及医学仪器,并且更具体而言涉及用于使用基于图像的技术例如针对高剂量率(hdr)近距离放射治疗或其他流程进行自适应规划和流程更新的系统和方法。
背景技术:
高剂量率(hdr)近距离放射治疗是针对前列腺癌的一种处置,其中,一些放射源通过若干中空导管被临时引入到前列腺中,以杀死癌变组织。在超声(us)引导的hdr近距离放射治疗中,通过使中空导管穿过引导网格,所述导管基于计划被植入前列腺内部。然后,通过将经直肠超声(trus)探头从基部平移到顶端(apex)来生成三维(3d)us体积。在图像上分割前列腺和导管,并且导管的位置被发送到计算机,计算机对放射源在导管内部的位置(驻留位置)以及放射源应当在所述驻留位置处存在的时间的量(驻留时间)进行优化。然后,使用后装机(afterloader)来执行计划。这种方法的缺点在于,由于阴影和钙化,在us图像中的导管分割是繁琐和困难的。
已经提出了电磁(em)跟踪器来对导管进行定位。在这种类型的系统中,利用em跟踪器来跟踪探头,以通过将所述探头从前列腺基部到顶端的撤回来创建3d超声体积。同样地,所述引导网格在校准阶段中使用em跟踪的指针被关联到所述超声体积。em跟踪器与超声体积之间的关系在校准阶段之后是已知的。在插入导管之后,em跟踪的导丝通过导管被插入以将其定位在超声体积中。
即使在仔细的校准之后,在使用em跟踪所识别的导管的位置与作为明亮区域出现在超声体积中的导管的实际位置之间仍存在一些误差。如果不校正,该误差会导致对组织的显著的欠剂量或过剂量。针对该误差的原因可能是us图像与探头em跟踪器之间的原始校准误差的结果,并且也可能是由附近的金属物体所引起的em场生成器的磁场的变化,或者简单地由场生成器的不同距离和/或取向引起的em跟踪器的读数的变化。在另一方法中,可以采用超声跟踪技术来对导管进行定位。
当计划被转移到后装机时,后装机将放射源顺序地插入导管内部,以基于计划对组织进行辐照。总辐射时间能够达到半个小时。在该时间期间,患者或导管可能移动。另外,因为导管插入以及还有辐射,前列腺会肿胀。因此,导管相对于前列腺的相对位置会在辐射期间改变。在当前的实践中,这些因素都未被考虑。
技术实现要素:
根据本原理,一种用于对医学仪器进行动态定位的系统,包括:超声成像系统,其被配置为对在其中部署了一个或多个医学仪器的体积进行成像。配准模块被配置为将所述一个或多个医学仪器的至少两幅图像进行配准,以计算所述至少两幅图像之间的变换,所述至少两幅图像是在时间上间隔开的。规划模块被配置为使所述体积的位置以及所述一个或多个医学仪器的位置基于所述变换而被更新,并且继而根据经更新的位置来更新处置计划,使得在经更新的计划中考虑了所述体积的变化以及所述一个或多个医学仪器的位置的变化。
用于对医学仪器进行动态定位的另一种系统包括:跟踪系统,其被配置为跟踪一个或多个医学仪器的位置;引导网格,其被配置为接收所述一个或多个医学仪器以在所述一个或多个医学仪器被部署在体积中时辅助对所述一个或多个医学仪器的定位;以及超声成像系统,其被配置为对在其中部署了一个或多个医学仪器的体积进行成像。配准模块被配置为将所述一个或多个医学仪器的至少两幅图像进行配准,以计算所述至少两幅图像之间的变换,所述至少两幅图像是在时间上间隔开的。规划模块被配置为使所述体积的位置以及所述一个或多个医学仪器的位置基于所述变换而被更新,并且继而根据经更新的位置在处置期间来更新处置计划,使得在经更新的计划中考虑了所述体积的变化以及所述一个或多个医学仪器的位置的变化。
一种用于动态地定位医学仪器的方法,包括:跟踪一个或多个医学仪器在体积中的位置;在第一时刻,对在其中部署了一个或多个医学仪器的体积中的一个或多个医学仪器进行超声成像;在处置期间在随后的时刻对在其中部署了一个或多个医学仪器的体积中的一个或多个医学仪器进行超声成像;将第一时刻的体积与在随后的时刻的体积进行配准,以计算第一时刻的体积的图像与在随后的时刻的体积的图像之间的变换;使用所述变换来在所述图像之间更新所述体积中的一个或多个医学仪器与器官的位置;在规划模块中更新所述位置;并且使用经更新的位置来更新处置计划。
本公开的这些及其他目标、特征以及优点将从关于附图而阅读的下面的本公开的图解说明的实施例的详细描述而变得显而易见。
附图说明
本公开将参考如下附图来详细呈现对优选实施例的以下描述,在附图中:
图1是示出了根据一个实施例的用于使用超声图像的仪器定位的动态系统的框图/流程图;
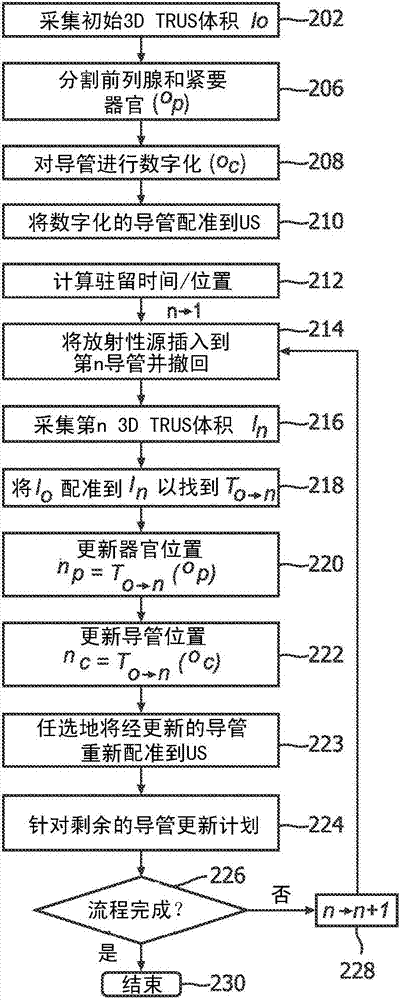
图2是示出了根据一个例示性实施例的用于动态仪器定位和规划的方法的流程图;并且
图3是根据另一例示性实施例的用于动态仪器定位和规划的另一方法的例程图。
具体实施方式
根据本原理,提供了用于在超声(us)中对诸如导管或针的医学仪器进行自动定位的系统和方法,其考虑了当前未注意的、可能发生的变量。根据特别有用的实施例,针对高剂量率(hdr)前列腺近距离放射治疗采用自适应规划。由于辐射性源被顺序地引入到导管中,在将所述源插入到每个导管中之前对计划进行调整是可能的。能够在组织辐照之前或期间考虑前列腺体积、前列腺或导管位置以及其他影响(移动等)的变化。这继而能够改善剂量覆盖的一致性并且增加处置质量。采用基于图像的配准方法来在图像坐标系(例如,超声坐标系)中配准导管的位置。
高剂量率(hdr)近距离放射治疗是一种通过由穿过中空导管被插入到前列腺中的一些放射源临时提供的内部辐射的针对前列腺癌的处置。需要对导管相对于前列腺解剖结构的准确定位以用于准确的规划和剂量递送。紧接在流程之前对导管进行数字化,并且计划被设计为将足够的剂量递送到靶标腺体但是避免(spare)其他器官。然后,所述计划被转移到后装机系统,所述后装机系统基于所述计划将放射源插入所述导管内部。在常规实践中,一旦辐射处置已经开始,就不再调整计划。然而,患者可能在辐射期间移动或者前列腺将响应于辐射和导管插入创伤而肿胀。因此,导管相对于前列腺的位置可能在辐照期间改变。
本原理提供了超声引导的自适应hdr规划,以检测和校正前列腺位置和体积的变化。调整针对hdr前列腺近距离放射治疗的计划的能力能够是在任何多模态近距离放射治疗系统中的重要特征。根据有用的实施例的hdr特异性自适应工作流程允许在辐射处置已经开始之后改变来精细调节处置计划的执行。可以采用对多个us体积的可变形的配准以及基于图像的配准以将所跟踪的导管的表示配准到us图像。可以采用跟踪技术来检测前列腺的位置和体积的改变以及任何导管移动。该信息被传递到处理单元,以用于对hdr近距离放射治疗的术中自适应规划。在一个实施例中,采用3d经直肠us(trus)探头以用于在辐射的递送期间对前列腺进行成像。在放射性胶囊被插入到新的导管中之前,采集新的3dus体积。该新的体积被可变形地配准到先前的体积或基线体积。该可变形的配准揭示了前列腺和其他紧要结构的新的位置和体积。同样地,在先前的体积中被数字化的位置和导管能够使用可变形的图像配准结果被转移到新的体积。另外,能够使用跟踪技术来测量导管的新的位置。该变形被馈送到计算机系统以相应地调整所述计划。
应当理解,将关于医学仪器来描述本发明;然而,本发明的教导要宽泛得多并且适用于任何成像仪器。在一些实施例中,在跟踪或分析复杂生物或机械系统中采用本原理。具体而言,本原理适用于生物系统的内部跟踪流程、身体中所有区域——例如肺、胃肠道、排泄器官、血管、前列腺、肾脏等——中的流程。附图中描绘的元件可以实现于硬件和软件的各种组合中并提供可以在单个元件或多个元件中进行组合的功能。
可以通过使用专用硬件以及与适当软件相关联的能够执行软件的硬件来提供附图中所示的各种元件的功能。当由处理器提供时,所述功能可以由单个专用处理器、单个共享处理器或者由多个独立处理器(其中一些可能是共享的)来提供。此外,不应将词语“处理器”或“控制器”的明确使用解释为排他性地指代能够执行软件的硬件,其能够隐含地包括,但不限于:数字信号处理器(“dsp”)硬件、用于存储软件的只读存储器(“rom”)、随机存取存储器(“ram”)和非易失性存储器。
此外,在本文中所提到原理、方面和本发明实施例的所有陈述以及其具体范例都意在涵盖其结构上和功能上的等价方案。此外,旨在使这样的等同要件既包括当前已知的等价方案,又包括未来开发的等价方案(即,所开发出的执行相同的功能的元件,而不管其结构如何)。因而,例如,本领域技术人员将认识到,在本文中所呈现的框图表示体现本发明的原理的示范性系统部件和/或电路的概念图。类似地,应当认识到,流程图、程序框图、状态转移图、伪码等均表示实质上可以在计算机可读存储介质内表示并且因而由计算机或处理器执行的各种过程,而不管是否明确示出了这样的计算机或处理器。
此外,本发明的实施例可以采取计算机程序产品的形式,可由提供程序代码的计算机可用或计算机可读介质访问所述计算机程序产品,以供计算机或者任何指令执行系统使用或者与之结合使用。就本说明书的目的而言,计算机可用或计算机可读介质可以是任何可以包括、存储、交换、传播或发送程序的设备,所述程序供指令执行系统、设备或装置使用或者与之结合使用。所述介质可以是电子、磁、光、电磁、红外或半导体系统(或者设备或装置)或传播介质。计算机可读介质的例子包括半导体或固态存储器、磁带、可移除计算机盘、随机存取存储器(ram)、只读存储器(rom)、刚性磁盘和光盘。当前的光盘的例子包括光盘—只读存储器(cd-rom)、光盘—读/写(cd-r/w)、蓝光碟tm和dvd。
现在参考附图,其中,相同的附图标记表示相同或相似的元件,并且首先参考图1,例示性示出了根据一个实施例的用于对医学仪器的自适应定位以及使用超声图像进行规划的系统100。系统100可以包括工作站或控制台112,从所述工作站或控制台监视和/管理流程。工作站112优选地包括一个或多个处理器114以及用于存储程序和应用的存储器116。存储器116可以存储图像处理模块115,图像处理模块115被配置为解读和比较来自超声成像系统110的图像。图像处理模块115被配置为收集或接收使用us探头128获得的图像。us探头128可以包括经直肠us(trus)探头(2d或3d),如将关于高剂量率(hdr)近距离放射治疗流程来例示性描述本原理。探头128可以采用光学跟踪的us探头、电磁(em)跟踪的us探头、非跟踪的3d探头等。图像处理模块115还可以被采用以提供诸如对成像体积或图像134中的仪器和/或组织的手动或自动数字化的功能。
在流程期间,医学仪器102,诸如导管、施加器或其他仪器,被插入到对象160(例如,患者)中,并且特别是诸如前列腺等的组织164中。在近距离放射治疗应用中,仪器102可以穿过引导网格162。引导网格162可以在流程之前(即,先验地)利用成像系统110的坐标系123来校准/配准。仪器102可以被配置为在其中包括或接收跟踪设备104,例如,em跟踪、光学形状感测设备/系统等。导管102,其为中空管,被插入到组织(对象160或器官164)中。然后,形状重建设备或跟踪设备104,诸如em跟踪的导丝或光学形状感测光纤被插入到导管102中并且被移除。事实上,一个em跟踪的导丝或光学形状感测(oss)光纤125能够被用于重建若干导管的形状。在其他实施例中,导管102和形状重建传感器(125)或跟踪设备104还可以被集成在一起。应当理解,也可以采用其他流程,诸如基于图像的配准和跟踪。
对于em跟踪而言,在一个例示性实施例中,使用场生成器122和跟踪系统处理模块124(例如,用于em跟踪)来跟踪仪器102的位置。生成em场,并且在em坐标系126中跟踪仪器102的移动。对于oss光纤跟踪,在一个例示性实施例中,使用来自光纤设备125和跟踪系统处理模块124(例如,用于光学形状感测)的反馈来跟踪仪器102的位置。模块124可以包括用于em跟踪和oss跟踪的分立的模块,但为了便于参考,已经作为单个模块进行了描述。由光纤设备的形状所生成的背向反射的光在其自身的坐标系(例如,坐标系127)中被跟踪。尽管仅需要单个跟踪方法,可以一起采用多个系统,或者可以采用其他跟踪系统。
根据一个实施例,基于图像的方法能够被用于使用配准模块136将来自em处理模块124的导管位置叠加或配准到图像处理模块115中的us体积上,并且因此,定位us体积中的导管102。在其他实施例中,可以利用模块124中的光学形状感测来替换em处理,并且em跟踪设备104可以由用于形状感测的光纤来替换。em信号或光学信号被用于确定仪器102的位置。仪器102优选包括导管,但是可以包括导丝、探头、内窥镜、其他医学部件等。
也可以采用其他配准系统和技术。例如,基于图像的配准是将数字化的导管配准到us体积的一种方式。如果导管在图像中被手动地数字化或者利用使用us的仪器跟踪(原位)数字化,则导管已经处在us坐标系中并且配准不是必要的。如果使用oss或em来跟踪探头128,并且以相同的方式对导管102进行数字化,则能够使用跟踪信息而无需依赖于图像来进行配准。
应当理解,根据本原理,理解器官和/或在器官之内或器官附近的医学设备的位置以多种不同的方式来进行。例如,可以采用3d顺序可变形的图像配准(图像到图像)138来跟踪总体器官、轮廓等。这能够在无需对探头或导管的任何跟踪的情况下完成。以这种方式,能够通过基于图像的配准并且利用对至少在第一图像中的导管的手动识别来完成一切(或者可能的自动的基于图像的导管识别)。这使用探头128,例如,体积超声探头或2dus探头,其位置由于步进器130(在其上对探头128和/或网格162进行致动)而是已知的、即利用步进器130的主动或被动位置编码,所以能够重建3dus图像。
利用空间跟踪,可以采用2d超声探头128以便于3dus的重建。可以使用例如em、oss、光学或其他跟踪机制(或者简单地对步进器130的机械主动/被动位置编码)来跟踪探头128。利用对导管102的空间跟踪或“映射”,执行仅一次映射(恰在插入之后),跟随有执行导管形状/位置到随后的图像的基于图像的传播,或者通过基于仪器到图像的配准模块140(也为可变形图像配准的形式)贯穿所述流程执行间歇地映射(例如,针对采集的每个3dus,或者针对每个第n幅图像)。空间跟踪的导管形状可能需要或者可能不需要配准到最新的3dus图像。
对于使用us的仪器跟踪(原位)的智能感测,仪器102总是被配准到超声,尽管可能受益于对图像的重新配准,例如“路径到体积”的配准可以提供比仅仅使用原位“本来就这样”更好的准确度。
可以如所描述的采用oss和em跟踪。如果利用与跟踪系统相同的跟踪模态来跟踪探头128,这是尤其有利的,那么类似于原位,所跟踪的路径的位置也将是在us坐标系中已知的(经历校准、跟踪误差等),但仍然可以受益于重新配准(“路径到图像”)而具有更好的准确度。如果不利用相同的模态来跟踪所述探头,则所跟踪的路径需要被重新配准到最新的图像。
在一个实施例中,工作站112包括用于查看对象(患者)160的内部图像的显示器118,并且可以包括体积的图像,作为另一图像或绘制的叠加图。显示器118也可以允许用户与工作站112以及其部件和功能或者系统100内的任何其他元件进行交互。这进一步地通过接口120来促进,其可以包括键盘、鼠标、操纵杆、触觉设备或者任何其他外围设备或控制设备以允许来自工作站112的用户反馈以及与工作站112的交互。
存储器116可以存储配准模块136,配准模块136优选地包括用于配准多个us体积(例如,随时间跟踪变化)的可变形图像配准模块138。配准模块136包括基于图像的配准模块140,以将导管的跟踪的表示配准到一幅或多幅us图像134。所跟踪的表示可以包括基于图像的跟踪、em、oss、原位或其他跟踪技术,以用于超声图像配准。
存储器116还包括自适应规划模块142,自适应规划模块142用于规划流程,诸如hdr前列腺近距离放射治疗流程等。作为计划的部分,或者在流程期间的任意时间处,所述规划模块或规划器142使用超声坐标系中的导管位置和感兴趣器官的勾勒来计算驻留位置和时间,以更新所述计划。可以针对高剂量率(hdr)近距离放射治疗或任何其他流程来计算剂量和驻留时间的量。所采用的配准方法的一个益处在于,在配准之后,导管和器官轮廓两者能够处在相同的坐标系中,并且能够被用于跟踪过程。
本原理提供了超声引导的自适应hdr规划,以检测和校正器官位置和体积的变化。调整针对hdr前列腺近距离放射治疗的计划的能力能够是在任何多模态近距离放射治疗系统中的重要特征。根据又一实施例的hdr特异性自适应工作流允许在辐射处置已经开始之后的改变以精细调节处置计划的执行。可以采用可变形的图像配准模块138和基于图像的配准模块140,以将仪器(导管)102的表示配准到us图像134。
可以采用跟踪技术来随时间检测前列腺的位置和体积的改变以及任何导管移动。如在em或oss中的跟踪不能够被用于检测例如前列腺的器官的位置和体积的改变。可变形图像配准模块138给出了关于(一个或多个)器官的位置或体积的变化的信息。为了更新导管102的位置,能够依赖跟踪技术(em、oss等)或可变形图像配准。
变化信息被传递到规划器142,规划器142用于对hdr近距离放射治疗或其他流程的术中自适应规划。在一个实施例中,采用3d经直肠us(trus)探头(128)以用于在辐射的递送期间对前列腺(164)进行成像。在放射性胶囊被插入到新的导管中之前,采集新的3dus体积。该新的体积被可变形地配准到先前的体积或基线体积。由模块138所提供该可变形的配准揭示了前列腺和其他紧要结构的新的位置和体积。同样地,在先前的体积中被数字化的位置和导管能够被转移到新的体积。另外,能够使用跟踪技术来测量导管的新的位置。所述信息被馈送到工作站112中,并且尤其是被馈送到规划模块142中,以相应地调整所述计划。
所述处置计划被发送到后装机146,后装机146然后控制放射源沿着引导管到导管102内的预先指定的位置的递送。遵循所述处置计划,所述源保持就位预先指定的驻留时间。所述源被沿着管返回到后装机146。
在本文中所描述的不同实施例可以根据需要采用图1的元件中的一些元件或所有元件。配准模块136和规划模块142以及图1中的其他元件将参考图2和图3更为详细地描述。
参考图2,流程图示出了本原理被集成到临床工作流中,以用于使用基线图像对hdr前列腺近距离放射治疗的自适应规划。在图2的实施例中,在每个步骤中,新的超声体积(n)被配准到第一超声体积(n-1)。假设患者针对在手术室中的流程准备好,并且所有必要的导管被插入到其前列腺或其他器官中。在插入所有的导管之后,执行随后的任务。在框202中,采集3d超声体积作为基线体积。能够使用静止3dtrus探头或者通过对被跟踪的2dtrus探头的撤回或旋转来采集所述体积。能够使用em、oss或者在具有平移和选择编码器的近距离放射治疗步进器上跟踪所述2dtrus探头。也能够跟踪3d探头。图像(134、图1)或体积被指定为:i0。
在框206中,靶标(在这种情况下为前列腺)以及其他紧要器官,诸如膀胱、尿道、直肠等,可以在us体积i0中勾画轮廓(分割)。在超声坐标系中的这些结构的位置被指定为:pus或0p。在框208中对导管进行数字化,并且在框210中其位置(0c)被配准到us体积。在us体积中对插入的导管进行数字化。能够通过多种方法来进行导管数字化。这些方法可以包括手动分割、电磁(em)跟踪、针对使用us的仪器跟踪(例如,原位跟踪)的智能感测、光学形状感测(oss)等。将数字化的导管配准到超声体积i0。导管在跟踪器坐标系中的位置(126,图1)是ctr,并且其在us坐标系中的位置(138,图1)是cus,使得cus=ttr→us*ctr。如果导管被手动地或者使用原位技术被数字化,则它们已经被配准到us体积,并且对ttr→us的识别是不必要的。如果采用跟踪技术(例如,em、oss等),则所跟踪的超声或基于图像的配准能够被用于识别ttr→us。
器官位置(和/或轮廓)以及所配准的数字化的导管被传递到规划模块142(图1),以在框212中确定沿着每个导管的放射源的驻留位置和驻留时间。所述计划被传送到后装机(146,图1)。后装涉及加载放射源。所述后装机将所述放射源放置在导管内部。在该阶段中,非放射性导管或施加器已经处在处置部位处。远程后装系统通过在屏蔽安全间中固定辐射源,来为健康护理专业人员提供保护免于辐射暴露。一旦导管已经被正确地安放在患者中,则它们通过一系列引导管被连接到后装机(具有放射源)。所述处置计划被发送到后装机,所述后装机然后控制所述源沿着引导管(导管)到导管内的预先指定的位置的递送。遵循所述处置计划,所述源保持就位预先指定的驻留时间。所述源被沿着管返回到所述后装机。第一源被插入到第一导管中,并且停留驻留时间,并且然后在框214中被撤回。
在源被从第一导管撤回之后,在框216中采集新的超声体积in。能够例如,使用静止3d探头或跟踪的2d探头来采集该新的us体积。
在框218中,新的(in)和旧的(i0)超声体积被使用例如demon配准算法或者其他配准算法的变型来可变形地配准。从旧的超声体积(i0)到新的超声体积(in)的变换是t0→n(或t0→1)。通过可变形图像配准模块138(图1)来执行可变形的配准。
在框220中,靶标和其他紧要器官的位置被更新到当前超声坐标系,为:npus=t0→n(0pus)。在框222中,更新导管位置。在一个实施例中,能够使用在框218中所计算的变换来更新导管位置,使得:ncus=t0→n(0cus)。在另一实施例中,下一导管能够使用诸如em、oss、超声跟踪技术等的跟踪方法在新的超声体积中被重新数字化,并且使用来自框218的变换来更新剩余的导管。在又一实施例中,能够使用诸如em、oss、超声跟踪技术等的跟踪方法在新的超声体积中对剩余的导管进行重新数字化。
在框223中,新数字化的导管的位置还能够被重新配准到新采集的超声体积,使用基于图像的配准方法等,如果必要的话。重新配准是任选的。注意到,新的数字化的导管能够被配准到us体积,使用上文参考图1所描述的配准方法中的任意配准方法。基于图像的配准是可能性之一。由于经初始数字化的导管被配准到i0,并且i0被配准到in,在跟踪的探头或静止3d探头或原位跟踪的情况下,新数字化的导管已经被配准,并且新的配准可能是冗余的。然而,重新配准能够增加准确性。
在该方法中,首先,基于可变形的配准方法(模块138,图1)来更新所有的导管的位置。然后,使用基于的图像的配准方法(使用基于图像的配准模块140,图1)来局部地优化新近跟踪的导管的位置。在另一实施例中,所有导管能够使用诸如em、oss、原位等的跟踪方法被重新数字化,并且被配准到新的超声体积。经重新数字化的导管的位置能够使用基于图像的配准(基于图像的配准模块140,图1)或其他跟踪方法被配准到新采集的超声体积。
在框224中,经更新的导管位置和经更新的器官位置被传送到规划模块142(图1)以更新所述计划。所述新的计划被传送到后装机,以将放射源插入到新的导管中。在源从导管撤回之后,重复从框214起的步骤。在图2的实施例中,在每个步骤中,新的超声体积被配准到第一超声体积。在这种情况下,针对体积n,在框214、216和218中,上标或下标是“n”。在框226中,执行检查以确定计划是否被完全执行。如果计划未完成,则在框228中推进(n变为n+1)步骤,并且处理返回到框214以进一步执行该计划。如果计划已经完成,则过程在框230中结束。
参考图3,流程图示出了本原理被集成到临床工作流中,以用于使用递增地更新的图像方法对hdr前列腺近距离放射治疗的自适应规划。在图3的实施例中,在每个步骤中,将新的超声体积(n)配准到先前的体积(n-1),并且更新是递增的。在框314、316和318中,图2)中的方程式中的上标或下标“0”被替换为“n-1”。假设为患者针对在手术室中的流程准备好,并且所有必要的导管被插入到其前列腺或其他器官中。在插入所有的导管之后,执行随后的任务。以与关于图2所描述的实质上相同的方式来执行框202-212。
如前,所述计划被传送到后装机(146,图1)。第一源被插入到第一导管中,并且停留驻留时间,并且然后在框314中被撤回。
在源被从第一导管撤回之后,在框316中采集新的超声体积in。在框218中,新的(in)和旧的(in-1)超声体积被使用例如demon配准算法或者其他配准算法的变型可变形地配准。从旧的超声体积(in-1)到新的超声体积(in)的变换是tn-1→n(或t0→1)。通过可变形图像配准模块138(图1)来执行可变形的配准。
在框320中,靶标和其他紧要器官的位置被更新到当前超声坐标系,为:npus=tn-1→n(n-1pus)。在框322中,更新导管位置。在一个实施例中,能够使用在框318中所计算的变换来更新导管位置,使得:ncus=tn-1→n(n-1cus)。在另一实施例中,下一导管能够使用诸如em、oss、原位等的跟踪方法在新的超声体积中被重新数字化,并且使用来自框318的变换来更新剩余的导管。在又一实施例中,能够使用诸如em、oss、原位等的跟踪方法对剩余的导管进行重新数字化。新数字化的导管的位置能够被配准到新采集的超声图像,使用基于图像的配准方法或者任何其他跟踪或配准方法。
在该方法中,首先,基于可变形的配准方法(模块138,图1)来更新所有的导管的位置。然后,使用基于的图像的配准方法(使用基于图像的配准模块140,图1)来局部地优化新跟踪的导管的位置。在另一实施例中,所有导管能够使用诸如em、oss、原位等的跟踪方法被重新数字化,并且被配准到新的超声体积。经重新数字化的导管的位置能够使用基于图像的配准(基于图像的配准模块140,图1)或者其他方法如所描述地被配准到新采集的超声体积。在框323中,新数字化的导管的位置还能够被重新配准到新采集的超声体积,使用基于图像的配准方法等,如果必要的话。重新配准是任选的。
在框324中,经更新的导管位置和经更新的器官位置被传送到规划模块142(图1)以更新所述计划。所述新的计划被传送到后装机,以将放射源插入到新的导管中。在源从导管撤回之后,来自框314的步骤被重复。在图3的实施例中,在每个步骤中,在框314、316和318中,新的超声体积被配准到先前的超声体积(n-1)。在框326中,执行检查以确定计划是否被完全执行。如果计划未完成,则在框328中推进(n变为n+1)步骤,并且处理返回到框314以进一步执行该计划。如果计划已经完成,则过程在框330中结束。
根据上述方法,在放射性胶囊被插入到新的导管中之前,采集新的3dus体积。所述新的体积被可变形地配准到基线体积(图2)或者被可变形地配准到先前的体积(图3)。所述可变形的配准揭示了前列腺、器官或其他结构的新的位置和体积。同样地,在先前的体积中被数字化的位置和导管能够被转移到新的体积。另外,能够使用跟踪技术来测量导管的新的位置。变形被馈送到计算机系统以相应地调整所述计划。
在解释所附权利要求书时,应当理解:
a)“包括”一词不排除在给定权利要求中所列举的其他元件或动作之外的元件或动作的存在;
b)在元件之前的词语“一”或“一个”不排除多个这样的元件的存在;
c)在权利要求中的任何参考标记不限制其范围;
d)若干“模块”可以由相同的项或硬件或软件实施的结构或功能来表示;
e)并不旨在需要特定序列的动作,除非明确指出。
已经描述了针对高剂量率近距离放射治疗的自适应规划和递送的优选实施例(其旨在例示性的而非限制性的),应当注意到,本领域技术人员在上述教导的基础上能够实现修改和变型。因此要理解,可以在所披露的公开的特定实施例中做出改变,这些改变处于所公开的实施例的由所附权利要求界定的范围之内。由此已经描述了细节并且尤其被专利法所要求的,在随附的权利要求中阐述了主张和期望由专利证书保护的内容。
- 还没有人留言评论。精彩留言会获得点赞!