治疗或预防中风的方法与流程
相关申请信息
本申请要求2014年11月17日提交的题为“治疗或预防中风的方法”的澳大利亚专利申请号240904606的优先权。其全部内容通过引用并入本文。
序列表
本申请与电子格式的序列表一同提交。该序列表的全部内容通过引用纳入本文。
领域
本公开涉及通过拮抗血管内皮生长因子(vegf)-b来治疗或预防对象中风的影响的方法。
技术背景
中风是仅次于心脏病的第二大死亡原因,也是澳大利亚的主要伤残原因。这是美国第三大死因,每年有十四万人死于中风。这也是美国严重长期残疾的主要原因。2005年至2050年期间美国中风预计费用为2.2万亿美元。
残疾影响75%的中风幸存者足以降低其就业能力。中风可以在身体,精神上,情绪上或三者的组合中影响对象。
中风可能导致的一些身体残疾包括肌肉无力,麻木,压疮,肺炎,失禁,失能(无法进行学习运动),进行日常活动困难,食欲减退,言语障碍,视力丧失和疼痛。如果中风足够严重,或在某些位置,如脑干部分,可能会导致昏迷或死亡。
中风引起的情绪问题可能源自大脑中情绪中心的直接损害,或者源自受到挫折和难以适应新的限制。中风后情绪困难包括抑郁,焦虑,恐慌发作,感情平淡(表达情绪失败),躁狂,冷漠和精神病。
中风引起的认知缺陷包括感知障碍,言语障碍,痴呆症,注意力和记忆力问题。中风患者可能不知道自己的残疾,这是一种称为无知症的病症。在被称为半疏忽的状况下,患者无法参与与受损半球相对的空间一侧的任何事物。
高达10%的中风患者发生癫痫发作,最常见于事件发生后的一周。中风的严重程度增加了癫痫发作的可能性。
中风是大脑功能的迅速发展损失,这是由于大脑供血的干扰。这可能是由于阻塞(血栓形成,动脉栓塞)或出血(血液渗漏)引起的局部缺血(血流不足)。因此,大脑的受影响区域无法发挥作用,这可能导致对象无法移动身体的一侧的一个或多个肢体,无法理解或组织言语,或无法看到一侧视野。中风经常导致神经元细胞死亡,并可导致死亡。
有两种常见的中风类型:(i)缺血性中风,由临时或永久性阻塞血液流向大脑引起,占中风病例的85%,和(ii)出血性中风,由血管破裂引起,占剩余病例的大部分。缺血性中风的最常见原因是大脑中动脉(颈内动脉下游的颅内动脉)阻塞,其损伤大脑(例如大脑皮层),例如大脑的运动和感觉皮层。这种损伤导致偏瘫,半麻醉,并且取决于损伤的脑半球而导致语言或视觉空间缺陷。
已经测试了一些神经保护剂在治疗中风方面的功效,但均失败,包括n-甲基-d-天冬氨酸受体拮抗剂(包括卢拜唑),纳美芬,氯咪唑,钙通道阻滞剂(包括α-氨基-3-羟基-5-甲基异恶唑-4-丙酸拮抗剂,5-羟色胺激动剂(例如瑞匹诺坦)和跨膜钾通道调节剂),替拉西沙星,抗icam-1抗体,人抗白细胞抗体(hu23f2g),抗血小板抗体(例如阿昔单抗),胞磷胆碱(外源形式的胞苷-5'-二磷酸胆碱)和碱性成纤维细胞生长因子。
从上述可以看出,在本领域中需要中风治疗剂。
还研究了生长因子vegf-b对神经元存活的影响,包括中风后。sun等.,j.cereb.bloodflowandmetab.,24:1146-1152,2004研究了缺乏vegf-b的小鼠的中风,发现缺乏这种生长因子导致明显更大的梗塞体积和神经损伤。li等.,jclin.invest.,118:913-923,2008显示,将vegf-b注射到已经诱导中风的小鼠的脑中,从而拯救神经元凋亡,再次表明该生长因子在中风后提供治疗益处的作用。扩展这些研究,li等,celladhesionandmigration,3:322-327,2009提出vegf-b保护神经元免于凋亡,并暗示这种生长因子可能具有治疗神经变性疾病的治疗价值。
技术实现要素:
在产生本发明时,本发明人研究了抑制vegf-b信号传导在接受的中风小鼠模型(例如缺血性中风)中的作用。本发明人通过在中风诱导之前或之后施用vegf-b拮抗剂(例如拮抗性抗体)来研究该生长因子的作用。与上述研究所暗示的相反,本发明人能够减少中风的影响,例如梗塞大小,脑内出血评分或血脑屏障损伤。这不同于防止中风的发生。本发明人还能够改善中风的溶栓治疗的结果,例如通过降低梗塞大小,出血(例如脑内出血)和致死性出血的数量。本发明人还表明,在中风后施用vegf-b拮抗剂(例如拮抗性抗体)延长了溶栓剂可以安全地施用于对象的时间。
发明人的发现为通过抑制vegf-b信号传导而减少对象中风的影响的方法提供依据。这些发现还为通过抑制vegf-b信号传导而预防或治疗对象中风的影响的方法提供依据。
例如,本发明提供一种降低对象中风影响的方法,包括给予对象抑制vegf-b信号传导的化合物。
本发明人还发现,它们可以降低患有中风的对象的出血发生率。因此,本公开另外提供了减少患有中风的对象的出血发生率的方法,所述方法包括施用抑制vegf-b信号传导的化合物。在一个实例中,该方法另外包括施用溶血栓化合物。
该发现还提供了继续治疗或开始治疗患有中风的对象以防止出血(例如脑内出血)的方法的基础,该方法包括施用抑制vegf-b信号传导的化合物。例如,在执行本文公开的方法之后,可以用抑制vegf-b信号传导的化合物来再次治疗对象以降低出血的风险或防止出血,例如脑内出血。
本发明人还发现,它们可以降低患有中风的对象的致死性出血的可能性。因此,本公开内容另外提供了降低患有中风的对象的致死性出血的可能性的方法,所述方法包括施用抑制vegf-b信号传导的化合物。在一个实例中,该方法另外包括施用溶血栓化合物。
本发明人还发现它们可以减少血脑屏障损坏或渗漏。因此,本发明人还提供了防止血脑屏障损坏或渗漏的方法,该方法包括施用抑制vegf-b信号传导的化合物。在一个实例中,血脑屏障损坏或渗漏与水肿有关。在一个实例中,血脑屏障损坏或渗漏是由于损伤,例如创伤和/或缺血引起的。
在本文所述的任何方法的一个实例中,在中风之前或之后施用抑制vegf-b信号传导的化合物。例如,化合物预防或治疗地施用。在一个实例中,化合物在中风前给予。在一个实例中,化合物在中风后给予。
在本文所述的任何方法的一个实例中,化合物在中风前给予,并且给予有中风风险的对象。
具有中风风险的示例性对象患有糖尿病和/或肥胖。例如,糖尿病是2型糖尿病。
患有中风风险的对象的额外或替代特征包括以下特征中的一个或多个:
已患有中风和/或瞬时缺血性发作;
具有中风家族史;
患有心脏病;
具有高血压;
低密度脂蛋白的血浆水平高;
具有代谢综合征;
具有心脏异常;和/或
经历手术。
在一个实例中,该对象另外为年龄在55岁以上,例如65岁以上或75岁以上。
在本文所述的任何方法的一个实例中,在中风后给予抑制vegf-b信号传导的化合物,并且所述方法包括给予抑制vegf-b信号传导的化合物和溶血栓化合物的组合。因此,治疗性地给予抑制vegf-b信号传导的化合物。
在本文描述的任何方法的一个实例中,抑制vegf-b信号传导的化合物在中风症状发作后约1至10小时之间给予。例如,抑制vegf-b信号传导的化合物在中风症状发作后约1至5小时之间给予。抑制vegf-b信号传导的化合物在中风症状发作后约1至4小时之间给予。抑制vegf-b信号传导的化合物在中风症状发作后约1小时给予。
中风的症状对技术人员来说是显而易见的,包括例如面部虚弱,手臂无力和/或言语困难中的一种或多种。
在本文所述的任何方法的一个实例中,在溶血栓化合物之前施用抑制vegf-b信号传导的化合物。例如,在溶血栓化合物之前约1小时至约10小时之间给予抑制vegf-b信号传导的化合物。例如,在溶血栓化合物之前约1小时至约6小时之间给予抑制vegf-b信号传导的化合物。例如,在溶血栓化合物之前约2小时至约6小时之间给予抑制vegf-b信号传导的化合物。例如,在溶血栓化合物之前约3小时至约5小时之间给予抑制vegf-b信号传导的化合物。例如,在溶血栓化合物前约4小时给予抑制vegf-b信号传导的化合物。
在本文描述的任何方法的一个实例中,抑制vegf-b信号传导的化合物在中风症状发作后约1小时和溶血栓化合物前约4小时给予。
在本文所述任何方法的一个实例中,所述抑制vegf-b信号通路的化合物的给予延长了可向对象安全给予溶血栓化合物的时间。因此,本公开内容还提供了一种用于延长溶血栓化合物可以安全地给予对象的时间的方法,所述方法包括给予抑制vegf-b信号传导的化合物,然后给予溶血栓化合物。
在本文描述的任何方法的一个实例中,溶血栓化合物在中风症状发作后两个小时以上给药。例如,溶血栓化合物在中风症状发作后三个小时以上给药。例如,溶血栓化合物在中风症状发作后四个小时以上给药。例如,溶血栓化合物在中风症状发作后五个小时以上给药。
在本文描述的任何方法的一个实例中,溶血栓化合物在大约中风症状的开始和中风症状发作后约十小时之间给予。例如,溶血栓化合物在中风症状发作后约四至约十小时给予。例如,溶血栓化合物在中风症状发作后约4至约8小时内给予。例如,溶血栓化合物在中风症状发作后约3至约6小时给予。例如,溶血栓化合物在中风症状发作后约4至约6小时给予。例如,溶血栓化合物在中风症状发作后约五个小时给药。
在本文所述的任何方法的一个实例中,抑制vegf-b信号传导的化合物在中风症状发作后约1小时给予,溶血栓化合物在中风症状发作后约5小时给予。
在本文所述的任何方法的一个实例中,所述溶血栓化合物选自组织纤溶酶原激活物、兰托普酶、瑞特普酶、葡萄球菌激酶、链激酶、丝裂霉素酶、去米曲普酶或尿激酶。
在本文描述的任何方法的一个实例中,对象具有升高的空腹血糖水平。例如,对象的空腹血糖水平大于150mg/dl。例如,对象的空腹血糖水平大于180mg/dl。例如,对象的空腹血糖水平大于200mg/dl。例如,对象的空腹血糖水平大于300mg/dl。例如,对象的空腹血糖水平大于400mg/dl。
在一个例子中,中风症状选自:
梗塞大小;
降低对象的出血发生率;
降低对象的致死出血的可能性;和/或
通过对象脑内出血评分评估出血评分;和/或
中风后对象血脑屏障损伤或渗漏。
在本文描述的任何方法的一个实例中,中风后对象的血脑屏障损伤或渗漏可能导致脑水肿。
用于评估前述各项的方法是本领域已知的和/或在此描述的。
中风的其他影响是本领域已知和/或本文描述的,包括例如运动障碍,例如麻痹,部分麻痹,言语不清,运动不协调,肌肉无力,低渗性,高渗性或非自愿异常运动。
在本文所述的任何方法的一个实例中,所述化合物以足以具有以下一种或多种作用的量给予:
降低对象中的梗塞大小;
降低脑出血评分所评估的对象的出血评分;
减少对象血脑屏障的损伤或渗漏;和/或
减少中风后对象的脑水肿。
在本文描述的任何方法的一个实例中,中风是缺血性中风。例如,中风是脑缺血性中风。
在本文所述任何方法的一个实例中,抑制vegf-b信号传导的化合物结合vegf-b。
例如,化合物是包含与vegf-b结合或特异性结合并中和vegf-b信号传导的抗体可变区的蛋白质。
在本文所述的任何方法的一个实例中,化合物是抗体模拟物。例如,该化合物是包含免疫球蛋白的抗原结合结构域的蛋白质,例如ignar,骆驼抗体或t细胞受体。
在本文描述的任何方法的一个实例中,化合物是结构域抗体(例如,仅包含重链可变区或仅包含与vegf-b结合的轻链可变区)或仅重链抗体(例如,骆驼抗体或ignar)或其可变区。
在本文所述的任何方法的一个实例中,化合物是包含fv的蛋白质。例如,蛋白质选自:
(i)单链fv片段(scfv);
(ii)二聚体scfv(di-scfv);或
(iv)双抗体;
(v)三抗体;
(vi)四抗体;
(vii)fab;
(viii)f(ab’)2;
(ix)fv;或
(x)与抗体的恒定区fc或重链恒定结构域(ch)2和/或ch3相连的(i)至(ix)之一。
在本文所述的任何方法的另一个实例中,化合物是抗体。示例性抗体是全长和/或裸抗体。
在本文描述的任何方法的一个实例中,化合物是重组,嵌合,cdr移植,人源化,同人源化(synhumanized),灵长类化,去免疫或人类的蛋白质。
在本文描述的任何方法的一个实例中,化合物是包含竞争性抑制抗体2h10与vegf-b的结合的抗体可变区的蛋白质。在一个实例中,蛋白质包括包含seqidno:3所示序列的重链可变区(vh)和包含seqidno:4所示序列的轻链可变区(vl)。
在一个实例中,化合物是包含抗体2h10的人源化可变区的蛋白质。例如,蛋白质包含可变区,其包含抗体2h10的vh和/或vl的互补决定区(cdr)。例如,该蛋白质包含:
(i)含下述的vh:
(a)cdr1,其包含seqidno:3的氨基酸25-34所示的序列;
(b)cdr2,其包含seqidno:3的氨基酸49-65所示的序列;和
(c)cdr3,其包含seqidno:3的氨基酸98-108所示的序列;和/或
(ii)含下述的vl:
(a)cdr1,其包含seqidno:4的氨基酸23-33所示的序列;
(b)cdr2,其包含seqidno:4的氨基酸49-55所示的序列;和
(c)cdr3,其包含seqidno:4的氨基酸88-96所示的序列。
在本文描述的任何方法的一个实例中,化合物是包含vh和vl的蛋白质,vh和vl是抗体2h10的人源化可变区。例如,该蛋白质包含:
(i)含下述的vh:
(a)cdr1,其包含seqidno:3的氨基酸25-34所示的序列;
(b)cdr2,其包含seqidno:3的氨基酸49-65所示的序列;和
(c)cdr3,其包含seqidno:3的氨基酸98-108所示的序列;和
(ii)含下述的vl:
(a)cdr1,其包含seqidno:4的氨基酸23-33所示的序列;
(b)cdr2,其包含seqidno:4的氨基酸49-55所示的序列;和
(c)cdr3,其包含seqidno:4的氨基酸88-96所示的序列。
如本领域技术人员显而易见的,由核酸编码的序列包括可能在表达过程中产生的该序列的所有变体。
在本文描述的任何方法的一个实例中,前述段落中的任一个的可变区或vh包含seqidno:5所示的序列。
在本文描述的任何方法的一个实例中,前述段落中的任一个的可变区或vl包含seqidno:6所示的序列。
在本文所述的任何方法的一个实例中,化合物是抗体。
在本文所述的任何方法的一个实例中,所述化合物是包括含有seqidno:5所示序列的vh和含有seqidno:6所示序列的vl的抗体。
在一个实例中,蛋白质或抗体是编码任何前述蛋白质或抗体的核酸编码的任何形式的蛋白质或抗体。
在一个实例中,蛋白质或抗体包含:
(i)含下述的vh:
(a)cdr1,其包含由包含seqidno:12的核酸所编码的序列,或包含seqidno:18的氨基酸序列;
(b)cdr2,其包含由包含seqidno:13的核酸所编码的序列,或包含seqidno:19的氨基酸序列;和
(c)cdr3,其包含由包含seqidno:14的核酸所编码的序列,或包含seqidno:20的氨基酸序列;和/或
(ii)含下述的vl:
(a)cdr1,其包含由包含seqidno:15的核酸所编码的序列,或包含seqidno:21的氨基酸序列;
(b)cdr2,其包含由包含seqidno:16的核酸所编码的序列,或包含seqidno:22的氨基酸序列;和
(c)cdr3,其包含由包含seqidno:17的核酸所编码的序列,或包含seqidno:23的氨基酸序列。
在一个实例中,蛋白质或抗体包含:
(i)含下述的vh:
(a)cdr1,其包含由包含seqidno:24的核酸所编码的序列,或包含seqidno:30的氨基酸序列;
(b)cdr2,其包含由包含seqidno:25的核酸所编码的序列,或包含seqidno:31的氨基酸序列;和
(c)cdr3,其包含由包含seqidno:26的核酸所编码的序列,或包含seqidno:32的氨基酸序列;和/或
(ii)含下述的vl:
(a)cdr1,其包含由包含seqidno:27的核酸所编码的序列,或包含seqidno:33的氨基酸序列;
(b)cdr2,其包含由包含seqidno:28的核酸所编码的序列,或包含seqidno:34的氨基酸序列;和
(c)cdr3,其包含由包含seqidno:29的核酸所编码的序列,或包含seqidno:35的氨基酸序列。
在一个实例中,蛋白质或抗体包含:
(i)含下述的vh:
(a)cdr1,其包含由包含seqidno:36的核酸所编码的序列,或包含seqidno:42的氨基酸序列;
(b)cdr2,其包含由包含seqidno:37的核酸所编码的序列,或包含seqidno:43的氨基酸序列;和
(c)cdr3,其包含由包含seqidno:38的核酸所编码的序列,或包含seqidno:44的氨基酸序列;和/或
(ii)含下述的vl:
(a)cdr1,其包含由包含seqidno:39的核酸所编码的序列,或包含seqidno:45的氨基酸序列;
(b)cdr2,其包含由包含seqidno:40的核酸所编码的序列,或包含seqidno:46的氨基酸序列;和
(c)cdr3,其包含由包含seqidno:41的核酸所编码的序列,或包含seqidno:47的氨基酸序列。
在一个实例中,化合物在组合物内。例如,组合物包含如本文所述的包含抗体可变区或vh或vl或抗体的蛋白质。在一个实例中,组合物另外包含蛋白质或抗体的一种或多种变体。例如,其包含缺失编码的c-末端赖氨酸残基的变体,脱酰氨基变体和/或糖基化变体和/或包含焦谷氨酸的变体的变体,例如在蛋白质和/或变体的n-末端缺失n-末端残基,例如抗体或v区中的n-末端谷氨酰胺和/或包含全部或部分分泌信号的变体。编码的天冬酰胺残基的脱氨基变体可能产生异天冬氨酸,并且产生天冬氨酸异构体,或甚至涉及相邻氨基酸残基的琥珀酰胺。编码的谷氨酰胺残基的脱氨基变体可能产生谷氨酸。当参考特定的氨基酸序列时,包括这种序列和变体的非均相混合物的组合物包括在内。
在本文描述的任何方法的一个实例中,抑制vegf-b信号传导的化合物抑制或阻止vegf-b的表达。例如,该化合物选自反义,sirna,rnai,核酶和dna酶。
在本文所述的任何方法的一个实例中,vegf-b是哺乳动物vegf-b,例如人vegf-b。
在本文描述的任何方法的一个实例中,对象是哺乳动物,例如灵长类动物,例如人。
本文所述的治疗方法可另外包括给予另外的化合物以减少,治疗或预防中风的影响。
本公开还提供了抑制vegf-b信号传导用于减少中风影响的化合物。
本公开还提供了抑制vegf-b信号传导的化合物在制备用于降低中风影响的药物中的用途。
本公开还提供了一种试剂盒,其包含抑制vegf-b信号的化合物,其与用于降低中风影响的说明书一起包装。任选地,试剂盒还包含溶血栓化合物。
本公开内容还提供了一种试剂盒,其包含抑制vegf-b信号传导的化合物,该化合物与说明书一起包装,用以将化合物与溶血栓化合物组合给予患有中风的对象。
本公开内容还提供了一种试剂盒,其包含溶血栓化合物,该化合物与说明书一起包装,用以将化合物与抑制vegf-b信号传导的化合物组合给予患有中风的对象。
本文描述了中风和化合物的示例性作用,并将其用于对前述六段所述实施例加以必要的修改。
附图说明
图1a显示用bodipy-c12示踪剂测量的用vegf-b蛋白处理2小时后脂肪酸的内皮细胞摄取显著增加的图示。值是标准化至对照的摄取比。*p<0.05,***p<0.001与对照相比。
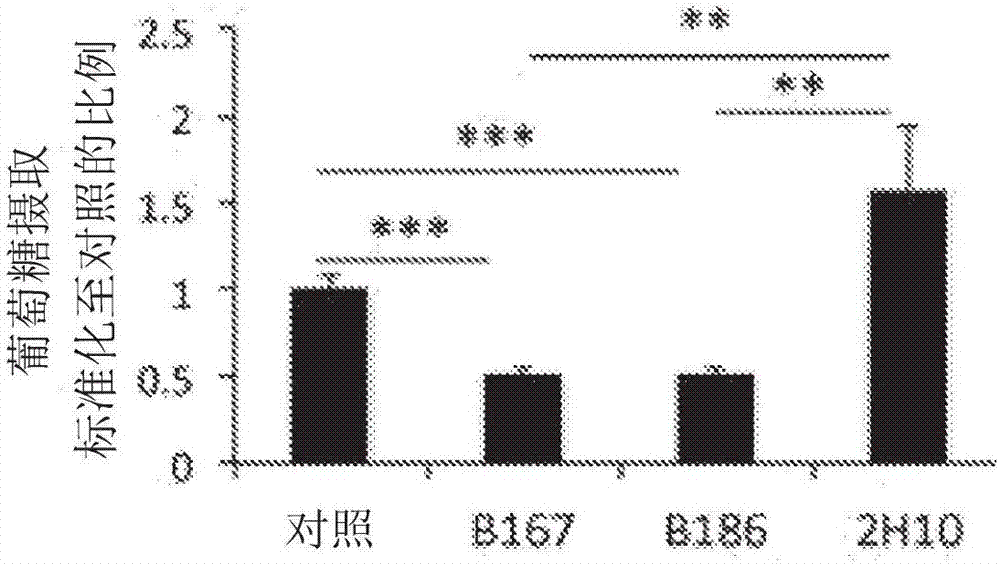
图1b显示用荧光葡萄糖类似物(2-nbdg)测量的用vegf-b蛋白处理2小时后内皮细胞葡萄糖摄取显著降低的图示。值是标准化至对照的摄取比。*p<0.05,**p<0.01,***p<0.001与对照相比。
图1c显示暴露于脂肪酸(fa;25μm棕榈酸酯和25μm油酸钠)2小时或过夜(o/n)的主要内皮细胞显示降低的摄取葡萄糖的能力(如使用2-nbdg所测)的图示。值是均值±sem。**p<0.01相比对照。
图2a显示饮食诱导的肥胖(dio)小鼠与正常食物的年龄匹配的小鼠相比升高的血糖水平的图示。值是均值±sem。**p<0.001相比对照。
图2b显示在缺血性中风后与正常食物的年龄匹配的小鼠相比,dio小鼠中梗塞体积更大的图示。通过ttc染色在72小时测量梗塞体积。值为均值+sem,n=10/组。*p<0.01相比对照。
图2c显示在缺血性中风后,与正常食物的年龄匹配的小鼠相比,dio小鼠出血评分增加的图示。通过评分系统72小时处评估出血。值为均值+sem,n=10/组。*p<0.01相比对照。
图2d是显示在缺血性中风3小时后,dio小鼠中qpcr测量的nrpl表达增加,而vegfb和其受体vegfr1(flt1)的转录水平与对侧对照没有显著差异。值为均值+sem,n=3/组。**p<0.01相比对照。
图3a显示用2h10的vegf-b拮抗作用,与用同种型对照igg治疗的小鼠相比,改善dio小鼠脑中葡萄糖类似物18f脱氧葡萄糖(18fdg)的摄取。2h10处理的饮食诱导的肥胖小鼠中的葡萄糖类似物摄取与在瘦小鼠中观察到的相当。n=2-5/组,平均值±sem。#p<0.05,**p<0.01。
图3b显示缺血性中风后,与正常食物的年龄匹配的小鼠相比,使用vegf-b阻断抗体2h10的预处理降低dio小鼠的梗塞体积的图示。通过2,3,5-三苯基四唑氯化物(ttc)染色在72小时测量梗塞体积。值为均值+sem,n=10/组。**p<0.01相比对照。
图3c显示缺血性中风后,与正常食物的年龄匹配的小鼠相比,使用vegf-b阻断抗体2h10的预处理降低dio小鼠的出血评分的图示。通过评分系统72小时处评估出血。值为均值+sem,n=10/组。**p<0.01相比对照。
图3d显示用抗vegf-b抗体2h10预防性治疗后,缺血性中风后1小时的缺血半暗带中葡萄糖转运蛋白glut-1的保留表达的图示。n=5/组。平均值±sem,*p<0.05相比对侧,#p<0.05相比对照。
图3e显示在缺血性中风后1小时,在dio小鼠中使用抗vegf-b抗体2h10进行预防性治疗减少血脑屏障渗漏(通过葡聚糖外渗测量)的图示。n=5/组,平均值±sem,**p<0.01。
图3f显示与igg对照处理的小鼠相比,预防性抗vegf-b抗体治疗在dio小鼠缺血性中风后降低闭合蛋白(occludin)丝氨酸磷酸化(丝氨酸残基490)的图示。在对侧半球和同侧半影区域用磷酸丝氨酸特异性抗闭合蛋白抗体进行染色,并将其表示为像素强度。n=3,*p<0.05.
图3g的示意图显示,与同种型对照治疗(igg)相比,通过抗vegf-b抗体2h10的预防性治疗阻断dio小鼠缺血性中风后3小时在脑血管中的脂质积累(通过血管亲脂素免疫染色测量)。平均值±sem,**p<0.01。
图4a显示用2h10抗体抑制vegf-b显著降低缺血性中风后dio小鼠晚期溶栓后的中风容积。通过ttc染色,测量缺血性中风后72小时的梗塞体积。n=6-10/组,平均值±sem,**p<0.01。
图4b显示用2h10抗体抑制vegf-b显著降低缺血性中风后dio小鼠晚期溶栓后的出血评分。缺血性中风后72小时组织学测量出血评分。n=6-10/组,平均值±sem,**p<0.01。
图4c是kaplanmeier存活分析,显示用2h10抗体对vegf-b的抑制改善了缺血性中风后饮食诱导的肥胖小鼠晚期溶栓后的存活结果。n=10/组,平均值±sem,*p<0.05。
序列表要点
seqidno:1是含有21个氨基酸n-末端信号序列的人vegf-b186异构体的氨基酸序列
seqidno:2是含有21个氨基酸n-末端信号序列的人vegf-b167异构体的氨基酸序列
seqidno:3是来自抗体2h10的vh的氨基酸序列。
seqidno:4是来自抗体2h10的vl的氨基酸序列。
seqidno:5是来自抗体2h10的人源化形式的vh的氨基酸序列。
seqidno:6是抗体2h10的人源化形式的vl的氨基酸序列。
seqidno:7是来自抗体4e12的vh的氨基酸序列。
seqidno:8是抗体4e12的vl的氨基酸序列。
seqidno:9是来自抗体2f5的vh的氨基酸序列。
seqidno:10是抗体2f5的vl的氨基酸序列。
seqidno:11是重组人组织纤溶酶原激活物的氨基酸序列。
seqidno:12是来自抗体2h10的vlcdr1的核苷酸序列
seqidno:13是来自抗体2h10的vlcdr2的核苷酸序列
seqidno:14是来自抗体2h10的vlcdr3的核苷酸序列
seqidno:15是来自抗体2h10的vhcdr1的核苷酸序列
seqidno:16是来自抗体2h10的vhcdr2的核苷酸序列
seqidno:17是来自抗体2h10的vhcdr3的核苷酸序列
seqidno:18是来自抗体2h10的vlcdr1的氨基酸序列。
seqidno:19是来自抗体2h10的vlcdr2的氨基酸序列。
seqidno:20是来自抗体2h10的vlcdr3的氨基酸序列。
seqidno:21是来自抗体2h10的vhcdr1的氨基酸序列。
seqidno:22是来自抗体2h10的vhcdr2的氨基酸序列。
seqidno:23是来自抗体2h10的vhcdr3的氨基酸序列。
seqidno:24是来自抗体2f5的vlcdr1的核苷酸序列
seqidno:25是来自抗体2f5的vlcdr2的核苷酸序列
seqidno:26是来自抗体2f5的vlcdr3的核苷酸序列
seqidno:27是来自抗体2f5的vhcdr1的核苷酸序列
seqidno:28是来自抗体2f5的vhcdr2的核苷酸序列
seqidno:29是来自抗体2f5的vhcdr3的核苷酸序列
seqidno:30是来自抗体2f5的vlcdr1的氨基酸序列。
seqidno:31是来自抗体2f5的vlcdr2的氨基酸序列。
seqidno:32是来自抗体2f5的vlcdr3的氨基酸序列。
seqidno:33是来自抗体2f5的vhcdr1的氨基酸序列。
seqidno:34是来自抗体2f5的vhcdr2的氨基酸序列。
seqidno:35是来自抗体2f5的vhcdr3的氨基酸序列。
seqidno:36是来自抗体4e12的vlcdr1的核苷酸序列
seqidno:37是来自抗体4e12的vlcdr2的核苷酸序列
seqidno:38是来自抗体4e12的vlcdr3的核苷酸序列
seqidno:39是来自抗体4e12的vhcdr1的核苷酸序列
seqidno:40是来自抗体4e12的vhcdr2的核苷酸序列
seqidno:41是来自抗体4e12的vhcdr3的核苷酸序列
seqidno:42是来自抗体4e12的vlcdr1的氨基酸序列。
seqidno:43是来自抗体4e12的vlcdr2的氨基酸序列。
seqidno:44是来自抗体4e12的vlcdr3的氨基酸序列。
seqidno:45是来自抗体4e12的vhcdr1的氨基酸序列。
seqidno:46是来自抗体4e12的vhcdr2的氨基酸序列。
seqidno:47是来自抗体4e12的vhcdr3的氨基酸序列。
一般说明
i.概述
通篇中,除非另有说明或上下文另有要求,应认为单个步骤、物质的组成、步骤的组或物质的组成的组包括一个和多个(即一个或多个)这些步骤、物质的组成、步骤的组或物质的组成的组。
本领域技术人员应理解,本发明易于进行除说明书中所述的那些以外的变化和修改。应理解本发明包含所有这些变化和修改。本发明还包括说明书中单独或共同提到或指出的所有步骤、特征、组合物和化合物,以及所述步骤或特征中任意两种或更多种或任意和全部组合。
本发明的范围不限于本文所述的具体实施例,实施例仅用于示例目的。功能上等同的产品、组合物和方法清楚地包含于本发明的范围内。
本发明的任何实施例都将经必要的修改以适用于本发明的任何其他实施例,除非另有明确说明。
除非另有明确定义,本文使用的所有技术和科学术语都具有与本领域普通技术人员的常规理解相同的含义(例如在细胞培养、分子遗传学、免疫学、免疫组化、蛋白质化学和生物化学领域)。
除非另有说明,本发明中使用的重组蛋白、细胞培养和免疫技术是标准方法,其是本领域技术人员熟知的。这类技术描述并解释于文献中,例如j.perbal,apracticalguidetomolecularcloning(《分子克隆实践指南》),约翰韦利森出版社(johnwileyandsons)(1984),j.sambrook等,molecularcloning:alaboratorymanual(《分子克隆:实验室指南》),冷泉港实验室出版社(coldspringharbourlaboratorypress)(1989),t.a.brown(编),essentialmolecularbiology:apracticalapproach(《精编分子生物学:实践指南》),卷1和2,irl出版社(1991),d.m.glover和b.d.hames(编),dnacloning:apracticalapproach(《dna克隆:实践指南》),卷1-4,irl出版社(1995和1996),以及f.m.ausubel等(编),currentprotocolsinmolecularbiology(《新编分子生物学实验指南》),格林出版联合公司和韦利科学公司(greenepub.associatesandwiley-interscience)(1988,包括直至今日的所有更新),edharlow和davidlane(编),antibodies:alaboratorymanual(《抗体:实验室手册》),冷泉港实验室出版社(1988),以及j.e.coligan等(编),currentprotocolsinimmunology(《新编免疫学实验指南》),约翰韦利森出版社(包括直至今日的所有更新)。
本文中可变区及其部分、免疫球蛋白、抗体及其片段的描述和定义由以下文献中的讨论进一步阐明:kabatsequencesofproteinsofimmunologicalinterest(感兴趣的免疫蛋白序列),马里兰州贝塞斯达,1987和1991,bork等,jmol.biol.242,309-320,1994,chothia和leskj.molbiol.196:901-917,1987,chothia等,nature342,877-883,1989和/或al-lazikani等,jmolbiol273,927-948,1997。
本文中对蛋白质或抗体的任何讨论将被理解为包括在制造和/或储存期间产生的蛋白质或抗体的任何变体。例如,在制造或储存过程中,抗体可以脱酰胺化(例如在天冬酰胺或谷氨酰胺残基)和/或具有改变的糖基化和/或将谷氨酰胺残基转化成焦谷氨酸和/或具有n-末端或c-末端,末端残基被去除或“剪切”和/或具有不完全加工的信号序列的部分或全部,并且因此保留在抗体的末端。应当理解,包含特定氨基酸序列的组合物可以是所述或编码的序列和/或所述或编码序列的变体的不均匀混合物。
术语“和/或”(例如“x和/或y”)应理解为表示“x和y”或“x或y”且应提供对全部两种含义或各种含义的明确支持。
整篇说明书中,词语“包括”或变体如“包含”或“含有”应理解为意味着包括所指的元素、整数或步骤,或成组的元素、整数或步骤,但不排除任何其它元素、整数或步骤,或成组的元素、整数或步骤。
本文所用术语“来源于”表示特定整数可获自特定来源,但不需要直接来自该来源。
选择的定义
vegf-b已知存在于两种主要同种型中,称为vegf-b186和vegf-b167。仅为了命名的目的,人vegf-b186的非限制性示例序列示于ncbi参考序列:np_003368.1,ncbi蛋白质登录号np_003368,p49765和aal79001以及seqidno:1。在本公开的上下文中,vegf-b186的序列可缺少21个氨基酸的n-末端信号序列(例如,如seqidno:1的氨基酸1至21所示)。仅为了命名的目的,人vegf-b167的非限制性示例示于ncbi参考序列:np_001230662.1,ncbi蛋白质登录号aal79000和aab06274以及seqidno:2。在本公开的上下文中,vegf-b167的序列可缺少21个氨基酸的n-末端信号序列(例如,如seqidno:2的氨基酸1至21所示)。可以使用本文提供的和/或在公知的数据库中的和/或使用标准技术确定vegf-b的其他序列(例如,如ausubel等,(编辑),《新编分子生物学实验指南》),格林出版联合公司和韦利科学公司(currentprotocolsinmolecularbiology,greenepub.associatesandwiley-interscience)(1988,包括直到现在的所有更新)或sambrook等,分子克隆:实验室手册》,冷泉港实验室出版社(molecularcloning:alaboratorymanual,coldspringharborlaboratorypress)(1989))。人vegf-b可以缩写为hvegf-b。在一个实例中,本文涉及的vegf-b是vegf-b167亚型。
本文涉及的vegf-b还包括如wo2006/012688中所述的vegf-b10-108肽。
如本文所使用的,术语“中风”应被认为是指通常快速发展的脑功能的丧失,这是由于对脑或脑干的血液流动的干扰。干扰可能是由例如血栓形成或栓塞引起的缺血(缺血),或可能由于出血引起。在一个例子中,脑功能的丧失伴随着神经元细胞死亡。在一个示例中,中风是由大脑或其区域的血液的干扰或丧失引起的。在一个例子中,中风是持续超过24小时的脑血管病因的神经缺陷,或者是在24小时内被死亡中断(如世界卫生组织所定义)。超过24小时症状持续时间将中风与瞬时缺血发作(tia)分离,其症状持续不超过24小时。中风症状包括偏瘫(身体一侧瘫痪);轻偏瘫(身体一侧的虚弱);面部肌肉无力;麻木;感觉减轻;改变嗅觉,味觉,听觉或视觉感觉;嗅觉,味觉,听觉或视觉丧失;眼睑下垂(上睑下垂);眼肌可检测的虚弱;压制反射减少;吞咽能力下降;瞳孔反射性降低;脸部感觉减弱;平衡降低;眼球震颤;改变呼吸频率;改变心率;胸锁乳突肌无力,头转向一侧的能力下降或无法将头转向一侧;舌头虚弱;失语(不能说语言或理解语言);失神(改变自愿行动);视野缺陷;记忆缺陷;半边忽视或半侧忽视(与病变相对的视野侧的空间的注意缺陷);无组织思维;混乱;发展超嗜性手势;厌恶症(持续否认存在缺陷);步行困难;改变运动协调;眩晕;不平衡;意识丧失;头痛;和/或呕吐。
术语“中风的影响”将被理解为包括梗塞大小,出血评分和/或血脑屏障损坏或渗漏中的一种或多种。然而,该术语不限于这些效果并且包括对象的任何变化,例如由中风引起的对象例如神经或身体变化的任何临床变化。这些变化或影响包括运动障碍,脑功能丧失或本文所述的任何症状。
术语“中风症状的发作”将被理解为指对象或其他人识别一种或多种中风症状的时间。本文描述了合适的症状。
如本文所用,术语“出血发生率”将被理解为指对象或对象群体遭受的出血的数量或大小。因此,对象的出血发生率的降低可以是对象的出血的数量或大小的减少或者由于中风导致的对象遭受一次或多次出血的可能性的降低。
术语“致死性出血的可能性”将被理解为表示给予化合物的对象相比患有中风并且未给予化合物的对象由于出血而死亡的可能性低。显然,这种可能性可以根据人口数据计算,而不是要求对每个对象进行并排比较。该术语还将明确支持减少由于中风引起的死亡的可能性,即,本公开另外提供了减少由于中风引起的死亡可能性的方法。上述关于减少中风影响的所有方法步骤将被视为同样适用于这种方法。
术语“血脑屏障”是指将循环血液与中枢神经系统中的细胞外液体分开的高选择性渗透屏障。血脑屏障的损坏或泄漏可能导致流体在脑细胞间隙或脑水肿中积累。血脑屏障的损坏可能是由于创伤性脑损伤或非外伤性原因,如脑膜炎或脑炎引起的缺血性中风,癌症或脑炎。
术语“溶血栓化合物”应被认为是诱导或介导或增强一个或多个血块破裂以限制血管的阻塞的化合物。溶血栓化合物可以通过纤溶酶刺激继发纤维蛋白溶解作用。示例性溶血栓剂包括组织纤溶酶原激活物(tpa),丝裂霉素酶(apsac),链激酶(sk),葡萄球菌激酶(sak),去米曲普酶或尿激酶(upa)。
在一个实例中,溶血栓化合物是“组织纤溶酶原激活物”或tpa。tpa是通过催化纤溶酶原转化为纤溶酶而参与血栓破裂的丝氨酸蛋白酶。在一个实例中,可以使用重组技术制造组织纤溶酶原激活物(tpa)。因此,其可以是重组组织纤溶酶原激活物(r-tpa),例如包含seqidno:11所示的序列。示例性的tpa包括阿替普酶,瑞替普酶,兰曲普酶或替奈普酶。
如本文所用,提及溶血栓化合物的“有效给予”(或类似)将意味着溶血栓化合物的给药提供了临床有效的结果,即,与在以相同的方式(例如,同时和/或具有相似血糖水平的患者)给予相同的溶血栓化合物的对象或对象的群体中所观察到的相比,给予vegf-b信号传导的抑制剂在降低中风影响方面具有改善。
基于本文描述,本领域技术人员显而易见的是,当讨论给予化合物的“组合”时,本公开内容考虑将化合物作为单一组合物给予,同时给予化合物(但作为单独的组合物)或依次给予化合物。
术语“重组”应理解为指人工遗传重组的产物。因此,对于包含抗体可变区的重组蛋白,该术语不包括作为b细胞成熟期间发生的天然重组的产物的在对象体内天然产生的抗体。然而,如果这类抗体被分离,其应被认为是包含抗体可变区的分离的蛋白质。类似地,如果编码蛋白质的核酸被分离并使用重组方法表达,所得蛋白质是包含抗体可变区的重组蛋白。重组蛋白还包括当其处于细胞、组织或对象(例如蛋白质在其中表达的细胞、组织或对象)内时通过人工重组方式表达的蛋白质。
术语“蛋白质”应包括单条多肽链(即通过肽键连接的一系列相邻氨基酸)或彼此共价或非共价连接的一系列多肽链(即多肽复合物)。例如,可使用合适的化学键或二硫键共价连接该一系列多肽链。非共价键的示例包括氢键、离子键、范德华力和疏水相互作用。
术语“多肽”或“多肽链”应从前述段落中理解为表示通过肽键连接的一系列相邻氨基酸。
本领域技术人员将意识到,“抗体”通常被认为是包含由多个多肽链组成的可变区的蛋白质,例如包含轻链可变区(vl)的多肽和包含重链可变区(vh)的多肽。抗体还通常包含恒定结构域,其中一些可以排列成恒定区,其在重链的情况下包括恒定片段或可结晶的片段(fc)。vh和vl相互作用形成包含能够特异性结合一个或几个紧密相关的抗原的抗原结合区的fv。通常,来自哺乳动物的轻链是κ轻链或λ轻链,哺乳动物的重链是α,δ,ε,γ或μ。抗体可以是任何类型(如igg、ige、igm、igd、iga和igy)、类(如igg1、igg2、igg3、igg4、iga1和iga2)或小类。术语“抗体”还包括人源化抗体,灵长类抗体,人抗体,合成人类抗体和嵌合抗体。
术语“全长抗体”、“完整的抗体”或“全抗体”互换使用以指基本完整形式的抗体,与抗体的抗原结合片段相对。具体而言,全抗体包含具有重链和轻链(包含fc区)的那些抗体。该恒定结构域可以是野生型序列恒定结构域(如人野生型序列恒定结构域)或其氨基酸序列变体。
如本文所用,“可变区”指本文所定义抗体的轻链和/或重链的部分,其能够特异性结合抗原并包含互补决定区(cdr)(即cdr1、cdr2和cdr3)和框架区(fr)的氨基酸序列。示例性可变区包含三个或四个fr(如fr1、fr2、fr3和任选的fr4)以及三个cdr。在来自ignar的蛋白质的情况下,蛋白质可能缺少cdr2。vh指重链的可变区。vl指轻链的可变区。
本文所用术语“互补决定区”(同义词cdr;即cdr1、cdr2和cdr3)指抗体可变结构域的氨基酸残基,其存在对抗原结合非常重要。每个可变结构域通常具有被鉴定为cdr1,cdr2和cdr3的三个cdr区。分配给cdr和fr的氨基酸位置可以根据kabat系统(《感兴趣的免疫蛋白序列》国家卫生院,马里兰州,贝塞达斯(sequencesofproteinsofimmunologicalinterest,nationalinstitutesofhealth,bethesda,md.,)1987和1991)或本领域其他编号系统来确定,例如chothia和leskj.molbiol.196:901-917,1987;chothia等.nature342,877-883,1989;和/或al-lazikani等,jmolbiol273:927-948,1997的规范编号系统;lefranc等devel.andcompar.immunol.,27:55-77,2003的imgt编号系统;或honnegher和plükthunj.mol.biol.,309:657-670,2001的aho编号系统。
“框架区”(fr)是除cdr残基以外的其他可变结构域残基。
本文所用术语“fv”应理解为指任何蛋白质,无论其由多个多肽或单个多肽组成,其中vl和vh连接并形成具有抗原结合位置(即能够特异性结合抗原)的复合物。形成抗原结合位置的vh和vl可以在单条多肽链中或不同多肽链中。此外,本发明的fv(以及本发明的任何蛋白质)可具有多个抗原结合位置,其可结合或不结合相同的抗原。该术语应理解为包括直接来源于抗体的片段以及对应于使用重组方法生产的这类片段的蛋白质。在一些实施例中,vh不与重链恒定结构域(ch)1相连和/或vl不与轻链恒定结构域(cl)相连。示例性含fv多肽或蛋白质包括fab片段、fab’片段、f(ab’)片段、scfv、双抗体、三抗体、四抗体或更高级的复合物,或者与恒定区或其结构域(如ch2或ch3结构域)相连的任意前述物质,如小抗体。“fab片段”由抗体的单价抗原结合片段组成且可通过使用木瓜蛋白酶消化全抗体以生成由完整轻链和一部分重链组成的片段来生产或者可使用重组方法来生产。通过使用胃蛋白酶处理全抗体随后还原以生成由完整轻链和一部分重链(包含vh和单个恒定结构域)组成的分子,可获得抗体的“fab'片段”。通过该方式处理,每个抗体可获得两个fab'片段。还可通过重组方法生产fab'片段。抗体的“f(ab')2片段”由通过两个二硫键固定在一起的两个fab'片段的二聚体组成,并通过使用胃蛋白酶处理全抗体分子而不进行后续还原来获得。“fab2”片段是包含两个fab片段的重组片段,这两个fab片段使用例如亮氨酸拉链或ch3结构域连接。“单链fv”或“scfv”是含有抗体的可变区片段(fv)的重组分子,其中轻链的可变区和重链的可变区通过合适、灵活的多肽接头共价连接。
对于蛋白质或其抗原结合位置与抗原的相互作用,本文所用术语“结合”指该相互作用取决于抗原上是否存在特定结构(如抗原决定簇或表位)。例如,抗体识别并结合特定蛋白质结构而非普遍的蛋白质。如果抗体结合表位“a”,在含有标记的“a”和蛋白质的反应中存在含有表位“a”(或游离、未结合的“a”)的分子会降低与该抗体结合的标记的“a”的量。
本文所用术语“特异性结合”或“特异地结合”应理解为表示:与同替代性抗原或细胞的反应或连接相比,本发明的蛋白质更频繁、更快速、更久和/或亲和力更高地与特定抗原或表达该物质的细胞反应或连接。例如,蛋白质以比与其它生长因子(例如vegf-a),或由多反应天然抗体(即通过已知结合人类天然存在的多种抗原的天然存在的抗体)通常识别的抗原,实质上更高的亲和力(例如,20倍或40倍或60倍或80倍至100倍或150倍或200倍)与vegf-b结合。通常,但非必须,提及结合时指特异性结合,且各术语应理解为对其他术语提供明确支持。
本文所用术语“中和”应理解为指蛋白质能够通过vegf-r1阻碍、降低或阻止细胞中vegf-b-信号转导。确定中和的方法是本领域已知的和/或描述于本文中。
本文所用术语“预防”包括给予本发明化合物从而停止或阻碍至少一种病症症状的发展。
本文所用术语“治疗”包括给予本发明蛋白质从而降低或消除特定疾病或病症的至少一种症状或减缓疾病或病症的进展。
本文所用术语“对象”应理解为指包括人的任何动物,例如哺乳动物。示例性对象包括但不限于人和非人灵长类动物。例如,该对象是人。
降低中风的影响
本文的公开内容提供了例如减少对象中风的一种或多种影响的方法,包括向对象给予抑制vegf-b信号传导的化合物。
在一个实例中,所述对象患有糖尿病。例如,患有糖尿病的对象具有临床接受的糖尿病标志物,例如:
空腹血浆葡萄糖大于或等于7nmol/l或126mg/dl;
偶尔血浆葡萄糖(一天中的任何时间摄取)大于或等于11.1nmol/l或200mg/dl,伴有糖尿病症状。
口服葡萄糖耐量试验(ogtt)值大于或等于11.1nmol/l或200mg/dl,以两小时的间隔测量。ogtt是在两到三个小时的时间段内完成的。
在一个实例中,所述对象患有1型糖尿病。
在一个实例中,所述对象患有2型糖尿病。
本公开的方法可以容易地应用于中枢神经系统中的任何形式的缺血。例如,对象可以呈现视网膜缺血的迹象和/或症状。因此,本公开的方法将被用于减少中枢神经系统缺血例如视网膜缺血的影响。
在一个实例中,对象处于中风危险之中,但是还没有发作。如果患者发生中风的风险高于对照群体,则对象处于危险之中。对照群体可以包括从一般群体随机选择的一个或多个对象(例如,根据年龄,性别,种族和/或族群),其尚未被诊断或具有中风家族史。如果发现与该中风相关的“风险因素”与该对象相关联,则可将对象视为中风风险。风险因素可以包括与给定疾病相关的任何活性,性状,事件或特征,例如通过对对象群体的统计学或流行病学研究。因此,即使确定潜在危险因素的研究没有具体包括该对象,也可将该对象归类为处于中风危险之中。例如,进行心脏手术的对象处于短暂的脑缺血发作(或中风)的风险中,因为与未进行心脏手术的对象的群体相比,在进行心脏手术的对象中,暂时性脑缺血发作的频率增加。
在一个实例中,处于中风危险中的对象包括在脑或中枢神经系统上进行外科手术的对象,例如血管外手术,夹持,支架置入或微导管化。这些对象还包括在影响供给大脑的血管(即将大脑连接到心脏,例如颈动脉和颈静脉)的体内其他地方进行手术或在向视网膜供血的动脉上进行手术的那些。对象的一个示例类别是经历血管内手术以治疗脑动脉瘤的那些。经历这些类型手术的对象处于中风风险增加之中。
在一个例子中,处于中风风险中的对象也包括吸烟者,高血压患者,糖尿病患者,高胆固醇血症患者。风险特别高的对象是那些曾经有过中风,轻微中风或短暂性脑缺血发作的患者。
如上所述,本公开的方法实现以下一个或多个效果:
降低对象中的梗塞大小;
降低通过对象脑内出血评分评估的出血评分;和/或
减少对象血脑屏障的损伤或渗漏;和/或
减少中风后对象的脑水肿。
用于评估梗塞大小的方法是本领域已知的,并且包括例如锝(echnetium)-99m司他比锝(sestamibi)单光子发射计算机断层摄影(spect),计算机断层扫描或磁共振成像。
评估脑内出血评分的方法描述于例如hemphil等,stroke,32:891-897,2001中。可以使用例如mri或ct扫描来确定出血的存在,例如脑内出血。
也可以使用mri检测血脑屏障损坏/渗漏/渗透性,任选使用示踪剂。
在一个实例中,本公开的方法减少了本领域已知或本文所述的任何中风症状。
对本领域技术人员显而易见的是,对象中风症状或影响的“减少”将与已经患有中风但未接受本文所述方法治疗的另一对象相比较。这不一定需要两个对象的并排比较。而可以依赖群体数据。例如,评估未接受本文所述方法的治疗的患有中风的对象群体(任选地,与治疗对象相似的对象的群体,例如年龄,体重,糖尿病状态,血糖水平),并且平均值与用本文所述的方法处理的对象或群体的结果进行比较。
vegf-b信号传导抑制剂
包含抗体可变区的蛋白质
示例性vegf-b信号传导抑制剂包含抗体可变区,例如,结合vegf-b并中和vegf-b信号传导的抗体或抗体片段。
在一个实例中,抗体可变区特异性结合vegf-b。
包含其可变区的合适的抗体和蛋白质是本领域已知的。
例如,wo2006/012688中描述了抗vegf-b抗体及其片段。
在一个实例中,抗vegf-b抗体或其片段是竞争性抑制2h10与vegf-b或其抗原结合片段的结合的抗体。在一个实例中,抗vegf-b抗体或其片段是抗体2h10或其嵌合、cdr移植或人源化形式或其抗原结合片段。在这方面,抗体2h10包含具有seqidno:3所示的序列的vh,以及包含seqidno:4所示的序列的vl。在wo2006/012688中描述了该抗体的示例性嵌合和人源化形式。
在一个实例中,抗vegf-b抗体或其片段包含具有seqidno:5所示的序列的vh,以及具有seqidno:6所示的序列的vl。
在一个实例中,抗vegf-b抗体或其片段是竞争性抑制4e12与vegf-b或其抗原结合片段的结合的抗体。在一个实例中,抗vegf-b抗体或其片段是抗体4e12或其嵌合、cdr移植或人源化形式或其抗原结合片段。在这方面,抗体4e12包含具有seqidno:7所示的序列的vh,以及包含seqidno:8所示的序列的vl。
在一个实例中,化合物是包含抗体4e12的人源化可变区的蛋白质。例如,蛋白质包含可变区,其包含抗体4e12的vh和/或vl的互补决定区(cdr)。例如,该蛋白质包含:
(i)含下述的vh:
(a)cdr1,其包含seqidno:7的氨基酸25-34所示的序列;
(b)cdr2,其包含seqidno:7的氨基酸49-65所示的序列;和
(c)cdr3,其包含seqidno:7的氨基酸98-105所示的序列;和/或
(ii)含下述的vl:
(a)cdr1,其包含seqidno:8的氨基酸24-34所示的序列;
(b)cdr2,其包含seqidno:8的氨基酸50-56所示的序列;和
(c)cdr3,其包含seqidno:8的氨基酸89-97所示的序列。
在一个实例中,抗vegf-b抗体或其片段是竞争性抑制2f5与vegf-b或其抗原结合片段的结合的抗体。在一个实例中,抗vegf-b抗体或其片段是抗体2f5或其嵌合、cdr移植或人源化形式或其抗原结合片段。在这方面,抗体2e5包含具有seqidno:9所示的序列的vh,以及包含seqidno:10所示的序列的vl。
在一个实例中,化合物是包含抗体2f5的人源化可变区的蛋白质。例如,蛋白质包含可变区,其包含抗体2f5的vh和/或vl的互补决定区(cdr)。
例如,该蛋白质包含:
(i)含下述的vh:
(a)cdr1,其包含seqidno:9的氨基酸25-34所示的序列;
(b)cdr2,其包含seqidno:9的氨基酸49-65所示的序列;和
(c)cdr3,其包含seqidno:9的氨基酸98-107所示的序列;和/或
(ii)含下述的vl:
(a)cdr1,其包含seqidno:10的氨基酸24-34所示的序列;
(b)cdr2,其包含seqidno:10的氨基酸50-56所示的序列;和
(c)cdr3,其包含seqidno:10的氨基酸89-96所示的序列。
在另一个实例中,使用例如本领域已知或本文简要描述的标准方法制备包含其可变区的抗体或蛋白质。
基于免疫的方法
为了产生抗体,任选地用任何合适的或期望的佐剂和/或药学上可接受的运载体配制的vegf-b或其携带表位的片段或其部分或其修饰形式或编码其的核酸(“免疫原”)以可注射组合物形式给予对象(例如,非人类动物对象,例如小鼠,大鼠,鸡等)。示例性的非人类动物是哺乳动物,例如鼠动物(例如大鼠或小鼠)。注射可以是鼻内,肌肉内,皮下,静脉内,皮内,腹膜内或其他已知途径。任选地,免疫原被给予多次。用于制备和表征抗体的方法是本领域已知的(参见例如《抗体:实验室手册》,冷泉港实验室(antibodies:alaboratorymanual,coldspringharborlaboratory)1988)。在wo2006/012688中描述了在小鼠中产生抗vegf-b抗体的方法。
通过在免疫后各点对免疫的动物的血液进行取样来监测多克隆抗体的产生。如果需要,可以给予第二次加强注射以实现所需抗体滴度。重复加强和效价测定的过程直至达到合适的效价。在获得所需免疫原性水平时,对免疫的动物取血并分离和储存血清,和/或将该动物用于生成单克隆抗体(mab)。
单克隆抗体是本公开所涵盖的示例性抗体。通常,单克隆抗体的产生涉及在足以刺激产生抗体的细胞的条件下用免疫原免疫对象(例如,啮齿动物,例如小鼠或大鼠)。在一些实例中,将经遗传工程改造以表达人抗体并且不表达鼠抗体蛋白质的小鼠免疫以产生抗体(例如,如pct/us2007/008231和/或lonberg等,nature368(1994):856-859中所述)。免疫后,产生抗体的体细胞(例如b淋巴细胞)与永生细胞例如永生性骨髓瘤细胞融合。用于产生这种融合细胞(杂交瘤)的各种方法在本领域是已知的,并且描述于例如kohler和milstein,nature256,495-497,1975。然后可以在足以产生抗体的条件下培养杂交瘤细胞。
本公开考虑了用于产生抗体的其它方法,例如abl-myc技术(例如在largaespada等,curr.top.microbiol.immunol,166,91-96.1990中所述)。
基于文库的方法
本公开还包括筛选抗体或包含其抗原结合结构域(例如包含其可变区)的蛋白质的文库,以鉴定vegf-b结合抗体或包含其可变区的蛋白质。
本公开所涵盖的文库的实例包括初始文库(来自未经挑战(unchallenged)的对象),免疫文库(来自用抗原免疫的对象)或合成文库。通过常规技术(例如,如sambrook和russell编辑的《分子克隆:实验室手册》第三版第1-3卷,冷泉港实验室出版社,2001,所述)克隆编码抗体或其区域的核酸,并用于使用本领域已知的方法编码和展示蛋白质。用于产生蛋白质文库的其它技术描述于例如us6300064(例如,morphosysag的hucal文库);us5885793;us6204023;us6291158;或us6248516中。
根据本公开的蛋白质可以是可溶性分泌蛋白质,或者可以作为融合蛋白质呈现在细胞或颗粒(例如,噬菌体或其它病毒,核糖体或孢子)的表面上。各种展示库格式在本领域中是已知的。例如,文库是体外展示库(例如,核糖体展示文库,共价展示文库或mrna展示文库,例如,如us7270969中所述)。在另一个实例中,展示文库是噬菌体展示文库,其中包含抗体的抗原结合结构域的蛋白质在噬菌体上表达,例如如us6300064;us5885793;us6204023;us6291158;或us6248516所述。其它噬菌体展示方法是本领域已知的,并且由本公开涵盖。类似地,细胞展示的方法被本公开涵盖,例如细菌展示文库,例如us5516637中所述;酵母展示文库,例如如us6423538或哺乳动物展示文库中所述。
筛选展示文库的方法是本领域已知的。在一个实例中,使用亲和纯化筛选本公开的展示文库,例如scopes所述(《蛋白质纯化:原理和实践》第三版中,(proteinpurification:principlesandpractice,thirdedition)springerverlag,1994)。亲和纯化方法通常包括使包含文库展示的抗原结合结构域的蛋白质与靶抗原(例如vegf-b)接触,并且在洗涤后洗脱那些仍然结合抗原的结构域。
如果需要,通过筛选鉴定的任何可变区或scfv容易修饰成完整的抗体。将可变区或scfv修饰或转格式成完整抗体的示例性方法描述于例如jones等,jimmunolmethods.354:85-90,2010;或jostock等,jimmunolmethods,289:65-80,2004。或者或另外,使用标准克隆方法,例如,ausubel等(刊于:《新编分子生物学方法》(currentprotocolsinmolecularbiology).韦利科学出版社,isbn047150338,1987)和/或sambrook等(刊于:《分子克隆:实验室手册》(molecularcloning:alaboratorymanual),冷泉港实验室出版社,纽约,第三版2001)所述。
去免疫的、嵌合的、人源化的、同人源化的,灵长类化的和人的蛋白质
本公开的蛋白质可以是人源化蛋白质。
术语“人源化蛋白质”应理解为指包含人样可变区(human-likevariableregion)的蛋白质,其包含移植于来自人抗体的fr上或插入来自人抗体的fr中的来自非人物种(如小鼠或大鼠或非人灵长类动物)的抗体的cdr(该抗体类型还称为“cdr移植抗体”)。人源化蛋白质还包含下述蛋白质:其中人蛋白质的一个或多个残基被一个或多个氨基酸取代修饰和/或人蛋白质的一个或多个fr残基被相应非人残基替代。人源化蛋白质还可包含不是在人抗体也不是在非人抗体中发现的残基。该蛋白质的任何其他区域(如fc区)通常是人的。可使用本领域已知的方法进行人源化,例如us5225539、us6054297、us7566771或us5585089。术语“人源化蛋白质”还包括超人源化蛋白质,例如us7732578中所述。
本公开的蛋白质可以是人蛋白质。本文所用术语“人蛋白质”指具有人中发现(例如人种系或体细胞中或来自使用这类区域生产的文库)的可变和任选的恒定抗体区的蛋白质。该“人”抗体可包含不是由人序列编码的氨基酸残基,例如通过体外随机或定点突变导入的突变(特别是涉及少量蛋白质残基(例如该蛋白质的残基中的1、2、3、4或5个)中的突变或保守性取代的突变)。这些“人抗体”无需作为人免疫应答的结果而生成,而是,可使用重组方法(如筛选噬菌体展示文库)和/或通过包含编码人抗体恒定和/或可变区的转基因动物(如小鼠)和/或使用指导选择(例如us5565332中所述)来生成。该术语还包括这类抗体的亲和成熟形式。出于本发明的目的,人抗体可被认为包含以下蛋白质,该蛋白质包含来自人抗体的fr或含有来自人fr的共有序列的序列的fr且其中一个或多个cdr是随机或半随机的,例如us6300064和/或us6248516中所述。
本公开的蛋白质可以是同人源化蛋白质。术语“同人源化蛋白质”指通过wo2007/019620中所述方法制备的蛋白质。同人源化蛋白质包含抗体的可变区,其中该可变区包含来自新世界(newworld)灵长类动物抗体可变区的fr和来自非新世界灵长类动物抗体可变区的cdr。例如,同人源化蛋白质包含抗体的可变区,其中该可变区包含来自新世界灵长类动物抗体可变区的fr和来自小鼠或大鼠抗体的cdr。
本公开的蛋白质可以是灵长类化蛋白质。“灵长类化蛋白质”包含来自抗体的可变区,其在非人灵长类动物(如猕猴)的免疫后生成。任选地,该非人灵长类动物抗体的可变区与人恒定区相连以生成灵长类动物化抗体。用于生产灵长类化抗体的示例性方法描述于us6113898。
在一个实例中,本公开的蛋白质是嵌合蛋白。术语“嵌合蛋白”指以下蛋白质,其中抗原结合结构域来自特定物种(如鼠,如小鼠或大鼠)或属于特定抗体类或亚类,而该蛋白质的剩余部分来自来源于其他物种(例如人或非人灵长类动物)的蛋白质或属于另一抗体类或亚类。在一个实施例中,嵌合蛋白是嵌合抗体,其包含来自非人抗体(如鼠抗体)的vh和/或vl且该抗体的剩余部分来自人抗体。这类嵌合蛋白的生产是本领域已知的且可通过标准方法实现(描述于例如us6331415;us5807715;us4816567和us4816397)。
本发明还涉及去免疫化蛋白质,例如wo2000/34317和wo2004/108158中所述。去免疫化抗体和蛋白质除去(即突变)了一个或多个表位(如b细胞表位或t细胞表位),从而降低对象产生针对该抗体或蛋白质的免疫应答的可能性。
包含抗体可变区的其他蛋白质
本公开还涉及包含抗体的可变区或抗原结合结构域的其它蛋白质,例如:
(i)单结构域抗体,其是包含抗体vh或vl的全部或部分的单个多肽链(参见例如us6248516);
(ii)双抗体,三抗体和四抗体,例如us5844094和/或us2008152586中所述;
(iii)scfv,例如us5260203中所述;
(iv)微抗体(minibody),例如us5837821中所述;
(v)“钥匙和孔”双特异性抗体,如us5731168中所述;
(vi)异源偶联蛋白质,如us4676980中所述;
(vii)使用化学交联剂生产的异源偶联蛋白质,如us4676980中所述;
(viii)fab'-sh片段,例如shalaby等,j.exp.med.,175:217-225,1992所述;或
(ix)fab3(如ep19930302894中所述)。
恒定域融合
本公开内容涵盖包含抗体的可变区和恒定区或fc或其结构域例如ch2和/或ch3结构域的蛋白质。合适的恒定区和/或结构域对本领域技术人员来说是显而易见的,和/或这些多肽的序列可从公众可获得的数据库中容易获得。kabat等人还提供了一些合适的恒定区/结构域的描述。
恒定区和/或其结构域可用于提供生物活性,例如二聚化,延长的血清半衰期,例如通过结合fcrn(新生儿fc受体),抗原依赖性细胞毒性(adcc),补体依赖性细胞毒性(cdc),抗原依赖性细胞吞噬作用(adcp)。
本公开还涉及包含突变体恒定区或结构域的蛋白质,例如us7217797;us7217798;或us20090041770(具有增加的半衰期)或us2005037000(增加的adcc)中所述。
稳定化的蛋白质
本公开的中和蛋白质可以包含igg4恒定区或稳定化的igg4恒定区。术语“稳定化的igg4恒定区”应理解为指经修饰以降低fab臂交换或经历fab臂交换的倾向或形成半抗体或形成半抗体的倾向的igg4恒定区。“fab臂交换”指针对人igg4的一种蛋白修饰类型,其中igg4重量和相连的轻链(半分子)被交换成来自另一igg4分子的重链-轻链对。因此,igg4分子可能需要识别两个不同抗原的两个不同的fab臂(导致双特异性分子)。fab臂交换在体内天然发生并可在体外被纯化的血细胞或还原剂(如还原型谷胱甘肽)诱导。当igg4抗体解离以形成两个分子(各分子含有单条重链和单条轻链)时,形成“半抗体”。
在一个实施例中,稳定化的igg4恒定区包含根据kabat的系统的铰链区的241位处的脯氨酸(kabat等,sequencesofproteinsofimmunologicalinterest(免疫学感兴趣的蛋白质序列),华盛顿特区,美国,健康与人类服务部,1987和/或1991)。该位置对应于根据eu编码系统的铰链区的228位(kabat等,sequencesofproteinsofimmunologicalinterest(免疫学感兴趣的蛋白质序列),华盛顿特区,美国,健康与人类服务部,2001和edelman等,proc.natl.acad.usa,63,78-85,1969)。在人igg4中,该残基通常是丝氨酸。在使用脯氨酸取代丝氨酸后,该igg4铰链区包含序列cppc。在该方面,本领域技术人员应理解,“铰链区”是连接fc和fab区的抗体重链恒定区的富脯氨酸部分,其赋予抗体的两个fab臂移动性。该铰链区包含半胱氨酸残基,其涉及重链间二硫键。根据kabat的编码系统,其通常定义为从人igg1的glu226延伸至pro243。可通过将形成重链间二硫(s-s)键的第一和最后一个半胱氨酸残基置于相同位置来将其他igg同种型的铰链区与igg1序列对齐(参见例如wo2010/080538)。
其他基于蛋白质的vegf-b信号传导抑制剂
可能干扰vegf-b与其受体的生产性相互作用的其它蛋白质包括突变型vegf-b蛋白。
在一个实例中,抑制剂是包含结合vegf-b(和,例如基本上不与vegf-a结合)的vegf-r1的一个或多个结构域的可溶性蛋白质。在一个实例中,可溶性蛋白质另外包含抗体的恒定区,例如igg1抗体。例如,可溶性蛋白质另外包含fc区和任选的抗体的铰链区,例如igg1抗体。
在一个实例中,蛋白质抑制剂是抗体模拟物,例如包含以类似于抗体的方式结合靶蛋白质的可变区的蛋白质支架。关于示例性抗体模拟物的描述如下。
免疫球蛋白和免疫球蛋白片段
本公开的化合物的实例是包含免疫球蛋白的可变区的蛋白质,例如t细胞受体或重链免疫球蛋白(例如,ignar,骆驼抗体)。
重链免疫球蛋白
重链免疫球蛋白与许多其他免疫球蛋白(例如抗体)形式在结构上不同,虽然其包含重链,但不包含轻链。因此,这些免疫球蛋白也称为“仅重链抗体”。重链免疫球蛋白发现于例如驼科动物和软骨鱼中(也称作ignar)。
天然产生的重链免疫球蛋白中存在的可变区通常称作驼科动物免疫球蛋白中的“vhh结构域”和ignar中的v-nar,从而将其与常规4链抗体中存在的重链可变区(其称作“vh结构域”)和常规4链抗体中存在的轻链可变区(其称作“vl结构域”)区分。
重链免疫球蛋白不需要轻链的存在以高亲和力和高特异性结合相关抗原。这意味着单结构域结合片段可以衍生自易于表达并且通常是稳定和可溶的重链免疫球蛋白。
来自驼科动物的重链免疫球蛋白及其可变区和其生产和/或分离和/或使用方法的一般描述参见以下参考文献(但不限于此):wo94/04678、wo97/49805和wo97/49805。
来自软骨鱼的重链免疫球蛋白及其可变区和其生产和/或分离和/或使用方法的一般描述参见wo2005/118629(但不限于此)。
v-样蛋白质
本公开的化合物的实例是t细胞受体。t细胞受体具有两个v结构域,其结合成类似于抗体的fv组件的结构。novotny等,procnatlacadsciusa88:8646-8650,1991描述了t细胞受体的两个v-结构域(称为α和β)如何融合并表达为单链多肽,以及如何改变表面残基以类似于抗体scfv而直接降低疏水性。描述包含两个v-α和v-β结构域的单链t细胞受体或多聚体t细胞受体的生产的其他公开包括wo1999/045110或wo2011/107595。
包含抗原结合结构域的其它非抗体蛋白质包括通常为单体的具有v样结构域的蛋白质。包含这种v样结构域的蛋白质的实例包括ctla-4,cd28和icos。包含这种v样结构域的蛋白质的进一步公开包括在wo1999/045110中。
模拟抗体蛋白
在一个实例中,本公开的化合物是模拟抗体蛋白(adnectin)。模拟抗体蛋白基于人纤维连接蛋白的第十个纤连蛋白iii型(10fn3)结构域,其中环区被改变以赋予抗原结合能力。例如,可以对10fn3结构域的β-夹心的一端的三个环进行工程改造以使模拟抗体蛋白能够特异性识别抗原。详细内容参见us20080139791或wo2005/056764。
抗运载蛋白(anticalins)
在另一个实例中,本公开的化合物是抗运载蛋白。抗运载蛋白衍生自脂质运载蛋白,其是运输小疏水分子如类固醇,二价位素,类视色素和脂质的细胞外蛋白质家族。脂质运载蛋白具有刚性β-折叠二级结构,在锥形结构的开口端具有多个环,其可被工程化以结合抗原。这种工程改造的脂质运载蛋白被称为抗运载蛋白。有关抗运载蛋白的进一步描述,请参见us7250297b1或us20070224633。
亲和体
在另一个实例中,本公开的化合物是亲和体。亲和体是衍生自金黄色葡萄球菌的蛋白a的z结构域(抗原结合结构域)的支架,其可被工程改造以结合抗原。z结构域由约58个氨基酸的三螺旋束组成。文库通过表面残基的随机化产生。详见ep1641818。
高亲合性多聚体
在另一个实例中,本公开的化合物是高亲合性多聚体。高亲合性多聚体是衍生自a结构域支架家族的多结构域蛋白。约35个氨基酸的天然结构域采用限定的二硫键结构。多样性是通过改变a结构域家族所显示的自然变异产生的。详见wo2002088171。
darpin
在另一个实例中,本公开的化合物是设计的锚蛋白重复蛋白(darpin)。darpin衍生自锚蛋白,其是介导整合膜蛋白与细胞骨架的附着的蛋白质家族。单个锚蛋白重复是由两个α-螺旋和β-转角组成的33个残基基序。它们可以被工程改造成通过随机化每个重复的β-转角和第一个α-螺旋中的残基来结合不同的靶抗原。可以通过增加模块数量(亲和力成熟的方法)来增加它们的结合界面。详见us20040132028。
生产蛋白质的方法
重组表达
在重组蛋白的情况下,可将编码该物质的核酸克隆至载体,随后转染至宿主细胞,例如大肠杆菌细胞、酵母细胞、昆虫细胞或哺乳动物细胞(如猿cos细胞、中华仓鼠卵巢(cho)细胞、人胚胎肾(hek)细胞或不另外生产抗体的骨髓瘤细胞)。用于表达本公开的蛋白的示例性细胞是cho细胞、骨髓瘤细胞或hek细胞。实现这些目的的分子克隆技术是本领域已知的且描述于例如ausubel等(编),currentprotocolsinmolecularbiology(《新编分子生物学实验指南》),格林出版联合公司和韦利科学公司(1988,包括直至今日的所有更新)或sambrook等,molecularcloning:alaboratorymanual(《分子克隆:实验室手册》),冷泉港实验室出版社(1989)。多种克隆和体外扩增方法适用于重组核酸的构建。生产重组抗体的方法是本领域已知的,参见例如us4816567或us5530101。
分离后,插入核酸使其可操作地连接于表达构建体或表达载体中的启动子以用于进一步克隆(dna的扩增)或用于在无细胞系统或细胞中表达。
本文所用术语“启动子”应取其最广泛的含义并包括基因组基因的转录调控序列,包括tata盒或精确的转录起始所必需的起始元件,其具有或不具有改变核酸表达的其他调控元件(如上游激活序列、转录因子结合位点、增强子和沉默子),例如在对发育和/或外部刺激的应答中,或以组织特异性方式。本文中,术语“启动子”还用于描述重组、合成或融合核酸或衍生物,其对所可操作地连接的核酸赋予、激活或增强其表达。示例性启动子可含有一个或多个特定调控元件的其他拷贝以进一步增强表达和/或改变所述核酸的空间表达和/或时间表达。
本文所用术语“可操作地连接”指相对于核酸定位启动子,使得该核酸的表达受该启动子的控制。
可以获得用于在细胞中表达的许多载体。载体组分通常包括但不限于以下一种或多种:信号序列、编码抗体(例如来源于本文提供的信息)的序列、增强子元件、启动子和转录终止序列。本领域技术人员应理解用于抗体表达的合适序列。示例性信号序列包括原核分泌信号(如pelb、碱性磷酸酶、青霉素酶、ipp或热稳定肠毒素ii)、酵母分泌信号(如转化酶前导物、α因子前导物或酸性磷酸酶前导物)或哺乳动物分泌信号(如单纯疱疹gd信号)。
哺乳动物细胞中有活性的示例性启动子包括巨细胞病毒立即早期启动子(cmv-ie)、人延伸因子1-α启动子(ef1)、小核rna启动子(u1a和u1b)、α-肌球蛋白重链启动子、猿病毒40启动子(sv40)、劳氏肉瘤病毒启动子(rsv)、腺病毒主要晚期启动子、β-肌动蛋白启动子;包含cmv增强子/β-肌动蛋白启动子或免疫球蛋白启动子或其活性片段的杂交体调控元件。有用的哺乳动物宿主细胞系的示例是通过sv40转化的猴肾cv1系(cos-7,atcccrl1651);人胚胎肾系(293或亚克隆的293细胞,用于在悬浮培养物中生长);幼仓鼠肾细胞(bhk,atccccl10);或中华仓鼠卵巢细胞(cho)。
适用于酵母细胞(例如选自下组的酵母细胞:毕赤酵母(pichiapastoris)、酿酒酵母(saccharomycescerevisiae)和粟酒裂殖酵母(s.pombe))中表达的典型启动子包括但不限于:adh1启动子、gal1启动子、gal4启动子、cup1启动子、pho5启动子、nmt启动子、rpr1启动子或tef1启动子。
将分离的核酸或包含该物质的表达构建体导入细胞用于表达的方法是本领域技术人员已知的。用于给定细胞的技术依赖于已知的成功技术。将重组dna导入细胞的方法包括微注射、deae-葡聚糖介导的转染、脂质体介导的转染(如通过使用脂质转染胺试剂(美国马里兰州的吉布科公司(gibco))和/或细胞转染试剂(美国马里兰州的吉布科公司))、peg介导的dna摄取、电穿孔和微粒轰击(例如通过使用dna包覆的钨或金颗粒(美国威斯康星州的安哥路斯特公司(agracetusinc.)))等。
用于生产该抗体的宿主细胞可在多种培养基中培养,这取决于使用的细胞类型。市售可得的培养基(如ham'sf10(西格玛公司)、极限必需培养基(mem)(西格玛公司)、rpml-1640(西格玛公司)和达尔伯克改良伊格尔培养基(dmem)(西格玛公司))适用于培养哺乳动物细胞。用于培养本文所讨论的其他细胞类型的培养基是本领域已知的。
蛋白质纯化
生产/表达后,使用本领域已知的方法纯化本公开的蛋白质。这种纯化提供了基本上不含非特异性蛋白质,酸,脂质,碳水化合物等的本公开的蛋白质。在一个实例中,蛋白质将处于制剂中,其中制剂中超过约90%(例如95%,98%或99%)的蛋白质是本公开的蛋白质。
使用肽纯化的标准方法来获得本公开的分离的蛋白质,包括但不限于各种高压(或高效)液相色谱(hplc)和非hplc多肽分离方案,例如尺寸排阻色谱法,离子交换色谱法,疏水相互作用色谱法,混合模式色谱法,相分离方法,电泳分离,沉淀方法,盐溶/盐析方法,免疫色谱法和/或其他方法。
在一个实例中,亲和纯化可用于分离包含标记的融合蛋白。使用亲和层析法分离蛋白质的方法是本领域已知的,并且例如scopes所述(刊于:proteinpurification:principlesandpractice(《蛋白纯化:原理和实践》),第三版,施普林格弗莱格公司(springerverlag),1994)。例如,结合标记的抗体或化合物(在多组氨酸标签的情况下,可以是例如镍-nta)被固定在固体支持物上。然后将包含蛋白质的样品与固定的抗体或化合物在足以发生结合的条件下接触一段时间。洗涤后除去任何未结合或非特异性结合的蛋白质,蛋白质被洗脱。
在包含抗体的fc区的蛋白质的情况下,蛋白a或蛋白g或其修饰形式可用于亲和纯化。蛋白a可用于分离包含人γ,γ2或γ4重链fc区的纯化蛋白质。蛋白g被推荐用于所有小鼠fc同种型和人γ3。
基于核酸的vegf-b信号传导抑制剂
在本公开的一个实例中,根据本公开任何实例的本文所述的治疗和/或预防方法涉及降低vegf-b的表达。例如,这种方法包括给予减少核酸的转录和/或翻译的化合物。在一个实例中,化合物是核酸,例如反义多核苷酸,核酶,pna,干扰rna,sirna,微小rna。
反义核酸
术语“反义核酸”应被认为是指与编码如本公开的任何示例中所述的多肽的特定mrna分子的至少一部分互补的并且能够干扰转录后事件(例如mrna翻译)的dna或rna或其衍生物(例如,lna或pna)或其组合。反义方法的使用在本领域中是已知的(参见例如hartmann和endres(编辑),反义方法手册(manualofantisensemethodology),kluwer出版社(1999))。
本公开的反义核酸将在生理条件下与靶核酸杂交。反义核酸包括对应于结构基因或编码区的序列或影响对基因表达或剪接的控制的序列。例如,反义核酸可以对应于编码vegf-b或5'非翻译区(utr)或3'utr或它们的组合的核酸的靶向编码区。内含子序列可能是部分互补的,其可能在转录过程中或之后被剪接出,例如仅与目的基因的外显子序列互补。反义序列的长度应为编码vegf-b的核酸的至少19个连续核苷酸,例如至少50个核苷酸,例如至少100、200、500或1000个核苷酸。可以使用与整个基因转录物互补的全长序列。长度可以是100-2000个核苷酸。反义序列与靶向转录物的同一性程度应至少为90%,例如95-100%。
针对vegf-b的示例性反义核酸描述于例如wo2003/105754中。
催化核酸
术语“催化核酸”是指dna分子或含dna分子(在本领域中也称为“脱氧核酶”或“dna酶”)或rna或含rna分子(也称为“核酶”或“rna酶”),其特异性识别不同的底物并催化该底物的化学修饰。催化核酸中的核酸碱基可以是碱基a,c,g,t(和用于rna的u)。
通常,催化性核酸含有用于特异性识别靶核酸的反义序列和切割酶活性的核酸(本文中也称为“催化结构域”)。在本公开中有用的核酶类型是锤头核酶和发夹核酶。
rna干扰
rna干扰(rnai)可用于特异性抑制特定蛋白质的产生。不受理论的限制,该技术依赖于dsrna分子的存在,所述dsrna分子含有基本上与目的基因的mrna或其一部分相同的序列,在本文情况下是编码vegf-b的mrna。方便地,dsrna可以从重组载体宿主细胞中的单个启动子产生,其中正义和反义序列侧翼是无关序列,其使得正义和反义序列能够杂交以形成dsrna分子,其具有无关序列来形成环状结构。本公开的合适的dsrna分子的设计和生产完全在本领域技术人员的能力范围内,特别是考虑到wo99/32619,wo99/53050,wo99/49029和wo01/34815。
杂交的正义和反义序列的长度应分别为至少19个连续核苷酸,例如至少30或50个核苷酸,例如至少100、200、500或1000个核苷酸。可以使用与整个基因转录物相对应的全长序列。长度可以是100-2000个核苷酸。正向和反义序列与目标转录物的同一性程度应至少为85%,例如至少90%,例如95-100%。
示例性的小干扰rna(“sirna”)分子包含与靶mrna的约19-21个连续核苷酸相同的核苷酸序列。例如,sirna序列开始于二核苷酸aa,包含约30-70%的gc含量(例如30-60%,例如40-60%,例如约45%-55%),并且与其将被引入的哺乳动物的基因组中的靶基因之外的任何核苷酸序列不具有高百分比同一性,例如通过标准blast搜索确定。降低vegf-b表达的示例性sirna可从santacruz生物科技公司或novus生物公司购得。
降低vegf-b表达的短发夹rna(shrna)也是本领域已知的,可从santacruz生物科技公司购得。
筛选试验
可以使用本领域已知的技术来鉴定抑制vegf-b信号传导的化合物,例如如下所述。类似地,可以使用本领域已知的技术来确定或估计适用于本文所述方法的vegf-b信号传导抑制剂的量,例如如下所述。
中和试验
对于结合vegf-b并抑制信号传导的化合物,可以使用中和试验。
在一个实例中,中和试验包括在存在或不存在可检测标记的可溶性vegf-r1时将vegf-b与化合物接触或在表达vegf-r1或可溶性vegf-r1的细胞存在或不存在下将可检测标记的vegf-b与化合物接触。然后评估与vegf-r1结合的vegf-b的水平。在化合物存在下,与不存在化合物相比,结合的vegf-b的水平降低表明该化合物抑制vegf-b与vegf-r1的结合,并且因此导致抑制vegf-b信号传导。
在wo2006/012688中描述了另一种中和试验法,并且涉及将包含固定在固体支持物上的第二ig样结构域的vegf-r1片段与和化合物预孵育的亚饱和浓度的重组vegf-b接触。洗涤后除去未结合的蛋白质,将固定的蛋白质与抗vegf-b抗体接触,测定结合的抗体量(指示固定的vegf-b)。相比不存在该化合物时的水平,降低结合抗体水平的化合物被认为是vegf-b信号传导的抑制剂。
在另一个实例中,使用依赖于vegf-b信号传导增殖的细胞来鉴定抑制vegf-b信号传导的化合物,例如,如wo2006/012688中所述修饰的baf3细胞以表达掺入人的红细胞生成素受体的细胞内结构域和vegf-r1的细胞外结构域的嵌合受体。细胞在vegf-b存在下和化合物存在或不存在下培养。然后使用标准方法,例如集落形成试验,胸苷掺入或另外合适的细胞增殖标记物的摄取(例如mts染料还原试验)来评估细胞增殖。在vegf-b存在下降低增殖水平的化合物被认为是vegf-b信号传导的抑制剂。
还可以使用标准方法评价化合物与vegf-b结合的能力。评估与蛋白质结合的方法是本领域已知的,例如scopes所述(刊于:proteinpurification:principlesandpractice(《蛋白纯化:原理和实践》),第三版,施普林格弗莱格公司(springerverlag),1994)。这种方法通常包括标记化合物并使其与固定的vegf-b接触。清洗以除去非特异性结合的化合物后,检测标签的量和作为结果的结合的化合物。当然,化合物可以被固定化,并且vegf-b被标记。还可使用平移型试验(panning-typeassay)。或者或此外,可以使用表面等离振子共振试验。
表达试验
通过使细胞与化合物接触并确定vegf-b的表达水平来鉴定减少或阻止vegf-b表达的化合物。确定核酸水平的基因表达的合适方法是本领域已知的,包括例如定量聚合酶链反应(qpcr)或微阵列试验。在蛋白质水平上确定表达的合适方法也是本领域已知的,包括例如酶联免疫吸附试验(elisa),荧光连接免疫吸附试验(flisa),免疫荧光或western印迹。
体内试验
本文所述的化合物可以在动物模型中测试活性。在一个实例中,动物模型是代谢功能障碍和高血糖的模型。例如,饮食诱导的肥胖(dio)小鼠模型。这是一个成熟的实验范例,小鼠的外周组织中发育过度或异位脂质沉积,与胰岛素敏感性和葡萄糖摄取受损有关,小鼠表现出肥胖、高胰岛素血症、高血糖、血脂异常和高血压(harberg,c.e.,等.nature490,426-430;collins,s.,等pysiology&behaviour81,243-248)。
存在用于在非人类动物对象中诱导缺血性中风的各种已知技术,例如主动脉/腔静脉闭塞,外部颈部韧带或袖带,出血或低血压,颅内高压或颈总动脉闭塞,双血管闭塞和低血压,四血管闭塞,单侧颈总动脉闭塞(仅一些物种),内皮素-1诱导的动脉和静脉收缩,中脑动脉闭塞(mcao),自发性脑梗死(自发性高血压大鼠),大球栓塞,血栓栓塞或微球栓塞。出血性中风可以通过将胶原酶输入大脑来建模。
在一个实例中,中风模型包括中脑动脉闭塞(mcao)以产生缺血性中风,如先前在su等naturemedicine,2008;14:731-737中所述。
药物组合物和治疗方法
抑制vegf-b信号传导的化合物(合成活性成分)可用于胃肠外,外用,口服或局部给药,气雾剂给药或透皮给药,用于预防性或治疗性治疗。在一个实例中,化合物肠胃外给药,例如皮下或静脉内给予。
待给予的化合物的配制将根据所选择的给药途径和制剂(例如溶液,乳剂,胶囊)而变化。可以在生理上可接受的运载体中制备包含待给予化合物的合适的药物组合物。对于溶液或乳剂,合适的运载体包括例如水溶液或醇/水溶液,乳液或悬浮液,包括盐水和缓冲介质。胃肠道外载剂可包括氯化钠溶液、林格右旋糖、右旋糖和氯化钠、乳酸林格溶液或固定油。各种合适的水性运载体是本领域技术人员已知的,包括水,缓冲水,缓冲盐水,多元醇(例如甘油,丙二醇,液体聚乙二醇),葡萄糖溶液和甘氨酸。静脉内载剂可以包括各种添加剂,防腐剂或流体,营养物质或电解质补充剂(参见《雷明顿药物科学》(remington'spharmaceuticalscience)第16版,mack编,1980)。组合物可任选地含有药学上可接受的辅助物质,以接近生理条件,如ph调节和缓冲剂和毒性调节剂,例如乙酸钠,氯化钠,氯化钾,氯化钙和乳酸钠。根据本领域已知的冻干和重建技术,该化合物可以在使用前冻干以储存并在合适的载体中重建。
所选培养基中活性成分的最佳浓度可以根据本领域技术人员已知的程序经验性地确定,并且将取决于所需的最终药物制剂。
本公开的化合物的给药剂量范围是足够大以产生所需效果的剂量范围。例如,组合物包含治疗或预防有效量的化合物。
如本文所用,术语“有效量”应被认为是指足够量的化合物以抑制/减少/预防对象中vegf-b的信号传导。技术人员将知道,这样的量将根据例如化合物和/或特定对象和/或所治疗的中风的类型和/或严重程度而变化。因此,该术语不应被解释为将本公开限制于特定量,例如化合物的重量或数量。
如本文所用,术语“治疗有效量”应被认为是指足够量的化合物以减少或抑制一种或多种中风症状。
本文所用术语“预防有效量”应理解为指足以预防或抑制或延迟中风的一种或多种可检测症状发生的化合物的量。
在一个实例中,化合物以有效地具有以下一种或多种效果的量给予:
减少或防止血脑屏障的破坏;
减少或防止脑中的血管通透性;
降低或防止大脑梗塞大小;和/或
减少或防止颅内出血。
剂量不宜大到引起不良副作用,如超粘滞综合征,肺水肿,充血性心力衰竭等。通常,剂量将随着患者的年龄、病症、性别和疾病的程度而变化,并且可以由本领域技术人员确定。如果发生任何并发症,可由医师调整剂量。
剂量可以在约0.1mg/kg至约300mg/kg之间变化,例如约0.2mg/kg至约200mg/kg,例如约0.5mg/kg至约20mg/kg,每天一次或多次剂量给药,持续一天或几天。
在一些实例中,化合物以比随后(维持剂量)高的初始(或加载)剂量给予。例如,化合物以约1mg/kg至约30mg/kg的初始剂量给予。然后以约0.001mg/kg至约1mg/kg的维持剂量给予该化合物。维持剂量可以每隔7-35天给予,例如每14或21或28天给予。
在一些实例中,使用剂量递增方案,其中化合物最初以比后续剂量中使用的剂量低的剂量给予。该剂量方案在对象最初遭受不良事件的情况下是有用的。
在对象未对治疗产生适当应答的情况下,可在一周内给予多重剂量。或者或此外,可给予递增的剂量。
在一个实例中,本公开的化合物与至少一种目前正在使用或正用于预防或治疗中风的已知化合物组合使用。这些已知化合物的实例包括但不限于常见的溶血栓剂,例如组织纤溶酶原激活物(例如阿替普酶,替勃拉普酶,替奈普酶),丝裂霉素酶,链激酶,尿激酶,纤维蛋白酶,脱米替普酶和葡萄球菌激酶。
此外,本公开的方法还可以包括共同给予至少一种其它治疗剂用于治疗与中风直接或间接相关的另一种疾病,包括但不限于:血脂异常,高血压,肥胖,神经病和/或视网膜病变等。可与本发明化合物共同给予的药剂的其它实例是皮质类固醇;免疫抑制药物;抗生素;抗高血压和利尿药物(如ace抑制剂);脂质降低剂如胆汁螯合剂树脂,考来烯胺,考来替泊,烟酸,更特别是用于降低胆固醇和甘油三酯的药剂和药物(例如贝特类(例如gemvibroziltm)和hmg-coa抑制剂如lovastatintm,atorvastatintm,fluvastatintm,lescoltm),lipitortm,mevacortm),pravacholtm,pravastatintm,simvastatintm,zocortm,cerivastatintm)等);抑制脂质的肠吸收的化合物(例如依泽替米德);烟酸;和维生素d。
从上文将显而易见,本公开提供了对对象的伴随治疗性治疗的方法,包括向有需要的对象给予有效量的第一化合物和第二化合物,其中所述药剂是本公开的化合物(即vegf-b信号传导的抑制剂),第二种药剂用于预防或治疗中风。
如本文所用,术语“伴随”如短语“伴随治疗”包括在第二药剂存在下给予第一药剂。伴随的治疗方法包括共同给予第一种,第二种,第三种或其它药剂的方法。伴随的治疗性治疗方法还包括其中在第二种或另外的药剂存在下给予第一种或其它药剂的方法,其中例如可以先前给予第二种或其它药剂。不同操作者可以逐步执行伴随的治疗方法。例如,一个操作者可以向对象给予第一药剂,并且第二操作者可以向对象给予第二药剂,并且可以在同一时间或几乎相同的时间或在较远的时间执行所述给药步骤,只要第一试剂(和/或其他药剂)在第二药剂(和/或另外的药剂)存在下给药之后。操作者和对象可以是相同的实体(例如人)。
可以从给予本发明化合物的时间开始测定另外的治疗剂的给药时间。间隔可以是例如5分钟到24或48小时。间隔可以是例如15分钟至6小时,15分钟至4.5小时,15分钟至3小时,15分钟至1小时,30分钟至6小时,或30分钟至3小时,或30分钟至4.5小时,或1至3小时,或1至4.5小时,或1至5小时,或1至6小时,或1至7小时,或1至8小时,或1至9小时,或1至10小时。
在一个实例中,本公开还提供了减少中风影响或治疗对象中风的方法,所述方法包括向对象给予溶血栓剂,其中对象正在接受或已经接受(例如,自从中风症状发作)vegf-b信号传导的抑制剂,给予患有中风并接受另一种治疗的对象。
试剂盒
本公开的另一个实例提供了包含如上所述用于治疗中风的化合物的试剂盒。
在一个实例中,试剂盒包含(a)容器,其包含本文所述的抑制vegf-b信号传导的化合物和/或本文所述的溶血栓化合物,任选地在药学上可接受的运载体或稀释剂中;和(b)具有用于减少对象中风的影响的说明书的包装插页。
根据本公开的该示例,包装插页在容器上或与容器相关联。合适的容器包括例如,瓶、小瓶和注射器等。该容器可由各种材料如玻璃或塑料制成。所述容器装载或包含有效于治疗中风的组合物,并且可具有无菌进入端口(例如,所述容器可以是具有皮下注射针可刺穿塞子的静脉输液袋或小瓶)。组合物中至少一种活性剂是抑制vegf-b信号传导的化合物。标签或包装插页表明组合物用于治疗符合治疗条件的对象,例如具有或易患中风的对象,并提供关于化合物和任何其他药物的给药量和间隔的具体指导。试剂盒还可以包含另外的容器,其包含药学上可接受的稀释缓冲液,例如用于注射的抑菌水(bwfi),磷酸盐缓冲盐水,林格氏溶液和/或葡萄糖溶液。试剂盒还可以包括从商业和用户的观点所需的其它材料,包括其它缓冲液,稀释剂,过滤器,针头和注射器。
本发明包括以下非限制性实施例。
实施例
实施例1:人原代脑源性内皮细胞中增加的脂肪酸摄取降低体外葡萄糖摄取
用vegf-b刺激的原代内皮细胞具有增加的脂肪酸摄取和降低的葡萄糖摄取
在37℃、5%co2的细胞培养箱中,将人原代脑微血管内皮细胞,hbmec(传代数<5)在含有5%胎牛血清(fcs)的补体包被的内皮基底培养基的24孔板中培养。刺激前6小时,用无脂肪酸牛血清白蛋白(faf-bsa)代替fcs,使内皮细胞饥饿。通过加入载剂(对照),100ng/mlvegf-b167(b167),100ng/mlvegf-b186(b186)或2μg/ml抗-vegf-b抗体2h10刺激细胞2小时。
刺激后,测量bodipy标记的脂肪酸(fa)或荧光葡萄糖类似物(2-nbdg)的摄取。2-nbdg用作葡萄糖摄取的标记物。细胞与bodipy-c12或2-nbdg示踪剂分别孵育5或20分钟。在添加2-nbdg之前,将细胞用kreb's林格缓冲液洗涤10分钟,以除去培养基来源的葡萄糖。用fa或葡萄糖示踪剂孵育后,在图像获取和定量之前洗涤和固定细胞。
用100ng/ml各vegf-b同种型(vegf-b167或vegf-b186)的刺激显著增加脂肪酸(fa)摄取并显著降低葡萄糖摄取。用阻断vegf-b抗体2h10单独处理不显著改变脂肪酸或葡萄糖摄取,但是观察到降低的fa摄取和增加的葡萄糖摄取的趋势,指示培养的内皮细胞中vegf-b的内源性产生和分泌。
这些数据显示,脑血管内皮细胞能够以增加的fa摄取和降低的葡萄糖摄取对vegf-b作出反应,表明脂质和葡萄糖的摄取可以以相互的方式在脑内皮中关联。
图1a和1b显示了用vegf-b蛋白处理的原代脑源性内皮细胞中增加的fa摄取和降低的葡萄糖摄取。
原代内皮细胞暴露于脂肪酸降低葡萄糖摄取
在棕榈酸钠和油酸钠(50μm)的混合物存在或不存在下培养人原代内皮细胞2小时或过夜,然后经历2-nbdg示踪剂并测定葡萄糖摄取。
暴露于富含fa的环境和脂质负载的内皮细胞显示体外摄取葡萄糖的能力显著降低。这表明体内高脂质环境中的内皮细胞,例如饮食诱导的肥胖(dio)模型中的内皮细胞可能类似地响应,并且这将理解为体内dio设置中组织葡萄糖摄取减少。
图1c显示暴露于脂肪酸的原代内皮细胞中葡萄糖摄取减少。暴露于脂质负载的内皮细胞表现出显著降低摄取葡萄糖的能力,这表明内皮细胞中fa的暴露和摄取降低了葡萄糖摄取。
实施例2:饮食诱导肥胖的小鼠具有增加的血糖水平和增加的缺血性中风的发病率
饮食诱导肥胖(dip)的小鼠血糖水平升高
三周龄的c57bl/6小鼠喂食高脂肪饮食(60%卡路里来自脂肪)或低脂肪对照饮食(正常食物,10%卡路里来自脂肪)15周。在食物取出后的同一时间测量血糖2小时,作为稳定血糖水平的平均值。切断尾巴,用葡萄糖计测量血滴。
根据以前的研究(hagberg等,nature2012;collins等,physiology&behavior2004),dio小鼠与正常食物中的年龄匹配小鼠相比,显示升高的血糖水平。
图2a显示,与正常食物中的年龄匹配的小鼠相比,具有dio的小鼠具有增加的血糖水平。
dip小鼠具有更严重的中风和增加的自发性出血发生率和较大的梗塞
将三周龄的雄性c57bl/6j小鼠置于高脂肪饮食(60%卡路里来自脂肪)或低脂肪对照饮食(正常食物,10%卡路里来自脂肪)至少12周,然后诱发脑缺血(中脑动脉闭塞(mcao)模型)。
为了使用mcao模型诱导脑缺血,将小鼠用水合氯醛(450mg/kg)麻醉,并将其置于解剖显微镜下。左侧mca通过开颅手术暴露,并且将激光多普勒血流探针置于从mca的分叉的大脑皮质表面1.5mm背侧中值。将探针连接到流量计,并且从用连续数据采集程序记录的组织灌注单元(tpu)确定相对脑血流量(cbf)。将3.5mw540nm激光从6cm的距离导向mca,通过尾静脉注射玫瑰红染料(rb)(50mg/kg)。当tpu下降到小于20%的预闭塞水平并且在激光撤出10分钟内不反弹时,实现了稳定闭塞。
为了确定梗塞体积,取出脑,切成2mm厚的冠状切片,并用4%2,3,5-三苯基四唑氯化物(ttc)染色。确定脑内五个冠状位的梗塞面积,并测量梗塞和半球体积。通过测量和并从对侧半球的体积中减去非梗塞的同侧半球的体积来计算梗塞体积。
dio小鼠比瘦小鼠有更严重的中风,自发性出血发生率显著增加,较大梗塞。dio模型的中风结果明显比正常饮食对照小鼠更糟,无论是在梗塞大小方面还是自发脑内出血(ich)发生率增加。
图2b和2c显示,具有dio的小鼠具有较大的中风体积并且在缺血性中风后出血增加。
具有dio的小鼠在脑缺血后显著增加vegf-b受体nrpl的表达
如上所述,对dio小鼠进行mcao。缺血后3小时,灌注并处死小鼠,同侧和对侧半球均质化,并制备总rna。通过qpcr定量vegfb及其受体vegfr1(flt1)和神经毡蛋白-1(nrpl)的转录水平。
相对于非缺血对侧半球,直到缺血3小时时vegfb和vegfr1表达均没有显著增加,然而在mcao后3小时,缺血半球nrpl的表达增加了近3倍,表明vegf-b信号可能在脑缺血期间局部增加。
图2d显示缺血性中风后dio小鼠的nrpl表达显著增加,而不是vegf-b或flt1表达。
实施例3:用中和抗vegf-b抗体(2h10)进行预防性治疗可预防dio小鼠的缺血性中风发展
vegf-b拮抗作用改善dio小鼠脑中葡萄糖摄取
c57bl/6j小鼠喂食正常食物(瘦肉)或高脂肪食物(dio),dio小鼠用同种型对照或抗vegf-b2h10抗体(16mg/kg)每周两次治疗30周,随后进行[18f]-dgpet成像。
与瘦肉对照小鼠相比,dio降低了脑中葡萄糖摄取(使用标记的葡萄糖类似物测定),并且具有dio的小鼠中的vegf-b的长期抑制作用显著改善了脑中的葡萄糖摄取。这些数据表明,与外周组织相似,与dio相关的全身代谢紊乱可能会降低大脑从血液中摄取葡萄糖的能力,vegf-b信号可能在dio模型中调节cns葡萄糖代谢中发挥作用。
图3a显示用2h10的vegf-b拮抗作用改善dio小鼠脑中的葡萄糖摄取。
预防性抗vegf-b处理显著降低dio小鼠缺血性中风的严重程度
为了直接测试vegf-b是否促进神经血管功能障碍,并在代谢紊乱的背景下增加缺血性中风的严重程度,在具有dio小鼠、有或没有针对vegf-b、2h10或同种型对照的单克隆抗体处理的小鼠中诱导血栓性中风。
在具有16mg/kg的任一抗体的mcao之前的第7天,第3天和第1小时,用3次注射(i.p.)处理小鼠1周。然后将小鼠进行光血栓性mcao并如上所述进行分析。在dio背景下用vegf-b阻断抗体2h10处理显著降低了梗塞大小和ich。
图3b和3c显示了dio小鼠用vegf-b阻断抗体(2h10)预防性治疗改善了缺血性中风后的结果。
用抗vegf-b预防性处理的dio小鼠在脑缺血后保留葡萄糖转运蛋白glut-1的表达
将三周龄的c57bl/6j小鼠喂食高脂肪食物17周,然后在mcao前第7天,第3天和第1小时通过ip注射用16mg/kg的同种型对照或抗vegf-b2h10抗体预处理1周。
用对照或2h10抗体预处理的dio小鼠在mcao后1小时灌注并固定在pfa中,并进行振荡切片。切片用针对glut-1的抗体染色并用免疫荧光检测。
dio小鼠脑血管中葡萄糖转运蛋白glut-1的染色证实,在缺血区边界,早在mcao后1小时,glut-1染色与非缺血半球中类似血管(对侧)相比明显下降。
在mcao部分保留半暗带血管中的glut-1抗原之前,用vegf-b阻断抗体2h10预处理一周。这表明用2h10阻断vegf-b信号可以通过保留glut-1葡萄糖转运蛋白功能来促进缺血半暗带中血管的更好的葡萄糖摄取,并且这又使该区域血流减少的血管更好地应付半暗带的缺氧和低血糖环境。
图3d显示与非缺血对侧半球相比,预处理的vegf-b阻断抗体2h10与缺血性脑半球中glut-1的保留质膜表达相关的dio小鼠。绘制免疫荧光的相对区域。
预防性抗vegf-b处理可以减少dio小鼠脑缺血后的血脑屏障渗漏
dio小鼠用如上所述的2h10或同种型对照抗体预先处理,随后是mcao。在诱导mcao之前,用70kda荧光葡聚糖示踪剂注射(iv)小鼠以允许分析bbb通透性。在mcao诱导后1小时,灌注小鼠,轻度后固定,并分析脑的bbb通透性。
早在mcao后1小时,在dio小鼠中观察到bbb完整性的显著丧失。这通过用vegf-b阻断抗体2h10处理显著降低。这表明阻断vegf-b在缺血的第一个小时改善dio小鼠的脑血管功能。
图3e显示用vegf-b阻断抗体2h10的预处理减少dio小鼠在缺血性中风后1小时血脑屏障渗漏。
预防性抗vegf-b处理减少dio小鼠脑缺血后闭合蛋白磷酸化的诱导
dio小鼠用如上所述的2h10或同种型对照抗体预处理一周,随后是mcao。在缺血后3小时,灌注小鼠,收集脑并立即冷冻。获得冷冻切片,并用磷酸丝氨酸特异性抗闭合蛋白抗体(丝氨酸残基490)进行免疫荧光染色,并对荧光强度进行定量。
闭合蛋白是紧密连接蛋白,其在mcao和缺血再灌注损伤后迅速磷酸化(muthusamy等journalofcerebralbloodflowandmetabolism2014)。以前已经显示,丝氨酸残基490上的闭合蛋白的磷酸化涉及bbb破坏和通透性(murakami等diabetes2012;murakami等thejournalofbiologicalchemistry2009)。
与mcao后3小时的对侧半球(对侧)相比,同型对照(igg)处理的dio小鼠在半暗带(同侧)中显示出增加的闭合蛋白丝氨酸磷酸化(ps490),表明缺血半球中内皮紧密连接解构和血管通透性的增加。用抗vegf-b抗体2h10的处理减少同侧半球半暗带区域中的闭合蛋白磷酸化的诱导,支持用抗vegf-b抗体2h10的治疗赋予增强的bbb完整性的观点。
图3f显示抗vegf-b治疗在dio小鼠中减少缺血性中风后的闭合蛋白磷酸化。
预防性抗vegf-b处理阻止脑缺血后dio小鼠脑血管中的脂质积聚
由于vegf-b信号下调葡萄糖摄取并增加脂质摄取(如上所示),检查在瘦和肥胖小鼠中和用2h10抗体治疗的肥胖小鼠中的mcao之后的脑血管脂质积聚。
dio小鼠用如上所述的2h10或同种型对照抗体预先处理,随后是mcao。没有预处理和瘦的年龄匹配对照的dio小鼠也经受mcao。在缺血后3小时,灌注小鼠,收集脑并立即冷冻。获得冷冻切片,用针对脂滴包被蛋白,亲脂素/围脂滴蛋白2(perilipin2)的抗体染色并定量。
在mcao的3小时内观察到缺血半球中脂质向脑血管的显著摄取。相对于非缺血性对侧半球,观察到脂肪细胞染色很少,在瘦小鼠缺血半球的血管周围也存在显著脂质摄取。然而,这显著小于在dio小鼠中观察到的,而在这些肥胖小鼠中,血管周围脂质积聚的增加在很大程度上被2h10治疗所阻断。
这些数据表明,即使在瘦小鼠中,mcao也迅速诱导脂质摄取,可能有助于满足缺血组织中的代谢需求,并且dio极大地加剧了这种响应。脑血管床中的过度和异位脂质积累可能是有害的,特别是在mcao后的氧和葡萄糖剥夺的背景下。
图3g显示缺血性中风后脑血管中的脂质积累通过用抗vegf-b抗体2h10预防性处理而被阻断。
实施例4:组合tpa溶血栓的治疗性抗vegf-b治疗降低梗塞大小,出血并增加dio小鼠的存活率
将具有dio的小鼠进行mcao,并用2h10或同种型对照抗体(16mg/kg)在中风后1小时处理,如上所述。另外4小时后,小鼠通过静脉内输注tpa(阿替普酶,10mg/kg)接受溶栓治疗以溶解诱导的血块。然后如上所述分析存活动物的分离的大脑。
通常,溶血栓tpa治疗的功效随时间减少,而出血转化的风险升高(ahmed等lancetneurology2010)。目前结果表明,mcao后1小时用2h10进行延迟治疗,随后4小时后进行tpa溶血栓治疗,导致梗塞大小减小,出血减少,并预防致死性出血,因为与进行延迟tpa溶血栓治疗的同种型治疗对照相比,2h10治疗动物的存活率显著升高。
结果表明vegf-b拮抗剂在中风中作为tpa治疗的潜在辅助治疗的治疗潜力,其可以通过减少出血性并发症来改善tpa溶血栓的安全性和/或可延长tpa的治疗窗口。在临床环境中,治疗窗口的延长是用溶血栓疗法治疗更多患者的最重要一步。
图4a-c显示vegf-b阻断抗体2h10对vegf-b的抑制改善晚期溶血栓后的结果。
序列表
<110>csl有限公司(csllimited)
b-创新瑞典股份公司(b-creativeswedenab)
<120>治疗或预防中风的方法
<130>518558
<160>47
<170>patentinversion3.5
<210>1
<211>207
<212>prt
<213>智人(homosapiens)
<220>
<221>信号
<222>(1)..(21)
<223>信号序列
<400>1
metserproleuleuargargleuleuleualaalaleuleuglnleu
151015
alaproalaglnalaprovalserglnproaspalaproglyhisgln
202530
arglysvalvalsertrpileaspvaltyrthrargalathrcysgln
354045
proarggluvalvalvalproleuthrvalgluleumetglythrval
505560
alalysglnleuvalprosercysvalthrvalglnargcysglygly
65707580
cyscysproaspaspglyleuglucysvalprothrglyglnhisgln
859095
valargmetglnileleumetileargtyrproserserglnleugly
100105110
glumetserleuglugluhisserglncysglucysargprolyslys
115120125
lysaspseralavallysproaspargalaalathrprohishisarg
130135140
proglnproargservalproglytrpaspseralaproglyalapro
145150155160
serproalaaspilethrhisprothrproalaproglyproserala
165170175
hisalaalaproserthrthrseralaleuthrproglyproalaala
180185190
alaalaalaaspalaalaalaserservalalalysglyglyala
195200205
<210>2
<211>188
<212>prt
<213>智人(homosapiens)
<220>
<221>信号
<222>(1)..(21)
<223>信号序列
<400>2
metserproleuleuargargleuleuleualaalaleuleuglnleu
151015
alaproalaglnalaprovalserglnproaspalaproglyhisgln
202530
arglysvalvalsertrpileaspvaltyrthrargalathrcysgln
354045
proarggluvalvalvalproleuthrvalgluleumetglythrval
505560
alalysglnleuvalprosercysvalthrvalglnargcysglygly
65707580
cyscysproaspaspglyleuglucysvalprothrglyglnhisgln
859095
valargmetglnileleumetileargtyrproserserglnleugly
100105110
glumetserleuglugluhisserglncysglucysargprolyslys
115120125
lysaspseralavallysproaspserproargproleucysproarg
130135140
cysthrglnhishisglnargproaspproargthrcysargargarg
145150155160
cysargargargserpheleuargcysglnglyargglyleugluleu
165170175
asnproaspthrcysargcysarglysleuargarg
180185
<210>3
<211>119
<212>prt
<213>人工
<220>
<223>抗体2h10的vh的氨基酸序列
<400>3
valglnleuglnglnproglythrgluleuvallysproglyalaser
151015
vallysleusercyslysalaserglytyrthrphethrglyphetrp
202530
ilehistrpvallysglnargproglyglnglyleuglutrpilegly
354045
hisileasnproglyasnglyglythrasntyrasnglulysphelys
505560
argmetalathrleuthrvalasplysserserserthralatyrmet
65707580
glnleuserserleuthrsergluaspseralavaltyrtyrcysala
859095
argsertyrserasntyrvalargalametasptyrtrpglyglngly
100105110
thrservalthrvalserser
115
<210>4
<211>106
<212>prt
<213>人工
<220>
<223>抗体2h10的vl的氨基酸序列
<400>4
ileglnmetthrglnthrthrserserleuseralaserleuglyasp
151015
argvalthrilesercysargalaserglnaspileserasnpheleu
202530
asntrptyrglnglnlysproaspglythrvallysleuleuiletyr
354045
tyrthrserthrleuhisserglyvalproserargpheserglyser
505560
glyserglythrasptyrserleuthrileserasnleugluglnglu
65707580
aspilealathrtyrphecysglnglnglylysthrleuproprothr
859095
pheglyglyglythrlysleugluilelys
100105
<210>5
<211>119
<212>prt
<213>人工
<220>
<223>抗体2h10的人源化形式的vh的氨基酸序列
<400>5
valglnleuvalglnserglyalagluvallyslysproglyalaser
151015
vallysvalsercyslysalaserglytyrthrphethrglyphetrp
202530
ilehistrpvalargglnalaproglyglnglyleuglutrpmetgly
354045
hisileasnproglyasnglyglythrasntyrasnglulysphelys
505560
argargvalthrmetthrargasplysserileserthralatyrmet
65707580
gluleuserargleuargseraspaspthralavaltyrtyrcysala
859095
argsertyrserasntyrvalargalametasptyrtrpglyglngly
100105110
thrleuvalthrvalserser
115
<210>6
<211>107
<212>prt
<213>人工
<220>
<223>抗体2h10的人源化形式的vl的氨基酸序列
<400>6
aspileglnmetthrglnserproserserleuseralaservalgly
151015
aspargvalthrilethrcysargalaserglnaspileserasnphe
202530
leuasntrptyrglnglnlysproglylysalaprolysleuleuile
354045
tyrtyrthrserthrleuhisserglyvalproserargphesergly
505560
serglyserglythraspphethrleuthrileserserleuglnpro
65707580
gluaspphealathrtyrtyrcysglnglnglylysthrleupropro
859095
thrpheglyglyglythrlysvalgluilelys
100105
<210>7
<211>116
<212>prt
<213>人工
<220>
<223>抗体4e12的vh的氨基酸序列
<400>7
valglnproglnglnproglyalagluleuvallysproglyalaser
151015
vallysmetsercyslysalaserglyaspthrphethrasnsertrp
202530
ileglytrpvalthrglnargproglyglnglyleuglutrpilegly
354045
aspilepheproglyserglyhisthrasntyrasnglulysphelys
505560
asnargalathrleuthrvalaspthrserserserthralatyrmet
65707580
leuleuserserleuthrseraspaspseralavaltyrtyrcysval
859095
ilegluasntyralatrpphealatyrtrpglyglnglythrleuval
100105110
thrvalserala
115
<210>8
<211>107
<212>prt
<213>人工
<220>
<223>抗体4e12的vl的氨基酸序列
<400>8
aspilevalmetthrglnserglnlysphemetserserservalgly
151015
aspargvalservalthrcyslysalaserglnasnvalasnthrasn
202530
valalatrptyrglnglnlysglnglyglnserproargproleuile
354045
tyrseralaserserargcysserglyvalproaspargphethrgly
505560
serglypheglythraspphethrleuthrileserasnvalglnser
65707580
gluaspleualaglutyrphecysglnglntyrhisserpheproleu
859095
thrpheglyalaglyalalysleuaspleulys
100105
<210>9
<211>118
<212>prt
<213>人工
<220>
<223>抗体2f5的vh的氨基酸序列
<400>9
valglnleuglnglnserglyprogluleuvallysproglythrser
151015
valargilesercyslysalaserglytyrthrphethrthrphetyr
202530
ilehistrpvallysglnargproglyglnglyleuglutrpilegly
354045
trpphetyrproglyasnvalasnthrasntyrasnglulysleulys
505560
glylysalathrleuthralaasplysserserseralaalatyrleu
65707580
glnleuasnserleuthrsergluaspseralavaltyrphecysthr
859095
argserprotyrtyrglytyrvalpheasptyrtrpglyglnglythr
100105110
thrleuthrvalserser
115
<210>10
<211>107
<212>prt
<213>人工
<220>
<223>抗体2f5的vl的氨基酸序列
<400>10
aspilevalmetthrglnserhislysphemetserthrservalgly
151015
aspargvalserilethrcyslysalaserglnaspvalglythrala
202530
valalatrptyrglnglnlysproglyglnserprolysleuleuile
354045
tyrtrpalaserthrarghisthrglyvalproaspargphethrgly
505560
serglyserglythraspphethrleuthrileserasnvalglnser
65707580
gluaspleualaasptyrphecysglnglntyrserserserleuthr
859095
pheglyalaglyalathrlysleugluleulys
100105
<210>11
<211>527
<212>prt
<213>人工序列
<220>
<223>重组人组织纤溶酶原激活剂
<400>11
sertyrglnvalilecysargaspglulysthrglnmetiletyrgln
151015
glnhisglnsertrpleuargprovalleuargserasnargvalglu
202530
tyrcystrpcysasnserglyargalaglncyshisservalproval
354045
lyssercyssergluproargcyspheasnglyglythrcysglngln
505560
alaleutyrpheseraspphevalcysglncysprogluglypheala
65707580
glylyscyscysgluileaspthrargalathrcystyrgluaspgln
859095
glyilesertyrargglythrtrpserthralagluserglyalaglu
100105110
cysthrasntrpasnserseralaleualaglnlysprotyrsergly
115120125
argargproaspalaileargleuglyleuglyasnhisasntyrcys
130135140
argasnproaspargaspserlysprotrpcystyrvalphelysala
145150155160
glylystyrsersergluphecysserthrproalacysserglugly
165170175
asnseraspcystyrpheglyasnglyseralatyrargglythrhis
180185190
serleuthrgluserglyalasercysleuprotrpasnsermetile
195200205
leuileglylysvaltyrthralaglnasnproseralaglnalaleu
210215220
glyleuglylyshisasntyrcysargasnproaspglyaspalalys
225230235240
protrpcyshisvalleulysasnargargleuthrtrpglutyrcys
245250255
aspvalprosercysserthrcysglyleuargglntyrserglnpro
260265270
glnpheargilelysglyglyleuphealaaspilealaserhispro
275280285
trpglnalaalailephealalyshisargargserproglygluarg
290295300
pheleucysglyglyileleuilesersercystrpileleuserala
305310315320
alahiscyspheglngluargpheproprohishisleuthrvalile
325330335
leuglyargthrtyrargvalvalproglygluglugluglnlysphe
340345350
gluvalglulystyrilevalhislysglupheaspaspaspthrtyr
355360365
aspasnaspilealaleuleuglnleulysseraspserserargcys
370375380
alaglngluserservalvalargthrvalcysleuproproalaasp
385390395400
leuglnleuproasptrpthrglucysgluleuserglytyrglylys
405410415
hisglualaleuserprophetyrsergluargleulysglualahis
420425430
valargleutyrproserserargcysthrserglnhisleuleuasn
435440445
argthrvalthraspasnmetleucysalaglyaspthrargsergly
450455460
glyproglnalaasnleuhisaspalacysglnglyaspserglygly
465470475480
proleuvalcysleuasnaspglyargmetthrleuvalglyileile
485490495
sertrpglyleuglycysglyglnlysaspvalproglyvaltyrthr
500505510
lysvalthrasntyrleuasptrpileargaspasnmetargpro
515520525
<210>12
<211>33
<212>dna
<213>人工序列
<220>
<223>2h10vlcdr1的核苷酸序列
<400>12
agggcaagtcaggacattagcaattttttaaac33
<210>13
<211>21
<212>dna
<213>人工序列
<220>
<223>2h10vlcdr2的核苷酸序列
<400>13
tacacatcaacattacactca21
<210>14
<211>27
<212>dna
<213>人工序列
<220>
<223>2h10vlcdr3的核苷酸序列
<400>14
caacagggtaaaacgcttcctcccacg27
<210>15
<211>30
<212>dna
<213>人工序列
<220>
<223>2h10vhcdr1的核苷酸序列
<400>15
ggctacactttcactggcttctggatacac30
<210>16
<211>51
<212>dna
<213>人工序列
<220>
<223>2h10vhcdr2的核苷酸序列
<400>16
catattaatcctggcaatggtggcactaactacaatgagaagttcaagaga51
<210>17
<211>33
<212>dna
<213>人工序列
<220>
<223>2h10vhcdr3的核苷酸序列
<400>17
tcctatagtaactacgtgcgggctatggactac33
<210>18
<211>11
<212>prt
<213>人工序列
<220>
<223>2h10vlcdr1的氨基酸序列
<400>18
argalaserglnaspileserasnpheleuasn
1510
<210>19
<211>7
<212>prt
<213>人工序列
<220>
<223>2h10vlcdr2的氨基酸序列
<400>19
tyrthrserthrleuhisser
15
<210>20
<211>9
<212>prt
<213>人工序列
<220>
<223>2h10vlcdr3的氨基酸序列
<400>20
glnglnglylysthrleuproprothr
15
<210>21
<211>10
<212>prt
<213>人工序列
<220>
<223>2h10vhcdr1的氨基酸序列
<400>21
glytyrthrphethrglyphetrpilehis
1510
<210>22
<211>17
<212>prt
<213>人工序列
<220>
<223>2h10vhcdr2的氨基酸序列
<400>22
hisileasnproglyasnglyglythrasntyrasnglulysphelys
151015
arg
<210>23
<211>11
<212>prt
<213>人工序列
<220>
<223>2h10vhcdr3的氨基酸序列
<400>23
sertyrserasntyrvalargalametasptyr
1510
<210>24
<211>33
<212>dna
<213>人工序列
<220>
<223>2f5vlcdr1的核苷酸序列
<400>24
aaggccagtcaggatgtgggtactgctgtagcc33
<210>25
<211>21
<212>dna
<213>人工序列
<220>
<223>2f5vlcdr2的核苷酸序列
<400>25
tgggcatccacccggcacact21
<210>26
<211>24
<212>dna
<213>人工序列
<220>
<223>2f5vlcdr3的核苷酸序列
<400>26
caacaatatagcagctctctcacg24
<210>27
<211>30
<212>dna
<213>人工序列
<220>
<223>2f5vhcdr1的核苷酸序列
<400>27
ggctacaccttcacaaccttctatatacac30
<210>28
<211>51
<212>dna
<213>人工序列
<220>
<223>2f5vhcdr2的核苷酸序列
<400>28
tggttttatcctggaaatgttaataccaactacaatgagaagctcaagggc51
<210>29
<211>30
<212>dna
<213>人工序列
<220>
<223>2f5vhcdr3的核苷酸序列
<400>29
tccccttactacggctacgtttttgactac30
<210>30
<211>11
<212>prt
<213>人工序列
<220>
<223>2f5vlcdr1的氨基酸序列
<400>30
lysalaserglnaspvalglythralavalala
1510
<210>31
<211>7
<212>prt
<213>人工序列
<220>
<223>2f5vlcdr2的氨基酸序列
<400>31
trpalaserthrarghisthr
15
<210>32
<211>8
<212>prt
<213>人工序列
<220>
<223>2f5vlcdr3的氨基酸序列
<400>32
glnglntyrserserserleuthr
15
<210>33
<211>10
<212>prt
<213>人工序列
<220>
<223>2f5vhcdr1的氨基酸序列
<400>33
glytyrthrphethrthrphetyrilehis
1510
<210>34
<211>17
<212>prt
<213>人工序列
<220>
<223>2f5vhcdr2的氨基酸序列
<400>34
trpphetyrproglyasnvalasnthrasntyrasnglulysleulys
151015
gly
<210>35
<211>10
<212>prt
<213>人工序列
<220>
<223>2f5vhcdr3的氨基酸序列
<400>35
serprotyrtyrglytyrvalpheasptyr
1510
<210>36
<211>33
<212>dna
<213>人工序列
<220>
<223>4e12vlcdr1的核苷酸序列
<400>36
aaggccagtcagaatgtgaacactaatgtagcc33
<210>37
<211>21
<212>dna
<213>人工序列
<220>
<223>4e12vlcdr2的核苷酸序列
<400>37
tcggcatcctcccggtgcagt21
<210>38
<211>27
<212>dna
<213>人工序列
<220>
<223>4e12vlcdr3的核苷酸序列
<400>38
cagcaatatcacagctttccgctcacg27
<210>39
<211>30
<212>dna
<213>人工序列
<220>
<223>4e12vhcdr1的核苷酸序列
<400>39
ggcgacaccttcaccaactcctggataggc30
<210>40
<211>51
<212>dna
<213>人工序列
<220>
<223>4e12vhcdr2的核苷酸序列
<400>40
gatatttttcctgggagtggtcatactaactacaatgagaagttcaagaac51
<210>41
<211>24
<212>dna
<213>人工序列
<220>
<223>4e12vhcdr3的核苷酸序列
<400>41
gagaattatgcctggtttgcttat24
<210>42
<211>11
<212>prt
<213>人工序列
<220>
<223>4e12vlcdr1的氨基酸序列
<400>42
lysalaserglnasnvalasnthrasnvalala
1510
<210>43
<211>7
<212>prt
<213>人工序列
<220>
<223>4e12vlcdr2的氨基酸序列
<400>43
seralaserserargcysser
15
<210>44
<211>9
<212>prt
<213>人工序列
<220>
<223>4e12vlcdr3的氨基酸序列
<400>44
glnglntyrhisserpheproleuthr
15
<210>45
<211>10
<212>prt
<213>人工序列
<220>
<223>4e12vhcdr1的氨基酸序列
<400>45
glyaspthrphethrasnsertrpilegly
1510
<210>46
<211>17
<212>prt
<213>人工序列
<220>
<223>4e12vhcdr2的氨基酸序列
<400>46
aspilepheproglyserglyhisthrasntyrasnglulysphelys
151015
asn
<210>47
<211>8
<212>prt
<213>人工序列
<220>
<223>4e12vhcdr3的氨基酸序列
<400>47
gluasntyralatrpphealatyr
15
- 还没有人留言评论。精彩留言会获得点赞!