基于磁共振成像的施源位置定位方法和施源器外管与流程
本申请涉及施源器定位技术领域,尤其涉及一种基于磁共振成像的施源位置定位方法和施源器外管。
背景技术:
临床上在后装治疗过程中,对施源器的定位通常是通过正侧位X光片或者三维计算机断层(Computed Tomography,CT)扫描得到的。随着磁共振成像(Magnetic Resonance Imaging,MRI)的发展,其无辐射、高分辨率、高软组织对比度的优势,使之应用越来越广泛。
在20世纪70年代以后,后装放射治疗得到了发展,特别是在妇科腔内放疗中得到了肯定。20世纪80年代后期,反应堆生产出高强度微型铱-192源,加之经由最初的机械和电机阶段逐渐向电脑控制发展,使后装治疗进入了新阶段。后装放射治疗是指把不带放射源的治疗容器(施源器)置于治疗部位,由电脑遥控步进电机(后装机)将放射源送入施源器进行放射治疗,如此可避免防止治疗过程中医务人员因放射受伤。由于放置位置准确、距病体组织近等优点,在治疗妇科、鼻咽、食道、支气管、直肠、膀胱、乳腺及胰腺等肿瘤中,取得了明显的临床治疗效果。后装机的作用是通过施源管将放射源准确、安全、定时地放置到人体病变部位。
后装治疗作为外照射的辅助治疗手段,根据平方反比定律,近放射源处的剂量随距离变化要比远源处大得多。利用这一特征,肿瘤组织可以得到有效的杀伤剂量,而临近的正常组织可得到保护。由此可见,作为后装治疗的质量保证之一就是放射源的到位精度,直接影响到治疗效果。
目前后装治疗的工作流程是,根据医生的诊断结果,将消毒后的施源管插入病人治疗部位中,并固定好;然后用模拟机拍摄正侧位X光片或者三维CT图像,定位施源管的位置,制定各点的最佳治疗时间,设计治疗计划;将施源管与后装治疗机接通,然后通过操作后装机控制系统执行放疗计划;当完成一定量的辐照之后,在后装机电脑控制下,放射源自动退回到储源器,完成一次近距离后装治疗。
随着磁共振成像技术的发展,磁共振成像无辐射、高分辨率、高软组织对比度等优点,使得磁共振成像越来越受到人们的重视。临床上用模拟机拍摄正侧位X光片,根据坐标重建结果制定治疗计划,虽然可以实现后装内照射治疗,但是治疗计划简单、剂量精确度很低,无法正确评估病变范围和正常组织的情况进而给予个性化精确的放射治疗剂量方案。
中国专利CN101152090A公布了一种“可用于CT扫描的宫颈癌单管式后装施源器”,能够通过CT机进行扫描成像的宫颈癌后装施源器,它包括一中空的施源管道,管道的一端与后装机施源管连接,另一端为病灶治疗端,该治疗端是由具有屏蔽功能材料制成的椭圆形内管构成,在内管中心上设置有一圆孔,该圆孔与施源管道相通,在内管外还活动式的套接有一采用CT兼容的高分子材料制成的圆筒形外管,该发明可以通过CT扫描获得病变部位的三维图像,从而准确的估计病变范围和周围正常组织情况,为个体化精确地进行放射治疗提供图像数据依据。
目前,通过CT三维成像可以实现施源器的定位、制定精确地放疗计划,但是CT图像软组织对比度差,而通常内照射治疗都是针对软组织腔道,CT图像并不能较好呈现。根据磁共振成像的原理,三维磁共振图像可以清晰的呈现病变部位和周围器官的组织结构,但是目前适用于磁共振成像的高分子材料制成的施源器管道在磁共振成像中往往因为没有信号,在三维图像上体现为黑色,因而导致磁共振三维图像不能发挥原有的优势准确地对施源管位置进行定位,也影响了周围组织病变情况的可观察性。
技术实现要素:
为解决现有技术中的上述问题,本申请的一个目的在于提出一种基于磁共振成像的施源位置定位方法和施源器,可以在磁共振图像中精确定位施源器外管的位置,并清晰显示施源器外管周围组织器官的形态和病变情况,有效提高治疗精度。
为达到上述目的,本申请实施例提出的基于磁共振成像的施源位置定位方法包括:将管壁中具有容室的施源器外管插入预测施源部位,并进行三维磁共振成像;根据所述容室中的显像剂确定具体的施源位置。
为达到上述目的,本申请实施例提出的基于磁共振成像的施源器的施源器外管,所述施源器外管的管壁中具有容室,所述容室中填充有用于磁共振成像的显像剂。
由以上本申请实施例提供的技术方案可见,通过将管壁中具有填充有显像剂的容室的施源器外管插入预测施源部位进行三维磁共振扫描,能够在三维磁共振成像中高亮显示施源器外管,可准确定位施源器外管的位置,清晰显示病变组织以及周边组织器官的形态构造和病变情况,提供更好的软组织对比度,更好的呈现病变部位的组织特性,从而可以精确定位施源器外管所处的位置,并且为精确设计放疗计划、准确控制放射源的驻留部位和时间提供依据,提高治疗精度和安全性。
本申请附加的方面和优点将在下面的描述中部分给出,部分将从下面的描述中变得明显,或通过本申请的实践了解到。
附图说明
为了更清楚地说明本申请实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本申请的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
图1是本申请一实施例提出的基于磁共振成像的施源位置定位方法的流程示意图;
图2是本申请一实施例的基于磁共振成像的施源器的施源器外管的横截面结构示意图;
图3是本申请一实施例的基于磁共振成像的施源器的结构示意图;
图4是本申请一实施例的基于磁共振成像的施源器的施源器内管的示意图;
图5是本申请另一实施例提出的基于磁共振成像的施源位置定位方法的流程示意图;
图6是本申请另一实施例提出的基于磁共振成像的施源位置的深度位置计算的模型示意图;
图7是本申请另一个实施例的施源器内管的横切面示意图。
具体实施方式
本申请实施例提供一种基于磁共振成像的施源位置定位方法和施源器。
为了使本技术领域的人员更好地理解本申请中的技术方案,下面将结合本申请实施例中的附图,对本申请实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本申请一部分实施例,而不是全部的实施例。基于本申请中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都应当属于本申请保护的范围。
图1是本申请一实施例提出的基于磁共振成像的施源位置定位方法的流程示意图,如图1所示,该方法包括:
步骤101,将管壁中具有容室的施源器外管插入预测施源部位,并进行三维磁共振成像。
其中,容室例如可以是均匀设置在施源器外管的管壁中的多个孔状空间,或者,施源器外管的内壁与外壁之间的夹层,以及其他可能的形式。容室中填充的显像剂在磁共振成像中呈高信噪比,能够在三维磁共振成像中呈高亮显像。
其中,显像剂可以是油、水或者其他适用于磁共振成像的对比增强剂(或显像剂、造影剂等),预先封闭填充在所述定位管中,以确保在三维磁共振图像中高亮显示施源器外管的位置。对比增强剂例如是DTPA(钆-二乙烯二胺五醋酸)的络合物等。
步骤102,根据所述容室中的显像剂确定具体的施源位置。
本发明所述的施源器外管由MRI兼容的高分子材料制成。
需要理解的是,与现有的CT定位的内照射治疗相比,三维磁共振定位的内照射治疗方案辐射更低,并可以提供更好的软组织对比度。由于内照射治疗主要针对人体中的腔体病变进行治疗,因此较好的呈现病变组织和周边器官,是制定精确地放疗计划的基本条件。
在实际应用中,先将施源器外管提前插入病人体内,容室中预先填充用于磁共振成像的显像剂,确保在三维磁共振图像中准确显示施源器外管的位置。三维磁共振扫描完成,根据三维磁共振图像中病变组织和正常组织或者器官的情况以及施源器外管的位置制定放射治疗的治疗计划。然后根据内照射治疗的需要,插入合适的施源器内管,内管的插入角度根据定位图像进行调整,内管中插入放射源通道。为了不同治疗的需要,可以设计不同结构的施源器内管,以适应对放射源通道的数量和位置等的不同需求。
本实施例通过将管壁中具有填充有显像剂的容室的施源器外管插入预测施源部位进行三维磁共振扫描,能够在三维磁共振成像中高亮显示施源器外管,可准确定位施源器外管的位置,清晰显示病变组织以及周边组织器官的形态构造和病变情况,提供更好的软组织对比度,更好的呈现病变部位的组织特性,从而可以精确定位施源器外管所处的位置,并且为精确设计放疗计划、准确控制放射源的驻留部位和时间提供依据,提高治疗精度和安全性。
基于同一发明构思,本申请实施例还提供了一种基于磁共振成像的施源器的施源器外管,可以用于实现上述实施例所描述的方法,如下面的实施例所述。由于基于磁共振成像的施源器的施源器外管解决问题的原理与基于磁共振成像的施源位置定位方法相似,因此基于磁共振成像的施源器的实施可以参见基于磁共振成像的施源位置定位方法的实施,重复之处不再赘述。尽管以下实施例所描述的装置较佳地以硬件来实现,但是软件,或者软件和硬件的组合的实现也是可能并被构想的。
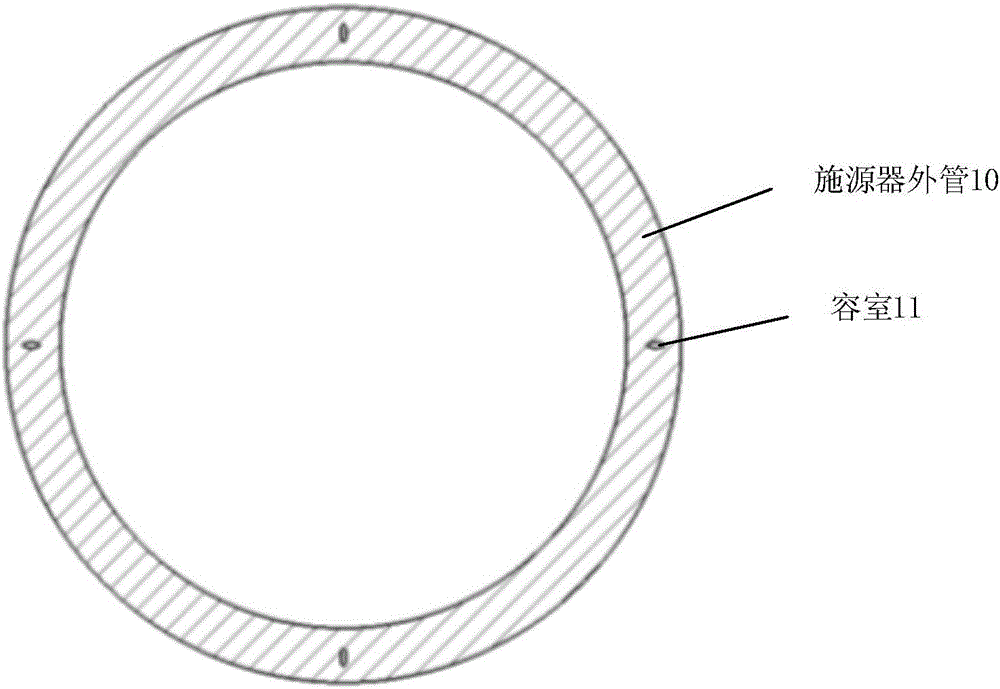
图2是本申请一实施例的基于磁共振成像的施源器的施源器外管的横截面结构示意图。
如图2所示,该基于磁共振成像的施源器的施源器外管10,所述施源器外管10的管壁中具有容室11,所述容室11中填充有用于磁共振成像的显像剂。其中,容室例如可以是均匀设置在施源器外管的管壁中的多个孔状空间,或者,施源器外管的内壁与外壁之间的夹层等。容室中填充的显像剂在磁共振成像中呈高信噪比,能够在三维磁共振成像中呈高亮显像。
其中,显像剂可以是油、水或者其他适用于磁共振成像的对比增强剂(或显像剂、造影剂等),预先封闭填充在所述定位管中,以确保在三维磁共振图像中高亮显示施源器外管的位置。对比增强剂例如是DTPA(钆-二乙烯二胺五醋酸)的络合物等。
在本申请的一个实施例中,所述容室的横截面与所述横截面到所述施源器外管的管口的距离一一对应。具体地,每个横截面的面积或宽度可以随所述横截面在施源器外管中的深度而变化。当容室是位于所述施源器外管的内壁与外壁之间的夹层时,随着在施源器外管中的深度增加,夹层的厚度可以越来越小或越来越大,从而能够根据磁共振图像中夹层的横截面厚度确定该横截面距离施源器外管管口的相对深度。当容室是多个径向的孔状空间时,可以使每个或其中一个孔状空间为锥形,从而该孔状空间的横截面随该横截面到管口的距离而变化。实际设计中深度定位装置可以有多种设计,例如反向圆锥形等,原理相同,在此不再赘述。
在本申请的一个实施例中,当所述容室是图2所示的均匀设置在施源器外管的管壁中的多个孔状空间时,多个孔状空间在横截面方向上呈均匀角度分布,从而在填充显像剂后进行三维磁共振扫描得到的图像中,可以根据每个孔状空间的位置确定具体的施源部位与所述施源器外管的相对角度。
如图3所示是采用本实施例的施源器外管的施源器的结构示意图,在进行放射源照射时,本实施例的施源器外管可以搭配后装机20(图中未示出)、放射源通道30、施源器内管40使用。
本发明所述的施源器外管10由MRI兼容的高分子材料制成,表面设有预设精度的刻度,所述刻度可以包括纵深刻度和角度刻度等一个或多个维度的刻度。操作人员可以根据施源器外管上的刻度准确判断施源器内管放入施源位置的深度和/或角度,在三维磁共振图像中,也可以辅助定位施源器外管所处的位置和偏差。
根据本申请的一个实施例,施源器可以包括至少一组所述施源器外管。具体地,施源器外管的数量根据治疗的需求不限一个,每个施源器外管都配有与之精确匹配(例如包括长度、直径的匹配和接口连接关系的匹配等)的施源器内管,施源器内管的结构如图4所示。当进行放射治疗时,施源器内管通过预设的结构与施源器外管卡接固定,通过内管上的孔状通道插入所述放射源通道。具体的卡接固定方式根据实际需求进行设计,本申请对此不做限定。放射源通道的一端通过预设接口与后装机相连,另一端放入施源器内管,为病灶治疗端。在治疗时,在后装机的计算机控制下根据放疗计划导入放射源到放射源通道中的预设位置。
本实施例通过将管壁中具有填充有显像剂的容室的施源器外管插入预测施源部位进行三维磁共振扫描,能够在三维磁共振成像中高亮显示施源器外管,可准确定位施源器外管的位置,清晰显示病变组织以及周边组织器官的形态构造和病变情况,提供更好的软组织对比度,更好的呈现病变部位的组织特性,从而可以精确定位施源器外管所处的位置,并且为精确设计放疗计划、准确控制放射源的驻留部位和时间提供依据,提高治疗精度和安全性。
图5是本申请另一实施例提出的基于磁共振成像的施源位置定位方法的流程示意图,如图5所示,该方法包括:
步骤201,将管壁中具有容室的施源器外管插入预测施源部位,并进行三维磁共振成像。
具体地,治疗前先将消毒后的施源器外管插入病人体内,进行磁共振三维成像。操作者可根据经验或已知的信息预测施源部位的位置,将插有所述定位管的施源器外管插入到估计的施源部位。
其中,显像剂可以是油、水或者其他适用于磁共振成像的对比增强剂(或显像剂、造影剂等),预先封闭填充在所述定位管中,以确保在三维磁共振图像中高亮显示施源管的位置。对比增强剂例如是DTPA(钆-二乙烯二胺五醋酸)的络合物等。
步骤202,根据所述容室中的显像剂确定具体的施源位置。
通过三维磁共振扫描成像来确定施源器外管在体内的位置,以及周围组织器官的情况,准确评估病变范围以及与周围重要器官的关系,在此基础上制定个体化的放射治疗计划,进而确定当前施源器外管的位置与实际的施源位置的偏差,并进行施源器外管位置调整。
所述容室的横截面的面积或宽度等特征可随所述横截面到所述施源器外管的管口的距离而变化,且所述横截面与所述距离一一对应,可根据所述容室的横截面确定所述施源位置到所述施源器外管管口的相对深度。以容室包括一个或多个圆锥形的孔状空间为例,本申请一个实施例的深度位置计算方法如图6所示,在病变部位的横断面磁共振图像中,可以测量得到孔状空间的宽度d,图中D和H分别为圆锥形底面的直径和圆锥高度,D和H对于特定的施源器外管是已知的,因此可以求得病变部位距离圆锥顶端的距离为h=H×d/D,实际设计中可用于深度定位的容室还可以有其他形状的设计,原理相同,不再赘述。
当所述容室为均匀设置在所述施源器外管的管壁中的多个孔状空间(纵向条状等)时,还可以根据所述多个孔状空间中的显像剂,确定所述施源位置与所述施源器外管的相对角度。容室之外的管壁在磁共振图像中显示为黑色,由于孔状空间中填充了显像剂,因此在图像中很容易准确的找到能够定位角度的孔状空间,实际操作中为了便于直接观察角度,可以设计更多的孔状空间结构使角度刻度更细。
步骤203,根据所述施源位置调整所述施源器外管的位置。
施源器外管的位置调整好后,将施源管固定在确定好的施源位置。
步骤204,确定放射剂量分布及其所需的放射源通道的数量和分布结构。
根据施源位置的具体情况,可以精确设计放射治疗计划,例如放射源的照射位置、照射角度、照射剂量等,根据实际的放射源放置需求确定放射源通道的数量和分布结构。
步骤205,选取与所述数量和分布结构的放射源通道对应的施源器内管。
为了配合不同的治疗需求,施源器内管的结构多种多样,如:施源器内管上放射源通道的数量不同,通道的分布位置不同等。图7所示为一个实施例的包括多个放射源通道的施源器内管的横截面。
步骤206,根据所述施源位置将施源器内管固定于所述施源器外管中。
步骤207,将连接后装机的放射源通道插入对应的施源器内管中,对所述施源位置进行放射源照射。
本申请的实施例通过将管壁中具有填充有显像剂的容室的施源器外管插入预测施源部位进行三维磁共振扫描,能够在三维磁共振成像中高亮显示施源器外管,可准确定位施源器外管的位置,清晰显示病变组织以及周边组织器官的形态构造和病变情况,提供更好的软组织对比度,更好的呈现病变部位的组织特性,从而可以精确定位施源器外管所处的位置,并且为精确设计放疗计划、准确控制放射源的驻留部位和时间提供依据,提高治疗精度和安全性。
需要说明的是,在本申请的描述中,术语“第一”、“第二”等仅用于描述目的,而不能理解为指示或暗示相对重要性。此外,在本申请的描述中,除非另有说明,“多个”的含义是两个或两个以上。
流程图中或在此以其他方式描述的任何过程或装置描述可以被理解为,表示包括一个或更多个用于实现特定逻辑功能或过程的步骤的可执行指令的代码的模块、片段或部分,并且本申请的优选实施方式的范围包括另外的实现,其中可以不按所示出或讨论的顺序,包括根据所涉及的功能按基本同时的方式或按相反的顺序,来执行功能,这应被本申请的实施例所属技术领域的技术人员所理解。
应当理解,本申请的各部分可以用硬件、软件、固件或它们的组合来实现。在上述实施方式中,多个步骤或装置可以用存储在存储器中且由合适的指令执行系统执行的软件或固件来实现。例如,如果用硬件来实现,和在另一实施方式中一样,可用本领域公知的下列技术中的任一项或他们的组合来实现:具有用于对数据信号实现逻辑功能的逻辑门电路的离散逻辑电路,具有合适的组合逻辑门电路的专用集成电路,可编程门阵列(PGA),现场可编程门阵列(FPGA)等。
本技术领域的普通技术人员可以理解实现上述实施例装置携带的全部或部分步骤是可以通过程序来指令相关的硬件完成,所述的程序可以存储于一种计算机可读存储介质中,该程序在执行时,包括装置实施例的步骤之一或其组合。
在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本申请的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不一定指的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任何的一个或多个实施例或示例中以合适的方式结合。
尽管上面已经示出和描述了本申请的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本申请的限制,本领域的普通技术人员在本申请的范围内可以对上述实施例进行变化、修改、替换和变型。
- 还没有人留言评论。精彩留言会获得点赞!