治疗2型糖尿病患者的制作方法
本发明的主题为药物组合,其在2型糖尿病患者中用于控制血糖、用于降低hba1c值、空腹血糖或/和餐后2小时血糖、用于预防体重增加或/和引起体重减轻、用于降低低血糖风险,该组合包含
(i)利西拉来或/和其药物上可接受的盐,
(ii)甘精胰岛素或/和其药物上可接受的盐,和
(iii)任选地二甲双胍或/和其药物上可接受的盐。
在健康人中,胰腺释放胰岛素与血糖浓度紧密相关。餐后出现的血糖水平增加被胰岛素分泌的相应增加快速地抵消。在空腹条件下,血浆胰岛素水平降至基础值,其足以保证血糖对胰岛素敏感的器官和组织的持续供应并且保持肝葡萄糖生成在夜间处于低水平。
与i型糖尿病不同的是,在2型糖尿病中通常不缺乏胰岛素,但在许多情况下,特别是在进行性病例中,认定胰岛素治疗为最适当的疗法,如果需要与口服施用的抗糖尿病药物组合的话。
历时若干年的血中葡萄糖水平升高而无初始症状表示显著的健康风险。可由美国的大规模dcct研究(thediabetescontrolandcomplicationstrialresearchgroup(1993)n.engl.j.med.329,977-986)所清楚地显示出血糖水平的长期增加是发展糖尿病并发症的主要原因。糖尿病并发症的实例为微血管和大血管损伤,其本身可能显示于视网膜病变、肾病或者神经病变且导致失明、肾衰竭和骨端丧失,且伴随有心血管疾病的风险。因此可确定改善的糖尿病疗法主要需要针对将血糖保持尽可能接近地保持在生理学范围内。
特定的风险存在于患有2型糖尿病的超重患者,例如具有≥30kg/m2的体重指数(bmi)的患者。在这些患者中,糖尿病风险与超重的风险重迭,这导致例如心血管疾病的增加(相对于具有正常体重的2型糖尿病患者而言)。
化合物despro36毒蜥外泌肽-4(1-39)-lys6-nh2(ave0010,利西拉来)为毒蜥外泌肽-4的衍生物。在wo01/04156中将ave0010披露为seqidno:93:
seqidno:1:利西拉来(44个氨基酸)
h-g-e-g-t-f-t-s-d-l-s-k-q-m-e-e-e-a-v-r-l-f-i-e-w-l-k-n-g-g-p-s-s-g-a-p-p-s-k-k-k-k-k-k-nh2
seqidno:2:毒蜥外泌肽-4(39个氨基酸)
h-g-e-g-t-f-t-s-d-l-s-k-q-m-e-e-e-a-v-r-l-f-i-e-w-l-k-n-g-g-p-s-s-g-a-p-p-p-s-nh2
毒蜥外泌肽(exendin)是可降低血糖浓度的一类肽。毒蜥外泌肽类似物利西拉来的特征在于天然毒蜥外泌肽-4序列的c-末端截短。利西拉来包含不存在于毒蜥外泌肽-4的六个c-末端赖氨酸残基。
利西拉来也称为des-38-脯氨酸-毒蜥外泌肽-4(吉拉毒蜥(helodermasuspectum))-(1-39)-肽基五-l-赖氨酰基-l-赖氨酰胺(cas编号320367-13-3)。在本发明中,“利西拉来”包括其药物上可接受的盐。本领域技术人员知晓利西拉来的适当的药物上可接受的盐。
甘精胰岛素为人胰岛素的类似物。甘精胰岛素为31b-32b-di-arg人胰岛素,其在a21位的天冬酰胺进一步被甘氨酸取代。甘精胰岛素也称为gly(a21)-arg(b31)-arg(b32)人胰岛素。甘精胰岛素的cas编号为160337-95-1。在本发明中,“甘精胰岛素”包括其药物上可接受的盐。本领域技术人员知晓甘精胰岛素的适当的药物上可接受的盐。
二甲双胍的国际非专有名为1,1-二甲基双胍(cas编号657-24-9)。二甲双胍为在治疗非胰岛素依赖性糖尿病(2型糖尿病)(其对饮食改变不应答)中使用的双胍类降血糖药。二甲双胍通过改善胰岛素敏感性并降低葡萄糖的肠吸收来改善血糖控制。二甲双胍通常口服施用。然而,在肥胖患者中由二甲双胍控制2型糖尿病可能是不适当的。因此,在这些患者中,可能需要对于控制2型糖尿病的额外的措施。本申请使用的“二甲双胍”包括其药物上可接受的盐。本领域技术人员知晓二甲双胍的适当的药物上可接受的盐。
在本发明的实施例中,利西拉来、甘精胰岛素和任选地二甲双胍的组合效果已经在肥胖的2型糖尿病患者中测试,该患者使用单独的基础胰岛素或基础胰岛素与一至三种选自由下列组成的群组:二甲双胍、磺酰脲类、二肽基-肽酶-4(dpp-4)抑制剂和格列奈类的口服抗糖尿病药物的组合并未得到良好的控制。甚至通过该治疗,该糖尿病患者仍然具有约为9.2至9.5mmol/l的空腹血糖浓度和约为8.5%的hba1c值。餐后2小时血糖为约13.8至14.5mmol/l(249至262mg/dl)。这些值仍然超过正常血糖值。
令人惊讶的是,通过用利西拉来、甘精胰岛素和任选地二甲双胍的组合治疗可观察到空腹血糖浓度降低至约6.6mmol/l(119mg/dl)。鉴于使用每日一次或每日三次的谷赖胰岛素(insulinglulisine)的比较治疗,利西拉来治疗的体重降低在统计学上是有优势的。
终止上述预先治疗且滴定甘精胰岛素(任选地与二甲双胍组合)达12周实现了空腹smpg的血糖靶标为4.4至5.6mmol/l而无复发性或严重低血糖,然后开始使用利西拉来、甘精胰岛素和任选地二甲双胍的组合治疗导致了空腹血糖浓度由9.16mmol/l至6.91mmol/l的初始降低以及hba1c由8.51%至7.87%的初始降低。
鉴于使用每日一次或每日三次的谷赖胰岛素的比较治疗,利西拉来治疗所记载的低血糖在数字上显著较低。
因此,相对于膳食胰岛素(如谷赖胰岛素)而言,甘精胰岛素与利西拉来和任选地二甲双胍的组合可称为优选的选择,从而得到有意义的具有较少低血糖且具有体重减轻的血糖靶标,这是因为基础胰岛素+口服抗糖尿病化合物或基础胰岛素+膳食胰岛素(推注施用)难于控制肥胖的、胰岛素治疗的2型糖尿病患者。
本发明的第一方面为用于在2型糖尿病患者中控制血糖的药物组合,该组合包含
(i)利西拉来或/和其药物上可接受的盐,
(ii)甘精胰岛素或/和其药物上可接受的盐,和
(iii)任选地二甲双胍或/和其药物上可接受的盐。
在该方面,优选地,待治疗的2型糖尿病用单独的化合物(b)和任选地化合物(c)并未得到充分(adequately)控制。
如经本申请披露的实施例所证实,本申请所述的组合可用于改善血糖控制。在本发明中,“改善血糖控制”或“控制血糖”具体是指改善餐后2小时血糖浓度、改善空腹血糖浓度或/和改善hba1c值。
具体地,“改善血糖控制”或“控制血糖”包括改善餐后2小时血糖浓度。
具体地,“改善血糖控制”或“控制血糖”包括降低餐后2小时血糖浓度。降低具体是指餐后2小时血糖浓度达到正常血糖值或至少接近这些值。
具体地,“改善血糖控制”或“控制血糖”包括改善空腹血糖浓度。
具体地,改善空腹血糖浓度包括降低空腹血糖浓度。降低具体是指空腹血糖浓度达到正常血糖值或至少接近这些值。
具体地,“改善血糖控制”或“控制血糖”包括改善hba1c值。
具体地,改善hba1c值包括降低hba1c值。降低hba1c值具体是指hba1c值降低至低于6.5%或7%。
本发明的另一方面为药物组合,其用于在2型糖尿病患者中改善hba1c值、空腹血糖或/和餐后2小时血糖,该组合包含
(i)利西拉来或/和其药物上可接受的盐,
(ii)甘精胰岛素或/和其药物上可接受的盐,和
(iii)任选地二甲双胍或/和其药物上可接受的盐。
在该方面,优选地,待治疗的2型糖尿病用单独的化合物(b)和任选地化合物(c)并未得到充分控制。
在本发明中,正常血糖值为具体为60-140mg/dl(相应于3.3至7.8mmol/l)的血糖浓度。该范围具体是指在空腹条件和餐后条件下的血糖浓度。
2型糖尿病诊断标准包括:
-空腹血糖浓度(fpg)为≥7.0mmol/l(126mg/dl),或
-餐后血糖浓度为>11.1mmol/l(200mg/dl),如世界卫生组织所述进行(definition,diagnosisandclassificationofdiabetesmellitusanditscomplications.part1:diagnosisandclassificationofdiabetesmellitus.who/ncd/ncs/99.2.geneva;1999),使用含有溶于水中的75g无水葡萄糖当量的糖负荷,或
-糖尿病症状+随机血糖≥200mg/dl(11.1mmol/l)。
这些标准描述于globalidf/ispadguidelinefordiabetesinchildhoodandadolescence(internationaldiabetesfederation,isbn2-930229-72-1)。
2型糖尿病的诊断不应当基于单一的血糖浓度。诊断可需要对空腹和/或餐后血糖水平持续的观察和/或口服葡萄糖耐量测试。
根据craig(type2diabetes2014:15(suppl.20):4–17),空腹血糖(fpg)和激发后(加载后)血糖可如下分类:
-fpg<5.6mmol/l(100mg/dl)=正常空腹葡萄糖浓度。
-fpg5.6至6.9mmol/l(100–125mg/dl)=受损的空腹葡萄糖浓度。
-fpg≥7.0mmol/l(126mg/dl)=糖尿病的临时性诊断(诊断必须如上所述确认)。
当使用口服葡萄糖耐量测试(ogtt)时,相应的分类如下:
-2小时加载后葡萄糖<7.8mmol/l(140mg/dl)=正常葡萄糖耐量。
-2小时加载后葡萄糖7.8至<11.1mmol/l(140–200mg/dl)=受损的葡萄糖耐量。
-2小时加载后葡萄糖≥11.1mmol/l(200mg/dl)=糖尿病的临时性诊断(诊断必须如上所述确认)。
受损的葡萄糖耐量(igt)和受损的空腹葡萄糖浓度(ifg)为正常的葡萄糖稳态和糖尿病之间的碳水化合物代谢紊乱的自然病史的中间阶段。
在本发明中,空腹血糖的正常血糖值为特别是<5.6mmol/l的血糖浓度。
在本发明中,本申请定义的餐后血糖的正常血糖为特别是<7.8mmol/l的血糖浓度。
在本发明中,通过具体的抗糖尿病治疗而“未得到充分控制”具体地是指该治疗并不足以除去2型糖尿病的症状。具体地,通过该治疗而“未得到充分控制”是指患者并未达到在例如餐后2小时血糖浓度、hba1c值或/和空腹血糖浓度方面的正常血糖值。
本发明的待治疗的2型糖尿病患者可为患有2型糖尿病的受试者,其中2型糖尿病通过用基础胰岛素单一疗法治疗并未得到充分控制。
本发明的待治疗的2型糖尿病患者可为患有2型糖尿病的受试者,其中2型糖尿病通过用单独的基础胰岛素和二甲双胍的组合治疗并未得到充分控制,例如(a)用剂量为至少1.0g/天的二甲双胍或至少1.5g/天的二甲双胍治疗至少3个月,或/和(b)用剂量为最大2.0g/天的二甲双胍治疗至少3个月或最大3.5g/天的二甲双胍治疗至少3个月。
本发明的待治疗的2型糖尿病患者可为患有2型糖尿病的受试者,其中待治疗的2型糖尿病用单独的化合物(b)和任选地化合物(c)并未得到充分控制。
通过本发明的治疗,可在经本申请所述的具体治疗未得到充分控制的2型糖尿病患者中实现2型糖尿病的充分控制。
本申请使用的“基础胰岛素”包括甘精胰岛素、地特胰岛素和低精蛋白胰岛素(isophaneinsulin)(nph胰岛素)。基础胰岛素具体地选自由下列组成的群组:甘精胰岛素、地特胰岛素和低精蛋白胰岛素(nph胰岛素)。
本申请使用的“本发明的待治疗的”、“本发明的治疗”或“本发明的疗法”涉及通过药物组合治疗2型糖尿病患者,该药物组合包含本申请所述的
(i)利西拉来或/和其药物上可接受的盐,
(ii)甘精胰岛素或/和其药物上可接受的盐,和
(iii)任选地二甲双胍或/和其药物上可接受的盐。
本发明的另一方面为用于在2型糖尿病患者中预防体重增加或/和引起体重减轻的药物组合,该组合包含
(i)利西拉来或/和其药物上可接受的盐,
(ii)甘精胰岛素或/和其药物上可接受的盐,和
(iii)任选地二甲双胍或/和其药物上可接受的盐。
在该方面,优选地,待治疗的2型糖尿病用单独的化合物(b)和任选地化合物(c)并未得到充分控制。
本发明的实施例证实了本申请的组合可降低本申请定义的2型糖尿病患者的体重,其中比较治疗(每日一次或每日三次的谷赖胰岛素)引起了显著的体重增加。
本发明的另一方面为用于在2型糖尿病患者中降低低血糖风险的药物组合,该组合包含
(i)利西拉来或/和其药物上可接受的盐,
(ii)甘精胰岛素或/和其药物上可接受的盐,和
(iii)任选地二甲双胍或/和其药物上可接受的盐。
在该方面,优选地,待治疗的2型糖尿病用单独的化合物(b)和任选地化合物(c)并未得到充分控制。
本发明的实施例证实了鉴于使用每日一次或每日三次的谷赖胰岛素的比较治疗,本申请的组合治疗所记载的低血糖在数字上显著较低。
低血糖为在糖尿病的短期和长期血糖控制中的关键限制因素。尽管对糖尿病的血糖控制得到稳定改善,但是基于群体的数据表明低血糖仍然为i型和2型糖尿病人群的主要问题(americandiabetesassociation,workgrouponhypoglycemia:definingandreportinghypoglycemiaindiabetes.diabetescare28(5),2005,1245-1249)。
当施用本申请所述的2型糖尿病患者时,本发明的组合可预防低血糖。“预防低血糖”包括降低低血糖事件的数目和/或低血糖事件的严重性。本申请所述的组合适用于防止低血糖。
在本发明中,低血糖为这样的病症,其中2型糖尿病患者经历了低于70mg/dl(或低于3.9mmol/l)、低于60mg/dl(或低于3.3mmol/l)、低于54mg/dl(或低于3.0mmol/l)、低于50mg/dl、低于40mg/dl或低于36mg/dl的血糖浓度。
在本发明中,“症状性低血糖”或“症状性低血糖事件”为与由低血糖导致的临床症状相关的病症,其中血糖浓度可为低于70mg/dl(或低于3.9mmol/l)、低于60mg/dl(或低于3.3mmol/l)、低于54mg/dl(或低于3.0mmol/l)、低于50mg/dl或低于40mg/dl。临床症状可为例如发汗、心悸、饥饿、不安、焦虑、疲劳、易怒、头痛、集中力缺失、嗜眠、精神病症、视觉障碍、瞬时感觉缺陷、瞬时运动缺陷、混乱、惊厥和昏迷。在本发明中,可选择本申请所述的症状性低血糖的一种或多种临床症状。症状性低血糖可与口服碳水化合物施用后的快速恢复相关。症状性低血糖事件优选具有低于60mg/dl(或低于3.3mmol/l)的血糖浓度。
在本发明中,“严重症状性低血糖”或“严重症状性低血糖事件”为具有由低血糖导致的本申请所述的临床症状的病症,其中血糖浓度可为低于70mg/dl(或低于3.9mmol/l)、低于54mg/dl(或低于3.0mmol/l)或低于36mg/dl(或低于2.0mmol/l)。严重症状性低血糖可与由低血糖事件导致的急性神经功能缺损相关。在严重症状性低血糖中,患者可能需要其他人的帮助以积极地施用碳水化合物、高血糖素或其他复苏行动。这些发作可与诱导癫痫发作、意识丧失或昏迷的急性神经低血糖症相关。血糖测量可能在该事件过程中不可用,但是认为有助于使血糖恢复正常的神经系统恢复可以充分地证明该事件由低的血糖浓度引起。严重症状性低血糖事件优选具有低于36mg/dl(或低于2.0mmol/l)的血糖浓度。
严重症状性低血糖的定义可包括所有事件,其中神经功能缺损严重到足以阻止自我治疗,且因此认为该事件使得患者处于对他们自己或其他人造成伤害的风险。急性神经功能缺损可为选自由下列组成的群组:嗜眠、精神病症、视觉障碍、瞬时感觉缺陷、瞬时运动缺陷、混乱、惊厥和昏迷的至少一种。“需要帮助”是指患者可能无法自我完成治疗。当不需要帮助时,出于善意而帮助患者不应当认为是“需要帮助”事件。
严重症状性低血糖可与口服碳水化合物、静脉内施用葡萄糖或/和施用高血糖素后的快速恢复相关。
在本发明中,“记载的症状性低血糖”或“记载的症状性低血糖事件”为这样的事件,在该事件过程中低血糖的典型症状所伴有的经测量的血糖浓度为≤70mg/dl(≤3.9mmol/l)或小于或等于54mg/dl(≤3.0mmol/l)。认为由低血糖事件导致的临床症状为例如增多的发汗、神经过敏、虚弱/无力、颤抖、头晕、食欲增加、心悸、头痛、睡眠障碍、混乱、癫痫发作、意识丧失、昏迷。
在本发明中,“无症状性低血糖”或“无症状性低血糖事件”为这样的事件,其不伴有低血糖的典型症状,但所具有的经测量的血糖浓度低于或等于70mg/dl(3.9mmol/l)或小于或等于54mg/dl(3.0mmol/l)。
在本发明中,“可能的症状性低血糖”或“可能的症状性低血糖事件”为这样的事件,在该事件过程中低血糖的症状不伴有血糖确定,但该事件可能由小于或等于70mg/dl(或小于或等于3.9mmol/l)或小于或等于54mg/dl(或小于或等于3.0mmol/l)的血糖浓度引起;用口服碳水化合物治疗的症状而未进行血糖测试。
在本发明中,“相对低血糖”或“相对低血糖事件”为这样的事件,在该事件过程中患有糖尿病的人报告有任何低血糖的典型症状,且该症状解释为表明低血糖,但经测量的血糖浓度大于70mg/dl(或大于3.9mmol/l)。
在本发明中,低血糖可为症状性低血糖、严重症状性低血糖、记载的症状性低血糖、可能的症状性低血糖、相对症状性低血糖或无症状性低血糖。优选的是症状性低血糖,更优选的是严重症状性低血糖。
本申请使用的“降低低血糖风险”可包括降低低血糖的发生率。每个患者年(patientyear)的低血糖发生率可针对每个患者计算为:365.25x(低血糖的事件数目)/(暴露的天数),并且根据事件的类型和治疗组进行汇总。当将本申请所述的制剂施用至本申请所述的2型糖尿病患者时,本申请使用的“降低低血糖风险”还可包括预防患者的低血糖。本申请使用的“降低低血糖风险”还可包括降低低血糖事件数目和/或降低低血糖事件的严重性。
患有本发明的待治疗的2型糖尿病的2型糖尿病患者可为肥胖的。如果体重指数为至少30kg/m2,则可认为该患者肥胖。在本发明中,肥胖2型糖尿病患者所具有的体重指数可为至少30kg/m2。肥胖的2型糖尿病患者所具有的体重可为至少87kg、至少88kg、至少89kg或至少90kg。在使用本发明的组合的疗法开始前,2型糖尿病患者可为肥胖的。
待治疗的患者的年龄可为小于50岁。患者的年龄也可为至少50岁或50至64岁的范围。患者的年龄也可为至少65岁或65至74岁的范围。患者的年龄也可为至少75岁。优选的是患者的年龄为至少65岁。
本发明的待治疗的2型糖尿病患者可患有用基础胰岛素单一疗法或基础胰岛素和选自由下列组成的群组:单独的二甲双胍、磺酰脲类、dpp-4抑制剂或格列奈类的单独使用的一至三种口服抗糖尿病药物未得到充分控制的2型糖尿病。在该情况下,基础胰岛素具体选自由下列组成的群组:甘精胰岛素、地特胰岛素和低精蛋白胰岛素(nph胰岛素)。此外,优选地,该待治疗的2型糖尿病用单独的化合物(b)和任选地化合物(c)并未得到充分控制。
当用基础胰岛素单一疗法或基础胰岛素和选自由下列组成的群组:单独的二甲双胍、磺酰脲类、dpp-4抑制剂或格列奈类的单独使用的一至三种口服抗糖尿病药物治疗时,本发明的待治疗的2型糖尿病患者所具有的空腹血糖可为至少9mmol/l或至少9.5mmol/l。具体地,在使用本发明的组合的疗法开始前,该患者所具有的该空腹血糖可为至少9mmol/l或至少9.5mmol/l。在该情况下,基础胰岛素具体地选自由下列组成的群组:甘精胰岛素、地特胰岛素和低精蛋白胰岛素(nph胰岛素)。此外,优选地,该待治疗的2型糖尿病用单独的化合物(b)和任选地化合物(c)并未得到充分控制。
在使用本发明的组合的疗法开始前,当用单独的化合物(b)和任选地化合物(c)治疗时,患者所具有的空腹血糖的范围为5.6至6.9mmol/l。该范围可认为是受损的空腹血糖浓度。
在使用本发明的组合的疗法开始前,当用单独的化合物(b)和任选地化合物(c)治疗时,患者所具有的空腹血糖可为至少6.6mmol/l、至少6.7mmol/l、至少6.8mmol/l或至少6.9mmol/l。
当用基础胰岛素单一疗法或基础胰岛素和选自由下列组成的群组:单独的二甲双胍、磺酰脲类、dpp-4抑制剂或格列奈类的单独使用的一至三种口服抗糖尿病药物治疗时,本发明的待治疗的2型糖尿病患者所具有的hba1c可为至少8.5%。具体地,在使用本发明的组合的疗法开始前,患者所具有的该hba1c可为至少8.5%。在该情况下,基础胰岛素具体地选自由下列组成的群组:甘精胰岛素、地特胰岛素和低精蛋白胰岛素(nph胰岛素)。此外,优选地,该待治疗的2型糖尿病用单独的化合物(b)和任选地化合物(c)并未得到充分控制。
在使用本发明的组合的疗法开始前,当用单独的化合物(b)和任选地化合物(c)治疗时,患者所具有的hba1c可为至少7.5%或至少7.8%。
具体地,本发明的待治疗的患者并未接受用磺酰脲类、dpp-4抑制剂和格列奈类中的至少一种的联合治疗(concomitanttreatment)。
具体地,在本发明的待治疗的患者中,在本发明的疗法开始前,2型糖尿病已经诊断达至少1年或至少2年。
施用本发明的组合可包括以下步骤:
(i)施用化合物(b)和(c)达至少4周,和
(ii)继续通过施用化合物(a)、(b)和(c)治疗,
其中调节(滴定)在步骤(i)或/和(ii)中待施用的化合物(b)的量以使得达到或至少接近预定空腹血糖水平或/和预定的自我监测血糖水平。具体地,调节(滴定)化合物(b)在步骤(i)中进行。
步骤(i)中,本发明的药物组合的化合物(b)和(c)可施用至少4周、至少8周、至少12周或至少16周。优选地,步骤(i)包括施用化合物(b)和(c)达至少约12周。
步骤(i)可进行最大约8周、最大约12周、最大约16周、最大约20周或最大约24周。优选的是步骤(i)的持续时间为约12周。
在未施用化合物(a)的情况下,可进行步骤(i)。如经本发明的实施例所证实,用甘精胰岛素、利西拉来和任选地二甲双胍的组合的治疗可改善空腹血糖浓度、hba1c值、体重和低血糖风险,如果该治疗起始于施用单独的甘精胰岛素和任选地二甲双胍的话。按照该治疗方案,可降低甘精胰岛素的剂量。
在本发明的药物组合物中,调节步骤(i)或/和(ii)中待施用的化合物(b)的量以使得达到或至少接近预定空腹血糖水平或/和预定的自我监测血糖水平。步骤(i)或/和(ii)中待施用的化合物(b)的量可基于血糖浓度的每日测量进行调节。具体地,可调节步骤(i)或/和(ii)中待施用的化合物(b)的量以使得达到或至少接近:
(i)约4.4mmol/l至约5.6mmol/l的空腹血糖水平或/和空腹自我监测的血糖水平,或/和
(ii)约7.8mmol/l(或约140mg/dl)或更低的自我监测的血糖水平(smpg)。
本申请使用的“自我监测的血糖(smpg)”可为“4-点自我监测的血糖”或“7-点自我监测的血糖”。该4-点和7-点自我监测的血糖值具体为包括空腹和餐后条件下的平均血糖浓度。
“4-点自我监测的血糖”具体是指每日四次测量血糖且由此计算平均血糖浓度。具体地,该4-点自我监测的血糖测量在早餐前、早餐后、晚餐前和晚餐后进行。
“7-点自我监测的血糖”具体是指每日七次测量血糖且由此计算平均血糖浓度。具体地,该7-点自我监测的血糖测量在早餐前、早餐后、午餐前、午餐后、晚餐前、晚餐后和入睡时进行。
本申请使用的“空腹自我监测的血糖(smpg)”由患者在早餐前测量,具体地在甘精胰岛素或/和利西拉来注射和任选摄取二甲双胍前测量。
在本发明中,2型糖尿病患者所具有的hba1c值的范围可为7%至10%。具体地,待治疗的2型糖尿病患者所具有的hba1c值可为至少约7%、至少约7.5%、至少约7.8%、至少约8%、至少约8.5%或至少约9%。这些值超过了正常血糖值,指示如果用抗糖尿病化合物治疗,则2型糖尿病并未得到充分控制,如本申请所述。
本发明的待治疗的2型糖尿病患者所具有的餐后2小时血糖浓度可为至少11.1mmol/l、至少12mmol/l、至少13mmol/l、至少13.5mmol/l或至少14mmol/l。这些血糖浓度超过了正常血糖浓度,指示如果用抗糖尿病化合物治疗,则2型糖尿病并未得到充分控制,如本申请所述。
“餐后”为糖尿病学领域技术人员熟知的术语。术语“餐后”具体描述了在进食后或/和在试验条件下暴露于葡萄糖后的阶段。在健康人中,该阶段的特征在于血糖浓度的增加和随后降低。餐后阶段通常结束于进食后或/和暴露于葡萄糖后至多2小时(餐后2小时血糖浓度)。
餐后血糖的确定是熟知的(参见例如crapo等,diabetes,1977,26(12):1178-1183)。
本发明的待治疗的2型糖尿病患者所具有的空腹血糖浓度可为至少8mmol/l、至少8.5mmol/l、至少9mmol/l或至少9.5mmol/l。这些血糖浓度超过了正常血糖浓度,指示如果用抗糖尿病化合物治疗,则2型糖尿病并未得到充分控制,如本申请所述。
在本发明中,二甲双胍可根据符合市售许可条例的通常已知的二甲双胍施用方案施用。例如,二甲双胍可每日一次、每日两次或每日三次施用。具体地,在本申请披露的疗法开始前应用的二甲双胍剂量在本申请披露的(a)利西拉来或/和其药物上可接受的盐和(b)甘精胰岛素或/和其药物上可接受的盐的组合中继续使用。
在本发明中,二甲双胍可口服施用。技术人员知晓适于通过口服施用治疗2型糖尿病的二甲双胍制剂。二甲双胍可施用至有此需要的2型糖尿病患者,其施用量足以引起治疗效果。二甲双胍可以至少1.0g/天或至少1.5g/天的剂量施用。二甲双胍可以最大2.0g/天或最大3.5g/天的剂量施用。每日二甲双胍剂量可分为两个或三个分开的剂量。对于口服施用,二甲双胍可配制为固体剂型,如片剂或丸剂。二甲双胍可用适当的药物上可接受的载体、佐剂或/和辅助物质配制。
在本发明中,利西拉来或/和其药物上可接受的盐可在对于施用甘精胰岛素和任选地二甲双胍的附加疗法中施用。
在本发明中,术语“附加”、“附加治疗”和“附加疗法”涉及使用甘精胰岛素和利西拉来和任选地二甲双胍的本发明的治疗。二甲双胍、甘精胰岛素或/和利西拉来可各自以每日一次剂量施用。二甲双胍、甘精胰岛素和利西拉来可通过不同的施用途径施用。二甲双胍可口服施用,且利西拉来和甘精胰岛素可肠胃外施用。
具体地,“附加”、“附加治疗”和“附加疗法”是指在本申请披露的本发明的治疗开始前施用的二甲双胍的剂量可在本发明的治疗中继续使用。
在本发明中,利西拉来包括其药物上可接受的盐。本领域技术人员知晓利西拉来的适当的药物上可接受的盐。本发明采用的利西拉来的优选的药物上可接受的盐为利西拉来的乙酸盐。
在本发明中,利西拉来或/和其药物上可接受的盐可施用至有此需要的2型糖尿病患者,其量足以引起治疗效果。
在本发明中,利西拉来或/和其药物上可接受的盐可用适当的药物上可接受的载体、佐剂或/和辅助物质配制。
利西拉来或/和其药物上可接受的盐可通过例如注射(如肌内或皮下注射)进行肠胃外施用。适当的注射装置,例如包含含有活性成分的注射器和注射针的所谓“笔”,是已知的。利西拉来或/和其药物上可接受的盐可以适当的量施用,例如该量的范围为10μg至20μg/剂量。
在本发明中,利西拉来或/和其药物上可接受的盐可以10μg至20μg的范围的每日剂量施用。利西拉来或/和其药物上可接受的盐可经每日一次注射施用。利西拉来或/和其药物上可接受的盐可在早餐前约30分钟施用。
在本发明中,利西拉来或/和其药物上可接受的盐可在液体组合物中提供,其优选为水性制剂。优选的是该液体组合物适于肠胃外施用,具体为注射。本领域技术人员已知利西拉来的该液体组合物。本发明的液体组合物可具有酸性或生理学ph。酸性ph优选的范围为ph1-6.8、ph3.5-6.8或ph3.5-5。生理学ph优选的范围为ph2.5-8.5、ph4.0-8.5或ph6.0-8.5。ph可通过药物上可接受的稀酸(通常为hcl)或药物上可接受的稀碱(通常为naoh)来调节。
包含利西拉来或/和其药物上可接受的盐的液体组合物可包含适当的防腐剂。适当的防腐剂可选自由下列组成的群组:苯酚、间甲酚、苯甲醇和对羟基苯甲酸酯。优选的防腐剂为间甲酚。
包含利西拉来或/和其药物上可接受的盐的液体组合物可包含张度剂。适当的张度剂可选自由下列组成的群组:甘油、乳糖、山梨醇、甘露醇、葡萄糖、nacl、含有钙或者镁的化合物如cacl2。该甘油、乳糖、山梨醇、甘露醇和葡萄糖的浓度范围可为100-250mm。nacl的浓度可为多至150mm。优选的张度剂为甘油。
包含利西拉来或/和其药物上可接受的盐的液体组合物可包含0.5μg/ml至20μg/ml,优选1μg/ml至5μg/ml的甲硫氨酸。优选地,该液体组合物包含l-甲硫氨酸。
在本发明中,甘精胰岛素或/和其药物上可接受的盐可以液体组合物中提供,其优选为含水制剂。优选的是液体组合物适于肠胃外施用,特别是注射。技术人员知晓甘精胰岛素的该液体组合物。
可将表面活性剂加入至包含甘精胰岛素的药物制剂,例如,具体为非离子表面活性剂。具体地,优选药物上可接受的常规表面活性剂,如:多元醇如甘油、山梨醇等的偏酯和脂肪酸酯和醚(
包含甘精胰岛素或/和其药物上可接受的盐的制剂可额外地含有防腐剂(例如苯酚、间甲酚、对甲酚和对羟基苯甲酸酯)、张度剂(例如甘露醇、山梨醇、乳糖、右旋糖、海藻糖、氯化钠、甘油)、缓冲物质、盐、酸和碱以及其他赋形剂。这些物质在每种情况下可单独存在或可选择地作为混合物存在。
甘油、葡萄糖、乳糖、山梨醇和甘露醇可存在于包含甘精胰岛素或/和其药物上可接受的盐的药物制剂中,其浓度为100-250mm,nacl的浓度为多至150mm。缓冲物质例如磷酸盐、乙酸盐、柠檬酸盐、精氨酸、甘氨酰甘氨酸或tris(即2-氨基-2-羟基甲基-1,3-丙二醇)缓冲液以及相应的盐可以5-250mm、优选10-100mm的浓度存在。其他赋形剂可尤其是盐或精氨酸。
包含甘精胰岛素或/和其药物上可接受的盐的制剂的锌浓度为由存在0-1000μg/ml、优选20-400μg/ml锌、最优选90μg/ml所达到的浓度范围。然而,锌可以氯化锌的形式存在,但盐不限于氯化锌。
在包含甘精胰岛素或/和其药物上可接受的盐的药物制剂中,甘油和/或甘露醇可以100-250mmol/l的浓度存在,和/或nacl优选以多至150mmol/l的浓度存在。
在包含甘精胰岛素或/和其药物上可接受的盐的药物制剂中,缓冲物质可以5-250mmol/l的浓度存在。
甘精胰岛素或/和其药物上可接受的盐可以60-6000nmol/ml、优选240-3000nmol/ml的浓度存在于药物制剂中。
包含甘精胰岛素或/和其药物上可接受的盐的制剂的ph的范围可为ph1-6.8,优选ph3.5–6.8,更优选ph3.5-4.5,甚至更优选ph4.0-4.5。
本发明的另一方面为包含以下的组合在制备用于在2型糖尿病患者中控制血糖的药物中的用途:
(a)利西拉来或/和其药物上可接受的盐,
(b)甘精胰岛素或/和其药物上可接受的盐,和
(c)任选地二甲双胍或/和其药物上可接受的盐,
其中优选地,待治疗的2型糖尿病用单独的化合物(b)和任选地化合物(c)并未得到充分控制。在该方面,患者可为本申请定义的患者。
本发明的另一方面为包含以下的组合在制备用于在2型糖尿病患者中改善hba1c值、空腹血糖或/和餐后2小时血糖的药物中的用途:
(a)利西拉来或/和其药物上可接受的盐,
(b)甘精胰岛素或/和其药物上可接受的盐,和
(c)任选地二甲双胍或/和其药物上可接受的盐,
其中优选地,待治疗的2型糖尿病用单独的化合物(b)和任选地化合物(c)并未得到充分控制。在该方面,患者可为本申请定义的患者。
本发明的另一方面为包含以下的组合在制备用于在2型糖尿病患者中预防体重增加或/和引起体重减轻的药物中的用途:
(a)利西拉来或/和其药物上可接受的盐,
(b)甘精胰岛素或/和其药物上可接受的盐,和
(c)任选地二甲双胍或/和其药物上可接受的盐,
其中优选地,待治疗的2型糖尿病用单独的化合物(b)和任选地化合物(c)并未得到充分控制。在该方面,患者可为本申请定义的患者。
本发明的另一方面为包含以下的组合在制备用于在2型糖尿病患者中降低低血糖风险的药物中的用途:
(a)利西拉来或/和其药物上可接受的盐,
(b)甘精胰岛素或/和其药物上可接受的盐,和
(c)任选地二甲双胍或/和其药物上可接受的盐,
其中优选地,待治疗的2型糖尿病用单独的化合物(b)和任选地化合物(c)并未得到充分控制。在该方面,患者可为本申请定义的患者。
本发明的另一方面为在2型糖尿病患者中控制血糖的方法,该方法包括施用包含以下的组合:
(i)利西拉来或/和其药物上可接受的盐,
(ii)甘精胰岛素或/和其药物上可接受的盐,和
(iii)任选地二甲双胍或/和其药物上可接受的盐,
其中优选地,待治疗的2型糖尿病用单独的化合物(b)和任选地化合物(c)并未得到充分控制。在该方面,患者可为本申请定义的患者。
本发明的另一方面为在2型糖尿病患者中改善hba1c值、空腹血糖或/和餐后2小时血糖的方法,该方法包括施用包含以下的组合:
(a)利西拉来或/和其药物上可接受的盐,
(b)甘精胰岛素或/和其药物上可接受的盐,和
(c)任选地二甲双胍或/和其药物上可接受的盐,
其中优选地,待治疗的2型糖尿病用单独的化合物(b)和任选地化合物(c)并未得到充分控制。在该方面,患者可为本申请定义的患者。
本发明的另一方面为在2型糖尿病患者中预防体重增加或/和引起体重减轻的方法,该方法包括施用包含以下的组合:
(a)利西拉来或/和其药物上可接受的盐,
(b)甘精胰岛素或/和其药物上可接受的盐,和
(c)任选地二甲双胍或/和其药物上可接受的盐,
其中优选地,待治疗的2型糖尿病用单独的化合物(b)和任选地化合物(c)并未得到充分控制。在该方面,患者可为本申请定义的患者。
本发明的另一方面为在2型糖尿病患者中降低低血糖风险的方法,该方法包括施用包含以下的组合:
(a)利西拉来或/和其药物上可接受的盐,
(b)甘精胰岛素或/和其药物上可接受的盐,和
(c)任选地二甲双胍或/和其药物上可接受的盐,
其中优选地,待治疗的2型糖尿病用单独的化合物(b)和任选地化合物(c)并未得到充分控制。在该方面,患者可为本申请定义的患者。
本申请的主题以如下各项进行描述:
1.药物组合,其在2型糖尿病患者中用于控制血糖、用于降低hba1c值、空腹血糖或/和餐后2小时血糖、用于预防体重增加或/和引起体重减轻、用于降低低血糖风险,该组合包含
(i)利西拉来或/和其药物上可接受的盐,
(ii)甘精胰岛素或/和其药物上可接受的盐,和
(iii)任选地二甲双胍或/和其药物上可接受的盐。
2.项1的用于该用途的药物组合,其中待治疗的2型糖尿病用单独的化合物(b)和任选地化合物(c)并未得到充分控制。
3.项1或2的用于该用途的药物组合,其中待治疗的患者是肥胖的。
4.前述各项中任一项的用于该用途的药物组合,其中待治疗的患者所具有的体重指数为至少30kg/m2。
5.前述各项中任一项的用于该用途的药物组合,其中待治疗的患者的年龄为至少65岁。
6.前述各项中任一项的用于该用途的药物组合,其中在使用项1的组合的疗法开始前,当用基础胰岛素单一疗法或基础胰岛素和选自由下列组成的群组:单独的二甲双胍、磺酰脲类、dpp-4抑制剂或格列奈类的单独使用的一至三种口服抗糖尿病药物治疗时,患者所具有的空腹血糖为至少9mmol/l。
7.前述各项中任一项的用于该用途的药物组合,其中在使用项1的组合的疗法开始前,当用单独的化合物(b)和任选地化合物(c)治疗时,患者所具有的空腹血糖浓度的范围为5.6至6.9mmol/l或空腹血糖浓度为至少6.6mmol/l。
8.前述各项中任一项的用于该用途的药物组合,其中在使用项1组合的疗法开始前,当用基础胰岛素单一疗法或基础胰岛素和选自由下列组成的群组:单独的二甲双胍、磺酰脲类、dpp-4抑制剂或格列奈类的单独使用的一至三种口服抗糖尿病药物治疗时,患者所具有的hba1c为至少8.5%。
9.前述各项中任一项的用于该用途的药物组合,其中在使用项1组合的疗法开始前,当用单独的化合物(b)和任选地化合物(c)治疗时,患者所具有的hba1c为至少7.5%。
10.项6-9中任一项的用于该用途的药物组合,其中基础胰岛素选自由下列组成的群组:甘精胰岛素、地特胰岛素和低精蛋白胰岛素(nph胰岛素)。
11.前述各项中任一项的用于该用途的药物组合,其中患者并未接受用磺酰脲类、dpp-4抑制剂和格列奈类中的至少一种的联合治疗。
12.前述各项中任一项的用于该用途的药物组合,其中在待治疗的患者中,在用化合物(a)、(b)和任选地(c)的疗法开始前,2型糖尿病已经诊断达至少1年或至少2年。
13.前述各项中任一项的用于该用途的药物组合,其中施用组合包括以下步骤:
(i)施用化合物(b)和(c)达至少4周,和
(ii)继续通过施用化合物(a)、(b)和(c)治疗,
其中调节步骤(i)中待施用的化合物(b)的量以使得达到或至少接近预定空腹血糖水平或/和预定的自我监测血糖水平。
14.项13的用于该用途的药物组合,其中调节步骤(i)中待施用的化合物(b)的量以使得达到或至少接近:
(i)约4.4mmol/l至约5.6mmol/l的空腹血糖水平或/和空腹自我监测的血糖水平,或/和
(ii)约7.8mmol/l(或约140mg/dl)或更低的自我监测的血糖水平(smpg)。
15.项14的用于该用途的药物组合,其中(ii)中的自我监测的血糖水平为4-点自我监测的血糖水平或7-点自我监测的血糖水平。
16.前述各项中任一项的用于该用途的药物组合,其中制备利西拉来或/和其药物上可接受的盐以用于肠胃外施用。
17.前述各项中任一项的用于该用途的药物组合,其中制备利西拉来或/和其药物上可接受的盐以用于以选自10μg至20μg的范围的每日剂量施用。
18.前述各项中任一项的用于该用途的药物组合,其中制备甘精胰岛素或/和其药物上可接受的盐以用于肠胃外施用。
19.前述各项中任一项的用于该用途的药物组合,其中制备二甲双胍或/和其药物上可接受的盐以用于口服施用。
20.用于改善血糖控制、用于降低hba1c值或/和空腹血糖、用于预防体重增加或/和引起体重减轻、用于降低低血糖风险的方法,该方法包括向有此需要的受试者施用项1-18中任一项的组合。
21.项20的方法,其中待治疗的2型糖尿病用单独的化合物(b)和任选地化合物(c)并未得到充分控制。
22.项20或21的方法,其中该受试者为如在项2-15中任一项定义的受试者。
本发明在下述实施例和附图中进行进一步说明。
附图说明
图1-经访视hba1c(%)由基线的平均变化的图-mitt群体
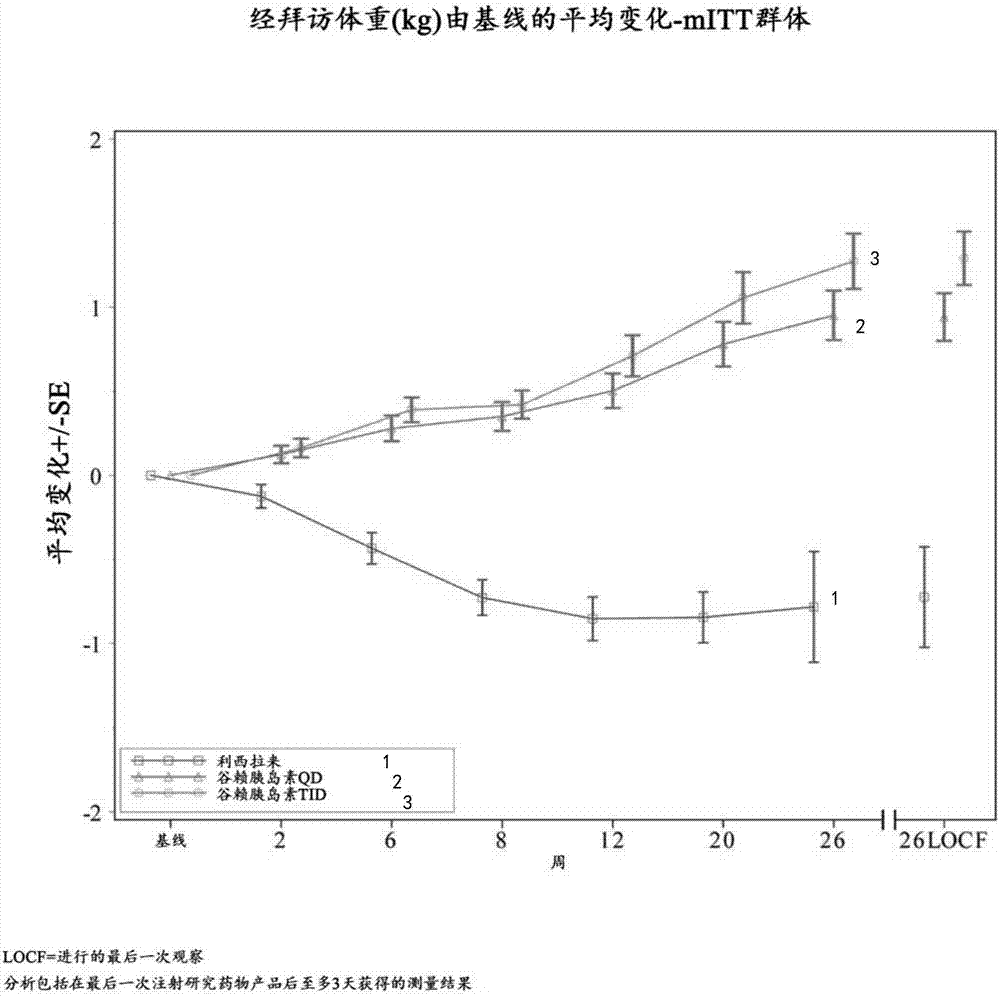
图2-经访视体重(kg)由基线的平均变化的图-mitt群体
图3-经访视平均甘精胰岛素每日剂量(u)的图-mitt群体
图4-经访视平均谷赖胰岛素每日剂量(u)的图-mitt群体
图5-经访视平均总胰岛素剂量(u)的图-mitt群体
图6-图示研究设计。1甘精胰岛素应当在晚餐或早餐时每日一次经皮下注射(根据患者的/研究者的喜好)。注射时间(晚餐或早餐)应当在v2固定且在整个研究中保持相同。2注射利西拉来应当在晚餐或早餐前30-60分钟进行(与在三个不同天之间的最高自我监测的2h-ppg中值相关)。用于利西拉来施用的进食(meal)应当在整个26周治疗期内保持相同。3注射谷赖胰岛素应当在晚餐或早餐前0-15分钟完成(与在三个不同天之间的最高自我监测的2h-ppg中值相关)。用于谷赖胰岛素施用的进食应当在整个26周治疗期内保持相同。4在早餐、午餐和晚餐前注射谷赖胰岛素。
实施例1
随机化、标签公开、活性对照、3-臂平行组、26周研究,其在患有用甘精胰岛素(用或不用二甲双胍)未得到充分控制的2型糖尿病的患者中比较利西拉来与每日一次的谷赖胰岛素和每日三次的谷赖胰岛素的效能和安全性
1.缩写
ae:不良事件
ancova:协方差分析
bmi:体重指数
ci:置信区间
cmh:cochran-mantel-haenszel
ecg:心电图
fpg:空腹血糖
glp-1:高血糖素样肽-1
imp:研究药物产品
locf:进行的最后一次观察
ls:最小二乘法
mitt:修改的治疗意图
pg:血糖
pt:优先项
qd:每天(每日一次)
sae:严重不良事件
smpg:自我测量的血糖
soc:系统器官分类
teae:治疗突发的不良事件
tid:每天三次(每日三次)
2.概述
3.结果
3.1研究患者
3.1.1患者责任
表1-分析群体
注意:对安全性群体患者按照实际接受的治疗(进行治疗)进行制表。对于其他群体,按照他们的随机化治疗对患者进行制表。
3.1.2研究安排
表2-患者安排-随机化群体
a:针对该研究未安排救援疗法,取而代之的是如果在第12周或之后的hba1c值高于8.5%,并且如果适当的校正行为失败且4周后重复的hba1c保持高于8.5%,则推荐中断。
注意:使用随机化患者的数目作为分母计算百分比。
3.1.3人口统计和基线特征
表3-在筛查时或基线的人口统计和患者特征-随机化群体
bmi=体重指数.
a:imp注射的进食由4-点smpg确定,仅呈现利西拉来和谷赖胰岛素qd组。
表4-筛查时或基线的疾病特征-随机化群体
glp-1=高血糖素样肽-1。
3.1.4剂量和治疗顺应性
表5-治疗顺应性-安全性群体
imp:研究药物产品
注意:顺应性比率(%)=(对于施用间隔的实际imp注射的总数/对于施用间隔的预期imp注射的总数)×100。
3.2效能
3.2.1主要效能终末点
表6-由基线至第26周的平均hba1c变化(%)-mitt群体
locf=进行的最后一次观察。
a协方差分析(ancova)模型使用治疗组(利西拉来、谷赖胰岛素qd和谷赖胰岛素tid)、hba1c(<8%,≥8%)的v7(周-1)等级、二甲双胍使用的随机化等级和国家作为固定效应并使用基线hba1c值作为协变量。
b利西拉来与谷赖胰岛素qd之间或利西拉来与谷赖胰岛素tid之间的ls平均值差异。
分析包括直至在最后一次注射研究药物产品后14天获得的测量。
包括同时具有基线和第26周(locf)测量的患者。
表7-由基线至第26周的平均体重变化(kg)-mitt群体
locf=进行的最后一次观察。
a协方差分析(ancova)模型使用治疗组(利西拉来、谷赖胰岛素qd和谷赖胰岛素tid)、hba1c(<8%,≥8%)的v7(周-1)等级、二甲双胍使用的随机化等级和国家作为固定效应及基线体重作为协变量。
b利西拉来与谷赖胰岛素qd之间或利西拉来与谷赖胰岛素tid之间的ls平均值差异。
分析包括直至在最后一次注射研究药物产品后3天获得的测量。
包括同时具有基线和第26周(locf)测量的患者。
图1显示mitt群体中通过访视由基线的平均hba1c变化(%)。图2显示了mitt群体中通过访视由基线的平均体重变化(kg)。
3.2.2其他关键效能终末点
表8-由基线至第26周的平均空腹血糖变化(mmol/l)-mitt群体
locf=进行的最后一次观察。
a协方差分析(ancova)模型使用治疗组(利西拉来、谷赖胰岛素qd和谷赖胰岛素tid)、hba1c(<8%,≥8%)的v7(周-1)等级、二甲双胍使用的随机化等级和国家作为固定效应及基线空腹血糖作为协变量。b利西拉来与谷赖胰岛素qd之间或利西拉来与谷赖胰岛素tid之间的ls平均值差异。
分析包括直至在最后一次注射研究药物产品后1天获得的测量。
包括同时具有基线和第26周(locf)测量的患者。
表9-由基线至第26周的平均甘精胰岛素剂量变化(u)-mitt群体
locf=进行的最后一次观察。
a协方差分析(ancova)模型使用治疗组(利西拉来、谷赖胰岛素qd和谷赖胰岛素tid)、hba1c(<8%,≥8%)的v7(周-1)等级、二甲双胍使用的随机化等级和国家作为固定效应及基线甘精胰岛素剂量作为协变量。
b利西拉来与谷赖胰岛素qd之间或利西拉来与谷赖胰岛素tid之间的ls平均值差异。分析包括直至在最后一次注射研究药物产品的日期获得的测量。
包括同时具有基线和第26周(locf)测量的患者。
图3显示了mitt群体中通过访视的平均甘精胰岛素每日剂量(u)。图4显示了mitt群体中通过访视的平均每日谷赖胰岛素剂量(u)。图5显示了mitt群体中通过访视的平均总体胰岛素剂量(u)。
3.3安全性
3.3.1治疗突发的不良事件
表10-不良事件分布的综述:治疗突发的不良事件-安全性
teae:治疗突发的不良事件,sae:严重不良事件
n(%)=具有至少一个teae的患者数目和百分数。
表11-通过主要soc和pt在任何治疗组中具有以pt≥3%出现的teae的患者数目(%)-安全性
teae:治疗突发的不良事件,soc:系统器官分类;
meddra17.1
n(%)=具有至少一个teae的患者数目和百分数。
注意:该表格按照soc国际认可等级以及利西拉来主要进食组中pt的频率降低来分类。
3.3.2严重的治疗突发的不良事件
表12-具有按照主要soc和pt呈现的治疗突发的sae的患者数目(%)-安全性群体
teae:治疗突发的不良事件,soc:系统器官分类,pt:优先项
meddra17.1
a基底细胞癌报道为“发际上方左侧的癌”
n(%)=具有至少一个治疗突发sae的患者数目和百分数。
注意:该表格按照soc国际认可等级和利西拉来主要进食组中pt的频率降低来分类。
3.3.3导致永久性imp中断的不良事件
表13-在进行治疗阶段经历按照主要soc和pt导致永久性治疗中断的teae的患者数目(%)-安全性群体
teae:治疗突发的不良事件,soc:系统器官分类,pt:优先项
meddra17.1
n(%)=具有至少一个导致永久性治疗中断的teae的患者数目和百分数。
note:该表格按照soc国际认可等级来利西拉来组中pt的频率降低来分类。
3.3.4其他显著不良事件
症状性低血糖
表14-在teae阶段满足方案定义的症状性低血糖的汇总-安全性群体
症状性低血糖=按照方案定义的症状性低血糖(伴有血糖<60mg/dl[3.3mmol/l]或与对抗措施(如果未得到血糖)的快速恢复相关)。
治疗阶段=由首次注射研究药物产品直至最后一次注射研究药物产品后3天的时间。
1:计算为(具有事件的患者数目*100/总体暴露+患者年中的3天)。
2:计算为(事件数目*100/总体暴露+患者年中的3天)。
变应性反应
表15-在teae阶段过程中具有由arac判定为变应性反应的事件的患者数目(%)-安全性群体
arac=变应性反应评估委员会。imp=研究药物产品。
胰腺炎
表16-在teae阶段过程中具有由psac判定为胰腺炎的任何事件的患者数目(%)-安全性群体
psac=胰腺炎安全性评估委员会
降钙素
表17-具有以特定不良事件形式报道的降钙素增加(>=20ng/l)的teae的患者数目(%)-安全性群体
teae:治疗突发的不良事件
实施例2
在肥胖的t2dm中相对于谷赖胰岛素qd或tid而言使用膳食利西拉来qd促进基础甘精胰岛素:getgoal-duo2基于证据的试验
为了提供关于如何促进基础胰岛素(bi)的证据,发明人对具有t2dm的不良控制的bi治疗的(≥6mo±1-3oads)肥胖成人探究了治疗选择,其使所述患者随机化接受利西拉来20μgqd(lixi)、谷赖胰岛素qd(glu-1)或glutid(glu-3),所有均已添加甘精胰岛素(ig)±二甲双胍,如果在12周ig优化进行阶段后hba1c保持>7-9%,则停止使用其他oad。26周的共同主要终末点为:(1)lixi相对于glu-1而言在hba1c降低方面的非劣效性(95%ci上限<0.4%);以及(2)lixi相对于glu-3而言,在hba1c降低方面的非劣效性(2a)或在体重变化方面的优势性(单侧α≤0.025)(2b)。评估了fpg、ppg、ig剂量、组合结果、ae和低血糖。每组随机化298名患者(t2dm持续时间12年,bi持续时间3年,体重~90kg)。满足了所有共同主要终末点,这是由于lixi相对于glu-1和glu-3而言在hba1c降低方面为非劣效性的且相对于上述后两者而言在体重损失方面是统计学有优势的(表)。lixi相对于glu-1和glu-3而言在记载的低血糖方面均在数字上显著较低。总之,如果耐受,则bi+lixi可成为优选的选择以促进bi,从而得到有意义的血糖靶标,其具有较少的低血糖和体重减轻(相对于膳食胰岛素),这是因为basalplus或basal/bolus难于控制肥胖的胰岛素治疗的t2dm。
表
*早餐前用利西拉来或谷赖胰岛素治疗的mitt群体的亚组;
n为针对mitt群体的数目(所有患者接受≥1剂量的研究药物,其同时具有基线评估和≥1基线后评估)。
序列表
<110>赛诺菲-安万特德国有限公司
<120>治疗2型糖尿病患者
<130>59868pwo
<150>ep15159064.3
<111>2015-03-13
<160>2
<170>patentinversion3.5
<210>1
<211>44
<212>prt
<213>人工
<220>
<223>despro36-exendin毒蜥外泌肽-4(1-39)-lys6-nh2
<400>1
hisglygluglythrphethrseraspleuserlysglnmetgluglu
151015
glualavalargleupheileglutrpleulysasnglyglyproser
202530
serglyalaproproserlyslyslyslyslyslys
3540
<210>2
<211>39
<212>prt
<213>吉拉毒蜥(helodermasuspectum)
<220>
<223>毒蜥外泌肽-4-nh2
<400>2
hisglygluglythrphethrseraspleuserlysglnmetgluglu
151015
glualavalargleupheileglutrpleulysasnglyglyproser
202530
serglyalaproproproser
35
- 还没有人留言评论。精彩留言会获得点赞!