对尿液的回流的非侵入式检测的制作方法
本发明涉及一种用于对从膀胱流动到肾脏中的尿液的非侵入式检测的系统、方法和装置。所述方法、系统和装置依赖于在不同时间点进行的测量且可用于检测膀胱输尿管反流(vur)。所述系统、方法和装置被设计成检测尿液体积在输尿管、膀胱和/或肾脏中的变化。所述系统、方法和装置通过生物电阻抗或电阻抗断层成像(eit)技术来测量导电率变化。
背景技术:
vur是一种主要发生在幼龄儿童中的病症且涉及从膀胱通过输尿管到肾脏中的尿液的回流并且可对肾脏造成危及生命的损害。vur可涉及单个或双重泌尿收集系统,即单个输尿管(单侧)或两个输尿管(两侧)。对基于在排尿期膀胱尿道造影术(vcug)程序(这是目前用于诊断vur的最高准则)期间所观察到的患者、父母和医师的焦虑水平来对儿童检测膀胱输尿管反流(vur)的非侵入式方法的需要是明显的。在此上下文中,检测包含病症的初始诊断以及监测已诊断的患者以确定病症是否已经消退或有进展,以及在手术之后监测患者以确定病症是否已经消退或有进展。
初级vur主要发生在幼龄儿童(<5岁)中。据估计,所述病症在小儿群体的1%至2%和呈现有泌尿道感染(uti)的儿童的30%到40%中是普遍的。vur是肾实质性损伤(rpd)或肾瘢痕的风险因素。在大面积瘢痕的情况下,肾脏损伤可导致高血压、降低的肾脏功能、蛋白尿且在某些情况下导致终末期肾脏疾病(esrd)。在意大利的患有长期肾衰竭(crf)的儿童的一个前瞻性、基于群体的注册表中,考虑到所有患者中的25.4%患有crf,vur是crf的单个主要病因。将得益于本发明的患者群体包含呈现有uti的患者(尤其那些低于5岁的患者)、患有肾积水的儿童以及那些患有vur的患者的同胞和子女。
目前,当放射科医生将一儿童归类为患有疑似vur时,他们可使用肾脏膀胱超声波(rbus)、排尿期膀胱尿道造影术(vcug)、核膀胱像和或二巯基丁二酸(dmsa)来评估。目前用于分析患有疑似vur的患者的这些方法中的每一种具有与其相关的至少一个重大缺陷:
●vcug是用于对vur定级的最高准则,然而,其同时涉及导管插入法和大量辐射暴露。在vcug期间,将导管放置在患者的尿道中且将不透射线造影剂通过导管滴注到膀胱中。随着膀胱被充盈而观察肾脏、输尿管和膀胱,且荧光检查用于在排尿期间对患者成像以检测vur。
●rbus,其不被视为vur的可靠指示符(大致26%精确)。
●dmsa是一种昂贵的测试,其涉及大量辐射暴露且必须由核医学专员进行。dmsa可以不检测vur,而用于指示在肾脏中是否已经存在损伤。
●核膀胱像还需要导管通道和辐射暴露以精确检测vur。将放射性核素滴注到膀胱中且使用伽玛相机对患者成像。然而,辐射暴露减少,图像质量可能较差。
如果vur被诊断或治疗,那么要求每隔一定间隔重复测试以确定反流是否已经消退或有进展。通常基于在初始vcug评估期间由儿童、父母和治疗医师所经历的焦虑水平而避免重复vcug测试。在所限定的时间点处,肾脏中的尿液体积的变化是膀胱输尿管反流(vur)的指示,所述体积的变化即随着膀胱压力在排尿或充盈期间增大,或随着膀胱压力在将压力手动地或通过系统自身施加到腹部且因此施加到膀胱而增大。如果患者罹患vur,那么在肾脏和或输尿管内的阻抗将在排尿期间增加,如果不存在vur,那么可观察到在肾脏和或输尿管中存在少量变化或没有变化。
生物电阻抗测量涉及使用一对皮肤接触电极来将电流馈入到身体中,并测量在邻近肾脏或输尿管的身体的表面处的相同或第二电极对之间的所得电压。一种用于测量生物电阻抗的设备从美国专利第6339722b1号已知。这种生物电阻抗测量系统用于确定关于体液的生物参数。
电阻抗断层成像(eit)提供基于跨平面的阻抗变化的阻抗分布图像,其中所述阻抗分布图像由电极的位置限定。在美国专利第20030216664a1号中描述使用eit系统来显示与身体的部位相关的阻抗分布图像的原理。
现有技术描述使用生物电阻抗来分析腹膜后出血、膀胱病症、膀胱功能和膀胱体积以及胃食道反流的概念。然而,没有文件描述将生物电阻抗作为测量肾脏功能或到肾脏中的尿液反流的非侵入式方法来使用。
研究已分析膀胱中的阻抗变化,以将信号提供给患者以指示患有截瘫或患有展示出膀胱充盈水平的感知受损的其它病症(可导致失禁或对泌尿生殖系统损伤)的患者的膀胱体积的变化。研究已展示在膀胱充盈期间和在膀胱使用生物电阻抗排尿之后的阻抗的动态变化。举例来说,描述用于基于生物电阻抗来监测膀胱尿液体积的装置的现有技术包含美国专利第5103835号和第cn104605850号中所描述的内容,所述专利cn104605850描述用于基于eit来监测膀胱尿液体积的方法。eit还用于监测来自肾脏的出血(腹膜后出血)。研究估计肾脏周围的空间中的阻抗变化是否可用于将存在内部出血的信息提供给医疗工作者。这对于监测被诊断患有肾脏钝伤或在进行肾脏手术之后的患者来说是有利的指示。
现有技术还描述使用生物电阻抗,更具体地说使用eit来监测胃食道反流(gor)。gor在胃部内容物从胃部朝向食管流动时发生。已建议将eit作为用于去除对于患者插管的需要来检测gor的可能方式。然而,在调查使用eit作为识别gor的替代方法的可行性的研究中,已推断出尚不可能使用eit精确地检测gor。所述研究表明,这可基于食管在身体中的深处位置、在没有反流发作期间在食管中观察到的变化以及反流流体和食管内容物的阻抗范围。
基于所关注的不同流体的阻抗范围、持续时间和事件的定时、外部器官的影响、病症的病理生理学、患者群体以及器官尺寸,技术人员将不能显而易见eit的使用对于yur的检测将是合适的或有效的。
不同流体的导电率:不同生物组织和流体具有不同导电率,其中所关注区域与周围区域之间的导电率的差越大,检测阻抗变化就越容易。举例来说,在检测vur时,尿液与肾脏的导电率(在100khz的频率下)分别为大致2.3s/m和0.17s/m,差为2.13s/m。其中,膀胱与尿液之间的差是2.09s/m且肾脏与血液的差是0.53s/m。取决于所食用的食物,在gor期间不可估计导电率改变值,这是由于胃部内容物的导电率导电率显著变化。其结果是,更容易检测尿液与肾脏之间的阻抗差且另外有可能通过使用进一步增大尿液的阻抗的口服溶液(例如具有高盐或离子浓度的溶液)而进一步增加导电率差值。
持续时间与定时:eit系统最适用于检测在已知时间段突然发生的动态变化。膀胱充盈、肾脏出血和gor通常是随机的,且发生在长时间、不可预测的时间段内。这限制了eit对于这些应用的效用。相比而言,vur在高导电流体(尿液)的浪涌从膀胱行进到输尿管或肾脏(在膀胱压力增大时)时发生(例如排尿——可预测且快速的事件)。当儿童排尿时,vur和高压力事件的同时发生提供已知时间段,且这个数据可用于反馈到系统中以限定所关注的时间段和参考时间帧从而在基线(在没有排尿发生时)上以及在排尿期间收集生物电阻抗测量值以检测vur。外部器官的影响——生物电阻抗测量值由外部因素影响,所述外部因素包含所关注区域周围的器官的活性。基于这一点,测量值将取决于所监测到的身体的位置受影响,且不同数据分析方法必须用于考虑周围器官的活性。举例来说,在监测胃食管反流(gor)时,需要考虑非常接近于食管的器官的活性。这些活性可包含呼吸(肺部中的空气)、心脏跳动和胃部内容物的分解。相比而言,可影响膀胱输尿管反流的生理参数可包含肠道蠕动、呼吸和膀胱中的尿液体积。
所述病症的病理生理学和患者群组:初级vur大体上由膀胱与输尿管之间短于正常壁内通道导致且存在于年龄在六个月与五岁之间的儿童中且通常将随着儿童成长而解决。vur通常在患者呈现有反复性或发热性尿道感染时诊断。胃食管反流可同时存在于成人和儿童中且通常归因于肥胖、节食和抽烟或疝气(在某些情况下)。胃食管反流通常与其它胃部症状一起遭遇。除尿道感染(初级vur的风险因子)以外。vur是无症状的:在病症发生时,患者无法感觉,而罹患胃食管反流的患者具有例如胃灼热的相异症状。
反流发源的器官和测量到的位置不同:vur在尿液从膀胱朝向肾脏行进通过输尿管时发生,然而,gor在胃部内容物从胃部朝向食管流动时发生。肾脏对膀胱来说是独立器官,然而,食管直接连接到胃部。胃食管反流在食管中被监测,且,在其已经行进通过输尿管之后在肾脏中监测到vur,且因此其在被监测到之前已经行进通过其它空间而进入不同器官。eit结果还将取决于电极与所关注区域的距离。食管位于最接近于胸腔的正面且肾脏位于接近于背部,恰好在肋骨下方。必须选定电极材料和大小并将其放置在取决于器官的位置使对每一病症的读数优化的位置中。
其它群组已参看用于检测vur的非侵入式方式。wo2000027286公开检测vur存在或不存在于患者中的无源声波方法,所述方法包括从恰好在排尿的发病之前的时间将声音从患者的腹部放大,且随后检测vur的音频信号特征存在或不存在于放大声波中。使用这种方法的临床研究未能解释11%的情况中的信号。us20100222699公开非侵入式温热疗法,所述非侵入式温热疗法使用发射能量来加热身体组织和流体(膀胱中的尿液)且非侵入式地测量目标流体和周围组织(肾脏)中的所得温度变化,从而检测和/或治疗各种生理病症,例如膀胱输尿管反流。安全问题可归因于使用微波能量来加热儿童的内脏。
本发明的目的
本发明的目的是提供一种装置、系统和方法以确定功能性肾脏特征,所述肾脏特征指示尿液在输尿管、膀胱和/或肾脏中的体积变化的,所述指示可用于检测yur以及所述yur是否有可能具有临床意义且患者是否要求进一步评估。
另外的目的是提供相对便宜、便携式且非侵入式的装置。换句话说,将不涉及辐射暴露或导管插入法的使用。又一目的是提供一种最小化由儿童、父母和医疗工作者在诊断vur时所经历的焦虑,进而改良与临床指南的符合性的系统、装置和方法。特殊目的是提供一种可在医院的急诊部、医师的办公室或诊所中的医疗点使用以便简化患者护理的装置、系统和方法。目的还在于使用所述系统来跟踪先前诊断的患者以确定其原始病症是否已改善或恶化。另外,其目的是提供一种可以允许患者在方便和舒适的位置中经受连续监测的系统、装置和方法。在某些情形下,还存在改良具有临床意义的vur的精确检测的需要,且这可通过在多个排尿周期内收集数据由本发明实现以便提供病症的更精确反映。所述系统和方法应以易于由用户感知和解释的方式显示功能性肾脏特征。
技术实现要素:
因此,本发明提供一种用于使用生物电阻抗技术或电阻抗断层成像(eit)来测量在个体内从膀胱流动到肾脏或输尿管的尿液的系统,所述系统包括配置成记录在肾脏或输尿管中的阻抗测量值的阻抗测量模块,和配置成从阻抗测量模块接收数据的处理器,所述数据是在一段时间内采集的阻抗测量值,且所述处理器进一步配置成分析测量值或测量值的群组之间的差值以提供肾脏的体积变化的指示。
换句话说,所述系统测量尿液在肾脏中的存在或体积。
阻抗测量模块可包括适用于记录阻抗测量值的多个电极,所述电极适用于以导电接触放置或与皮肤电容耦合且可连接到控制单元。
阻抗测量模块可包括至少两个电极。所述电极可并入到可穿戴单元中。控制单元也可并入到可穿戴单元中。
处理器可配置成产生曲线或图像以提供在一段时间内肾脏中的尿液体积变化的指示。
可随着膀胱压力在排尿或充盈期间增大,或随着膀胱压力在将压力手动地或通过系统自身施加到腹部且因此施加到膀胱时增大来采集测量值。数据可在排尿期间收集且与在没有发生排尿时所采集的基线测量值进行比较。
所述系统可包括用于将可穿戴单元固定到身体的构件,所述构件选自快速释放固定件、弹性带、可围绕大腿和/或肩部或颈部固定的背带、围兜、支架、悬带或绕颈系带。
本发明还提供一种用于检测在个体内从膀胱流动到肾脏或输尿管的尿液的方法,所述方法包括:记录发生在输尿管、膀胱和/或肾脏中的导电率变化,所述导电率变化指示输尿管、膀胱和/或肾脏中的体积变化,其中导电率变化通过生物电阻抗或电阻抗断层成像来检测,且将这些体积与控制值进行比较以指示vur存在或不存在于测试个体中。
在另一方面中,本发明提供一种用于使用生物电阻抗技术或电阻抗断层成像来检测在个体内从膀胱流动到肾脏的尿液的装置,其中所述装置包括:配置成记录肾脏或输尿管中的阻抗测量值的阻抗测量模块;和配置成从阻抗测量模块接收数据的处理器,所述数据是在一段时间内采集到的阻抗测量值,且所述处理器进一步配置成分析测量值或测量值的群组之间的差值,从而提供在一段时间内输尿管和/或肾脏中的体积变化的指示。
本发明涉及一种通过记录发生在输尿管、膀胱或肾脏中的阻抗变化来检测人类和动物体内从膀胱在朝向肾脏的方向上流动的尿液的系统、方法和装置,所述阻抗变化将指示输尿管、膀胱或肾脏中的尿液体积的变化。行进到肾脏的尿液的体积可在膀胱压力自然地增大时(在排尿或膀胱充盈期间)或在通过在膀胱上手动地按压或通过测量在排尿之后保留在膀胱中的尿液的残余体积引起时的时段期间测量。
因此,本发明提供一种用于使用生物电阻抗来测量和检测从膀胱流动到肾脏的尿液的方法、装置和系统,其中所述系统/装置包括阻抗测量模块,所述阻抗测量模块包括测量一定时间段内的阻抗变化的至少两个电极和控制单元。所述系统/装置还包括接收阻抗测量值并分析输出以估计一定时间段内的阻抗变化的处理器。所述分析可输出曲线以显示阻抗随时间的平均变化。曲线可在基线上(在没有发生排尿时)且在排尿期间分析以确定曲线的变化是否可在基线测量值与排尿期间的测量值之间观察到,或所述变化是否在排尿期间随时间增大。阻抗的变化可与vur相关。
为了进一步分析生物电阻抗输出,系统/装置可使用电阻抗断层成像技术。阻抗测量模块可包括多个电极和控制单元,所述多个电极可围绕在肾脏的水平面处的身体平面而放置,所述控制单元注入电流并且测量一定时间段内的阻抗变化。处理器接收阻抗测量值且分析输出以估计阻抗分布图像在一定时间段内的变化。
系统/装置的阻抗测量模块可包括并入到可穿戴单元中的多个电极和电子控制单元,所述电极围绕单元的外周间隔开,所述控制单元可连接到可穿戴单元且控制单元可连接到处理器,所述处理器可配置成接收并分析在一段时间内的阻抗测量值。处理器可集成到显示单元中或可与显示单元连接,所述显示单元向用户传达尿液体积在输尿管、膀胱和/或肾脏中是否存在变化。
可穿戴单元可包括束带或贴片。
电极可围绕束带的全部外周大致均匀地间隔开。替代地,所述多个电极可围绕束带的部分外周均匀地间隔开以形成半阵列。贴片可粘贴到患者,所述贴片含有电极。
所述电极可在电流注入和电压测量两种期间成对运作。电流施加在电极对之间且电压在电极对之间测量。
束带可形成于两个层中,在所述两个层中,电极带的外层材料优选地是防水的以防止水进入到电子组件中。内层可包括电极和/或结合粘合剂和/或高摩擦材料(例如硅酮或乙烯)的离散部分以防止移动。所述材料优选地选定为生物兼容性的。
所述电极彼此将不接触且可包括与皮肤接触的导电材料(具有8到105ohm/sq的近似平均表面电阻率)的离散部分。所述电极可以直接导电接触或电容耦合到身体表面。所述电极可与非导电材料(例如胶层)接触,所述非导电材料与皮肤接触。超声成像或x射线可用于识别输尿管、膀胱和/或肾脏的准确位置以确保恰当地安置电极或束带或贴片。
电极带或贴片可包括有源电极,其中每一电极含有有源电子芯片。
在本发明的上下文中的有源电极可使用与gaggero等人相同的配置,所述配置含有嵌入有电压缓冲器、开关和微处理器的芯片。有源电极产生用于从局部区域刺激和测量电势的激励作用。还可将有源电极称为激励电极、定位电极或治疗电极。在使用中,电子芯片可含有电极。有源电子芯片可通过例如柔性印刷电缆、排线或总线线路的连接而彼此连接且可以类似方式连接到控制单元。替代地,可将芯片集成到控制单元中且经由例如柔性、平缓或印刷电缆的总线线路连接到电极。
束带可进一步包括用于将其固持在患者的躯体的正面的构件。这种构件可以是出于安全性的快速释放固定件或允许调整身体体型或身材且用于将束带固定在患者上的弹性带。替代地,束带可包括可绕大腿和/或肩部和/或颈部固定以用于将束带和控制单元固定在患者上围绕的背带。在此类实施例中,控制单元可直接附接到背带且从背带拆卸。在替代实施例中,装置可包括围兜、支架、悬带或绕颈系带以将束带和控制单元支撑在患者上。在又一实施例中,控制单元和电极可直接附接到包括可吸收(尿布或尿布类)材料的尿布或短裤。束带可在背面更宽且在正面更窄以确保患者的呼吸不受限制。
为了检测vur,装置/系统可在排尿期间以及排尿之前或之后测量阻抗变化(以获取基线测量值)。对于患有vur的患者,在排尿期间,尿液反流的体积可与所流经尿液的体积成比例。在排尿期间,可能需要尿液的预限定体积以检测vur。装置/系统可包括排尿传感器(例如润湿指示器、和/或湿度或温度传感器)。排尿传感器(例如润湿指示器和湿度或温度传感器)的功能是在预限定体积的尿液已流经时向人发信并提供在排尿已开始和结束时以及在将接收到数据并且分析数据时的时间点和信号。这对于幼龄儿童和可能未经过厕所训练的婴儿来说是尤其重要的,在这些患者中,排尿是不可预测的且有时所流经尿液的体积极小。其结果是,所述系统可能需要记录且不断收集数据长达四个小时以在流经充足体积的尿液的情况下捕获反流事件。在较长时间段内收集数据要求控制单元含有更大电池电力和更高数据存储容量。这可转换为更大且更重的电池和存储介质且因此更大的控制单元。并入有传感器(例如润湿指示器和湿度或温度)的一些优点包含系统尽可能保持较轻且紧密的,以使得其对于儿童佩戴是可拆卸且舒适的,需要更少的数据分析,减小信号处理时间——如果呈现数小时的数据,那么用户或处理器不知道排尿何时发生且可能需要分析大量的数据。可将来自传感器的信号输入到反馈回路中且用于激活控制单元以开始测量排尿何时开始并在排尿完成之后停止测量。这允许装置/系统仅在排尿期间测量阻抗变化和基线且产生更轻更紧密的控制单元和更高效的数据处理。传感器还可用于在显著体积的尿液已流经时和/或在排尿开始或结束时发射信号。所述信号可以是噪声或光或显示在控制单元或显示单元上的颜色变化。
如果用户察觉到已流经充足体积的尿液,那么它们将不需要去除装置,其中过早地去除装置可能扰乱电极位置且影响结果的精确性。
有时,成人尿布和婴儿尿布都已并入有润湿指示器。一般来说,润湿指示器在与大量的液体接触时显示颜色变化。然而,对于本发明的装置/系统,这种指示器将与特定量的液体相关,所述指示器将指示可检测到反流事件(如果其已发生)。这可通过在与已知吸收性的吸收剂芯接触的底片材料的内侧上将润湿指示器应用到热熔性粘合剂,从而在存在特定体积的流体时激活指示器来实现。
湿度和温度传感器也已并入到成人和婴儿尿布中。湿度或温度传感器可在液体与传感器接触时经受生理或化学变化。这转而可导致可由控制单元检测到的电信号的变化。控制单元可预编程以辨识电子信号从而在事件之前激活系统且在事件之后去激活系统。可能合适的传感器包含阻抗传感器、电容性传感器、压电传感器或温度传感器,其中的全部都是市售的。
装置/系统还可包括移动传感器,例如并入到控制单元中的适用于指示患者的过量移动的振荡器,所述过量移动可产生噪声且可影响结果的精确性。移动传感器可发射噪声或显示光以指示显著移动发生的时间。
移动传感器可用于与如上文所描述的排尿传感器结合且移动传感器可仅在液体与湿度或温度传感器接触时激活。当收集数据用于分析时,这将仅在排尿期间或恰好在排尿之后发生过量移动时提供警报。
为了检测vur,患者上的电极的位置必须尽可能保持静止,具体地说,在排尿期间且在排尿前或排尿后大致10到40秒,适当地20到40秒(以获取基线测量值)。最小化移动以减小系统中可导致测量误差的噪声至关重要。并入移动传感器的目的在于向操作装置/系统的人发信在测量期间过量移动发生的时间以及在这种情况下数据可能不适用于分析。幼龄儿童和婴儿通常是不可预测的且难以保持静止。如果存在电极带的过量移动,那么患者噪声可引入到信号中,这可导致影响结果的精确性的测量误差。
移动传感器可使用可包含加速计、陀螺仪或振荡器的市售组件来测量过量移动。
阻抗测量模块、控制单元可使用与gaggero等人相同的配置,所述配置包括电流源、信号测量电路和信号发生器电路。信号发生器电路可连接到电流源且可包括波形合成数模转换器(dac)、滤波器和放大器。控制单元功能性可使用现场可编程门阵列(fpga)来实施。信号测量电路适于测量有源电子芯片对之间的电压且可包括放大器、滤波器和模数转换器(adc)。替代地,微控制器可用于放置fpga。
控制单元在并未主动地测量时可与束带分离。当控制单元与束带分离时,其可连接到显示单元以在监测之前对装置/系统进行编程或在监测之后提取数据。可将频率、电流注入幅值和帧率编程到装置/系统中。由控制单元供应的频率可在1到200khz,优选地50到150khz,更优选地50到100khz的范围内。由电子控制单元供应的注入电流可在0.1与10ma,优选地1到7ma,更优选地1到4ma的范围内。注入模式可在0到15,更优选地0或1的范围内。图像率可在1到50帧每秒的范围内。选定参数以优化用于监测尿液的系统的灵敏度,且所述参数可取决于患者bmi而变化。这些值保持在安全患者辅助电流内。较低电流应用于较低频率以维持患者的安全。
控制单元可由便携式可再充电电池供电,例如轻质锂聚合物电池等等,或电力可从主电源供应或任选地经由usb充电器或经由感应供应。控制单元可完全地包围电池和电流源、信号产生和信号测量电路。壳体可设计成滑件并通过磁性锁定或双按钮锁定控制单元的任一侧而锁定到外壳中。所述壳体可以是正方形、长椭圆形或半球形。可将控制单元设计成锁定电极带。
合适的电池组、连接电缆、处理器和观察监测器将根据本文中的描述由本领域中的技术人员理解。
系统可另外包括用户接口或显示单元。在控制单元与可穿戴单元分离时,用户接口或显示单元优选地可连接到控制单元以在监测之前对装置/系统进行编程或在采集到测量值之前和之后向处理器传达数据。可将处理器集成到显示单元中或连接到显示单元,所述显示单元可包括经由以太网、无线、蓝牙或usb等等连接到控制单元的智能手机、平板计算机、膝上型计算机或个人计算机等等。替代地,可将显示单元和/或处理器中的全部或部分集成到控制单元中。结果(例如尿液体积变化)可直接显示在控制单元或显示单元上。
处理器可并入有软件,所述软件可上传到显示单元以允许用户在采集到测量值之前选择用于阻抗测量模块的输入参数(例如频率、电流和图像率)。在采集到测量值之后,软件可分析并向用户显示结果。输出(已处理)数据可包括显示阻抗变化的曲线。这些阻抗变化可进一步处理且用于构建算法中的信号模式或重构图像。
可将系统设计成利用现有生物电阻抗技术,例如用于阻抗呼吸描记法以产生曲线的生物电阻抗技术。生物电阻抗是一种检测阻抗变化的非侵入式成像技术。将电极置于与皮肤接触且电流施加在至少2个电极之间且所得电压在相同或不同电极之间测量。生物电阻抗可用于在生物阻抗的变化涉及肾脏和或输尿管中的尿液的体积及汇集时检测并监测vur。生物电阻抗系统通常包括与患者的皮肤接触的2到4个电极。
优选地,可将系统设计成利用电阻抗断层成像(eit)以得到跨平面的阻抗分布。系统包含围绕平面与皮肤接触的多个电极。将电流施加在电极对之间且所得电压从电极对的不同集合测量。记录并分析电压测量值分布以重构阻抗分布的图像。
一种典型eit系统包括以帧操作的8到32个电极。在每一帧期间,系统注入具有正确幅值的电流,测量电压且控制每一电极中的所有开关。举例来说,如果使用16个电极,那么每一帧(即测量值的每一完整集合)由16×16个电压测量值组成。
作为一个实例,可首先通过电极对(16,1)注入电流,且通过全部电极对测量所得电压差。一旦电压被测量,就通过将电流注入相邻电极对中且在所有电极对中再次测量,直到再次到达用于注入电流的原始位置来重复所述过程。所有这些测量值构成数据帧,且产生跨平面的电压分布。eit系统的电流、频率、帧率和注入模式设置可在测量之前限定,这些设置可保持不变直到测量结束为止。
在本发明的装置/系统中,所测量电压的变化用于重构跨肾脏或输尿管的平面的阻抗分布图像,所述阻抗分布图像反映输尿管、膀胱和/或肾脏中的尿液体积的变化。
在处理器中采用算法可用于产生曲线和重构图像;检测、计算和量化vur的强度;通知可与患者一起存在的医疗保健提供者或远程监测儿童。可将这种分析并入到处理器软件中,所述处理器软件设计成部署在运行不同操作系统的多种台式和移动计算系统上。
eit系统的处理器可用于产生在电极的平面中的阻抗分布的重构图像。这可使用由adler等人2009年描述的线性重构算法来进行。一种平均阻抗分布图像可在基线(没有排尿)上产生,且平均或积分阻抗分布图像在排尿时间内产生。对被限定为平均重构阻抗图像(ium)关于基线重构阻抗图像(ibm)的变化的阻抗变化进行评估以确定患者是否患有vur。另外,包含最大阻抗变化及最大平均比率的度量值可从重构图像或原始数据提取且随时间绘制以补充且显示阻抗分布图像的支持数据。
本发明还提供一种用于检测从膀胱流动到肾脏的尿液的方法,所述方法包括记录发生在输尿管、膀胱和/或肾脏中的阻抗变化,所述阻抗变化在阻抗变化由生物电阻抗和eit技术检测到时指示输尿管、膀胱和/或肾脏中的尿液体积的变化。
在所述方法中,尿液体积的变化优选地可通过在排尿之前、排尿期间以及直接在排尿之后记录的测量值来识别。优选地处理所测量电压的变化以构建指示输尿管、膀胱和/或肾脏中的尿液体积的变化的重构阻抗分布图像中的图案。
所关注的时间点期间(例如排尿期间)的电压测量值的变化可与参考值(基线测量值)进行比较,其中排尿期间的测量值可与排尿之前和之后的测量值进行比较,以产生无vur或中度到重度vur(iii级到v级vur)的指示。
附图说明
图1是包括阻抗测量模块的系统的框图,所述阻抗测量模块可以是电极带、总线线路、控制单元、电池、显示单元和连接电缆以及可并入到显示单元中的处理器。
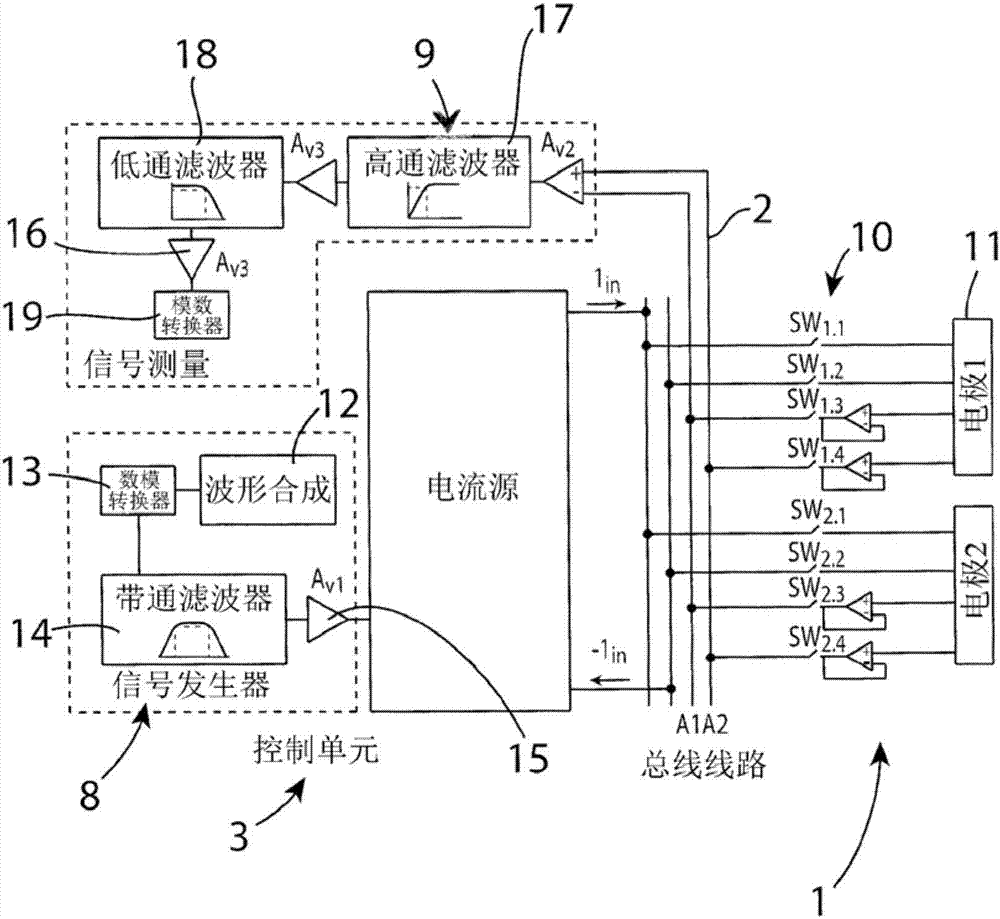
图2是阻抗测量模块和可用于产生并测量控制单元的信号的步骤的图式,所述控制单元包括电流源、信号发生器和信号测量系统、连接总线线路以及包括连接到电极的有源电子芯片的电极带。
图3a是展示肾脏、输尿管和膀胱的目标解剖结构的概观。
图3b展示定位在肾脏的肾/骨盆区域上方的电极。这是用于监测vur的初级目标区域。
图4展示有源电子芯片(c)在2层材料之间的电极带中的可能布置。外部层(d)用以保护有源电子芯片且内部层(b)含有导电材料(a)部分。
图5a展示具有以半圆布置分布的8个有源电子芯片的电极带的一个实施例。所述束带背面比正面更厚,在电子芯片上方具有内部织物且具有用于在正面紧固的叠加velcro条带。
图5b是图5a的实施例的透视图。
图6a展示具有16个均匀分布的电极和用于紧固束带的可调节带的电极带的一实施例。所述束带具有用于在正面紧固的可调节velcro条带和覆盖电极的内部织物。
图6b是图6a的实施例的透视图。
图7a是具有长椭圆形控制单元和外壳的一实施例的透视图。
图7b是针对测量而附接的图7a的实施例的透视图。
图8是设计成锁定电极带的控制单元的一实施例的透视图。
图9是具有与图8a和8b相同的锁定机构的替代形状控制单元的一实施例的透视图。
图10a是正方形控制单元的一实施例的前向透视图,所述正方形控制单元可通过控制单元中的固定环连接到束带。
图10b是正方形控制单元的一实施例的后向透视图,所述正方形控制单元可通过控制单元中的固定环连接到束带。
图11a是竖直定位的控制单元的一实施例的透视图,其中所述控制单元在每一侧上连接到束带和来自上方的用于支撑的颈部背带。
图11b是本发明的一实施例,其中控制单元附接到束带和用于围绕颈部支撑的背带。图像展示由患者穿戴的装置。
图12a是本发明的一实施例的透视图,其中控制单元是半球形的且插入到背心中。图12b是由患者穿戴的12a中的本发明的一实施例。
图13a是电极带和控制单元的一实施例的透视图,其中所述控制单元插入到围兜中且连接到束带。图13b是由患者穿戴的13a中的本发明的一实施例。
图14a是本发明的一实施例,其中控制单元是长椭圆形的且成角度地附接到束带的正面和背面以使得控制单元横跨患者的胸腔定位。图14b是由患者穿戴的14a中的本发明的一实施例。
图15a是本发明的一实施例,其中束带和控制单元并入到短裤中。图15b是在由患者穿戴时图15a的实施例。
图16是使用肾脏的体外台式模型产生的曲线。所述曲线说明最大阻抗变化和最大平均比率、电阻率指数和平均电阻率。
图17(a)到(e)详述用于测量和处理阻抗分布图像以建立尿液是否在特定时间段行进到肾脏的步骤。
图18(a)到(f)表示用于处理阻抗分布图像的步骤和收集数据的时段,即膀胱充满的时间(例如恰好在排尿之前),在低于肾脏的升高压力导致vur的时间段期间(例如在排尿期间)以及在膀胱排空之后。
图19(a)到(e)表示当在15秒内注入10ml的液体时在猪科模型的临床前研究期间观察到的变化。所述曲线显示局部导电率变化,这是在一定时段期间所关注区域中的平均阻抗。
具体实施方式
本发明的装置/系统的阻抗测量模块和处理器图解展示于图1中,包括电极带(1)、总线线路(2)、控制单元(3)、电池(4)、显示单元(5)以及在阻抗测量模块与处理器之间的连接接口(6)。控制单元(3)通过usb、无线、蓝牙或以太网连接附接到显示单元(5)。
图2图解展示控制单元(3)的电路的电子装置,所述控制单元包括电流源(7)、信号发生器(8)和信号测量系统(9)、连接总线线路(2)以及包括连接到电极(11)的有源电子电路(10)的电极带(1)。通常,本发明的电极带(1)可含有8到32个电极(11)。在此图中,用于仅两个电极(11)的电路作为实例提供,其中其余电极可具有相同电路。每一有源电子电路(10)含有电压缓冲器、开关和用以调节开关的状态的微处理器。控制单元(3)包括电流源(7)、信号测量电路(9)和信号产生电路(8)。信号产生电路(8)连接到电流源(7)且包括波形合成(12)、数模转换器(dac)(13)、带通滤波器(14)和电压放大器(15)。信号测量电路(9)测量有源电子电路对之间的电压且包括电压放大器(16)、低通滤波器(17)和高通滤波器(18)以及模数(adc)转换器(19)。
图3a是展示肾脏、输尿管和膀胱的目标解剖结构的概观。在使用中,电极带(1)将邻近目标解剖结构放置以检测尿液的体积的变化。超声成像或x射线可用于识别输尿管、膀胱和/或肾脏的准确位置以确保恰当地定位装置。图3b展示定位在肾脏的肾盂区域上方的电极(11)。这是用于监测vur的初级目标区域。在vur期间,尿液通过输尿管行进到肾脏进入肾脏的肾盂区域。
如图4中所展示,电极带(1)中的有源电子电路(10)是可定位于两层材料之间的配置的实例。外部层(20)保护有源电子芯片(10)且内部层(21)含有导电材料部分。材料的外部层(20)是防水的以防止水进入到电子组件中。内部层(21)可并入有粘合剂或高摩擦材料(例如乙烯或硅酮)以防止移动且设计成使皮肤刺激最小化。内部层(21)包括非导电材料部分之间的导电材料部分,所述非导电材料部分将与皮肤和有源电子芯片(10)接触。有源电子芯片(10)通过例如柔性扁平电缆或柔性印刷电缆(22)的电缆彼此连接。
图5a和5b展示具有分布在半圆形布置中的8个电极(11)的电极带(1)的一个实施例。束带(1)在背面比在正面更厚,在电极(11)上方具有内部织物层且具有用于在正面紧固的叠加velcro条带(23)。在背部的较厚部分提供额外支撑,且在正面的较薄部分防止对呼吸的任何限制。
图6a和6b展示具有16个平均分布的电极(11)和用于紧固束带(1)的可调节带(24)的电极带(1)的替代实施例。束带(1)具有用于在正面紧固的可调节velcro条带和覆盖电极(11)的内部织物。
图7a和7b展示具有长椭圆形控制单元(3)和外壳(25)的一实施例的透视图。所述图将外壳(25)和控制单元(3)展示为两个分离组件。控制单元(3)在并未主动地测量时与外壳(25)分离。外壳(25)连接到电极带(1)且提供控制单元(3)到束带(1)的电触点。控制单元(3)可在并未主动地监测患者时与外壳(25)分离,且可连接到显示单元(5)以在监测之前对装置/系统进行编程或在监测之后提取数据。控制单元(3)可由例如轻质锂聚合物电池的便携式可再充电电池供电。壳体可设计成滑件并通过双按钮锁定控制单元(3)的任一侧锁定到外壳(25)中。
图8展示设计成锁定电极带(1)的控制单元(3)的一实施例。将束带(1)和控制单元(3)展示为两个分离组件。束带(1)还包括可调节velcro带(23)。
图9展示具有与图8相同的锁定机构和控制单元(3)配置的替代成形控制单元(3)的一实施例。
图10a展示正方形控制单元(3)的一实施例,所述正方形控制单元可通过控制单元(3)中的固定环(26)连接到束带(1)。正方形形状控制单元(3)在任何一个方向上减小其大小以防止对患者的移动的任何限制。图11a展示竖直定位的控制单元(3),所述控制单元在每一侧上连接到的束带(1)和来自上方的用于支撑的颈部背带(27)。控制单元(3)在每一侧上连接到束带(1)和来自上方的用于支撑的颈部背带。颈部带可提供控制单元(3)的支撑和平衡并将所述控制单元定位在束带(1)远端,从而潜在地减小对电极接触的干扰。
图11b展示本发明的一实施例,其中控制单元(3)附接到束带(1)和用于围绕颈部支撑的背带(27),如由患者所穿戴。
图12a和12b展示本发明的一实施例,其中控制单元(3)是半球形的且插入到背心(28)中。电极带(1)集成到具有围绕肩膀的支撑带(29)的背心(28)中以维持电极带(1)的位置并支撑控制单元(3)。电极带(1)连接到背心(28)的底部。可将控制单元(3)放置在胸腔的中央或背部上。背心(28)将提供控制单元(3)的支撑和平衡并将所述控制单元定位在束带(1)远端,从而潜在地减小对电极接触的干扰。
图13a和13b展示电极带(1)和控制单元(3)的一实施例,其中控制单元(3)插入到围兜(30)中且连接到束带(1)。将围兜(30)围绕患者的颈部放置以支撑束带(1)。控制单元(3)具有单个连接且放置在围兜(30)的口袋(31)中。围兜(30)为控制单元(3)提供支撑和平衡并将所述控制单元定位在束带(1)远端,从而潜在地减小对电极接触的干扰。
图14a和14b展示本发明的一实施例,其中控制单元(3)是长椭圆形的且成角度地附接到束带(1)的正面和背面,以使得控制单元(3)横跨患者的胸腔定位。带(32)穿过控制单元(3)且横跨身体对角地围绕患者的一个肩膀。这支撑且平衡控制单元(3)使其远离束带(1),从而防止对电极触点的干扰。
图15a和15b展示本发明的一实施例,其中束带(1)和控制单元(3)并入到短裤(33)中。短裤包括可吸收材料或可穿戴在尿布上面以允许在不移除短裤(33)的情况下排尿。短裤(33)中存在口袋(34)以固持控制单元(3)。这将支撑且平衡控制单元(3)使其远离束带(1),从而防止对电极接触的干扰。电极带(1)由内环(35)围绕腰带支撑以固定电极带(1)。
图17展示系统用以使用eit来检测肾脏或输尿管中的尿液的步骤。所述步骤涉及围绕在肾脏的水平面处的身体平面恰当地定位电极。使用阻抗测量模块以在一段时间内收集阻抗测量值。处理器随后从阻抗测量模块接收阻抗测量值并分析测量值以产生一系列阻抗分布图像(7),所述阻抗分布图像在使用阻抗测量模块的时段期间每秒(至少)收集一次。每一阻抗分布图像对应于液体在特定时间点流动到肾脏的体积。收集并处理(7)阻抗分布图像且输出平均阻抗分布图像(8)以提供发生在基线和排尿期间的平均变化。对排尿期间的平均阻抗分布图像进行滤波(9)并与在排尿之前或之后获取的基线图像进行比较。显示单元(10)向用户提供结果,这个信息用于指示vur是否正在发生。
图18进一步展示在测量并分析图像时的步骤和时间帧。平均阻抗分布图像可在排尿(15)之前(11)、期间(12)以及之后(13)获得。在时间0s(t0)处——此当膀胱充满(14)且患者将需要排尿时。t0记录为测量值的时间戳。装置/系统可在这之前或在此时激活。一旦排尿开始(15),就记录时间戳t1以表示排尿的开始。输出在t0与t1之间获得的阻抗分布图像的平均值(11)。
时间戳t2表示排尿结束,输出t1与t2之间的平均阻抗分布图像(12)。时间戳t3在测量结束时建立。输出t2与t3之间的平均eit阻抗分布图像(13)。比较图像(11,12,13)以确定尿液是否朝向肾脏行进。在未经过厕所训练的儿童中,医生可检查膀胱是否充满(例如使用超声波),可将外部压力放置在膀胱上,模拟膀胱收缩(例如排尿)。
图19表示来自临床前研究的结果。在临床前研究期间,猪科动物模型用于使用开放式反向输尿管输注来模拟vur。反流体积与膀胱容量之间的相关性用于建立反流体积。将这估计为10%与15%之间的膀胱容量。可使用(年龄+2)×30ml来估计膀胱体积。其结果是,实际考虑体积在8与30ml之间以模拟vur。根据用于研究的适当验收准则,基于最小平均vur体积来选定10ml的体积(儿童年龄6个月到2岁)。阻抗分布图像展示于图中。在输注到肾脏中之前以及输注到肾脏中期间,在不同时间点采集一系列图像。所述曲线显示区域导电率随时间的变化。
本发明的电极带(1)的所有实施例都含有电极(11)。
电极(11)并不彼此接触且包括将与皮肤接触的高导电材料(8到105ohm/sq的平均表面电阻率)的离散部分。电极(11)将与皮肤接触。电极布置包括在邻近所关注区域(即患者的膀胱、输尿管或肾脏)的身体表面上的多个电极(11)。电极(11)处于直接导电接触或电容耦合到身体表面。供用于本发明的合适的电极(10)材料包含镀金铜,附接到电极电路的不锈钢或导电纺织电极也可为合适的。电极材料可以是导电微纤维非编织超材料或吡咯导电聚合物。可穿戴单元可包括直接固定到身体以用于与在皮肤与电极之间的非导电溶液或凝胶层这类(例如超声凝胶或水)导电接触以减小皮肤的阻抗的电极。除凝胶层之外,在内表面上与患者的皮肤接触的粘合剂或高摩擦材料(例如硅酮、橡胶或乙烯)也可用于增加皮肤与束带之间的摩擦系数以帮助将束带固定在适当位置。
一种典型eit系统包括以帧操作的8到32个电极。在每一帧期间,系统注入具有正确幅值的电流,测量电压且控制每一电极中的所有开关。举例来说,如果使用16个电极,那么每一帧(即测量值的每一完整集合)由16×16个电压测量值组成。
作为一个实例,可首先通过电极对(16,1)注入电流,且通过全部电极对测量所得电压差。一旦电压被测量,就通过将电流注入相邻电极对中且在所有电极对中再次测量,直到再次到达用于注入电流的原始位置来重复所述过程。所有这些测量值构成数据帧,且产生跨平面的电压分布。
阻抗测量模块可包括具有集成电子装置(例如芯片)的电极,所述电子装置设计成尽可能接近患者以测量并缓冲电压以最小化可由于在高阻抗线路上的信号的模拟传输而出现的问题。开关、缓冲器和微处理器可用于控制在电极对之间的电流注入模式。这个电路描绘于图2中。有源电子电路(芯片)(10)。其中使用芯片,每一有源电子芯片具有用以多路复用接收到并传输到控制单元的信号的开关。举例来说,所述系统可具有用于注入并吸收电流的两个开关(分别是sw1,1和sw1,2)和用于缓冲电压并经由总线模拟线路a1和a2将电压传输到控制单元的两个开关(sw1,3和sw1,4)(参见图2中的电极1)。
电压缓冲器用于将电压从具有高输出阻抗水平的第一电路传送到具有低输入阻抗水平的第二电路。在每一测量期间,两个电极变为有源的。工作电极中的每一个将所缓冲信号传输到两个总线线路(a1或a2)中的一个。线路a1与a2之间的电压差由控制单元计算且模拟信号转换成数字信号。
有源电子芯片还可包括用以控制其状态(即在每一时刻哪些开关断开或闭合)的微处理器或只读存储器(rom)以及用以存储具有有源电子芯片的所有状态的表的存储器。另外,可要求表指针指出电流状态。每一有源电子芯片具有完全相同的表,但对于每一帧来说,指针在表中的不同位置处开始。在时钟脉冲从控制单元的数字部分发送(通过同步线路)时,状态指针变化,从而将对应配置应用到开关。当状态指针到达表的末尾时,其循环回到表的开始。因为指针开始于不同位置,所以这种实施方案要求每一有源电子芯片单独编程。
对于最终产品,每一有源电子芯片包括缓冲器、开关和实施于电路板中的微处理器/rom,这可布置在单个印刷电路板(pcb)中以最小化系统/装置的大小。有源电子芯片可随后通过焊接或类似方法直接附接到电极材料。
整个系统由阻抗测量模块控制单元控制,中央系统负责电极管理、信号采集、电流产生和与用户通信。
如图2中所描绘的信号采集的整个过程基于gaggero等人遵循的方法:
电流源可包括运算放大器或跨导放大器,实例包含耦合有变压器的浮动电流源、运算跨导放大器电流源、供应电流感测电流源、三相运算放大器电流源或howland电流源。
肾脏内的阻抗可从给定时间点处在邻近肾脏或输尿管的身体表面处的电极之间采集到的电压测量值来推断。
装置/系统可在排尿之前、排尿期间以及排尿之后采集测量值。排尿之前和或在排尿之后的电压读数用作基线测量值且从排尿期间的读数减去所述电压读数,从而确定在肾脏或输尿管中是否已发生电压的增加且因此阻抗的增加。如果阻抗的增加已发生,那么患者有可能罹患vur。替代地,如果在排尿之后残余尿液从肾脏流动到膀胱中且改变膀胱中的阻抗,那么患者可能罹患vur。类似地,膀胱内的阻抗可从在给定时间点处,在一个数据帧内在身体的表面处的所有有源电极对之间采集到的电压测量值来推断。处理器可使用软件算法和分类器以分析从装置/系统的测量模块所获取的数据。算法可用于使由阻抗测量模块产生的结果的精确性优化,用于检测输尿管、膀胱和/或肾脏中的尿液的阻抗变化及体积变化。替代地,显示单元可并入到系统中作为系统的便携式实施例。存在一定数量的电阻抗断层成像装置可供用于商业用途。这些装置通常用于监测危重症患者的肺脏功能。这些装置的结果显示为实时图像和从这些图像中导出的阻抗变化波形以及数值参数。
来自重构图像的图形输出(下文详述)为用户提供优化所关注区域中的灵敏度和特异性的额外信息。包含最大阻抗变化和最大平均比率的度量值可从阻抗分布图像提取且随时间绘制。
所关注区域的最大阻抗变化描述在分布图像内的所关注的所选区域(例如在肾脏的位置)随时间的最大阻抗响应。线性增加表示所关注区域中的尿液体积的增加。这个度量值可提供所关注区域中的较小阻抗变化的改良检测。
最大平均比率描述图像中的最大响应除以图像中的平均响应。度量值可提供与在所关注区域与重构图像中的背景之间的对比度相关的更详细的信息。提取例如所选关注区域(roi)(肾脏周围)中的最大导电率变化和最大平均比率的度量值以分析导电率变化趋势和图像质量。确切地说,最大平均比率可用于检测具有显著伪影的图像,所述图像可从分析中舍弃——例如如果roi中的导电率变化随时间的推移而增大,但最大平均比率低于一些帧中的某一阈值,那么这意味着在那些帧中肾脏中的导电率变化并不显著地高于其它处的导电率变化,这意味着那些图像有可能含有显著伪影且应舍弃。
以下详述电压测量值可如何由处理器分析:随时间的电压测量值转移到电极的平面中的阻抗分布的重构图像中。这可使用由adler等人2009年描述的线性重构算法来进行。在基线(没有排尿)处产生平均阻抗分布图像且在排尿期间将阻抗分布图像收集(大致1个图像每秒)为一系列重构图像(iu1、iu2、iu3等)。这一系列的阻抗变化(在排尿期间)可平均化或在排尿时间内整合以产生单个平均重构阻抗图像(ium)。可对平均图像(ium)、重构图像(iu1、iu2、iu3等)的系列和平均基线重构阻抗图像(ibm)进行滤波以去除图像伪影且分离肾脏区域。对图像的系列(iu1、iu2、iu3等)进行视觉分析以确定在排尿期间,肾脏周围的区域中的阻抗是否随时间增大。对被限定为平均重构阻抗图像(ium)关于基线重构阻抗图像(ibm)的变化的阻抗变化进行评估以确定患者是否患有vur。对图像进行评级以确定图像的质量并指示患者患有vur的概率。等级3、4或5指示显著体积的尿液行进到肾脏且指示患者患有vur。以下是所使用的评级和应用到重构图像的准则的描述。
以下方法可用于对图像进行滤波以去除伪影且分离肾脏周围的区域以改良结果的精确性:
(i)获取先验——对肾脏的位置的先验了解。这通过使用例如对不同年龄的儿童的ct扫描的历史数据来进行且使肾脏的位置与bmi相关联;(ii)图像处理,这可包含增大图像分辨率(从64×64个像素到256×256个像素)因此其变得较低‘像素化’或(iii)
使用模糊核
排尿期间的“平均阻抗分布图像”用于识别被限定为“所关注区域”的每一肾脏的位置。产生高斯(gaussian)模糊核以复制每一图像的所关注区域,根据高斯模糊式:
x和y表示每一像素的坐标,xkidney和ykidney表示在所关注区域内的中央位置,且σ是表示所关注区域的大小的高斯分布的标准差。覆叠表示高斯模糊核(对于每一肾脏有一个——“所关注区域”)的两个图像以获取表示每一肾脏的具有两个核的单个组合图像。将组合图像中的每一像素的值按比例从0和1缩放且所述值表示“滤波图像”。“滤波图像”乘以“平均阻抗分布图像”(以滤除图像伪影并针对每一输注分离肾脏区域)。这种方法也可对所述系列中的每一阻抗分布图像实施。
在当前实践下,呈现有uti的大体上所有儿童将涉及vcug成像以检测vur。如果本发明的装置/系统用于排除不患有vur(70%)的那些患者和患有轻度vur(22%)的那些患者,那么总计92%的先前已经考虑vcug成像的患者将并不需要涉及。
尽管在本文中参考特定实施例描述本发明,但本发明并不意图限于所展示的细节。相反,可以在权利要求书的等效物的范畴以及范围内且在不脱离本发明的情况下进行细节上的各种修改。
当在本文中参考本发明使用时,词语“包括(comprises/comprising)”和词语“具有/包含”用于指定所陈述的特征、整体、步骤或组件的存在,但是不排除一或多个其它特征、整体、步骤、组件或其群组的存在或添加。
应了解,为了清楚起见而在分开的实施例的情况下描述的本发明的某些特征还可以组合形式提供于单个实施例中。相反地,为简洁起见而在一个单一实施例的背景下描述的本发明的不同特征还可以分开地或以任何适合的子组合形式提供。
参考案
adler,a等人《使用电阻抗断层成像监测肺气和液体体积的变化(monitoringchangesinlungairandliquidvolumeswithelectricalimpedancetomography)》,应用生理学杂志(journalofappliedphysiology)83.5(1997年):1762-1767。
gaggeropo、adlera、brunnerjseitzp.《基于有源电极的电阻抗断层成像系统(electricalimpedancetomographysystembasedonactiveelectrodes)》,生理测量(physiolmeas.)2012年;33(5):831-47。
- 还没有人留言评论。精彩留言会获得点赞!