MPLA在制备电离辐射致肠道损伤防治药物中的应用的制作方法
本发明涉及医药技术领域,具体地说,是mpla(吡喃葡糖苷脂质a)在制备电离辐射致肠道损伤防治药物方面的应用。
背景技术:
随着核科学技术的广泛应用,战时核辐射、核恐怖袭击、平时核反应堆事故及临床上恶性肿瘤放疗等都可导致机体电离辐射损伤。机体各组织和器官损伤效应的严重程度与各组织的辐射敏感性密切相关。肠上皮细胞属高度辐射敏感组织,是辐射损伤的主要靶点之一,尤其是肠隐窝干细胞。电离辐射可以快速诱导小肠隐窝细胞发生凋亡、变性和坏死等病理改变。使肠隐窝干细胞及其干细胞龛遭受严重破坏,肠道干细胞分化为各类成熟细胞的功能受阻,造成肠隐窝-绒毛新陈代谢受到阻碍,肠绒毛上皮缺乏更新来源,肠绒毛上皮细胞广泛性脱落或坏死,上皮结构的完整性遭到破坏,肠道粘膜完整性丢失,机械屏障作用减弱,肠道免疫屏障遭到破坏,从而引起严重的胃肠道出血、呕吐、腹泻、菌血症、败血症和电解质紊乱等,形成胃肠综合症,在短期内(动物3-5天,人5-7天)导致死亡。对肠道放射损伤和肠型放射病的防治,国内外不少单位虽然曾开展过不少研究,包括干细胞移植、组织修复工程、细胞因子、化学药物、综合治疗等等,至今仍没有找到理想的预防或治疗药物。目前国内外对肠道放射损伤和肠型放射病仍缺乏有效的防治技术手段,成为放射医学领域迫切需求研究解决的关键难题之一。近年来研究发现激活toll样受体(tlrs)可促进受照肠上皮细胞增殖和肠道修复等,具有显著的辐射防治作用,尤其tlr4在这方面扮演着重要的角色。然而tlr4传统激动剂lps的毒性严重制约了其实际应用,亟需开展减毒增效探索。
mpla(吡喃葡糖苷脂质a,monophosphoryllipida)是沙门氏菌r595的突变体,是将lps(r)-3-羟基十四烷酰基和1-磷酸盐基团经过连续水解后得到的解毒化学衍生物,它的lipida部分可以与tlr4结合,mpla高效激活tlr4及其下游信号通路,诱导g-csf,il-12,ifn等细胞因子表达。mpla作为tlr4靶向配体,不仅在前期基础毒理学分析中证明其毒性低,而且目前将它作为佐剂在疫苗研发领域也得到广泛的应用,已被批准使用或已进入三期临床试验的有:乙型肝炎疫苗fendrix(hepatitisb),宫颈癌疫苗cervarix(humanpapillomavirus-16andhumanpapillomavirus-18),疟疾疫苗rts,s(malaria),过敏原产品pollinexquattro等等。文献报道mpla在欧洲和美国有超过300,000人次的临床试验未发现明显毒副作用。(schülkes,flaczyka,vogell,gaudenzion,angersi,
目前对于电离辐射致肠道损伤防护药物研究多处于临床前阶段,虽然有些药物放射防护效果,但存在着包括作用浓度高、活性偏低及存在明显的毒副作用,从而限制了临床应用,寻找无毒或低毒、高效的电离辐射致肠道损伤防护药物一直是医药界的追求热点。
mpla作为tlr4的激动剂,对肠道辐射损伤的防治作用显著,且具有明确的低毒特性。现有技术中未见有mpla对肠道辐射损伤的防治作用的相关报道。
技术实现要素:
本发明的目的在于提供吡喃葡糖苷脂质a(monophosphoryllipida,以下简称mpla)的新用途,即在制备电离辐射致肠道损伤防治药物中的应用。
为达到上述发明目的,本发明的第一方面,提供mpla(吡喃葡糖苷脂质a)在制备电离辐射致肠道损伤防治药物中的应用。
所述的mpla(吡喃葡糖苷脂质a),其化学式为c96h181n2o22p.h3n。
进一步的,所述的mpla(吡喃葡糖苷脂质a)是tlr4的高效激活剂,是通过激活tlr4防治电离辐射致肠道损伤。
进一步的,所述的药物是口服药物。
进一步的,所述的mpla(吡喃葡糖苷脂质a)的给药剂量为1μg/0.1ml,且在电离辐射前12小时给药。
进一步的,所述电离辐射为60coγ射线照射。
本发明的第二方面,提供一种电离辐射致肠道损伤防治药物,其活性成分为mpla(吡喃葡糖苷脂质a)。
进一步的,所述的电离辐射致肠道损伤防治药物还包括药学上可接受的辅料。
本发明所提供的mpla(吡喃葡糖苷脂质a)作为制备电离辐射致肠道损伤防治药物具有以下优点:
1、毒副作用小,目前将mpla作为佐剂在疫苗研发领域得到了广泛应用,文献报道mpla在欧洲和美国有超过300,000人次的临床试验未发现明显毒副作用;
2、疗效显著,照射前12小时以1μg/0.1ml浓度的剂量给药,能够显著调高15gy60coγ射线腹部照射后小鼠存活时间;保护接受电离辐射小鼠肠道绒毛结构完整,促进小鼠肠道隐窝细胞增殖,大幅度减少电离辐射致小鼠肠道隐窝细胞凋亡;
3、本发明提供的mpla作为制备电离辐射致肠道损伤防治药物具有毒副作用小、肠道辐射损伤防治疗效显著、用药安全方便等优势,显示出mpla在防护电离辐射致肠损伤中的独特之处,旨在为肠道辐射损伤的防治探索更有效的救治新途径、新技术;而目前国内外对肠道放射损伤和肠型放射病仍缺乏有效的防治技术手段,成为放射医学领域迫切需求研究解决的关键难题之一。因此,mpla作为制备电离辐射致肠道损伤防治药物在我国医学领域具有广阔的应用前景。
附图说明
图1为本发明15gy60coγ射线腹部照射后照射对照组和照射前mpla给药组小鼠存活曲线对比图;
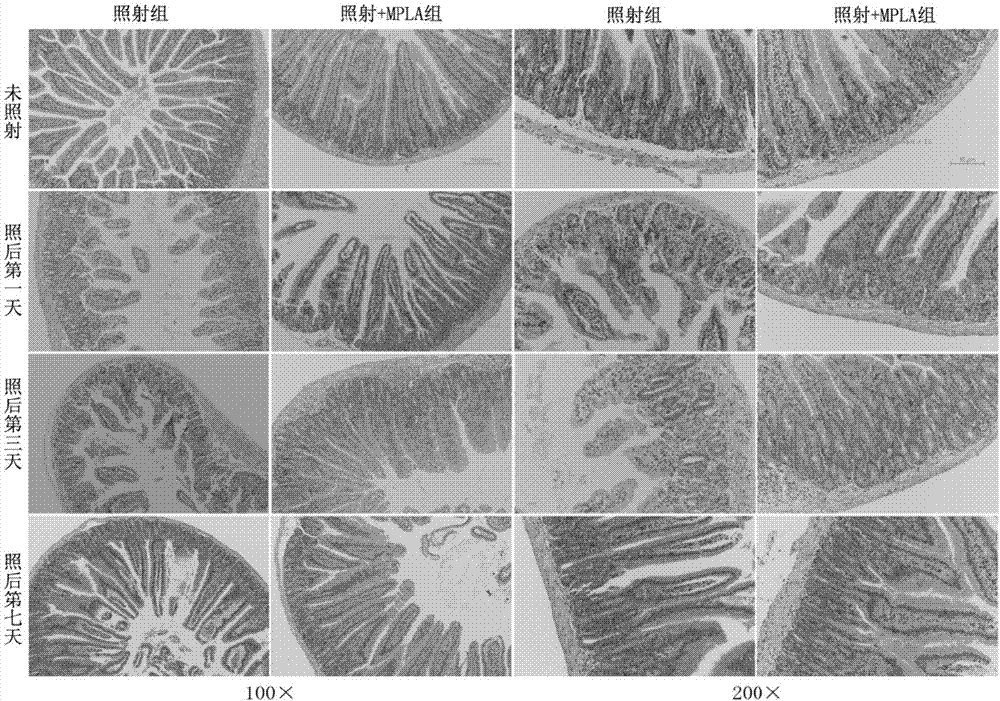
图2为本发明15gy60coγ射线腹部照射后照射对照组和照射前mpla给药组小鼠肠道绒毛和隐窝结构he切片对比图;
图3为本发明15gy60coγ射线腹部照射野生型小鼠和tlr4敲除小鼠后照射对照组和照射前mpla给药组小鼠隐窝细胞ki67+的改变;
图4为本发明15gy60coγ射线腹部照射野生型小鼠和tlr4敲除小鼠后照射对照组和照射前mpla给药组小鼠隐窝细胞γ-h2ax的改变。
图5为本发明15gy60coγ射线腹部照射野生型小鼠和tlr4敲除小鼠后照射对照组和照射前mpla给药组小鼠隐窝细胞的凋亡改变。
具体实施方式
下面结合实施例对本发明提供的具体实施方式作详细说明。
材料:野生型小鼠:中国科学院实验动物中心获得的6-8周龄的雌性c57bl/6小鼠。tlr4缺陷型小鼠:从南京大学模型动物研究中心获得。
mpla:购自美国invivogen公司。
其中,照射条件:辐射中心(第二军医大学海军医学院,中国上海)的60coγ射线照射。所有辐射动物接受单次剂量15gy,剂量率为1gy/min,均为腹部照射。
统计学处理:实施例的所有实验均重复3次以上,结果采用±s表示。采用sas统计软件对相关数据进行t检验,以p<0.05为有显著性差异。
实施例1:
首先建立辐射致肠道损伤小鼠模型,选用6-8周龄雌性c57bl/6小鼠,随机分为三组:照射组(15gy)8只和照射前12小时mpla给药组(15gy+mpla)8只及对照组8只;用60coγ射线对小鼠进行单次腹部照射,小鼠吸收剂量为15gy。通过胃内给药将mpla(0.1ml生理盐水中的1μg/小鼠)或生理盐水(0.1ml/小鼠)递送至相应组。在辐射暴露后每天早晨和晚上观察并记录小鼠(生理盐水或mpla预处理)30天。照射组小鼠在照射后1天即出现活动度显著下降,饮食量显著降低,而照射前mpla给药组在照射后小鼠活动度显著优于照射对照组。对小鼠存活天数进行分析,如附图1所示,mpla可有效延长照射后小鼠存活时间。因此,mpla可以改善受照小鼠的体征、延长受照小鼠存活时间。
实施例2:
(1)辐射致肠道损伤小鼠模型同实施例1;
(2)小鼠喂养:将小鼠置于25±1℃日常更换垫料的笼子中,保证水分及食物充足。
(3)选用6-8周龄雌性c57bl/6小鼠,随机分为两组:照射组(15gy)8只和照射前12小时mpla给药组(15gy+mpla)8只。通过胃内给药将mpla(0.1ml生理盐水中的1μg/小鼠)或生理盐水(0.1ml/小鼠)递送至相应组。在辐射暴露(1天,3天,7天)后的不同时间点,处死小鼠,取小肠组织,固定、蜡块包埋,切片后进行he染色。如附图2所示,电离辐射明显导致小鼠小肠绒毛断裂、脱落;照射前mpla给药组(照射+mpla)明显改善受照射后小鼠肠道结构,绒毛脱落减少。对绒毛长度、绒毛数量及隐窝数量进行定量分析,可明显看到照射前mpla给药组(照射+mpla)高于单纯腹部照射组。
实施例3:
(1)辐射致肠道损伤小鼠模型同实施例1;
(2)选用6-8周龄雌性c57bl/6小鼠及tlr4缺陷型小鼠,随机分为六组:①野生型小鼠未照射组②野生型小鼠腹部照射组(15gy)③野生型小鼠照射给mpla组④tlr4缺陷型小鼠未照射组⑤tlr4缺陷型小鼠腹部照射组(15gy)⑥野生型小鼠照射给mpla组。通过胃内给药将mpla(0.1ml生理盐水中的1μg/小鼠)或生理盐水(0.1ml/小鼠)递送至相应组。在照射3天后处死老鼠,取小肠组织,固定、蜡块包埋,切片后用抗ki-67抗体进行免疫组化染色。ki-67是细胞增殖的标志分子之一。如附图3所示,未照射组野生型小鼠肠道隐窝呈ki-67阳性,表明隐窝细胞具有持续增殖能力,单纯接受照射后3天的照射组野生型小鼠肠道ki-67阳性隐窝数显著降低,每个隐窝中的ki-67阳性细胞比率也显著下降。照射前mpla给药组(照射+mpla)野生型小鼠肠道隐窝ki-67阳性率和平均每个隐窝ki-67阳性细胞数得到大幅度恢复。而在tlr4缺陷型小鼠中照射前mpla给药组(照射+mpla)小鼠肠道隐窝ki-67阳性率和平均每个隐窝ki-67阳性细胞数没有恢复,说明mpla是通过tlr4有效促进小肠隐窝细胞的增殖。
实施例4:
(1)辐射致肠道损伤小鼠模型同实施例1;
(2)取实施例3中各组小鼠小肠蜡块,切片后用抗γ-h2ax抗体进行免疫组化染色,并对隐窝细胞中γ-h2axfoci的数量变化进行统计,如附图4所示。我们发现野生型小鼠和tlr4缺陷型小鼠的未照射组γ-h2axfoci的数量都很少,腹部照射后有了明显的数量上升。而照射前mpla给药组(照射+mpla)野生型小鼠肠道隐窝γ-h2axfoci较照射组有明显下降,说明mpla减轻电离辐射诱发的dna损伤,对电离辐射致肠道损伤起到了明显的防治作用;tlr4缺陷型小鼠中照射前mpla给药组(照射+mpla)小鼠肠道隐窝γ-h2axfoci较照射组没有变化,说明mpla是通过tlr4对电离辐射致肠道损伤起到有效的防治作用。
实施例5:
(1)辐射致肠道损伤小鼠模型同实施例1;
(2)取实施例3中各组小鼠小肠蜡块,切片后进行tunel染色,来明确细胞凋亡情况,并对隐窝细胞中tunel阳性细胞数量进行统计,如附图4所示。我们发现野生型小鼠和tlr4缺陷型小鼠的未照射组基本无凋亡细胞,腹部照射后有了明显的数量上升。而照射前mpla给药组(照射+mpla)野生型小鼠肠道隐窝细胞凋亡数较照射组有明显下降,说明mpla减轻电离辐射诱发的隐窝细胞凋亡;tlr4缺陷型小鼠中照射前mpla给药组(照射+mpla)小鼠肠道隐窝细胞数较照射组没有变化,说明mpla是通过tlr4对电离辐射致肠道损伤起到有效的防治作用。
以上已对本发明创造的较佳实施例进行了具体说明,但本发明创造并不限于所述实施例,熟悉本领域的技术人员在不违背本发明创造精神的前提下还可做出种种的等同的变型或替换,这些等同的变型或替换均包含在本申请权利要求所限定的范围内。
- 还没有人留言评论。精彩留言会获得点赞!