纯金金标植入体及金标注射器的制作方法
本实用新型涉及医疗器械领域,特别涉及一种纯金金标植入体及金标注射器。
背景技术:
为了高精度照射软组织中的肿瘤,需要在肿瘤内或旁植入金标,治疗中通过对金标的追踪实现对肿瘤的动态追踪。
金标植入一周后,与肿瘤形成相对稳定的几何关系,在治疗中确定了金标位置也就确定了肿瘤的位置,金标的动度也就代表肿瘤的动度。
但是金标在植入肿瘤组织或其周围特定软组织后,金标物容易发生移动,若移位发生在治疗前,不会带来风险,但可能会引起照射精度的下降,可以通过再次植入金标来解决;若在治疗中发生移位,可能会影响治疗的安全性和准确性,并且金标移动则照射位置也发生改变,可能引起放射性损伤甚至事故。因此,无论金标移位发生在治疗前,还是治疗中,都要积极采取措施,避免治疗的安全性和精确性受到影响。
技术实现要素:
本实用新型的目的在于提供一种纯金金标植入体以及金标注射器,以解决现有技术中存在的上述技术问题。
本实用新型提供的金标植入体,包括金标本体,所述金标本体由纯金制成,所述金标本体包括多个球体和连接段,多个所述球体自上而下通过连接段依次固接为一体。
进一步地,所述球体上设有凸起。
进一步地,所述凸起为十字形凸起。
进一步地,所述凸起为人字形凸起。
进一步地,所述凸起为V字形凸起。
进一步地,所述金标本体上设有纳米药物层。
进一步地,所述纳米药物层通过连接剂层粘接到所述金标本体上。
进一步地,所述连接剂层为生物粘合剂层。
进一步地,所述生物粘合剂层为纤维蛋白原层、凝血酶层、酪蛋白层、壳多糖层或壳聚糖层。
本实用新型提供的纯金金标植入体,具有如下优点:
通过多个球体和连接段增加金标本体与植入的肿瘤组织或其周围的特定软组织的稳定性,使金标本体不易发生移动,提高治疗的安全性和准确性,由于金标本体不易移动,在治疗过程中因金标本体发生移动使照射位置发生改变,可能引起放射性损伤甚至事故出现的概率也进一步降低。
另外,本实用新型还提供了一种金标注射器,包括注射针体以及上述纯金金标植入体,所述金标本体放置在所述注射针体内。
附图说明
为了更清楚地说明本实用新型具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本实用新型的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
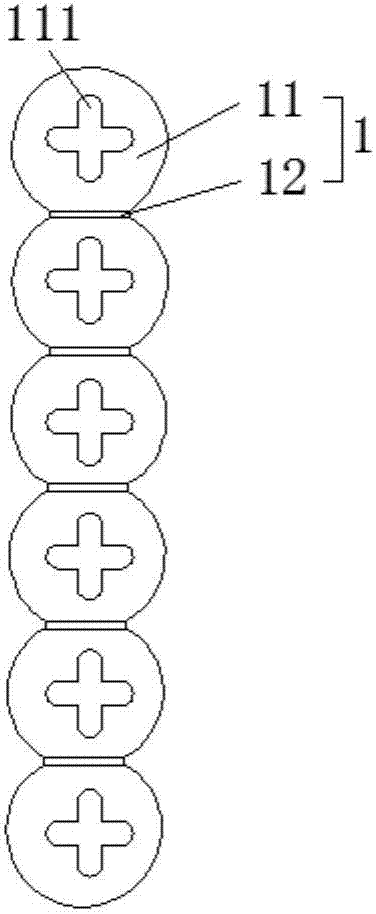
图1为本实用新型实施例一提供的纯金金标本体的结构主视图;
图2为本实用新型实施例二提供的纯金金标本体的结构主视图;
图3为本实用新型实施例三提供的纯金金标本体的结构主视图;
图4为本实用新型实施例四提供的纯金金标本体的结构主视图;
图5为本实用新型实施例五提供的纯金金标本体的结构主视图;
图6为图5中A处的局部放大图;
图7本实用新型实施例六提供的金标注射器的结构主视图;
图8为图7中B处的局部放大图。
附图标记:
1-金标本体; 11-球体; 12-连接段;
111-凸起; 2-纳米药物层; 3-连接剂层;
4-注射针体; 41-套管; 42-中空手柄;
43-推进器; 411-尖部; 44-推送杆;
45-推拉头。
具体实施方式
下面将结合附图对本实用新型的技术方案进行清楚、完整地描述,显然,所描述的实施例是本实用新型一部分实施例,而不是全部的实施例。基于本实用新型中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本实用新型保护的范围。
在本实用新型的描述中,需要说明的是,术语“中心”、“上”、“下”、“左”、“右”、“竖直”、“水平”、“内”、“外”等指示的方位或位置关系为基于附图所示的方位或位置关系,仅是为了便于描述本实用新型和简化描述,而不是指示或暗示所指的装置或元件必须具有特定的方位、以特定的方位构造和操作,因此不能理解为对本实用新型的限制。此外,术语“第一”、“第二”、“第三”仅用于描述目的,而不能理解为指示或暗示相对重要性。
在本实用新型的描述中,需要说明的是,除非另有明确的规定和限定,术语“安装”、“相连”、“连接”应做广义理解,例如,可以是固定连接,也可以是可拆卸连接,或一体地连接;可以是机械连接,也可以是电连接;可以是直接相连,也可以通过中间媒介间接相连,可以是两个元件内部的连通。对于本领域的普通技术人员而言,可以根据具体情况理解上述术语在本实用新型中的具体含义。
实施例一:
图1为本实用新型实施例一提供的纯金金标植入体的结构主视图;如图1所示,本实用新型提供的金标植入体,包括金标本体1,所述金标本体1由纯金制成,所述金标本体1包括多个球体11和连接段12,多个所述球体11自上而下通过连接段12依次固接为一体。
多个所述球体11的圆心共线设置。
纯金是指24K金,也就是说它的含金量是100%。在理论上100%的金才能称为24K金,但在现实中不可能有100%的黄金,所以中国规定:含量达到99.6%以上(含99.6%)的黄金才能称为24K金。
本实用新型提供的金标植入体,具有如下优点:
通过多个球体11和连接段12增加金标本体1与植入的肿瘤组织或其周围的特定软组织的稳定性,使金标本体1不易发生移动,提高治疗的安全性和准确性,由于金标本体1不易移动,降低在治疗过程中因金标本体1发生移动使照射位置发生改变,可能引起放射性损伤甚至事故出现的概率。
实施例二:
图2为本实用新型实施例二提供的纯金金标植入体的结构主视图;如图2所示,本实用新型提供的金标植入体,包括金标本体1,所述金标本体1由纯金制成,所述金标本体1包括多个球体11和连接段12,多个所述球体11自上而下通过连接段12依次固接为一体。
金标本体1的长度为0.1mm-10mm,直径为0.1mm-1.5mm。
多个所述球体11上分别设有凸起111,所述凸起111为十字形凸起。
通过球体11上的凸起111进一步增加与植入的肿瘤组织或其周围的特定软组织的稳定性。
实施例三:
图3为本实用新型实施例三提供的金标植入体的结构主视图;如图3所示,本实用新型提供的纯金金标植入体,包括金标本体1,所述金标本体1由纯金制成,所述金标本体1包括多个球体11和连接段12,多个所述球体11自上而下通过连接段12依次固接为一体。
多个所述球体11上分别设有凸起111,所述凸起111为人字形凸起。
实施例四:
图4为本实用新型实施例四提供的纯金金标植入体的结构主视图;如图4所示,本实用新型提供的金标植入体,包括金标本体1,所述金标本体1由纯金制成,所述金标本体1包括多个球体11和连接段12,多个所述球体11自上而下通过连接段12依次固接为一体。
多个所述球体11上分别设有凸起111,所述凸起111为V字形凸起。
需要说明的是,凸起111的形状和结构除了十字形、人字形和V 字形以外,还可采用其他形状,在此就不一一举例。
实施例五:
图5为本实用新型实施例五提供的金标植入体的结构主视图,图 6为图5中A处的局部放大图,如图5-6所示,本实用新型提供的纯金金标植入体,包括金标本体1,所述金标本体1由纯金制成,所述金标本体1包括多个球体11和连接段12,多个所述球体11自上而下通过连接段12依次固接为一体。
所述金标本体1上设有纳米药物层2。
所述纳米药物层2通过连接剂层3粘接到所述金标本体1上。
所述连接剂层3为生物粘合剂层。
所述生物粘合剂层为纤维蛋白原层、凝血酶层、酪蛋白层、壳多糖层或壳聚糖层。
胶原蛋白是生物高分子,动物结缔组织中的主要成分,也是哺乳动物体内含量最多、分布最广的功能性蛋白,占蛋白质总量的25%~ 30%,某些生物体甚至高达80%以上。
胶原蛋白种类较多,常见类型为Ⅰ型、Ⅱ型、Ⅲ型、Ⅴ型和Ⅺ型。
胶原蛋白因具有良好的生物相容性、可生物降解性以及生物活性,因此在食品、医药、组织工程、化妆品等领域获得广泛的应用。比如中国传统的胶原保健品“阿胶”,主要是以驴皮为原料(其实就是驴皮中所含胶原蛋白),具有较高的滋补保健作用,有中药三宝之一的美誉。
凝血酶:是一种在人体抗凝,促凝的凝血级联反应中有着重要作用的生物活性蛋白。
酪蛋白层:酪蛋白是一种含磷钙的结合蛋白,对酸敏感,pH较低时会沉淀。
酪蛋白是哺乳动物包括母牛,羊和人奶中的主要蛋白质,又称:干酪素、酪朊、乳酪素。
壳多糖层:壳多糖(chitin)又称几丁质。为N-乙酰葡糖胺通过β连接聚合而成的结构同多糖。广泛存在于甲壳类动物的外壳、昆虫的甲壳和真菌的胞壁中,也存在于一些绿藻中;主要是用来作为支撑身体骨架,以及对身体起保护的作用。
壳聚糖层:壳聚糖(chitosan)又称脱乙酰甲壳素,是由自然界广泛存在的几丁质(chitin)经过脱乙酰作用得到的,化学名称为聚葡萄糖胺(1-4)-2-氨基-B-D葡萄糖。
自1859年,法国人Rouget首先得到壳聚糖后,这种天然高分子的生物官能性和相容性、血液相容性、安全性、微生物降解性等优良性能被各行各业广泛关注,在医药、食品、化工、化妆品、水处理、金属提取及回收、生化和生物医学工程等诸多领域的应用研究取得了重大进展。针对患者,壳聚糖降血脂、降血糖的作用已有研究报告。同时,壳聚糖被作为增稠剂、被膜剂列入国家食品添加剂使用标准 GB-2760。
纳米药物,指通过一定的微细加工方式直接操纵原子、分子或原子团、分子团,使其重新排列组合,形成新的具有纳米尺度的物质或结构,一种具有同生物膜性质类似的磷脂双分子层结构载体的药物。
在药物研究领域,由于纳米技术的不断渗透和影响,引发了药物领域一场深远的革命,从而出现了纳米药物这一新名词。
纳米药物是指以纳米级高分子纳米粒(nano-particles,NP)、纳米球(nano.spheres NS)、纳米囊(nano-capsules,NC)等为载体,与药物以一定方式结合在一起后制成的药物,其粒径可能超过100nm,但通常应小于500nm。纳米药物也可以是直接将原料药物加工制成的纳米粒。
纳米药物的应用不仅改善了药物剂型的理化特性,而且提高了药物的靶向性、缓释性等。研究显示纳米颗粒具有将高浓度药物直接作用于癌细胞而又避开健康组织的能力。
纳米药物的特性:
1)磁场作用下的靶向性利用纳米载体与磁性物质结合,使其具有磁性。
同时,由体外附加磁场,或者通过手术植入具有磁场效应的导管、支架等材料在体内特定区域形成磁场。将靶器官暴露于磁场中,以此控制磁性纳米载体在体内的分布,使其集中分布于靶器官。
有研究显示磁性纳米载体能借助磁场使其所装载的化疗药物定向集中于靶向部位(肿瘤组织),提高靶向部位的药物浓度、增强治疗效果,同时降低其它部位的药物浓度,减少毒副反应。
2)主动靶向性将单克隆抗体共价交联或吸附到纳米粒表面,形成具有免疫活性纳米粒,并应用于抗肿瘤药物的研究也取得了一定的结果。
2、纳米药物的控释性
因很多化疗药物半衰期短、维持其有效抗肿瘤浓度时间较短。有些化疗药物只对处于特定增殖周期的肿瘤细胞发挥作用,而对其他增殖周期的细胞不发挥作用,然而肿瘤细胞的细胞周期通常是不同步的,因此,维持较长时间有效的血药浓度对于肿瘤治疗也非常重要。
3、纳米药物吸收率高
纳米药物有助于提高药物的吸收率,载药纳米粒可以改变膜运转机制,增加药物对生物膜的透过性,有利于药物透皮吸收及细胞内药效的发挥。
如装载抗肿瘤药物阿霉素的纳米粒可使其药效较普通阿霉素增加10倍,原因在于载药纳米粒的粘附性及其小的粒径能够延长药物滞留时间,增加药物与肠壁的接触时间和接触面积,提高其口服吸收的生物利用率。
4、纳米抗肿瘤药物代表
目前基于纳米技术的临床抗肿瘤药物代表为脂质体阿霉素、白蛋白结合型紫杉醇。
其中脂质体阿霉素为阿霉素与脂质纳米颗粒结合起来改变了药物的生物分布,从而减少了阿霉素的心脏毒性,白蛋白结合型紫杉醇也消除了化疗药物和有机溶剂聚氧乙烯蓖麻油的不良反应,可以不需要使用任何溶剂直接应用。
目前正在研发的药物还有BIND-014,该药物为靶向前列腺特异性膜抗原(PSMA)的含有多西他赛的纳米颗粒药物。
已有研究显示该药物在晚期实体瘤患者中取得了很好的安全性、耐受性以及有效性的结果。
另一种药物填充金元素的纳米颗粒被证实能够杀死培养的人细胞中的Bb细胞淋巴瘤,在未化疗的情况下能够抑制小鼠体内人B细胞淋巴瘤的生长。
而正在研发的覆盖有膀胱癌特异性配体并荷载紫杉醇的靶向性颗粒将3倍最大耐受剂量的药物输送至移植了患者肿瘤的小鼠,获得了良好的疾病控制并且不良反应可耐受。
在多发性骨髓瘤的治疗方面,纳米颗粒也显示出了一定的潜力,克服了应用多柔比星引起的耐药问题,经过纳米颗粒避免了其中一个耐药受体极迟抗原-4(VLA-4)与微环境相互作用,更直接、更有效地靶向作用于肿瘤。
实施例六:
图7为本实用新型实施例六提供的金标注射器的结构主视图,图 8为图7中B处的局部放大图;如图7-图8所示,本实施例提供的金标植入器,包括注射针体4以及上述纯金金标植入体,所述金标本体 1放置在所述注射针体4内。
所述注射针体4包括套管41、中空手柄42、推进器43和推送杆体44,套管41端部设有尖部411,套管41另一端连接中空手柄42,推进器43设置在套管41内,推进器43距套管41端部之间留有用于放置金标本体1的空隙,推送杆44一端与推进器43连接,推送杆 44另一端穿过中空手柄42并安装推拉头45。
使用时,将金标本体1装入套管41前端部的空隙内,将套管41 穿刺到需要标记的病变器官内,推动推拉头45带动推送杆44从而带动推进器43将金标本体1推出套管并注入病变器官内。
最后应说明的是:以上各实施例仅用以说明本实用新型的技术方案,而非对其限制;尽管参照前述各实施例对本实用新型进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本实用新型各实施例技术方案的范围。
- 还没有人留言评论。精彩留言会获得点赞!