对肠道的离子跨细胞转运体的作用剂、氯离子通道活化剂、肾脏疾病的预防或治疗剂或者排便促进剂的制作方法
本发明涉及含有特定的菌或其处理物的对肠道的离子跨细胞转运体的作用剂、氯离子通道活化剂、肾脏疾病的预防或治疗剂或者排便促进剂。
背景技术:
已知氯离子(Cl-)、钙离子(Ca2+)、钠离子(Na+)、钾离子(K+)等不仅掌管水/电解质转运、分泌或细胞容积的调节等,而且作为左右细胞应答的因子发挥重要的作用。例如,氯离子通道为转运氯离子的离子转运膜蛋白。有报告指出有各种各样的离子跨细胞转运体存在于神经、肌肉、上皮等的细胞膜,并参与各种生理机能或细胞防御机制。
在肠道中,氯离子与腹泻或便秘等的病况密切相关,作为由氯离子的平衡的异常导致的疾病,已知有难治性便秘、强直性肌萎缩、肾结石等呈现高钙尿症的疾病、焦虑、失眠症、囊性纤维化、癫痫、麻痹症、哮喘、支气管炎、神经功能障碍等(专利文献1)。
另一方面,已知加氏乳杆菌(Lactobacillus gasseri)的菌体、其菌体处理物或其混合物通过抑制大肠的氯离子通道从而抑制水分分泌,其结果,具有减少肠道的水分含量的作用(专利文献2)。然而,至今为止仍没有关于活化氯离子通道的菌等的报告。
现有技术文献
专利文献
专利文献1:日本专利第4786866号
专利文献2:日本特开第2014-101282号公报
技术实现要素:
本发明要解决的技术问题
本发明的目的在于提供新型的对肠道的离子跨细胞转运体的作用剂、氯离子通道活化剂、肾脏疾病的预防或治疗剂或者排便促进剂。另外,本发明的目的还在于提供具有对肠道的离子跨细胞转运体的作用能力、氯离子通道活化能力、肾脏疾病的预防或治疗效果、或者促进排便能力的新型菌处理物及其制备方法。
解决技术问题的技术手段
为了解决上述技术问题,本申请的发明人进行了研究,其结果发现,特定的菌或其处理物对肠道的离子跨细胞转运体发挥作用、活化氯离子通道,对肾脏疾病的预防或治疗有效,或者具有促进排便的作用,进一步反复进行研究,获得了各种新发现,从而完成了本发明。
即,本发明涉及以下发明。
[1]一种对肠道的离子跨细胞转运体的作用剂,其含有双歧杆菌(Bifidobacterium)属或乳酸杆菌(Lactobacillus)属的菌或其处理物(其中,不包括离子转运体为氯离子通道且作用为抑制的情况、离子转运体为Na+K+Cl-共转运体(NKCC1)且作用为抑制的情况、菌为婴儿双歧杆菌35624(Bifidobacterium infantis 35624)的情况及菌为唾液乳杆菌UCC118(Lactobacillus salivarius UCC118)的情况)。
[2]根据所述[1]所述的剂,其对离子跨细胞转运体的作用为氯离子通道的活化。
[3]根据所述[1]或[2]所述的剂,其为排便促进剂。
[4]一种肾脏疾病的预防或治疗剂,其含有双歧杆菌(Bifidobacterium)属或乳酸杆菌(Lactobacillus)属的菌或其处理物,且菌处理物为不含菌发酵代谢产物的处理物,给药对象不包括狗或猫。
[5]根据所述[1]~[4]中任一项所述的剂,其中,双歧杆菌(Bifidobacterium)属的菌为长双歧杆菌(Bifidobacterium longum)、两歧双歧杆菌(Bifidobacterium bifidum)、短双歧杆菌(Bifidobacterium breve)、青春双歧杆菌(Bifidobacterium adolescentis)、婴儿双歧杆菌(Bifidobacterium infantis)、假长双歧杆菌(Bifidobacterium pseudolongum)或嗜热双歧杆菌(Bifidobacterium thermophilum)。
[6]根据所述[1]~[5]中任一项所述的剂,其中,双歧杆菌(Bifidobacterium)属的菌为长双歧杆菌CLA8013菌株(Bifidobacterium longum CLA8013,保藏编号:NITE BP-02352)或长双歧杆菌MM-2菌株(Bifidobacterium longum MM-2,保藏编号:NITE BP-818)。
[7]根据所述[1]~[6]中任一项所述的剂,其中,乳酸杆菌(Lactobacillus)属的菌为嗜酸乳杆菌(Lactobacillus acidophilus)、约氏乳杆菌(Lactobacillus johnsonii)、加氏乳杆菌(Lactobacillus gasseri)、干酪乳杆菌(Lactobacillus casei)、植物乳杆菌(Lactobacillus plantarum)、德氏乳杆菌保加利亚亚种(Lactobacillus delbrueckii subsp.bulgaricus)、德氏乳杆菌乳酸亚种(Lactobacillus delbrueckii subsp.lactis)、发酵乳杆菌(Lactobacillus fermentum)、瑞士乳杆菌(Lactobacillus helveticus)、副干酪乳杆菌副干酪亚种(Lactobacillus paracasei subsp.paracasei)、罗伊氏乳杆菌(Lactobacillus reuteri)、鼠李糖乳杆菌(Lactobacillus rhamnosus)、唾液乳杆菌(Lactobacillus salivarius)或短乳杆菌(Lactobacillus brevis)。
[8]根据所述[1]~[6]中任一项所述的剂,其中,乳酸杆菌(Lactobacillus)属的菌为嗜酸乳杆菌JCM1132株(Lactobacillus acidophilus JCM1132)、约氏乳杆菌JCM2012株(Lactobacillus johnsonii JCM2012)或加氏乳杆菌JCM5813株(Lactobacillus gasseri JCM5813)。
[9]一种菌株,其为长双歧杆菌CLA8013菌株(Bifidobacterium longum CLA8013,保藏编号:NITE BP-02352)。
[10]一种菌处理物的制备方法,其为双歧杆菌(Bifidobacterium)属或乳酸杆菌(Lactobacillus)属的菌处理物的制备方法,其特征在于,包括以下工序,并且不包含发酵工序:
将菌混悬于不含糖的溶剂(其中,不包括纯化水及生理盐水)或含DMEM(Dulbecco’s Modified Eagle Medium)及Ham’s F-12的溶剂中,得到菌悬液的工序;
将菌悬液放置于厌氧条件下的工序;以及
用过滤器过滤经放置的菌悬液的上清液,得到滤液作为处理物的工序。
[11]一种悬浊液的上清液,所述悬浊液含有双歧杆菌(Bifidobacterium)属或乳酸杆菌(Lactobacillus)属的菌以及不含糖的溶剂(其中,不包括纯化水及生理盐水)或含DMEM及Ham’s F-12的溶剂(其中,上清液不包含双歧杆菌(Bifidobacterium)属或乳酸杆菌(Lactobacillus)属的菌)。
发明效果
本发明能够提供一种新型的对肠道的离子跨细胞转运体的作用剂。本发明的剂在可活化氯离子通道、预防或治疗肾脏疾病方面、或者在具有促进排便的作用方面,具有特别显著的效果。
附图说明
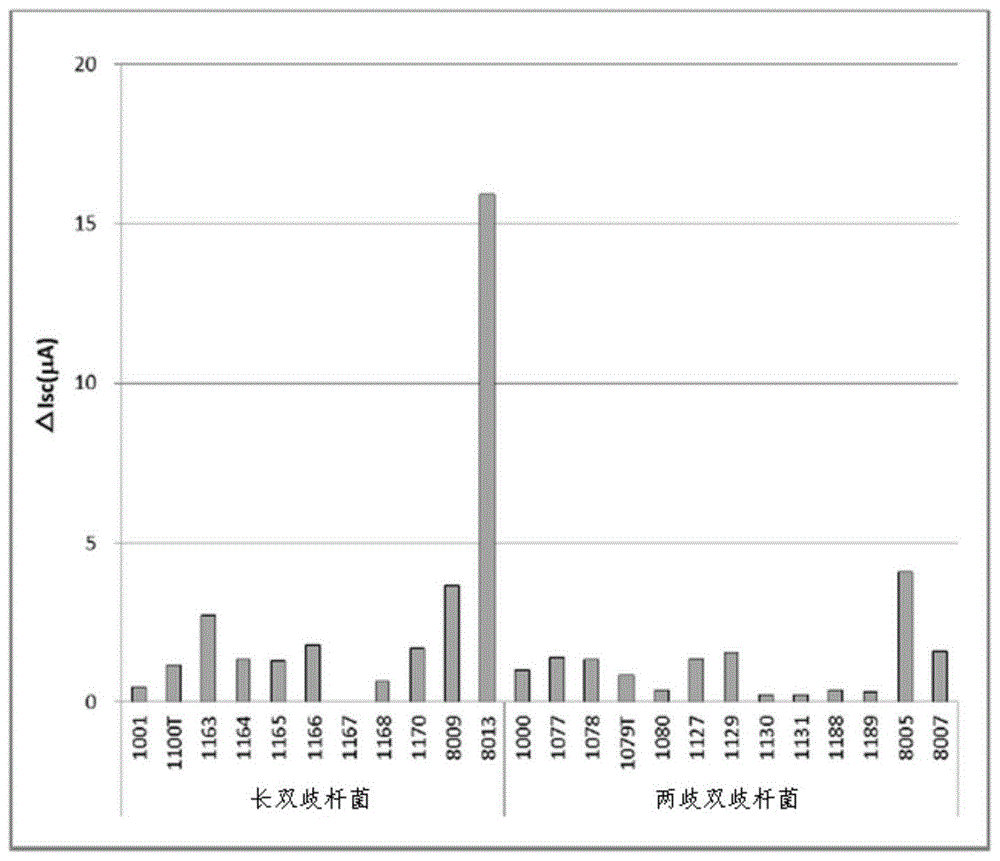
图1为示出由属于双歧杆菌(Bifidobacterium)属的菌的处理物引起的肠道上皮细胞(T84)中的短路电流变化的图。
图2为示出由属于乳酸杆菌(Lactobacillus)属的菌的处理物引起的肠道上皮细胞(T84)中的短路电流变化的图。
图3为示出直至测定血清BUN(尿素氮)为止的试验时间表的图。
图4为示出血清BUN值的测定结果的图。
图5为示出红色粪便排出时间的测定结果的图。
图6为示出经各溶剂(纯化水、生理盐水、DMEM/F-12或PBS(-))处理后的8013E在肠道上皮细胞(T84)中的短路电流变化的图。
图7为示出血清BUN值的测定结果的图。
具体实施方式
本发明提供一种对肠道的离子跨细胞转运体的作用剂,其含有属于双歧杆菌(Bifidobacterium)属或乳酸杆菌(Lactobacillus)属的菌或其处理物。具体而言,例如提供氯离子通道活化剂、肾脏疾病的预防或治疗剂或者排便促进剂。本发明的剂含有上述乳酸菌或其处理物即可,也可以进一步含有其他成分。上述菌可以单独使用1种,也可以混合使用2种以上。
本发明的剂含有属于双歧杆菌(Bifidobacterium)属或乳酸杆菌(Lactobacillus)属的菌。作为属于双歧杆菌(Bifidobacterium)属的乳酸菌,优选长双歧杆菌(Bifidobacterium longum)、两歧双歧杆菌(Bifidobacterium bifidum)、短双歧杆菌(Bifidobacterium breve)、青春双歧杆菌(Bifidobacterium adolescentis)、婴儿双歧杆菌(Bifidobacterium infantis)、假长双歧杆菌(Bifidobacterium pseudolongum)、嗜热双歧杆菌(Bifidobacterium thermophilum)等,其中,更优选长双歧杆菌(Bifidobacterium longum)或两歧双歧杆菌(Bifidobacterium bifidum)。作为长双歧杆菌(Bifidobacterium longum)或两歧双歧杆菌(Bifidobacterium bifidum),优选长双歧杆菌CLA8013(Bifidobacterium longum CLA8013,保藏编号:NITE BP-02352)、长双歧杆菌ID8009(Bifidobacterium longum ID8009)、长双歧杆菌ID1163(Bifidobacterium longum ID1163)、长双歧杆菌MM-2(Bifidobacterium longum MM-2:ID1001,保藏编号:NITE BP-818)或两歧双歧杆菌ID8005(Bifidobacterium bifidum ID8005),进一步优选长双歧杆菌CLA8013(Bifidobacterium longum CLA8013,保藏编号:NITE BP-02352)或长双歧杆菌MM-2(Bifidobacterium longum MM-2:ID1001,保藏编号:NITE BP-818)。作为属于乳酸杆菌(Lactobacillus)属的乳酸菌,优选嗜酸乳杆菌(Lactobacillus acidophilus)、约氏乳杆菌(Lactobacillus johnsonii)、加氏乳杆菌(Lactobacillus gasseri)、干酪乳杆菌(Lactobacillus casei)、植物乳杆菌(Lactobacillus plantarum)、德氏乳杆菌保加利亚亚种(Lactobacillus delbrueckii subsp.bulgaricus)、德氏乳杆菌乳酸亚种(Lactobacillus delbrueckii subsp.lactis)、发酵乳杆菌(Lactobacillus fermentum)、瑞士乳杆菌(Lactobacillus helveticus)、副干酪乳杆菌副干酪亚种(Lactobacillus paracasei subsp.paracasei)、罗伊氏乳杆菌(Lactobacillus reuteri)、鼠李糖乳杆菌(Lactobacillus rhamnosus)、唾液乳杆菌(Lactobacillus salivarius)、短乳杆菌(Lactobacillus brevis)等,其中,更优选嗜酸乳杆菌(Lactobacillus acidophilus)、加氏乳杆菌(Lactobacillus gasseri)或约氏乳杆菌(Lactobacillus johnsonii)。作为嗜酸乳杆菌(Lactobacillus acidophilus)、加氏乳杆菌(Lactobacillus gasseri)或约氏乳杆菌(Lactobacillus johnsonii),更优选嗜酸乳杆菌JCM1132(Lactobacillus acidophilus JCM1132;ID2152T)、加氏乳杆菌JCM5813(Lactobacillus gasseri JCM5813;ID2145)、约氏乳杆菌JCM2012(Lactobacillus johnsonii JCM2012;ID2153T),进一步优选嗜酸乳杆菌JCM1132(Lactobacillus acidophilus JCM1132;ID2152T)。
这些菌体可以容易地从例如ATCC或IFO等机关或财团法人The Japan Bifidus Foundation等获得。另外,长双歧杆菌CLA8013及长双歧杆菌MM-2已经存放在了独立行政法人制品评价技术基盘机构专利微生物保藏中心(千叶县木更津市上总镰足2-5-8 122号室,邮编292-0818)的下述保藏编号的位置。此外,也可以适当地使用市售的菌体。
长双歧杆菌CLA8013(保藏日期:2016年9月21日,保藏编号:NITE BP-02352,识别标识:Bifidobacterium longum CLA8013)
长双歧杆菌MM-2(保藏日期:2009年9月17日,保藏编号:NITE BP-818,识别标识:Bifidobacterium longum MM-2)
本发明的剂不包含婴儿双歧杆菌35624(Bifidobacterium infantis35624)及唾液乳杆菌UCC118(Lactobacillus salivarius UCC118)。
只要能够发挥本发明的效果,也可以含有除上述乳酸菌以外的有用菌。例如可列举出Bacillus subtilis 129BIO H(α)(枯草芽孢杆菌129BIO H(α))等Bacillus subtilis(枯草芽孢杆菌)、Bacillus mesentericus(马铃薯杆菌)、Bacillus polyfermenticus(多发酵芽胞杆菌)等糖化菌;例如Bacillus coagulans(凝结芽孢杆菌)等有孢子性乳酸菌;Bacillus toyoi(东洋芽孢杆菌)、Bacillus licheniformis(地衣芽孢杆菌)、Clostridium butyricum(酪酸梭菌)等酪酸菌;Leuconostoc mesenteroides(肠膜明串珠菌)等Leuconostoc(明串珠菌)属、Lactococcus lactis(乳酸乳球菌)、Lactococcus cremoris(乳脂乳球菌)等Lactococcus(乳球菌)属、Tetragenococcus halophilus(嗜盐四联球菌)等Tetragenococcus(四联球菌)属、Pediococcus acidilactici(乳酸片球菌)、Pediococcus pentosaceus(戊糖片球菌)等Pediococcus(片球菌)属、Oenococcus oeni(酒类酒球菌)等Oenococcus(酒球菌)属等乳球菌属;以及其他的有用菌。
这些菌体可以容易地从例如ATCC或IFO等机关获得。此外,也可以适当地使用市售的菌体。
上述菌体能够通过以公知的条件或以其为准的条件进行培养而得到。例如,通常在约25~45℃左右下,将上述乳酸菌的1种或2种以上在含有葡萄糖、酵母抽提物、蛋白胨等的液体培养基上进行约4~72小时的好氧或厌氧培养,从培养液中收集菌体并洗涤,由此能够得到湿菌体。
本发明中使用的菌优选为活菌,但也可以是包含干燥物(菌体干燥物)等的死菌,也可以是混合了活菌和死菌的物质等。作为菌体干燥物,优选单微米(single micron)的菌体干燥物。菌体干燥物通常是指经干燥的各个菌体或者经干燥的菌体的聚集体。此外,单微米是指将小数点第1位四舍五入的1~10μm。
在本发明中,菌处理物是指对菌施加了某些处理的物质,该处理没有特别限定。作为菌处理物,例如可以为该菌体与溶剂的混合液、其上清液或离心后的上清液等,也可以为使用过滤器等将其过滤后的滤液等。所述菌体和溶剂的混合液若为将菌体和溶剂混合而成的物质,则也可以为悬浊液。作为菌体与溶剂的混合液,例如可以使用在约25~45℃左右、在好氧或厌氧条件下放置约30分钟~3天左右的混合液,也可以直接使用混合而成的混合液。此外,菌处理物也可以为从菌处理物中提取的提取物等。本发明有时将其简单地写为提取物。此外,菌处理物也可以为例如按照公知的技术将滤液或提取物、混合液浓缩、粉末化、冷冻干燥而成的物质等。另外,本发明中的菌处理物不包含菌发酵代谢产物。作为溶剂,例如可列举出含磷酸缓冲液(PBS)等且不含糖的溶剂、或DMEM/F-12等培养液等。磷酸缓冲液(PBS)可以使用添加有钙盐及镁盐的磷酸缓冲液(PBS(+)),也可以使用未添加钙盐及镁盐的磷酸缓冲液(PBS(-))。离心条件没有特别限定,离心力可以为2,500~10,000×G。过滤器的筛孔的大小只要为能够将菌过滤的筛孔的大小即可,例如能够使用市售的0.1μm~1μm(例如0.22μm)的过滤器。DMEM/F-12等培养液可以含糖,也可以不含糖。另外,本发明中的溶剂不含纯化水及生理盐水。
在本发明中,菌发酵代谢产物是指,例如将菌播种在含有脱脂乳粉、乳糖、葡萄糖、蛋白胨、酵母抽提物等的菌增殖培养基上,在一定温度(例如20℃~40℃)下培养一定时间(例如2~60小时)后的菌发酵代谢液等。
本发明中的菌处理物可以含有菌,也可以不含菌,优选不含菌。然而,当本发明中的菌处理物中含有未发酵的菌时,不受上述限定。
在本发明中,肠道例如可以为十二指肠、空肠、回肠等小肠;盲肠、升结肠、横结肠、降结肠、乙状结肠、直肠等大肠等。进一步,在本发明中,肠道可以为在体内的状态,也可以将肠道切出至体外,或者也可以切开腹部将肠道的一部分从活体中取出。
在本发明中,离子跨细胞转运体为经由细胞的离子转运体,有时也被记作跨细胞离子转运体。作为离子转运体,例如可列举出离子通道、离子共转运体、离子交换转运体等。作为离子通道,例如可列举出氯离子通道、钙离子通道、钠离子通道、钾离子通道、阳离子通道等。作为氯离子通道,例如可列举出CFTR氯离子通道等。作为离子共转运体,例如可列举出Na+K+Cl-共转运体(NKCC1)等。作为离子交换转运体,例如可列举出Cl-/HCO3-交换转运体(DRA)等。
在本发明中,作用于离子跨细胞转运体是指例如使离子跨细胞转运体的机能活化、抑制离子跨细胞转运体的机能等,从而使其机能发生变化等。具体而言,例如是指使氯离子通道活化、使钙离子通道活化、使钠离子通道活化、使钾离子通道活化、使阳离子通道活化、使Na+K+Cl-共转运体(NKCC1)活化、使Cl-/HCO3-交换转运体(DRA)活化等。此外,具体而言,例如是指抑制钙离子通道、抑制钠离子通道、抑制钾离子通道、抑制阳离子通道、抑制Cl-/HCO3-交换转运体(DRA)等。
但是,在本发明中,不包括:
离子转运体为氯离子通道且作用为抑制的情况;
离子转运体为Na+K+Cl-共转运体(NKCC1)且作用为抑制的情况;
菌为婴儿双歧杆菌35624(Bifidobacterium infantis 35624)的情况;以及
菌为唾液乳杆菌UCC118(Lactobacillus salivarius UCC118)的情况。
以下,关于本发明的对肠道的离子跨细胞转运体的作用剂,按照各个实施方式进行说明。具体而言,对氯离子通道的活化剂、肾脏疾病的预防或治疗剂及排便促进剂进行说明。
作为本发明的一个实施方式,例如可列举出氯离子通道的活化剂。在本发明中,将氯离子通道活化是指例如与给药本发明的剂前的状态相比,离子的跨细胞转运能力变大等。离子的跨细胞转运能力例如能够利用短路电流法(唐木晋一郎、桑原厚和、日本药理学杂志(Folia Pharmacol.Jpn.)123,211~218(2004)上皮细胞膜中的电解质转运的电生理学测定法:短路电流法)进行测定。
作为本发明的一个实施方式,例如可列举出肾脏疾病的预防或治疗剂。在本发明中,肾脏疾病的预防或治疗剂对肾脏疾病的预防或治疗有用。在本发明中,肾脏疾病的“预防”是指例如作用于肠道的离子跨细胞转运体、离子通道从而阻止肾脏疾病的发病,肾脏疾病的“治疗”是指例如由肾脏疾病引发的症状的缓解或者彻底治愈。作为肾脏疾病,例如可列举出肾功能衰竭、尿毒症、糖尿病肾病、慢性肾小球肾炎等。肾脏疾病例如可以为慢性的肾脏疾病,也可以为急性的肾脏疾病。作为慢性肾脏疾病,例如可列举出慢性肾功能衰竭、慢性肾小球肾炎、糖尿病肾病、肾病综合征等。作为急性肾脏疾病,例如可列举出急性肾小球肾炎、急性肾功能衰竭、溶血性尿毒症综合征等。
在本发明中,判断肾脏疾病改善的方法没有特别限定,可通过公知的方法等进行判断。作为用于判断通过给药本发明的菌或其处理物或者本发明的剂而使肾脏疾病得到了改善的方法,例如可列举出测定血清中BUN(尿素氮)的方法等。使用测定血清中BUN的方法时,例如通过给药菌或菌处理物或剂,BUN的值与给药前相比有所下降的情况下,可判断为对肾脏疾病具有改善效果。
作为本发明的一个实施方式,例如可列举出排便促进剂。其原因在于,本发明的剂具有氯离子通道活化作用,其结果,能够使肠道的水分含量增加,得到促进排便的作用。
在本发明中,排便促进剂例如能够促进生理性排便或缩短从进食到排便的时间。
在本发明中,判断促进排便的效果的方法没有特别限定,例如可列举出根据排便次数、从进食到排便的时间、粪便中含有的水分含量等进行判断的方法。
本发明的剂能够通过单独使用菌或其处理物、或者将其与其他成分混合,从而用作用于药品、类药品(quasi drugs)、饮食品、食品添加物、饲料等的制造的原料;或者能够直接以药品、类药品、饮食品、食品添加物、饲料等形态进行使用。本发明的组合物可以不含辅酶Q10。即,作为本发明的一个实施方式,可列举出药品组合物、类药品组合物、饮食品组合物、食品添加物组合物、饲料组合物等。这样的包含本发明的剂的药品组合物也是本发明的优选实施方式之一。
考虑各个成分的物理化学性质、生物学性质等而将本发明的药品组合物的剂型设为适合给药的剂型即可。优选设为适合口服给药的口服剂。此外,本发明的药品组合物的剂型也可以为非口服剂。作为口服剂的剂型,例如可列举出片剂(包含糖衣片)、微丸剂、细粒剂、散剂、颗粒剂、丸剂、咀嚼片、锭剂、胶囊剂等固体剂;水剂、混悬剂、乳剂、糖浆剂、酏剂等液体剂;果冻状制剂等半固体剂等。其中,优选片剂、散剂、液体剂或混悬剂。进一步,本发明的药品组合物除乳酸菌以外,也可以适当含有赋形剂(例如,白糖、乳糖、淀粉、结晶纤维素、磷酸钠、碳酸镁、果胶、糊精、黄蓍胶等)、粘合剂(例如,淀粉、明胶、羧甲基纤维素钠、甲基纤维素、羟丙基甲基纤维素、羟丙基纤维素、聚乙烯吡咯烷酮、果胶、黄蓍胶等)、崩解剂(例如淀粉、羧甲基纤维素钠、黄蓍胶等)、润滑剂(例如滑石、硬脂酸镁、硬脂酸钙、聚乙二醇、蔗糖脂肪酸酯等)、稳定剂(亚硫酸氢钠、硫代硫酸钠、乙二胺四乙酸钠、柠檬酸钠、抗坏血酸、二丁基羟基甲苯等)、增稠剂(羧甲基纤维素钠等)、载体(低熔点蜡、可可脂等)、着色剂、赋香剂(香料)、光亮剂、稀释剂、缓冲剂、乳化剂、分散剂、助悬剂、防腐剂、吸收促进剂、调味剂等本领域中使用的公知的添加剂等。制剂中所含的菌或其处理物的总量通常能够从相对于最终制剂整体为约0.000001~99质量%的范围中适当地选择并决定。其中,优选含有约0.05~约50质量%,更优选含有约0.1~约25质量%。
在本发明中,优选口服用的固体剂(片剂(包含糖衣片)、丸剂、胶囊剂、散剂、颗粒剂等),能够将有效成分与例如赋形剂(乳糖、甘露醇、葡萄糖、微晶纤维素、淀粉等)、粘合剂(羟丙基纤维素、聚乙烯吡咯烷酮、偏硅酸铝镁等)、崩解剂(纤维素乙二醇酸钙等)、润滑剂(硬脂酸镁等)、稳定剂、助溶剂(谷氨酸、天冬氨酸等)等添加剂混合,并按照常用方法进行制剂化。根据需要,也可以进一步用包衣剂(白糖、明胶、羟丙基纤维素、羟丙基甲基纤维素苯二甲酸酯等)进行包覆,或者也可以用2种以上的层进行包覆。
以固体制剂的形态使用本发明的剂时,根据干燥方法可以单纯地混合粉末,此外,也可以压缩该粉末而制成颗粒或制成片剂。通过湿法制造颗粒、片剂时,可使用粘合剂的水溶液进行捏合、干燥,制成目标固体剂。进一步,也可将以此方式得到的粉末或颗粒填充于胶囊,制成胶囊剂。
例如,制造片剂时,可以使用公知的压片机。作为该压片机,例如可列举出单冲压片机或旋转式压片机等。此外,丸剂、咀嚼片或锭剂的制备方法按照公知的方法进行即可,例如能够使用与制造片剂相同的手段进行制作。
为了将微量的有效成分(菌或其处理物)与大量的其他粉末混合从而得到均匀的混合物,优选采用所谓的逐步混合法。例如,将有效成分与体积为其100~200倍的粉末混合从而得到均匀的粉末,将其与剩余的粉末混合,即可得到均匀稀释的粉末。
对于含水物质的干燥而言,可以采取喷雾干燥、L-干燥、冷冻干燥等手段。
在本发明中,口服用的液体剂(水剂、混悬剂、乳剂、糖浆剂、酏剂等)通过将有效成分溶解、混悬或乳化于通常使用的稀释剂(纯化水、乙醇或其混合液等)而进行制剂化。进一步,该液体剂也可以含有润湿剂、混悬剂、乳化剂、甜味剂、调味剂、芳香剂、防腐剂、缓冲剂等。
作为非口服剂,可列举出注射剂(例如,皮下注射剂、静脉注射剂、肌内注射剂、腹腔注射剂)、点滴剂、外用剂(例如,经鼻给药制剂、经皮制剂、软膏剂)、栓剂(例如,直肠栓剂、阴道栓剂)等。这些制剂可利用该领域通常实施的手法,使用上述药学上允许的添加剂而进行制剂化。制剂中所含的菌或其处理物的总量通常能够从相对于最终制剂整体为约0.000001~99质量%的范围中适当地选择并决定。其中,优选包含约0.05~约50质量%,更优选包含约0.1~约25质量%。
在本发明中,作为非口服剂,例如可列举出注射剂。注射剂包括溶液、悬浊液、乳浊液及使用时进行溶解或混悬而使用的固体注射剂。注射剂通过将有效成分溶解、混悬或乳化于溶剂而进行制剂化。作为溶剂,例如可使用注射用蒸馏水、生理盐水、植物油、丙二醇、聚乙二醇、乙醇这样的醇类等及它们的组合。进一步,该注射剂也可含有稳定剂、助溶剂(谷氨酸、天冬氨酸、吐温80(注册商标)等)、助悬剂、乳化剂、安抚剂、缓冲剂、防腐剂等。其可在最终工序中通过灭菌或无菌操作法制造。此外,也能够通过制造无菌的固体剂例如冷冻干燥品、并在使用前将其溶解于无菌化或者无菌的注射用蒸馏水或其他的溶剂中而制造注射剂。
进一步,作为非口服剂,例如可列举出栓剂。该组合物可按照通常使用的方法制造。
本发明中使用的菌通常为厌氧性,在干燥状态下不耐受空气或氧气,而且不耐受高温和湿气,因此在进行组合物的制剂化时优选尽可能的在非活性气体的存在下或真空、低温下进行处理。只要能够发挥本发明的效果,则组合物的制剂化时的温度没有特别限定,可按照公知的方法决定。
在本发明中,对包含人类的动物的菌的给药剂量优选为约1×103~1×1011个/成人/次,更优选为约1×106~1×1011个/成人/次,进一步优选为约1×109~1×1011个/成人/次。
在本发明中,对包含人类的动物的菌处理物的给药剂量优选为约1×103~1×1014个菌处理物/成人/次,更优选为约1×106~1×1014个菌处理物/成人/次,进一步优选为约1×109~1×1014个菌处理物/成人/次。
在本发明中,组合物的使用间隔取决于对象(例如,大鼠)、途径(例如,口服给药)、形态(例如,液体剂)等,例如,本发明的组合物可以1天使用1~5次,可以1周使用1~5次,也可以1个月使用1~5次等。
在本发明中,组合物的使用时间取决于对象(例如,小鼠)、途径(例如,口服给药)、形态(例如,液体剂)、使用间隔等,例如可以为1天~6天,可以为1周~4周,也可以为1个月~12个月。此外,例如也可以持续使用组合物等。
在本发明中,作为剂的给药对象,例如可以对动物(例如,人、大鼠、小鼠、兔子、羊、猪、牛、猫、狗、猴等)进行给药。
在本发明中,肾脏疾病的预防或治疗剂的给药对象优选为除狗及猫以外的动物(例如,人、大鼠、小鼠、兔子、羊、猪、牛、猴等)。
作为本发明的药品组合物的适应症,可列举出炎症性肠病、溃疡性结肠炎、克罗恩病、肠结核、传染性肠炎、非传染性肠炎、急性肠炎、急性胃肠炎、慢性肠炎、肠易激综合征(IBS)、结肠癌、肠梗阻、便秘、肾炎、肾功能衰竭、肾病综合征、糖尿病肾病、肾小球性肾炎、肾结石、多囊肾、肾性贫血、肾硬化症、肾积水等。
对于本发明的剂而言,作为除药品组合物以外的其他组合物的原料,例如能够使用上述菌或其处理物,按照公知的方法,制备其他的组合物。相对于除药品组合物以外的其他组合物的菌或其处理物的含量,例如能够从相对于组合物整体为约0.000001~99质量%的范围中适当地选择并决定。
在本发明中,作为饮食品,例如可列举出清凉饮料、乳饮料、发酵乳、酸奶、乳酸菌饮料、补剂(supplement)等。
本发明包含一种菌处理物的制备方法,其为双歧杆菌(Bifidobacterium)属或乳酸杆菌(Lactobacillus)属的菌处理物的制备方法,其特征在于,包括以下工序,并且不包含发酵工序:
将菌混悬于不含糖的溶剂(其中,不包括纯化水及生理盐水)或含DMEM及Ham’s F-12的溶剂中,得到菌悬液的工序;
将菌悬液放置于厌氧条件下的工序;以及
用过滤器过滤经放置的菌悬液的上清液,得到滤液作为处理物的工序。
在本发明中,作为不含糖的溶剂,例如可列举出含磷酸的溶液、磷酸缓冲液(PBS)等,但是本发明不包含纯化水及生理盐水。含磷酸的溶液为至少含有磷酸的溶液即可。磷酸缓冲液(PBS)可以使用添加有钙盐及镁盐的磷酸缓冲液(PBS(+)),也可以使用未添加钙盐及镁盐的磷酸缓冲液(PBS(-))。就离子跨细胞转运能力较高这一点而言,优选使用PBS(-)。作为糖,例如可列举出乳糖、蔗糖、低聚糖、糖醇等。
在本发明中,作为DMEM,可以使用包含例如甘氨酸、L-精氨酸盐酸盐、L-胱氨酸二盐酸盐、L-谷氨酰胺、L-组氨酸盐酸盐单水合物、L-异亮氨酸、L-亮氨酸、L-赖氨酸盐酸盐、L-甲硫氨酸、L-苯丙氨酸、L-丝氨酸、L-苏氨酸、L-色氨酸、L-酪氨酸二钠盐水合物、L-缬氨酸、D-泛酸钙、氯化胆碱、叶酸、i-肌醇、烟酰胺、盐酸吡哆醇、核黄素、盐酸硫胺素、无水氯化钙、硝酸铁九水合物、无水硫酸镁、氯化钾、氯化钠、碳酸氢钠、无水磷酸二氢钠、D-葡萄糖、酚红等的DMEM等。
在本发明中,作为Ham’s F-12,可以使用包含例如甘氨酸、L-丙氨酸、L-精氨酸盐酸盐、L-天冬酰胺一水合物、L-天冬氨酸、L-半胱氨酸盐酸盐一水合物、L-谷氨酸、L-谷氨酰胺、L-组氨酸盐酸盐单水合物、L-异亮氨酸、L-亮氨酸、L-赖氨酸盐酸盐、L-甲硫氨酸、L-苯丙氨酸、L-脯氨酸、L-丝氨酸、L-苏氨酸、L-色氨酸、L-酪氨酸二钠盐水合物、L-缬氨酸、生物素、氯化胆碱、D-泛酸钙、叶酸、烟酰胺、盐酸吡哆醇、核黄素、盐酸硫胺素、维生素B12、i-肌醇、无水氯化钙、五水硫酸铜、七水合硫酸亚铁、氯化钾、无水氯化镁、氯化钠、碳酸氢钠、无水磷酸二氢钠、七水合硫酸锌、D-葡萄糖、次黄嘌呤、亚油酸、硫辛酸、腐胺二盐酸盐(putrescine dihydrochloride)、胸苷、酚红、丙酮酸钠等的Ham’s F-12等。
在本发明中,作为含有DMEM及Ham’s F-12的溶剂,例如可列举出混合DMEM及Ham’s F-12而成的溶剂、含有DMEM及Ham’s F-12的溶液、含有DMEM及Ham’s F-12的培养基等。
在本发明中,作为含有DMEM及Ham’s F-12的培养基,例如可以混合市售商品等而使用,也可以使用已经被混合的市售商品等(DMEM/F-12培养基(赛默飞世尔科技公司制造)),也可以使用不含糖的市售商品等。
作为本发明中使用的DMEM/F-12培养基,例如也可以使用将市售商品等中包含的各个成分(L-谷氨酰胺、酚红、丙酮酸钠、无水氯化钙、氯化钾、无水氯化镁、无水硫酸镁、氯化钠、碳酸氢钠、无水磷酸氢二钠、无水磷酸二氢钠、五水硫酸铜、硝酸铁九水合物、七水合硫酸亚铁、七水合硫酸锌、L-丙氨酸、L-精氨酸盐酸盐、L-天冬酰胺一水合物、L-天冬氨酸、L-胱氨酸二盐酸盐、L-半胱氨酸盐酸盐一水合物、L-谷氨酸、L-谷氨酰胺、甘氨酸、L-组氨酸盐酸盐单水合物、L-异亮氨酸、L-亮氨酸、L-赖氨酸盐酸盐、L-甲硫氨酸、L-苯丙氨酸、L-脯氨酸、L-丝氨酸、L-苏氨酸、L-色氨酸、L-酪氨酸二钠盐水合物、L-缬氨酸、D-生物素、D-泛酸钙、氯化胆碱、叶酸、i-肌醇、烟酰胺、盐酸吡哆醇、核黄素、盐酸硫胺素、维生素B12、D-葡萄糖、次黄嘌呤、亚油酸、硫辛酸、腐胺二盐酸盐、胸苷等)混合而制作成的培养基。从简便性的点出发,优选使用市售商品DMEM/F-12。
在本发明中,放置于厌氧下是指,例如优选进行氮气置换使上部空间(headspace)中的氧浓度为零,或者使用培养罐时,将其放置于菌悬液中的D.O.值(溶解氧浓度)为1.0ppm以下的条件下,作为特别优选的方法,例如可列举出将菌悬液放置于通过用氮气进行置换从而将D.O.值(溶解氧浓度)调节至0.5ppm以下的厌氧条件下的方法等,但并不限定于此。
在本发明中,放置菌悬液是指,例如将菌与不含糖的溶剂(其中,不包括纯化水及生理盐水)或含DMEM及Ham’s F-12的溶剂混合后,不对菌悬液和/或装有菌悬液的容器进行任何操作,进行静置。静置时间没有特别限定,例如可以是30分钟以上、1小时以上、6小时以上等,也可以是24小时以下、3天以下等。此外,静置菌悬液时的温度没有特别限定,例如只要为菌能够繁殖的温度即可。静置菌悬液时的条件取决于菌的性质等,例如可以是好氧条件下,也可以是厌氧条件下等。
在本发明中,过滤器为筛孔的大小能够将菌过滤的过滤器即可,例如可以使用市售的0.1μm~1μm(例如,0.22μm)的过滤器。
在本发明中,例如也可以进一步包含对滤液的处理物进行浓缩、粉末化、冷冻干燥等的工序。
在本发明中,不含发酵工序是指,例如乳酸菌不进行发酵,在进行制备方法中的所有工序后所得到的处理物中,不含因乳酸菌而产生的发酵后的代谢产物等。
在本发明中,判断有无由乳酸菌造成的发酵的方法没有特别限定,例如有以下方法:制作菌悬液,然后在放置菌悬液的工序的前后,测定菌悬液的pH,将与放置前的pH值相比放置后的pH值下降的情况(酸性侧的pH值发生变化)判断为有发酵,不包含在本发明中。
本发明包含向动物给药双歧杆菌(Bifidobacterium)属或乳酸杆菌(Lactobacillus)属的菌或其处理物从而使氯离子通道活化的方法、预防或治疗肾脏疾病的方法或者促进排便的方法。
本发明还包含用于制备氯离子通道的活化剂、肾脏疾病的预防或治疗药或者排便促进剂的、双歧杆菌(Bifidobacterium)属或乳酸杆菌(Lactobacillus)属的菌或其处理物的应用。
本发明进一步包含用于氯离子通道的活化、肾脏疾病的预防或治疗或者促进排便的双歧杆菌(Bifidobacterium)属或乳酸杆菌(Lactobacillus)属的菌或其处理物。
本发明还包含用于动物中的氯离子通道的活化、肾脏疾病的预防或治疗或者促进排便的双歧杆菌(Bifidobacterium)属或乳酸杆菌(Lactobacillus)属的菌或其处理物的应用。
实施例
以下,通过实施例对本发明进行详细说明,但是这些实施例是本发明的一个例子,本发明的技术范围并不限定于此,对于具备本领域中的通常知识的技术人员而言,可在本发明的技术构思内进行各种变形。
[实施例1](菌处理物的制备)
作为属于双歧杆菌(Bifidobacterium)属或乳酸杆菌(Lactobacillus)属的菌,使用以下菌:
长双歧杆菌(B.longum):
ID1001(MM-2,保藏编号:NITE BP-818)、JCM1217(ID1100T)、ID1163、ID1164、ID1165、ID1166、ID1167、ID1168、ID1170、ID8009、CLA8013(保藏编号:NITE BP-02352);
两歧双歧杆菌(B.bifidum):
ID1000、ID1077、ID1078、JCM1255(ID1079T)、ID1080、ID1127、ID1129、ID1130、ID1131、ID1188、ID1189、ID8005、ID8007;
加氏乳杆菌(L.gasseri):
ID2000、JCM1131(ID2151T)、ID2089、ID2092、ID2093、ID2100、ID2101、ID2124、ID2144、JCM5813(ID2145)、ID2146;
约氏乳杆菌(L.johnsonii):
JCM2012(ID2153T)、ID2091、ID2095、ID2096、ID2126、ID2142、ID2143、ID2154;
嗜酸乳杆菌(L.acidophilus):
JCM1132(ID2152T)、ID2073、ID2107、ID2109、ID2110;
副干酪乳杆菌副干酪亚种(L.paracasei subsp.paracasei):
JCM8130(ID2148T)、ID2003、ID2004、ID2005、ID2012、ID2013、ID2014、ID2019、ID2031、ID2032、ID2033。
其中,B.longum JCM1217(长双歧杆菌JCM1217)(ID1100T)、B.bifidum JCM1255(两歧双歧杆菌JCM1255)(ID1079T)、L.gasseri JCM5813(加氏乳杆菌JCM5813)(ID2145)、L.gasseri JCM1131(加氏乳杆菌JCM1131)(ID2151T)、L.johnsonii JCM2012(约氏乳杆菌JCM2012)(ID2153T)、L.acidophilus JCM1132(嗜酸乳杆菌JCM1132)(ID2152T)、L.paracasei subsp.paracasei JCM8130(副干酪乳杆菌副干酪亚种JCM8130)(ID2148T)为各个菌种的标准菌株。
使用10mL的含1%葡萄糖、0.1%吐温80的GAM(Nissui Pharmaceuti cal Co.,Ltd.)培养基,在37℃下对各菌株的冷冻保藏菌株(约1×106~1×108个)进行18~30小时的厌氧培养。培养后,进行离心(3,000×G,10min.,R.T.)并丢弃上清液,用PBS(-)洗涤后,再次混悬于10mL的DMEM/F-12(赛默飞世尔科技公司制造)中,在37℃、厌氧条件下放置24小时后,离心并用过滤器(0.22μm)过滤上清液,制备滤液作为菌处理物(抽提物:以下有时简写为E)。
(细胞培养)
用含10%FBS、青霉素〃链霉素的DMEM/F-12培养株化人结肠上皮细胞T84,以4×104细胞/cm2进行播种并每隔5~7天进行继代培养。以5×105细胞/孔播种于膜嵌套(snapwell)(corning,costar、1.13cm2)并每隔3天更换培养基,将培养了5~7天的细胞用于试验。
(短路电流法)
短路电流法中使用尤斯灌流室系统(Ussing chamber system)(Physiologic Instruments公司制造)进行测定。将为单层(monolayer)的T84细胞连同膜嵌套(snapwell)垂直设置在尤斯灌流室(Ussing chamber)中,将5ml的保温为37℃的克雷布-林格液(Krebs-Ringer液)充满粘附有T84细胞的膜嵌套的左右,放置20分钟以上,待经由T84细胞膜的电流值(Isc)稳定后,开始试验。将100μL的菌处理物添加在相当于T84细胞的黏膜侧的上侧(相对于膜嵌套,为与粘附有细胞的面相反的一侧),然后观察Isc的变化(ΔIsc),比较跨细胞离子分泌的变化。ΔIsc为在添加检体后、变化最大的Isc值与添加检体时(0小时)的Isc值的差。
(菌处理物的离子跨细胞转运能力)
肠内的水分含量影响内容物的硬度或肠内移动,是便秘或者腹泻的原因之一。由于肠道中水的分泌吸收与经由存在于肠道上皮的氯离子通道的氯离子的移动同步发生,因此氯离子的移动成为了水的移动的指标。因此,使用肠道上皮细胞(T84细胞),通过使用了尤斯灌流室(Ussing chamber)的短路电流法研究菌中的离子的跨细胞转运能力。将通过使用了T84细胞的短路电流法测定的、基于各菌处理物的离子的跨细胞转运能力的结果示于图1(Bifidobacterium)、图2(Lactobacillus)。在B.longum CLA8013(长双歧杆菌CLA8013)的菌处理物中显示最大ΔIsc。
此外,将作为氯离子通道抑制剂的CFTRinh172(Sigma C992-25MG)10mM(DMSO溶解)以成为5μL/5mL克雷布-林格液(终浓度10μm)的方式处理于T84细胞的黏膜侧,2分钟后将100μL的B.longum CLA8013的菌处理物添加至T84细胞的黏膜侧。未用CFTRinh172处理(DMSO处理)时的B.longum CLA8013的菌处理物的ΔIsc为11.38μA,而用CFTRinh172处理时的B.longum CLA8013的菌处理物的ΔIsc为3.50μA,通过氯离子通道抑制剂,B.longum CLA8013的菌处理物的作用减弱。该结果显示,长双歧杆菌B.longum CLA8013的菌处理物在肠道中使氯离子通道活化。由此可知,由于菌处理物具有氯离子通道活化作用,因此具有由促进水分分泌而带来的促进排便的作用。
[实施例2](菌处理物的制备)
菌(Bifidobacterium longum CLA8013)处理物的制备方法
使用10mL的含1%葡萄糖、0.1%吐温80的GAM(Nissui Pharmaceutical Co.,Ltd.)培养基,在37℃下对菌株B.longum CLA8013的冷冻保藏菌株(约1×108个)进行30小时的厌氧培养。培养后,进行离心(3,000×G,10min.,R.T.)并丢弃上清液,用PBS(-)洗涤后,再次混悬于10mL的PBS(-)中,在37℃、厌氧条件下放置24小时后,离心并用过滤器(0.22μm)过滤上清液,得到滤液作为菌(B.longum CLA8013)处理物(8013E)。
将以使吸光度260nm为33的方式用PBS(-)稀释8013E而成的物质作为8013E(10)、以使吸光度260nm为3.3的方式用PBS(-)稀释8013E而成的物质作为8013E(1)。
(菌(B.longum CLA8013)处理物对慢性肾脏病模型小鼠的改善作用)
1.对慢性肾脏病模型小鼠的菌处理物的给药
以图3所示的时间表实施试验。用普通饲料(CE-2,CLEA Japan,Inc.制造)饲养雄性C57BL/6小鼠(CLEA Japan,Inc.)直至6周龄。7周龄时,分为用普通饲料饲养的普通饲料组(Normal)和用含有0.2%腺嘌呤(和光公司制造)的普通饲料(腺嘌呤食物)饲养的腺嘌呤食物饲料组而进行饲养。6周后,正常(Normal)组用灌胃针以0.2mL/只、1天1次强制口服给药PBS(-)12天。
腺嘌呤食物饲料组在6周的腺嘌呤食物饲养后,恢复为普通饲料,分为PBS(-)给药组(RF)、菌(B.longum CLA8013)处理物给药组(RF+8013E(1)、RF+8013E(10)),RF组、RF+8013E(1)及RF+8013E(10)组分别用灌胃针以0.2mL/只、1天1次的用量强制口服给药PBS(-)、8013E(1)及8013E(10)12天。
在最终给药18小时后进行解剖。
2.血清BUN的测定
将使用DetectX尿素氮检测试剂盒(Urea Nitrogen Colorimetric Detection Kit)(ARBOR ASSAYS公司制造)测定的各组小鼠血清中BUN(尿素氮)的结果示于图4。各组分别测定5只或者6只。得到的结果以平均值±标准偏差(mean±S.D.)表示(*:p<0.05vs正常组,#:p<0.05vsRF,Steel-Dwass法)。确认到与正常组相比,RF组中作为肾功能的指标的血清BUN浓度上升。与RF组相比,RF+8013E(1)及RF+8013E(10)组的血清BUN浓度降低,能够确认到8013E的剂量依赖性效果,能够确认到RF+8013E(10)组与RF组有显著差异。该结果显示8013E改善肾功能。另外,确认到试验期间的体重因腺嘌呤食物饲养而减少,在开始试验药物给药时通过将饲料恢复至普通饲料体重得以恢复,然而即使给药8013E也没有确认到对体重恢复的影响,与RF组显示相同的倾向。
[实施例3](菌处理物的制备)
菌(Bifidobacterium longum CLA8013)处理物的制备方法
使用10mL的含1%葡萄糖、0.1%吐温80的GAM(Nissui Pharmaceutical Co.,Ltd.)培养基,在37℃下对菌株B.longum CLA8013的冷冻保藏菌株(约1×108个)进行30小时的厌氧培养。培养后,进行离心(3,000×G,10min.,R.T.)并丢弃上清液,用PBS(-)洗涤后,再次混悬于10mL的PBS(-)中,在37℃、厌氧条件下放置24小时后,离心并用过滤器(0.22μm)过滤上清液,得到滤液作为菌(B.longum CLA8013)处理物(8013E)。
(菌处理物的总肠道转运能力)
1.对SD大鼠的菌(B.longum CLA8013)处理物的给药
分别对雄性6周龄SD大鼠(Japan SLC,Inc.制造)进行1周的预备饲养。预备饲养后,分组为正常组和8013E组。正常组以0.5mL/只的剂量强制口服给药PBS(-)1次、8013E组以0.5mL/只的剂量强制口服给药8013E 1次。给药结束后,以1mL/只的剂量强制口服给药洋红{(Ca-rmine)(WAKO)3g/50mL(0.5%羧甲基纤维素)}水溶液1次。
2.大鼠总肠道转运能力的测定(图5)
给药洋红溶液后,分别测定各组中8只的排出染成红色的粪便的时间(*:p<0.05vs对照组(曼-惠特尼U检验(Mann-Whitney’s U test)))。得到的结果以平均值±标准偏差表示。与正常组相比,8013E组的红色粪便排出时间显著缩短,确认到了由8013E带来的促进排便的效果。
[实施例4](溶剂种类对离子跨细胞转运能力的影响)
(菌处理物的制备)
菌(B.longum CLA8013)处理物的制备方法
使用10mL的含1%葡萄糖、0.1%吐温80的GAM(Nissui Pharmaceutical Co.,Ltd.)培养基,在37℃下对菌株B.longum CLA8013的冷冻保藏菌株进行30小时的厌氧培养。培养后,进行离心(3,000×G,10min.,R.T.)并丢弃上清液,用PBS(-)洗涤后,再次混悬于10mL的各溶剂(纯化水、生理盐水、DMEM/F-12或PBS(-))中,在37℃、厌氧条件下放置24小时后,离心并用过滤器(0.22μm)过滤上清液,制备滤液作为菌(B.longum CLA8013)处理物(8013E)。
(细胞培养)
用含10%FBS、青霉素〃链霉素的DMEM/F-12培养株化人结肠上皮细胞T84,以4×104细胞/cm2进行播种并每隔5~7天进行继代培养。以5×105细胞/孔播种于膜嵌套(snapwell)(costar,1.13cm2)并每隔3天更换培养基,将培养了5~7天的细胞用于试验。
(短路电流法)
以与实施例1的短路电流法相同的方法求出ΔIsc。
(菌(B.longum CLA8013)处理物的离子跨细胞转运能力)
将结果示于图6。菌处理物制造中使用的溶剂为PBS(-)时,菌处理物的离子跨细胞转运能力最高,其次,使用的溶剂为DMEM/F-12时,菌处理物的离子跨细胞转运能力较高。根据这些结果确认到:通过使菌体混悬于PBS(-),可制备效果更高的处理物。此外,将菌体混悬于DMEM/F-12并放置时,pH没有变化。根据该结果可知,基于菌体的发酵与由菌处理物带来的离子跨细胞转运能力的增加无关。
混悬于不含糖的DMEM/F-12时,也确认到了菌处理物的离子跨细胞转运能力变高。
[实施例5](菌的制备)
菌(B.longum MM-2(长双歧杆菌MM-2):ID1001)的制备方法
利用与实施例2同样的方法,对菌(B.longum MM-2)进行12~18小时的厌氧培养。然后使用PBS(-)以菌数成为5×109个/mL的方式制备并使用回收的菌体。
(菌体(B.longum MM-2)对慢性肾脏病模型小鼠的改善作用)
利用与实施例2同样的时间表及方法,以菌数1×109个/0.2mL/只的剂量对小鼠给药制备后的菌体,并在最终给药的18小时后进行解剖。然后,利用与实施例2中记载的方法同样的方法,分别测定各组中5只或10只的血清BUN。将测定结果示于图7。得到的结果以平均值±标准偏差表示(**:p<0.01vs正常组,#:p<0.05vsRF)。确认到与正常组相比,RF组中作为肾功能的指标的血清BUN浓度上升。与RF组相比,RF+MM-2组的血清BUN浓度降低。该结果显示MM-2菌体改善肾功能。另外,确认到试验期间的体重因腺嘌呤食物饲养而减少,在开始试验药物给药时通过将饲料恢复至普通饲料体重得以恢复,然而即使给药MM-2菌体也没有确认到对体重恢复的影响,与RF组显示相同的倾向。
在本发明中,认为:例如若给药的菌或其处理物具有长双歧杆菌MM-2菌株所具有的程度的离子跨细胞转运能力,则通过给药该菌或其处理物,存在能够改善肾功能的可能性。
本发明暗示了:例如使用未发酵的菌时,即使作为含有菌的处理物而给药,也能够改善肾功能。
以下,例示出掺合有本发明的对肠道的离子跨细胞转运体的作用剂、氯离子通道活化剂、肾脏疾病的预防或治疗剂和/或排便促进剂的药品、饮食品及饲料的具体的处方。各处方例的右侧的数值是指各含有成分的质量%。
处方例1:药品(片剂)
处方例3:饮食品(健康饮品)
处方例6:饲料(家畜用饲料)
掺合饲料 97.5%
菌(Bifidobacterium longum CLA8013)处理物 2.5%
工业实用性
本发明的剂对氯离子通道的活化、肾脏疾病的预防或治疗和/或促进排便是有用的,可以用作药品、补剂等。
- 还没有人留言评论。精彩留言会获得点赞!