一种抗肿瘤疫苗复合物及制备方法、注射剂及应用与流程
本发明涉及抗肿瘤领域,更特别地,涉及一种抗肿瘤疫苗复合物及制备方法、注射剂及应用。
背景技术:
化疗、放疗、靶向治疗等是治疗肿瘤的常规治疗方法,但其总体的治疗效果有限,且容易出现耐药或者治疗抵抗。恶性肿瘤常具备侵袭性和易复发的生物学特征,同时肿瘤组织存在着极其复杂的免疫抑制性微环境,因此需要设计靶向性更强、毒副作用更小、且能改善免疫微环境的个体化治疗方案。随着肿瘤基因组学和免疫学的快速发展,免疫疗法已成为最有潜力的肿瘤治疗手段。由于肿瘤细胞含有肿瘤抗原,机体的免疫系统能通过识别肿瘤抗原将肿瘤细胞和正常细胞区分开,进而实现特异性的清除。肿瘤疫苗是将肿瘤抗原以多种形式,如肿瘤细胞裂解液、肿瘤相关蛋白或抗原多肽以及表达肿瘤抗原的相关基因等方式导入患者体内,同时在细胞因子、趋化因子等佐剂的辅助下,通过克服肿瘤微环境中的免疫抑制状态,增强免疫原性,激活患者自身的免疫系统,诱导机体产生细胞免疫和体液免疫,从而达到控制或清除肿瘤的目的。目前,肿瘤疫苗已成为肿瘤治疗领域的研究热点。
目前临床已经获批的肿瘤疫苗包括树突状细胞(dc)疫苗sipuleucel-t(provenge)和宫颈癌疫苗,而个体化疫苗仅有sipuleucel-t疫苗。dc作为已知的功能最强的专职抗原递呈细胞,是引发抗肿瘤免疫应答的关键细胞。事实上,肿瘤微环境中的dc浸润较少且大多处于非功能状态,因此将载有肿瘤抗原的自体来源的dc进行体外培育和扩增,通过产生大量的dc肿瘤疫苗,是提高机体抗肿瘤免疫应答的有效途径。2010年4月,美国fda批准了以dc为主要效应细胞的自体细胞免疫治疗药物sipuleucel-t,以治疗轻微症状的转移性去势抵抗性前列腺癌。但是sipuleucel-t疫苗疗效较差,激活效率低、不精确、抗原少,且价格昂贵。
肿瘤裂解液是目前比较有潜力的肿瘤疫苗成分。肿瘤裂解物由外科手术切除后获得的自体肿瘤细胞将患者肿瘤细胞体外裂解以产生细胞碎片。理论上,肿瘤裂解液将含有大量和广谱的肿瘤抗原,但是肿瘤裂解液在机体的利用率极低且免疫原性较弱,因此难以作为有效的肿瘤疫苗。
因此,探索免疫激活能力强、抗原谱广泛的个体化疫苗仍是我们的重要努力方向。
技术实现要素:
为解决以上问题,本发明提供了一种抗肿瘤疫苗复合物及制备方法、注射剂及应用,解决现有疫苗疗效较差,激活效率低、不精确、抗原少,且价格昂贵等问题。
一种抗肿瘤疫苗复合物,由富含ros的细胞微泡和免疫激活剂物理混合制得。
所述富含ros的细胞微泡内的活性氧含量不低于细胞内活性氧含量。
所述富含ros的细胞微泡的粒径为100-1000纳米。
一种抗肿瘤疫苗复合物的制备方法,包括以下步骤:
1):获取新鲜肿瘤组织后进行原代肿瘤细胞培养,获得原代肿瘤细胞;
2):使用x线或电子线照射原代肿瘤细胞,使肿瘤细胞胞内大量富集ros,并分泌出含高浓度ros的微泡;
3):收集含ros的肿瘤细胞微泡;
4):向步骤3)中的微泡中加入免疫激活剂进行物理混合。
所述步骤4)中的免疫激活剂为cpg或氢氧化铝佐剂。
所述免疫激活剂为cpg时,在所述步骤4)中混合后的浓度为100~500μg/ml;所述免疫激活剂为氢氧化铝佐剂时,在所述步骤4)中混合后的浓度为10~20mg/ml。
所述步骤1)中的肿瘤组织为自体离体肿瘤组织。
一种抗肿瘤疫苗复合物注射剂。
一种抗肿瘤疫苗复合物的应用,包括应用于肺癌、乳腺癌、脑胶质瘤、卵巢癌、胃癌、结直肠癌、骨肉瘤、前列腺癌、宫颈癌、恶性胸腔积液或黑色素瘤等肿瘤。
优选地,所述富含ros的微泡由x线或电子线体外照射自体来源的肿瘤细胞产生。
优选地,所述微泡放疗剂量为8-20gy。
优选地,所述微泡收集时间为放疗后的第2-7天。
本发明具有以下优点:
①可利用肿瘤病人术后或者穿刺标本,实现个体化肿瘤治疗;
②相较于放疗,本技术可通过皮内经淋巴系统注射反复多次给药,具有和安全等优点;
③相较于化疗,本技术主要通过激活机体自身免疫系统,不含任何化疗药物,生物安全性较好。
④制备工艺简单,便于规模化生产;
⑤本发明制得的药剂可应用于各种实体肿瘤,是一种广谱性的抗肿瘤疗法。
附图说明
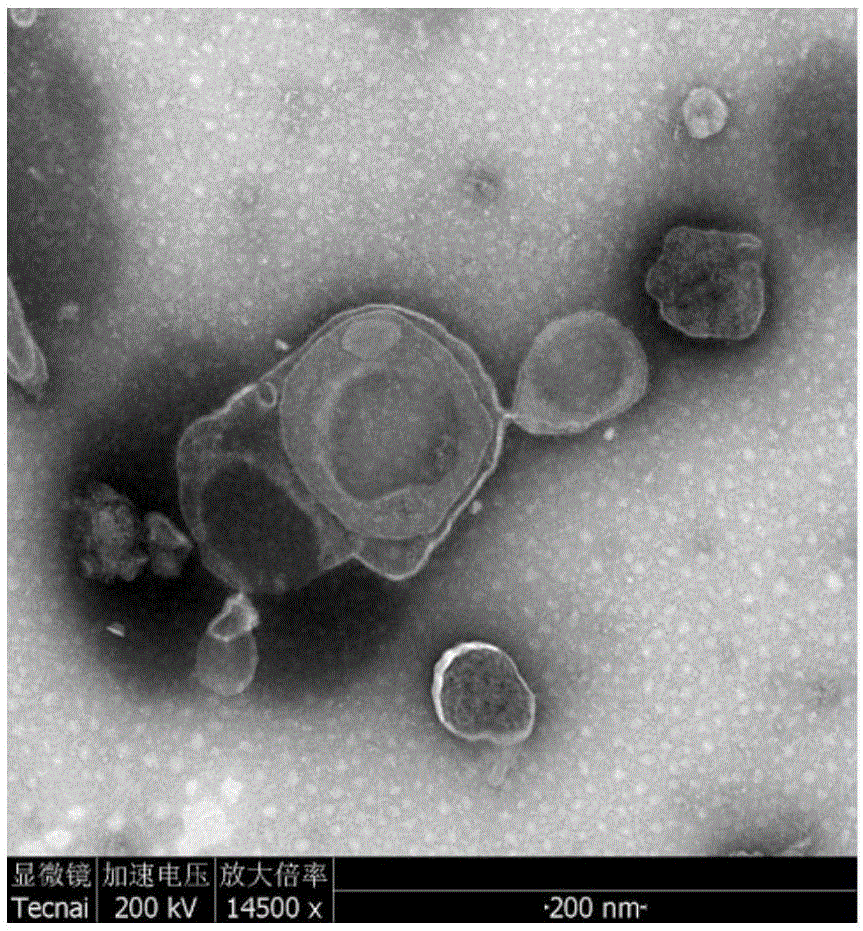
图1为本发明放疗产生微泡的电镜图;
图2为本发明对照组和微泡组中bmdc表面活化标志物cd86表达的数目分布图;
图3为本发明对照组和微泡组中bmdc以表面活化标志物mhcⅱ表达的数目分布图;
图4为本发明放疗微泡和紫外微泡中的ros含量对比;
图5为本发明肿瘤细胞和放疗微泡中的ros含量对比;
图6为本发明放疗微泡与紫外微泡或肿瘤裂解液在肿瘤预防中的作用对比;
图7为本发明抗肿瘤疫苗复合物联合pd-1单抗治疗lewis皮下瘤的肿瘤体积变化;
图8为本发明抗肿瘤疫苗复合物联合pd-1单抗治疗lewis皮下瘤的小鼠生存。
具体实施方式
以下结合实例对本发明的原理和特征进行描述,所举实例只用于解释本发明,并非用于限定本发明的范围。
一种抗肿瘤疫苗复合物,由富含ros的细胞微泡和免疫激活剂物理混合制得。
所述富含ros的细胞微泡内的活性氧含量不低于细胞内活性氧含量。
所述富含ros的细胞微泡的粒径为100-1000纳米。
一种抗肿瘤疫苗复合物的制备方法,包括以下步骤:
1):获取新鲜肿瘤组织后进行原代肿瘤细胞培养,获得原代肿瘤细胞;
2):使用x线或电子线照射原代肿瘤细胞,使肿瘤细胞胞内大量富集ros,并分泌出含高浓度ros的微泡;
3):收集含ros的肿瘤细胞微泡;
4):向步骤3)中的微泡中加入免疫激活剂进行物理混合。
所述步骤4)中的免疫激活剂为cpg或氢氧化铝佐剂。
所述免疫激活剂为cpg时,在所述步骤4)中混合后的浓度为100~500μg/ml;所述免疫激活剂为氢氧化铝佐剂时,在所述步骤4)中混合后的浓度为10~20mg/ml。
所述步骤1)中的肿瘤组织为自体离体肿瘤组织。
一种抗肿瘤疫苗复合物注射剂。
一种抗肿瘤疫苗复合物的应用,包括应用于肺癌、乳腺癌、脑胶质瘤、卵巢癌、胃癌、结直肠癌、骨肉瘤、前列腺癌、宫颈癌、恶性胸腔积液或黑色素瘤等肿瘤。
比较多种方式处理肿瘤细胞而产生的微泡或者肿瘤裂解液,结果放疗产生的肿瘤来源的微泡具有最佳的预防肿瘤发生的效果。在下文中,设置实施例以验证本发明。本发明的所述放疗微泡的结构如图1所示。
本发明原理为:在使用放疗照射肿瘤细胞后,细胞将大量分泌富含ros的微泡。联合富含ros的细胞微泡和免疫激活剂共同皮内注射荷瘤小鼠后,能产生较强的体外和淋巴结内dc激活效应,相比较紫外线照射获得的微泡,本发明提供的抗肿瘤疫苗复合物能大幅提升预防模型中的肿瘤复发率。同时,在肿瘤治疗模型中,抗肿瘤疫苗复合物并未产生抗肿瘤效应,仅仅在与pd-1单抗联合后才能引起较强的抗肿瘤效应,且该效应远远强于单独的pd-1单抗组。
在肿瘤放疗过程中,其在体效应很大程度上是依靠直接或间接产生大量活性氧(reactiveoxygenspeties,ros)进而造成肿瘤细胞dna损伤。体外实验表明,在一定放射剂量条件下,肿瘤细胞能分泌大量的微泡,且该微泡含有大量的ros。微泡能在特定刺激条件下由活细胞分泌出,其直径为100~1000nm的微囊泡结构。微泡富含蛋白质、dna、rna和各类脂质等生物活性分子,其参与了细胞之间的信息传递。获得肿瘤组织标本,原代培养获得肿瘤细胞,利用放疗照射获得含有大量ros的微泡,将这些微泡与免疫激活剂回输作用于机体的淋巴结,将极大增强pd-1/pd-l1单抗的功效。
以下结合实验对本发明作进一步说明。
1.构建具有杀伤效应的放疗微泡以及保存
在直径为10cm的培养皿中培养肿瘤细胞,待细胞融合度达70%时,进行20gy单次或8gy×3次(每天8gy,连续3天)x线或电子线放射,24h后换液20ml,于放疗后72h时,收集细胞培养上清,采用梯度离心法提取微泡,即:先1000g离心10min以去除残留细胞,随后离心14000g、2min除去碎片成分,然后留上清离心14000g60min,弃上清,沉淀即为所需要的微泡,将微泡用生理盐水洗2遍,最后加1ml的pbs重悬置于4℃备用,3天内使用最佳。如图1所示,电镜下可见微泡为球形颗粒物,直径为100nm-1000nm之间。
2.放疗微泡体外激活小鼠骨髓来源树突状细胞(bmdc)
无菌条件下提取雄性7-8周小鼠的骨髓,在体外用20ug/mlgm-csf刺激7天后,即可获得bmdc,将bmdc加到六孔板中,5×105/孔,向每孔中加入上述微泡悬液100μl.继续在培养箱中培养24h后,通过流式细胞仪检测dc细胞活化的标志物cd80、cd86、mhcⅱ、ccr7的表达。如图2所示,cd86、mhcⅱ表达显著升高,证明放疗微泡在体外能显著激活小鼠骨髓来源树突状细胞(bmdc)。
3.放疗微泡的ros检测
按照上述方法获得微泡后,将终浓度为10μm的dcfh-da加到微泡沉淀中重悬。37℃孵育10min,再用无血清培养基洗涤3次,充分去除未被摄入微泡里的dcfh-da。通过流式细胞术检测微泡中ros的含量。如图3所示,放疗产生的微泡中ros的含量为正常细胞的350余倍,为紫外产生的微泡中ros含量的10倍以上。
4.放疗微泡抗肿瘤疫苗复合物的制备
向以上放疗微泡溶液中加入免疫佐剂cpg或氢氧化铝佐剂,使cpg终浓度为300μg/ml或氢氧化铝佐剂浓度为10-20mg/ml,充分混匀后,即为抗肿瘤疫苗复合物。
5.抗肿瘤疫苗复合物联合pd-1单抗治疗实体瘤的动物实验
建立c57小鼠皮下lewis肺癌移植瘤模型:以每只鼠5×105个lewis细胞的接种量种植于c57小鼠右侧大腿皮下,待肿瘤体积达到约30mm3(大约肿瘤接种后7天)时,于足垫和尾根部各接种抗肿瘤复合物25μl,腹腔注射pd-1单抗200ug/只,每2天给药一次,共给药3次。每2天测量肿瘤体积一次。如图4-5所示,抗肿瘤疫苗复合物可以显著增强pd-1单抗的抗肿瘤功效。
以上所述仅为本发明的较佳实施例,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!