一种银纳米团簇-铁蛋白新型仿生药物的制备方法、药物及应用与流程
1.本发明属于生物医药领域,具体地说,涉及一种银纳米团簇-铁蛋白新型仿生药物的制备方法、药物及应用。
背景技术:
2.贵金属团簇由于其独特的几何结构和新颖的功能,已经成为新型功能纳米材料,在生物医学工程等领域有非常重要的作用。贵金属团簇如au、ag或pt等在几十个原子形成的纳米粒径尺度下,具有宏观贵金属物质不具备的表面效应、小尺寸效应和宏观量子隧道效应等,展现出强大的光学、热学、电化学和催化特性,通过可控调节纳米团簇的生长、尺寸、空间结构等,可以有效调节其与结构相关的物理、化学和生物学功能。
3.其中,纳米银材料已在妇科、泌尿外科、皮肤科和烧伤外科治疗中作为高效抗菌治疗剂用于临床治疗,在近年来的研究中,更是展现出高效对抗多种病毒(如hbv、aiv、hiv等)的功效。但是,由于银纳米团簇在水溶液中倾向于聚集,合成稳定长效的纳米银团簇具有高度挑战性,因此如何提高纳米银材料的安全性使之有效应用于人体尤为重要。
4.铁蛋白是在动植物、微生物体内广泛存在的一种可溶性储铁蛋白。生命体内的铁蛋白主要由蛋白质外壳和水合氧化铁核两部分构成,典型的铁蛋白是由二十四个亚基组成的高度对称的中空的球形结构。这种球形中空结构具有三个界面:内表面、外表面以及亚基之间的接触面。外表面可用于连接具有特殊功能的配体,内表面可作为纳米反应器用于纳米复合材料的合成,亚基之间的接触面则可用于指导铁蛋白的解聚与重组、合成不同亚基比例的铁蛋白及打破铁蛋白的对称性结构。
5.以人源天然生物蛋白质为模板仿生合成新型有机-无机杂化纳米药物是一种有效的路径,此方法构建的复合纳米药物既具备高度稳定性、高度生物相容性和安全性,又具有无机纳米材料的独特物理化学特性。
6.有鉴于此特提出本发明。
技术实现要素:
7.本发明要解决的技术问题在于克服现有技术的不足,提供一种银纳米团簇-铁蛋白新型仿生药物的制备方法、药物及应用。采用本发明的制备方法,可控合成不同尺径的银纳米团簇-铁蛋白新型仿生药物,且药物纯度高、具备高度稳定性和长效性、高度生物相容性和安全性。
8.为解决上述技术问题,本发明采用技术方案的基本构思是:
9.本发明的第一目的在于提供一种银纳米团簇-铁蛋白新型仿生药物的制备方法,包括:
10.(1)制备铁蛋白;
11.(2)将铁蛋白与含银离子的溶液混合形成混合溶液,孵育;
12.(3)添加还原剂至混合溶液,混匀,调节ph,孵育;
13.(4)反应结束后超滤去除还原剂,纯化,获得银纳米团簇-铁蛋白新型仿生药物。
14.本发明以天然生物蛋白为界面配体,在蛋白的氧化酶还原位点上,可控合成不同尺径银纳米团簇。全重链铁蛋白具有24个亚基的中空球形结构,外径约为12nm,内径约为8nm。每两个亚基彼此平行,首尾相对,由中部的活性氨基酸残基形成一个亚铁氧化酶还原位点,可作为贵金属团簇例如银纳米团簇的成核点,全重链铁蛋白共有24个亚铁氧化酶还原位点,根据蛋白质结构分子动力学模拟计算,在全重链铁蛋白的限域空间内,最多可合成12个银纳米团簇,如图1所示。
15.本发明的银纳米团簇-铁蛋白新型仿生药物的制备方法中,步骤简单,将铁蛋白与含银离子的溶液混合形成混合溶液后,加入还原剂,并通过调节反应物浓度、摩尔比、温度、ph和反应周期时长,可以实现银纳米团簇在成核位点的“点控制”生长,得到一系列不同尺径的银纳米团簇-铁蛋白复合药物,且得到的药物具有纯度高、生物相容性好、合成均一的优势,新型复合药物长效性和生物相容性大大提高,且在抗菌、抗病毒领域具有非常大的应用潜力。
16.进一步的方案,步骤(2)中,所述含银离子的溶液选自硝酸银溶液、氟化银溶液、银氨溶液中的至少一种。
17.进一步的方案,步骤(2)中,所述含银离子的溶液为硝酸银溶液,加入的硝酸银与铁蛋白的摩尔比为200-1500:1;
18.优选的,加入的硝酸银与铁蛋白的摩尔比为300-1200:1。
19.本发明的制备方法中,为了控制合成不同尺径的贵金属团簇需要精细的条件调控,若反应摩尔比如过高,或温度过高,反应体系则会出现杂质,形成不均一的、大的银颗粒;反应摩尔比过小,或温度过低,反应时间不足,则反应不充分,不能合成符合要求大小的银团簇。
20.进一步的方案,步骤(2)中,所述铁蛋白的初始溶液的浓度为70-150pm;
21.优选的,铁蛋白的初始溶液的浓度为90-120pm,更优选100pm;
22.所述铁蛋白选自全重链人源铁蛋白。本发明中采用天然全重链铁蛋白,已有天然的成核位点,并采用分子动力学模拟成核的位置和数量,生物兼容性更高。
23.进一步的方案,步骤(3)中,所述还原剂选自硼氢化钠、抗坏血酸中的至少一种;
24.优选的,所述还原剂为硼氢化钠;
25.优选的,加入的硼氢化钠与铁蛋白的摩尔比为150-200:1。
26.进一步的方案,步骤(3)中,根据需要获取的银纳米团簇的尺径调整孵育时间;
27.优选的,需要获取的银纳米团簇的尺径为1-4nm,孵育时间为2-50h。
28.进一步的方案,步骤(2)和步骤(3)中,孵育的温度为37℃。
29.进一步的方案,步骤(3)中,调节ph至8.5-9.0;
30.优选的,调节ph至8.5。
31.本发明的第二目的在于提供一种采用如上任意一种方案或者组合方案所述的制备方法制备的银纳米团簇-铁蛋白新型仿生药物。
32.本发明的第三目的在于提供一种如上任意一种方案或者组合方案所述的银纳米团簇-铁蛋白新型仿生药物在抗菌、和/或抗病毒方面的应用。
33.优选的,所述的抗病毒方面的应用包括抗乙肝病毒。
34.采用上述技术方案后,本发明与现有技术相比具有以下有益效果:
35.1、采用本发明的制备方法,可控合成不同尺径的银纳米团簇-铁蛋白新型仿生药物,且药物纯度高、具备高度稳定性和长效性、高度生物相容性和安全性。
36.2、本申请的银纳米团簇-铁蛋白新型仿生药物在广谱抗菌、抗病毒等领域具有非常大的应用,例如在抗乙肝病毒方面效果特别优异。
37.下面结合附图对本发明的具体实施方式作进一步详细的描述。
附图说明
38.附图作为本发明的一部分,用来提供对本发明的进一步的理解,本发明的示意性实施例及其说明用于解释本发明,但不构成对本发明的不当限定。显然,下面描述中的附图仅仅是一些实施例,对于本领域普通技术人员来说,在不付出创造性劳动的前提下,还可以根据这些附图获得其他附图。在附图中:
39.图1是本发明以全重链人源铁蛋白为界面配体的银纳米团簇结构设计示意图;
40.其中,1为人源铁蛋白,2为银纳米团簇;
41.图2是本发明不同尺径的银纳米团簇-铁蛋白仿生药物的合成过程中不同孵育时间下溶液颜色变化示意图;
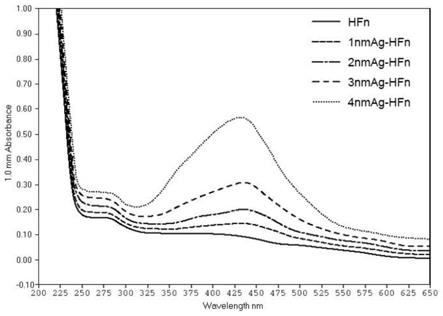
42.图3是本发明不同尺径的银纳米团簇-铁蛋白仿生药物的吸收峰的示意图;
43.图4是本发明典型的银纳米团簇-铁蛋白仿生药物的冷冻电镜成像图。
44.需要说明的是,这些附图和文字描述并不旨在以任何方式限制本发明的构思范围,而是通过参考特定实施例为本领域技术人员说明本发明的概念。
具体实施方式
45.为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例中的附图,对实施例中的技术方案进行清楚、完整地描述,以下实施例用于说明本发明,但不用来限制本发明的范围。
46.实施例1
47.1、制备全重链人源铁蛋白
48.选择全重链人源铁蛋白,其ncbi基因序列号为:2495。扩增获得全重链人源铁蛋白基因片段后,按照常规的基因重组方法构建含有全重链人源铁蛋白基因片段的表达载体,转入到大肠杆菌中,获得重组大肠杆菌。
49.重组大肠杆菌在37℃发酵培养,od值达到0.6-0.8时加入0.4mmiptg诱导4小时过量表达,经过离子交换柱和分子筛、纯化得到全重链人源铁蛋白,纯度可达95%以上,1l菌液可得纯化的全重链人源铁蛋白20mg以上。
50.2、将获得的全重链人源铁蛋白稀释,获得浓度为100pm的全重链人源铁蛋白溶液加入反应管中,再加入硝酸银;其中,硝酸银和铁蛋白按照300:1的摩尔比混合,37℃振荡孵育2小时;
51.3、反应管中加入硼氢化钠/氢基硼氢化钠溶液(按照还原剂和铁蛋白200:1的摩尔比),迅速混匀,同时将反应体系ph值调到8.5,溶液体系需经过透析以去除其中的氯离子,
以防止形成氯化银沉淀中严格避免氯离子,37℃孵育4h;整个反应过程需要遮光。
52.4、反应结束后用50kd超滤管超滤,以除去反应体系中剩余的还原剂,并经过分子筛superdex200进一步纯化,得到高纯度的一系列不同尺径银纳米团簇-铁蛋白新型仿生药物溶液。
53.实施例2
54.1、制备全重链人源铁蛋白
55.选择全重链人源铁蛋白,其ncbi基因序列号为:2495。扩增获得全重链人源铁蛋白基因片段后,按照常规的基因重组方法构建含有全重链人源铁蛋白基因片段的表达载体,转入到大肠杆菌中,获得重组大肠杆菌。
56.重组大肠杆菌在37℃发酵培养,od值达到0.8时加入0.4mmiptg诱导4小时过量表达,经过离子交换柱和分子筛、纯化得到全重链人源铁蛋白,纯度可达95%以上,1l菌液可得纯化的全重链人源铁蛋白20mg以上。
57.2、将获得的全重链人源铁蛋白稀释,获得浓度为100pm的全重链人源铁蛋白溶液加入反应管中,再加入硝酸银;其中,硝酸银和铁蛋白按照500:1的摩尔比混合,37℃振荡孵育2小时;
58.3、反应管中加入硼氢化钠/氢基硼氢化钠溶液(按照还原剂和铁蛋白200:1的摩尔比),迅速混匀,同时将反应体系ph值调到9.0,溶液体系需经过透析以去除其中的氯离子,以防止形成氯化银沉淀中严格避免氯离子,37℃孵育12h;整个反应过程需要遮光。
59.4、反应结束后用50kd超滤管超滤,以除去反应体系中剩余的还原剂,并经过分子筛superdex200进一步纯化,得到高纯度的一系列不同尺径银纳米团簇-铁蛋白新型仿生药物溶液。
60.实施例3
61.1、制备全重链人源铁蛋白
62.选择全重链人源铁蛋白,其ncbi基因序列号为:2495。扩增获得全重链人源铁蛋白基因片段后,按照常规的基因重组方法构建含有全重链人源铁蛋白基因片段的表达载体,转入到大肠杆菌中,获得重组大肠杆菌。
63.重组大肠杆菌在37℃发酵培养,od值达到0.8时加入0.4mmiptg诱导4小时过量表达,经过离子交换柱和分子筛、纯化得到全重链人源铁蛋白,纯度可达95%以上,1l菌液可得纯化的全重链人源铁蛋白20mg以上。
64.2、将获得的全重链人源铁蛋白稀释,获得浓度为90pm的全重链人源铁蛋白溶液加入反应管中,再加入硝酸银;其中,硝酸银和铁蛋白按照700:1的摩尔比混合,37℃振荡孵育2小时;
65.3、反应管中加入硼氢化钠/氢基硼氢化钠溶液(按照还原剂和铁蛋白200:1的摩尔比),迅速混匀,同时将反应体系ph值调到8.5,溶液体系需经过透析以去除其中的氯离子,以防止形成氯化银沉淀中严格避免氯离子,37℃孵育24h;整个反应过程需要遮光。
66.4、反应结束后用50kd超滤管超滤,以除去反应体系中剩余的还原剂,并经过分子筛superdex200进一步纯化,得到高纯度的一系列不同尺径银纳米团簇-铁蛋白新型仿生药物溶液。
67.实施例4
68.1、制备全重链人源铁蛋白
69.选择全重链人源铁蛋白,其ncbi基因序列号为:2495。扩增获得全重链人源铁蛋白基因片段后,按照常规的基因重组方法构建含有全重链人源铁蛋白基因片段的表达载体,转入到大肠杆菌中,获得重组大肠杆菌。
70.重组大肠杆菌在37℃发酵培养,od值达到0.8时加入0.4mmiptg诱导4小时过量表达,经过离子交换柱和分子筛、纯化得到全重链人源铁蛋白,纯度可达95%以上,1l菌液可得纯化的全重链人源铁蛋白20mg以上。
71.2、将获得的全重链人源铁蛋白稀释,获得浓度为120pm的全重链人源铁蛋白溶液加入反应管中,再加入硝酸银;其中,硝酸银和铁蛋白按照1200:1的摩尔比混合,37℃振荡孵育2小时;
72.3、反应管中加入硼氢化钠/氢基硼氢化钠溶液(按照还原剂和铁蛋白200:1的摩尔比),迅速混匀,同时将反应体系ph值调到8.5,溶液体系需经过透析以去除其中的氯离子,以防止形成氯化银沉淀中严格避免氯离子,37℃孵育48h;整个反应过程需要遮光。
73.4、反应结束后用50kd超滤管超滤,以除去反应体系中剩余的还原剂,并经过分子筛superdex200进一步纯化,得到高纯度的一系列不同尺径银纳米团簇-铁蛋白新型仿生药物溶液。
74.以上实施例1到实施例4中,加入还原剂进行孵育后4小时左右,可以观察到溶液颜色开始变化,银团簇开始长成,随着反应时间增加,溶液的颜色由浅黄色至褐色变化,如图2所示,显示的颜色逐渐加深。各反应管反应4h,12h,24h,48h,分别在亚铁氧化酶还原位点上可以合成约1nm(实施例1)、2nm(实施例2)、3nm(实施例3)、4nm(实施例4)的银纳米团簇。
75.如图3所示的紫外吸收峰测定结果显示,不同尺径的银团簇纳米药物均具有银团簇的典型吸收峰,吸收峰在团簇410nm—440nm之间,证明银团簇已成功合成。
76.利用冷冻电子显微镜成像表征银纳米团簇-铁蛋白的空间结构,并测量银团簇的尺径大小。图4为本发明典型的银纳米团簇-铁蛋白仿生药物的冷冻电镜成像图。银纳米团簇的合成不影响铁蛋白的天然结构,合成后铁蛋白的球状纳米结构保持完好,粒径均一。
77.实施例5
78.1、制备全重链人源铁蛋白
79.选择全重链人源铁蛋白,其ncbi基因序列号为:2495。扩增获得全重链人源铁蛋白基因片段后,按照常规的基因重组方法构建含有全重链人源铁蛋白基因片段的表达载体,转入到大肠杆菌中,获得重组大肠杆菌。
80.重组大肠杆菌在37℃发酵培养,od值达到0.8时加入0.4mmiptg诱导4小时过量表达,经过离子交换柱和分子筛、纯化得到全重链人源铁蛋白,纯度可达95%以上,1l菌液可得纯化的全重链人源铁蛋白20mg以上。
81.2、将获得的全重链人源铁蛋白稀释,获得浓度为150pm的全重链人源铁蛋白溶液,加入四个反应管中。每个反应管中分别加入一定量的硝酸银;其中,硝酸银和铁蛋白分别按照200:1,500:1,700:1,1500:1的摩尔比混合,37℃振荡孵育2小时;
82.3、每个反应管中加入抗坏血酸溶液(按照还原剂和铁蛋白150:1的摩尔比),迅速混匀,同时将反应体系ph值调到8.5-9,各溶液体系需经过透析以去除其中的氯离子,以防止形成氯化银沉淀中严格避免氯离子,37℃孵育;为控制合成不同尺径银纳米团簇,控制各
样品的孵育生长反应时间分别为4h,12h,24h,48h;整个反应过程需要遮光。
83.4、反应结束后用50kd超滤管超滤,以除去反应体系中剩余的还原剂,并经过分子筛superdex200进一步纯化,得到高纯度的一系列不同尺径银纳米团簇-铁蛋白新型仿生药物溶液。
84.结果:加入还原剂进行孵育后4小时左右,可以观察到溶液颜色开始变化,银团簇开始长成,随着反应时间增加,溶液的颜色由浅黄色至褐色变化,显示的颜色逐渐加深。各反应管反应4h,12h,24h,48h,分别在亚铁氧化酶还原位点上可以合成约1nm、2nm、3nm、4nm的银纳米团簇,
85.紫外吸收峰测定结果显示,不同尺径的银团簇纳米药物均具有银团簇的典型吸收峰,吸收峰在团簇410nm—440nm之间,证明银团簇已成功合成。
86.利用冷冻电子显微镜成像表征银纳米团簇-铁蛋白的空间结构,并测量银团簇的尺径大小。银纳米团簇的合成不影响铁蛋白的天然结构,合成后铁蛋白的球状纳米结构保持完好,粒径均一。
87.试验例1
88.条件摸索试验
89.(1)反应物浓度对产物的影响
90.银纳米团簇-铁蛋白新型仿生药物的制备过程中,作为反应物的铁蛋白的浓度的变化对获得的产物也有不同的影响。本试验中设定不同的铁蛋白的浓度:50pm、100pm、500pm以及1um,分别作为试验组1-4,看其对最终获得的银纳米团簇-铁蛋白新型仿生药物的影响。除表1中列出的参数外,具体步骤参照实施例1。
91.表1
92.试验组铁蛋白浓度吸收峰外观试验组150pm425nm-450nm澄清试验组2100pm425nm-540nm澄清试验组3500pm无溶液轻度浑浊试验组41um无溶液浑浊,大量絮状沉淀
93.如表1中所示,本试验经过调整多种反应物浓度,确定合成反应需要反应物浓度较低的情况下完成(低于100pm级别),以增加银离子与铁蛋白的充分接触和在成核位点上的吸附,反应物浓度过高,接触不充分,反应体系不稳定,局部会出现氢氧化银沉淀。因浓度越低,获得等量的反应产物所需体积越大,因此最优选100pm。
94.(2)硝酸银与铁蛋白的摩尔比对产物的影响
95.银纳米团簇-铁蛋白新型仿生药物的制备过程中,硝酸银与铁蛋白的摩尔比对获得的产物也有不同的影响。本试验中设定不同的硝酸银与铁蛋白的摩尔比:100:1、200:1、500:1、700:1、1200:1以及1500:1,分别作为试验组1-6,看其对最终获得的银纳米团簇-铁蛋白新型仿生药物的影响。除表2中列出的参数外,具体步骤参照实施例1。
96.表2
[0097][0098][0099]
结果如表2中所示,银溶液与铁蛋白的摩尔比决定了所合成银纳米团簇的尺径,低于本申请所述摩尔比则反应不充分,无法达到目标尺径;而高于本申请所述摩尔比,合成的银纳米团簇尺径偏差过大,吸收峰显示反应体系形成尺径大于10nm的银纳米颗粒,并肉眼可见黑色银颗粒沉淀。
[0100]
(3)还原剂与铁蛋白的摩尔比对产物的影响
[0101]
银纳米团簇-铁蛋白新型仿生药物的制备过程中,还原剂与铁蛋白的摩尔比对获得的产物也有不同的影响。本试验中设定不同的硼氢化钠与铁蛋白的摩尔比:100:1、200:1、500:1、以及1000:1,分别作为试验组1-4,看其对最终获得的银纳米团簇-铁蛋白新型仿生药物的影响。除表3中列出的参数外,具体步骤参照实施例1。
[0102]
表3
[0103][0104]
结果如表3中所示,硼氢化钠与铁蛋白的摩尔比决定了反应速率,反应条件高于本专利所述摩尔比,反应过快会形成大量副反应产物,出现肉眼可见银颗粒沉淀;低于本专利所述摩尔比,反应速度较慢,或反应不充分,充分考虑缩短反应的时间周期,优选200:1。
[0105]
(4)温度对产物的影响
[0106]
银纳米团簇-铁蛋白新型仿生药物的制备过程中,不同的反应温度对获得的产物
也有不同的影响。本试验中设定多个反应温度,具体包括10℃、20℃、30℃、37℃和45℃,看其对最终获得的银纳米团簇-铁蛋白新型仿生药物的影响。
[0107]
结果表明,当温度低于本申请所述反应温度37℃,合成特定尺径的银纳米团簇需要进一步增加反应时间,增加了生产成本;温度高于本申请所述反应温度37℃,反应进行太快,合成的银尺径偏差过大等,同时温度高增加了铁蛋白的不稳定性。
[0108]
(5)ph对产物的影响
[0109]
银纳米团簇-铁蛋白新型仿生药物的制备过程中,不同的反应ph对获得的产物也有不同的影响。本试验中设定多个ph,具体包括ph为4.5、7、8.5和10,看其对最终获得的银纳米团簇-铁蛋白新型仿生药物的影响。
[0110]
表4
[0111][0112]
结果如图4所示,银纳米团簇-铁蛋白仿生药物的合成过程中ph需要严格控制,因氢氧根离子有弱还原剂功能,且可以保护还原剂的稳定性,ph过高会使反应体系出现氢氧化银沉淀,ph过低还原反应不能完成。本申请选择最佳ph为8.5。
[0113]
试验例2
[0114]
稳定性试验
[0115]
常规合成银纳米团簇的方法为:将银盐和保护剂放于水溶液中,反应生成可溶性银络合物,再缓慢加入还原剂,生成纳米银团簇。具体包括:称取1
×
10-3
mol/l的agn03和0.01mol/l的d-麦芽糖适量倒入至反应器皿中,缓慢滴加nh4·
h2o至浓度为5
×
10-3
mol/l。向反应体系中加入一定量naoh使溶液ph值升至11.5。将所得纳米银团簇溶液用超滤装置超滤,用1l去离子水将纳米银溶液洗净至ph为中性备用。
[0116]
将上述常规合成银纳米团簇作为对照组。
[0117]
将按照实施例1的方法制备的银纳米团簇-铁蛋白新型仿生药物作为实验组。
[0118]
稳定性试验的方法:将对照组和实验组的样品,在常温下避光保存1个月,检测其银团簇吸收峰及样品外观形态。结果列于表1中。
[0119]
表5
[0120][0121]
由以上结果可以看出,常规合成的银纳米团簇在溶液中极易形成聚集而丧失功效,以本方法合成的银纳米团簇仿生药物,在常温下避光保存1个月,其银团簇吸收峰不发生改变,4℃避光条件下可保存6个月以上,-80℃条件下可长期保存,稳定性好。
[0122]
试验例3
[0123]
药效试验
[0124]
将对数期的hepg 2.2.15细胞用0.25%胰酶消化后成混悬液,计数并调节其浓度至6
×
104个/ml,接种到96孔培养板中,每孔100μl,置于培养箱中24h。待细胞贴壁后,吸出上清液,加入不同浓度的含药培养基(5、10、25、50nm),每孔100μl,每个浓度设5个复孔。同时用无菌pbs做同倍数稀释,各样品标记清楚。按照elisa分析方法,采用hbsag和hbeag诊断试剂盒,测定hepg2.2.15细胞第3d上清液中hbsag和hbeag的含量。计算cbc的抗原抑制率及半数抑制浓度(ic50),方法如下:
[0125]
(1)预先从4℃冰箱里取出hbsag诊断试剂盒、hbeag诊断试剂盒,及待测样品放在室温平衡30min。
[0126]
(2)根据实验设计,选择一定区域的反应板条,并做好标记。
[0127]
(3)每孔加入50μl待检样本、阳标、阴标、空白,各设3孔。
[0128]
(4)封板后37℃避光孵育30min。
[0129]
(5)各孔加入50μl酶结合物。
[0130]
(6)手动悬空轻轻震荡10s左右。
[0131]
(7)封板后37℃避光孵育30min。
[0132]
(8)配制工作浓度的洗涤液(取48ml纯化水,加入2ml洗涤液,充分混匀后,配成50ml工作浓度的洗涤液,现配现用)。
[0133]
(9)吸出各孔红色液体,将上述配置好的工作浓度洗涤液加满各孔,放置30-60s,吸干,重复5次后,在吸水纸上扣干。
[0134]
(10)加显色剂a+b各50μl,混匀。
[0135]
(11)手动悬空轻轻震荡10s。
[0136]
(12)封板后37℃避光孵育30min。
[0137]
(13)在各孔内加入50μl终止液。
[0138]
(14)手动悬空轻轻震荡5s混匀。
[0139]
(15)10min内450nm处读取各孔od值。
[0140]
(16)计算抗原抑制率公式:
[0141]
抗原抑制率(%)=(1-药物组od值/阴性对照组od值)
×
100%
[0142]
结果有效性:参考值=阴性标准品平均od值
×
2.1
[0143]
阴性标准品od值<0.05按0.05算。当阴性标准品od值<0.1时,结果有效;反之无效。
[0144]
表6 4nm尺径银纳米团簇-铁蛋白新型仿生药物对hepg2.2.15细胞hbsag和hbeag表达的影响
[0145][0146]
与银纳米团簇-铁蛋白5nm比较,*p<0.1,**p<0.01,***p<0.001
[0147]
抗乙肝病毒的试验数据显示,银纳米团簇-铁蛋白新型仿生药物抗乙肝病毒效果随着银纳米团簇直径增大,效果更好。以4nm尺径的银纳米团簇-铁蛋白新型仿生药物为例,浓度在50nm的条件下,乙肝病毒抗原抑制率达到约90%。
[0148]
以上所述仅是本发明的较佳实施例而已,并非对本发明作任何形式上的限制,虽然本发明已以较佳实施例揭露如上,然而并非用以限定本发明,任何熟悉本专利的技术人员在不脱离本发明技术方案范围内,当可利用上述提示的技术内容作出些许更动或修饰为等同变化的等效实施例,但凡是未脱离本发明技术方案的内容,依据本发明的技术实质对以上实施例所作的任何简单修改、等同变化与修饰,均仍属于本发明方案的范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1