纳米粒子递送体系的制作方法
本发明涉及一种纳米粒子递送体系及其结合物。更特别地,本发明提供用于将药物产品递送至对象体内的纳米粒子递送体系。
背景技术:
当前,化学疗法被认为是全世界人群中最常见的癌症治疗方法。
然而,众所周知,基本上所有此类用于化学疗法的药物以及在用于其它治疗应用时固有地具有相关的副作用。
在临床实践中,副作用仍被认为是癌症治疗和对象临床治疗中的挑战性问题。减少与药物或治疗相关的副作用被认为是重要的问题,因为这也涵盖了药物的实际治疗效果。
药物递送体系(dds)的设计能够用于解决或至少改善与药物副作用相关的一些问题,以及解决临床负荷以及在一些情况下与溶解度相关的问题。
dds可以包括具体的药物靶向/递送、在保持必要的治疗效果的同时降低毒性以及新型且更安全的医疗产品的开发。
已经开发出许多先进的药物递送体系(dds),目的是改善药物产品或活性药物成分(api)的生物利用度,这可以防止或减少过早降解以及增加药物摄取,这能够示出通过控制药物向对象的释放速率来将药物浓度保持在必要的治疗水平内,这已示出可以通过靶向于患病部位和靶细胞来减少副作用。
在现有技术中,在药物递送体系方面已经进行了许多尝试和开发,例如通过合并新的或新型的材料以运载和递送抗癌药物,从而使在向对象递送药物过程期间的副作用最小化或减少的靶向癌症治疗。
在现有技术中,已经提出了多种纳米结构材料以用于生物学和医学、用于生物成像以及还用于药物递送。
此外,在现有技术范围内,在药物递送中已经使用纳米粒子-载体型装置以用于药物的靶向传输和药物的受控释放,以及用于释放活性药物成分(api)和/或其它治疗性化合物。例如,已经显示,纳米粒子刺激耐药性细胞的内吞作用,从而提高细胞内的药物浓度。
然而,一直关注的是使用诸如纳米粒子的递送粒子,其涉及对象体内的毒性和累积的问题,以及这样的递送粒子结块在一起并累积的问题,从而有效地加载具有药物或治疗性分子或化合物的粒子,并且有效且持续地递送至对象体内。
此外,药物递送体系应该能够适当地控制api或治疗性分子或化合物向对象的释放和递送,从而具有适合于特定临床应用的必要的释放曲线(profile),例如向对象提供必要的血浆浓度或水平。
因此,为了克服现有技术及与其相关的此类缺点,为了改善对象的生活质量及其临床治疗,需要改善的药物递送产品、组合物和体系。
发明目的
本发明的目的是提供一种纳米粒子递送体系,所述纳米粒子递送体系克服或至少部分改善了与现有技术相关的至少一些缺陷。
技术实现要素:
在第一方面,本发明提供一种结合物,所述结合物包含:
纳米粒子,所述纳米粒子用于将药物递送至对象体内的治疗部位;
可释放地连接至所述纳米粒子的药物分子,其中所述药物分子在所述对象体内的所述治疗部位处具有治疗效果;和
可释放地连接至所述纳米粒子的疾病靶向分子;
其中当所述结合物邻近于对象的患病组织时,所述疾病靶向分子将所述结合物保持在所述患病组织附近;
所述药物分子从所述纳米粒子释放,从而向所述患病组织提供治疗效果;
随后所述疾病靶向分子从所述纳米粒子释放,使得被保持的所述纳米粒子被释放,并且使得所述纳米粒子可从所述患病组织散开。
优选地,所述纳米粒子为纳米金刚石,所述纳米金刚石的尺寸在25nm至80nm的范围内,更优选在35nm至65nm的范围内,更优选具有约50nm的尺寸。
优选地,所述疾病靶向分子是癌症靶向分子,并且其中所述患病组织是癌组织。
优选地,所述药物分子为蒽环霉素。优选地,所述药物分子为盐酸阿霉素c27h29no11(dox)。
或者,所述药物分子可以为甲氨蝶呤c20h22n8o5(mtx)。
所述药物分子可以通过分子间力附着至所述纳米粒子,由此所述药物分子可通过所述患病组织附近的酸性环境的改变而从所述纳米粒子释放。
优选地,所述纳米粒子为纳米金刚石,并且所述药物分子通过分子间力附着至纳米金刚石上的人血清白蛋白涂层,由此所述药物分子可通过所述患病组织附近的酸性环境的改变而从所述纳米粒子释放,从而将所述药物分子递送至对象的患病组织。
所述疾病靶向分子可以通过乙烯-乙酸乙烯基酯聚合物与所述纳米粒子连接,以及其中所述纳米粒子与所述疾病靶向分子之间的连接可通过用红外辐射照射所述纳米粒子而产生的热来分解,从而使所述纳米粒子从所述对象的患病组织释放。
优选地,所述疾病靶向分子为癌症。优选地,所述癌症靶向分子为胃泌激素。
在第二方面,本发明提供药物溶液,所述药物溶液包含多种根据第一方面所述的结合物和液体载体。
优选地,所述溶液为用于向对象进行静脉内递送的溶液。
在第三方面,本发明提供第一方面的结合物的用途,用于制造用于对象的预防或治疗的药剂。
在第四方面,本发明提供向需要治疗处理的对象提供治疗处理的方法,所述方法包括将治疗量的所述第二方面的药物溶液递送至所述对象的步骤。
附图说明
为了能够获得对上述发明的更精确的理解,将参考在附图中示出的本发明的具体实施方案对以上简要描述的本发明进行更具体的说明。本文中所呈现的附图可能未按比例绘制,并且附图或如下描述中对尺寸的任何引用都是针对所公开的实施方案具体而言的。
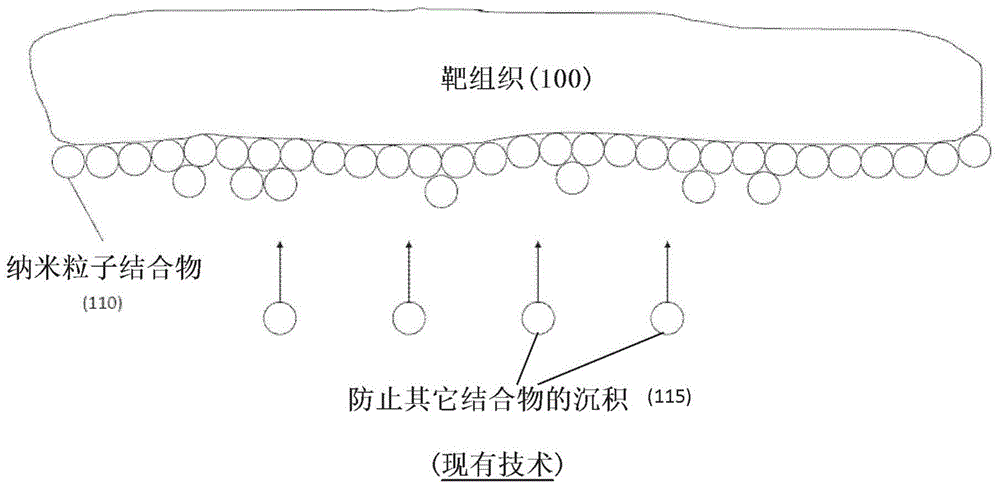
图1显示了现有技术的纳米粒子的示意图,所述纳米粒子在对象的组织部位处结块;
图2a显示了根据本发明的结合物的示意图;
图2b显示了与癌组织接合的图2a的结合物的示意图;
图2c显示了图2a和图2b的结合物,其中药物分子从图2a的结合物的纳米粒子释放;
图2d显示了图2a至2c的结合物,其中图2a至2c的癌症靶向分子从所述结合物的纳米粒子释放;
图2e显示了从图2a至2d的癌组织释放的图2a至2d的结合物。
具体实施方式
本发明人已经发现了现有技术的纳米粒子药物递送体系的缺点,并且在确定了现有技术的问题之后,提供了一种克服或至少改善了现有技术的问题的体系和结合物。
图1显示了现有技术的纳米粒子结合物110的示意图,所述纳米粒子结合物110在对象的组织部位100处结块。
已经将纳米粒子与疾病靶向分子结合使用,以靶向于特定的组织100。这样的组织如癌症或受感染的组织在细胞表面上具有特定的抗原。
将与纳米粒子结合的疾病靶向分子与抗原组合,使得纳米粒子结合物110能够粘合至组织细胞表面。
这种效果特别用于生物标记以识别特定组织,例如癌症或受感染的组织。纳米粒子的另一种用途是用于靶向药物递送。纳米粒子能够与疾病靶向分子和药物分子两者结合,以向对象的组织提供治疗效果。
疾病靶向分子促进纳米粒子结合物110与特定组织100的细胞表面的粘合。在粘合之后,结合的药物分子能够自发释放,或在外部影响下释放,从而将药物靶向地递送至对象的组织。
然而,如本发明人所指出的,在完成了将药物分子递送至组织的期望任务之后,残留的纳米粒子造成长期问题,并且对对象身体的安全性产生累积影响。
例如,一些纳米粒子可能具有特定的反应性,并且所导致的在体内的累积被认为是及其不希望的。即使在使用一些稳定的纳米粒子的情况下,由于它们可能在累积于人内时形成大尺寸的聚集体,并且例如阻塞毛细血管或肾小管的通路,因此从临床角度出发存在问题。
在药物递送的情况下,因为纳米粒子比抗原具有相对更大的尺寸,所以在组织表面上累积的纳米粒子复合物还可能防止其它纳米粒子结合物115的进一步沉积。因此,本发明人已经确定,在完成期望的药物递送任务后需要除去纳米粒子结合物110,从而至少增加或更有效地递送药物分子以达到治疗效果。
因为已经发现了现有技术的缺点,所以本发明人已经提供了一种方案,如参考接下来描述和显示的附图2a至2e的参考所显示和描述的。
参考图2a,显示了根据本发明的纳米粒子-疾病靶向分子-药物结合物200。纳米粒子210与疾病靶向分子230和药物分子220共轭。
如本领域技术人员将理解的,这样的图不是按比例绘制的并且仅示意性显示了临床环境,并且进一步将理解的是,可以在纳米粒子210上提供许多疾病靶向分子230和药物分子220,并不一定仅一个,示出为一个仅出于说明的目的。
参考图2b,疾病靶向分子230能够靶向于患病组织240,然后将该结合物粘合至组织240。
现在参考图2c,在通过疾病靶向分子230将结合物200附着至组织240之后,或者当结合物在患病组织240的适当的近处时,药物分子220能够自发地或在外部影响下从纳米粒子230释放。释放出的药物分子220能够局部作用于靶患病组织240如癌组织。
现在如图2d所示,在完成将药物分子220递送至靶患病组织240的任务之后,纳米粒子210能够自发地或在外部影响下从疾病靶向分子230释放。
由此,如现在在图2e中所示,纳米粒子210能够从组织240移开并被除去,由此使得能够沉积其它结合物并且将它们各自的药物分子递送至组织,由于纳米粒子从组织240释放,从而防止了不期望的阻塞和局部结块的影响,如本发明人所确定的。
如本领域技术人员将理解的,在疾病靶向分子230附着至组织240上时,在疾病靶向分子230附着至组织240上之后,或甚至在结合物200在组织240的适当近处的情况下在疾病靶向分子230附着至组织240上之前,可以从纳米粒子210释放药物分子220,使得药物分子220可以向其提供适当的临床效果。
在本发明内,在一个优选的实施方案中,纳米粒子210可以为纳米金刚石。纳米金刚石在本质上是金刚石,从而它们在化学上是稳定的。对于包含色心如nv(氮空位)中心的纳米金刚石,它们还能够用作生物标记中的荧光剂,这在本发明的一些应用中可能是有用的。
作为实例,可以用诸如-cooh、-nh2、-oh的不同官能团对纳米金刚石的表面进行改性。这些官能团使得纳米金刚石与不同的分子反应并连接在一起,并具有粘结或粘附作用。
除了官能团外,还能够在纳米金刚石上发现sp2碳。这些sp2碳能够吸收红外光以产生热。
根据本发明的实施方案,可以将纳米金刚石与作为生长激素的胃泌激素分子共轭。
对于根据本发明的胃肠癌的治疗应用来说,因为癌细胞的生长特性高,所以已经大量发现了胃泌激素的受体。因此,作为这样的癌症靶向剂分子的实例,可以将胃泌激素用作靶向于癌症组织240的癌症疾病靶向分子230。
通过与edc(1-乙基-3-(3-二甲基氨基丙基)碳二亚胺盐酸盐)和磺基-nhs(n-羟基磺基琥珀酰亚胺)反应,能够实施纳米金刚石210与胃泌激素230的结合。
交联剂反应产生连接-cooh和-nh2官能团的共价键。例如,纳米粒子的纳米金刚石210和胃泌激素230能够通过该反应直接连接在一起。
此外,聚合物也可以参与反应以充当纳米金刚石210与胃泌激素230之间的桥。作为实例,这样的聚合物可以为乙烯-乙酸乙烯基酯聚合物,其具有-cooh或-nh2基团以参与与edc和磺基-nhs的交联反应。
乙烯-乙酸乙烯基酯在高温下断裂,因此通过对纳米金刚石210进行照射而产生的热能够用于从癌症靶向胃泌激素230释放纳米金刚石210,从而使纳米金刚石从患病组织中移出,如参考本发明所述的。
作为蒽环霉素的阿霉素(doxorubicin,dox)是提供作用于癌细胞组织240的治疗效果的化学治疗药物。它能够用作药物分子220以形成根据本发明的纳米粒子-疾病靶向分子-药物结合物200。
通过与人血清白蛋白(hsa)混合,能够将纳米金刚石与dox结合。由于诸如范德华力和氢键的分子间力而使得hsa能够在纳米金刚石表面上形成涂层,dox负载在hsa上。该过程对ph敏感,并且dox药物分子220能够在酸性环境如组织中癌细胞周围的酸性环境中释放,从而提供必要的治疗效果。
在本发明的一个实施方案中,结合物的整个体系可以为通过乙烯-乙酸乙烯基酯聚合物与癌症靶向胃泌激素230结合的纳米金刚石210。用作药物分子220的dox与具有hsa的纳米金刚石结合。
纳米金刚石-胃泌激素-dox结合物能够靶向于癌组织240并释放药物dox220。在释放药物之后或大约释放时,可以在癌组织240上照射红外光以释放纳米金刚石210。
因此,能够除去纳米金刚石210而不存在在体内累积和结合并且防止其它dox通过其它结合物递送的风险。
这种纳米金刚石-胃泌激素-dox结合物能够用于例如治疗胃肠癌。释放的dox作用于管道内的癌组织,然后纳米金刚石被释放并通过排泄除去。
在其它实施方案中,也能够在对象的皮肤上进行类似的应用。靶组织不一定为癌组织,例如黑素瘤。也能够用纳米金刚石-靶向剂-药物结合物来治疗也能够用疾病靶向分子来靶向的任何皮肤异常如伤口或色素沉着,并向其递送治疗剂。
如本领域技术人员将理解的,本发明的上述实施方案为示例性实施方案,并且尽管所述实例通常涉及使用纳米金刚石作为纳米粒子,并且用于治疗癌症,但在其它或替代实施方案中,所述纳米粒子可以为其它纳米粒子并且组织疾病可以为其它疾病或除癌症以外的疾病。
在实验性实施方案中,已经使用被称为dox的盐酸阿霉素c27h29no11对本发明进行了描述。dox为用于治疗癌症的化学治疗药剂。这包括乳腺癌、膀胱癌、卡波济(kaposi)肉瘤、淋巴瘤和急性淋巴细胞性白血病。它经常与其它化学治疗剂一起使用,并且本发明适用于组合治疗。
将理解的是,可以使用其它抗癌药物,例如被称为mtx的经验式为c20h22n8o5的甲氨蝶呤。甲氨蝶呤为化学治疗剂和免疫系统抑制剂。它用于治疗癌症、自身免疫疾病、异位妊娠和药物流产。它用于的癌症类型包括乳腺癌、白血病、肺癌、淋巴瘤和骨肉瘤。用于的自身免疫疾病的类型包括牛皮癣、类风湿性关节炎和克罗恩(crohn)病。它能够通过口服或注射给药。
还将理解的是,在替代实施方案中,本发明的结合物可以具有多于一种附着至其上的药物分子。
- 还没有人留言评论。精彩留言会获得点赞!