用于使用在先图像进行图像改进的计算机断层摄影系统和方法与流程
相关申请的交叉引用
本申请要求十一项美国临时专利申请的权益,其包括2018年11月30日提交的序列号62/773,712(代理人案卷号38935/04001);2018年11月30日提交的序列号62/773,700(代理人案卷号38935/04002);2019年1月25日提交的序列号62/796,831(代理人案卷号38935/04004);2019年2月1日提交的序列号62/800,287(代理人案卷号38935/04003);2019年2月5日提交的序列号62/801,260(代理人案卷号38935/04006);2019年3月4日提交的序列号62/813,335(代理人案卷号38935/04007);2019年3月20日提交的序列号62/821,116(代理人案卷号38935/04009);2019年4月19日提交的序列号62/836,357(代理人案卷号38935/04016);2019年4月19日提交的序列号62/836,352(代理人案卷号38935/04017);2019年5月6日提交的序列号62/843,796(代理人案卷号38935/04005);以及2019年7月25日提交的序列号62/878,364(代理人案卷号38935/04008)。本申请还涉及在同一天提交的十个非临时美国专利申请,其包括题为“multimodalradiationapparatusandmethods”的代理人案卷号38935/04019;题为“apparatusandmethodsforscalablefieldofviewimagingusingamulti-sourcesystem”的代理人案卷号38935/04020;题为“integratedhelicalfan-beamcomputedtomographyinimage-guidedradioationtreatmentdevice”的代理人案卷号38935/04011;题为“optimizedscanningmethodsandtomographysystemusingregionofinterestdata”的代理人案卷号38935/04013;题为“helicalcone-beamcomputhedtomographyimagingwith”代理人案卷号38935/04015;题为“multi-passcomputedtomographyscansforimprovedworkflowandperformance”的代理人案卷号38935/04021;题为“methodandapparatusforscatterestimationincone-beamcomputedtomography”代理人案卷号38935/04012;题为“asymmetricscatterfittingforoptimalpanelreadoutincone-beamcomputedtomography”的代理人案卷号38935/04014;题为“methodandapparatusforimprovingscatterestimationandcorrectioninimaging”的代理人案卷号38935/04018;以及题为“methodandapparatusforimagereconstructionandcorrectionusinginter-fractionalinformation”的和代理人案卷号38935/04022。所有上述专利申请(一个或多个)和专利(一个或多个)的内容通过引用全部并入本文。
所公开的技术的方面涉及计算机断层摄影(ct)成像,并且更具体地涉及用于使用来自在先或以其他方式先前采集的图像的信息进行图像改进的ct系统和方法(包括作为图像引导放射治疗(igrt)的部分)。
背景技术:
计算机断层摄影(ct)成像通常涉及将患者或患者的一部分暴露于放射源,并定位放射检测器以接收来自放射源的x射线放射。放射源和检测器被移动到患者周围的多个位置,并且所接收的放射被用于生成患者的图像。在一些情况下,患者或患者的一些部分可能被放射源不充分地照射,从而导致截断的图像数据或不足的投影。
放射诊疗是ct成像以更高频率被使用的一个区域(area)。放射诊疗通常通过将高能x射线束(例如,在兆伏范围内的能量水平)定向肿瘤或患者体内的其他感兴趣区而被执行。治疗的目标是将高能x射线束聚焦在感兴趣区上,同时使周围组织的暴露最小化。所谓的图像引导放射诊疗(igrt)可以利用ct成像来收集患者的图像,以用于基于图像的预递送步骤(其可以包括治疗规划)。ct图像采集还可以用于确认诊疗放射束被正确地定向到感兴趣区并对其进行治疗。
技术实现要素:
在一个实施例中,一种用于使用在先图像数据来改进扫描图像质量的方法包括:接收对应于患者的在先图像的图像数据;获得所述患者的投影图像数据,其中,所获得的投影图像数据被截断;基于所获得的所述患者的投影图像数据来重构患者图像;将所述在先图像与所重构的患者图像进行配准;基于所配准的先前图像来生成虚拟投影数据;以及重构补充的投影图像数据集以创建改进的患者图像,其中,所述补充的投影图像数据集包括所获得的投影图像数据和所述虚拟投影数据。
关于一个实施例描述和/或示出的特征可以以相同的方式或类似的方式用于一个或多个其它实施例和/或与其它实施例的特征组合或代替其它实施例的特征。
本发明的描述不以任何方式限制权利要求中使用的词语或权利要求或发明的范围。权利要求中使用的词语具有其全部普通含义。
附图说明
在并入说明书并构成说明书的一部分的附图中,示出了本发明的实施例,其与上面给出的本发明的一般描述和下面给出的详细描述一起用于举例说明本发明的实施例。应当理解,附图中所示的元件边界(例如,框、框组或其他形状)表示边界的一个实施例。在一些实施例中,一个元件可以被设计为多个元件,或者多个元件可以被设计为一个元件。在一些实施例中,被示为另一元件的内部部件的元件可以被实现为外部部件,反之亦然。此外,元件可以不按比例绘制。
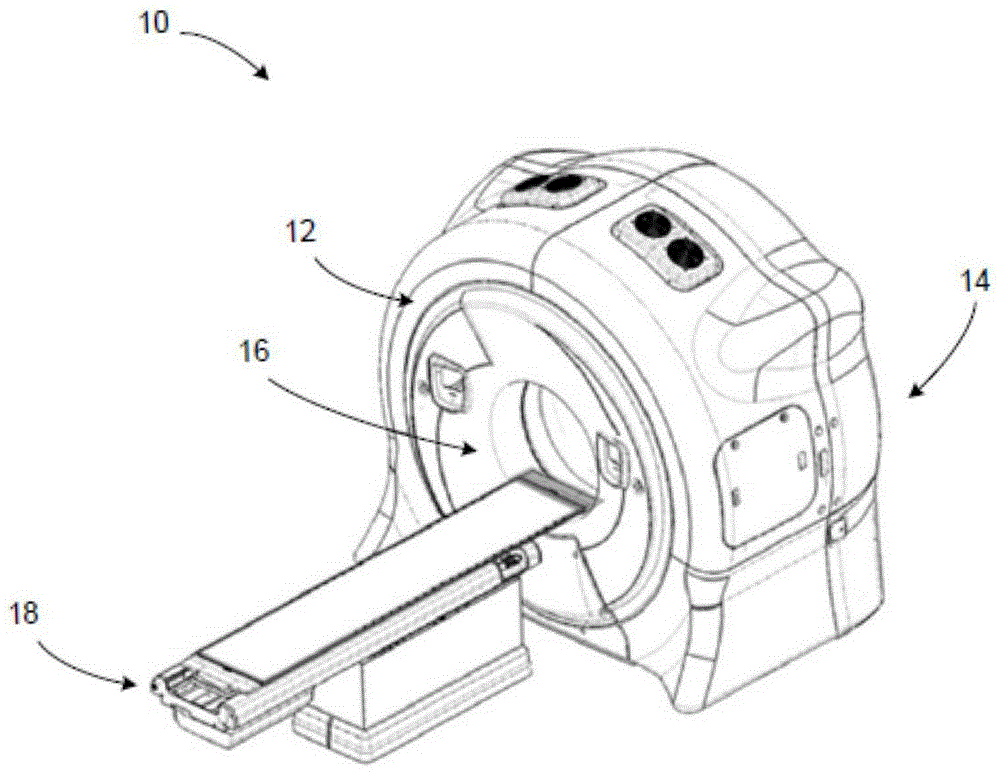
图1是根据所公开技术的一个方面的示例性放射诊疗递送设备的透视图;
图2是根据所公开技术的一个方面的示例性放射诊疗递送设备的示意图;
图3是描绘生成改进或校正的图像的示例性方法的流程图;
图4是示出与所公开的技术的各方面相关联的示例性数据的框图;
图5是描绘生成改进或校正的图像的另一示例性方法的流程图;
图6是描述利用数据一致性实施生成改进或校正的图像的示例性方法的流程图;
图7是描述利用数据一致性实施和在先图像细化来生成改进或校正的图像的示例性方法的流程图;
图8是描述利用数据一致性实施生成改进或校正的图像的示例性方法的流程图;
图9是描述利用数据一致性实施和在先图像细化来生成改进或校正的图像的示例性方法的流程图;
图10是描述使用放射诊疗设备的igrt的示例性方法的流程图;
图11是描述示例性的基于图像的预递送步骤的框图;以及
图12是描述在成像或基于图像的预递送步骤期间可以利用的示例性数据的框图。
应当注意,所有附图都是示意性的,并且未按比例绘制。为了附图的清楚和方便,这些图的各部分的相对尺寸和比例已经被放大或缩小地示出。相同的参考数字通常用于表示不同实施例中的相应或类似特征。因此,附图(一个或多个)和说明书本质上应被认为是说明性的而非限制性的。
具体实施方式
以下内容包括在整个公开中可以使用的示例性术语的定义。所有术语的单数和复数形式都落入每个含义内。
如本文所使用的“部件”可以被定义为硬件的一部分、软件的一部分或其组合。硬件的一部分可以至少包括处理器和存储器的一部分,其中存储器包括要执行的指令。部件可以与设备相关联。
如本文所使用的“逻辑”与“电路”同义,包括但不限于硬件、固件、软件和/或执行(一个或多个)功能或(一个或多个)动作的每一者的组合。例如,基于期望的应用或需要,逻辑可以包括软件控制的微处理器、诸如专用集成电路(asic)的离散逻辑、或其他编程的逻辑器件和/或控制器。逻辑也可完全体现为软件。
如本文所使用的“处理器”包括但不限于实际上任何数量的处理器系统或独立处理器(例如任何组合的微处理器、微控制器、中央处理单元(cpu)和数字信号处理器(dsp))中的一个或多个。处理器可以与支持处理器(例如随机存取存储器(ram)、只读存储器(rom)、可编程只读存储器(prom)、可擦除可编程只读存储器(eprom)、时钟、解码器、存储器控制器或中断控制器等)的操作的各种其它电路相关联。这些支持电路可以在处理器或其相关电子封装的内部或外部。支持电路与处理器操作地通信。支持电路不一定在框图或其它附图中与处理器分开示出。
如本文所使用的“信号”包括但不限于一个或多个电信号,其包括模拟或数字信号、一个或多个计算机指令、比特或比特流等。
如本文所使用的“软件”包括但不限于一个或多个计算机可读和/或可执行指令,其使得计算机、处理器、逻辑和/或其他电子设备以期望的方式执行功能、动作和/或行为。指令可以以各种形式(诸如例程、算法、模块或包括来自动态链接源或库的单独应用或代码的程序)体现。
如下面更详细地讨论的,所公开的技术的方面涉及ct成像系统和方法,其中,在先或以其他方式先前采集的患者图像(例如,规划图像)能够用于补充或以其他方式改进所采集的ct图像,这种情况包括当表示所采集的ct图像的所采集的投影数据可能被截断或以其他方式不完整/不足以准确地表示被扫描的对象/患者时。在一些实施例中,与在先图像相关联的某些属性和/或信息被用于补充所采集的图像,而不是在先图像本身。
本公开认识到,在ct成像流程中(例如,在扇形束或锥形束ct(cbct)成像流程中)采集的数据可能不足以重构足够质量的图像(例如,对于分析重构方法),这可能最终导致图像伪影(例如,锥形束伪影)。在一个示例中,典型的cbct源轨迹是圆形的。然而,从这样的轨迹采集的数据不足以用于位于圆形平面之外的图像像素的精确图像重构。这种数据不足导致锥形束伪影,并且当成像平面远离轨迹平面移动时(或者检测器的纵向覆盖范围变得更大),伪影可能变得更糟。
另一种典型的锥形束数据采集几何形状是螺旋形的。对于这样的轨迹,由于有限的投影数据,用于良好图像质量的感兴趣体积通常短于纵向或轴向方向上的扫描长度。在螺旋轨迹的开始或结束处,可能没有足够的投影数据用于良好的图像重构,或者重构的图像可能包含太多的伪影。
在这些示例中,上述图像伪影通常在轴向方向上是低频。一种典型的解决方案可以是使用附加轨迹来采集更多数据。以圆形轨迹为例,附加到圆形轨迹的附加线将提供用于在延伸的纵向体积中的精确图像重构的附加数据。然而,这种额外的扫描将需要额外的时间、增加患者剂量和/或潜在地使成像工作流程复杂化。
本公开认识到上述缺失或不足的数据通常对应于低频。这些附加数据的良好近似对于例如图像重构可能是足够的。所公开的技术的各方面可以使用在先或先前采集的图像(例如,规划ct图像)和应用于该数据集的虚拟投影器(projector)来生成用于改进的图像重构的附加数据。这种方法可应用于许多源轨迹(包括但不限于圆形轨迹和螺旋形轨迹)。将进一步讨论,这种方法可以与一个或多个迭代图像重构技术组合。
虽然将结合作为在先规划图像(例如,为了生成用于与igrt流程结合使用的治疗规划的目的而在治疗之前采集的图像)的在先或先前采集的图像来描述所公开的技术的方面,但是将认识到,可以在一般成像环境中(例如,在与任何igrt应用分离的标准计算机断层摄影成像环境中)执行所公开的技术的方面。
例如,在一些实施例中,所公开的技术涉及与放射诊疗系统分离的ct系统。在其它实施例中,放射诊疗递送设备和方法可以利用用于ct的集成低能放射源,以与igrt结合使用或作为igrt的一部分。特别地,例如,放射诊疗递送设备和方法可以将用于在台架中成像的低能放射源与用于诊疗处理的高能放射源组合。在一个实施例中,低能放射源是作为ct系统的一部分的千伏(kv)放射源,而用于诊疗处理的高能放射源是兆伏(mv)放射源。以下提及kv放射源的实施例也可以利用其它低能放射源。
如上所述,图像采集系统不需要与具有专用kv成像源的igrt系统相关联。例如,所涉及的图像采集系统可以包括mvx射线管和mvx射线检测器、kvx射线管和kvx射线检测器、或两者的组合。如下面更详细讨论的,这些成像源和检测器可以以各种组合安装在ct状台架上(例如,具有滑环)、机器人臂上、两个机器人臂上和/或其它安装设备上。
根据一个实施例,该方法可以在图1和图2所示的系统上执行,并在下面对其进行描述。然而,应当理解,在不背离所公开的技术的范围的情况下,可以在不同的计算机断层摄影成像系统(例如,mvct系统和/或kvct系统,其中源和/或检测器可操作地耦合到一个或多个机器人臂,例如c形臂系统)上执行该成像方法。
参考图1和图2,提供了一种放射诊疗设备10。应当理解,放射诊疗设备10可以用于各种应用,包括但不限于图像引导放射治疗或诊疗(igrt)。放射诊疗设备10可以用于执行下面更全面描述的成像方法。放射诊疗设备10包括可旋转台架系统(其被称为台架12),其由支撑单元或壳体14支撑或以其他方式容纳在其中。这里的台架指的是包括一个或多个台架(例如,环或c形臂)的台架系统,当一个或多个台架围绕靶旋转时,台架能够支撑一个或多个放射源和/或相关的检测器。例如,在一个实施例中,第一放射源及其相关的检测器可以安装到台架系统的第一台架,第二放射源及其相关的检测器可以安装到台架系统的第二台架。在另一个实施例中,多于一个的放射源和相关联的检测器(一个或多个)可以被安装到台架系统的同一台架(其包括例如,其中台架系统仅包括一个台架)。台架、放射源和放射检测器的各种组合可以被组合到各种台架系统配置中,以在相同的装置内对相同的体积进行成像和/或处理。例如,kv和mv放射源可以安装在台架系统的相同或不同台架上,并且作为igrt系统的一部分选择性地用于成像和/或治疗。如果安装到不同的台架,放射源能够独立地旋转,但是仍然能够同时对相同(或几乎相同)的体积成像。可旋转环形台架12能够实现每分钟10转(rpm)或更高(例如,使用快速滑环旋转,包括例如高达10rpm、高达20rpm、高达60rpm或更高rpm)。可旋转台架12限定台架孔16,患者可以移动进入并通过该台架孔,并且被定位用于成像和/或治疗。根据一个实施例,可旋转台架12被配置为滑环台架,以提供成像放射源和相关联的放射检测器的连续旋转,同时为检测器接收的成像数据提供足够的带宽。滑环台架可以消除台架在交替方向上的旋转,以便卷绕和解开承载与设备相关联的电力和信号的线缆。如下面更全面地讨论的,即使当集成到igrt系统中时,这样的配置也能够允许连续的螺旋的(例如,扇形束、锥形束等)计算机断层摄影。如上所述,单旋转cbct的主要问题是在除了中心切片(包含旋转的切片)之外的所有切片上的采样不足。这可以通过螺旋轨迹锥形束成像来克服。
患者支撑件18邻近可旋转台架12被定位,并且配置成通常在水平位置支撑患者,以便纵向移动到可旋转台架12中和内部,患者支撑件18可以例如在垂直于台架12的旋转平面的方向上(沿着或平行于台架12的旋转轴)移动患者。患者支撑件18可以可操作地耦合到患者支撑件控制器,用于控制患者和患者支撑件18的移动,患者支撑件控制器可以与可旋转台架12和安装到旋转台架的放射源同步,用于根据命令的成像和/或治疗规划围绕患者纵轴旋转。在一些实施例中,一旦患者支撑件处于孔16中,患者支撑件也可以在有限范围内上下、左右移动,以调整患者位置用于最佳治疗。应当理解,在不脱离所公开的技术的范围的情况下,可以采用其它变型。例如,可旋转台架12和患者支撑件可被控制,使得当支撑件被控制为相对于可旋转台架12移动(以恒定或可变的速度)时,台架12以“前后移动的”方式(例如,交替的顺时针旋转和逆时针旋转)(如上所述,与连续地相反)围绕支撑在患者支撑件上的患者旋转。在另一实施例中,采用连续的步进拍摄(step-and-shoot)的圆形扫描,患者支撑件18在纵向方向上的运动(步进)与可旋转机架12的扫描绕转(拍摄)交替,直到期望的体积被捕获。设备10能够进行基于体积和基于平面的成像采集。例如,在各种实施例中,设备10可以用于采集体积图像和/或平面图像,并且执行下面描述的相关联的处理方法。
可以利用各种其它类型的放射源和/或患者支撑件移动来实现放射源和患者的相对运动以便产生投影数据。可以使用放射源和/或患者支撑件的非连续运动、连续但可变/非恒定(包括线性和非线性)线性移动、速度和/或轨迹等及其组合(其包括与上述放射诊疗设备10的各种实施例组合)。
如图2所示,放射诊疗设备10包括与可旋转台架12耦合的第一放射源20或由可旋转台架12支撑的第一放射源20。根据一个实施例,第一放射源20被配置为诊疗放射源(例如用于治疗患者体内感兴趣区的肿瘤的高能放射源)。应当理解,诊疗放射源可以是高能x射线束(例如兆伏(mv)x射线束)和/或高能粒子束(例如电子束、质子束或较重的离子束,例如碳)或其它合适形式的高能放射,而不脱离本公开技术的范围。在一个实施例中,第一放射源20包括1mev或更大的兆电子伏峰值光子能量(mev)。在一个实施例中,高能x射线束具有大于0.8mev的平均能量。在另一个实施例中,高能x射线束具有大于0.2mev的平均能量。在另一实施例中,高能x射线束具有大于150kev的平均能量。通常,第一放射源20具有比第二放射源30更高的能级(峰值和/或平均值等)。
下面详细描述的成像系统包括第二放射源30,其可以是产生相对低强度和低能量成像放射的独立x射线成像源。在一个实施例中,第二放射源30是x射线源,其被配置为千伏(kv)源(例如,具有在大约20kv到大约150kv范围内的能量水平的临床x射线源)。在一个实施例中,kv放射源包括高达150kev的千电子伏峰值光子能量(kev)。成像放射源可以是适于成像的任何类型的透射源。例如,成像放射源可以是例如x射线生成源(包括用于ct)或产生具有足够能量和通量的光子的任何其它方式(例如,γ源(例如,钴-57,122kev处的能量峰)、x射线荧光源(例如通过pbk线的荧光源,在约70kev处和在约82kev处的两个峰)等)。这里对x射线、x射线成像、x射线成像源等的引用是特定实施例的示例。在各种其它实施例中,可以互换地使用其它成像透射源。
还应当理解,第一放射源20可以向支撑在患者支撑件18上的患者体内的感兴趣区(roi)发射一个或多个放射束(通常由22表示)。第一放射源可以根据治疗规划发射一个或多个放射束。还将理解,治疗规划可以包括关于源角位置、波束几何形状、波束强度、调制、暴露等的详细参数。
在一个实施例中,第一放射源20是产生诊疗放射(例如mv)的linac,并且成像系统包括产生相对低强度和低能量成像放射(例如kv)的独立的第二放射源30。在其它实施例中,第一放射源20可以是放射性同位素(例如co-60,其通常具有>1mev的能量)。第一放射源20可以根据治疗规划向支撑在患者支撑件18上的患者体内的感兴趣区(roi)发射一个或多个放射束(通常由22表示)。
如下面详细讨论的,放射源20、30可以彼此结合使用,以提供更高质量和更好利用的图像。在其他实施例中,至少一个附加放射源可以耦合到可旋转台架12,并且被操作以在与放射源20、30的峰值光子能量不同的峰值光子能量处采集投影数据。
尽管图1和2描述了具有被安装到环形台架12上的放射源20的放射诊疗设备10,但是其它实施例可以包括其它类型的可旋转成像装置(例如包括c形臂台架和基于机器人臂的系统)。在基于台架的系统中,台架使成像放射源30围绕穿过等中心点的轴旋转。基于台架的系统包括c形臂台架,其中成像放射源30以悬臂方式安装在穿过等中心点的轴上并绕该轴旋转。基于台架的系统还包括环形台架,例如具有大致环形形状的可旋转台架12,其中患者的身体延伸穿过环/环形面的孔,并且成像放射源30安装在环的周边上并围绕穿过等中心点的轴旋转。在一些实施例中,台架12连续旋转。在其它实施例中,台架12利用基于线缆的系统,该系统反复地旋转和反转。
第一检测器24可以耦合到可旋转台架12或由其支撑,并且被定位成接收来自第一放射源20的放射22。第一检测器24可以检测或测量未衰减的放射量,因此推断实际上被患者或相关联的患者roi衰减的放射(通过与最初产生的放射比较)。当第一放射源20旋转并向患者发射放射时,第一检测器24可以检测或以其他方式收集来自不同角度的衰减数据。所收集的衰减数据可以被处理和重构为患者身体的一个或多个图像。
集成在放射诊疗设备10内的成像系统可以提供用于设置(例如,对准和/或配准)、规划和/或引导放射递送流程(治疗)的当前图像。典型的设置是通过将当前(治疗中)图像与治疗前图像信息(例如,在先或以其他方式先前获取的图像信息)进行比较来完成的。治疗前图像信息可以包括例如ct数据、cbct数据、磁共振成像(mri)数据、正电子发射断层摄影(pet)数据或3d旋转血管造影(3dra)数据和/或从这些或其他成像模态获得的任何信息。在一些实施例中,成像系统可以跟踪治疗中的患者、靶或roi运动。
常规的治疗中图像通常包括cbct或二维图像(通常为x射线)。可以在一个或多个不同的观察点(例如,立体x射线图像)处采集x射线,并且可以将所采集的x射线与从三维治疗前图像信息中导出的二维数字重构射线照片(drr)进行比较。cbct可以直接从靶体积的2d投影中构建3d体积图像。如本领域所公知的,在一个实施例中,cbct具有以更各向同性的空间分辨率从围绕靶体积的单次台架旋转形成3d图像体积的能力。在其它实施例中,cbct可以利用螺旋扫描轨迹。然而,如上所述,散射、不完整数据和/或伪影对于cbct系统可能是严重的问题,从而限制了图像质量。可以理解,使用传统技术,这些和其它传统的放射诊疗治疗中的成像系统缺乏产生适合于基于图像的预递送步骤的高质量和/或使图像完整的能力,所述基于图像的预递送步骤包括实时治疗规划。
如图2所示,集成在放射诊疗设备10内的成像系统包括耦合到可旋转台架12的第二放射源30或由可旋转台架12支撑的第二放射源30。如上所述,第二放射源30可被配置为具有低于第一治疗放射源20的能量级别的用于高质量治疗中图像(通常表示为32)的成像放射源(例如kv)。
第二检测器34(例如二维平面检测器或曲面检测器)可以耦合到可旋转台架12或由可旋转台架12支撑。第二检测器34被定位成接收来自第二放射源30的放射。检测器34可以检测或以其他方式测量未衰减的放射量,并因此推断实际上被患者或相关联的患者roi衰减的放射(通过与最初生成的放射相比较)。当第二放射源30旋转并向患者发射放射时,检测器34可以检测或以其他方式收集来自不同角度的衰减数据。
准直器或波束成形器组件(通常表示为36)相对于第二放射源30被定位,以选择性地控制和调整由第二放射源30发射的放射束32的形状,以选择性地暴露第二放射检测器34的有效区域的一部分或一区(region)。准直器36还可以控制放射束32如何被定位在检测器34上。在一个实施例中,准直器36可以具有一个运动度/维度(例如,以形成更细或更粗的狭缝)。在另一个实施例中,准直器36可以具有两个运动度/维度(例如,以形成各种大小的矩形)。在其它实施例中,准直器36可以具有各种其它动态控制的形状(包括例如平行四边形)。所有这些形状都可以在扫描期间动态地被调整。在一些实施例中,准直器的阻挡部分可以被旋转和/或平移。
准直器/波束成形器36可以以多种方式被配置,以允许其调整由第二放射源30发射的放射束32的形状。例如,准直器36可以被配置成包括一组钳口(jaw)或其他合适的构件,其限定和选择性地调整(来自第二放射源30的放射束可以以准直方式穿过的)孔径的大小。根据一个示例性配置,准直器36可以包括上钳口和下钳口,其中上钳口和下钳口可在不同方向(例如,平行方向)上移动,以调整来自第二放射源30的放射束穿过的孔的大小,并且还调整射束32相对于患者的位置以仅照射患者的待成像部分,以用于优化成像和最小化患者剂量。例如,准直器可以被配置为多叶片准直器(mlc),该mlc可以包括多个交错的叶片,所述多个交错的叶片可操作以移动到最小打开或关闭位置与最大打开位置之间的一个或多个位置。应当理解,叶片可以移动到期望的位置以实现由放射源发射的放射束的期望形状。在一个实施例中,mlc能够具有亚毫米的靶定位精度。
根据一个实施例,来自第二放射源30的放射束32的形状可以在图像采集期间改变。换句话说,根据一个示例性实施方式,可以在扫描之前或期间调整准直器36的叶片位置和/或孔径宽度。例如,根据一个实施例,准直器36可以在第二放射源30的旋转期间被选择性地控制和动态地调整,使得放射束32具有带有足够的原发(primary)/阴影区的形状,并且被调整为在成像期间仅包括感兴趣的对象(例如,前列腺)。取决于期望的图像采集,由第二放射源30发射的放射束32的形状可以在扫描之前、期间和/或之后被选择性地控制,所述期望的图像采集可以基于成像和/或诊疗反馈,如以下更详细讨论的。
还应当理解,第一放射源20可以包括波束成形器或准直器,或者与波束成形器或准直器相关联。与第一放射源20相关联的准直器/波束成形器可以以多种方式被配置,这类似于与第二放射源30相关联的准直器36。
准直器组件36可以被控制以采用多种几何形状调节由第二放射源30发射的放射束32的形状,所述形状包括但不限于具有低至一个检测器行宽的波束厚度(宽度)或包括多个检测器行的扇形束、厚扇形束或锥形束,所述宽度或多个检测器行可以仅是检测器的有效区域的一部分。在各种实施例中,波束的厚度可以暴露几厘米的较大检测器有效区域。例如,5-6厘米检测器中的3-4厘米(在检测器平面的纵向上测量)可以被选择性地暴露于成像放射32。然而,在其他实施例中,各种其他暴露和有效区域大小或暴露与有效检测器区域的比率可以是合适的。
根据一个示例性实施例,上文已经将放射诊疗设备10描述为包括第一放射源20、第二放射源30、被定位为接收来自第一放射源20的放射的第一放射检测器24和被定位为接收来自第二放射源30的放射的第二放射检测器34。然而,将意识到,在不脱离所公开技术的范围的情况下,放射诊疗设备10可以包括第一放射源20(例如,治疗放射源)、第二放射源30(例如,kv放射源)和仅被定位为接收来自第二放射源30的放射检测器34。
放射源20可以被安装、配置和/或移动到与放射源30相同的平面或不同的平面(偏移)中。在一些实施例中,通过偏移放射平面可以逐渐地减少由放射源20、30的同时激活引起的散射。在其他实施例中,可以通过使激活交错来避免散射。例如,在同时进行多模式成像的情况下,可以同时进行采集,而不需要同时进行单独的脉冲。在另一个实施例中,基于阴影的散射校正的使用可用于(例如)解决kv检测器上的mv散射的问题。
被集成作为放射诊疗设备,装置10可以提供用于设置(例如,对准和/或配准)、规划和/或引导放射递送流程(治疗)的图像。典型的设置是通过将当前(治疗中)图像与治疗前图像信息进行比较来完成的。治疗前图像信息可以包括例如ct数据、cbct数据、mri数据、pet数据或3d旋转血管造影(3dra)数据,和/或从这些或其他成像模态获得的任何信息。在一些实施例中,设备10可以跟踪治疗中的患者、靶或roi运动。
重构处理器40可以可操作地耦合到第一检测器24和/或第二检测器34。在一个实施例中,重构处理器40被配置为基于由检测器24、34从放射源20、30接收的放射生成患者图像。将意识到,重构处理器40可以被配置为用于执行下面更全面描述的方法。装置10还可以包括存储器44,其适于存储信息(包括但不限于处理和重构算法和软件、成像参数、来自在先或以其他方式先前采集的图像(例如,规划图像)的图像数据、治疗规划等)。
放射诊疗设备10可以包括操作者/用户接口48,其中放射诊疗设备10的操作者可以与放射诊疗设备10交互或以其他方式控制放射诊疗设备10,以提供与扫描或成像参数等相关的输入。操作者接口48可以包括任何合适的输入设备(例如键盘、鼠标、语音激活的控制器等)。放射诊疗设备10还可以包括显示器52或其它的人可读元件,以向放射诊疗设备10的操作者提供输出。例如,显示器52可以允许操作者观察重构的患者图像和与放射诊疗设备10的操作相关的其它信息(例如成像或扫描参数)。
应当理解,相对于第二放射源30被定位的准直器组件36可以被构造为提供对由第二放射源30发射的放射束的动态准直。
可以控制准直器组件36,使得来自第二放射源30的波束32基于正在执行的特定成像任务覆盖第二检测器34的同样多或同样少的部分。例如,准直器36可以被选择性地控制以提供扇形束,该扇形束具有来自单个检测器行的扇形厚度,该扇形厚度可以是亚毫米(其可高达几厘米)(包括例如3-4厘米的波束厚度(在检测器平面中的纵向方向上测量))。根据所公开的技术的方面,这种波束配置可以用在连续的螺旋的扇形束成像模式中。在其它实施例中,可以使用圆形成像模式,其包括使用较大的扇形束或锥形束厚度。例如,对于任何模式,准直器36可以被选择性地控制以提供具有大约一厘米厚度的波束。根据另一示例性实施例,准直器36可以被选择性地控制以提供具有大于一厘米或几厘米的厚度的波束(其包括例如在大约两厘米和大约四厘米之间)。根据另一示例性实施例,准直器36可以被选择性地控制以提供具有在大约十五厘米和大约三十厘米之间的厚度的波束32。根据另一示例性实施例,准直器36可以被选择性地控制以提供具有在大约三十五厘米和大约四十厘米之间的厚度的波束32。通常,可以控制系统和波束几何形状以产生薄(例如,单行)、厚(例如,多行)或锥形的波束。
根据一个实施方式,来自第二放射源30的射束32的几何形状可以在图像采集期间改变。换句话说,根据一个示例性实施方式,可以在扫描之前或期间准直器36的叶片位置和/或孔径宽度可被调整。例如,根据一个实施例,在第二放射源30的旋转期间准直器36可被选择性地控制和动态地调整,使得波束32具有仅包括成像期间的感兴趣对象(例如前列腺)的矩形几何形状。
如图2所示,放射诊疗设备10包括可操作地连接到放射诊疗系统10的一个或多个部件的控制器(通常表示为60)。控制器60控制放射诊疗装置10的整体功能和操作,包括向第一放射源20和/或第二放射源30以及控制可旋转台架12的旋转速度和位置的台架马达控制器提供功率和定时信号。应当理解,控制器60可以包括以下各项中的一个或多个:患者支撑件控制器、台架控制器、被耦合到第一放射源20和/或第二放射源30的控制器、准直器组件控制器、被耦合到第一检测器24和/或第二检测器34的控制器等。在一个实施例中,控制器60是可以控制其它部件、设备和/或控制器的系统控制器。
在各种实施例中,重构处理器40、操作者接口48、显示器52、控制器60和/或其他部件可以组合成一个或多个部件或设备。
放射诊疗系统10可以包括各种部件、逻辑和软件。在一个实施例中,控制器60包括处理器、存储器和软件。作为示例而非限制,放射诊疗系统(例如,图1和图2中所示的放射诊疗系统10)可以包括各种其他设备和部件(例如,台架、放射源、准直器、检测器、控制器、电源、患者支撑件等),其可以实现与针对特定应用的成像和/或igrt相关的一个或多个例程或步骤。其中,例程可以包括成像、基于图像的预递送步骤和/或治疗递送,其包括可以存储在存储器中的相应设备设置、配置和/或位置(例如,路径/轨迹)。其它例程包括与数据和图像处理相关联的过程和/或算法,其包括例如以下描述的过程。此外,控制器(一个或多个)可以根据存储在存储器中的一个或多个例程或过程来直接或间接地控制一个或多个设备和/或部件。直接控制的一个例子是设置与成像或治疗相关联的各种放射源或准直器参数(功率、速度、位置、定时、调制等)。间接控制的一个例子是将位置、路径、速度等传达到患者支撑件控制器或其它外围设备。可以以任何适当的方式布置可能与放射诊疗设备10相关联的各种控制器的层级,以将适当的命令和/或信息传达到期望的设备和部件。
此外,本领域技术人员将理解,可以利用其它计算机系统配置来实现该系统和方法。本发明的所示方面可以在分布式计算环境中实现,其中某些任务由通过通信网络链接的本地或远程处理设备来执行。例如,在一个实施例中,重构处理器40可以与单独的系统相关联。在分布式计算环境中,程序模块可以位于本地和远程存储器存储设备中。例如,可以与放射诊疗设备10一起使用远程数据库、本地数据库、云计算平台、云数据库或其组合。
放射诊疗设备10可以利用用于实现本发明的各个方面的示例性环境(包括计算机),其中,所述计算机包括控制器60(例如,包括处理器和存储器,其可以是存储器44)和系统总线。系统总线可以将包括但不限于存储器的系统部件耦合到处理器,并且可以与其他系统、控制器、部件、设备和处理器通信。存储器可以包括只读存储器(rom)、随机存取存储器(ram)、硬盘驱动器、闪存驱动器和任何其它形式的计算机可读介质。存储器可以存储各种软件和数据,其包括例程和参数(其可以包括例如治疗规划)。
第一放射源20和/或第二放射源30可以可操作地连接到控制器60,该控制器被配置成控制第一放射源20和第二放射源30的相对操作。例如,第二放射源30可以与第一放射源20同时控制和操作。另外,或者可选地,第二放射源30可以与第一放射源20顺序控制和操作,这取决于所实施的具体治疗和成像规划。
应当理解,第二检测器34可以采用多种配置,而不脱离所公开的技术的范围。如图2所示,第二检测器34可被配置为平板检测器(例如,多行平板检测器)。根据另一示例性实施例,第二检测器34可被配置为弯曲的检测器。
无论第二检测器34的配置或几何形状如何,应当理解,相对于第二放射源30被定位或以其它方式与其相关联的准直器组件36可以被选择性地控制,以控制由第二放射源30发射的放射束32的形状,从而选择性地暴露第二放射检测器34的部分或全部。例如,根据一个示例性实施例,来自第二放射源的波束可以被准直或以其它方式被控制,以提供成像放射的扇形或锥形束。应当理解,可以基于特定的期望的成像应用来控制波束的大小和几何形状。根据所公开的技术的一个示例,准直器组件36可以被选择性地控制,使得由第二放射源发射的放射束32是扇形束(其具有大于和小至大约一厘米的扇形束厚度)。如上所述,由第二放射源发射的放射束32的几何形状可以在扫描期间或之后改变,这取决于期望的图像采集(其可以基于成像和/或诊疗反馈)。
应当理解,第二放射源30和被定位成接收来自第二放射源30的放射的第二检测器34可以被配置为在成像扫描期间提供围绕患者的连续旋转。此外,使第二放射源30的运动和暴露与患者支撑件的纵向运动同步可以在流程期间提供患者图像的连续的螺旋的扇形束采集。
下面的流程图和框图示出了根据上述系统的与ct和/或igrt相关联的示例性配置和方法。示例性方法可以在逻辑、软件、硬件或其组合中执行。另外,尽管以一定顺序呈现了流程和方法,但是可以以不同的顺序(包括串行和/或并行)执行方框。特别地,例如,第一放射源20和第二放射源30可以顺序地和/或同时地被激活。因此,尽管被顺序地示出,但是以下步骤(包括成像、图像处理、基于图像的预递送步骤和治疗递送),可以同时被执行(包括实时地被执行)。此外,可以使用附加步骤或更少步骤。
图3是用于生成改进或校正图像的示例性方法300的流程图。该方法300包括利用图像配准和分析重构算法的图像校正方案。图4是示出与方法300相关联的示例性数据的框图400。继续参考图3和图4,在步骤310,输入数据包括但不限于从可用的源轨迹
在步骤320,可以执行使用原发数据
在步骤330,在初始重构
步骤340包括设计或以其他方式生成将提供缺失数据的附加的源轨迹片段,以用于靶向的感兴趣体积的改进的图像重构。然后,沿着该附加的源轨迹,虚拟前向投影器被应用于i1以生成一组新的投影数据,其被表示为p1。这种前向投影器可以利用一种或多种合适的方法(例如siddon或joseph的方法),而不脱离所公开的技术的范围。在一个实施例中,这种前向投影方法可使用与原发数据
然而,应当理解,用于所述附加的片段的检测器配置可以允许不同的尺寸和检测器像素大小。以圆形源轨迹为例,这种附加的源轨迹片段可以是连接到圆形轨迹的线或弧,并且投影器可以包括管电势、管电流、光谱等。对于螺旋轨迹,附加的一条源轨迹可以在纵向方向上从初始源轨迹延伸,并且可以是例如螺旋、线和弧的形式。
在步骤350,执行使用
现在参考图5,提供了示例性图像处理/生成方法500的流程图。应当理解,图像生成方法500可以包括与igrt流程结合的成像方法(例如ct),其中可以在治疗流程之前和/或期间捕获患者图像。在一个实施例中,方法500可以与放射诊疗设备10相关联,如上所述。在这种示例性情况下,在先或以其他方式先前采集的图像可以是治疗前或规划图像。或者,结合图5描述的成像方法500可独立于igrt应用而进行。
方法500在步骤510开始,其中接收对应于在先或先前采集的患者图像的图像数据。根据一个实施例,所接收的图像数据可以是在先ct图像(例如规划图像)。或者,所接收的图像可以来自另一成像模态(例如,磁成像共振(mr)图像)。根据一个实施例,所接收的图像数据可以是来自在先规划图像的ct图像数据,所述在先规划图像被收集以用于igrt流程并与igrt流程结合使用。
在步骤520,可以获得患者的投影图像数据(例如,通过使用例如设备10的ct成像操作,诸如kv成像操作、mv成像操作等)。根据一个实施例,可以至少轴向地截断所获得的投影图像数据。根据另一实施例,可以横向地以及轴向地截断所获得的投影图像数据。在其他实施例中,代替截断数据或除了截断数据之外,投影图像数据可以包括伪像。在一些实施例中,使用截断数据和/或具有伪影的数据的能力可以允许更快的扫描,这还可以减少图像放射剂量。例如,在一些实施例中,对截断数据和/或具有伪像的数据进行校正或改进的能力允许增加螺旋节距,从而导致更快的扫描,而不管所产生的缺陷。
在步骤530,可以基于所获得的患者的投影图像数据执行图像重构以生成或获得患者图像。应当理解,在不脱离所公开的技术的范围的情况下,可以采用多种重构技术/算法中的任何一种。例如,fdk算法可以与圆形图像采集轨迹一起使用,并且加权滤波反投影可以与螺旋图像采集轨迹一起使用。
在步骤540,患者的在先图像可以与获得的(重构的)患者图像配准(例如,使用应用几何形状变换和/或局部位移以对准相应图像的任何合适的过程)。应当理解,在不脱离所公开的技术的范围的情况下,可以采用任何合适的图像配准方法。例如,可以使用适当的刚性图像配准过程(例如,其中像素均匀地移动和/或旋转,使得每个像素到像素的关系在变换之后保持相同)将患者的在先图像与所获得的患者图像配准。根据另一范例,可以使用合适的可变形图像配准过程(例如,在像素到像素关系改变的情况下)将患者的在先图像与所获得的患者图像配准。
在步骤550,可以基于在先或以其他方式先前采集的图像(例如,规划图像)生成虚拟投影数据,以提供补充的投影图像数据集(包括患者的所获得的投影图像数据和虚拟投影数据)。应当理解,该步骤可以包括设计或采用附加的源轨迹片段(其理论上将提供缺失数据,以用于改进靶向的感兴趣体积的图像重构)。然后,沿着该附加源轨迹,可以将虚拟前向投影器应用于配准的在先或以其他方式先前采集的图像,以生成新投影数据集。这种前向投影器可以利用一种或多种合适的方法(例如siddon方法或joseph方法),而不脱离所公开的技术的范围。这种前向投影方法应当使用与所获得的投影图像数据相同的数据采集配置,以确保图像数据集一致。
然而,应当理解,用于附加的片段的检测器配置可以允许不同的尺寸和检测器像素大小。以圆形源轨迹为例,这种附加的源轨迹片段可以是连接到圆形轨迹的线或弧,并且投影器可以包括管电势、管电流、光谱等。对于螺旋轨迹,附加源轨迹可以在纵向方向上从初始源轨迹延伸,并且可以是例如螺旋、线和弧的形式。
在步骤560,可以重构补充的投影图像数据集。再次,将理解,在不背离所公开的技术的范围的情况下,可以部署任何数量的重构算法或方法。在步骤570,可以输出改进的或以其他方式补充的患者图像以用于在多个诊断和/或治疗应用。改进的或以其他方式补充的患者图像将是基于补充的投影图像数据的。以这种方式,改进的或以其他方式补充的患者图像是基于在投影图像数据采集期间未捕获的图像数据的。
图6是用于生成改进或校正图像的另一示例性方法600的流程图。该方法600包括利用图像配准、分析重构和迭代重构算法的图像校正方案。方法600可以扩展方法300以用于实施的数据一致性。为了解释的目的,将理解,通常的情况是投影数据和在先/规划图像不一致,因为患者解剖结构可能在两个不同时间之间不相同。因此,例如,利用如上参考图3所述的图像改进/校正方法,使用p1重构的图像可能导致新的伪影。这种问题可以通过使用迭代过程实施重构和原发投影数据之间的数据一致性来克服。
图6的方法600可以利用例如来自图3的步骤310到350的校正或改进的图像(如上所述),如步骤610所示。特别地,在620的输入可以包括图3的步骤360中所示的方法300的输出u1。在步骤620,k被设置为等于1并且
为了解释的目的,fp指前向投影,而recon指解析重构算法,其可以与用于上面关于图3描述的初始重构的算法相同或不同。
在步骤630,例如使用与用于原发投影数据
在步骤640,计算新投影数据
然后在步骤650,从当前图像
在步骤660,基于特定标准(在670产生输出
图7是用于生成改进或校正图像的另一示例性方法700的流程图。该方法700包括利用图像配准、分析重构和迭代重构算法的图像校正方案。方法700可扩展方法600,另外将迭代过程应用于校正方案以及一致性实施。应当理解,图7中所示的方法700包括在先图像细化方法。例如,由图6的方法600生成的图像
在该实施例中,在步骤710,方法700执行步骤310,并且j被设置为等于1。接下来的步骤720执行步骤320到350(其包括基于迭代j来校正图像并细化在先图像)。在步骤730,方法700执行步骤620(其包括基于迭代j)。下一步骤740执行步骤630到660(其包括其k个循环并基于迭代j以实施一致性)。在步骤750,方法700确定是否停止配准循环。在步骤760,如果不满足停止标准,则j递增到j+1,
方法600和/或方法700还可以与方法500组合以进一步改进输出的患者图像。例如,图8是示例性图像处理/生成方法800的流程图。该方法800包括来自方法500的步骤510到560、步骤810(其结合/组合如上所述的方法600),并且在820处输出改进的患者图像。图9是另一示例性图像处理/生成方法900的流程图。该方法900包括来自方法500的步骤510到560、步骤910(其结合/组合如上所述的方法600)、步骤920(其结合/组合如上所述的方法700),并且在930处输出改进的患者图像。
图10是描述使用放射诊疗设备(例如,放射诊疗设备10)的igrt的示例性方法1000的流程图。患者的在先图像数据1005可供使用(例如,在先图像
接下来,在步骤1030,至少部分地基于来自步骤1010的成像数据1015来执行下面讨论的一个或多个基于图像的预递送步骤。如下面更详细地讨论的,步骤1030可以包括确定与诊疗处理和(后续)成像规划相关联的各种参数。在一些实施例中,基于图像的预递送步骤(1030)可能在治疗递送(1040)之前需要更多成像(1010)。步骤1030可以包括基于成像数据1015调整治疗规划,作为自适应放射疗法例程的部分。在一些实施例中,基于图像的预递送步骤1030可以包括实时治疗规划。实施例还可以包括同时、重叠和/或交替激活成像和诊疗放射源。实时治疗规划可以涉及这些类型的成像和诊疗放射激活技术(同时、重叠和/或交替)中的任何或全部。
接下来,在步骤1040,使用高能放射源(例如,来自第一放射源20的mv放射)执行诊疗处理递送。步骤1040根据治疗规划向患者递送治疗剂量1045。在一些实施例中,igrt方法1000可以包括返回到步骤1010,以便以各种间隔进行附加成像,随后是根据需要的基于图像的预递送步骤(1030)和/或治疗递送(1040)。以这种方式,可以在igrt期间使用能够进行自适应诊疗的放射诊疗设备10来产生和利用成像数据1015。如上所述,步骤1010、1020、1030和/或1040可以同时、重叠和/或交替执行。
igrt可以包括至少两个一般目标:(i)将高度适形的剂量分布递送至所述靶体积;以及(ii)在每个治疗分次(fraction)中以高精度递送治疗波束。第三个目标可以是在每分次用尽可能少的时间内完成两个一般目标。精确地递送治疗波束需要利用高质量图像来识别和/或跟踪分次内的靶体积的位置的能力。增加递送速度的能力需要根据治疗规划准确、精确和快速地移动放射源的能力。
图11是描述可以与上述步骤1030相关联的示例性的基于图像的预递送步骤/选项的框图1100。应当理解,上述放射诊疗设备(例如,放射诊疗设备10)可以生成kv图像,所述图像可以以多种方式被使用(包括用于基于图像的预递送步骤(1030)),而不脱离本发明的范围。例如,由放射诊疗设备生成的图像1015可以用于在治疗之前对准患者(1110)。患者对准可以包括将当前成像数据1015与较早治疗前扫描和/或规划(其包括治疗规划)相关联的成像数据相关联或配准。患者对准还可以包括关于患者相对于放射源的物理位置的反馈,以验证患者是否物理上在递送系统的范围内。如果需要,患者可以相应地被调整。在一些实施例中,患者对准成像可以故意地具有较低的质量以最小化剂量,但是提供足够的对准信息。
由放射诊疗设备生成的图像还能够用于治疗规划或重新规划(1120)。在各种实施例中,步骤1120可以包括确认治疗规划、修改治疗规划、生成新的治疗规划和/或从一组治疗规划(有时被称为“当日规划”)中选择治疗规划。例如,如果成像数据1015显示靶体积或roi与当开发治疗规划时相同,则可以确认治疗规划。然而,如果靶体积或roi不相同,则可能需要重新规划诊疗处理。在重新规划的情况下,由于(在步骤1010由x射线成像设备10生成的)成像数据1015的高质量,成像数据1015可以用于治疗规划或重新规划(例如,生成新的或修改的治疗规划)。以这种方式,不需要通过不同设备的治疗前ct成像。在一些实施例中,确认和/或重新规划可以是在各种治疗之前和/或之后正在进行的流程。
根据另一示范性使用范例,由放射诊疗设备10生成的图像能够用于计算成像剂量(1130),其可以用于对患者的总剂量的持续确定和/或用于随后的成像规划。随后成像的质量也可以作为治疗规划的一部分来确定,例如,以平衡质量和剂量。根据另一示例性用例,由放射诊疗设备10生成的图像可以用于计算治疗剂量(1140),其可以用于对患者的总剂量的持续确定和/或可以被包括作为治疗规划或重新规划的一部分。
根据其他示例性用例,由放射诊疗设备10生成的图像可以与规划或调整其他成像(1150)和/或其他治疗(1160)参数或规划结合使用,其包括例如作为自适应治疗和/或治疗规划生成的部分。根据另一示例性用例,由放射诊疗设备10生成的图像可以与自适应治疗监视(1170)结合使用,其可以包括监视治疗递送并且根据需要进行适配。
应当理解,基于图像的预递送步骤(1030)不是相互排斥的。例如,在各种实施例中,计算治疗剂量(1140)可以是单独的步骤和/或可以是自适应诊疗监视(1170)和/或治疗规划(1120)的一部分。在各种实施例中,基于图像的预递送步骤(1030)可以自动地和/或在人工参与的情况下手动地执行。
图12是描绘了可以在成像(1010)和/或随后的基于图像的预递送步骤(1030)(除了在先数据1005,还包括治疗规划1120)期间使用的示例性数据源的框图1200。检测器数据1210表示由图像放射检测器34接收的数据。投影数据1220是由入射到准直束区域中的放射产生的数据,该准直波束区域可以被称为原发区。半影数据1230是由入射到半影区或区域中的放射产生的数据。散射数据1240是由入射在外围或散射(仅)区或区域中的放射生成的数据。
半影数据1230和/或散射数据1240可以用于提高由成像步骤1010产生的图像的质量。在一些实施例中,半影数据1230和/或散射数据1240可以与投影数据1220组合和/或鉴于可应用的成像设置1250、治疗设置1260(例如,如果同时成像和治疗放射)以及在成像检测器34处的数据收集时与放射诊疗设备10相关联的任何其他数据1270而被分析。
如上所述,所公开的技术的各方面涉及计算机断层摄影(ct)成像系统和方法,其中在先或先前采集的患者图像(例如规划图像)可以用于补充或以其他方式改进所采集的ct图像。其中,表示所采集的ct图像的所采集的投影数据可能被截断或以其他方式不完整/不足以准确地恢复被扫描对象/患者,以用于准确且稳定的图像重构。所公开的方法避免了使用一个或多个附加轨迹来采集数据的附加扫描,从而避免了增加的患者剂量并且避免了成像工作流程的复杂性。
尽管已经关于特定方面、实施例或多个实施例示出和描述了所公开的技术,但是显然,本领域技术人员在阅读和理解本说明书和附图之后将想到等效的变更和修改。特别地,关于由上述元件(部件、组件、设备、构件、组成等)执行的各种功能,除非另外指出,否则用于描述这些元件的术语(包括对“手段”的引用)旨在对应于执行所描述的元件的指定功能的任何元件(即,功能上等同),即使结构上不等同于执行所公开的技术的本文所示的示例性方面、一个或多个实施例中的功能的所公开的结构。另外,虽然上文可能已相对于若干所说明方面或实施例中的仅一者或一者以上描述所揭示技术的特定特征,但此特征可与其它实施例的一个或一个以上其它特征组合,如对于任何给定或特定应用可能需要且有利。
虽然本文所讨论的实施例涉及上文所讨论的系统和方法,但是这些实施例旨在是示例性的,并且不旨在将这些实施例的适用性限制为仅本文所阐述的那些讨论。虽然已经通过对本发明的实施例的描述对本发明进行了说明,并且虽然已经相当详细地描述了实施例,但是申请人的意图不是将所附权利要求的范围限制或以任何方式限制到这样的细节。本领域技术人员将容易想到附加的优点和修改。因此,本发明在其更广泛的方面不限于所示出和描述的具体细节、代表性装置和方法以及说明性示例。因此,在不脱离申请人的总体发明构思的实质或范围的情况下,可以偏离这些细节。
- 还没有人留言评论。精彩留言会获得点赞!