作为TLR信号传导的调节剂的化合物和组合物的制作方法
作为tlr信号传导的调节剂的化合物和组合物
1.相关申请的交叉引用
2.本技术要求2019年3月26日提交,题为“compounds as modulators of tlr2 signaling”的美国临时申请第62/824,170号以及2019年3月26日提交,题为“compounds as modulators of tlr2 signaling”的美国临时申请第62/824,189号的优先权,所述美国临时申请的内容据此出于所有目的通过引用以它们的整体并入本文。
技术领域
3.本公开涉及化合物、包含此类化合物的药物组合物、以及此类化合物在治疗炎症性疾病和与包括但不限于蛋白质错误折叠的炎症性信号传导过程相关的某些神经病症的方法中或在用于治疗所述炎症性疾病和某些神经病症的药剂中的用途。
背景技术:
4.toll样受体(tlr)是免疫系统的哨兵受体。当这些受体在细胞表面上活化时,它们引发对含有tir结构域的衔接蛋白家族的募集,所述衔接蛋白诱导信号传导级联,所述信号传导级联最终导致细胞类型特异性炎症性应答,从而导致促炎性介体诸如il1、il6、il8和tnfα的升高。在哺乳动物细胞上表达的不同tlr受体之中,tlr2与tlr1或tlr6形成异二聚体以与各种微生物源性配体一起引发炎症性应答。在各种细菌配体之中的是脂多糖(lps)、酰化脂肽、脂聚糖、肽聚糖、孔蛋白(porin)、糖基磷脂酰肌醇锚定物、以及其他细菌细胞壁组分诸如来自肺炎链球菌(streptococous pneumonia)的脂磷壁酸(lipoteichoic acid,lta)。除微生物活化tlr2之外,还已发现在包括帕金森氏病(parkinson’s disease,pd)、路易体痴呆(dementia with lewy bodies)、多系统萎缩(msa)和阿尔茨海默氏病(alzheimer’s disease,ad)的神经变性疾病的动物模型中,神经元释放的寡聚蛋白质诸如α-突触核蛋白(asyn)的异常聚集可诱导类似炎症性应答。参见例如kim等人,nat.commun.2013,4,1562。
5.tlr2通过异二聚体诱导信号传导的能力允许辨别各种识别模式,此允许设计具有特定抑制模式的配体。kajava等人,j.biol.chem.2010,285,6227。因此,主要与特定病理性激动剂诸如寡聚病原性α-突触核蛋白竞争,但不影响细菌性或病毒性感染的促炎性信号传导中涉及的其他配体的抑制剂,或非竞争性tir-myd88抑制剂诸如通过细胞内tir-myd88抑制来间接充当tlr2的非竞争性抑制剂的化合物,将可用作潜在治疗剂。
6.toll样受体的功能已与各种蛋白质折叠、蛋白质二聚化和炎症性过程,并且与相关疾病诸如阿尔茨海默氏病(gambuzza,m.等人,“toll-like receptors in alzheimer’s disease:a therapeutic perspective,”cns neurol.disord.durg targets 2014,13(9),1542-58)、帕金森氏病和伴有痴呆的帕金森氏病(beraud,d.等人,“misfoldedα-synuclein and toll-like receptors:therapuetic targets for parkinson's disease,”parkinsonism relat.disord.2012,18(增刊1),s17-20)、额颞性痴呆、路易体痴呆(路易体病)、多系统萎缩(vieira,b.等人,“neuroinflammation in multiple system atrophy:
response to and cause of a-synuclein aggregation,”front.cell neurosci.2015,9,437)、肌萎缩性侧索硬化(casula,m.等人,“toll-like receptor signaling in amyotrophic lateral sclerosis spinal cord tissue,”neuroscience 2011,179,233-43)、亨廷顿氏病(huntington’s disease)(kalathur,r.k.r.等人,“huntington’s disease and its therapeutic target genes:a global functional profile based on the hd research crossroads database,”bmc neurology2012,12,47)、炎症性疾病、哮喘和慢性阻塞性肺病(copd)(zuo,l.等人,“molecular regulation of toll-like receptors in asthma and copd,”front.physiol.2016,6,312)、慢性消化性溃疡(smith,s.,“roll of toll-like receptors in helicobacter pylori infection and immunity,”world j.gastrointest.pathophysiol.2014,5(3),133-146)、结核病(harding,c.v.等人,“regulation of antigen presentation by mycobacterium tuberculosis:a role for toll-like receptors,”nat.rev.microbiol.2010,8(4),296-307)、类风湿性关节炎(huang,q.-q.等人,“roll of toll like receptors in rheumatoid arthritis,”curr.rheumatol.rep.2009,11(5),357-364)、慢性鼻窦炎(zhang,q.等人,“differential expression of toll-like receptor pathway genes in chronic rhinosinusitis with or without nasal polyps,”acta otolaryngol.2013,133(2),165-173)、肝炎(包括乙型肝炎和丙型肝炎)(zhang,e.等人,“toll-like receptor(tlr)-mediated innate immune responses in control of hepatitis b virus(hbv)infection,”med.microbiol.immunol.2015,204(1),11-20;howell,j.等人,“toll-like receptors in hepatitis c infection:implications for pathogenesis and treatment,”j.gastroenterol.hepatol.2013,28(5),766-776)、痛风、狼疮、牛皮癣、牛皮癣性关节炎(santegoets,k.c.m.等人,“toll-like receptors in rheumatic diseases:are we paying a high price for our defense against bugs?”febs letters 2011,585(23),3660-3666)、血管炎、喉炎、胸膜炎(chen,x.等人,“engagement of toll-like receptor 2on cd4(+)t cells facilitates local immune responses in patients with tuberculous pleurisy,”j.infect.dis.2009,200(3),399-408)、湿疹(miller,l.s.,“toll-like receptors in skin,”adv.dermatol.2008,24,71-87)、胃炎(schmausser,b.等人,“toll-like receptors tlr4,tlr5 and tlr9 on gastric carcinoma cells:an implication for interaction with helicobacter pylori,”int.j.med.microbiol.2005,295(3),179-85)、血管炎(song,g.g.等人,“toll-like receptor polymorphisms and vasculitis susceptibility:meta-analysis and systematic review,”mol.biol.rep.2013,40(2),1315-23)、喉炎(king,s.n.等人,“characterization of the leukocyte response in acute vocal fold injury,”plos one,2015;10(10):e0139260)、过敏反应(gangloff,s.c.等人,“toll-like receptors and immune response in allergic disease,”clin.rev.allergy immunol.2004,26(2),115-25)、多发性硬化症(miranda-hernandez,s.等人,“role of toll-like receptors in multiple sclerosis,”am.j.clin.exp.immunol.2013,2(1),75-93)、克罗恩氏病(crohn’s disease)(cario,e.,“toll-like receptors in inflammatory bowel diseases:a decade later,”inflamm.bowel dis.2010,16(9),1583-1597)以及创伤性脑损伤(hua,f.
等人,“genomic profile of toll-like receptor pathways in traumatically brain-injured mice:effect of exogenous progesterone,”j.neuroinflammation 2011,8,42)相关联。
7.可通过外部结构域(激动剂口袋)或通过涉及在信号传导期间介导同型和异型相互作用的细胞质tir结构域的机制来活化tlr2的信号转导路径。蛋白质myd88和tirap(mal)涉及于这个类型的信号传导中。
8.重要的是,tlr2中在bb环内的保守脯氨酸p681(brown v.等人(2006)european journal of immunology 36,742-753)涉及于二聚化机制中。这个环中的由p681h所致的突变消除了对myd88的募集和信号传导。因此,在这个环的附近结合,并且限制它在二聚化过程期间的移动的化合物将可用作tlr2活化的抑制剂。
9.tlr9是一种涉及于宿主防御机制中的模式识别受体。tlr9的持续或不适当活化已牵涉于许多不同中枢神经系统(cns)和外周病症中。因此,单独或与tlr2阻断组合的tlr9抑制可提供治疗益处。其中已牵涉tlr9的cns病症包括帕金森氏病(maatouk等人,nat commun.2018年6月22日;9(1):2450);肌萎缩性侧索硬化(o’rourke等人,science.2016年3月18日;351(6279):1324-9);格林-巴利综合征(guillain-barre syndrome)(wang等人,immunol invest.2011,2012;41(2):171-82);脊髓损伤(li等人,brain behav immun.2019年8月;80:328-343;li等人,j.neuroinflammation.2020年2月25日;17(1):73;david等人,neurobiol dis.2013年6月;54:194-205;pallottie等人,sci rep.2018年6月7日;8(1):8723);以及多发性硬化症(prinz等人,j clin invest.2006feb;116(2):456-64)。其中已牵涉tlr9的外周病症是范围广泛的,并且包括多种形式的组织损伤(mcalpine等人,proc natl acad sci u s a.2018年12月4日;115(49):e11523-e11531)、慢性疼痛(david等人,neurobiol dis.2013年6月;54:194-205)以及牛皮癣(balak等人,clin immunol.2017年1月;174:63-72)。
10.本文描述了具有高效能和选择性的充当tlr2的拮抗剂和/或tlr9的抑制剂的化合物。
技术实现要素:
11.在一个方面,本文提供了一种式(a)化合物:
[0012][0013]
或互变异构体、或任何前述项的药学上可接受的盐,
[0014]
其中
[0015]
r1和r2中的一者是
–
oh,并且另一者选自由以下组成的组:-cn、卤素、-c(o)ra、-ch=nrj、-s(o)rb、-s(o)2rc、-nhc(o)rd、-nhs(o)2re、-c
1-c6烷基-rf、-c
2-c6烯基-rg、未被取代或被取代的c
3-c8环烷基、未被取代或被取代的c
3-c8环烯基以及未被取代或被取代的杂环烷基;
[0016]
ra、rb、rc和re各自独立地是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
1-c6卤代烷基、未被取代或被取代的杂环基、未被取代或被取代的杂芳基、苯甲酰基或苯乙烯基;
[0017]
rd是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
1-c6卤代烷基、未被取代或被取代的杂环基、未被取代或被取代的杂芳基或苯甲酰基;
[0018]
rf和rg各自独立地是
–
oh、未被取代的杂芳基、
–
nr
mrn
、苯甲酰基或苯乙烯基;
[0019]rm
和rn各自独立地是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基或未被取代或被取代的环烷基;
[0020]rj
是未被取代或被取代的杂环基、未被取代或被取代的杂芳基、未被取代或被取代的芳基、-ork、-nhrk、-nhc(o)rk、-nhs(o)2rk或-nhc(nh)nhr
aa
;
[0021]raa
是未被取代或被取代的c
1-c6烷基、未被取代或被取代的c
3-c8环烷基、未被取代或被取代的芳基、未被取代或被取代的杂环烷基或未被取代或被取代的杂芳基;
[0022]rk
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基、或芳基,其中rk的所述c
1-c6烷基未被取代或被杂环基或杂芳基取代;
[0023]
r3是h、c
1-c6烷基、c
1-c6烷氧基或卤素,其中r3的所述c
1-c6烷基烷基和c
1-c6烷氧基各自独立地未被取代或被一个或多个卤素取代;
[0024]
其中当r2是br时,r3是h、c
1-c6烷基、c
1-c6烷氧基、cl、f或i;
[0025]
g1和g2各自独立地是ch或n,其中当g1是n时,g2是ch,并且当g2是n时,g1是ch;
[0026]
指示环是芳族的;
[0027]
y1是c或n;
[0028]
y2是ch、n、nh、s或o;
[0029]
y3是c或n;
[0030]
y4是ch、n、nh、s或o;
[0031]
y5是cr7、n、nh、s或o;
[0032]
其中y1、y2、y3、y4和y5中的至多一者是s或o,并且y1、y2、y3、y4和y5中的至多四者是n或nh;
[0033]
r7是h或c
1-c6烷基;
[0034]
n是0、1、2或3;
[0035]
r4是烷氧基或
[0036]
指示环是饱和的,部分不饱和的,或完全不饱和的;
[0037]
g3是ch(x
1-r
6a
)、c(x
1-r
6a
)、n、n(x
1-r
6a
)、s或o;
[0038]
g4是ch(x
2-r
6b
)、c(x
2-r
6b
)、n、n(x
2-r
6b
)、s或o;
[0039]
g5是ch(x
3-r
6c
)、c(x
3-r
6c
)、n、n(x
3-r
6c
)、s或o;
[0040]
g6是ch(x
4-r
6d
)、c(x
4-r
6d
)、n、n(x
4-r
6d
)、s或o;并且
[0041]
g7是n、c或ch;
[0042]
x1、x2、x3和x4各自独立地是不存在的,是地是不存在的,是
[0043]
m是1-6;
[0044]r6a
、r
6b
、r
6c
和r
6d
各自独立地是氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基、-c
1-c6烷基-杂环基、-oc(o)-杂环基、-c(o)rh、-s(o)2nr
w1rw2
、-s(o)2ry或-nr
z1
s(o)2r
z2
,其中r
6a
、r
6b
、r
6c
和r
6d
的所述c
1-c6烷基和c
1-c6烷氧基各自独立地未被取代或被一个或多个选自由环烷基和卤素组成的组的基团取代;r
6a
、r
6b
、r
6c
和r
6d
的所述芳基和杂芳基各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、c
3-c8环烷基、-oh和c
1-c6烷基-oh组成的组的基团取代;并且r
6a
、r
6b
、r
6c
和r
6d
的所述杂环基、-c
1-c6烷基-杂环基和-oc(o)-杂环基各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、c
1-c6烷基-oh、=o和=s组成的组的基团取代;
[0045]
每个rh独立地选自由h、c
1-c6烷基、c
1-c6烷氧基和c
3-c8环烷基以及-nrrrs组成的组;
[0046]
每个r
p
独立地是h或c
1-c6烷基;
[0047]
每个rq独立地是c
2-c3烷基、-c(o)r
t
、-c(o)oru、-c(o)nrv;
[0048]
每个rr、rs、r
w1
和r
z1
独立地选自h和c
1-c6烷基;并且
[0049]
每个r
t
、ru、rv、r
w2
、ry和r
z2
独立地选自h、c
1-c6烷基、未被取代或被取代的c
3-c8环烷基以及未被取代或被取代的杂环基;
[0050]
或
[0051]
g5是ch(x
3-r
6c
)或c(x
3-r
6c
),g6是ch(x
4-r
6d
)或c(x
4-r
6d
),并且r
6c
和r
6d
连同它们所连接的碳原子一起形成6元芳基、6元杂环基或6元杂芳基环;其中所述6元芳基、6元杂环基和6元杂芳基环各自独立地未被取代或被取代。
[0052]
在式(a)的一些实施方案中,
[0053]
y1是c或n;
[0054]
y2是ch、n、nh、s或o;
[0055]
y3是c或n;
[0056]
y4是ch、n、nh、s或o;
[0057]
y5是ch、n、nh、s或o;
[0058]
其中y1、y2、y3、y4和y5中的至多一者是s或o,并且y1、y2、y3、y4和y5中的至多三者是n或nh。
[0059]
在式(a)的一些实施方案中,r1和r2中的一者是
–
oh,并且另一者选自由以下组成的组:-cn、卤素、-c(o)ra、-ch=nrj、-s(o)rb、-s(o)2rc、-nhc(o)rd、-nhs(o)2re、-c
1-c6烷基-rf、-c
2-c6烯基-rg、未被取代或被取代的c
3-c8环烷基、未被取代或被取代的c
3-c8环烯基以及未被取代或被取代的杂环烷基;ra、rb、rc和re各自独立地是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
1-c6卤代烷基、未被取代或被取代的杂环基、未被取代或被取代的杂芳基、苯甲酰基或
苯乙烯基;rd是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
1-c6卤代烷基、未被取代或被取代的杂环基、未被取代或被取代的杂芳基或苯甲酰基;rf和rg各自独立地是
–
oh、未被取代的杂芳基、
–
nr
mrn
、苯甲酰基或苯乙烯基;rm和rn各自独立地是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基或未被取代或被取代的环烷基;rj是未被取代或被取代的杂环基、未被取代或被取代的杂芳基、未被取代或被取代的芳基、-ork、-nhrk、-nhc(o)rk、-nhs(o)2rk或-nhc(nh)nh2;rk是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基、或芳基,其中rk的所述c
1-c6烷基未被取代或被杂环基或杂芳基取代。
[0060]
在一个方面,本文提供了一种式(b)化合物:
[0061][0062]
或互变异构体、或任何前述项的药学上可接受的盐,
[0063]
其中
[0064]
l选自由以下组成的组:-c≡c-、*-nhc(o)-、*-c(o)nh-、-nhc(o)nh-、*-nhs(o)
2-、*-nhs(o)(=nh)-、*-s(o)(=nh)nh-、*-s(o)2nh-、*-s(o)nhnh-、*-nhnhs(o)-、*-c(o)nhnh-、*-nhnhc(o)-、*
–
nhc(o)o-和*
–
oc(o)nh-,其中*代表与y7的连接点;
[0065]
y1和y2各自独立地是cr
x
或n;
[0066]rx
是氢或卤素;
[0067]
当l是-c≡c-时,r
1a
和r
2a
中的一者是
–
oh,并且另一者选自由以下组成的组:-c(o)r
a1
、-ch=nr
j1
、-s(o)r
b1
、-s(o)2r
c1
、-nhc(o)r
d1
、-nhs(o)2r
e1
、-c
1-c6烷基-r
f1
、-c
2-c6烯基-r
g1
、c
3-c8环烷基、c
3-c8环烯基以及5或6元杂环烷基,其中所述c
3-c8环烷基和c
3-c8环烯基各自独立地未被取代或被一个或多个=o取代,并且所述5或6元杂环烷基未被取代或被一个或多个独立地选自由c
1-c6烷基、c
3-c8环烷基、=o和
–
c(o)o-c
1-c6烷基组成的组的取代基取代;
[0068]
当l是*-nhc(o)-、*-c(o)nh-、-nhc(o)nh-、*-nhs(o)
2-、*-s(o)2nh-、*-s(o)nhnh-、*-c(o)nhnh-或*
–
nhc(o)o-时,r
1a
和r
2a
中的一者是
–
oh,并且另一者选自由-c(o)h、-ch=nr
j1
和组成的组;
[0069]ra1
是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
1-c6卤代烷基、3至6元杂环基或5至10元杂芳基或苯甲酰基,其中r
a1
的所述3至10元杂环基未被取代或被一个或多个独立地选自由c
1-c6烷基、c
3-c8环烷基、=o和
–
c(o)o-c
1-c6烷基组成的组的基团取代,并且r
a1
的所述5至10
oh组成的组的基团取代;并且r
6a1
、r
6b1
、r
6c1
和r
6d1
的所述3至10元杂环基、-c
1-c6烷基-5至6元杂环基和-oc(o)-5至6元杂环基各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、-oh、c
1-c6烷基-oh、=o、=s、卤基、c
3-c8环烷基、-c(o)nh-c
3-c8环烷基、c
6-c
12
芳基和5至6元杂环基组成的组的基团取代;
[0088]
每个r
h1
独立地选自由h、c
1-c6烷基、c
1-c6烷氧基、c
3-c8环烷基和-nr
r1rs1
组成的组;
[0089]
每个r
p1
独立地是h或c
1-c6烷基;
[0090]
每个r
q1
独立地是c
2-c3烷基、-c(o)r
t1
、-c(o)or
u1
或-c(o)nr
v1
;
[0091]
每个r
r1
、r
s1
、r
w1a
和r
z1a
独立地选自h和c
1-c6烷基;并且
[0092]
每个r
t1
、r
u1
、r
v1
、r
w2a
、r
y1
和r
z2a
独立地选自h、c
1-c6烷基、未被取代或被取代的c
3-c8环烷基以及未被取代或被取代的杂环基;
[0093]
或
[0094]
y5是ch(x
3a-r
6c1
)或c(x
3a-r
6c1
),y6是ch(x
4a-r
6d1
)或c(x
4a-r
6d1
),并且r
6c1
和r
6d1
连同它们所连接的碳原子一起形成6元芳基、6元杂环基或6元杂芳基环;其中所述6元芳基、6元杂环基和6元杂芳基环各自独立地未被取代或被一个或多个选自由c
1-c6烷基和
–
c(o)o-c
1-c6烷基组成的组的基团取代;
[0095]
其中r
6a1
、r
6b1
、r
6c1
和r
6d1
中的至多一者是c
1-c6烷氧基或
–
oh;并且
[0096]
(1)当l是-c≡c-时,y1和y2各自是ch,r
1a
和r
2a
中的一者是-c(o)h、-ch2oh、-c(o)ch3或-nhc(o)ch3,并且r
3a
是h,不同于环己基、苯基、吡啶基或萘基,并且r
6c1
是氢、c
2-c3烷基、c
2-c5烷氧基、br、cl、i、-nr
p1rq1
、c
6-c
12
芳基、3至10元杂环基、5至10元杂芳基、-c
1-c6烷基-5至6元杂环基、-oc(o)-5至6元杂环基、-c(o)r
h1
、-s(o)2nr
w1arw2a
、-s(o)2r
y1
或-nr
z1a
s(o)2r
z2a
,并且每个r
h1
独立地选自由c
1-c6烷基、c
1-c6烷氧基、c
3-c8环烷基和-nr
r1rs1
组成的组;
[0097]
(2)当l是-c≡c-时,y1和y2各自是ch,r
1a
和r
2a
中的一者是-c(o)h,并且r
3a
是
–
ch3、t-bu或c
2-c3烷氧基,不同于苯基和吡啶基,r
b1
和r
d1
不同于并且r
6c1
不同于
–
oh;
[0098]
(3)当l是-c≡c-时,y1和y2各自是ch,r
1a
和r
2a
中的一者是哌啶基、吡咯烷基、吡咯烷酮、哌嗪基、吗啉基或噻二唑烷酮1,1-二氧化物,并且r
3a
是h,不同于萘基,并且r
6c1
不同于氟基;
[0099]
(4)当l是*-nhs(o)
2-或*-s(o)2nh-时,y1和y2各自是ch,r
1a
和r
2a
中的一者是-c(o)
h、-ch=nr
j1
或并且r
3a
是h或br,不同于苯基,并且r
6a1
、r
6b1
、r
6c1
和r
6d1
各自独立地是氢、c
2-c6烷基、c
1-c6烷氧基、-oh、-nr
p1rq1
、c
6-c
12
芳基、3至10元杂环基、5至10元杂芳基、-c
1-c6烷基-5至6元杂环基、-oc(o)-5至6元杂环基、-c(o)r
h1
、-s(o)2nr
w1arw2a
、-s(o)2r
y1
或-nr
z1a
s(o)2r
z2a
;
[0100]
(5)当l是*-c(o)nh-或*-nhc(o)-时,y1和y2各自是ch,r
1a
和r
2a
中的一者是-c(o)h,并且r
3a
是h或cl,不同于苯基,并且r
6a1
不同于
–
cf3;并且
[0101]
(6)当l是-nhc(o)nh-时,y1和y2各自是ch,r
1a
和r
2a
中的一者是-c(o)h或并且r
3a
是h或cl,不同于环己基,并且r
6c1
不同于氯基。
[0102]
在式(b)的一些实施方案中,r
j1
是c
1-c6烷基、5至6元杂环基、5至6元杂芳基、6至12元芳基、-or
k1
、-nhr
k1
、-n(c
1-c6烷基)r
k1
、-nhc(o)r
k1
、-nhs(o)2r
k1
或-nhc(nh)nh2,其中r
j1
的所述5至6元杂环基未被取代或被一个或多个选自由c
1-c6烷基、c
3-c8环烷基、=o、
–
c(o)nh-c
1-c6烷基和
–
c(o)o-c
1-c6烷基组成的组的取代基取代,并且r
j1
的所述5至6元杂芳基和6至12元芳基各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基组成的组的取代基取代;并且r
6a1
、r
6b1
、r
6c1
和r
6d1
各自独立地是氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
p1rq1
、c
6-c
12
芳基、3至10元杂环基、5至10元杂芳基、-c
1-c6烷基-5至6元杂环基、-oc(o)-5至6元杂环基、-c(o)r
h1
、-s(o)2nr
w1arw2a
、-s(o)2r
y1
或-nr
z1a
s(o)2r
z2a
,其中r
6a1
、r
6b1
、r
6c1
和r
6d1
的所述c
1-c6烷基和c
1-c6烷氧基各自独立地未被取代或被一个或多个选自由c
3-c8环烷基和卤素组成的组的基团取代;r
6a1
、r
6b1
、r
6c1
和r
6d1
的所述c
6-c
12
芳基和5至10元杂芳基各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、-oh和c
1-c6烷基-oh组成的组的基团取代;并且r
6a1
、r
6b1
、r
6c1
和r
6d1
的所述3至10元杂环基、-c
1-c6烷基-5至6元杂环基和-oc(o)-5至6元杂环基各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、-oh、c
1-c6烷基-oh、=o和=s组成的组的基团取代。
[0103]
在另一方面,本文提供了包含至少一种式(a)或式(b)化合物诸如表1a或表1b的化合物、或其互变异构体、或任何前述项的药学上可接受的盐,任选地还包含药学上可接受的赋形剂的药物组合物。
[0104]
在另一方面,本文提供了一种治疗与tlr2异二聚化相关的疾病或疾患的方法,所述方法包括向需要此治疗的受试者施用有效量的至少一种式(a)或式(b)化合物诸如表1a
或表1b的化合物、或其互变异构体、或任何前述项的药学上可接受的盐,和/或包含至少一种式(a)或式(b)化合物诸如表1a或表1b的化合物的药物组合物。在本文所述的任何方法的一些实施方案中,疾病或疾患选自由以下组成的组:阿尔茨海默氏病、帕金森氏病、额颞性痴呆、路易体痴呆(路易体病)、伴有痴呆的帕金森氏病、多系统萎缩、肌萎缩性侧索硬化、亨廷顿氏病、进行性核上麻痹(psp)、c型尼曼-皮克病(niemann-pick disease type c)、炎症性疾病、哮喘、慢性阻塞性肺病(copd)、慢性消化性溃疡、肠易激疾病、结核病、类风湿性关节炎、骨关节炎、慢性鼻窦炎、肝炎、乙型肝炎、丙型肝炎、痛风、狼疮、胸膜炎、湿疹、胃炎、牛皮癣、牛皮癣性关节炎、血管炎、喉炎、过敏反应、多发性硬化症、克罗恩氏病、创伤性脑损伤、cidp(慢性炎症性脱髓鞘性多发性神经病变)、中风、缺血性心脏病、特应性皮炎、寻常痤疮、红斑痤疮、非酒精性脂肪肝病、非酒精性脂肪性肝炎、角膜创伤、角膜病症、角膜hsv、施塔加特病(stargardt disease)(青少年黄斑变性)、年龄相关的黄斑变性、败血症、糖尿病创伤、单纯疱疹病毒、以及抗真菌、抗细菌、抗病毒和抗肿瘤疾病或疾患。
[0105]
在另一方面,本文提供了一种干扰细胞中tlr2的异二聚化,或调节、阻止、减缓、逆转或抑制细胞中的tlr2异二聚化的方法,所述方法包括使所述细胞与有效量的至少一种式(a)或式(b)化合物诸如表1a或表1b的化合物、或其互变异构体、或任何前述项的药学上可接受的盐,以及/或者与至少一种包含至少一种式(a)或式(b)化合物诸如表1a或表1b的化合物的药物组合物接触,其中所述接触是体外的,离体的,或体内的。
[0106]
在另一方面,本文提供了一种治疗与tlr9的抑制相关的疾病或疾患的方法,所述方法包括向需要此治疗的受试者施用有效量的至少一种式(a)或式(b)化合物诸如表1a或表1b的化合物、或其互变异构体、或任何前述项的药学上可接受的盐,和/或包含至少一种式(a)或式(b)化合物诸如表1a或表1b的化合物的药物组合物。在本文所述的任何方法的一些实施方案中,疾病或疾患是中枢神经系统(cns)或外周病症。在一些实施方案中,cns病症是帕金森氏病、肌萎缩性侧索硬化、格林-巴利综合征、脊髓损伤或多发性硬化症。在一些实施方案中,外周病症包括多种形式的组织损伤、慢性疼痛和牛皮癣。
[0107]
本公开的额外实施方案、特征和优势将根据以下具体实施方式以及通过本公开的实施而显而易知。
[0108]
为了简洁起见,本说明书中引用的包括专利的出版物的公开内容通过引用并入本文。
具体实施方式
[0109]
本公开涉及化合物、包含此类化合物的药物组合物、以及此类化合物在治疗炎症性疾病和与包括但不限于蛋白质错误折叠的炎症性信号传导过程相关的某些神经病症的方法中或在用于治疗所述炎症性疾病和某些神经病症的药剂中的用途。
[0110]
应了解本公开不限于所述特定实施方案,因此,当然可变化。还应了解本文所用的术语仅出于描述特定实施方案的目的,并且不意图具有限制性。
[0111]
除非另外定义,否则本文所用的所有技术和科学术语都具有与由本公开所属领域中的普通技术人员通常理解相同的含义。本文提及的所有专利、申请、公布申请以及其他出版物都通过引用以它们的整体并入本文。如果这个章节中阐述的定义与通过引用并入本文的专利、申请或其他出版物中阐述的定义相反,或以其他方式与所述定义不一致,那么这个
章节中阐述的定义优先于通过引用并入本文的定义。
[0112]
除非上下文另外明确规定,否则如本文中以及随附权利要求中所用,单数形式“一个(种)(a/an)”和“这个(种)(the)”包括复数个(种)指示物。还应注意权利要求可被起草来排除任何任选要素。因此,这个陈述意图充当与叙述权利要求要素关联使用诸如“只有”、“仅有”等的排他性术语或使用“否定性”限制的前提基础。
[0113]
如本文所用,术语“包括”、“含有”和“包含”以它们的开放非限制性意义加以使用。
[0114]
为提供更简明描述,本文给出的一些定量表述未用术语“约”来限定。应了解,无论是否明确使用术语“约”,本文给出的每个数量都意图指代实际给定值,并且它还意图指代此给定值的将基于本领域中的普通技术而得以合理推断的近似值,包括此给定值的归因于实验和/或测量条件的等效值和近似值。每当产率以百分比形式给出时,此产率是指给出所述产率所针对的实体的质量相对于相同实体的可在特定化学计量条件下获得的最大量。除非以不同方式指示,否则以百分比形式给出的浓度是指质量比。
[0115]
除非另外定义,否则本文所用的所有技术和科学术语都具有与由本公开所属领域中的普通技术人员通常理解相同的含义。尽管在实施或测试本公开时也可使用与本文所述的那些方法和材料类似或等效的任何方法和材料。本文提及的所有出版物都通过引用并入本文以对引用所述出版物所关联的方法和/或材料进行公开和描述。
[0116]
除非另外指示,否则通常根据本领域中熟知以及如在整篇本说明书中引用和讨论的各种一般性和更特定参考文献中所述的常规方法来进行本发明实施方案的方法和技术。参见例如loudon,organic chemistry,第四版,new york:oxford university press,2002,第360-361、1084-1085页;smith和march,march's advanced organic chemistry:reactions,mechanisms,and structure,第五版,wiley-interscience,2001。
[0117]
在本文中用于命名主题化合物的命名法说明于本文实施例中。这个命名法已通常使用可商购获得的14.0版chembiodraw ultra软件来获得。
[0118]
应了解,为明晰起见在单独实施方案的情形下描述的本公开的某些特征还可在单一实施方案中组合地提供。相反,为简洁起见在单一实施方案的情形下描述的本公开的各种特征还可单独或以任何适合子组合提供。关于由变量表示的化学基团的实施方案的所有组合都由本公开具体地包括,并且在本文中公开,就好像单独地和明确地公开每一个组合一样,只要是此类组合包括作为稳定化合物的化合物(即可被分离、表征以及测试生物活性的化合物)即可。此外,描述此类变量的实施方案中所列的化学基团的所有子组合也由本公开具体地包括,并且在本文中公开,就好像单独地和明确地在本文中公开化学基团的每一个此子组合一样。
[0119]
化合物
[0120]
在本文中,包括在发明内容中以及在随附权利要求中详述了化合物及其盐(诸如药学上可接受的盐)。还提供了本文所述的所有化合物的用途,所述所有化合物包括本文所述的化合物的任何和所有立体异构体,包括几何异构体(例如顺/反异构体或e/z异构体)、对映异构体、非对映异构体、以及它们的处于任何比率的混合物,包括外消旋混合物;盐和溶剂化物,以及制备此类化合物的方法。本文所述的任何化合物都还可被称为药物。
[0121]
在一个方面,提供了式(a)化合物:
[0122][0123]
或互变异构体、或任何前述项的药学上可接受的盐,
[0124]
其中
[0125]
r1和r2中的一者是
–
oh,并且另一者选自由以下组成的组:-cn、卤素、-c(o)ra、-ch=nrj、-s(o)rb、-s(o)2rc、-nhc(o)rd、-nhs(o)2re、-c
1-c6烷基-rf、-c
2-c6烯基-rg、未被取代或被取代的c
3-c8环烷基、未被取代或被取代的c
3-c8环烯基以及未被取代或被取代的杂环烷基;
[0126]
ra、rb、rc和re各自独立地是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
1-c6卤代烷基、未被取代或被取代的杂环基、未被取代或被取代的杂芳基、苯甲酰基或苯乙烯基;
[0127]
rd是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
1-c6卤代烷基、未被取代或被取代的杂环基、未被取代或被取代的杂芳基或苯甲酰基;
[0128]
rf和rg各自独立地是
–
oh、未被取代的杂芳基、
–
nr
mrn
、苯甲酰基或苯乙烯基;
[0129]rm
和rn各自独立地是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基或未被取代或被取代的环烷基;
[0130]rj
是未被取代或被取代的杂环基、未被取代或被取代的杂芳基、未被取代或被取代的芳基、-ork、-nhrk、-nhc(o)rk、-nhs(o)2rk或-nhc(nh)nhr
aa
;
[0131]raa
是未被取代或被取代的c
1-c6烷基、未被取代或被取代的c
3-c8环烷基、未被取代或被取代的芳基、未被取代或被取代的杂环烷基或未被取代或被取代的杂芳基;
[0132]rk
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基、或芳基,其中rk的所述c
1-c6烷基未被取代或被杂环基或杂芳基取代;
[0133]
r3是h、c
1-c6烷基、c
1-c6烷氧基或卤素,其中r3的所述c
1-c6烷基烷基和c
1-c6烷氧基各自独立地未被取代或被一个或多个卤素取代;
[0134]
其中当r2是br时,r3是h、c
1-c6烷基、c
1-c6烷氧基、cl、f或i;
[0135]
g1和g2各自独立地是ch或n,其中当g1是n时,g2是ch,并且当g2是n时,g1是ch;
[0136]
指示环是芳族的;
[0137]
y1是c或n;
[0138]
y2是ch、n、nh、s或o;
[0139]
y3是c或n;
[0140]
y4是ch、n、nh、s或o;
[0141]
y5是cr7、n、nh、s或o;
[0142]
其中y1、y2、y3、y4和y5中的至多一者是s或o,并且y1、y2、y3、y4和y5中的至多四者是n或nh;
[0143]
r7是h或c
1-c6烷基;
[0144]
n是0、1、2或3;
[0145]
r4是烷氧基或
[0146]
指示环是饱和的,部分不饱和的,或完全不饱和的;
[0147]
g3是ch(x
1-r
6a
)、c(x
1-r
6a
)、n、n(x
1-r
6a
)、s或o;
[0148]
g4是ch(x
2-r
6b
)、c(x
2-r
6b
)、n、n(x
2-r
6b
)、s或o;
[0149]
g5是ch(x
3-r
6c
)、c(x
3-r
6c
)、n、n(x
3-r
6c
)、s或o;
[0150]
g6是ch(x
4-r
6d
)、c(x
4-r
6d
)、n、n(x
4-r
6d
)、s或o;并且
[0151]
g7是n、c或ch;
[0152]
x1、x2、x3和x4各自独立地是不存在的,是各自独立地是不存在的,是
[0153]
m是1-6;
[0154]r6a
、r
6b
、r
6c
和r
6d
各自独立地是氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基、-c
1-c6烷基-杂环基、-oc(o)-杂环基、-c(o)rh、-s(o)2nr
w1rw2
、-s(o)2ry或-nr
z1
s(o)2r
z2
,其中r
6a
、r
6b
、r
6c
和r
6d
的所述c
1-c6烷基和c
1-c6烷氧基各自独立地未被取代或被一个或多个选自由环烷基和卤素组成的组的基团取代;r
6a
、r
6b
、r
6c
和r
6d
的所述芳基和杂芳基各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、c
3-c8环烷基、-oh和c
1-c6烷基-oh组成的组的基团取代;并且r
6a
、r
6b
、r
6c
和r
6d
的所述杂环基、-c
1-c6烷基-杂环基和-oc(o)-杂环基各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、c
1-c6烷基-oh、=o和=s组成的组的基团取代;
[0155]
每个rh独立地选自由h、c
1-c6烷基、c
1-c6烷氧基和c
3-c8环烷基以及-nrrrs组成的组;
[0156]
每个r
p
独立地是h或c
1-c6烷基;
[0157]
每个rq独立地是c
2-c3烷基、-c(o)r
t
、-c(o)oru、-c(o)nrv;
[0158]
每个rr、rs、r
w1
和r
z1
独立地选自h和c
1-c6烷基;并且
[0159]
每个r
t
、ru、rv、r
w2
、ry和r
z2
独立地选自h、c
1-c6烷基、未被取代或被取代的c
3-c8环烷基以及未被取代或被取代的杂环基;
[0160]
或
[0161]
g5是ch(x
3-r
6c
)或c(x
3-r
6c
),g6是ch(x
4-r
6d
)或c(x
4-r
6d
),并且r
6c
和r
6d
连同它们所连接的碳原子一起形成6元芳基、6元杂环基或6元杂芳基环;其中所述6元芳基、6元杂环基和6元杂芳基环各自独立地未被取代或被取代。
[0162]
在式(a)的一些实施方案中,
[0163]
y1是c或n;
[0164]
y2是ch、n、nh、s或o;
[0165]
y3是c或n;
[0166]
y4是ch、n、nh、s或o;
[0167]
y5是ch、n、nh、s或o;
[0168]
其中y1、y2、y3、y4和y5中的至多一者是s或o,并且y1、y2、y3、y4和y5中的至多三者是n或nh;并且
[0169]
r1和r2中的一者是
–
oh,并且另一者选自由以下组成的组:-cn、卤素、-c(o)ra、-ch=nrj、-s(o)rb、-s(o)2rc、-nhc(o)rd、-nhs(o)2re、-c
1-c6烷基-rf、-c
2-c6烯基-rg、未被取代或被取代的c
3-c8环烷基、未被取代或被取代的c
3-c8环烯基以及未被取代或被取代的杂环烷基;ra、rb、rc和re各自独立地是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
1-c6卤代烷基、未被取代或被取代的杂环基、未被取代或被取代的杂芳基、苯甲酰基或苯乙烯基;rd是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
1-c6卤代烷基、未被取代或被取代的杂环基、未被取代或被取代的杂芳基或苯甲酰基;rf和rg各自独立地是
–
oh、未被取代的杂芳基、
–
nr
mrn
、苯甲酰基或苯乙烯基;rm和rn各自独立地是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基或未被取代或被取代的环烷基;rj是未被取代或被取代的杂环基、未被取代或被取代的杂芳基、未被取代或被取代的芳基、-ork、-nhrk、-nhc(o)rk、-nhs(o)2rk或-nhc(nh)nh2;rk是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基、或芳基,其中rk的所述c
1-c6烷基未被取代或被杂环基或杂芳基取代。
[0170]
在一些实施方案中,当任何特定基团被取代时,所指示基团被一个或多个选自由以下组成的组的取代基取代:氧代基、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、卤素、-cn、-or
a1
、-sr
a1
、-nr
a2ra3
、-no2、-c=nh(or
a1
)、-c(o)r
a1
、-oc(o)r
a1
、-c(o)or
a1
、-c(o)nr
a2ra3
、-oc(o)nr
a2ra3
、-nr
a1
c(o)r
a2
、-nr
a1
c(o)or
a2
、-nr
a1
c(o)nr
a2ra3
、-s(o)r
a1
、-s(o)2r
a1
、-nr
a1
s(o)r
a2
、-c(o)nr
a1
s(o)r
a2
、-nr
a1
s(o)2r
a2
、-c(o)nr
a1
s(o)2r
a2
、-s(o)nr
a2ra3
、-s(o)2nr
a2ra3
、-p(o)(or
a2
)(or
a3
)、c
3-c8环烷基、3-12元杂环基、5至10元杂芳基、c
6-c
14
芳基、-(c
1-c3亚烷基)cn、-(c
1-c3亚烷基)or
a1
、-(c
1-c3亚烷基)sr
a1
、-(c
1-c3亚烷基)nr
a2ra3
、-(c
1-c3亚烷基)cf3、-(c
1-c3亚烷基)no2、-c=nh(or
a1
)、-(c
1-c3亚烷基)c(o)r
a1
、-(c
1-c3亚烷基)oc(o)r
a1
、-(c
1-c3亚烷基)c(o)or
a1
、-(c
1-c3亚烷基)c(o)nr
a2ra3
、-(c
1-c3亚烷基)oc(o)nr
a2ra3
、-(c
1-c3亚烷基)nr
a1
c(o)r
a2
、-(c
1-c3亚烷基)nr
a1
c(o)or
a2
、-(c
1-c3亚烷基)nr
a1
c(o)nr
a2ra3
、-(c
1-c3亚烷基)s(o)r
a1
、-(c
1-c3亚烷基)s(o)2r
a1
、-(c
1-c3亚烷基)nr
a1
s(o)r
a2
、-c(o)(c
1-c3亚烷基)nr
a1
s(o)r
a2
、-(c
1-c3亚烷基)nr
a1
s(o)2r
a2
、-(c
1-c3亚烷基)c(o)nr
a1
s(o)2r
a2
、-(c
1-c3亚烷基)s(o)nr
a2ra3
、-(c
1-c3亚烷基)s(o)2nr
a2ra3
、-(c
1-c3亚烷基)p(o)(or
a2
)(or
a3
)、-(c
1-c3亚烷基)(c
3-c8环烷基)、-(c
1-c3亚烷基)(3-12元杂环基)、-(c
1-c3亚烷基)(5-10元杂芳基)和-(c
1-c3亚烷基)(c
6-c
14
芳基),其中所述一个或多个取代基各自独立地未被取代或被一个或多个选自由以下组成的组的其他取代基取代:卤素、氧代基、-or
a4
、-nr
a4ra5
、-c(o)r
a4
、-cn、-s(o)r
a4
、-s(o)2r
a4
、-p(o)(or
a4
)(or
a5
)、-(c
1-c3亚烷基)or
a4
、-(c
1-c3亚烷基)nr
a4ra5
、-(c
1-c3亚烷基)c(o)r
a4
、-(c
1-c3亚烷基)s(o)r
a4
、-(c
1-c3亚烷基)s(o)2r
a4
、-(c
1-c3亚烷基)p(o)(or
a4
)(or
a5
)、c
3-c8环烷基、c
1-c6烷基以及被氧代基、-oh或卤素取代的c
1-c6烷基;其中每个r
a1
独立地是氢、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基、c
6-c
14
芳基、5-6元杂芳基或3-6元杂环基,其中所述c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基、c
6-c
14
芳基、5-6元杂芳基和3-6元杂环基独立地未被取代或被卤素、氧代基、-cn、-or
a6
、-nr
a6ra7
、-p(o)(or
a6
)(or
a6
)、苯基、被卤素取代
oh组成的组的基团取代;并且r
6a
、r
6b
、r
6c
和r
6d
的所述3至10元杂环基、-c
1-c6烷基-5至6元杂环基和-oc(o)-5至6元杂环基各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、c
1-c6烷基-oh、=o和=s组成的组的基团取代;
[0179]
rh选自由h、c
1-c6烷基、c
1-c6烷氧基、c
3-c8环烷基和-nrrrs组成的组;
[0180]rp
是h或c
1-c6烷基;
[0181]rq
是c
2-c3烷基、-c(o)r
t
、-c(o)oru、-c(o)nrv;
[0182]rr
、rs、r
w1
和r
z1
各自独立地选自h和c
1-c6烷基;并且
[0183]rt
、ru、rv、r
w2
、ry和r
z2
各自独立地选自h、c
1-c6烷基、未被取代或被取代的c
3-c8环烷基以及未被取代或被取代的杂环基;
[0184]
或
[0185]
g5是ch(x
3-r
6c
)或c(x
3-r
6c
),g6是ch(x
4-r
6d
)或c(x
4-r
6d
),并且r
6c
和r
6d
连同它们所连接的碳原子一起形成6元芳基、6元杂环基或6元杂芳基环;其中所述6元芳基、6元杂环基和6元杂芳基环各自独立地未被取代或被一个或多个选自由c
1-c6烷基和
–
c(o)o-c
1-c6烷基组成的组的基团取代;并且
[0186]
其中r
6a
、r
6b
、r
6c
和r
6d
中的至多一者是c
1-c6烷氧基或
–
oh。
[0187]
在一些实施方案中,式(a)化合物是式(a-1a)或(a-1b)化合物:
[0188][0189]
其中r1、r2、r3、g1、g2、g3、g4、g5、g6、g7、y1、y2、y3、y4、y5和n如对于式(a)所定义。
[0190]
在一些实施方案中,式(a)化合物是式(a-2a)或(a-2b)化合物:
[0191][0192]
其中r1、r2、r3、g1、g2、g3、g4、g5、g6、g7、y1、y2、y3、y4和y5如对于式(a)所定义。
[0193]
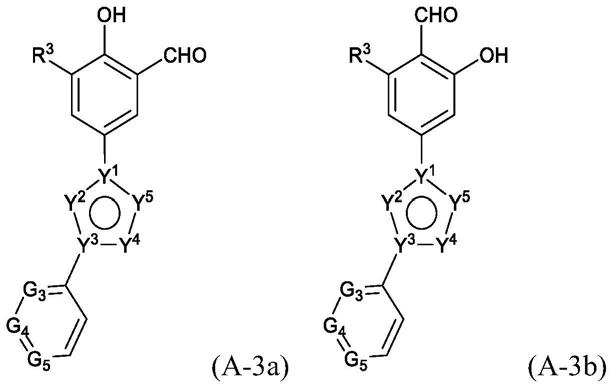
在一些实施方案中,式(a)化合物是式(a-3a)或(a-3b)化合物,
[0194][0195]
其中r3、g3、g4、g5、y1、y2、y3、y4和y5如对于式(a)所定义。
[0196]
在一些实施方案中,式(a)化合物是式(a-4a)、(a-4b)、(a-4c)、(a-4d)、(a-4e)、(a-4f)、(a-4g)、(a-4h)或(a-4i)化合物:
[0197]
[0198][0199]
其中r1、r2、r3、r
6b
和r
6c
如对于式(a)所定义。
[0200]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)、(a-2b)、(a-3a)和(a-3b)的一些实施方案中,y1是c。在其他实施方案中,y1是n。在一些实施方案中,y2是ch。在一些实施方案中,y2是n。在一些实施方案中,y2是nh。在一些实施方案中,y2是s。在其他实施方案中,y2是o。在一些实施方案中,y3是c。在其他实施方案中,y3是n。在一些实施方案中,y4是ch。在一些实施方案中,y4是n。在一些实施方案中,y4是nh。在一些实施方案中,y4是s。在其他实施方案中,y4是o。在一些实施方案中,y5是cr7,其中r7是h或c
1-c6烷基。在一些实施方案中,y5是ch。在一些实施方案中,y5是cr7,其中r7是c
1-c6烷基。在一些实施方案中,y5是c(ch3)。在一些实施方案中,y5是n。在一些实施方案中,y5是nh。在一些实施方案中,y5是s。在其他实施方案中,y5是o。
[0201]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)、(a-2b)、(a-3a)和(a-3b)的一些实施方案中,y1、y2、y3、y4和y5中的一者是n,并且其余各者不同于n。在一些实施方案中,y1、y2、y3、y4和y5中的两者是n,并且其余各者不同于n。在其他实施方案中,y1、y2、y3、y4和y5中的三者是n,并且其余各者不同于n。在其他实施方案中,y1、y2、y3、y4和y5中的四者是n。在式(a)的一些实施方案中,y1、y2、y3、y4和y5中的一者是s,并且其余各者不同于s。在式(a)的一些实施方案中,y1、y2、y3、y4和y5中的一者是o,并且其余各者不同于o。在一些实施方案中,y1、y2、y3、y4和y5中的至多一者是s或o。在一些实施方案中,y1、y2、y3、y4和y5中的至多三者是n或nh。在一些
实施方案中,y1、y2、y3、y4和y5中的至多四者是n或nh。
[0202]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)、(a-2b)、(a-3a)和(a-3b)的一些实施方案中,选自由以下组成的组:选自由以下组成的组:
[0203]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)、(a-2b)、(a-3a)和(a-3b)的一些实施方案中,是在一些实施方案中,是在一些实施方案中,是在一些实施方案中,是在一些实施方案中,是在其他实施方案中,选自由以下组成
的组:在式(a)的一些实施方案中,选自由以下组成的组:选自由以下组成的组:在一些实施方案中,选自由以下组成的组:选自由以下组成的组:在一些实施方案中,选自由以下组成的组:在其他实施方案中,选自由以下组成的组:选自由以下组成的组:在一些实施方案中,是在一些实施方案中,是
[0204]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)、(a-2b)、(a-3a)和(a-3b)的一些实施方
案中,选自由以下组成的组:选自由以下组成的组:在一些实施方案中,r1是
–
oh,并且r2是
–
c(o)h。在其他实施方案中,r2是
–
oh,并且r1是
–
c(o)h。在一些实施方案中,r1是
–
oh,r2是
–
c(o)h,并且r3是卤基。在其他实施方案中,r2是
–
oh,r1是
–
c(o)h,并且r3是卤基。在一些实施方案中,r1是
–
oh,r2是
–
c(o)h,并且r3是氟基。在其他实施方案中,r2是
–
oh,r1是
–
c(o)h,并且r3是氟基。
[0205]
在式(a),包括式(a-1a)、(a-2a)、(a-3a)、(a-4a)、(a-4b)、(a-4c)、(a-4d)、(a-4e)、(a-4f)、(a-4g)、(a-4h)和(a-4i)的一些实施方案中,r1是
–
oh,并且r2选自由以下组成的组:-cn、卤素、-c(o)ra、-ch=nrj、-s(o)rb、-s(o)2rc、-nhc(o)rd、-nhs(o)2re、-c
1-c6烷基-rf、-c
2-c6烯基-rg、未被取代或被取代的c
3-c8环烷基、未被取代或被取代的c
3-c8环烯基以及未被取代或被取代的杂环烷基。在一些实施方案中,r1是
–
oh,并且r2选自由以下组成的组:-cn、卤素、-c(o)ra、-ch=nrj、-s(o)rb、-s(o)2rc、-nhc(o)rd、-nhs(o)2re、-c
1-c6烷基-rf、-c
2-c6烯基-rg、c
3-c8环烷基、c
3-c8环烯基以及杂环烷基,其中所述c
3-c8环烷基、c
3-c8环烯基以及杂环烷基任选地被一个或多个选自由以下组成的组的取代基取代:c
1-c6烷基、c
1-c6卤代烷基、卤基、-oh、-c(o)h、-c(o)oh、-c(o)oc
1-c6烷基、-oc
1-c6烷基和c
3-c8环烷基。在一些实施方案中,ra、rb、rc和re各自独立地是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
1-c6卤代烷基、未被取代或被取代的杂环基、未被取代或被取代的杂芳基、苯甲酰基或苯乙烯基。在一些实施方案中,ra、rb、rc和re各自独立地是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
1-c6卤代烷基、杂环基、杂芳基、苯甲酰基或苯乙烯基,其中所述杂环基和杂芳基任选地被一个或多个选自由以下组成的组的取代基取代:c
1-c6烷基、c
1-c6卤代烷基、卤基、-oh、-c(o)h、-c(o)oh、-c(o)oc
1-c6烷基、-oc
1-c6烷基和c
3-c8环烷基。在一些实施方案中,rd是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
1-c6卤代烷基、未被取代或被取代的杂环基、未被取代或被取代的杂芳基或苯甲酰基。在一些实施方案中,rd是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
1-c6卤代烷基、杂环基、杂芳基或苯甲酰基,其中所述杂环基和杂芳基任选地被一个或多个选自由以下组成的组的取代基取代:c
1-c6烷基、c
1-c6卤代烷基、卤基、-oh、-c(o)h、-c(o)oh、-c(o)oc
1-c6烷基、-oc
1-c6烷基和c
3-c8环烷基。在一些实施方案中,rf和rg各自独立地是
–
oh、未被取代的杂芳基、
–
nr
mrn
、苯甲酰基或苯乙烯基,其中rm和rn各自独立地是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基或c
3-c8环烷基,其中所述c
3-c8环烷基任选地被一个或多个选自由以下组成的组的取代基取代:c
1-c6烷基、c
1-c6卤代烷基、卤基、-oh、-c(o)h、-c(o)oh、-c(o)oc
1-c6烷基、-oc
1-c6烷基和c
3-c8环烷基。在一些实施方案中,rj是杂环基、芳基、-ork、-nhrk、-nhc(o)rk、-nhs(o)2rk或-nhc(nh)nh2,其中所述杂环基和芳基任选地被一个或多个选自由以下组成的组的取代基取代:c
1-c6烷基、c
1-c6卤代烷基、卤基、-oh、-c(o)h、-c(o)oh、-c(o)oc
1-c6烷基、-oc
1-c6烷基和c
3-c8环烷基。在一些实施方案中,r1是
–
oh,并且r2选自由以下组成的组:-cn、
卤素、-c(o)h、-ch=nrj、未被取代或被取代的c
3-c8环烷基、未被取代或被取代的c
3-c8环烯基以及未被取代或被取代的杂环烷基。
[0206]
在式(a),包括式(a-1b)、(a-2b)、(a-3b)、(a-4a)、(a-4b)、(a-4c)、(a-4d)、(a-4e)、(a-4f)、(a-4g)、(a-4h)和(a-4i)的一些实施方案中,r2是
–
oh,并且r1选自由以下组成的组:-cn、卤素、-c(o)ra、-ch=nrj、-s(o)rb、-s(o)2rc、-nhc(o)rd、-nhs(o)2re、-c
1-c6烷基-rf、-c
2-c6烯基-rg、未被取代或被取代的c
3-c8环烷基、未被取代或被取代的c
3-c8环烯基以及未被取代或被取代的杂环烷基。在一些实施方案中,r2是
–
oh,并且r1选自由以下组成的组:-cn、卤素、-c(o)ra、-ch=nrj、-s(o)rb、-s(o)2rc、-nhc(o)rd、-nhs(o)2re、-c
1-c6烷基-rf、-c
2-c6烯基-rg、c
3-c8环烷基、c
3-c8环烯基以及杂环烷基,其中所述c
3-c8环烷基、c
3-c8环烯基以及杂环烷基任选地被一个或多个选自由以下组成的组的取代基取代:c
1-c6烷基、c
1-c6卤代烷基、卤基、-oh、-c(o)h、-c(o)oh、-c(o)oc
1-c6烷基、-oc
1-c6烷基和c
3-c8环烷基。在一些实施方案中,ra、rb、rc和re各自独立地是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
1-c6卤代烷基、未被取代或被取代的杂环基、未被取代或被取代的杂芳基、苯甲酰基或苯乙烯基。在一些实施方案中,ra、rb、rc和re各自独立地是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
1-c6卤代烷基、杂环基、杂芳基、苯甲酰基或苯乙烯基,其中所述杂环基和杂芳基任选地被一个或多个选自由以下组成的组的取代基取代:c
1-c6烷基、c
1-c6卤代烷基、卤基、-oh、-c(o)h、-c(o)oh、-c(o)oc
1-c6烷基、-oc
1-c6烷基和c
3-c8环烷基。在一些实施方案中,rd是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
1-c6卤代烷基、未被取代或被取代的杂环基、未被取代或被取代的杂芳基或苯甲酰基。在一些实施方案中,rd是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
1-c6卤代烷基、杂环基、杂芳基或苯甲酰基,其中所述杂环基和杂芳基任选地被一个或多个选自由以下组成的组的取代基取代:c
1-c6烷基、c
1-c6卤代烷基、卤基、-oh、-c(o)h、-c(o)oh、-c(o)oc
1-c6烷基、-oc
1-c6烷基和c
3-c8环烷基。在一些实施方案中,rf和rg各自独立地是
–
oh、未被取代的杂芳基、
–
nr
mrn
、苯甲酰基或苯乙烯基,其中rm和rn各自独立地是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基或c
3-c8环烷基,其中所述c
3-c8环烷基任选地被一个或多个选自由以下组成的组的取代基取代:c
1-c6烷基、c
1-c6卤代烷基、卤基、-oh、-c(o)h、-c(o)oh、-c(o)oc
1-c6烷基、-oc
1-c6烷基和c
3-c8环烷基。在一些实施方案中,rj是杂环基、芳基、-ork、-nhrk、-nhc(o)rk、-nhs(o)2rk或-nhc(nh)nh2,其中所述杂环基和芳基任选地被一个或多个选自由以下组成的组的取代基取代:c
1-c6烷基、c
1-c6卤代烷基、卤基、-oh、-c(o)h、-c(o)oh、-c(o)oc
1-c6烷基、-oc
1-c6烷基和c
3-c8环烷基。在一些实施方案中,r2是
–
oh,并且r1选自由以下组成的组:-cn、卤素、-c(o)h、-ch=nrj、未被取代或被取代的c
3-c8环烷基、未被取代或被取代的c
3-c8环烯基以及未被取代或被取代的杂环烷基。
[0207]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)、(a-2b)、(a-3a)、(a-3b)、(a-4a)、(a-4b)、(a-4c)、(a-4d)、(a-4e)、(a-4f)、(a-4g)、(a-4h)和(a-4i)的一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是-ch=nrj,其中rj是未被取代或被取代的杂环基、未被取代或被取代的芳基、-ork、-nhrk、-nhc(o)rk、-nhs(o)2rk或-nhc(nh)nh2。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是-ch=nrj,其中rj是未被取代或被取代的杂环基、未被取代或被取代的芳基、-ork、-nhrk、-nhc(o)rk、-nhs(o)2rk或-nhc(nh)nhr
aa
,其中r
aa
是未被取代或被取代的c
1-c6烷基、未被取代或被取代的c
3-c8环烷基、未被取代或被取代的芳基、未被取代或被取代的杂环烷基或未被取代或被取代的杂芳基。在一些实施方案中,r
aa
是未被取代
或被取代的c
1-c6烷基。在某些实施方案中,r
aa
是被
–
oh或-(och2ch2)voh取代的c
1-c6烷基,其中v是1、2或3。在一些实施方案中,r
aa
是未被取代或被取代的c
3-c8环烷基。在一些实施方案中,r
aa
是未被取代或被取代的芳基。在一些实施方案中,r
aa
是未被取代或被取代的c
6-c
14
芳基。在一些实施方案中,r
aa
是未被取代或被取代的杂环烷基。在一些实施方案中,r
aa
是未被取代或被取代的3至18元杂环烷基。在一些实施方案中,r
aa
是未被取代或被取代的3至6元杂环烷基。在一些实施方案中,r
aa
是未被取代或被取代的杂芳基。在一些实施方案中,r
aa
是未被取代或被取代的5至18元杂芳基。在一些实施方案中,r
aa
是未被取代或被取代的5至10元杂芳基。在一些实施方案中,r
aa
是c
3-c8环烷基、c
6-c
14
芳基、3至18元杂环烷基或5至18元杂芳基,各自任选地被c
1-c6烷基取代。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是未被取代或被取代的4至12元杂环基。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是未被取代或被取代的5至6元杂环基。在某些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是未被取代的杂环基。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是-ch=nrj,其中rj是吡咯烷基、吡唑烷基、咪唑烷基、四氢呋喃基、1,3-二氧杂环戊烷基、四氢噻吩基、氧硫杂环戊烷基、环丁砜基、哌啶基、哌嗪基、四氢吡喃基、二氧杂环己烷基、硫杂环己烷基、二硫杂环己烷基、三硫杂环己烷基、吗啉基或硫代吗啉基。在其他实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是被一个或多个选自由c
1-c6烷基、c
3-c8环烷基和氧代基组成的组的取代基取代的杂环基。在一些实施方案中,rj是杂环基,其中所述杂环基的一个或多个氮和/或硫原子任选地被氧化以提供n-氧化物、-s(o)-或
–
so
2-部分。
[0208]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)、(a-2b)、(a-3a)、(a-3b)、(a-4a)、(a-4b)、(a-4c)、(a-4d)、(a-4e)、(a-4f)、(a-4g)、(a-4h)和(a-4i)的一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是未被取代或被取代的芳基。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是未被取代或被取代的6至14元芳基。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是未被取代的苯基或萘基。在其他实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是被一个或多个选自由c
1-c6烷基、c
3-c8环烷基和氧代基组成的组的取代基取代的苯基或萘基。
[0209]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)、(a-2b)、(a-3a)、(a-3b)、(a-4a)、(a-4b)、(a-4c)、(a-4d)、(a-4e)、(a-4f)、(a-4g)、(a-4h)和(a-4i)的一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是-ork。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是-oc
1-c6烷基。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是-oc
1-c6烯基或-oc
1-c6炔基。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是-oc
3-c8环烷基。在其他实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是
–
o-芳基。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是-nhrk。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是-nhc
1-c6烷基。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是-nhc
1-c6烯基或-nhc
1-c6炔基。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是-nhc
3-c8环烷基。在其他实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是
–
nh-芳基。在一些实施方
案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是-nhc(o)rk。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是-nhc(o)c
1-c6烷基。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是-nhc(o)c
1-c6烯基或-nhc(o)c
1-c6炔基。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是-nhc(o)c
3-c8环烷基。在其他实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是
–
nhc(o)-芳基。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是-nhs(o)2rk。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是-nhs(o)2c
1-c6烷基。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是-nhs(o)2c
1-c6烯基或-nhs(o)2c
1-c6炔基。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是-nhs(o)2c
3-c8环烷基。在其他实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是
–
nhs(o)
2-芳基。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是-nhc(nh)nhr
aa
。在一些实施方案中,r
aa
是未被取代或被取代的c
1-c6烷基。在某些实施方案中,r
aa
是被
–
oh或-(och2ch2)voh取代的c
1-c6烷基,其中v是1、2或3。在一些实施方案中,r
aa
是未被取代或被取代的c
3-c8环烷基。在一些实施方案中,r
aa
是未被取代或被取代的芳基。在一些实施方案中,r
aa
是未被取代或被取代的c
6-c
14
芳基。在一些实施方案中,r
aa
是未被取代或被取代的杂环烷基。在一些实施方案中,r
aa
是未被取代或被取代的3至18元杂环烷基。在一些实施方案中,r
aa
是未被取代或被取代的3至6元杂环烷基。在一些实施方案中,r
aa
是未被取代或被取代的杂芳基。在一些实施方案中,r
aa
是未被取代或被取代的5至18元杂芳基。在一些实施方案中,r
aa
是未被取代或被取代的5至10元杂芳基。在一些实施方案中,r
aa
是c
3-c8环烷基、c
6-c
14
芳基、3至18元杂环烷基或5至18元杂芳基,各自任选地被c
1-c6烷基取代。
[0210]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)、(a-2b)、(a-3a)、(a-3b)、(a-4a)、(a-4b)、(a-4c)、(a-4d)、(a-4e)、(a-4f)、(a-4g)、(a-4h)和(a-4i)的一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是-nhc(nh)nh2。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是-ch=nrj,其中-ch=nrj选自由以下组成的组:选自由以下组成的组:
在一些实施方案中,-ch=nrj选自由以下组成的组:的组:
[0211]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)、(a-2b)、(a-3a)、(a-3b)、(a-4a)、(a-4b)、(a-4c)、(a-4d)、(a-4e)、(a-4f)、(a-4g)、(a-4h)和(a-4i)的一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是-c
1-c6烷基-rf,其中rf选自由
–
oh、未被取代的杂芳基、
–
nr
mrn
、苯甲酰基或苯乙烯基组成的组,并且rm和rn各自独立地是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基或未被取代或被取代的c
3-c8环烷基。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是-c
2-c6烯基-rg,其中rg选自由
–
oh、未被取代的杂芳基、
–
nr
mrn
、苯甲酰基或苯乙烯基组成的组,并且rm和rn各自独立地是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基或未被取代或被取代的c
3-c8环烷基。在一些实施方案中,rm和rn各自独立地是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、或未被取代的c
3-c8环烷基、或被一个或多个选自由c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
1-c6烷氧基、c
1-c6卤代烷基、-oh和卤基组成的组的取代基取代的c
3-c8环烷基。在一些实施方案中,rm是未被取代或被取代的c
3-c8环烷基,并且rn是h、c
1-c6烷基、c
2-c6烯基或c
2-c6炔基。在一些实施方案中,rm是c
3-c8环烷基,并且rn是h。
[0212]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)、(a-2b)、(a-3a)、(a-3b)、(a-4a)、(a-4b)、(a-4c)、(a-4d)、(a-4e)、(a-4f)、(a-4g)、(a-4h)和(a-4i)的一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是未被取代的c
3-c8环烷基。在其他实施方案中,r1和r2中的一者是
–
oh,并且另一者是被取代的c
3-c8环烷基。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是未被取代的c
3-c8环烯基。在其他实施方案中,r1和r2中的一者是
–
oh,并且另一者是被取代的c
3-c8环烯基。
[0213]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)、(a-2b)、(a-3a)、(a-3b)、(a-4a)、(a-4b)、(a-4c)、(a-4d)、(a-4e)、(a-4f)、(a-4g)、(a-4h)和(a-4i)的一些实施方案中,r3选自由c
1-c6烷基、c
1-c6烷氧基和卤素组成的组。在一些实施方案中,r3是甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基或叔丁基。在一些实施方案中,r3是甲基、乙基、异丙基或叔丁基。在一些实施方案中,r3是甲氧基、乙氧基、丙氧基、异丙氧基、丁氧基或叔丁氧基。在一些实施方案中,r3是f、cl、br或i。在一些实施方案中,r3是
–
och3。在一些实施方案中,r3是f。在其他实施方案中,r3是h。
[0214]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)、(a-2b)、(a-3a)、(a-3b)、(a-4a)、(a-4b)、(a-4c)、(a-4d)、(a-4e)、(a-4f)、(a-4g)、(a-4h)和(a-4i)的一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是-c(o)h。在一些实施方案中,r1是
–
oh,r2是-c(o)h,并且r3是h。在一些实施方案中,r1是
–
oh,r2是-c(o)h,并且r3是未被取代的c
1-c6烷基。在一些实施方案
中,r1是
–
oh,r2是-c(o)h,并且r3是c
1-c6卤代烷基。在一些实施方案中,r1是
–
oh,r2是-c(o)h,并且r3是未被取代的c
1-c6烷氧基。在一些实施方案中,r1是
–
oh,r2是-c(o)h,并且r3是被一个或多个卤素取代的c
1-c6烷氧基。在其他实施方案中,r1是
–
oh,r2是-c(o)h,并且r3是卤素。在某些实施方案中,r1是
–
oh,r2是-c(o)h,并且r3是氟基。在某些实施方案中,r1是
–
oh,r2是-c(o)h,并且r3是甲基。在一些实施方案中,r1是
–
oh,r2是-c(o)h,并且r3是甲氧基。在一些实施方案中,r2是
–
oh,r1是-c(o)h,并且r3是h。在一些实施方案中,r2是
–
oh,r1是-c(o)h,并且r3是未被取代的c
1-c6烷基。在一些实施方案中,r2是
–
oh,r1是-c(o)h,并且r3是c
1-c6卤代烷基。在一些实施方案中,r2是
–
oh,r1是-c(o)h,并且r3是未被取代的c
1-c6烷氧基。在一些实施方案中,r2是
–
oh,r1是-c(o)h,并且r3是被一个或多个卤素取代的c
1-c6烷氧基。在其他实施方案中,r2是
–
oh,r1是-c(o)h,并且r3是卤素。在某些实施方案中,r2是
–
oh,r1是-c(o)h,并且r3是氟基。在某些实施方案中,r2是
–
oh,r1是-c(o)h,并且r3是甲基。在一些实施方案中,r2是
–
oh,r1是-c(o)h,并且r3是甲氧基。
[0215]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)和(a-2b)的一些实施方案中,g1和g2各自是ch。在一些实施方案中,g1是ch,并且g2是n。在其他实施方案中,g1是n,并且g2是ch。
[0216]
在式(a),包括式(a-1a)和(a-1b)的一些实施方案中,n是0。在一些实施方案中,n是1。在一些实施方案中,n是2。在其他实施方案中,n是3。在一些实施方案中,r4是c
1-c6烷氧基。在一些实施方案中,r4是甲氧基、乙氧基、丙氧基、异丙氧基、丁氧基、异丁氧基、仲丁氧基或叔丁氧基。在其他实施方案中,r4是在一些实施方案中,n是0,并且r4是烷氧基。在一些实施方案中,n是0,并且r4是在一些实施方案中,n是1,并且r4是烷氧基。在一些实施方案中,n是1,并且r4是在一些实施方案中,n是2,并且r4是烷氧基。在一些实施方案中,n是2,并且r4是在一些实施方案中,n是3,并且r4是烷氧基。在一些实施方案中,n是3,并且r4是
[0217]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)和(a-2b)的一些实施方案中,g3是ch(x
1-r
6a
)、c(x
1-r
6a
)、n、n(x
1-r
6a
)、s或o;g4是ch(x
2-r
6b
)、c(x
2-r
6b
)、n、n(x
2-r
6b
)、s或o;g5是ch(x
3-r
6c
)、c(x
3-r
6c
)、n、n(x
3-r
6c
)、s或o;g6是ch(x
4-r
6d
)、c(x
4-r
6d
)、n、n(x
4-r
6d
)、s、o,或是不存在的;并且g7是n、c或ch,其中g1、g2、g3、g4、g5、g6和g7各自具有零电荷(例如g1、g2、g3、g4、g5、g6和g7的氮不是阳离子性的)。
[0218]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)和(a-2b)的一些实施方案中,是其中r
6a
、r
6b
、r
6c
和r
6d
中的一者或多者选自由以下组成的组:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、c
6-c
12
芳基、3至10元杂环基、5至10元杂芳基、-c
1-c6烷基-5至6元杂环基、-oc(o)-5至6元杂环基、-c(o)rh、-s(o)2nr
w1rw2
、-s(o)2ry和-nr
z1
s(o)2r
z2
。
[0219]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)和(a-2b)的一些实施方案中,是其中r
6c
选自由以下组成的组:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、c
6-c
12
芳基、3至10元杂环基、5至10元杂芳基、-c
1-c6烷基-5至6元杂环基、-oc(o)-5至6元杂环基、-c(o)rh、-s(o)2nr
w1rw2
、-s(o)2ry或-nr
z1
s(o)2r
z2
。在一些实施方案中,r
6c
是未被取代的c
1-c6烷基。举例来说,在一些实施方案中,r
6c
是甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基和叔丁基。在一些实施方案中,r
6c
是被一个或多个选自由c
3-c8环烷基和卤素组成的组的基团取代的c
1-c6烷基。在一些实施方案中,r
6c
是c
1-c6烷氧基。举例来说,在一些实施方案中,r
6c
是甲氧基、乙氧基、丙氧基、异丙氧基、丁氧基、异丁氧基、仲丁氧基和叔丁氧基。在一些实施方案中,r
6c
是被一个或多个选自由c
3-c8环烷基和卤素组成的组的基团取代的c
1-c6烷氧基。在一些实施方案中,r
6c
是卤基。举例来说,在一些实施方案中,r
6c
是氟基、氯基或溴基。在其他实施方案中,r
6c
是c
1-c6卤代烷基。举例来说,在一些实施方案中,r
6c
是氟乙基、三氟甲基、二氟甲基、三氟乙基和三氯甲基。在一些实施方案中,r
6c
是-c(o)rh,其中rh是h、c
1-c6烷基、c
1-c6烷氧基、c
3-c8环烷基或-nrrrs。举例来说,在一些实施方案中,r
6c
是-c(o)h、-c(o)ch3、-c(o)oc(ch3)3或
–
c(o)-环丙基。在一些实施方案中,r
6c
是未被取代的5至6元杂环。在一些实施方案中,r
6c
是被一个或多个选自由以下组成的组的基团取代的5至6元杂环:c
1-c6烷基、c1-c6烷氧基、卤基、-oh、c
1-c6烷基-oh、=o和=s。在一些实施方案中,r
6c
是吡咯烷基、吡唑烷基、咪唑烷基、四氢呋喃基、1,3-二氧杂环戊烷基、四氢噻吩基、氧硫杂环戊烷基、环丁砜基、哌啶基、哌嗪基、四氢吡喃基、二氧杂环己烷基、硫杂环己烷基、二硫杂环己烷基、三硫杂环己烷基、吗啉基或硫代吗啉基,各自任选地被一个或多个选自由以下组成的组的取代基取代:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、c
1-c6烷基-oh、=o和=s。在一些实施方案中,r
6c
是吡咯烷基、吡唑烷基、咪唑烷基、四氢呋喃基、1,3-二氧杂环戊烷基、四氢噻吩基、氧硫杂环戊烷基、环丁砜基、哌啶基、哌嗪基、四氢吡喃基、二氧杂环己烷基、硫杂环己烷基、二硫杂环己烷基、三硫杂环己烷基、吗啉基或硫代吗啉基。在一些实施方案中,r
6c
是吡咯烷基。在某些实施方案中,r
6c
是4-吡咯烷-1-基。在一些实施方案中,r
6c
是未被取代的5至10元杂芳基。在一些实施方案中,r
6c
是被一个或多个选自由以下组成的组的基团取代的5至10元杂芳基:c
1-c6烷基、c
1-c6烷氧基、-oh和c
1-c6烷基-oh。在一些实施方案中,r
6c
是吡咯基、吡唑基、咪唑基、三唑基、四唑基、呋喃基、异噁唑基、噁唑基、噁二唑基、噻吩基、异噻唑基、噻唑基、噻二唑基、吡啶基、哒嗪基、嘧啶基、吡嗪基、三嗪基或四嗪基,各自被一个或多个选自由以下组成的组的取代基取代:c
1-c6烷基、c
1-c6烷氧基、-oh和c
1-c6烷基-oh。在一些实施方案中,r
6c
是吡咯基、吡唑基、咪唑基、三唑基、四唑基、呋喃基、异噁唑基、噁唑基、噁二唑基、噻吩基、异噻唑基、噻唑基、噻二唑基、吡啶基、哒嗪基、嘧啶基、吡嗪基、三嗪基或四嗪基。
[0220]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)和(a-2b)的一些实施方案中,是其中r
6b
选自由以下组成的组:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、c
6-c
12
芳基、3至10元杂环基、5至10元杂芳基、-c
1-c6烷基-5至6元杂环基、-oc(o)-5至6元杂环基、-c(o)rh、-s(o)2nr
w1rw2
、-s(o)2ry或-nr
z1
s(o)2r
z2
。在一些实施方案中,r
6b
是未被取代的c
1-c6烷基。举例来说,在一些实施方案中,r
6b
是甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基和叔丁基。在一些实施方案中,r
6b
是被一个或多个选自由c
3-c8环烷基和卤素组成的组的基团取代的c
1-c6烷基。在一些实施方案中,r
6b
是c
1-c6烷氧基。举例来说,在一些实施方案中,r
6b
是甲氧基、乙氧基、丙氧基、异丙氧基、丁氧基、异丁氧基、仲丁氧基和叔丁氧基。在一些实施方案中,r
6b
是被一个或多个选自由c
3-c8环烷基和卤素组成的组的基团取代的c
1-c6烷氧基。在一些实施方案中,r
6b
是卤基。举例来说,在一些实施方案中,r
6b
是氟基、氯基或溴基。在其他实施方案中,r
6b
是c
1-c6卤代烷基。举例来说,在一些实施方案中,r
6b
是氟乙基、三氟甲基、二氟甲基、三氟乙基和三氯甲基。在一些实施方案中,r
6b
是-c(o)rh,其中rh是h、c
1-c6烷基、c
1-c6烷氧基、c
3-c8环烷基或-nrrrs。举例来说,在一些实施方案中,r
6b
是-c(o)h、-c(o)ch3、-c(o)oc(ch3)3或
–
c(o)-环丙基。在一些实施方案中,r
6b
是未被取代的5至6元杂环。在一些实施方案中,r
6b
是被一个或多个选自由以下组成的组的基团取代的5至6元杂环:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、c
1-c6烷基-oh、=o和=s。在一些实施方案中,r
6b
是吡咯烷基、吡唑烷基、咪唑烷基、四氢呋喃基、1,3-二氧杂环戊烷基、四氢噻吩基、氧硫杂环戊烷基、环丁砜
基、哌啶基、哌嗪基、四氢吡喃基、二氧杂环己烷基、硫杂环己烷基、二硫杂环己烷基、三硫杂环己烷基、吗啉基或硫代吗啉基,各自被一个或多个选自由以下组成的组的取代基取代:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、c
1-c6烷基-oh、=o和=s。在一些实施方案中,r
6b
是吡咯烷基、吡唑烷基、咪唑烷基、四氢呋喃基、1,3-二氧杂环戊烷基、四氢噻吩基、氧硫杂环戊烷基、环丁砜基、哌啶基、哌嗪基、四氢吡喃基、二氧杂环己烷基、硫杂环己烷基、二硫杂环己烷基、三硫杂环己烷基、吗啉基或硫代吗啉基。在一些实施方案中,r
6b
是未被取代的5至10元杂芳基。在一些实施方案中,r
6b
是被一个或多个选自由以下组成的组的基团取代的5至10元杂芳基:c
1-c6烷基、c
1-c6烷氧基、-oh和c
1-c6烷基-oh。在一些实施方案中,r
6b
是吡咯基、吡唑基、咪唑基、三唑基、四唑基、呋喃基、异噁唑基、噁唑基、噁二唑基、噻吩基、异噻唑基、噻唑基、噻二唑基、吡啶基、哒嗪基、嘧啶基、吡嗪基、三嗪基或四嗪基,各自被一个或多个选自由以下组成的组的基团取代:c
1-c6烷基、c
1-c6烷氧基、-oh和c
1-c6烷基-oh。在一些实施方案中,r
6b
是吡咯基、吡唑基、咪唑基、三唑基、四唑基、呋喃基、异噁唑基、噁唑基、噁二唑基、噻吩基、异噻唑基、噻唑基、噻二唑基、吡啶基、哒嗪基、嘧啶基、吡嗪基、三嗪基或四嗪基。
[0221]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)和(a-2b)的一些实施方案中,是其中r
6a
选自由以下组成的组:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、c
6-c
12
芳基、3至10元杂环基、5至10元杂芳基、-c
1-c6烷基-5至6元杂环基、-oc(o)-5至6元杂环基、-c(o)rh、-s(o)2nr
w1rw2
、-s(o)2ry或-nr
z1
s(o)2r
z2
。在一些实施方案中,r
6a
是未被取代的c
1-c6烷基。举例来说,在一些实施方案中,r
6a
是甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基和叔丁基。在一些实施方案中,r
6a
是被一个或多个选自由c
3-c8环烷基和卤素组成的组的基团取代的c
1-c6烷基。在一些实施方案中,r
6a
是c
1-c6烷氧基。举例来说,在一些实施方案中,r
6a
是甲氧基、乙氧基、丙氧基、异丙氧基、丁氧基、异丁氧基、仲丁氧基和叔丁氧基。在一些实施方案中,r
6a
是被一个或多个选自由c
3-c8环烷基和卤素组成的组的基团取代的c
1-c6烷氧基。在一些实施方案中,r
6a
是卤基。举例来说,在一些实施方案中,r
6a
是氟基、氯基或溴基。在其他实施方案中,r
6a
是c
1-c6卤代烷基。举例来说,在一些实施方案中,r
6a
是氟乙基、三氟甲基、二氟甲基、三氟乙基和三氯甲基。在一些实施方案中,r
6a
是-c(o)rh,其中rh是h、c
1-c6烷基、c
1-c6烷氧基、c
3-c8环烷基或-nrrrs。举例来说,在一些实施方案中,r
6a
是-c(o)h、-c(o)ch3、-c(o)oc(ch3)3或
–
c(o)-环丙基。在一些实施方案中,r
6a
是未被取代的5至6元杂环。在一些实施方案中,r
6a
是被一个或多个选自由以下组成的组的基团取代的5至6元杂环:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、c
1-c6烷基-oh、=o和=s。在一些实施方案中,r
6a
是吡咯烷基、吡唑烷基、咪唑烷基、四氢呋喃基、1,3-二氧杂环戊烷基、四氢噻吩基、氧硫杂环戊烷基、环丁砜基、哌啶基、哌嗪基、四氢吡喃基、二氧杂环己烷基、硫杂环己烷基、二硫杂环己烷基、三硫杂环己烷基、吗啉基或硫代吗啉基,各自被一个或多个选自由以下组成的组的取代基取代:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、c
1-c6烷基-oh、=o和=s。在一些实施方案中,r
6a
是吡咯
烷基、吡唑烷基、咪唑烷基、四氢呋喃基、1,3-二氧杂环戊烷基、四氢噻吩基、氧硫杂环戊烷基、环丁砜基、哌啶基、哌嗪基、四氢吡喃基、二氧杂环己烷基、硫杂环己烷基、二硫杂环己烷基、三硫杂环己烷基、吗啉基或硫代吗啉基。在一些实施方案中,r
6a
是未被取代的5至10元杂芳基。在一些实施方案中,r
6a
是被一个或多个选自由以下组成的组的基团取代的5至10元杂芳基:c
1-c6烷基、c
1-c6烷氧基、-oh和c
1-c6烷基-oh。在一些实施方案中,r
6a
是吡咯基、吡唑基、咪唑基、三唑基、四唑基、呋喃基、异噁唑基、噁唑基、噁二唑基、噻吩基、异噻唑基、噻唑基、噻二唑基、吡啶基、哒嗪基、嘧啶基、吡嗪基、三嗪基或四嗪基,各自被一个或多个选自由以下组成的组的取代基取代:c
1-c6烷基、c
1-c6烷氧基、-oh和c
1-c6烷基-oh。在一些实施方案中,r
6a
是吡咯基、吡唑基、咪唑基、三唑基、四唑基、呋喃基、异噁唑基、噁唑基、噁二唑基、噻吩基、异噻唑基、噻唑基、噻二唑基、吡啶基、哒嗪基、嘧啶基、吡嗪基、三嗪基或四嗪基。
[0222]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)和(a-2b)的一些实施方案中,是其中r
6b
和r
6d
各自独立地选自由以下组成的组:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、c
6-c
12
芳基、3至10元杂环基、5至10元杂芳基、-c
1-c6烷基-5至6元杂环基、-oc(o)-5至6元杂环基、-c(o)rh、-s(o)2nr
w1rw2
、-s(o)2ry或-nr
z1
s(o)2r
z2
。在一些实施方案中,是其中r
6a
和r
6c
各自独立地选自由以下组成的组:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、c
6-c
12
芳基、3至10元杂环基、5至10元杂芳基、-c
1-c6烷基-5至6元杂环基、-oc(o)-5至6元杂环基、-c(o)rh、-s(o)2nr
w1rw2
、-s(o)2ry或-nr
z1
s(o)2r
z2
。在一些实施方案中,是
[0223]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)和(a-2b)的一些实施方案中,是
其中r
6b
、r
6c
和r
6d
中的一者或多者选自由以下组成的组:c
1-c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基和5至10元杂芳基。在一些实施方案中,是其中r
6a
、r
6c
和r
6d
中的一者或多者选自由以下组成的组:c
1-c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基和5至10元杂芳基。在一些实施方案中,是其中r
6a
、r
6b
和r
6d
中的一者或多者选自由以下组成的组:c
1-c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基和5至10元杂芳基。在一些实施方案中,是其中r
6b
和r
6d
中的一者或两者选自由以下组成的组:c
1-c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基和5至10元杂芳基。在一些实施方案中,是
其中r
6a
和r
6c
中的一者或两者选自由以下组成的组:c
1-c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基和5至10元杂芳基。在一些实施方案中,选自由以下组成的组:
[0224]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)和(a-2b)的一些实施方案中,是在一些实施方案中,是其中r
6c
选自由以下组成的组:氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、c
6-c
12
芳基、3至10元杂环基、5至10元杂芳基、-c
1-c6烷基-5至6元杂环基、-oc(o)-5至6元杂环基、-c(o)rh、-s(o)2nr
w1rw2
、-s(o)2ry和-nr
z1
s(o)2r
z2
。在某些实施方案中,r
6c
是
–
c(o)oc(ch3)3。
[0225]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)和(a-2b)的一些实施方案中,是在一些实施方案中,是
[0226]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)和(a-2b)的任何前述实施方案中,r
6a
、r
6b
、r
6c
和r
6d
中的一者或多者选自由以下组成的组:c
1-c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基和5至10元杂芳基。在一些实施方案中,r
6a
、r
6b
、r
6c
和r
6d
中的一者或多者是未被取代或被一个或多个选自由以下组成的组的基团取代的c
6-c
12
芳基:c
1-c6烷基、c
1-c6烷氧基、-oh和c
1-c6烷基-oh。举例来说,在一些实施方案中,r
6a
、r
6b
、r
6c
和r
6d
中的一者是苯基或萘基。在一些实施方案中,r
6a
、r
6b
、r
6c
和r
6d
中的一者或多者是未被取代或被一个或多个选自由以下组成的组的基团取代的3至10元杂环基:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、c
1-c6烷基-oh、=o和=s。举例来说,在一些实施方案中,r
6a
、r
6b
、r
6c
和r
6d
中的一者是吡咯烷基、吡唑烷基、咪唑烷基、四氢呋喃基、1,3-二氧杂环戊烷基、四氢噻吩基、氧硫杂环戊烷基、环丁砜基、哌啶基、哌嗪基、四氢吡喃基、二氧杂环己烷基、硫杂环己烷基、二硫杂环己烷基、三硫杂环己烷基、吗啉基、硫代吗啉基、四氢喹啉基、四氢异喹啉基、十氢喹啉基、十氢异喹啉基、吲哚啉基、异吲哚啉基、四氢萘啶基或六氢苯并咪唑基,各自独立地未被取代或被一个或多个选自由以下组成的组的基团取代:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、c
1-c6烷基-oh、=o和=s。
[0227]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)和(a-2b)的一些实施方案中,r
6a
、r
6b
、r
6c
和r
6d
中的一者选自由以下组成的组:c
1-c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基和5至10元杂芳基。在某些实施方案中,r
6a
、r
6b
、r
6c
和r
6d
中的一者选自由以下组成的组:甲基、乙基、f、cl、
–
cf3、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡唑基和三唑基。在某些实施方案中,r
6a
、r
6b
、r
6c
和r
6d
中的一者选自由以下组成的组:吡咯烷基、哌啶基、吗啉基、哌嗪基、吡唑基和三唑基,各自任选地被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、c
1-c6烷基-oh、=o和=s组成的组的基团取代。在一些实施方案中,r
6a
、r
6b
、r
6c
和r
6d
中的两者或三者选自由以下组成的组:甲基、乙基、f、cl、
–
cf3、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡唑基和三唑基。在一些实施方案中,r
6a
、r
6b
、r
6c
和r
6d
中的一者选自由以下组成的组:甲基、乙基、甲氧基、f、cl、
–
cf3、在一些实施方案中,r
6a
、r
6b
、r
6c
和r
6d
中的一者选自由以下组成的组:中的一者选自由以下组成的组:
[0228]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)和(a-2b)的其他实施方案中,r
6a
、r
6b
、r
6c
和r
6d
各自是h。
[0229]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)、(a-2b)、(a-3a)和(a-3b)的一些实施方
案中,g3是ch(x
1-r
6a
)、c(x
1-r
6a
)或n(x
1-r
6a
),x1是不存在的,是并且r
6a
是氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基、-c
1-c6烷基-杂环基、-oc(o)-杂环基、-c(o)rh、-s(o)2nr
w1rw2
、-s(o)2ry或-nr
z1
s(o)2r
z2
,其中r
6a
的所述c
1-c6烷基和c
1-c6烷氧基各自独立地未被取代或被一个或多个选自由环烷基和卤素组成的组的基团取代;r
6a
的所述芳基和杂芳基各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、c
3-c8环烷基、-oh和c
1-c6烷基-oh组成的组的基团取代;并且r
6a
的所述杂环基、-c
1-c6烷基-杂环基和-oc(o)-杂环基各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、c
1-c6烷基-oh、=o和=s组成的组的基团取代;rh选自由h、c
1-c6烷基、c
1-c6烷氧基和c
3-c8环烷基以及-nrrrs组成的组;r
p
是h或c
1-c6烷基;rq是c
2-c3烷基、-c(o)r
t
、-c(o)oru、-c(o)nrv;rr、rs、r
w1
和r
z1
各自独立地选自h和c
1-c6烷基;并且r
t
、ru、rv、r
w2
、ry和r
z2
各自独立地选自h、c
1-c6烷基、未被取代或被取代的c
3-c8环烷基以及未被取代或被取代的杂环基。
[0230]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)、(a-2b)、(a-3a)和(a-3b)的一些实施方案中,g3是ch(x
1-r
6a
)或c(x
1-r
6a
),其中x1是不存在的;r
6a
是氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基或-c(o)rh,其中c
1-c6烷基和c
1-c6烷氧基未被取代或被c
3-c8环烷基或卤素取代;r
p
是h或c
1-c6烷基;rq是c
2-c3烷基;并且rh选自由h、c
1-c6烷基、c
1-c6烷氧基或c
3-c8环烷基组成的组。在一些实施方案中,g3是ch(x
1-r
6a
)或c(x
1-r
6a
),其中x1是m是1-6;r
6a
是氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基或-c(o)rh,其中c
1-c6烷基和c
1-c6烷氧基未被取代或被c
3-c8环烷基或卤素取代;r
p
是h或c
1-c6烷基;rq是c
2-c3烷基;并且rh选自由h、c
1-c6烷基、c
1-c6烷氧基或c
3-c8环烷基组成的组。在一些实施方案中,g3是n或n(x
1-r
6a
),其中x1是不存在的;r
6a
是氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基或-c(o)rh,其中c
1-c6烷基和c
1-c6烷氧基未被取代或被c
3-c8环烷基或卤素取代;r
p
是h或c
1-c6烷基;rq是c
2-c3烷基;并且rh选自由h、c
1-c6烷基、c
1-c6烷氧基或c
3-c8环烷基组成的组。在一些实施方案中,g3是n或n(x
1-r
6a
),其中x1是是m是1-6;r
6a
是氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基或-c(o)rh,其中c
1-c6烷基和c
1-c6烷氧基未被取代或被c
3-c8环烷基或卤素取代;r
p
是h或c
1-c6烷基;rq是c
2-c3烷基;并且rh选自由h、c
1-c6烷基、c
1-c6烷氧基或c
3-c8环烷基组成的组。在任何先前实施方案中的一些中,r
6a
是甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基或叔丁基。在任何先前实施方案中的一些中,r
6a
是被c
3-c8环烷基或卤素取代的c
1-c6烷基。在任何先前实施方案中的一些中,r
6a
是甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、异丁氧基、仲丁氧基或叔丁氧基。在任何先前实施方案中的一些中,r
6a
是被c
3-c8环烷基或卤素取代的c
1-c6烷氧基。在任何先前实施方案中的一些中,r
6a
是氟基、氯基、溴基或碘基。在任何先前实施方案中的一些中,r
6a
是-n(ch2ch3)2、-n(ch2ch2ch3)2或-n(ch2ch3)(ch2ch2ch3)。在任何先前实施方案中的一些中,r
6a
是苯基或萘基。在任何先前实施方案中的一些中,r
6a
是5至14元杂环基。在一些实施方案中,r
6a
是5至6元杂环基。在任何先前实施方案中的一些中,r
6a
是吡咯烷基、吡唑烷基、咪唑烷
基、四氢呋喃基、1,3-二氧杂环戊烷基、四氢噻吩基、氧硫杂环戊烷基、环丁砜基、哌啶基、哌嗪基、四氢吡喃基、二氧杂环己烷基、硫杂环己烷基、二硫杂环己烷基、三硫杂环己烷基、吗啉基或硫代吗啉基。在任何先前实施方案中的一些中,r
6a
是5至14元杂芳基。在一些实施方案中,r
6a
是5至6元杂芳基。在任何先前实施方案中的一些中,r
6a
是吡咯基、吡唑基、咪唑基、三唑基、四唑基、呋喃基、异噁唑基、噁唑基、噁二唑基、噻吩基、异噻唑基、噻唑基、噻二唑基、吡啶基、哒嗪基、嘧啶基、吡嗪基、三嗪基或四嗪基。在任何先前实施方案中的一些中,r
6a
是芳基、杂环基或杂芳基,各自被c
1-c6烷基取代。在任何先前实施方案中的一些中,r
6a
是-c(o)h、-c(o)c
1-c6烷基、-c(o)c
1-c6烷氧基或-c(o)c
3-c8环烷基。在任何先前实施方案中的一些中,r
6a
是-oh、-nr
prq
、芳基、杂环基、杂芳基、未被取代的c
1-c6烷氧基、或被c
3-c8环烷基或卤素取代的c
1-c6烷氧基。在任何先前实施方案中的一些中,r
6a
是氢、-ch3、-oh、-och3、-c(o)oc(ch3)3、-n(ch2ch3)2、苯基、吗啉基、哌啶基、哌嗪基、4-乙基哌嗪基、吡咯烷基、吡唑基、环丙基甲氧基或环丙烷羰基。在一些实施方案中,g3是s。在其他实施方案中,g3是o。
[0231]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)、(a-2b)、(a-3a)和(a-3b)的一些实施方案中,g4是ch(x
2-r
6b
)、c(x
2-r
6b
)或n(x
2-r
6b
),其中x2是不存在的,是r
6b
是氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基、-c
1-c6烷基-杂环基、-oc(o)-杂环基、-c(o)rh、-s(o)2nr
w1rw2
、-s(o)2ry或-nr
z1
s(o)2r
z2
,其中r
6b
的所述c
1-c6烷基和c
1-c6烷氧基各自独立地未被取代或被一个或多个选自由环烷基和卤素组成的组的基团取代;r
6b
的所述芳基和杂芳基各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、c
3-c8环烷基、-oh和c
1-c6烷基-oh组成的组的基团取代;并且r
6b
的所述杂环基、-c
1-c6烷基-杂环基和-oc(o)-杂环基各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、c
1-c6烷基-oh、=o和=s组成的组的基团取代;rh选自由h、c
1-c6烷基、c
1-c6烷氧基和c
3-c8环烷基以及-nrrrs组成的组;r
p
是h或c
1-c6烷基;rq是c
2-c3烷基、-c(o)r
t
、-c(o)oru、-c(o)nrv;rr、rs、r
w1
和r
z1
各自独立地选自h和c
1-c6烷基;并且r
t
、ru、rv、r
w2
、ry和r
z2
各自独立地选自h、c
1-c6烷基、未被取代或被取代的c
3-c8环烷基以及未被取代或被取代的杂环基。
[0232]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)、(a-2b)、(a-3a)和(a-3b)的一些实施方案中,g4是ch(x
2-r
6b
)或c(x
2-r
6b
),其中x2是不存在的;r
6b
是氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基或-c(o)rh,其中c
1-c6烷基和c
1-c6烷氧基未被取代或被c
3-c8环烷基或卤素取代;r
p
是h或c
1-c6烷基;rq是c
2-c3烷基;并且rh选自由h、c
1-c6烷基、c
1-c6烷氧基或c
3-c8环烷基组成的组。在一些实施方案中,g4是ch(x
2-r
6b
)或c(x
2-r
6b
),其中x2是m是1-6;r
6b
是氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基或-c(o)rh,其中c
1-c6烷基和c
1-c6烷氧基未被取代或被c
3-c8环烷基或卤素取代;r
p
是h或c
1-c6烷基;rq是c
2-c3烷基;并且rh选自由h、c
1-c6烷基、c
1-c6烷氧基或c
3-c8环烷基组成的组。在一些实施方案中,g4是n或n(x
2-r
6b
),其中x2是不存在的;r
6b
是氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基或-c(o)rh,其中c
1-c6烷基和c
1-c6烷氧基未被取代或被c
3-c8环烷基或卤素取代;r
p
是h或c
1-c6烷基;rq是c
2-c3烷基;并且rh选自由h、c
1-c6烷基、c
1-c6烷氧基或c
3-c8环烷基组成的组。在一些实施方案中,g4是n
或n(x
2-r
6b
),其中x2是m是1-6;r
6b
是氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基或-c(o)rh,其中c
1-c6烷基和c
1-c6烷氧基未被取代或被c
3-c8环烷基或卤素取代;r
p
是h或c
1-c6烷基;rq是c
2-c3烷基;并且rh选自由h、c
1-c6烷基、c
1-c6烷氧基或c
3-c8环烷基组成的组。在任何先前实施方案中的一些中,r
6b
是甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基或叔丁基。在任何先前实施方案中的一些中,r
6b
是被c
3-c8环烷基或卤素取代的c
1-c6烷基。在任何先前实施方案中的一些中,r
6b
是甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、异丁氧基、仲丁氧基或叔丁氧基。在任何先前实施方案中的一些中,r
6b
是被c
3-c8环烷基或卤素取代的c
1-c6烷氧基。在任何先前实施方案中的一些中,r
6b
是氟基、氯基、溴基或碘基。在任何先前实施方案中的一些中,r
6b
是-n(ch2ch3)2、-n(ch2ch2ch3)2或-n(ch2ch3)(ch2ch2ch3)。在任何先前实施方案中的一些中,r
6b
是苯基或萘基。在任何先前实施方案中的一些中,r
6b
是5至14元杂环基。在一些实施方案中,r
6b
是5至6元杂环基。在任何先前实施方案中的一些中,r
6b
是吡咯烷基、吡唑烷基、咪唑烷基、四氢呋喃基、1,3-二氧杂环戊烷基、四氢噻吩基、氧硫杂环戊烷基、环丁砜基、哌啶基、哌嗪基、四氢吡喃基、二氧杂环己烷基、硫杂环己烷基、二硫杂环己烷基、三硫杂环己烷基、吗啉基或硫代吗啉基。在任何先前实施方案中的一些中,r
6b
是5至14元杂芳基。在一些实施方案中,r
6b
是5至6元杂芳基。在任何先前实施方案中的一些中,r
6b
是吡咯基、吡唑基、咪唑基、三唑基、四唑基、呋喃基、异噁唑基、噁唑基、噁二唑基、噻吩基、异噻唑基、噻唑基、噻二唑基、吡啶基、哒嗪基、嘧啶基、吡嗪基、三嗪基或四嗪基。在任何先前实施方案中的一些中,r
6b
是芳基、杂环基或杂芳基,各自被c
1-c6烷基取代。在任何先前实施方案中的一些中,r
6b
是-c(o)h、-c(o)c
1-c6烷基、-c(o)c
1-c6烷氧基或-c(o)c
3-c8环烷基。在任何先前实施方案中的一些中,r
6b
是-oh、-nr
prq
、芳基、杂环基、杂芳基、未被取代的c
1-c6烷氧基、或被c
3-c8环烷基或卤素取代的c
1-c6烷氧基。在任何先前实施方案中的一些中,r
6b
是氢、-ch3、-oh、-och3、-c(o)oc(ch3)3、-n(ch2ch3)2、苯基、吗啉基、哌啶基、哌嗪基、4-乙基哌嗪基、吡咯烷基、吡唑基、环丙基甲氧基或环丙烷羰基。在一些实施方案中,g4是s。在其他实施方案中,g4是o。
[0233]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)、(a-2b)、(a-3a)和(a-3b)的一些实施方案中,g5是ch(x
3-r
6c
)、c(x
3-r
6c
)或n(x
3-r
6c
),其中x3是不存在的,是r
6c
是氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基、-c
1-c6烷基-杂环基、-oc(o)-杂环基、-c(o)rh、-s(o)2nr
w1rw2
、-s(o)2ry或-nr
z1
s(o)2r
z2
,其中r
6c
的所述c
1-c6烷基和c
1-c6烷氧基各自独立地未被取代或被一个或多个选自由环烷基和卤素组成的组的基团取代;r
6c
的所述芳基和杂芳基各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、c
3-c8环烷基、-oh和c
1-c6烷基-oh组成的组的基团取代;并且r
6c
的所述杂环基、-c
1-c6烷基-杂环基和-oc(o)-杂环基各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、c
1-c6烷基-oh、=o和=s组成的组的基团取代;rh选自由h、c
1-c6烷基、c
1-c6烷氧基和c
3-c8环烷基以及-nrrrs组成的组;r
p
是h或c
1-c6烷基;rq是c
2-c3烷基、-c(o)r
t
、-c(o)oru、-c(o)nrv;rr、rs、r
w1
和r
z1
各自独立地选自h和c
1-c6烷基;并且r
t
、ru、rv、r
w2
、ry和r
z2
各自独立地选自h、c
1-c6烷基、未被取代或被取代的c
3-c8环烷基以及未被取代或被取代的杂环基。r6d
)、c(x
4-r
6d
)或n(x
4-r
6d
),其中x4是不存在的,是r
6d
是氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基、-c
1-c6烷基-杂环基、-oc(o)-杂环基、-c(o)rh、-s(o)2nr
w1rw2
、-s(o)2ry或-nr
z1
s(o)2r
z2
,其中r
6d
的所述c
1-c6烷基和c
1-c6烷氧基各自独立地未被取代或被一个或多个选自由环烷基和卤素组成的组的基团取代;r
6d
的所述芳基和杂芳基各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、c
3-c8环烷基、-oh和c
1-c6烷基-oh组成的组的基团取代;并且r
6d
的所述杂环基、-c
1-c6烷基-杂环基和-oc(o)-杂环基各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、c
1-c6烷基-oh、=o和=s组成的组的基团取代;rh选自由h、c
1-c6烷基、c
1-c6烷氧基和c
3-c8环烷基以及-nrrrs组成的组;r
p
是h或c
1-c6烷基;rq是c
2-c3烷基、-c(o)r
t
、-c(o)oru、-c(o)nrv;rr、rs、r
w1
和r
z1
各自独立地选自h和c
1-c6烷基;并且r
t
、ru、rv、r
w2
、ry和r
z2
各自独立地选自h、c
1-c6烷基、未被取代或被取代的c
3-c8环烷基以及未被取代或被取代的杂环基。
[0236]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)和(a-2b)的一些实施方案中,g6是ch(x
4-r
6d
)或c(x
4-r
6d
),其中x4是不存在的;r
6d
是氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基或-c(o)rh,其中c
1-c6烷基和c
1-c6烷氧基未被取代或被c
3-c8环烷基或卤素取代;r
p
是h或c
1-c6烷基;rq是c
2-c3烷基;并且rh选自由h、c
1-c6烷基、c
1-c6烷氧基或c
3-c8环烷基组成的组。在一些实施方案中,g6是ch(x
4-r
6d
)或c(x
4-r
6d
),其中x4是m是1-6;r
6d
是氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基或-c(o)rh,其中c
1-c6烷基和c
1-c6烷氧基未被取代或被c
3-c8环烷基或卤素取代;r
p
是h或c
1-c6烷基;rq是c
2-c3烷基;并且rh选自由h、c
1-c6烷基、c
1-c6烷氧基或c
3-c8环烷基组成的组。在一些实施方案中,g6是n或n(x
4-r
6d
),其中x4是不存在的;r
6d
是氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基或-c(o)rh,其中c
1-c6烷基和c
1-c6烷氧基未被取代或被c
3-c8环烷基或卤素取代;r
p
是h或c
1-c6烷基;rq是c
2-c3烷基;并且rh选自由h、c
1-c6烷基、c
1-c6烷氧基或c
3-c8环烷基组成的组。在一些实施方案中,g6是n或n(x
4-r
6d
),其中x4是m是1-6;r
6d
是氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基或-c(o)rh,其中c
1-c6烷基和c
1-c6烷氧基未被取代或被c
3-c8环烷基或卤素取代;r
p
是h或c
1-c6烷基;rq是c
2-c3烷基;并且rh选自由h、c
1-c6烷基、c
1-c6烷氧基或c
3-c8环烷基组成的组。在任何先前实施方案中的一些中,r
6d
是甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基或叔丁基。在任何先前实施方案中的一些中,r
6d
是被c
3-c8环烷基或卤素取代的c
1-c6烷基。在任何先前实施方案中的一些中,r
6d
是甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、异丁氧基、仲丁氧基或叔丁氧基。在任何先前实施方案中的一些中,r
6d
是被c
3-c8环烷基或卤素取代的c
1-c6烷氧基。在任何先前实施方案中的一些中,r
6d
是氟基、氯基、溴基或碘基。在任何先前实施方案中的一些中,r
6d
是-n(ch2ch3)2、-n(ch2ch2ch3)2或-n(ch2ch3)(ch2ch2ch3)。在任何先前实施方案中的一些中,r
6d
是苯基或萘基。在任何先前实施方案中的一些中,r
6d
是5至14元杂环基。在一些实施方案中,r
6d
是5至6元杂环基。在任何先前实施方案中的一些中,r
6d
是吡咯烷基、吡唑烷基、咪唑烷基、四氢呋喃基、
1,3-二氧杂环戊烷基、四氢噻吩基、氧硫杂环戊烷基、环丁砜基、哌啶基、哌嗪基、四氢吡喃基、二氧杂环己烷基、硫杂环己烷基、二硫杂环己烷基、三硫杂环己烷基、吗啉基或硫代吗啉基。在任何先前实施方案中的一些中,r
6d
是5至14元杂芳基。在一些实施方案中,r
6d
是5至6元杂芳基。在任何先前实施方案中的一些中,r
6d
是吡咯基、吡唑基、咪唑基、三唑基、四唑基、呋喃基、异噁唑基、噁唑基、噁二唑基、噻吩基、异噻唑基、噻唑基、噻二唑基、吡啶基、哒嗪基、嘧啶基、吡嗪基、三嗪基或四嗪基。在任何先前实施方案中的一些中,r
6d
是芳基、杂环基或杂芳基,各自被c
1-c6烷基取代。在任何先前实施方案中的一些中,r
6d
是-c(o)h、-c(o)c
1-c6烷基、-c(o)c
1-c6烷氧基或-c(o)c
3-c8环烷基。在任何先前实施方案中的一些中,r
6d
是-oh、-nr
prq
、芳基、杂环基、杂芳基、未被取代的c
1-c6烷氧基、或被c
3-c8环烷基或卤素取代的c
1-c6烷氧基。在任何先前实施方案中的一些中,r
6d
是氢、-ch3、-oh、-och3、-c(o)oc(ch3)3、-n(ch2ch3)2、苯基、吗啉基、哌啶基、哌嗪基、4-乙基哌嗪基、吡咯烷基、吡唑基、环丙基甲氧基或环丙烷羰基。在一些实施方案中,g6是s。在其他实施方案中,g6是o。在一些实施方案中,g6是不存在的。
[0237]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)和(a-2b)的一些实施方案中,g5是ch(x
3-r
6c
),g6是ch(x
4-r
6d
),环是饱和的,并且r
6c
和r
6d
连同它们所连接的碳原子一起形成6元杂环基环;其中所述杂环基环未被取代或被取代。在一些实施方案中,g5是c(x
3-r
6c
),g6是c(x
4-r
6d
),是部分不饱和的或完全不饱和的,并且r
6c
和r
6d
连同它们所连接的碳原子一起形成6元芳基、杂环基或杂芳基环;其中每个6元芳基、杂环基和杂芳基环未被取代或被取代。在一些实施方案中,g5是c(x
3-r
6c
),g6是c(x
4-r
6d
),是完全不饱和的,并且r
6c
和r
6d
连同它们所连接的碳原子一起形成6元芳基、杂环基或杂芳基环;其中每个6元芳基、杂环基和杂芳基环未被取代或被取代。在一些实施方案中,r
6c
和r
6d
连同它们所连接的碳原子一起形成苯基环。在一些实施方案中,r
6c
和r
6d
连同它们所连接的碳原子一起形成6元杂环基或杂芳基环,其中所述6元杂环基或杂芳基环含有一个、两个或三个选自由n、s和o组成的组的杂原子。在一些实施方案中,r
6c
和r
6d
连同它们所连接的碳原子一起形成未被取代的6元芳基、杂环基或杂芳基环。在一些实施方案中,r
6c
和r
6d
连同它们所连接的碳原子一起形成6元芳基、杂环基或杂芳基环,其中所述6元芳基、杂环基或杂芳基环被一个或多个选自由以下组成的组的取代基取代:c
1-c6烷基、c
1-c6卤代烷基、卤基、-oh、-c(o)h、-c(o)oh、-c(o)oc
1-c6烷基、-oc
1-c6烷基和c
3-c8环烷基。
[0238]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)和(a-2b)的一些实施方案中,g7是n。在一些实施方案中,g7是c。在其他实施方案中,g7是ch。
[0239]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)和(a-2b)的一些实施方案中,r
6a
、r
6b
、r
6c
和r
6d
中的一者选自由以下组成的组:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基和-c(o)rh,其中r
6a
、r
6b
、r
6c
和r
6d
的所述c
1-c6烷基和c
1-c6烷氧基各自独立地未被取代或被c
3-c8环烷基或卤素取代;并且r
6a
、r
6b
、r
6c
和r
6d
中的其余各者各自是h。在一些实施方案中,r
6a
、r
6b
、r
6c
和r
6d
中的一者选自由以下组成的组:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、6至12元芳基、3至12元杂环基、5至12元杂芳基和-c(o)rh,其中r
6a
、r
6b
、r
6c
和r
6d
的所述c
1-c6烷基和c
1-c6烷氧基各自独立地未被取代或被c
3-c8环烷基或卤素取代;并且r
6a
、r
6b
、r
6c
和r
6d
中的其余各者各自是h。在一些实施方案中,r
6a
、r
6b
、r
6c
和r
6d
中的两者选自由以
下组成的组:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基和-c(o)rh,其中r
6a
、r
6b
、r
6c
和r
6d
的所述c
1-c6烷基和c
1-c6烷氧基各自独立地未被取代或被c
3-c8环烷基或卤素取代;并且r
6a
、r
6b
、r
6c
和r
6d
中的其余各者各自是h。在一些实施方案中,r
6a
、r
6b
、r
6c
和r
6d
中的两者选自由以下组成的组:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、6至12元芳基、3至12元杂环基、5至12元杂芳基和-c(o)rh,其中r
6a
、r
6b
、r
6c
和r
6d
的所述c
1-c6烷基和c
1-c6烷氧基各自独立地未被取代或被c
3-c8环烷基或卤素取代;并且r
6a
、r
6b
、r
6c
和r
6d
中的其余各者各自是h。
[0240]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)和(a-2b)的一些实施方案中,r
6a
、r
6b
、r
6c
和r
6d
中的一者选自由以下组成的组:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基和-c(o)rh,其中r
6a
、r
6b
、r
6c
和r
6d
的所述c
1-c6烷基和c
1-c6烷氧基各自独立地未被取代或被c
3-c8环烷基或卤素取代;并且r
6a
、r
6b
、r
6c
和r
6d
中的其余各者各自是h。在一些实施方案中,r
6a
、r
6b
、r
6c
和r
6d
中的一者选自由以下组成的组:-c
1-c6烷基-杂环基、-oc(o)-杂环基、-s(o)2nr
w1rw2
、-s(o)2ry和-nr
z1
s(o)2r
z2
;其中r
w1
和r
z1
各自独立地选自h和c
1-c6烷基,并且r
w2
、ry和r
z2
各自独立地选自h、c
1-c6烷基、未被取代或被取代的c
3-c8环烷基以及未被取代或被取代的3至12元杂环基。
[0241]
在式(a),包括式(a-1a)、(a-1b)、(a-2a)和(a-2b)的一些实施方案中,r
6a
、r
6b
、r
6c
和r
6d
中的两者选自由以下组成的组:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基和-c(o)rh,其中r
6a
、r
6b
、r
6c
和r
6d
的所述c
1-c6烷基和c
1-c6烷氧基各自独立地未被取代或被c
3-c8环烷基或卤素取代;并且r
6a
、r
6b
、r
6c
和r
6d
中的其余各者各自是h。
[0242]
在式(a)的一些实施方案中,r3是h、c
1-c3烷基、c
1-c6烷氧基或卤素,其中r3的所述c
1-c6烷基和c
1-c6烷氧基各自独立地未被取代或被一个或多个卤素取代。在一些实施方案中,当r2是
–
c(o)h时,r3是甲氧基,并且是r
6a
、r
6b
、r
6c
和r
6d
中的至少一者选自c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
prq
、芳基、杂环基、杂芳基、-c
1-c6烷基-杂环基、-oc(o)-杂环基、-c(o)rh、-s(o)2nr
w1rw2
、-s(o)2ry和-nr
z1
s(o)2r
z2
。在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中rj是被一个或多个选自由c
1-c6烷基、c
3-c8环烷基和氧代基组成的组的取代基取代的苯基或萘基。在一些实施方案中,n是0,并且r4是在一些实施方案中,r1和r2中的一者是
–
oh,并且另一者是
–
ch=nrj,其中nrj是未被取代或被取代的4至12元杂环基。在一些实施方案中,是
[0243]
在一些实施方案中,本文提供了表1a中所述的化合物及其盐。
[0244]
表1a.
[0245]
[0246]
[0247]
[0248]
[0249]
[0250]
[0251]
[0252]
[0253]
[0254]
[0255]
[0256]
[0257]
[0258]
[0259]
[0260]
[0261]
[0262]
[0263]
[0264][0265]
以及它们的药学上可接受的盐。
[0266]
在一个方面,提供了式(b)化合物:
[0267][0268]
或互变异构体、或任何前述项的药学上可接受的盐,
[0269]
其中
[0270]
l选自由以下组成的组:-c≡c-、*-nhc(o)-、*-c(o)nh-、-nhc(o)nh-、*-nhs(o)
2-、*-nhs(o)(=nh)-、*-s(o)(=nh)nh-、*-s(o)2nh-、*-s(o)nhnh-、*-nhnhs(o)-、*-c(o)nhnh-、*-nhnhc(o)-、*
–
nhc(o)o-和*
–
oc(o)nh-,其中*代表与y7的连接点;
[0271]
y1和y2各自独立地是cr
x
或n;
[0272]rx
是氢或卤素;
[0273]
当l是-c≡c-时,r
1a
和r
2a
中的一者是
–
oh,并且另一者选自由以下组成的组:-c(o)r
a1
、-ch=nr
j1
、-s(o)r
b1
、-s(o)2r
c1
、-nhc(o)r
d1
、-nhs(o)2r
e1
、-c
1-c6烷基-r
f1
、-c
2-c6烯基-r
g1
、c
3-c8环烷基、c
3-c8环烯基以及5或6元杂环烷基,其中所述c
3-c8环烷基和c
3-c8环烯基各自独立地未被取代或被一个或多个=o取代,并且所述5或6元杂环烷基未被取代或被一个或多个独立地选自由c
1-c6烷基、c
3-c8环烷基、=o和
–
c(o)o-c
1-c6烷基组成的组的取代基取代;
[0274]
当l是*-nhc(o)-、*-c(o)nh-、-nhc(o)nh-、*-nhs(o)
2-、*-s(o)2nh-、*-s(o)nhnh-、*-c(o)nhnh-或*
–
nhc(o)o-时,r
1a
和r
2a
中的一者是
–
oh,并且另一者选自由-c(o)h、-ch=nr
j1
和组成的组;
[0275]ra1
是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
1-c6卤代烷基、3至6元杂环基或5至10元杂芳基或苯甲酰基,其中r
a1
的所述3至10元杂环基未被取代或被一个或多个独立地选自由c
1-c6烷基、c
3-c8环烷基、=o和
–
c(o)o-c
1-c6烷基组成的组的基团取代,并且r
a1
的所述5至10元杂芳基未被取代或被一个或多个独立地选自由c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基组成的组的基团取代;
[0276]rb1
、r
c1
、r
d1
和r
e1
各自独立地是h、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
1-c6卤代烷基、3至10元杂环基、5至10元杂芳基、苯甲酰基或苯乙烯基,其中r
b1
、r
c1
、r
d1
和r
e1
的所述3至10元杂环基和5至10元杂芳基各自独立地选自由c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基组成的组;
[0277]rf1
和r
g1
各自独立地是
–
oh、未被取代的5至6元杂芳基、
–
nr
m1rn1
、苯甲酰基或苯乙烯基;
[0278]rm1
是未被取代或被一个或多个选自c
1-c6烷基和卤基的基团取代的c
3-c8环烷基;
[0279]rn1
是h、c
1-c6烷基、c
2-c6烯基或c
2-c6炔基;
[0280]rj1
是c
1-c6烷基、5至6元杂环基、5至6元杂芳基、6至12元芳基、-or
k1
、-nhr
k1
、-n(c
1-c6烷基)r
k1
、-nhc(o)r
k1
、-nhs(o)2r
k1
或-nhc(nh)nhr
bb
,其中r
j1
的所述5至6元杂环基未被取代或被一个或多个选自由c
1-c6烷基、c
3-c8环烷基、=o、
–
c(o)nh-c
1-c6烷基和
–
c(o)o-c
1-c6烷基组成的组的取代基取代,并且r
j1
的所述5至6元杂芳基和6至12元芳基各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基组成的组的取代基取代;
[0281]rbb
是未被取代或被取代的c
1-c6烷基、未被取代或被取代的c
3-c8环烷基、未被取代或被取代的芳基、未被取代或被取代的杂环烷基或未被取代或被取代的杂芳基;
[0282]
每个r
k1
独立地是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中r
k1
的所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代;
[0283]r3a
是h、c
1-c6烷基、c
1-c6烷氧基或卤素,其中r
3a
的所述c
1-c6烷基和c
1-c6烷氧基各自独立地未被取代或被一个或多个卤素取代;
[0284]
指示环是饱和的,部分不饱和的,或完全不饱和的;
[0285]
y3是ch(x
1a-r
6a1
)、c(x
1a-r
6a1
)、n、n(x
1a-r
6a1
)、s或o;
[0286]
y4是ch(x
2a-r
6b1
)、c(x
2a-r
6b1
)、n、n(x
2a-r
6b1
)、s或o;
[0287]
y5是ch(x
3a-r
6c1
)、c(x
3a-r
6c1
)、n、n(x
3a-r
6c1
)、s或o;
[0288]
y6是ch(x
4a-r
6d1
)、c(x
4a-r
6d1
)、n、n(x
4a-r
6d1
)、s或o;
[0289]
y7是n、c或ch;并且
[0290]
y8是n、nh、c或ch;
[0291]
x
1a
、x
2a
、x
3a
和x
4a
各自独立地是不存在的,是各自独立地是不存在的,是
[0292]
m1是1-6;
[0293]r6a1
、r
6b1
、r
6c1
和r
6d1
各自独立地是氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
p1rq1
、c
6-c
12
芳基、3至10元杂环基、5至10元杂芳基、-c
1-c6烷基-5至6元杂环基、-oc(o)-5至6元杂环基、-c(o)r
h1
、-s(o)2nr
w1arw2a
、-s(o)2r
y1
、-nr
z1a
s(o)2r
z2a
或-n(ch3)ch2c(ch3)3,其中r
6a1
、r
6b1
、r
6c1
和r
6d1
的所述c
1-c6烷基和c
1-c6烷氧基各自独立地未被取代或被一个或多个选自由c
3-c8环烷基和卤素组成的组的基团取代;r
6a1
、r
6b1
、r
6c1
和r
6d1
的所述c
6-c
12
芳基和5至10元杂芳基各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、-oh和c
1-c6烷基-oh组成的组的基团取代;并且r
6a1
、r
6b1
、r
6c1
和r
6d1
的所述3至10元杂环基、-c
1-c6烷基-5至6元杂环基和-oc(o)-5至6元杂环基各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、-oh、c
1-c6烷基-oh、=o、=s、卤基、c
3-c8环烷基、-c(o)nh-c
3-c8环烷基、c
6-c
12
芳基和5至6元杂环基组成的组的基团取代;
[0294]
每个r
h1
独立地选自由h、c
1-c6烷基、c
1-c6烷氧基、c
3-c8环烷基和-nr
r1rs1
组成的组;
[0295]
每个r
p1
独立地是h或c
1-c6烷基;
[0296]
每个r
q1
独立地是c
2-c3烷基、-c(o)r
t1
、-c(o)or
u1
或-c(o)nr
v1
;
[0297]
每个r
r1
、r
s1
、r
w1a
和r
z1a
独立地选自h和c
1-c6烷基;并且
[0298]
每个r
t1
、r
u1
、r
v1
、r
w2a
、r
y1
和r
z2a
独立地选自h、c
1-c6烷基、未被取代或被取代的c
3-c8环烷基以及未被取代或被取代的杂环基;
[0299]
或
[0300]
y5是ch(x
3a-r
6c1
)或c(x
3a-r
6c1
),y6是ch(x
4a-r
6d1
)或c(x
4a-r
6d1
),并且r
6c1
和r
6d1
连同它们所连接的碳原子一起形成6元芳基、6元杂环基或6元杂芳基环;其中所述6元芳基、6元杂环基和6元杂芳基环各自独立地未被取代或被一个或多个选自由c
1-c6烷基和
–
c(o)o-c
1-c6烷基组成的组的基团取代;并且
[0301]
其中r
6a1
、r
6b1
、r
6c1
和r
6d1
中的至多一者是c
1-c6烷氧基或
–
oh。
[0302]
在式(b)的一些实施方案中,以下中的一项或多项适用:
[0303]
(1)当l是-c≡c-时,y1和y2各自是ch,r
1a
和r
2a
中的一者是-c(o)h、-ch2oh、-c(o)ch3或-nhc(o)ch3,并且r
3a
是h,不同于环己基、苯基、吡啶基或萘基,并且r
6c1
是氢、c
2-c3烷基、c
2-c5烷氧基、br、cl、i、-nr
p1rq1
、c
6-c
12
芳基、3至10元杂环基、5至10元杂芳基、-c
1-c6烷基-5至6元杂环基、-oc(o)-5至6元杂环基、-c(o)r
h1
、-s(o)2nr
w1arw2a
、-s(o)2r
y1
或-nr
z1a
s(o)2r
z2a
,并且每个r
h1
独立地选自由c
1-c6烷基、c
1-c6烷氧基、c
3-c8环烷基和-nr
r1rs1
组成的组;
[0304]
(2)当l是-c≡c-时,y1和y2各自是ch,r
1a
和r
2a
中的一者是-c(o)h,并且r
3a
是
–
ch3、t-bu或c
2-c3烷氧基,不同于苯基和吡啶基,r
b1
和r
d1
不同于并且r
6c1
不同于-oh;
[0305]
(3)当l是-c≡c-时,y1和y2各自是ch,r
1a
和r
2a
中的一者是哌啶基、吡咯烷基、吡咯烷酮、哌嗪基、吗啉基或噻二唑烷酮1,1-二氧化物,并且r
3a
是h,不同于萘基,并且r
6c1
不同于氟基;
[0306]
(4)当l是*-nhs(o)
2-或*-s(o)2nh-时,y1和y2各自是ch,r
1a
和r
2a
中的一者是-c(o)h、-ch=nr
j1
或并且r
3a
是h或br,不同于苯基,并且r
6a1
、r
6b1
、r
6c1
和r
6d1
各自独立地是氢、c
2-c6烷基、c
1-c6烷氧基、-oh、-nr
p1rq1
、c
6-c
12
芳基、3至10元杂环基、5至10元杂芳基、-c
1-c6烷基-5至6元杂环基、-oc(o)-5至6元杂环基、-c(o)r
h1
、-s(o)2nr
w1arw2a
、-s(o)2r
y1
或-nr
z1a
s(o)2r
z2a
;
c6烷基-oh组成的组的基团取代;并且r
6a1
、r
6b1
、r
6c1
和r
6d1
的所述3至10元杂环基、-c
1-c6烷基-5至6元杂环基和-oc(o)-5至6元杂环基各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、-oh、c
1-c6烷基-oh、=o和=s组成的组的基团取代。
[0312]
在一些实施方案中,式(b)化合物是式(b-1a)或(b-1b)化合物:
[0313][0314]
其中r
1a
、r
2a
、r
3a
、y1、y2、y3、y4、y5、y6、y7、y8和l如对于式(b)所定义。
[0315]
在一些实施方案中,式(b)化合物是式(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)或(b-2n)化合物:
[0316]
[0317]
[0318][0319]
其中r
1a
、r
2a
、r
3a
、y1、y2、y3、y4、y5、y6、y7和y8如对于式(b)所定义。
[0320]
在一些实施方案中,式(b)化合物是式(b-3a)、(b-3b)、(b-3c)、(b-3d)、(b-3e)、(b-3f)、(b-3g)、(b-3h)、(b-3i)、(b-3j)、(b-3k)、(b-3l)、(b-3m)或(b-3n)化合物:
[0321]
sr
a1
、-nr
a2ra3
、-no2、-c=nh(or
a1
)、-c(o)r
a1
、-oc(o)r
a1
、-c(o)or
a1
、-c(o)nr
a2ra3
、-oc(o)nr
a2ra3
、-nr
a1
c(o)r
a2
、-nr
a1
c(o)or
a2
、-nr
a1
c(o)nr
a2ra3
、-s(o)r
a1
、-s(o)2r
a1
、-nr
a1
s(o)r
a2
、-c(o)nr
a1
s(o)r
a2
、-nr
a1
s(o)2r
a2
、-c(o)nr
a1
s(o)2r
a2
、-s(o)nr
a2ra3
、-s(o)2nr
a2ra3
、-p(o)(or
a2
)(or
a3
)、c
3-c8环烷基、3-12元杂环基、5至10元杂芳基、c
6-c
14
芳基、-(c
1-c3亚烷基)cn、-(c
1-c3亚烷基)or
a1
、-(c
1-c3亚烷基)sr
a1
、-(c
1-c3亚烷基)nr
a2ra3
、-(c
1-c3亚烷基)cf3、-(c
1-c3亚烷基)no2、-c=nh(or
a1
)、-(c
1-c3亚烷基)c(o)r
a1
、-(c
1-c3亚烷基)oc(o)r
a1
、-(c
1-c3亚烷基)c(o)or
a1
、-(c
1-c3亚烷基)c(o)nr
a2ra3
、-(c
1-c3亚烷基)oc(o)nr
a2ra3
、-(c
1-c3亚烷基)nr
a1
c(o)r
a2
、-(c
1-c3亚烷基)nr
a1
c(o)or
a2
、-(c
1-c3亚烷基)nr
a1
c(o)nr
a2ra3
、-(c
1-c3亚烷基)s(o)r
a1
、-(c
1-c3亚烷基)s(o)2r
a1
、-(c
1-c3亚烷基)nr
a1
s(o)r
a2
、-c(o)(c
1-c3亚烷基)nr
a1
s(o)r
a2
、-(c
1-c3亚烷基)nr
a1
s(o)2r
a2
、-(c
1-c3亚烷基)c(o)nr
a1
s(o)2r
a2
、-(c
1-c3亚烷基)s(o)nr
a2ra3
、-(c
1-c3亚烷基)s(o)2nr
a2ra3
、-(c
1-c3亚烷基)p(o)(or
a2
)(or
a3
)、-(c
1-c3亚烷基)(c
3-c8环烷基)、-(c
1-c3亚烷基)(3-12元杂环基)、-(c
1-c3亚烷基)(5-10元杂芳基)和-(c
1-c3亚烷基)(c
6-c
14
芳基),其中所述一个或多个取代基各自独立地未被取代或被一个或多个选自由以下组成的组的其他取代基取代:卤素、氧代基、-or
a4
、-nr
a4ra5
、-c(o)r
a4
、-cn、-s(o)r
a4
、-s(o)2r
a4
、-p(o)(or
a4
)(or
a5
)、-(c
1-c3亚烷基)or
a4
、-(c
1-c3亚烷基)nr
a4ra5
、-(c
1-c3亚烷基)c(o)r
a4
、-(c
1-c3亚烷基)s(o)r
a4
、-(c
1-c3亚烷基)s(o)2r
a4
、-(c
1-c3亚烷基)p(o)(or
a4
)(or
a5
)、c
3-c8环烷基、c
1-c6烷基以及被氧代基、-oh或卤素取代的c
1-c6烷基;其中每个r
a1
独立地是氢、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基、c
6-c
14
芳基、5-6元杂芳基或3-6元杂环基,其中所述c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基、c
6-c
14
芳基、5-6元杂芳基和3-6元杂环基独立地未被取代或被卤素、氧代基、-cn、-or
a6
、-nr
a6ra7
、-p(o)(or
a6
)(or
a6
)、苯基、被卤素取代的苯基、c
1-c6烷基或被卤素、-oh或氧代基取代的c
1-c6烷基取代;r
a2
和r
a3
各自独立地是氢、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基、c
6-c
14
芳基、5-6元杂芳基或3-6元杂环基,其中所述c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基、c
6-c
14
芳基、5-6元杂芳基和3-6元杂环基各自独立地未被取代或被卤素、氧代基、-cn、-or
a6
、-nr
a6ra7
、c
1-c6烷基或被卤素、-oh或氧代基取代的c
1-c6烷基取代;并且r
a4
、r
a5
、r
a6
和r
a7
各自独立地是氢、c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、被一个或多个卤素取代的c
1-c6烷基、被一个或多个卤素取代的c
2-c6烯基、或被一个或多个卤素取代的c
2-c6炔基。
[0325]
在式(b),包括式(b-1a)和(b-1b)的一些实施方案中,l是-c≡c-。在一些实施方案中,l是*-nhc(o)-,其中*代表与y7的连接点。在一些实施方案中,l是*-c(o)nh-,其中*代表与y7的连接点。在一些实施方案中,l是-nhc(o)nh-。在一些实施方案中,l是*-nhs(o)
2-,其中*代表与y7的连接点。在一些实施方案中,l是*-nhs(o)(=nh)-,其中*代表与y7的连接点。在一些实施方案中,l是*-s(o)(=nh)nh-,其中*代表与y7的连接点。在一些实施方案中,l是*-s(o)2nh-,其中*代表与y7的连接点。在一些实施方案中,l是*-s(o)nhnh-,其中*代表与y7的连接点。在一些实施方案中,l是*-nhnhs(o)-,其中*代表与y7的连接点。在一些实施方案中,l是*-c(o)nhnh-,其中*代表与y7的连接点。在一些实施方案中,l是*-nhnhc(o)-,其中*代表与y7的连接点。在一些实施方案中,l是*
–
nhc(o)o-,其中*代表与y7的连接点。在一些实施方案中,l是*
–
oc(o)nh-,其中*代表与y7的连接点。
[0326]
在式(b),包括式(b-1a)和(b-1b)的一些实施方案中,l是-c≡c-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-c(o)r
a1
。在一些实施方案中,l是-c≡c-,并且r
1a
和r
2a
中的一
者是
–
oh,并且另一者是-c(o)h。在一些实施方案中,l是-c≡c-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
。在一些实施方案中,l是-c≡c-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-s(o)r
b1
或-s(o)2r
c1
。在一些实施方案中,l是-c≡c-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-nhc(o)r
d1
或-nhs(o)2r
e1
。在一些实施方案中,l是-c≡c-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-c
1-c6烷基-r
f1
或-c
2-c6烯基-r
g1
。在一些实施方案中,l是-c≡c-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-c(o)h。在一些实施方案中,l是-c≡c-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
。在一些实施方案中,l是-c≡c-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是c
1-c6烷基。在一些实施方案中,l是-c≡c-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的5至6元杂环基:c
1-c6烷基、c
3-c8环烷基、=o、
–
c(o)nh-c
1-c6烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,l是-c≡c-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的5至6元杂芳基:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在其他实施方案中,l是-c≡c-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的6至12元芳基:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,l是-c≡c-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-or
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在一些实施方案中,l是-c≡c-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhr
k1
或-n(c
1-c6烷基)r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在一些实施方案中,l是-c≡c-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc(o)r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在其他实施方案中,l是-c≡c-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhs(o)2r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在其他实施方案中,l是-c≡c-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc(nh)nh2。在其他实施方案中,l是-c≡c-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是
[0327]
在式(b),包括式(b-1a)和(b-1b)的一些实施方案中,l是*-nhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-c(o)h。在一些实施方案中,l是*-nhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
。在一些实施方案中,l是*-nhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是c
1-c6烷基。在一些实施方案中,l是*-nhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的5至6元杂环基:c
1-c6烷基、c
3-c8环烷基、=o、
–
c(o)nh-c
1-c6烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,l是*-nhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的5至6元杂芳基:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在其他实施方案
中,l是*-nhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的6至12元芳基:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,l是*-nhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-or
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在一些实施方案中,l是*-nhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhr
k1
或-n(c
1-c6烷基)r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在一些实施方案中,l是*-nhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc(o)r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在其他实施方案中,l是*-nhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhs(o)2r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在其他实施方案中,l是*-nhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc(nh)nh2。在其他实施方案中,l是*-nhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是
[0328]
在式(b),包括式(b-1a)和(b-1b)的一些实施方案中,l是*-c(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-c(o)h。在一些实施方案中,l是*-c(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
。在一些实施方案中,l是*-c(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是c
1-c6烷基。在一些实施方案中,l是*-c(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的5至6元杂环基:c
1-c6烷基、c
3-c8环烷基、=o、
–
c(o)nh-c
1-c6烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,l是*-c(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的5至6元杂芳基:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在其他实施方案中,l是*-c(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的6至12元芳基:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,l是*-c(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-or
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在一些实施方案中,l是*-c(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhr
k1
或-n(c
1-c6烷基)r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在一些实施方案中,l是*-c(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc(o)r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在其他实施方案中,l是*-c(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhs(o)2r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取
代或被5至6元杂环基或5至6元杂芳基取代。在其他实施方案中,l是*-c(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc(nh)nh2。在其他实施方案中,l是*-c(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是
[0329]
在式(b),包括式(b-1a)和(b-1b)的一些实施方案中,l是-nhc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-c(o)h。在一些实施方案中,l是-nhc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
。在一些实施方案中,l是-nhc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是c
1-c6烷基。在一些实施方案中,l是-nhc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的5至6元杂环基:c
1-c6烷基、c
3-c8环烷基、=o、
–
c(o)nh-c
1-c6烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,l是-nhc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的5至6元杂芳基:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在其他实施方案中,l是-nhc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的6至12元芳基:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,l是-nhc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-or
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在一些实施方案中,l是-nhc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhr
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在一些实施方案中,l是-nhc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc(o)r
k1
或-n(c
1-c6烷基)r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在其他实施方案中,l是-nhc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhs(o)2r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在其他实施方案中,l是-nhc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc(nh)nh2。在其他实施方案中,l是-nhc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是
[0330]
在式(b),包括式(b-1a)和(b-1b)的一些实施方案中,l是*-nhs(o)
2-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-c(o)h。在一些实施方案中,l是*-nhs(o)
2-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
。在一些实施方案中,l是*-nhs(o)
2-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是c
1-c6烷基。在一些实施方案中,l是*-nhs(o)
2-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的5至6元杂环基:c
1-c6烷基、c
3-c8环烷基、=o、
–
c(o)nh-c
1-c6烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,l是*-nhs(o)
2-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成
的组的取代基取代的5至6元杂芳基:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在其他实施方案中,l是*-nhs(o)
2-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的6至12元芳基:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,l是*-nhs(o)
2-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-or
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在一些实施方案中,l是*-nhs(o)
2-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhr
k1
或-n(c
1-c6烷基)r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在一些实施方案中,l是*-nhs(o)
2-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc(o)r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在其他实施方案中,l是*-nhs(o)
2-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhs(o)2r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在其他实施方案中,l是*-nhs(o)
2-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc(nh)nh2。在其他实施方案中,l是*-nhs(o)
2-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是
[0331]
在式(b),包括式(b-1a)和(b-1b)的一些实施方案中,l是*-nhs(o)(=nh)-或*-s(o)(=nh)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-c(o)h。在一些实施方案中,l是*-nhs(o)(=nh)-或*-s(o)(=nh)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
。在一些实施方案中,l是*-nhs(o)(=nh)-或*-s(o)(=nh)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是c
1-c6烷基。在一些实施方案中,l是*-nhs(o)(=nh)-或*-s(o)(=nh)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的5至6元杂环基:c
1-c6烷基、c
3-c8环烷基、=o、
–
c(o)nh-c
1-c6烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,l是*-nhs(o)(=nh)-或*-s(o)(=nh)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的5至6元杂芳基:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在其他实施方案中,l是*-nhs(o)(=nh)-或*-s(o)(=nh)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的6至12元芳基:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,l是*-nhs(o)(=nh)-或*-s(o)(=nh)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-or
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在一些实施方案中,l是*-nhs(o)(=nh)-或*-s(o)(=nh)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhr
k1
或-n(c
1-c6烷基)r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在一些实施方案中,l是*-nhs(o)(=nh)-或*-s(o)(=nh)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc(o)r
k1
,其中r
k1
是c1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在其他实施方案中,l是*-nhs(o)(=nh)-或*-s(o)(=nh)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhs(o)2r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在其他实施方案中,l是*-nhs(o)(=nh)-或*-s(o)(=nh)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc(nh)nh2。在其他实施方案中,l是*-nhs(o)
2-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是
[0332]
在式(b),包括式(b-1a)和(b-1b)的一些实施方案中,l是*-s(o)2nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-c(o)h。在一些实施方案中,l是*-s(o)2nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
。在一些实施方案中,l是*-s(o)2nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是c
1-c6烷基。在一些实施方案中,l是*-s(o)2nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的5至6元杂环基:c
1-c6烷基、c
3-c8环烷基、=o、
–
c(o)nh-c
1-c6烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,l是*-s(o)2nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的5至6元杂芳基:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在其他实施方案中,l是*-s(o)2nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的6至12元芳基:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,l是*-s(o)2nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-or
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在一些实施方案中,l是*-s(o)2nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhr
k1
或-n(c
1-c6烷基)r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在一些实施方案中,l是*-s(o)2nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc(o)r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在其他实施方案中,l是*-s(o)2nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhs(o)2r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在其他实施方案中,l是*-s(o)2nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc(nh)nh2。在其他实施方案中,l是*-s(o)2nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是
[0333]
在式(b),包括式(b-1a)和(b-1b)的一些实施方案中,l是*-s(o)nhnh-或*-nhnhs(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-c(o)h。在一些实施方案中,l是*-s(o)nhnh-或*-nhnhs(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
。在一些实施方案
中,l是*-s(o)nhnh-或*-nhnhs(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是c
1-c6烷基。在一些实施方案中,l是*-s(o)nhnh-或*-nhnhs(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的5至6元杂环基:c
1-c6烷基、c
3-c8环烷基、=o、
–
c(o)nh-c
1-c6烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,l是*-s(o)nhnh-或*-nhnhs(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的5至6元杂芳基:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在其他实施方案中,l是*-s(o)nhnh-或*-nhnhs(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的6至12元芳基:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,l是*-s(o)nhnh-或*-nhnhs(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-or
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在一些实施方案中,l是*-s(o)nhnh-或*-nhnhs(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhr
k1
或-n(c
1-c6烷基)r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在一些实施方案中,l是*-s(o)nhnh-或*-nhnhs(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc(o)r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在其他实施方案中,l是*-s(o)nhnh-或*-nhnhs(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhs(o)2r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在其他实施方案中,l是*-s(o)nhnh-或*-nhnhs(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc(nh)nh2。在其他实施方案中,l是*-s(o)nhnh-或*-nhnhs(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是
[0334]
在式(b),包括式(b-1a)和(b-1b)的一些实施方案中,l是*-c(o)nhnh-或*-nhnhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-c(o)h。在一些实施方案中,l是*-c(o)nhnh-或*-nhnhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
。在一些实施方案中,l是*-c(o)nhnh-或*-nhnhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是c
1-c6烷基。在一些实施方案中,l是*-c(o)nhnh-或*-nhnhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的5至6元杂环基:c
1-c6烷基、c
3-c8环烷基、=o、
–
c(o)nh-c
1-c6烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,l是*-c(o)nhnh-或*-nhnhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的5至6元杂芳基:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在其他实施方案中,l是*-c(o)nhnh-或*-nhnhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的6至12元芳基:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,l是*-c(o)nhnh-或*-nhnhc(o)-,并
且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-or
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在一些实施方案中,l是*-c(o)nhnh-或*-nhnhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhr
k1
或-n(c
1-c6烷基)r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在一些实施方案中,l是*-c(o)nhnh-或*-nhnhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc(o)r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在其他实施方案中,l是*-c(o)nhnh-或*-nhnhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhs(o)2r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在其他实施方案中,l是*-c(o)nhnh-或*-nhnhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc(nh)nh2。在其他实施方案中,l是*-c(o)nhnh-或*-nhnhc(o)-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是
[0335]
在式(b),包括式(b-1a)和(b-1b)的一些实施方案中,l是*-nhc(o)o-或*
–
oc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-c(o)h。在一些实施方案中,l是*-nhc(o)o-或*
–
oc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
。在一些实施方案中,l是*-nhc(o)o-或*
–
oc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是c
1-c6烷基。在一些实施方案中,l是*-nhc(o)o-或*
–
oc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的5至6元杂环基:c
1-c6烷基、c
3-c8环烷基、=o、
–
c(o)nh-c
1-c6烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,l是*-nhc(o)o-或*
–
oc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的5至6元杂芳基:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在其他实施方案中,l是*-nhc(o)o-或*
–
oc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代或被一个或多个选自由以下组成的组的取代基取代的6至12元芳基:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,l是*-nhc(o)o-或*
–
oc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-or
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在一些实施方案中,l是*-nhc(o)o-或*
–
oc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhr
k1
或-n(c
1-c6烷基)r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在一些实施方案中,l是*-nhc(o)o-或*
–
oc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc(o)r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c
2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在其他实施方案中,l是*-nhc(o)o-或*
–
oc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhs(o)2r
k1
,其中r
k1
是c
1-c6烷基、c
2-c6烯基、c2-c6炔基、c
3-c8环烷基或6至12元芳基,其中所述c
1-c6烷基未被取代或被5至6元杂环基或5至6元杂芳基取代。在其他实施方案中,l是*-nhc(o)o-或*
–
oc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc(nh)nh2。在其他实施方案中,l是*-nhc(o)o-或*
–
oc(o)nh-,并且r
1a
和r
2a
中的一者是
–
oh,并且另一者是
[0336]
在任何前述实施方案中的一些中,r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是5至6元杂环基,其中r
j1
的所述5至6元杂环基未被取代或被一个或多个选自由以下组成的组的取代基取代:c
1-c6烷基、c
3-c8环烷基、=o、
–
c(o)nh-c
1-c6烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,r
j1
选自由以下组成的组:吡咯烷基、吡唑烷基、咪唑烷基、四氢呋喃基、1,3-二氧杂环戊烷基、四氢噻吩基、氧硫杂环戊烷基、环丁砜基、哌啶基、哌嗪基、四氢吡喃基、二氧杂环己烷基、硫杂环己烷基、二硫杂环己烷基、三硫杂环己烷基、吗啉基和硫代吗啉基,各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
3-c8环烷基、=o、
–
c(o)nh-c
1-c6烷基和
–
c(o)o-c
1-c6烷基组成的组的取代基取代。在一些实施方案中,r
j1
是5至6元杂环基,其中所述杂环基的一个或多个氮和/或硫原子任选地被氧化以提供n-氧化物、-s(o)-或
–
so
2-部分。在任何前述实施方案中的一些中,r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是5至6元杂芳基,其中r
j1
的所述5至6元杂芳基未被取代或被一个或多个选自由以下组成的组的取代基取代:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,r
j1
选自由以下组成的组:吡咯基、吡唑基、咪唑基、三唑基、四唑基、呋喃基、异噁唑基、噁唑基、噁二唑基、噻吩基、异噻唑基、噻唑基、噻二唑基、吡啶基、哒嗪基、嘧啶基、吡嗪基、三嗪基和四嗪基,各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基组成的组的取代基取代。在任何前述实施方案中的一些中,r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是6至12元芳基,其中r
j1
的所述6至12元芳基未被取代或被一个或多个选自由以下组成的组的取代基取代:c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基。在一些实施方案中,r
j1
选自由以下组成的组:苯基和萘基,各自独立地未被取代或被一个或多个选自由c
1-c6烷基、c
3-c8环烷基和
–
c(o)o-c
1-c6烷基组成的组的取代基取代。在任何前述实施方案中的一些中,r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是未被取代的-oc
1-c6烷基或被5至6元杂环基或5至6元杂芳基取代的-oc
1-c6烷基。在任何前述实施方案中的一些中,r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-oc
2-c6烯基或-oc
2-c6炔基。在一些实施方案中,r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-oc
3-c8环烷基或
–
o-6至12元芳基。在任何前述实施方案中的一些中,r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc
1-c6烷基、
–
nhc(o)c
1-c6烷基或
–
nhs(o)2c
1-c6烷基,各自未被取代或被5至6元杂环基或5至6元杂芳基取代。在任何前述实施方案中的一些中,r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc
2-c6烯基、-nhc
2-c6炔基、-nhc(o)c
2-c6烯基、-nhc(o)c
2-c6炔基、-nhs(o)2c
2-c6烯基或-nhs(o)2c
2-c6炔基。在一些实施方案中,r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc
3-c8环烷基、
–
nh-6至12元芳基、-nhc(o)c
3-c8环烷基、
–
nhc(o)-6至12元芳基、-nhs(o)2c
3-c8环烷基或
–
nhs(o)
2-6至12元芳基。在任何前述实施方案中的一些中,r
1a
和r
2a
中的一者是
–
oh,并且另一者是-chnr
j1
,其中r
j1
是-nhc(nh)nh2。在一些实施方案中,r
1a
和r
2a
中的一者是
–
oh,并且另一者是
–
ch=nr
j1
,其中r
j1
是-nhc(nh)nhr
bb
。在一些实施方案中,r
bb
是未被取代或被取
2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)、(b-2n)、(b-3a)、(b-3b)、(b-3c)、(b-3d)、(b-3e)、(b-3f)、(b-3g)、(b-3h)、(b-3i)、(b-3j)、(b-3k)、(b-3l)、(b-3m)和(b-3n)的一些实施方案中,r
1a
和r
2a
中的一者是
–
oh,并且另一者是-c(o)h。在一些实施方案中,r
1a
是
–
oh,r
2a
是-c(o)h,并且r
3a
是h。在一些实施方案中,r
1a
是
–
oh,r
2a
是-c(o)h,并且r
3a
是未被取代的c
1-c6烷基。在一些实施方案中,r
1a
是
–
oh,r
2a
是-c(o)h,并且r
3a
是c
1-c6卤代烷基。在一些实施方案中,r
1a
是
–
oh,r
2a
是-c(o)h,并且r
3a
是未被取代的c
1-c6烷氧基。在一些实施方案中,r
1a
是
–
oh,r
2a
是-c(o)h,并且r
3a
是被一个或多个卤素取代的c
1-c6烷氧基。在其他实施方案中,r
1a
是
–
oh,r
2a
是-c(o)h,并且r
3a
是卤素。在某些实施方案中,r
1a
是
–
oh,r
2a
是-c(o)h,并且r
3a
是氟基。在某些实施方案中,r
1a
是
–
oh,r
2a
是-c(o)h,并且r
3a
是甲基。在一些实施方案中,r
1a
是
–
oh,r
2a
是-c(o)h,并且r
3a
是甲氧基。在一些实施方案中,r
2a
是
–
oh,r
1a
是-c(o)h,并且r
3a
是h。在一些实施方案中,r
2a
是
–
oh,r
1a
是-c(o)h,并且r
3a
是未被取代的c
1-c6烷基。在一些实施方案中,r
2a
是
–
oh,r
1a
是-c(o)h,并且r
3a
是c
1-c6卤代烷基。在一些实施方案中,r
2a
是
–
oh,r
1a
是-c(o)h,并且r
3a
是未被取代的c
1-c6烷氧基。在一些实施方案中,r
2a
是
–
oh,r
1a
是-c(o)h,并且r
3a
是被一个或多个卤素取代的c
1-c6烷氧基。在其他实施方案中,r
2a
是
–
oh,r
1a
是-c(o)h,并且r
3a
是卤素。在某些实施方案中,r
2a
是
–
oh,r
1a
是-c(o)h,并且r
3a
是氟基。在某些实施方案中,r
2a
是
–
oh,r
1a
是-c(o)h,并且r
3a
是甲基。在一些实施方案中,r
2a
是
–
oh,r
1a
是-c(o)h,并且r
3a
是甲氧基。
[0342]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)和(b-2n)的一些实施方案中,y1和y2各自独立地是cr
x
,其中r
x
是h或卤素。在一些实施方案中,y1和y2各自独立地是ch、cf、ccl或cbr。在一些实施方案中,y1和y2各自是ch。在一特定实施方案中,y1是cf,并且y2是ch。在另一实施方案中,y1是ch,并且y2是cf。在一些实施方案中,y1是cr
x
,并且y2是n。举例来说,在一些实施方案中,y1是ch、cf、ccl或cbr,并且y2是n。在一些实施方案中,y1是n,并且y2是cr
x
。举例来说,在一些实施方案中,y1是n,并且y2是ch、cf、ccl或cbr。在其他实施方案中,y1和y2各自是n。
[0343]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)和(b-2n)的一些实施方案中,携带的环是饱和的,以致环完全由单键组成。饱和环的实例包括但不限于的环是饱和的,以致环完全由单键组成。饱和环的实例包括但不限于的环是饱和的,以致环完全由单键组成。饱和环的实例包括但不限于在一些实施方案中,携带的环是部分不饱和的,以致环是非芳族的,并且包含至少一个双键,诸如一个或两个双键。部分不饱和环的实例包
括但不限于括但不限于括但不限于在其他实施方案中,携带的环是完全不饱和的,并且包含两个或三个双键。在某些实施方案中,携带的环是完全不饱和的。在某些实施方案中,携带的环是完全不饱和的和芳族的。完全不饱和环的实例包括但不限于饱和的和芳族的。完全不饱和环的实例包括但不限于
[0344]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)和(b-2n)的一些实施方案中,y3是ch(x
1a-r
6a1
)或c(x
1a-r
6a1
),y4是ch(x
2a-r
6b1
)或c(x
2a-r
6b1
),y5是ch(x
3a-r
6c1
)或c(x
3a-r
6c1
),y6是ch(x
4a-r
6d1
)或c(x
4a-r
6d1
),并且携带的环是部分不饱和的。在一些实施方案中,y3是c(x
1a-r
6a1
),y4是c(x
2a-r
6b1
),y5是c(x
3a-r
6c1
),y6是c(x
4a-r
6d1
),并且携带的环是完全不饱和的。在一些实施方案中,y3是ch(x
1a-r
6a1
),y4是ch(x
2a-r
6b1
),y5是ch(x
3a-r
6c1
),y6是ch(x
4a-r
6d1
),并且携带的环是饱和的。在其他实施方案中,y3是ch(x
1a-r
6a1
)或c(x
1a-r
6a1
),y4是ch(x
2a-r
6b1
)或c(x
2a-r
6b1
),y5是ch(x
3a-r
6c1
)或c(x
3a-r
6c1
),并且y6是不存在的。
[0345]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)和(b-2n)的一些实施方案中,y3是ch(x
1a-r
6a1
)或c(x
1a-r
6a1
),y4是n或n(x
2a-r
6b1
),y5是ch(x
3a-r
6c1
)或c(x
3a-r
6c1
),y6是ch(x
4a-r
6d1
)或c(x
4a-r
6d1
),并且携带的环是部分不饱和的。在一些实施方案中,y3是c(x
1a-r
6a1
),y4是n,y5是c(x
3a-r
6c1
),y6是c(x
4a-r
6d1
),并且携带的环是完全不饱和的。在一些实施方案中,y3是ch(x
1a-r
6a1
),y4是n(x
2a-r
6b1
),y5是ch(x
3a-r
6c1
),y6是ch(x
4a-r
6d1
),并且携带的环是饱和的。在其他实施方案中,y3是ch(x
1a-r
6a1
)或c(x
1a-r
6a1
),y4是n或n(x
2a-r
6b1
),y5是ch(x
3a-r
6c1
)或c(x
3a-r
6c1
),并且y6是不存在的。
[0346]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)和(b-2n)的一些实施方案中,y3是n或n(x
1a-r
6a1
),y4是ch(x
2a-r
6b1
)或c(x
2a-r
6b1
),y5是ch(x
3a-r
6c1
)或c(x
3a-r
6c1
),y6是ch(x
4a-r
6d1
)或c(x
4a-r
6d1
),并且携带的环是部分不饱和的。在一些实施方案中,y3是n,y4是c(x
2a-r
6b1
),y5是c(x
3a-r
6c1
),y6是c(x
4a-r
6d1
),并且携带的环是完全不饱和的。在一些实施方案中,y3是n(x
1a-r
6a1
),y4是ch(x
2a-r
6b1
),y5是ch(x
3a-r
6c1
),y6是ch(x
4a-r
6d1
),并且携带的环是饱和的。在其他实施方案中,y3是n或n(x
1a-r
6a1
),y4是ch(x
2a-r
6b1
)或c(x
2a-r
6b1
),y5是ch(x
3a-r
6c1
)或c(x
3a-r
6c1
),并且y6是不存在的。
[0347]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)和(b-2n)的一些实施方案中,y3是ch(x
1a-r
6a1
)或c(x
1a-r
6a1
),y4是ch(x
2a-r
6b1
)或c(x
2a-r
6b1
),y5是n或n(x
3a-r
6c1
),y6是ch(x
4a-r
6d1
)或c(x
4a-r
6d1
),并且携带的环是部分不饱和的。在一些实施方案中,y3是c(x
1a-r
6a1
),y4是c(x
2a-r
6b1
),y5是n,y6是c(x
4a-r
6d1
),并且携带的环是完全不饱和的。在一些实施方案中,y3是ch(x
1a-r
6a1
),y4是ch(x
2a-r
6b1
),y5是n(x
3a-r
6c1
),y6是ch(x
4a-r
6d1
),并且携带的环是饱和的。在其他实施方案中,y3是ch(x
1a-r
6a1
)或c(x
1a-r
6a1
),y4是ch(x
2a-r
6b1
)或c(x
2a-r
6b1
),y5是n或n(x
3a-r
6c1
),并且y6是不存在的。
[0348]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)和(b-2n)的其他实施方案中,y3是n或n(x
1a-r
6a1
),y4是ch(x
2a-r
6b1
)或c(x
2a-r
6b1
),y5是n或n(x
1a-r
6c1
),y6是ch(x
4a-r
6d1
)或c(x
4a-r
6d1
),并且携带的环是部分不饱和的。在一些实施方案中,y3是n,y4是c(x
2a-r
6b1
),y5是n,y6是c(x
4a-r
6d1
),并且携带的环是完全不饱和的。在一些实施方案中,y3是n(x
1a-r
6a1
),y4是ch(x
2a-r
6b1
),y5是n(x
1a-r
6c1
),y6是ch(x
4a-r
6d1
),并且携带的环是饱和的。在其他实施方案中,y3是n或n(x
1a-r
6a1
),y4是ch(x
2a-r
6b1
)或c(x
2a-r
6b1
),y5是n或n(x
1a-r
6c1
),并且y6是不存在的。
[0349]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)和(b-2n)的某些实施方案中,r4和r5一起形成
–
s-,y3是ch(x
1a-r
6a1
),y4是n(x
2a-r
6b1
),y5是ch(x
1a-r
6a1
),y6是ch(x
1a-r
6a1
),并且携带的环是饱和环。在某些实施方案中,r4和r5一起形成
–
s-,y3、y5和y6各自是ch2,y4是n(x
2a-r
6b1
),并且携带的环是饱和环。
[0350]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)和(b-2n)的一些实施方案中,y3是ch(x
1a-r
6a1
)或c(x
1a-r
6a1
),其中x
1a
是不存在的。在一些实施方案中,y3是ch(x
1a-r
6a1
)或c(x
1a-r
6a1
),其中x
1a
是并且m1是1-6。在一些实施方案中,y3是n。在其他实施方案中,y3是n(x
1a-r
6a1
),其中x
1a
是不存在的。在一些实施方案中,y3是n(x
1a-r
6a1
),其中x
1a
是并且m1是1-6。在一些实施方案中,y3是s。在其他实施方案中,y3是o。在一些实施方案中,y3是ch(x
1a-r
6a1
)或c(x
1a-r
6a1
);x
1a
是不存在的,是m1是1-6;r
6a1
是氢、c
1-c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基或5至10元杂芳基。在一些实施方案中,y3是n或n(x
1a-r
6a1
);x
1a
是不存在的,是m1是1-6;并且r
6a1
是氢、c
1-c6烷基、c
1-c6卤代烷基、卤基、c6-c
12
芳基、3至10元杂环基或5至10元杂芳基。
[0351]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)、(b-2n)、(b-3a)、(b-3b)、(b-3c)、(b-3d)、(b-3e)、(b-3f)、(b-3g)、(b-3h)、(b-3i)、(b-3j)、(b-3k)、(b-3l)、(b-3m)和(b-3n)的一些实施方案中,y4是ch(x
2a-r
6b1
)或c(x
2a-r
6b1
),其中x
2a
是不存在的。在一些实施方案中,y4是ch(x
2a-r
6b1
)或c(x
2a-r
6b1
),其中x
2a
是是并且m1是1-6。在一些实施方案中,y4是n。在其他实施方案中,y4是n(x
2a-r
6b1
),其中x
2a
是不存在的。在一些实施方案中,y4是n(x
2a-r
6b1
),其中x
2a
是并且m1是1-6。在一些实施方案中,y4是s。在其他实施方案中,y4是o。在一些实施方案中,y4是ch(x
2a-r
6b1
)或c(x
2a-r
6b1
);x
2a
是不存在的,是m1是1-6;并且r
6b1
是氢、c
1-c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基或5至10元杂芳基。在一些实施方案中,y4是n或n(x
2a-r
6b1
);x
2a
是不存在的,是m1是1-6;并且r
6b1
是氢、c
1-c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基或5至10元杂芳基。
[0352]
在一些实施方案中,y5是ch(x
3a-r
6c1
)或c(x
3a-r
6c1
),其中x
3a
是不存在的。在一些实施方案中,y5是ch(x
3a-r
6c1
)或c(x
3a-r
6c1
),其中x
3a
是并且m1是1-6。在一些实施方案中,y5是n。在其他实施方案中,y5是n(x
3a-r
6c1
),其中x
3a
是不存在的。在一些实施方案中,y5是n(x
3a-r
6c1
),其中x
3a
是并且m1是1-6。在一些实施方案中,y5是s。在其他实施方案中,y5是o。在一些实施方案中,y5是ch(x
3a-r
6c1
)或c(x
3a-r
6c1
);x
3a
是不存在的,是m1是1-6;并且r
6c1
是氢、c
1-c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基或5至10元杂芳基。在一些实施方案中,y5是n或n(x
3a-r
6c1
);x
3a
是不存在的,是m1是1-6;并且r
6c1
是氢、c
1-c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基或5至10元杂芳基。
[0353]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)和(b-2n)的一些实施方案中,y3、y4、y5和y6中的一者是s或o。在一些实施方案中,y3、y4和y5中的一者是s或o。在一些实施方案中,y3是s。在一些实施方案中,y3是o。在一些实施方案中,y4是s。在一些实施方案中,y4是o。在一些实施方案中,y5是s。在一些实施方案中,y5是o。在一些实施方案中,y6是s。在一
些实施方案中,y6是o。
[0354]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)和(b-2n)的一些实施方案中,y3、y4、y5、y6、y7和y8中的一者是n。在一些实施方案中,y3、y4、y5、y6、y7和y8中的两者是n。在其他实施方案中,y3、y4、y5、y6、y7和y8中的三者是n。
[0355]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)和(b-2n)的一些实施方案中,y6是ch(x
4a-r
6d1
)或c(x
4a-r
6d1
),其中x
4a
是不存在的。在一些实施方案中,y6是ch(x
4a-r
6d1
)或c(x
4a-r
6d1
),其中x
4a
是并且m1是1-6。在一些实施方案中,y6是n。在其他实施方案中,y6是n(x
4a-r
6d1
),其中x
4a
是不存在的。在一些实施方案中,y6是n(x
4a-r
6d1
),其中x
4a
是并且m1是1-6。在一些实施方案中,y6是s。在其他实施方案中,y6是o。在一些实施方案中,y6是ch(x
4a-r
6d1
)或c(x
4a-r
6d1
);x
4a
是不存在的,是是不存在的,是m1是1-6;并且r
6d1
是氢、c
1-c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基或5至10元杂芳基。在一些实施方案中,y6是n或n(x
4a-r
6d1
);x
4a
是不存在的,是存在的,是m1是1-6;并且r
6d1
是氢、c
1-c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基或5至10元杂芳基。
[0356]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)和(b-2n)的一些实施方案中,y5是ch(x
3a-r
6c1
),y6是ch(x
4a-r
6d1
),环是饱和的,并且r
6c1
和r
6d1
连同它们所连接的碳原子一起形成6元杂环基环;其中所述杂环基环未被取代或被一个或多个选自由c
1-c6烷基和
–
c(o)o-c
1-c6烷基组成的组的基团取代。在一些实施方案中,y5是c(x
3a-r
6c1
),y6是c(x
4a-r
6d1
),是部分不饱和的或完全不饱和的,并且r
6c1
和r
6d1
连同它们所连接的碳原子一起形成6元芳基、6元杂环基或6元杂芳基环;其中所述6元芳基、6元杂环基和6元杂芳基环各自独立地未被取代或被一个或多个选自由c
1-c6烷基和
–
c(o)o-c
1-c6烷基组成的组的基团取代。在一些实施方案中,y5是c(x
3a-r
6c1
),y6是c(x
4a-r
6d1
),是完全不饱和的,并且r
6c1
和r
6d1
连同它们所连接的碳原子一起形成6元芳基、6元杂环基或6元杂芳基环;其中所述6元芳基、6元杂环基和6元杂芳基环各自独立地未被取代或被一个或多个选自由c
1-c6烷基和
–
c(o)o-c
1-c6烷基组成的组的基团取代。在一些实施方案中,r
6c1
和r
6d1
连同它们所连接的碳原子一起形成苯基环。在一些实施方案中,r
6c1
和r
6d1
连同它们所连接的碳原子一起形成6元杂环基或6元杂芳基环,其中所述6元杂环基或6元杂芳基环各自含有一个、两个或三个独立地选自由n、s和o组成的组的杂原子。在一些实施方案中,r
6c1
和r
6d1
连同它们所连接的碳原子一起形成未被取代的6元芳基、6元杂环基或6元杂芳基环。在一些实施方案中,r
6c1
和r
6d1
连同它们
所连接的碳原子一起形成6元芳基、6元杂环基或6元杂芳基环,其中所述6元芳基、6元杂环基或6元杂芳基环各自独立地被一个或多个选自由c
1-c6烷基和
–
c(o)o-c
1-c6烷基组成的组的取代基取代。
[0357]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)和(b-2n)的一些实施方案中,y7是n。在一些实施方案中,y7是c。在其他实施方案中,y7是ch。在一些实施方案中,y8是n。在一些实施方案中,y8是nh。在一些实施方案中,y8是c。在其他实施方案中,y8是ch。
[0358]
在一些实施方案中,y3是ch(x
1a-r
6a1
)、c(x
1a-r
6a1
)、n、n(x
1a-r
6a1
)、s或o;y4是ch(x
2a-r
6b1
)、c(x
2a-r
6b1
)、n、n(x
2a-r
6b1
)、s或o;y5是ch(x
3a-r
6c1
)、c(x
3a-r
6c1
)、n、n(x
3a-r
6c1
)、s或o;y6是ch(x
4a-r
6d1
)、c(x
4a-r
6d1
)、n、n(x
4a-r
6d1
)、s、o,或是不存在的;并且g7是n、c或ch,其中y1、y2、y3、y4、y5、y6和y7各自具有零电荷(例如y1、y2、y3、y4、y5、y6和y7的氮不是阳离子性的)。
[0359]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)和(b-2n)的一些实施方案中,是其中r
6a1
、r
6b1
、r
6c1
和r
6d1
中的一者或多者选自由以下组成的组:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
p1rq1
、c
6-c
12
芳基、3至10元杂环基、5至10元杂芳基、-c
1-c6烷基-5至6元杂环基、-oc(o)-5至6元杂环基、-c(o)r
h1
、-s(o)2nr
w1arw2a
、-s(o)2r
y1
和-nr
z1a
s(o)2r
z2a
。
[0360]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)和(b-2n)的一些实施方案中,是其中r
6c1
选自由以下组成的组:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
p1rq1
、c
6-c
12
芳基、3至10元杂环基、5至10元杂芳基、-c
1-c6烷基-5至6元杂环基、-oc(o)-5至6元杂环基、-c(o)r
h1
、-s(o)2nr
w1arw2a
、-s(o)2r
y1
或-nr
z1a
s(o)2r
z2a
。在一些实施方案中,r
6c1
是未被取代的c
1-c6烷基。举例来说,在一些实施方案中,r
6c1
是甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基和叔丁基。在一些实施方案中,r
6c1
是被一个或多个选自由c
3-c8环烷基和卤素组成的组的基团取代的c
1-c6烷基。在一些实施方案中,r
6c1
是c
1-c6烷氧基。举例来说,在一些实施方案中,r
6c1
是甲氧基、乙氧基、丙氧基、异丙氧基、丁氧基、异丁氧基、仲丁氧基和叔丁氧基。在一些实施方案中,r
6c1
是被一个或多个选自由c
3-c8环烷基和卤素组成的组的基团取代的c
1-c6烷氧基。在一些实施方案中,r
6c1
是卤基。举例来说,在一些实施方案中,r
6c1
是氟基、氯基或溴基。在其他实施方案中,r
6c1
是c
1-c6卤代烷基。举例来说,在一些实施方
nr
p1rq1
、c
6-c
12
芳基、3至10元杂环基、5至10元杂芳基、-c
1-c6烷基-5至6元杂环基、-oc(o)-5至6元杂环基、-c(o)r
h1
、-s(o)2nr
w1arw2a
、-s(o)2r
y1
或-nr
z1a
s(o)2r
z2a
。在一些实施方案中,r
6b1
是未被取代的c
1-c6烷基。举例来说,在一些实施方案中,r
6b1
是甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基和叔丁基。在一些实施方案中,r
6b1
是被一个或多个选自由c
3-c8环烷基和卤素组成的组的基团取代的c
1-c6烷基。在一些实施方案中,r
6b1
是c
1-c6烷氧基。举例来说,在一些实施方案中,r
6b1
是甲氧基、乙氧基、丙氧基、异丙氧基、丁氧基、异丁氧基、仲丁氧基和叔丁氧基。在一些实施方案中,r
6b1
是被一个或多个选自由c
3-c8环烷基和卤素组成的组的基团取代的c
1-c6烷氧基。在一些实施方案中,r
6b1
是卤基。举例来说,在一些实施方案中,r
6b1
是氟基、氯基或溴基。在其他实施方案中,r
6b1
是c
1-c6卤代烷基。举例来说,在一些实施方案中,r
6b1
是氟乙基、三氟甲基、二氟甲基、三氟乙基和三氯甲基。在一些实施方案中,r
6b1
是-c(o)r
h1
,其中r
h1
是h、c
1-c6烷基、c
1-c6烷氧基、c
3-c8环烷基或-nr
r1rs1
。举例来说,在一些实施方案中,r
6b1
是-c(o)h、-c(o)ch3、-c(o)oc(ch3)3或
–
c(o)-环丙基。在一些实施方案中,r
6b1
是被一个或多个选自由以下组成的组的基团取代的5至10元杂环基:c
1-c6烷基、c
1-c6烷氧基、-oh、c
1-c6烷基-oh、=o、=s、卤基、c
3-c8环烷基、-c(o)nh-c
3-c8环烷基、c
6-c
12
芳基和5至6元杂环基。在一些实施方案中,r
6b1
是氮杂双环[3.1.0]己烷基、呋喃并[3,4-c]吡咯基、氮杂螺[3.3]庚烷、6-氧代-5-氮杂螺[2.4]庚烷基、氮杂螺[2.4]庚烷基、异吲哚啉基、二氢异喹啉基、吡咯烷-1-基)哌啶基、吲哚啉基、苯并[b][1,4]噁嗪基、金刚烷-1-基)(甲基)氨基、氮杂双环[2.2.1]庚烷基)、氮杂双环[3.2.1]辛烷基或六氢环戊二烯并[c]吡咯基,各自任选地被一个或多个选自由以下组成的组的取代基取代:c
1-c6烷基、c
1-c6烷氧基、-oh、c
1-c6烷基-oh、=o、=s、卤基、c
3-c8环烷基、-c(o)nh-c
3-c8环烷基、c
6-c
12
芳基和5至6元杂环基。在一些实施方案中,r
6b1
是被一个或多个选自由以下组成的组的基团取代的吲哚啉基:c
1-c6烷基、c
1-c6烷氧基、-oh、c
1-c6烷基-oh、=o、=s、卤基、c
3-c8环烷基、-c(o)nh-c
3-c8环烷基、c
6-c
12
芳基和5至6元杂环基。在某些实施方案中,r
6b1
是被一个或多个独立选择的c
1-c6烷基和卤基取代的吲哚啉基。在一些实施方案中,r
6b1
是未被取代的5至6元杂环。在一些实施方案中,r
6b1
是被一个或多个选自由以下组成的组的基团取代的5至6元杂环:c
1-c6烷基、c
1-c6烷氧基、-oh、c
1-c6烷基-oh、=o、=s、卤基、c
3-c8环烷基、-c(o)nh-c
3-c8环烷基、c
6-c
12
芳基和5至6元杂环基。在一些实施方案中,r
6b1
是被一个或多个选自由以下组成的组的基团取代的5至6元杂环:c
1-c6烷基、c
1-c6烷氧基、-oh、c
1-c6烷基-oh、=o和=s。在一些实施方案中,r
6b1
是吡咯烷基、吡唑烷基、咪唑烷基、四氢呋喃基、1,3-二氧杂环戊烷基、四氢噻吩基、氧硫杂环戊烷基、环丁砜基、哌啶基、哌嗪基、四氢吡喃基、二氧杂环己烷基、硫杂环己烷基、二硫杂环己烷基、三硫杂环己烷基、吗啉基或硫代吗啉基。在一些实施方案中,r
6b1
是被苯基取代的哌嗪基。在一些实施方案中,r
6b1
是未被取代的5至10元杂芳基。在一些实施方案中,r
6b1
是被一个或多个选自由以下组成的组的基团取代的5至10元杂芳基:c
1-c6烷基、c
1-c6烷氧基、-oh和c
1-c6烷基-oh。在一些实施方案中,r
6b1
是吡咯基、吡唑基、咪唑基、三唑基、四唑基、呋喃基、异噁唑基、噁唑基、噁二唑基、噻吩基、异噻唑基、噻唑基、噻二唑基、吡啶基、哒嗪基、嘧啶基、吡嗪基、三嗪基或四嗪基。在一些实施方案中,r
6b1
是-n(ch3)ch2c(ch3)3。在一些
实施方案中,r
6b1
是
[0362]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)和(b-2n)的一些实施方案中,是其中r
6a1
选自由以下组成的组:c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
p1rq1
、c
6-c
12
芳基、3至10元杂环基、5至10元杂芳基、-c
1-c6烷基-5至6元杂环基、-oc(o)-5至6元杂环基、-c(o)r
h1
、-s(o)2nr
w1arw2a
、-s(o)2r
y1
或-nr
z1a
s(o)2r
z2a
。在一些实施方案中,r
6a1
是未被取代的c
1-c6烷基。举例来说,在一些实施方案中,r
6a1
是甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基和叔丁基。在一些实施方案中,r
6a1
是被一个或多个选自由c
3-c8环烷基和卤素组成的组的基团取代的c
1-c6烷基。在一些实施方案中,r
6a1
是c
1-c6烷氧基。举例来说,在一些实施方案中,r
6a1
是甲氧基、乙氧基、丙氧基、异丙氧基、丁氧基、异丁氧基、仲丁氧基和叔丁氧基。在一些实施方案中,r
6a1
是被一个或多个选自由c
3-c8环烷基和卤素组成的组的基团取代的c
1-c6烷氧基。在一些实施方案中,r
6a1
是卤基。举例来说,在一些实施方案中,r
6a1
是氟基、氯基或溴基。在其他实施方案中,r
6a1
是c
1-c6卤代烷基。举例来说,在一些实施方案中,r
6a1
是氟乙基、三氟甲基、二氟甲基、三氟乙基和三氯甲基。在一些实施方案中,r
6a1
是-c(o)r
h1
,其中r
h1
是h、c
1-c6烷基、c
1-c6烷氧基、c
3-c8环烷基或-nr
r1rs1
。举例来说,在一些实施方案中,r
6a1
是-c(o)h、-c(o)ch3、-c(o)oc(ch3)3或
–
c(o)-环丙基。在一些实施方案中,r
6a1
是未被取代的5至6元杂环。在一些实施方案中,r
6a1
是被一个或多个选自由以下组成的组的基团取代的5至6元杂环:c
1-c6烷基、c
1-c6烷氧基、-oh、c
1-c6烷基-oh、=o、=s、卤基、c
3-c8环烷基、-c(o)nh-c
3-c8环烷基、c
6-c
12
芳基和5至6元杂环基。在一些实施方案中,r
6a1
是被一个或多个选自由以下组成的组的基团取代的5至6元杂环:c
1-c6烷基、c
1-c6烷氧基、-oh、c
1-c6烷基-oh、=o和=s。在一些实施方案中,r
6a1
是吡咯烷基、吡唑烷基、咪唑烷基、四氢呋喃基、1,3-二氧杂环戊烷基、四氢噻吩基、氧硫杂环戊烷基、环丁砜基、哌啶基、哌嗪基、四氢吡喃基、二氧杂环己烷基、硫杂环己烷基、二硫杂环己烷基、三硫杂环己烷基、吗啉基或硫代吗啉基。在一些实施方案中,r
6a1
是被苯基取代的哌嗪基。在一些实施方案中,r
6a1
是被一个或多个选自由以下组成的组的基团取代的5至10元杂环基:c
1-c6烷基、c
1-c6烷氧基、-oh、c
1-c6烷基-oh、=o、=s、卤基、c
3-c8环烷基、-c(o)nh-c
3-c8环烷基、c
6-c
12
芳基和5至6元杂环基。在一些实施方案中,r
6a1
是被一个或多个选自由以下组成的组的基团取代的吲哚啉基:c
1-c6烷基、c
1-c6烷氧基、-oh、c
1-c6烷基-oh、=o、=s、卤基、c
3-c8环烷基、-c(o)nh-c
3-c8环烷基、c
6-c
12
芳基和5至6元杂环基。在一些实施方案中,r
6a1
是氮杂双环[3.1.0]己烷基、呋喃并[3,4-c]吡咯基、氮杂螺[3.3]庚烷、6-氧代-5-氮杂螺[2.4]庚烷基、氮杂螺[2.4]庚烷基、异吲哚啉基、二氢异喹啉基、吡咯烷-1-基)哌啶基、吲哚啉基、苯并[b][1,4]噁嗪基、金刚烷-1-基)(甲基)氨基、氮杂双环[2.2.1]庚烷基)、氮杂双环[3.2.1]辛烷基或六氢环戊二烯并[c]吡咯基,各自任选地被一个或多个选自由以下组成的组的取代基取代:c
1-c6烷基、c
1-c6烷氧
c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基和5至10元杂芳基。在一些实施方案中,是其中r
6a1
、r
6c1
和r
6d1
中的一者或多者选自由以下组成的组:c
1-c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基和5至10元杂芳基。在一些实施方案中,是其中r
6a1
、r
6b1
和r
6d1
中的一者或多者选自由以下组成的组:c
1-c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基和5至10元杂芳基。在一些实施方案中,是其中r
6b1
和r
6d1
中的一者或两者选自由以下组成的组:c
1-c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基和5至10元杂芳基。在一些实施方案中,是其中r
6a1
和r
6c1
中的一者或两者选自由以下组成的组:c
1-c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基和5至10元杂芳基。在一些实施方案中,是其中r
6b1
、r
6c1
和r
6d1
中的一者或多者选自由以下组成的组:c
1-c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基和5至10元杂芳基。在一些实施方案中,选自由以下组成的组:选自由以下组成的组:
[0365]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)和(b-2n)的一些实施方案中,是在一些实施方案中,是其中r
6c1
选自由以下组成的组:氢、c
1-c6烷基、c
1-c6烷氧基、卤基、-oh、-nr
p1rq1
、c
6-c
12
芳基、3至10元杂环基、5至10元杂芳基、-c
1-c6烷基-5至6元杂环基、-oc(o)-5至6元杂环基、-c(o)r
h1
、-s(o)2nr
w1arw2a
、-s(o)2r
y1
和-nr
z1a
s(o)2r
z2a
。在某些实施方案中,r
6c1
是
–
c(o)oc(ch3)3。
[0366]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)和(b-2n)的一些实施方案中,是是
[0367]
在任何前述实施方案中,r
6a1
、r
6b1
、r
6c1
和r
6d1
中的一者或多者选自由以下组成的组:c
1-c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基和5至10元杂芳基。在一些实施方案中,r
6a1
、r
6b1
、r
6c1
和r
6d1
中的一者或多者是未被取代或被一个或多个选自由以下组成的组的基团取代的c
6-c
12
芳基:c
1-c6烷基、c
1-c6烷氧基、-oh和c
1-c6烷基-oh。举例来说,在一些实施方案中,r
6a1
、r
6b1
、r
6c1
和r
6d1
中的一者是苯基或萘基。在一些实施方案中,r
6a1
、r
6b1
、r
6c1
和r
6d1
中的一者或多者是未被取代或被一个或多个选自由以下组成的组的基团取代的3至10元杂环基:c
1-c6烷基、c
1-c6烷氧基、-oh、c
1-c6烷基-oh、=o、=s、卤基、c
3-c8环烷基、-c(o)nh-c
3-c8环烷基、c
6-c
12
芳基和5至6元杂环基。在一些实施方案中,r
6a1
、r
6b1
、r
6c1
和r
6d1
中的一者或多者是未被取代或被一个或多个选自由以下组成的组的基团取代的3至10元杂环基:c
1-c6烷基、c
1-c6烷氧基、-oh、c
1-c6烷基-oh、=o和=s。举例来说,在一些实施方案中,r
6a1
、r
6b1
、r
6c1
和r
6d1
中的一者是吡咯烷基、吡唑烷基、咪唑烷基、四氢呋喃基、1,3-二氧杂环戊烷基、四氢噻吩基、氧硫杂环戊烷基、环丁砜基、哌啶基、哌嗪基、四氢吡喃基、二氧杂环己烷基、硫杂环己烷基、二硫杂环己烷基、三硫杂环己烷基、吗啉基、硫代吗啉基、四氢喹啉基、四氢异喹啉基、十氢喹啉基、十氢异喹啉基、吲哚啉基、异吲哚啉基、四氢萘啶基或六氢苯并咪唑基,各自独立地未被取代或被一个或多个选自由以下组成的组的基团取代:c
1-c6烷基、c
1-c6烷氧基、-oh、c
1-c6烷基-oh、=o、=s、卤基、c
3-c8环烷基、-c(o)nh-c
3-c8环烷基、c
6-c
12
芳基和5至6元杂环基。举例来说,在一些实施方案中,r
6a1
、r
6b1
、r
6c1
和r
6d1
中的一者是吡咯烷基、吡唑烷基、咪唑烷基、四氢呋喃基、1,3-二氧杂环戊烷基、四氢噻吩基、氧硫杂环戊烷基、环丁砜基、哌啶基、哌嗪基、四氢吡喃基、二氧杂环己烷基、硫杂环己烷基、二硫杂环己烷基、三硫杂环己烷基、吗啉基、硫代吗啉基、四氢喹啉基、四氢异喹啉基、十氢喹啉基、十氢异喹啉基、吲哚啉基、异吲哚啉基、四氢萘啶基或六氢苯并咪唑基,各自独立地未被取代或被一个或多个选自由以下组成的组的基团取代:c
1-c6烷基、c
1-c6烷氧基、-oh、c
1-c6烷基-oh、=o和=s。
[0368]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)和(b-2n)的一些实施方案中,r
6a1
、r
6b1
、r
6c1
和r
6d1
中的一者选自由以下组成的组:c
1-c6烷基、c
1-c6卤代烷基、卤基、c
6-c
12
芳基、3至10元杂环基和5至10元杂芳基。在某些实施方案中,r
6a1
、r
6b1
、r
6c1
和r
6d1
中的一者选自由以下组成的组:甲基、乙基、f、cl、
–
cf3、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡唑基和三唑基。在某些实施方案中,r
6a1
、r
6b1
、r
6c1
和r
6d1
中的一者选自由以下组成的组:吡咯烷基、哌啶基、吗啉基、哌嗪基、吡唑基和三唑基,各自任选地被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、-oh、c
1-c6烷基-oh、=o、=s、卤基、c
3-c8环烷基、-c(o)nh-c
3-c8环烷基、c
6-c
12
芳基和5至6元杂环基组成的组的基团取代。在某些实施方案中,r
6a1
、r
6b1
、r
6c1
和r
6d1
中的一者选自由以下组成的组:吡咯烷基、哌啶基、吗啉基、哌嗪基、吡唑基和三唑基,各自任选地被一个或多个选自由c
1-c6烷基、c
1-c6烷氧基、-oh、c
1-c6烷基-oh、=o和=s组成的组的基团取代。在一些实施方案中,r
6a1
、r
6b1
、r
6c1
和r
6d1
中的两者或三者选自由以下组成的组:甲基、乙基、f、cl、
–
cf3、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡唑基和三唑基。在其他实施方案中,r
6a1
、r
6b1
、r
6c1
和r
6d1
各自是h。
[0369]
在式(b),包括式(b-1a)、(b-1b)、(b-2a)、(b-2b)、(b-2c)、(b-2d)、(b-2e)、(b-2f)、(b-2g)、(b-2h)、(b-2i)、(b-2j)、(b-2k)、(b-2l)、(b-2m)和(b-2n)的一些实施方案中,r
6a1
、r
6b1
、r
6c1
和r
6d1
中的一者是任选地被一个或多个选自由以下组成的组的基团取代的吲哚啉基:c
1-c6烷基、c
1-c6烷氧基、-oh、c
1-c6烷基-oh、=o、=s、卤基、c
3-c8环烷基、-c(o)nh-c
3-c8环烷基、c
6-c
12
芳基和5至6元杂环基。在一些实施方案中,r
6a1
、r
6b1
、r
6c1
和r
6d1
中的一者是任选地被一个或多个独立选择的c
1-c6烷基和卤基取代的吲哚啉基。在一些实施方案中,r
6a1
、r
6b1
、r
6c1
和r
6d1
中的一者是3,3-二甲基吲哚啉-1-基或5-氟-3,3-二甲基吲哚啉-1-基。在一些实施方案中,r
6c1
是3,3-二甲基吲哚啉-1-基或5-氟-3,3-二甲基吲哚啉-1-基。在一些实施方案中,r
6a1
、r
6b1
、r
6c1
和r
6d1
中的一者是任选地被苯基取代的哌嗪基。在一些实施方案中,r
6a1
、r
6b1
、r
6c1
和r
6d1
中的一者是4-苯基哌嗪基。在一些实施方案中,r
6c1
是4-苯基哌嗪基。
[0370]
在一些实施方案中,本文提供了表1b中所述的化合物及其盐。
[0371]
表1b.
[0372]
[0373]
[0374]
[0375]
[0376]
[0377]
[0378]
[0379]
[0380]
[0381]
[0382]
[0383]
[0384]
[0385]
[0386][0387]
以及它们的药学上可接受的盐。
[0388]
本文给出的任何式或化合物,诸如式(i)、式(a)或式(b),或表1a和表1b的化合物,都意图代表具有由结构式以及某些变化形式或形式描绘的结构的化合物。具体地说,具有本文给出的任何式的化合物可含有旋转受阻的键,因此,以不同几何构型存在。另外,具有本文提供的任何式的化合物可具有不对称中心,因此,以不同对映异构或非对映异构形式存在。通式化合物的所有光学异构体和立体异构体以及它们的处于任何比率的混合物都被视为在所述式的范围内。因此,本文给出的任何式都意图代表外消旋物、一种或多种对映异构形式、一种或多种非对映异构形式、一种或多种阻转异构形式(例如几何异构形式)、以及它们的处于任何比率的混合物。当以特定立体化学构型描绘表1a或表1b的化合物时,本文还提供了所述化合物的任何替代性立体化学构型以及所述化合物的处于任何比率的立体异构体的混合物。表1a或表1b的任何化合物都意图代表外消旋物、一种或多种对映异构形式、一种或多种非对映异构形式、一种或多种阻转异构形式(例如几何异构形式)、以及它们的处于任何比率的混合物。此外,某些结构可以互变异构体形式或以阻转异构体形式存在。另外,本文给出的任何式都意指此类化合物的水合物、溶剂化物和非晶形式、以及它们的混合物,即使未明确列出此类形式。在一些实施方案中,溶剂是水,并且溶剂化物是水合物。
[0389]
式(a)和式(b)或表1a和表1b的化合物可被制备和/或配制成药学上可接受的盐。在一些实施方案中,药学上可接受的盐包括酸加成盐,所述酸加成盐用无机酸诸如盐酸、氢溴酸、硫酸、硝酸、磷酸等形成;或用有机酸诸如乙酸、草酸、丙酸、丁二酸、顺丁烯二酸、酒石酸等形成。这些盐可由无机或有机酸获得。药学上可接受的盐的非限制性实例包括硫酸盐、焦硫酸盐、硫酸氢盐、亚硫酸盐、亚硫酸氢盐、磷酸盐、磷酸一氢盐、磷酸二氢盐、偏磷酸盐、焦磷酸盐、氯化物、溴化物、碘化物、乙盐酸、丙酸盐、癸酸盐、辛酸盐、丙烯酸盐、甲酸盐、异丁酸盐、己酸盐、庚酸盐、丙炔酸盐、草酸盐、丙二酸盐、丁二酸盐、辛二酸盐、癸二酸盐、反丁烯二酸盐、顺丁烯二酸盐、丁炔-1,4-二酸盐、己炔-1,6-二酸盐、苯甲酸盐、氯苯甲酸盐、甲基苯甲酸盐、二硝基苯甲酸盐、羟基苯甲酸盐、甲氧基苯甲酸盐、邻苯二甲酸盐、磺酸盐、甲基磺酸盐、丙基磺酸盐、苯磺酸盐、二甲苯磺酸盐、萘-1-磺酸盐、萘-2-磺酸盐、苯基乙酸盐、苯基丙酸盐、苯基丁酸盐、柠檬酸盐、乳酸盐、γ-羟基丁酸盐、乙醇酸盐、酒石酸盐和扁桃酸盐。在一些实施方案中,当存在于母体化合物中的酸性质子被金属离子例如碱金属离子、碱土金属离子或铝离子替换;或与有机碱配位时,形成药学上可接受的盐。由药学上可接受的
有机无毒碱获得的盐包括以下各物的盐:伯胺、仲胺和叔胺;被取代的胺,包括天然存在的被取代的胺;环胺和碱性离子交换树脂,诸如异丙胺、三甲胺、二乙胺、三乙胺、三丙胺、乙醇胺、2-二乙基氨基乙醇、缓血酸胺、氨基丁三醇、二环己胺、咖啡因(caffeine)、普鲁卡因(procaine)、海卓胺(hydrabamine)、胆碱(choline)、甜菜碱(betaine)、乙二胺、葡糖胺、n-乙基还原葡糖胺、n-甲基还原葡糖胺、可可碱(theobromine)、嘌呤、哌嗪、哌啶、n-乙基哌啶、多胺树脂、氨基酸诸如赖氨酸、精氨酸、组氨酸,等。药学上可接受的碱加成盐的实例包括由无机碱获得的那些,诸如钠、钾、锂、铵、钙、镁、铁、锌、铜、锰、铝盐等。在一些实施方案中,有机无毒碱是l-氨基酸诸如l-赖氨酸和l-精氨酸、缓血酸胺、n-乙基还原葡糖胺和n-甲基还原葡糖胺。可接受的无机碱包括氢氧化铝、氢氧化钙、氢氧化钾、碳酸钠、氢氧化钠等。其他适合药学上可接受的盐的清单见于remington's pharmaceutical sciences,第17版,mack publishing company,easton,pa.,1985中。
[0390]
对于含有碱性氮的本文所述的化合物,可通过本领域中可用的任何适合方法制备药学上可接受的盐,例如用无机酸处理游离碱,所述无机酸诸如是盐酸、氢溴酸、硫酸、氨基磺酸、硝酸、硼酸、磷酸等,或用有机酸处理游离碱,所述有机酸诸如是乙酸、苯基乙酸、丙酸、硬脂酸、乳酸、抗坏血酸、顺丁烯二酸、羟基顺丁烯二酸、羟基乙磺酸、丁二酸、戊酸、反丁烯二酸、丙二酸、丙酮酸、草酸、乙醇酸、水杨酸、油酸、棕榈酸、月桂酸、吡喃糖苷酸诸如葡萄糖醛酸或半乳糖醛酸,α-羟基酸诸如扁桃酸、柠檬酸或酒石酸,氨基酸诸如天冬氨酸或谷氨酸,芳族酸诸如苯甲酸、2-乙酰氧基苯甲酸、萘甲酸或肉桂酸,磺酸诸如月桂基磺酸、对甲苯磺酸、甲烷磺酸、苯磺酸或乙烷磺酸,或酸诸如在本文中作为实例给出的那些酸的任何可相容混合物以及根据本技术中的普通技能水平被视为等效物或可接受替代物的任何其他酸及其混合物。
[0391]
本文描绘的化合物可以盐形式存在,即使盐未加以描绘,并且应了解本文提供的组合物和方法包括此处描绘的化合物的所有盐和溶剂化物以及化合物的非盐和非溶剂化物形式,如由熟练技术人员所充分了解。在一些实施方案中,本文提供的化合物的盐是药学上可接受的盐。
[0392]
本文详述的化合物,包括中间体和最终化合物的代表性实例在本文中描绘于表格和其他地方中。应了解,在一个方面,任何化合物都可用于本文详述的方法中,在适用时包括可被分离以及施用至个体的中间化合物。
[0393]
在一个变化形式中,本文化合物是被制备用于施用至个体的合成化合物。在另一变化形式中,提供了含有呈大致上纯净形式的化合物的组合物。在另一变化形式中,提供了包含本文详述的化合物以及药学上可接受的载体的药物组合物。在另一变化形式中,提供了施用化合物的方法。纯化形式、药物组合物和施用化合物的方法适于本文详述的任何化合物或其形式。
[0394]
本文提供的r1、r2、r3、r4、y1、y2、y3、y4、y5、g1、g2、g3、g4、g5、g6、g7、ra、rb、rc、rd、re、rf、rg、rh、rj、rk、rm、rn、r
p
、rq、rr、rs、r
t
、ru、rv、r
w1
、r
w2
、r
x
、ry、r
z1
、r
z2
、x1、x2、x3、x4、m、n、r
6a
、r
6b
、r
6c
和r
6d
的任何变化形式或实施方案都可与r1、r2、r3、r4、y1、y2、y3、y4、y5、g1、g2、g3、g4、g5、g6、g7、ra、rb、rc、rd、re、rf、rg、rh、rj、rk、rm、rn、r
p
、rq、rr、rs、r
t
、ru、rv、r
w1
、r
w2
、r
x
、ry、r
z1
、r
z2
、x1、x2、x3、x4、m、n、r
6a
、r
6b
、r
6c
和r
6d
的每个其他变化形式或实施方案组合,就好像已单独地和具体地描述每个组合一样。
[0395]
本文提供的r
1a
、r
2a
、r
3a
、l、y1、y2、y3、y4、y5、y6、y7、y8、r
a1
、r
b1
、r
c1
、r
d1
、r
e1
、r
f1
、r
g1
、r
h1
、r
j1
、r
k1
、r
m1
、r
n1
、r
p1
、r
q1
、r
r1
、r
s1
、r
t1
、r
u1
、r
v1
、r
w1a
、r
w2a
、r
x
、r
y1
、r
z1a
、r
z2a
、x
1a
、x
2a
、x
3a
、x
4a
、m1、r
6a1
、r
6b1
、r
6c1
和r
6d1
的任何变化形式或实施方案都可与r
1a
、r
2a
、r
3a
、l、y1、y2、y3、y4、y5、y6、y7、y8、r
a1
、r
b1
、r
c1
、r
d1
、r
e1
、r
f1
、r
g1
、r
h1
、r
j1
、r
k1
、r
m1
、r
n1
、r
p1
、r
q1
、r
r1
、r
s1
、r
t1
、r
u1
、r
v1
、r
w1a
、r
w2a
、r
x
、r
y1
、r
z1a
、r
z2a
、x
1a
、x
2a
、x
3a
、x
4a
、m1、r
6a1
、r
6b1
、r
6c1
和r
6d1
的每个其他变化形式或实施方案组合,就好像已单独地和具体地描述每个组合一样。
[0396]
本文提供的r1、r2、r3、r4、y1、y2、y3、y4、y5、g1、g2、g3、g4、g5、g6、g7、ra、rb、rc、rd、re、rf、rg、rh、rj、rk、rm、rn、r
p
、rq、rr、rs、r
t
、ru、rv、r
w1
、r
w2
、r
x
、ry、r
z1
、r
z2
、x1、x2、x3、x4、m、n、r
6a
、r
6b
、r
6c
、r
6d
、r
1a
、r
2a
、r
3a
、l、y1、y2、y3、y4、y5、y6、y7、y8、r
a1
、r
b1
、r
c1
、r
d1
、r
e1
、r
f1
、r
g1
、r
h1
、r
j1
、r
k1
、r
m1
、r
n1
、r
p1
、r
q1
、r
r1
、r
s1
、r
t1
、r
u1
、r
v1
、r
w1a
、r
w2a
、r
x
、r
y1
、r
z1a
、r
z2a
、x
1a
、x
2a
、x
3a
、x
4a
、m1、r
6a1
、r
6b1
、r
6c1
和r
6d1
的任何变化形式或实施方案都可与r1、r2、r3、r4、y1、y2、y3、y4、y5、g1、g2、g3、g4、g5、g6、g7、ra、rb、rc、rd、re、rf、rg、rh、rj、rk、rm、rn、r
p
、rq、rr、rs、r
t
、ru、rv、r
w1
、r
w2
、r
x
、ry、r
z1
、r
z2
、x1、x2、x3、x4、m、n、r
6a
、r
6b
、r
6c
、r
6d
、r
1a
、r
2a
、r
3a
、l、y1、y2、y3、y4、y5、y6、y7、y8、r
a1
、r
b1
、r
c1
、r
d1
、r
e1
、r
f1
、r
g1
、r
h1
、r
j1
、r
k1
、r
m1
、r
n1
、r
p1
、r
q1
、r
r1
、r
s1
、r
t1
、r
u1
、r
v1
、r
w1a
、r
w2a
、r
x
、r
y1
、r
z1a
、r
z2a
、x
1a
、x
2a
、x
3a
、x
4a
、m1、r
6a1
、r
6b1
、r
6c1
和r
6d1
的每个其他变化形式或实施方案组合,就好像已单独地和具体地描述每个组合一样。
[0397]
实施方案还涉及本文所述的化合物的药学上可接受的前药以及采用此类药学上可接受的前药的治疗方法。术语“前药”意指指定化合物的前体,所述前体在施用至受试者之后通过化学或生理过程诸如溶剂分解或酶促裂解,或在生理条件下(例如前药在致使达到生理ph时转化成式(a)或式(b)化合物),在体内产生所述化合物。“药学上可接受的前药”是无毒、生物可耐受、并且在其他方面在生物学上适于施用至受试者的前药。用于选择和制备适合前药衍生物的说明性程序例如描述于“design of prodrugs”,h.bundgaard编,elsevier,1985中。
[0398]
实施方案还涉及本文所述的化合物的药物活性代谢物以及此类代谢物在本文提供的方法中的用途。“药物活性代谢物”意指本文所述的化合物或其盐的在身体中的药理活性代谢产物。可使用本领域中已知或可用的常规技术确定化合物的前药和活性代谢物。参见例如bertolini等人,j.med.chem.1997,40,2011-2016;shan等人,j.pharm.sci.1997,86(7),765-767;bagshawe,drug dev.res.1995,34,220-230;bodor,adv.drug res.1984,13,255-331;bundgaard,design of prodrugs(elsevier press,1985);以及larsen,design and application of prodrugs,drug design and development(krogsgaard-larsen等人编,harwood academic publishers,1991)。
[0399]
化学定义
[0400]
除非另外指示,否则以下术语具有以下含义。任何未定义术语都具有它们的本领域公知含义。
[0401]
术语“烷基”是指具有指定碳原子数(即c
1-c
10
意指一个至十个碳原子)的直链或支链单价饱和烃基团或其组合。烷基的实例包括但不限于甲基(me)、乙基(et)、正丙基、异丙基、丁基、异丁基、仲丁基、叔丁基(tbu)、戊基、异戊基、叔戊基、己基、异己基以及根据本领域中的普通技术和本文提供的教示内容将被视为等效于前述实例中的任一者的基团。
[0402]
术语“烷氧基”是指
–
o-烷基。烷氧基的实例包括但不限于甲氧基、乙氧基、正丙氧
基、异丙氧基、正丁氧基、异丁氧基、仲丁氧基和叔丁氧基。
[0403]
术语“烯基”是指具有所指示碳原子数,并且具有一个或多个双键的不饱和直链或支链烃基团或其组合。烯基的实例包括但不限于乙烯基(ethenyl)(或乙烯基(vinyl))、烯丙基和丁-3-烯-1-基。包括在这个术语内的是顺式和反式异构体以及它们的混合物。
[0404]
术语“炔基”是指具有所指示碳原子数(例如2至8或2至6个碳原子)和至少一个碳-碳三键的不饱和直链或支链烃基团。炔基的实例包括但不限于乙炔基(-c≡ch)和炔丙基(-ch2c≡ch)。
[0405]
术语“亚烷基”是指是烷烃的基团的二价基团。亚烷基可为直链或支链二价烷基。“c
1-4
亚烷基”是指具有1至4个碳原子的亚烷基。
[0406]
术语“芳基”是指具有6至18个环碳原子,具有单环(苯基)或多稠环(诸如萘基、蒽基或茚满基)的单价芳族碳环基团,其中稠环任选地是芳族的,前提是芳基与母体结构的连接点是通过芳族环的原子来达成的。如本文定义的“芳基”涵盖诸如苯基和芴基的基团。
[0407]
术语“环烷基”是指具有3至10个环碳原子,具有单环或多环的环烃基团,所述多环包括稠合、桥接和螺环系统。适合环烷基的实例包括例如金刚烷基、环丙基、环丁基、环戊基、环辛基等。此类环烷基例如包括单环结构诸如环丙基、环丁基、环戊基、环辛基等,或多环结构诸如金刚烷基等。在一些情况下,环烷基是单环。在一些情况下,环烷基是3至6元环。
[0408]
术语“环烯基”是指具有4至10个环碳原子,具有单环和至少一个内部不饱和点的环状烯基,其可任选地被1至3个烷基取代。适合环烯基的实例包括例如环戊-3-烯基、环己-2-烯基、环辛-3-烯基等。
[0409]
术语“卤代烷基”是指如上所述的烷基,其中所述烷基上的一个或多个氢原子已被卤基替换。此类基团的实例包括但不限于氟烷基,诸如氟乙基、三氟甲基、二氟甲基、三氟乙基等。
[0410]
术语“杂芳基”是指单环、稠合双环或稠合多环芳族杂环(具有选自碳原子以及多达四个选自氮、氧和硫的杂原子的环原子的环结构),每个杂环具有3至12个环原子。杂芳基的说明性实例包括呈适当键合的部分的形式的以下实体:
[0411][0412]
术语“杂环基”或“杂环烷基”是指饱和或部分不饱和基团,具有单环或多稠环,包括稠合、桥接或螺环系统,并且具有3至20个环原子,包括1至10个杂原子。这些环原子选自由碳、氮、硫或氧组成的组。在某些实施方案中,杂环基团的一个或多个氮和/或硫原子任选地被氧化以提供n-氧化物、-s(o)-或
–
so
2-部分。杂环基团的说明性实例包括呈适当键合的
部分的形式的以下实体:
[0413][0414]
术语“卤素”代表氯、氟、溴或碘。术语“卤基”代表氯基、氟基、溴基或碘基。
[0415]
术语“氧代基”代表羰基氧。举例来说,被氧代基取代的环戊基是环戊酮。
[0416]
本领域技术人员将认识到以上列出或说明的种类不是详尽的,并且还可选择在这些定义术语的范围内的额外种类。
[0417]
术语“被取代”意指指定基团或部分携带一个或多个取代基,包括但不限于诸如以下的取代基:烷氧基、酰基、酰基氧基、羰基烷氧基、酰基氨基、氨基、氨基酰基、氨基羰基氨基、氨基羰基氧基、环烷基、环烯基、芳基、杂芳基、芳基氧基、氰基、叠氮基、卤基、羟基、硝基、羧基、硫醇、烷基硫基、环烷基、环烯基、烷基、烯基、炔基、杂环基、芳烷基、氨基磺酰基、磺酰基氨基、磺酰基、氧代基、羰基亚烷基烷氧基等。术语“未被取代”意指指定基团不携带取代基。术语“任选地被取代”意指指定基团未被取代或被一个或多个取代基取代。当术语“被取代”用于描述结构系统时,取代意图发生在所述系统上的任何化合价允许的位置处。当基团或部分携带超过一个取代基时,应了解所述取代基可为相同的,或不同于彼此。在一些实施方案中,被取代的基团或部分携带一个至五个取代基。在一些实施方案中,被取代的基团或部分携带一个取代基。在一些实施方案中,被取代的基团或部分携带两个取代基。在一些实施方案中,被取代的基团或部分携带三个取代基。在一些实施方案中,被取代的基团或部分携带四个取代基。在一些实施方案中,被取代的基团或部分携带五个取代基。
[0418]
本文描绘的任何式都意图代表具有那个结构式以及某些变化形式或形式的化合物。举例来说,本文给出的式意图包括外消旋形式、或一种或多种对映异构、非对映异构或几何异构体、或它们的混合物。另外,本文给出的任何式都意图还指代此种化合物的水合物、溶剂化物或多晶型物、或它们的混合物。
[0419]
本文给出的任何式都还意图代表化合物的未标记形式以及经同位素标记形式。经同位素标记化合物具有由本文给出的式描绘的结构,例外之处是一个或多个原子被具有所选原子质量或质量数的原子替换。可并入至本公开化合物中的同位素的实例包括氢、碳、氮、氧、磷、氟、氯和碘的同位素,诸如分别是2h、3h、
11
c、
13
c、
14
c、
15
n、
18
o、
17
o、
31
p、
32
p、
35
s、
18
f、
36
cl和
125
i。此类经同位素标记化合物可用于代谢研究(优选地采用
14
c)、反应动力学研究(采用例如2h或3h)、检测或成像技术[诸如正电子发射断层摄影术(pet)或单光子发射计算机断层摄影术(spect)],包括药物或底物组织分布测定中,或对患者的放射性治疗中。具体地说,对于pet或spect研究,经
18
f或
11
c标记化合物可为特别优选的。可如例如由brooks,d.j.,“positron emission tomography and single-photon emission computed tomography in central nervous system drug development,”neurorx2005,2(2),226-236以及其中引用的参考文献所述来进行pet和spect研究。此外,用重同位素诸如氘(即2h)取代可提供某些由较大代谢稳定性所致的治疗优势,例如体内半衰期增加或剂量需求降低。可通常通过执行以下描述的在流程中或在实施例和制备中公开的程序,用可易于获得的经同位素标记试剂替代非经同位素标记试剂来制备经同位素标记的本公开化合物及其前药。
[0420]
命名法“c
i-j”,其中j》i,当在本文中应用于一类取代基时,意图指代独立地实现从i至j,包括i和j的每一个碳成员数目的本公开的实施方案。举例来说,术语c
1-3
独立地指代具有一个碳成员(c1)的实施方案、具有两个碳成员(c2)的实施方案以及具有三个碳成员(c3)的实施方案。
[0421]
当超过一种连接可能性被允许时,本文提及的任何二取代基都意图涵盖各种此类可能性。举例来说,提及二取代基
–
a-b-,其中a≠b,在本文中是指a连接于第一被取代成员,并且b连接于第二被取代成员的此二取代基,并且这还指a连接于所述第二被取代成员,并且b连接于所述第一被取代成员的此二取代基。
[0422]
本公开还包括由式(a)和式(b)表示的化合物或表1a和表1b的化合物的药学上可接受的盐以及包含此类盐的药物组合物和使用此类盐的方法。
[0423]“药学上可接受的盐”意指本文表示的化合物的游离酸或碱的无毒、生物可耐受、或在其他方面在生物学上适于施用至受试者的盐。一般地参见s.m.berge,等人,“pharmaceutical salts,”j.pharm.sci.,1977,66,1-19。特定药学上可接受的盐是在药理学上有效,并且适于与受试者的组织接触而无过度毒性、刺激或过敏应答的那些。本文所述的化合物可具有酸性足够的基团、碱性足够的基团、两种类型的官能团,或每种类型超过一个官能团,因此与许多无机或有机碱以及无机和有机酸反应以形成药学上可接受的盐。
[0424]
药学上可接受的盐的实例包括硫酸盐、焦硫酸盐、硫酸氢盐、亚硫酸盐、亚硫酸氢盐、磷酸盐、磷酸一氢盐、磷酸二氢盐、偏磷酸盐、焦磷酸盐、氯化物、溴化物、碘化物、乙盐酸、丙酸盐、癸酸盐、辛酸盐、丙烯酸盐、甲酸盐、异丁酸盐、己酸盐、庚酸盐、丙炔酸盐、草酸盐、丙二酸盐、丁二酸盐、辛二酸盐、癸二酸盐、反丁烯二酸盐、顺丁烯二酸盐、丁炔-1,4-二酸盐、己炔-1,6-二酸盐、苯甲酸盐、氯苯甲酸盐、甲基苯甲酸盐、二硝基苯甲酸盐、羟基苯甲酸盐、甲氧基苯甲酸盐、邻苯二甲酸盐、磺酸盐、甲基磺酸盐、丙基磺酸盐、苯磺酸盐、二甲苯磺酸盐、萘-1-磺酸盐、萘-2-磺酸盐、苯基乙酸盐、苯基丙酸盐、苯基丁酸盐、柠檬酸盐、乳酸盐、γ-羟基丁酸盐、乙醇酸盐、酒石酸盐和扁桃酸盐。其他适合药学上可接受的盐的清单见于remington's pharmaceutical sciences,第17版,mack publishing company,easton,pa.,1985中。
[0425]
对于含有碱性氮的式(a)或式(b)化合物或表1a或表1b的化合物,可通过本领域中可用的任何适合方法制备药学上可接受的盐,例如用无机酸处理游离碱,所述无机酸诸如是盐酸、氢溴酸、硫酸、氨基磺酸、硝酸、硼酸、磷酸等,或用有机酸处理游离碱,所述有机酸诸如是乙酸、苯基乙酸、丙酸、硬脂酸、乳酸、抗坏血酸、顺丁烯二酸、羟基顺丁烯二酸、羟基乙磺酸、丁二酸、戊酸、反丁烯二酸、丙二酸、丙酮酸、草酸、乙醇酸、水杨酸、油酸、棕榈酸、月桂酸、吡喃糖苷酸诸如葡萄糖醛酸或半乳糖醛酸,α-羟基酸诸如扁桃酸、柠檬酸或酒石酸,氨基酸诸如天冬氨酸或谷氨酸,芳族酸诸如苯甲酸、2-乙酰氧基苯甲酸、萘甲酸或肉桂酸,磺酸诸如月桂基磺酸、对甲苯磺酸、甲烷磺酸或乙烷磺酸,或酸诸如在本文中作为实例给出的那些酸的任何可相容混合物以及根据本技术中的普通技能水平被视为等效物或可接受替代物的任何其他酸及其混合物。
[0426]
本公开还涉及式(a)或式(b)化合物或表1a和表1b的化合物的药学上可接受的前药以及采用此类药学上可接受的前药的治疗方法。术语“前药”意指指定化合物的前体,所述前体在施用至受试者之后通过化学或生理过程诸如溶剂分解或酶促裂解,或在生理条件
下(例如前药在致使达到生理ph时转化成式化合物),在体内产生所述化合物。“药学上可接受的前药”是无毒、生物可耐受、并且在其他方面在生物学上适于施用至受试者的前药。用于选择和制备适合前药衍生物的说明性程序例如描述于“design of prodrugs”,h.bundgaard编,elsevier,1985中。
[0427]
本公开还涉及式(a)或式(b)化合物或表1a和表1b的化合物的药物活性代谢物以及此类代谢物在本文提供的方法中的用途。“药物活性代谢物”意指式(a)或式(b)化合物或表1a和表1b的化合物或任何前述项的盐的在身体中的药理活性代谢产物。可使用本领域中已知或可用的常规技术确定化合物的前药和活性代谢物。参见例如bertolini等人,j.med.chem.1997,40,2011-2016;shan等人,j.pharm.sci.1997,86(7),765-767;bagshawe,drug dev.res.1995,34,220-230;bodor,adv.drug res.1984,13,255-331;bundgaard,design of prodrugs(elsevier press,1985);以及larsen,design and application of prodrugs,drug design and development(krogsgaard-larsen等人编,harwood academic publishers,1991)。
[0428]
药物组合物
[0429]
出于治疗目的,包含本文所述的化合物的药物组合物还可包含一种或多种药学上可接受的赋形剂。药学上可接受的赋形剂是无毒,并且在其他方面在生物学上适于施用至受试者的物质。此类赋形剂有助于本文所述的化合物的施用,并且可与活性成分相容。药学上可接受的赋形剂的实例包括稳定剂、润滑剂、表面活性剂、稀释剂、抗氧化剂、粘合剂、着色剂、增积剂、乳化剂或味道调节剂。在特定实施方案中,本公开的药物组合物是无菌组合物。可使用为本领域技术人员所知或变得可为本领域技术人员所用的混配技术制备药物组合物。
[0430]
本公开还考虑无菌组合物,包括合乎管控此类组合物的国家和地方法规的组合物。
[0431]
可根据本领域中已知的用于制备各种剂型的常规方法,将本文所述的药物组合物和化合物配制成在适合药物溶剂或载体中的溶液、乳液、混悬剂或分散液,或连同固体载体一起配制成丸剂、片剂、糖锭、栓剂、小袋剂、糖衣片、颗粒剂、粉剂、复原用粉剂、或胶囊。可通过适合递送途径诸如口服、胃肠外、经直肠、经鼻、表面或经眼途径或通过吸入来施用本公开的药物组合物。在一些实施方案中,组合物被配制用于静脉内或口服施用。
[0432]
对于口服施用,本公开化合物可以固体形式提供,诸如片剂或胶囊,或以溶液、乳液或混悬剂形式提供。为制备口服组合物,可配制本公开化合物以产生例如每日约0.01至约50mg/kg、或每日约0.05至约20mg/kg、或每日约0.1至约10mg/kg的剂量。额外剂量包括每日约0.1mg至1g、每日约1mg至约10mg、每日约10mg至约50mg、每日约50mg至约250mg、或每日约250mg至1g。口服片剂可包括一种或多种与可相容药学上可接受的赋形剂诸如稀释剂、崩解剂、粘合剂、润滑剂、甜味剂、调味剂、着色剂和防腐剂混合的活性成分。适合惰性填充剂包括碳酸钠和碳酸钙、磷酸钠和磷酸钙、乳糖、淀粉、糖、葡萄糖、甲基纤维素、硬脂酸镁、甘露糖醇、山梨糖醇等。示例性液体口服赋形剂包括乙醇、甘油、水等。淀粉、聚乙烯吡咯烷酮(pvp)、淀粉乙醇酸钠、微晶纤维素和海藻酸是示例性崩解剂。粘合剂可包括淀粉和明胶。如果存在,那么润滑剂可为硬脂酸镁、硬脂酸或滑石。如果需要,那么可用诸如单硬脂酸甘油酯或二硬脂酸甘油酯的材料包覆片剂以延迟在胃肠道中的吸收,或可用肠溶性包衣包覆。
[0433]
用于口服施用的胶囊包括硬质和软质明胶胶囊。为制备硬质明胶胶囊,可将一种或多种活性成分与固体、半固体或液体稀释剂混合。可通过将活性成分与水、油诸如花生油或橄榄油、液体石蜡、短链脂肪酸的甘油单酯和甘油二酯的混合物、聚乙二醇400或丙二醇混合来制备软质明胶胶囊。
[0434]
用于口服施用的液体可呈混悬剂、溶液、乳液或糖浆的形式,或可被冻干或呈现为干燥产品以在使用之前用水或其他适合媒介物复原。此类液体组合物可任选地含有:药学上可接受的赋形剂诸如助悬剂(例如山梨糖醇、甲基纤维素、海藻酸钠、明胶、羟乙基纤维素、羧甲基纤维素、硬脂酸铝凝胶等);非水性媒介物,例如油(例如杏仁油或分馏椰子油)、丙二醇、乙醇或水;防腐剂(例如对羟基苯甲酸甲酯或对羟基苯甲酸丙酯或山梨酸);湿润剂诸如卵磷脂;以及如果需要的话,调味剂或着色剂。
[0435]
本发明组合物可被配制用于以栓剂经直肠施用。对于胃肠外使用,包括静脉内、肌肉内、腹膜内、鼻内或皮下途径,本公开的剂可于缓冲至适当ph和等张性的无菌水性溶液或悬浮液中提供,或于胃肠外可接受的油中提供。适合水性媒介物包括林格氏溶液(ringer's solution)和等张氯化钠。此类形式可以单位剂量形式诸如安瓿或抛弃式注射装置呈现,以多次剂量形式诸如可从其取出适当剂量的小瓶呈现,或以可用于制备可注射制剂的固体形式或预浓缩物呈现。说明性输注剂量在历经在数分钟至数天的范围内的时期,约1至1000μg/kg/分钟的与药物载体掺混的剂的范围内。
[0436]
对于经鼻、吸入或口服施用,可使用例如还含有适合载体的喷雾制剂来施用本发明药物组合物。
[0437]
对于表面施加,本公开化合物可被配制成乳膏剂或软膏剂或适于表面施用的类似媒介物。对于表面施用,可将本发明化合物与药物载体在药物相对于媒介物是约0.1%至约10%的浓度下混合。施用本公开的剂的另一模式可利用贴片制剂来实现经皮递送。
[0438]
如本文所用,“治疗(treatment/treating)”是用于获得包括临床结果的有益或所需结果的方法。出于本公开的目的,有益或所需结果包括但不限于:减轻疾病、症状或疾患的严重性或阻抑疾病、症状或疾患的恶化,缓和症状以及/或者减弱症状的程度以及/或者预防与疾患相关的症状的恶化,遏止疾病、症状或疾患的发展,缓解疾病、症状或疾患,导致疾病、病症或症状的消退(就负面症状的严重性或频率而言),或终止疾病或疾患的症状。有益或所需结果还可为减缓、停止或逆转疾病或疾患的进行性过程。举例来说,有益作用可包括减缓帕金森氏病的从较早期(例如前驱期或1、2或3期)向较晚期(例如4或5期)的进展,或使帕金森氏病停止在前驱期或早期。
[0439]
如本文所用,“延迟”疾病或疾患的发展意指推迟、阻碍、减缓、延缓、稳定和/或推延所述疾病或疾患的发展。视病史和/或所治疗的个体而定,这个延迟可具有不同时长。如为本领域技术人员所显而易知,充分或显著延迟可实际上涵盖预防,因为个体不显现疾病或疾患。举例来说,“延迟”帕金森氏病(例如前驱个体中)的发展的方法是以下方法:当相较于不使用所述方法时,所述方法降低在给定时间范围内的疾病发展概率,以及/或者减轻在给定时间范围内的疾病程度。
[0440]
术语“受试者”是指需要此治疗的哺乳动物患者,诸如人。“受试者”可为人,或可为猫、狗、母牛、大鼠、小鼠、马、兔或其他驯化哺乳动物。
[0441]
特征在于蛋白质聚集的示例性疾病包括阿尔茨海默氏病、帕金森氏病、额颞性痴
呆、路易体痴呆(路易体病)、伴有痴呆的帕金森氏病、多系统萎缩、肌萎缩性侧索硬化、亨廷顿氏病、进行性核上麻痹(psp)和c型尼曼-皮克病、以及炎症性疾病诸如哮喘、慢性阻塞性肺病(copd)、慢性消化性溃疡、肠易激疾病、结核病、类风湿性关节炎、骨关节炎、慢性鼻窦炎、肝炎(诸如乙型肝炎或丙型肝炎)、痛风、狼疮、胸膜炎、湿疹、胃炎、牛皮癣、牛皮癣性关节炎、血管炎、喉炎、过敏反应、多发性硬化症、克罗恩氏病、创伤性脑损伤、cidp(慢性炎症性脱髓鞘性多发性神经病变)、中风、缺血性心脏病、特应性皮炎、寻常痤疮、红斑痤疮、非酒精性脂肪肝病、非酒精性脂肪性肝炎、角膜创伤、角膜病症、角膜hsv、施塔加特病(青少年黄斑变性)、年龄相关的黄斑变性、败血症、糖尿病创伤、单纯疱疹病毒、以及抗真菌、抗细菌、抗病毒和抗肿瘤疾病或疾患。
[0442]
在一个方面,本公开的化合物和药物组合物特异性靶向tlr2蛋白二聚体。因此,这些化合物和药物组合物可用于预防、逆转、减缓或抑制tlr2蛋白与其他天然蛋白质配体的二聚化,并且在本公开的方法中用于治疗与此二聚化相关或由此二聚化引起的神经和炎症性疾病。在一些实施方案中,治疗方法靶向帕金森氏病、阿尔茨海默氏病、路易体病、多系统萎缩、特应性皮炎、创伤性脑损伤或多发性硬化症。本公开的化合物、组合物和方法还用于缓和继发于蛋白质二聚化和/或错误折叠的有害影响,诸如神经元细胞死亡。在另一方面,本公开的化合物和药物组合物是tlr9的抑制剂。在一些实施方案中,本公开的化合物和药物组合物在本公开的方法中用于治疗中枢神经系统(cns)和外周病症。在一些实施方案中,治疗方法靶向帕金森氏病、肌萎缩性侧索硬化、格林-巴利综合征、脊髓损伤、多发性硬化症、多种形式的组织损伤、慢性疼痛或牛皮癣。
[0443]
在一些方面,本公开的化合物、组合物和方法用于抑制tlr2二聚化。在替代性方面,本公开的化合物、组合物和方法用于抑制tlr2与tlr1或与tlr6或与两者的二聚化。
[0444]
在本公开的抑制性方法中,“有效量”意指足以降低tlr2二聚化,减缓tlr2二聚化的进展,或逆转tlr2二聚化的量。可通过常规分析方法诸如以下描述的那些来进行对二聚化的量的测量。此调节可用于多种环境中,包括体外测定。在此类方法的一些实施方案中,细胞是神经细胞或hek或thp细胞。
[0445]
在本公开的治疗方法中,“有效量”意指足以总体上在需要此治疗的受试者中导致所需治疗益处的量或剂量。可在考虑常规因素例如施用或药物递送的模式或途径、剂的药物代谢动力学、感染的严重性和进程、受试者的健康状态、状况和重量,以及治疗医师的判断的情况下,通过常规方法诸如建模、剂量逐步升高或临床试验来确定本公开化合物的有效量或剂量。示例性剂量在每天每千克受试者的体重约1μg至2mg活性剂,诸如约0.05至100mg/kg/天、或约1至35mg/kg/天、或约0.1至10mg/kg/天的范围内。在替代性实施方案中,示例性剂量在每天约1mg至约1g,或每天约1-500、1-250、1-100、1-50、50-500、或250-500mg的范围内。总剂量可以单次或分次剂量单位(例如bid、tid、qid)给与。
[0446]
一旦已发生患者的疾病改善,即可调整剂量以进行预防性或维持治疗。举例来说,可随症状而变化来使施用剂量或施用频率或两者降低至维持所需治疗或防治作用所处的水平。当然,如果症状已被缓和至适当水平,那么可停止治疗。然而,在症状的任何复发后,患者可需要长期间歇治疗。患者还可需要长期慢性治疗。
[0447]
药物组合
[0448]
本文所述的本发明化合物可与一种或多种额外活性成分组合用于药物组合物或
方法中治疗神经变性病症。用于癌症应用的其他额外活性成分包括其他癌症治疗剂或缓和癌症化学治疗剂的不利影响的剂。此类组合可用于增加功效,改善其他疾病症状,降低一种或多种副作用,或降低本发明化合物的所需剂量。额外活性成分可以与本公开的化合物分开的药物组合物施用,或可与本公开的化合物一起包括在单一药物组合物中。额外活性成分可与本公开的化合物的施用同时,在本公开的化合物的施用之前或之后施用。
[0449]
组合剂包括额外活性成分,所述额外活性成分是已知或被发现在治疗本文讨论的疾病、病症、疾患和症状方面有效的那些,包括针对与疾病、病症或症状相关的另一靶标具有活性的那些,诸如但不限于a)解决蛋白质错误折叠的化合物(诸如降低这些蛋白质的产生,增加它们的清除,或改变它们的聚集和/或传播的药物);b)治疗此类病症的症状的化合物(例如多巴胺替代疗法);和c)通过补充性机制来充当神经保护剂的药物(例如靶向自体吞噬的那些、是抗氧化剂的那些、以及通过其他机制来起作用的那些,诸如腺苷a2a拮抗剂)。
[0450]
举例来说,本公开的组合物和制剂以及治疗方法可还包含其他药物或药品,例如可用于治疗或缓和与tlr2二聚化相关或由tlr2二聚化引起的神经或炎症性疾病例如帕金森氏病、阿尔茨海默氏病(ad)、路易体病(lbd)和多系统萎缩(msa)、或相关症状或状况的其他活性剂。举例来说,本公开的药物组合物可另外包含此类活性剂中的一者或多者,并且治疗方法可另外包括施用有效量的此类活性剂中的一者或多者。在某些实施方案中,额外活性剂可为抗生素(例如抗细菌或抑菌肽或蛋白质),例如针对革兰氏阳性或阴性细菌有效的那些,液体、细胞因子、免疫调控剂、消炎剂、补体活化剂,诸如包含胶原样结构域或纤维蛋白原样结构域(例如纤胶凝蛋白(ficolin))、碳水化合物结合结构域等的肽或蛋白质,以及它们的组合。额外活性剂包括可用于此类组合物和方法中的那些,包括多巴胺治疗药物、儿茶酚-o-甲基转移酶(comt)抑制剂、单胺氧化酶抑制剂、认知增强剂(诸如乙酰胆碱酯酶抑制剂或美金刚(memantine))、腺苷2a受体拮抗剂、β-分泌酶抑制剂或γ-分泌酶抑制剂。在特定实施方案中,至少一种本公开的化合物可与一种或多种选自由以下组成的组的药物一起在药物组合物或治疗方法中组合:塔克林(tacrine)(科奈斯(cognex))、多奈哌齐(donepezil)(安理申(aricept))、利凡斯的明(rivastigmine)(艾斯能(exelon))、加兰他敏(galantamine)(利忆灵(reminyl))、毒扁豆碱(physostigmine)、新斯的明(neostigmine)、艾考哌齐(icopezil)(cp-118954,5,7-二氢-3-[2-[1-(苯基甲基)-4-哌啶基]乙基]-6h-吡咯并-[4,5-f-]-1,2-苯并异噁唑-6-酮顺丁烯二酸盐)、er-127528(4-[(5,6-二甲氧基-2-氟-1-茚满酮)-2-基]甲基-1-(3-氟苯甲基)哌啶盐酸盐)、扎那哌齐(zanapezil)(tak-147;3-[1-(苯基甲基)哌啶-4-基]-1-(2,3,4,5-四氢-1h-1-苯并氮杂环庚三烯-8-基)-1-丙烷反丁烯二酸盐)、美曲膦酯(metrifonate)(t-588;(-)-r-α-[[2-(二甲基氨基)乙氧基]甲基]苯并[b]噻吩-5-甲醇盐酸盐)、fk-960(n-(4-乙酰基-1-哌嗪基)-对氟苯甲酰胺水合物)、tch-346(n-甲基-n-2-丙炔基二苯并[b,f]氧杂环庚三烯-10-甲胺)、sdz-220-581((s)-α-氨基-5-(膦酰基甲基)-[1,1'-联苯]-3-丙酸)、美金刚(纳蒙达(namenda)/埃克西巴(exiba))和1,3,3,5,5-五甲基环己-1-胺(奈拉美生(neramexane))、塔伦氟比(tarenflurbil)(氟卢里赞(flurizan))、曲米沙特(tramiprosate)(阿折梅德(alzhemed))、氯碘羟喹(clioquinol)、pbt-2(一种8-羟基喹啉衍生物)、1-(2-(2-萘基)乙基)-4-(3-三氟甲基苯基)-1,2,3,6-四氢吡啶、石杉碱a(huperzine a)、泊替瑞林
(posatirelin)、亮脯利特(leuprolide)或其衍生物、异丙克兰(ispronicline)、(3-氨基丙基)(正丁基)次膦酸(sgs-742)、n-甲基-5-(3-(5-异丙氧基吡啶基))-4-戊烯-2-胺(异丙克兰)、n-(2-羟基-3-磺基丙基)-n-甲基-n-辛基-1-癸铵内盐(zt-1)、水杨酸盐/酯、阿司匹林(aspirin)、阿莫西普林(amoxiprin)、贝诺酯(benorilate)、水杨酸胆碱镁(choline magnesium salicylate)、二氟尼柳(diflunisal)、菲斯胺(faislamine)、水杨酸甲酯(methyl salicylate)、水杨酸镁、水杨酸水杨酯、双氯芬酸(diclofenac)、乙酰氯芬酸(aceclofenac)、阿西美辛(acemetacin)、溴芬酸(bromfenac)、依托度酸(etodolac)、吲哚美辛(indometacin)、萘丁美酮(nabumetone)、舒林酸(sulindac)、托美丁(tolmetin)、布洛芬(ibuprofen)、卡洛芬(carprofen)、芬布芬(fenbufen)、非诺洛芬(fenoprofen)、氟比洛芬(flurbiprofen)、酮洛芬(ketoprofen)、酮咯酸(ketorolac)、氯索洛芬(loxoprofen)、萘普生(naproxen)、噻洛芬酸(tiaprofenic acid)、舒洛芬(suprofen)、甲灭酸(mefenamic acid)、甲氯灭酸(meclofenamic acid)、苯基丁氮酮(phenylbutazone)、阿扎丙酮(azapropazone)、安乃近(metamizole)、羟保泰松(oxyphenbutazone)、磺吡酮(sulfinprazone)、吡罗昔康(piroxicam)、氯诺昔康(lornoxicam)、美洛昔康(meloxicam)、替诺昔康(tenoxicam)、塞来昔布(celecoxib)、依托昔布(etoricoxib)、罗美昔布(lumiracoxib)、帕瑞昔布(parecoxib)、罗非昔布(rofecoxib)、伐地昔布(valdecoxib)、尼美舒利(nimesulide)、芳基烷酸、2-芳基丙酸(洛芬(profen))、n-芳基邻氨基苯甲酸(灭酸(fenamic acid))、吡唑烷衍生物、昔康(oxicam)、cox-2抑制剂、磺酰苯胺(sulphonanilide)、必需脂肪酸和米诺扎(2-(4-(4-甲基-6-苯基哒嗪-3-基)哌嗪-1-基)嘧啶二盐酸盐水合物)、或它们的组合。
[0451]
使用方法
[0452]
本文化合物和药物组合物可用于治疗或预防个体中的疾病或疾患。在一些实施方案中,提供了治疗与tlr2异二聚化相关的疾病或疾患的方法,所述方法包括向有需要的个体施用式(a)或式(b)化合物、或表1a或表1b的化合物、或它们的互变异构体、或任何前述项的药学上可接受的盐。在一些实施方案中,提供了治疗与tlr2异二聚化相关的疾病或疾患的方法,所述方法包括向受试者施用治疗有效量的至少一种如本文所述的化学实体。
[0453]
在一些实施方案中,提供了含有一种或多种式(a)或式(b)化合物、或表1a或表1b的化合物、或它们的互变异构体、或任何前述项的药学上可接受的盐的组合物,所述组合物用于治疗与tlr2异二聚化相关的疾病或疾患。在一些实施方案中,提供了含有至少一种如本文所述的化学实体的组合物,所述组合物用于治疗与tlr2异二聚化相关的疾病或疾患。
[0454]
本文还提供了式(a)或式(b)化合物、或表1a或表1b的化合物、或它们的互变异构体、或任何前述项的药学上可接受的盐制造用于治疗与tlr2异二聚化相关的疾病或疾患的药剂的用途。在一些实施方案中,提供了至少一种如本文所述的化学实体制造用于治疗与tlr2异二聚化相关的疾病或疾患的药剂的用途。
[0455]
在一些实施方案中,疾病或疾患选自阿尔茨海默氏病、帕金森氏病、额颞性痴呆、路易体痴呆(路易体病)、伴有痴呆的帕金森氏病、多系统萎缩、肌萎缩性侧索硬化、亨廷顿氏病、进行性核上麻痹(psp)、c型尼曼-皮克病、炎症性疾病、哮喘、慢性阻塞性肺病(copd)、慢性消化性溃疡、肠易激疾病、结核病、类风湿性关节炎、骨关节炎、慢性鼻窦炎、肝炎、乙型肝炎、丙型肝炎、痛风、狼疮、胸膜炎、湿疹、胃炎、牛皮癣、牛皮癣性关节炎、血管炎、喉炎、过
敏反应、多发性硬化症、克罗恩氏病、创伤性脑损伤、cidp(慢性炎症性脱髓鞘性多发性神经病变)、中风、缺血性心脏病、特应性皮炎、寻常痤疮、红斑痤疮、非酒精性脂肪肝病、非酒精性脂肪性肝炎、角膜创伤、角膜病症、角膜hsv、施塔加特病(青少年黄斑变性)、年龄相关的黄斑变性、败血症、糖尿病创伤、单纯疱疹病毒、以及抗真菌、抗细菌、抗病毒和抗肿瘤疾病或疾患。在一些实施方案中,疾病或疾患选自阿尔茨海默氏病、帕金森氏病、额颞性痴呆、路易体痴呆(路易体病)、伴有痴呆的帕金森氏病、多系统萎缩、肌萎缩性侧索硬化、亨廷顿氏病、炎症性疾病、哮喘、慢性阻塞性肺病(copd)、慢性消化性溃疡、结核病、类风湿性关节炎、慢性鼻窦炎、肝炎、乙型肝炎、丙型肝炎、痛风、狼疮、胸膜炎、湿疹、胃炎、牛皮癣、牛皮癣性关节炎、血管炎、喉炎、过敏反应、多发性硬化症、克罗恩氏病和创伤性脑损伤。
[0456]
还提供了用于干扰细胞中tlr2的异二聚化,或调节、阻止、减缓、逆转或抑制细胞中的tlr2异二聚化的方法,所述方法涉及使所述细胞与有效量的至少一种式(a)或式(b)化合物、或表1a或表1b的化合物、或它们的互变异构体、或任何前述项的药学上可接受的盐接触。在一些实施方案中,提供了用于干扰细胞中tlr2的异二聚化,或调节、阻止、减缓、逆转或抑制细胞中的tlr2异二聚化的方法,所述方法涉及使所述细胞与有效量的至少一种如本文所述的化学实体接触。在一些实施方案中,提供了抑制细胞中的tlr2活化的方法,所述方法包括使所述细胞与有效量的至少一种式(a)或式(b)化合物、或表1a或表1b的化合物、或它们的互变异构体、或任何前述项的药学上可接受的盐、或包含任何前述项的药物组合物接触,其中所述接触是体外的,离体的,或体内的。
[0457]
本文还提供了含有一种或多种式(a)或式(b)化合物、或表1a或表1b的化合物、或它们的互变异构体、或任何前述项的药学上可接受的盐的组合物,所述组合物用于干扰细胞中tlr2的异二聚化,或调节、阻止、减缓、逆转或抑制细胞中的tlr2异二聚化。在一些实施方案中,提供了含有至少一种如本文所述的化学实体的组合物,所述组合物用于干扰细胞中tlr2的异二聚化,或调节、阻止、减缓、逆转或抑制细胞中的tlr2异二聚化。
[0458]
本文另外提供了至少一种如本文所述的化学实体诸如式(a)或式(b)化合物、或表1a或表1b的化合物、或它们的互变异构体、或任何前述项的药学上可接受的盐制造用于干扰tlr2的异二聚化,或调节、阻止、减缓、逆转或抑制tlr2异二聚化的药剂的用途。
[0459]
在一些实施方案中,提供了治疗与tlr9的抑制相关的疾病或疾患的方法,所述方法包括向有需要的个体施用式(a)或式(b)化合物、或表1a或表1b的化合物、或它们的互变异构体、或任何前述项的药学上可接受的盐。
[0460]
在一些实施方案中,提供了含有一种或多种式(a)或式(b)化合物、或表1a或表1b的化合物、或它们的互变异构体、或任何前述项的药学上可接受的盐的组合物,所述组合物用于治疗与tlr9的抑制相关的疾病或疾患。在一些实施方案中,提供了含有至少一种如本文所述的化学实体的组合物,所述组合物用于治疗与tlr9的抑制相关的疾病或疾患。
[0461]
本文还提供了式(a)或式(b)化合物、或表1a或表1b的化合物、或它们的互变异构体、或任何前述项的药学上可接受的盐制造用于治疗与tlr9的抑制相关的疾病或疾患的药剂的用途。在一些实施方案中,提供了至少一种如本文所述的化学实体制造用于治疗与tlr9的抑制相关的疾病或疾患的药剂的用途。
[0462]
在一些实施方案中,疾病或疾患是中枢神经系统(cns)或外周病症。在一些实施方案中,疾病或疾患是帕金森氏病、肌萎缩性侧索硬化、格林-巴利综合征、脊髓损伤、多发性
硬化症、多种形式的组织损伤、慢性疼痛或牛皮癣。
[0463]
还提供了抑制细胞中的tlr9的方法,所述方法涉及使所述细胞与有效量的至少一种式(a)或式(b)化合物、或表1a或表1b的化合物、或它们的互变异构体、或任何前述项的药学上可接受的盐接触。在一些实施方案中,提供了用于抑制细胞中的tlr9的方法,所述方法涉及使所述细胞与有效量的至少一种如本文所述的化学实体接触。在一些实施方案中,提供了抑制细胞中的tlr9活化的方法,所述方法包括使所述细胞与有效量的至少一种式(a)或式(b)化合物、或表1a或表1b的化合物、或它们的互变异构体、或任何前述项的药学上可接受的盐、或包含任何前述项的药物组合物接触,其中所述接触是体外的,离体的,或体内的。
[0464]
本文还提供了含有一种或多种式(a)或式(b)化合物、或表1a或表1b的化合物、或它们的互变异构体、或任何前述项的药学上可接受的盐的组合物,所述组合物用于抑制细胞中的tlr9。在一些实施方案中,提供了含有至少一种如本文所述的化学实体的组合物,所述组合物用于抑制细胞中的tlr9。
[0465]
本文另外提供了至少一种如本文所述的化学实体诸如式(a)或式(b)化合物、或表1a或表1b的化合物、或它们的互变异构体、或任何前述项的药学上可接受的盐制造用于抑制tlr9的药剂的用途。
[0466]
在一些实施方案中,本文所述的化合物,诸如式(a)或式(b)化合物、或表1a或表1b的化合物、或它们的互变异构体、或任何前述项的药学上可接受的盐,抑制tlr2与tlr9两者。在一些实施方案中,提供了治疗与tlr2异二聚化和/或tlr9的抑制相关的疾病或疾患的方法,所述方法包括向有需要的个体施用式(a)或式(b)化合物、或表1a或表1b的化合物、或它们的互变异构体、或任何前述项的药学上可接受的盐。在一些实施方案中,提供了治疗与tlr2异二聚化和/或tlr9的抑制相关的疾病或疾患的方法,所述方法包括向受试者施用治疗有效量的至少一种如本文所述的化学实体。
[0467]
在一些实施方案中,提供了含有一种或多种式(a)或式(b)化合物、或表1a或表1b的化合物、或它们的互变异构体、或任何前述项的药学上可接受的盐的组合物,所述组合物用于治疗与tlr2异二聚化和/或tlr9的抑制相关的疾病或疾患。在一些实施方案中,提供了含有至少一种如本文所述的化学实体的组合物,所述组合物用于治疗与tlr2异二聚化和/或tlr9的抑制相关的疾病或疾患。
[0468]
本文还提供了式(a)或式(b)化合物、或表1a或表1b的化合物、或它们的互变异构体、或任何前述项的药学上可接受的盐制造用于治疗与tlr2异二聚化和/或tlr9的抑制相关的疾病或疾患的药剂的用途。在一些实施方案中,提供了至少一种如本文所述的化学实体制造用于治疗与tlr2异二聚化和/或tlr9的抑制相关的疾病或疾患的药剂的用途。
[0469]
药盒
[0470]
还提供了含有本文提供的任何化合物或药物组合物的制品和药盒。制品可包括具有标签的容器。适合容器包括例如瓶、小瓶和试管。容器可由多种材料诸如玻璃或塑料形成。容器可容纳本文提供的药物组合物。容器上的标签可指示药物组合物用于预防、治疗或阻抑本文所述的疾患,并且还可指示关于体内或体外使用的说明。
[0471]
在一个方面,本文提供了含有本文所述的化合物或组合物以及使用说明书的药盒。药盒可含有关于在有需要的个体中的与tlr2异二聚化相关的疾病或疾患的治疗中使用
的说明书,和/或关于在有需要的个体中的与tlr9的抑制相关的疾病或疾患的治疗中使用的说明书。药盒可另外含有可用于施用化合物或组合物的任何材料或设备,诸如小瓶、注射器或iv袋。药盒还可含有无菌包装。
[0472]
一般性合成方法
[0473]
可通过如在以下一般地以及在下文实施例中更具体地描述的许多工艺(诸如以下实施例中提供的流程)制备本公开化合物。在以下工艺描述中,符号在用于描绘的式中时应理解为代表以上关于本文的式所述的那些基团。
[0474]
当需要获得化合物的特定对映异构体时,这可使用用于分离或拆分对映异构体的任何适合常规程序由对映异构体的相应混合物实现。因此,举例来说,可通过例如外消旋物的对映异构体混合物和适当手性化合物的反应来产生非对映异构衍生物。可接着通过任何适宜手段,例如通过结晶来分离非对映异构体,并且回收所需对映异构体。在另一拆分工艺中,可使用手性高效液相色谱法分离外消旋物。或者,如果需要,那么可通过在所述工艺中的一者中使用适当手性中间体来获得特定对映异构体。
[0475]
当需要获得化合物的特定异构体或以其他方式纯化反应的产物时,色谱法、重结晶和其他常规分离程序还可与中间体或最终产物一起使用。
[0476]
还考虑本文提供的化合物或其药学上可接受的盐的溶剂化物。溶剂化物含有化学计算量或非化学计算量的溶剂,并且经常在结晶的过程期间形成。当溶剂是水时,形成水合物,或当溶剂是醇时,形成醇化物。
[0477]
在一些实施方案中,可根据流程a-1合成式(a)化合物。
[0478]
流程a-1.
[0479][0480]
其中r1、r2、r3、r4、g1、g2、y1、y2、y3、y4、y5和n如对于式(a)或本文详述的其任何变化形式所定义;hal是卤素;t是2或3;并且r是
–
oh、-o烷基或卤素,或
–
br
t
是
[0481]
在前述流程a-1的一些变化形式中,可根据流程a-1a合成式(a)化合物。
[0482]
流程a-1a.
[0483][0484]
其中r3、r4、ra和n如对于式(a)或本文详述的其任何变化形式所定义。
[0485]
在前述流程a-1的一些变化形式中,可根据流程a-1b合成式(a)化合物。
[0486]
流程a-1b.
[0487][0488]
其中r1、r2和r3如对于式(a)或本文详述的其任何变化形式所定义
[0489]
在一些实施方案中,可根据流程a-2合成式(a)化合物。
[0490]
流程a-2.
[0491]
[0492]
其中r1、r2、r3、y1、y2、y4、y5、g1、g2、g3、g4、g5、g6和g7如对于式(a)或本文详述的其任何变化形式所定义;hal是卤素;t是2或3;并且r是
–
oh、-o烷基或卤素,或
–
br
t
是是
[0493]
在前述流程a-2的一些变化形式中,可根据流程a-2a合成式(a)化合物。
[0494]
流程a-2a.
[0495][0496]
其中g3、g4、g5、g6和g7如对于式(a)或本文详述的其任何变化形式所定义。
[0497]
在前述流程a-2的一些变化形式中,可根据流程a-2b合成式(a)化合物。
[0498]
流程a-2b.
[0499][0500]
其中g3、g4、g5、g6和g7如对于式(a)或本文详述的其任何变化形式所定义。
[0501]
在一些实施方案中,可根据流程a-3合成式(a)化合物。
[0502]
流程a-3.
[0503][0504]
其中r3、rj、y1、y2、y3、y4、y5、g1、g2、g3、g4、g5、g6和g7如对于式(a)或本文详述的其任何变化形式所定义。
[0505]
在前述流程a-3的一些变化形式中,可根据流程a-3-a合成式(a)化合物。
[0506]
流程a-3-a.
[0507][0508]
其中rj如对于式(a)或本文详述的其任何变化形式所定义。
[0509]
在一些实施方案中,可根据流程a-4合成式(a)化合物。
[0510]
流程a-4.
[0511][0512]
其中r1、r2、r3、g1、g2、g3、g4、g5、g6和g7如对于式(a)或本文详述的其任何变化形式所定义,并且hal是卤素。
[0513]
在前述流程a-4的一些变化形式中,可根据流程a-4-a合成式(a)化合物。
[0514]
流程a-4-a.
[0515][0516]
其中r1、r2、r3、g3、g4、g5、g6和g7如对于式(a)或本文详述的其任何变化形式所定义,并且hal是卤素。
[0517]
在一些实施方案中,可根据流程a-5合成式(a)化合物。
[0518]
流程a-5.
[0519][0520]
其中r3、g1、g2、g3、g4、g5、g6和g7如对于式(a)或本文详述的其任何变化形式所定义,hal是卤素,并且pg1和pg2是适合保护基。
[0521]
在前述流程a-5的一些变化形式中,可根据流程a-5-a合成式(a)化合物。
[0522]
流程a-5-a.
[0523][0524]
其中r3、g3、g4、g5、g6和g7如对于式(a)或本文详述的其任何变化形式所定义,hal是卤素,并且pg1和pg2是适合保护基。
[0525]
在一些实施方案中,可根据流程b-1合成式(b)化合物。
[0526]
流程b-1.
[0527][0528]
其中r
3a
、y1、y2、y3、y4、y5、y6、y7和y8如对于式(b)或本文详述的其任何变化形式所定义;hal是卤素;并且pg是任何适合保护基。在一些变化形式中,适合保护基不是必需的,并且没有保护基存在于酚基团上。在其他变化形式中,适合保护基是pmb(4-甲氧基苯甲基)基团。
[0529]
在前述流程b-1的一些变化形式中,可根据流程b-1a合成式(b)化合物。
[0530]
流程b-1a.
[0531][0532]
其中r
3a
和r
6c1
如对于式(b)或本文详述的其任何变化形式所定义。在一些变化形式中,pmp是芳族醇的适合保护基。在一些变化形式中,适合保护基不是必需的,并且没有保护基存在于酚基团上。
[0533]
tms-diazomethane tms-重氮甲烷
[0534]
在一些实施方案中,可根据流程b-2a或流程b-2b合成式(b)化合物。
[0535]
流程b-2a.
[0536][0537]
流程b-2b.
[0538][0539]
其中r
3a
、y1、y2、y3、y4、y5、y6、y7和y8如对于式(b)或本文详述的其任何变化形式所定义;并且pg1和pg2是适合保护基。
[0540]
在前述流程b-2a的一些变化形式中,可根据流程b-2aa合成式(b)化合物。
[0541]
流程b-2aa.
[0542][0543]
其中y3、y4、y5、y6、y7和y8如对于式(b)或本文详述的其任何变化形式所定义。
[0544]
在一些实施方案中,可根据流程b-3a或流程b-3b合成式(b)化合物。
[0545]
流程b-3a.
[0546][0547]
流程b-3b.
[0548][0549]
其中r
3a
、y1、y2、y3、y4、y5、y6、y7和y8如对于式(b)或本文详述的其任何变化形式所定义。
[0550]
在前述流程b-3a的一些变化形式中,可根据流程b-3aa合成式(b)化合物。
[0551]
流程b-3aa.
[0552][0553]
其中y3、y4、y5、y6、y7和y8如对于式(b)或本文详述的其任何变化形式所定义。
[0554]
在一些实施方案中,可根据流程b-4a或流程b-4b合成式(b)化合物。
[0555]
流程b-4a.
[0556][0557]
流程b-4b.
[0558][0559]
其中r
2a
、r
3a
、y1、y2、y3、y4、y5、y6、y7和y8如对于式(b)或本文详述的其任何变化形式所定义,并且pg是适合保护基。
[0560]
在前述流程b-4a的一些变化形式中,可根据流程b-4aa合成式(b)化合物。
[0561]
流程b-4aa.
[0562][0563]
其中y3、y4、y5、y6、y7和y8如对于式(b)或本文详述的其任何变化形式所定义。
[0564]
化学合成
[0565]
现将通过参考以下具体实施例来描述可用于本公开的方法中的示例性化学实体。技术人员将认识到,为获得本文各种化合物,可适合地选择起始物料以使将通过酌情采用或不采用保护的反应流程来携带最终所需的取代基以产生所需产物。或者,可必要或可合乎需要的是在最终所需的取代基的位置中采用可通过反应流程携带,并且酌情用所需取代基替换的适合基团。此外,本领域技术人员将认识到可以可与特定侧基的官能性相容的任
何顺序进行以下流程中所示的转化。可在约0℃至所用有机溶剂的回流温度的温度下进行一般性流程中描绘的反应中的每一者。根据以下描述的方法,使用适合标记的起始物料制备如本文所述的经同位素标记化合物。此类物料通常可从经放射性标记化学试剂的商业供应商获得。
[0566]
实施例
[0567]
以下实施例被提供来说明而非限制本公开。本领域技术人员将认识到可通过选择适合起始物料和试剂来修改以下合成反应和流程以获得其他式(a)和式(b)化合物。使用以上所述的一般性方法制备化合物。
[0568]
以下缩写遍及实施例加以使用:buli(丁基锂)、dcm(二氯甲烷)、dmf(n,n-二甲基甲酰胺)、dmso(二甲基亚砜)、ea或etoac(乙酸乙酯)、meoh(甲醇)、pdcl2(dppf)((1,1'-双(二苯基膦基)二茂铁)二氯化钯(ii))、dppf(1,1'-双(二苯基膦基)二茂铁、pd(pph3)2cl2(双(三苯基膦)二氯化钯(ii))、pd(pph3)4(四(三苯基膦)钯(0))、pmb(4-甲氧基苯甲基)、pph3(三苯基磷烷)、ruphos(2-二环己基膦基-2
′
,6
′‑
二异丙氧基联苯)、ruphos pd g3((2-二环己基膦基-2
′
,6
′‑
二异丙氧基-1,1
′‑
联苯)[2-(2
′‑
氨基-1,1
′‑
联苯)]甲烷磺酸钯(ii))、tbaf(四丁基氟化铵)、tfa(三氟乙酸)、thf(四氢呋喃)、tms-重氮甲烷(四甲基甲硅烷基重氮甲烷)、tlc(薄层色谱法)、xantphos(4,5-双(二苯基膦基)-9,9-二甲基呫吨)、xantphos pd g3([(4,5-双(二苯基膦基)-9,9-二甲基呫吨)-2-(2
′‑
氨基-1,1
′‑
联苯)]甲烷磺酸钯(ii))、xphos(2-二环己基膦基-2
′
,4
′
,6
′‑
三异丙基联苯)以及xphos pd g3((2-二环己基膦基-2
′
,4
′
,6
′‑
三异丙基-1,1
′‑
联苯)[2-(2
′‑
氨基-1,1
′‑
联苯)]甲烷磺酸钯(ii))。
[0569]
实施例a1:2-羟基-3-甲氧基-5-(1-苯基-1h-吡唑-4-基)苯甲醛(化合物编号a1)
[0570][0571]
在30ml密封盖玻璃小瓶中,将5-溴-2-羟基-3-甲氧基苯甲醛(231mg,1.0mmol)、1-苯基-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)-1h-吡唑(324mg,1.2mmol)和na2co3(666mg,6.0mmol)悬浮于dmf-水(10ml)中。接着鼓泡氩气一分钟,并且将pd(pph3)4(63mg,0.05mmol)添加至反应小瓶中并用密封盖密闭,并且在具有含有金属珠粒的盘的搅拌器板上在105℃下继续16小时。接着冷却至室温,并且用水(10ml)稀释并转移至使用二氯甲烷的分液漏斗中。用1.0n hcl将水层酸化至ph约3.0-4.0,并且用额外二氯甲烷(2x 50ml)萃取。将合并的有机层用盐水洗涤,经硫酸钠干燥并蒸发。使用硅胶柱色谱法(己烷直至己烷-etoac(0-100%))纯化所得粗产物以产生呈淡黄色固体状的标题化合物(63mg,21%产率)。1h nmr(500mhz,氯仿-d)δ11.01(s,1h),9.99(s,1h),8.14(s,1h),7.96(s,1h),7.78
–
7.70(m,2h),7.49(t,j=7.9hz,2h),7.39
–
7.30(m,2h),7.27(m,1h)4.01(s,3h);lc-ms m/z[m+h]
+
,c
17h14
n2o3的计算值:295;实测值:295。
[0572]
实施例a2:2-羟基-3-甲氧基-5-(1-(2-吗啉代乙基)-1h-吡唑-4-基)苯甲醛(化合物编号a2)
[0573][0574]
如实施例a1中所述从5-溴-2-羟基-3-甲氧基苯甲醛(231mg,1.0mmol)和4-(2-(4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)-1h-吡唑-1-基)乙基)吗啉(369mg,1.2mmol)制备标题化合物以产生呈黄色胶状固体状的标题化合物(108mg,33%产率)。1h nmr(500mhz,氯仿-d)δ10.95(s,1h),9.95(s,1h),7.68(s,1h),7.50(s,1h),7.46(d,j=2.3hz,1h),7.18(d,j=2.0hz,1h),4.27(m,2h),3.97(s,3h),3.69(m,6h),2.81(m,2h),2.48
–
2.41(m,4h);lc-ms m/z[m+h]
+
,c
17h21
n3o4的计算值:332;实测值:332。
[0575]
实施例a3:5-(1-(3-氯苯基)-1h-吡唑-4-基)-2-羟基-3-甲氧基苯甲醛(化合物编号a3)
[0576][0577]
如实施例a1中所述从5-溴-2-羟基-3-甲氧基苯甲醛(231mg,1.0mmol)和1-(3-氯苯基)-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)-1h-吡唑(267mg,1.2mmol)制备标题化合物以产生呈黄色固体状的标题化合物顺/反混合物(53mg,16%产率)。1h nmr(500mhz,氯仿-d)δ11.01(s,1h),9.99(s,1h),8.13(s,1h),7.96(s,1h),7.79(t,j=2.1hz,1h),7.64(dd,j=8.3,2.1hz,1h),7.42(t,j=8.1hz,1h),7.35(d,j=1.9hz,1h),7.33
–
7.28(m,1h),7.25(d,j=1.9hz,1h),4.01(s,3h);lc-ms m/z[m+h]
+
,c
17h13
cln2o3的计算值:330;实测值:330。
[0578]
实施例a4:5-(1-苯甲基-1h-吡唑-4-基)-2-羟基-3-甲氧基苯甲醛(化合物编号a4)
[0579][0580]
如实施例a1中所述从5-溴-2-羟基-3-甲氧基苯甲醛(231mg,1.0mmol)和1-苯甲基-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)-1h-吡唑(341mg,1.2mmol)制备标题化合物以产生呈棕色固体状的标题化合物(115mg,37%产率)。1h nmr(500mhz,氯仿-d)δ10.94(s,1h),9.93(s,1h),7.78(s,1h),7.59(d,j=3.9hz,1h),7.43
–
7.31(m,3h),7.30
–
7.26(m,2h),7.24(d,j=2.0hz,1h),7.16(d,j=1.9hz,1h),5.32(s,2h),3.95(s,3h);lc-ms m/z[m+h]
+
,c
18h16
n2o3的计算值:309;实测值:309。
[0581]
实施例a5:2-羟基-3-甲氧基-5-(1-(四氢-2h-吡喃-4-基)-1h-吡唑-4-基)苯甲醛
(化合物编号a5)
[0582][0583]
如实施例a1中所述从5-溴-2-羟基-3-甲氧基苯甲醛(231mg,1.0mmol)和1-(四氢-2h-吡喃-4-基)-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)-1h-吡唑(334mg,1.2mmol)制备标题化合物以产生呈棕色固体状的标题化合物(68mg,23%产率)。1h nmr(500mhz,氯仿-d)δ10.95(s,1h),9.95(s,1h),7.75(s,1h),7.69(m,1h),7.27(d,j=2.0hz,1h),7.19(d,j=2.0hz,1h),4.39(tt,j=10.4,4.9hz,1h),4.21
–
4.08(m,2h),3.97(s,3h),3.57(td,j=11.6,2.9hz,2h),2.22
–
2.01(m,4h);lc-ms m/z[m+h]
+
,c
16h18
n2o4的计算值:303;实测值:303。
[0584]
实施例a6:5-(1-(4-氟苯基)-1h-吡唑-4-基)-2-羟基-3-甲氧基苯甲醛(化合物编号a6)
[0585][0586]
如实施例a1中所述从5-溴-2-羟基-3-甲氧基苯甲醛(231mg,1.0mmol)和(1-(4-氟苯基)-1h-吡唑-4-基)硼酸(247mg,1.2mmol)制备标题化合物以产生呈黄色固体状的标题化合物(52mg,17%产率)。1h nmr(500mhz,氯仿-d)δ11.00(s,1h),9.99(s,1h),8.07(d,j=0.7hz,1h),7.95(d,j=0.7hz,1h),7.73
–
7.68(m,2h),7.35(d,j=2.1hz,1h),7.25(d,j=2.0hz,1h),7.21
–
7.16(m,2h),4.00(s,3h);lc-ms m/z[m+h]
+
,c
17h13
fn2o3的计算值:313;实测值:313。
[0587]
实施例a7:2-羟基-3-甲氧基-5-(1-(3-甲氧基丙基)-1h-吡唑-4-基)苯甲醛(化合物编号a7)
[0588][0589]
如实施例a1中所述从5-溴-2-羟基-3-甲氧基苯甲醛(231mg,1.0mmol)和1-(3-甲氧基丙基)-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)-1h-吡唑(319mg,1.2mmol)制备标题化合物以产生呈黑色胶状固体状的标题化合物(132mg,45%产率)。1h nmr(500mhz,氯仿-d)δ10.95(s,1h),9.95(s,1h),7.74(d,j=0.9hz,1h),7.62(d,j=0.9hz,1h),7.26(d,j=1.9hz,1h),7.19(d,j=2.1hz,1h),4.26(t,j=6.9hz,2h),3.97(s,3h),3.37(t,j=5.9hz,2h),3.35(s,3h),2.16(ddd,j=12.8,7.0,5.9hz,2h);lc-ms m/z[m+h]
+
,c
15h18
n2o4的计算值:291;实测值:291。
[0590]
实施例a8:2-羟基-3-甲氧基-5-(1-(吡啶-2-基甲基)-1h-吡唑-4-基)苯甲醛(化合物编号a8)
[0591][0592]
如实施例a1中所述从5-溴-2-羟基-3-甲氧基苯甲醛(231mg,1.0mmol)和2-((4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)-1h-吡唑-1-基)甲基)吡啶(342mg,1.2mmol)制备标题化合物以产生呈灰白色固体状的标题化合物(76mg,25%产率)。1h nmr(500mhz,氯仿-d)δ10.96(s,1h),9.94(s,1h),8.60(dt,j=4.8,1.4hz,1h),7.79(d,j=8.2hz,2h),7.67(qd,j=7.5,1.7hz,1h),7.27(d,j=2.0hz,1h),7.25
–
7.22(m,1h),7.19(d,j=1.9hz,1h),7.15(dt,j=7.9,1.1hz,1h),5.47(s,2h),3.96(s,3h);lc-ms m/z[m+h]
+
,c
17h15
n3o3的计算值:310;实测值:310。
[0593]
实施例a9:2-羟基-3-甲氧基-5-(1-(3-(三氟甲基)苯基)-1h-吡唑-4-基)苯甲醛(化合物编号a9)
[0594][0595]
如实施例a1中所述从5-溴-2-羟基-3-甲氧基苯甲醛(231mg,1.0mmol)和(1-(3-(三氟甲基)苯基)-1h-吡唑-4-基)硼酸(307mg,1.2mmol)制备标题化合物以产生呈黄色固体状的标题化合物(97mg,27%产率)。1h nmr(500mhz,氯仿-d)δ11.01(s,1h),9.99(s,1h),8.19(s,1h),8.02(d,j=1.9hz,1h),7.99(s,1h),7.96(dt,j=7.9,1.6hz,1h),7.62(t,j=7.9hz,1h),7.58(d,j=7.8hz,1h),7.37(d,j=2.0hz,1h),7.26(s,1h),4.01(s,3h);lc-ms m/z[m+h]
+
,c
18h13
f3n2o3的计算值:363;实测值:363。
[0596]
实施例a10:2-羟基-3-甲氧基-5-(1-(4-甲氧基苯甲基)-1h-吡唑-4-基)苯甲醛(化合物编号a10)
[0597][0598]
如实施例a1中所述从5-溴-2-羟基-3-甲氧基苯甲醛(231mg,1.0mmol)和1-(4-甲氧基苯甲基)-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)-1h-吡唑(377mg,1.2mmol)制备标题化合物以产生呈黄色固体状的标题化合物(90mg,27%产率)。1h nmr(500mhz,氯仿-d)δ10.94(s,1h),9.93(s,1h),7.76(s,1h),7.54(s,1h),7.26
–
7.22(m,3h),7.15(d,j=1.9hz,1h),6.94
–
6.89(m,2h),5.28(s,2h),3.95(s,3h),3.80(s,3h);lc-ms m/z[m+h]
+
,c
19h18
n2o4的计算值:339;实测值:339。
[0599]
实施例a11:3-氟-2-羟基-5-(1-苯基-1h-吡唑-4-基)苯甲醛(化合物编号a11)
[0600][0601]
如实施例a1中所述从5-溴-3-氟-2-羟基苯甲醛(219mg,1.0mmol)和1-苯基-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)-1h-吡唑(324mg,1.2mmol)制备标题化合物以产生呈黄色固体状的标题化合物(86mg,30%产率)。1h nmr(500mhz,氯仿-d)δ10.89(s,1h),10.00(d,j=1.9hz,1h),8.13(s,1h),7.95(s,1h),7.76
–
7.70(m,2h),7.58
–
7.52(m,2h),7.49(dt,j=8.4,7.0hz,2h),7.38
–
7.29(m,1h);lc-ms m/z[m+h]
+
,c
16h11
fn2o2的计算值:283;实测值:283。
[0602]
实施例a12:2-羟基-3-甲基-5-(1-苯基-1h-吡唑-4-基)苯甲腈(化合物编号a12)
[0603][0604]
如实施例a1中所述从5-溴-2-羟基-3-甲基苯甲腈(216mg,1.0mmol)和1-苯基-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)-1h-吡唑(324mg,1.2mmol)制备标题化合物以产生呈灰白色固体状的标题化合物(98mg,36%产率)。1h nmr(500mhz,氯仿-d)δ8.10(s,1h),7.92(s,1h),7.74
–
7.69(m,2h),7.55
–
7.52(m,1h),7.52
–
7.49(m,1h),7.49
–
7.45(m,2h),7.33(td,j=7.3,1.0hz,1h),5.87(s,1h),2.34(s,3h);lc-ms m/z[m+h]
+
,c
17h13
n3o的计算值:276;实测值:276。
[0605]
实施例a13:2,3-二氟-5-(1-苯基-1h-吡唑-4-基)苯酚(化合物编号a13)
[0606][0607]
如实施例a1中所述从5-溴-2,3-二氟苯酚(209mg,1.0mmol)和1-苯基-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)-1h-吡唑(324mg,1.2mmol)制备标题化合物以产生呈灰白色固体状的标题化合物(172mg,63%产率)。1h nmr(500mhz,氯仿-d)δ8.08(s,1h),7.90(s,1h),7.76
–
7.66(m,2h),7.53
–
7.43(m,2h),7.39
–
7.28(m,1h),6.97(dt,j=7.1,2.0hz,1h),6.91(ddd,j=10.7,6.6,2.2hz,1h),5.55(s,1h);lc-ms m/z[m+h]
+
,c
15h10
f2n2o的计算值:273;实测值:273。
[0608]
实施例a14:2-氟-3-甲基-5-(1-苯基-1h-吡唑-4-基)苯酚(化合物编号a14)
[0609][0610]
如实施例a1中所述从5-溴-2-氟-3-甲基苯酚(205mg,1.0mmol)和1-苯基-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)-1h-吡唑(324mg,1.2mmol)制备标题化合物以产生呈白色固体状的标题化合物(102mg,38%产率)。1h nmr(500mhz,氯仿-d)δ8.07(s,1h),7.91(s,1h),7.77
–
7.64(m,2h),7.51
–
7.40(m,2h),7.36
–
7.29(m,1h),7.02(dd,j=7.9,2.3hz,1h),6.90(dd,j=6.5,2.2hz,1h),5.40(s,1h),2.32(d,j=2.1hz,3h);lc-ms m/z[m+h]
+
,c
16h13
fn2o的计算值:269;实测值:269。
[0611]
实施例a15:2-氯-6-氟-4-(1-苯基-1h-吡唑-4-基)苯酚(化合物编号a15)
[0612][0613]
如实施例a1中所述从4-溴-2-氯-6-氟苯酚(225mg,1.0mmol)和1-苯基-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)-1h-吡唑(324mg,1.2mmol)制备标题化合物以产生呈灰白色固体状的标题化合物(196mg,68%产率)。1h nmr(500mhz,氯仿-d)δ8.08(s,1h),7.89(d,j=4.1hz,1h),7.79
–
7.65(m,2h),7.51
–
7.44(m,2h),7.36
–
7.30(m,2h),7.20(dd,j=11.0,2.1hz,1h),5.90(s,1h);lc-ms m/z[m+h]
+
,c
15h10
clfn2o的计算值:290;实测值:290。
[0614]
实施例a16:2-氟-3-甲氧基-5-(1-苯基-1h-吡唑-4-基)苯酚(化合物编号a16)
[0615][0616]
如实施例a1中所述从5-溴-2-氟-3-甲氧基苯酚(221mg,1.0mmol)和1-苯基-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)-1h-吡唑(324mg,1.2mmol)制备标题化合物以产生呈棕色固体状的标题化合物(205mg,72%产率)。1h nmr(500mhz,氯仿-d)δ8.09(s,1h),7.92(s,1h),7.82
–
7.67(m,2h),7.56
–
7.42(m,2h),7.36
–
7.28(m,1h),6.82(dd,j=7.2,2.1hz,1h),6.69(dd,j=7.2,2.1hz,1h),5.41(d,j=3.9hz,1h),3.95(s,3h);lc-ms m/z[m+h]
+
,c
16h13
fn2o2的计算值:285;实测值:285。
[0617]
实施例a17:2-氯-6-甲基-4-(1-苯基-1h-吡唑-4-基)苯酚(化合物编号a17)
[0618][0619]
如实施例a1中所述从4-溴-2-氯-6-甲基苯酚(222mg,1.0mmol)和1-苯基-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)-1h-吡唑(324mg,1.2mmol)制备标题化合物以产生呈棕色固体状的标题化合物(179mg,63%产率)。1h nmr(500mhz,氯仿-d)δ8.07(s,1h),7.90(s,1h),7.75
–
7.69(m,2h),7.51
–
7.44(m,2h),7.36(d,j=2.1hz,1h),7.31(td,j=7.4,1.3hz,1h),7.23(d,j=2.0hz,1h),5.60(s,1h),2.33(s,3h);lc-ms m/z[m+h]
+
,c
16h13
cln2o的计算值:286;实测值:286。
[0620]
实施例a18:2,6-二氟-4-(1-苯基-1h-吡唑-4-基)苯酚(化合物编号a18)
[0621][0622]
如实施例a1中所述从4-溴-2,6-二氟苯酚(209mg,1.0mmol)和1-苯基-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)-1h-吡唑(324mg,1.2mmol)制备标题化合物以产生呈白色固体状的标题化合物(195mg,72%产率)。1h nmr(500mhz,氯仿-d)δ8.08(s,1h),7.89(s,1h),7.76
–
7.66(m,2h),7.55
–
7.41(m,2h),7.39
–
7.29(m,1h),7.17
–
7.03(m,2h),5.34(s,1h);lc-ms m/z[m+h]
+
,c
15h10
f2n2o的计算值:273;实测值:273。
[0623]
实施例a19:3-氟-2-羟基-5-(1-(4-(吡咯烷-1-基)苯基)-1h-吡唑-4-基)苯甲醛(化合物编号a19)
[0624][0625]
步骤1:4-溴-1-(4-(吡咯烷-1-基)苯基)-1h-吡唑
[0626]
在氮气保护下使4-溴-1h-吡唑(1.75g,12mmol.)、1-(4-溴苯基)吡咯烷(2.25g,10mmol)、碳酸钾(4.14g,30mmol)、cui(190mg,1.0mmol)和(1s,2s)-n,n'-二甲基-1,2-环己二胺(284mg,2mmol)于甲苯(100ml)中的混合物回流过夜。使混合物冷却至室温并过滤。将滤饼用乙酸乙酯洗涤。将滤液和洗涤液合并,并且浓缩。将残余物通过硅胶柱来纯化以产生所需标题产物(910mg,31%产率)。lc-ms m/z[m+h]
+
,c
13h14
brn3的计算值:292;实测值:292。
[0627]
步骤2:在95℃下在氮气氛围下将4-溴-1-(4-(吡咯烷-1-基)苯基)-1h-吡唑(292mg,1.0mmol)、3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(532mg,2.0mmol)、碳酸钾(414mg,3.0mmol)、pdcl2(dppf)(74mg,0.1mmol)于二噁烷/
水(3:1)(12ml)中的混合物加热2小时。使混合物冷却至室温并过滤。将滤饼用乙酸乙酯洗涤。将滤液和洗涤液合并,用水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法来纯化以产生呈黄色固体状的标题产物(49mg,14%产率)。1h nmr(dmso-d6,400mhz)δ:10.87(br,1h),10.32(s,1h),8.83(s,1h),8.12(s,1h),7.92(d,j=12.0hz,1h),7.79(s,1h),7.64(d,j=8.4hz,2h),6.64(d,j=8.4hz,2h),3.27(m,4h),1.97(m,4h);lc-ms m/z[m+h]
+
,c
20h18
fn3o2的计算值:352;实测值:352。
[0628]
实施例a20:3-氟-2-羟基-5-(1-(4-(哌啶-1-基)苯基)-1h-吡唑-4-基)苯甲醛(化合物编号a20)
[0629][0630]
步骤1:1-(4-(4-溴-1h-吡唑-1-基)苯基)哌啶
[0631]
如实施例a19的步骤1中所述从4-溴-1h-吡唑(1.75g,12mmol.)、1-(4-溴苯基)哌啶(2.40g,10mmol)制备标题化合物以产生标题化合物(1.16g,38%产率)。lc-ms m/z[m+h]
+
,c
14h16
brn3的计算值:306;实测值:306。
[0632]
步骤2:如实施例a19的步骤2中所述从1-(4-(4-溴-1h-吡唑-1-基)苯基)哌啶(306mg,1.0mmol)和3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(532mg,2.0mmol)制备标题化合物以产生呈黄色固体状的标题化合物(128mg,35%产率)。1h nmr(dmso-d6,400mhz)δ:10.88(s,1h),10.32(s,1h),8.90(s,1h),8.15(s,1h),7.92(d,j=12.0hz,1h),7.80(s,1h),7.67(d,j=8.8hz,2h),7.05(d,j=8.8hz,2h),3.18(m,4h),1.63(m,4h),1.55(m,2h);lc-ms m/z[m+h]
+
,c
21h20
fn3o2的计算值:366;实测值:366。
[0633]
实施例a21:3-氟-2-羟基-5-(1-(4-吗啉代苯基)-1h-吡唑-4-基)苯甲醛(化合物编号a21)
[0634][0635]
步骤1:4-(4-(4-溴-1h-吡唑-1-基)苯基)吗啉
[0636]
如实施例a19的步骤1中所述从4-溴-1h-吡唑(1.75g,12mmol.)、4-(4-溴苯基)吗啉(2.42g,10mmol)制备标题化合物以产生标题化合物(1.14g,37%产率)。lc-ms m/z[m+h]
+
,c
13h14
brn3o的计算值:308;实测值:308。
[0637]
步骤2:如实施例a19的步骤2中所述从4-(4-(4-溴-1h-吡唑-1-基)苯基)吗啉(308mg,1.0mmol)和3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯
甲醛(532mg,2.0mmol)制备标题化合物以产生呈黄色固体状的标题化合物(63mg,17%产率)。.1h nmr(dmso-d6,400mhz)δ:10.89(s,1h),10.32(s,1h),8.93(s,1h),8.17(s,1h),7.93(d,j=12.0hz,1h),7.81(s,1h),7.72(d,j=8.8hz,2h),7.08(d,j=9.2hz,2h),3.76(m,4h),3.16(m,4h);lc-ms m/z[m+h]
+
,c
20h18
fn3o3的计算值:368;实测值:368。
[0638]
实施例a22:3-氟-2-羟基-5-(1-(3-(吡咯烷-1-基)苯基)-1h-吡唑-4-基)苯甲醛(化合物编号a22)
[0639][0640]
步骤1:4-溴-1-(3-(吡咯烷-1-基)苯基)-1h-吡唑
[0641]
如实施例a19的步骤1中所述从4-溴-1h-吡唑(1.75g,12mmol.)、1-(3-溴苯基)吡咯烷(2.26g,10mmol)制备标题化合物以产生标题化合物(876mg,30%产率)。lc-ms m/z[m+h]
+
,c
13h14
brn3的计算值:292;实测值:292。
[0642]
步骤2:如实施例a19的步骤2中所述从4-溴-1-(3-(吡咯烷-1-基)苯基)-1h-吡唑(292mg,1.0mmol)和3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(532mg,2.0mmol)制备标题化合物以产生呈淡黄色固体状的标题化合物(81mg,23%产率)。1h nmr(dmso-d6,400mhz)δ:10.91(s,1h),10.33(s,1h),9.02(s,1h),8.20(s,1h),7.96(d,j=12.0hz,1h),7.83(s,1h),7.26(m,1h),7.07(m,1h),7.00(s,1h),6.48(d,j=7.6hz,1h),3.31(m,4h),1.99(m,4h);lc-ms m/z[m+h]
+
,c
20h18
fn3o2的计算值:352;实测值:352。
[0643]
实施例a23:3-氟-2-羟基-5-(1-(3-(哌啶-1-基)苯基)-1h-吡唑-4-基)苯甲醛(化合物编号a23)
[0644][0645]
步骤1:1-(3-(4-溴-1h-吡唑-1-基)苯基)哌啶
[0646]
如实施例a19的步骤1中所述从4-溴-1h-吡唑(1.75g,12mmol.)、1-(3-溴苯基)哌啶(2.40g,10mmol)制备标题化合物以产生标题化合物(1.28g,42%产率)。lc-ms m/z[m+h]
+
,c
14h16
brn3的计算值:306;实测值:306。
[0647]
步骤2:如实施例a19的步骤2中所述从1-(3-(4-溴-1h-吡唑-1-基)苯基)哌啶(306mg,1.0mmol)和3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(532mg,2.0mmol)制备标题化合物以产生呈黄色固体状的标题化合物(110mg,30%产率)。1h nmr(dmso-d6,400mhz)δ:10.91(s,1h),10.33(s,1h),9.05(s,1h),8.21(s,1h),7.95(d,j=12.0hz,1h),7.83(s,1h),7.38(s,1h),7.28(m,1h),7.23(m,1h),6.87(d,j=8.0hz,1h),3.25(m,4h),1.65(m,4h),1.58(m,2h);lc-ms m/z[m+h]
+
,c
21h20
fn3o2的计算值:366;实测值:366。
[0648]
实施例a24:3-氟-2-羟基-5-(1-(3-吗啉代苯基)-1h-吡唑-4-基)苯甲醛(化合物编号a24)
[0649][0650]
步骤1:4-(3-(4-溴-1h-吡唑-1-基)苯基)吗啉
[0651]
如实施例a19的步骤1中所述从4-溴-1h-吡唑(1.75g,12mmol.)、4-(3-溴苯基)吗啉(2.42g,10mmol)制备标题化合物以产生标题化合物(524mg,17%产率)。lc-ms m/z[m+h]
+
,c
13h14
brn3o的计算值:308;实测值:308。
[0652]
步骤2:如实施例a19的步骤2中所述从4-(3-(4-溴-1h-吡唑-1-基)苯基)吗啉(308mg,1.0mmol)和3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(532mg,2.0mmol)制备标题化合物以产生呈黄色固体状的标题化合物(144mg,39%产率)。1h nmr(dmso-d6,400mhz)δ:10.92(s,1h),10.33(s,1h),9.06(s,1h),8.22(s,1h),7.95(d,j=12.0hz,1h),7.83(s,1h),7.40(s,1h),7.33(m,2h),6.90(d,j=7.6hz,1h),3.78(m,4h),3.22(m,4h);lc-ms m/z[m+h]
+
,c
20h18
fn3o3的计算值:368;实测值:368。
[0653]
实施例a25:2-羟基-3-甲氧基-5-(1-苯基-1h-吡唑-3-基)苯甲醛(化合物编号a25)
[0654][0655]
如实施例a1中所述从5-溴-2-羟基-3-甲氧基苯甲醛(231mg,1.0mmol)和1-苯基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)-1h-吡唑(324mg,1.2mmol)制备标题化合物以产生呈黄色固体状的标题化合物(163mg,55%产率)。1h nmr(500mhz,氯仿-d)δ11.13(s,1h),10.01(s,1h),7.98(d,j=2.5hz,1h),7.80
–
7.73(m,3h),7.68(d,j=1.9hz,1h),7.49(dd,j=8.6,7.4hz,2h),7.32(td,j=7.4,1.1hz,1h),6.75(d,j=2.5hz,1h),4.03(s,3h);lc-ms m/z[m+h]
+
,c
17h14
n2o3的计算值:295;实测值:295。
[0656]
实施例a26:3-氟-2-羟基-5-(1-苯基-1h-吡唑-3-基)苯甲醛(化合物编号a26)
[0657][0658]
如实施例a1中所述从5-溴-3-氟-2-羟基苯甲醛(219mg,1.0mmol)和1-苯基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)-1h-吡唑(324mg,1.2mmol)制备标题化合物以产生呈黄色固体状的标题化合物(168mg,59%产率)。1h nmr(500mhz,氯仿-d)δ10.98(s,1h),10.02(d,j=1.9hz,1h),7.98(d,j=2.5hz,1h),7.92(d,j=10.9hz,2h),7.79
–
7.74(m,2h),7.53
–
7.45(m,2h),7.38
–
7.29(m,1h),6.73(d,j=2.5hz,1h);lc-ms m/z[m+h]
+
,c
16h11
fn2o2的计算值:283;实测值:283。
[0659]
实施例a27:3-氟-2-羟基-5-(1-(4-(吡咯烷-1-基)苯基)-1h-吡唑-3-基)苯甲醛(化合物编号a27)
[0660][0661]
步骤1:3-溴-1-(4-(吡咯烷-1-基)苯基)-1h-吡唑
[0662]
如实施例a19的步骤1中所述从3-溴-1h-吡唑(1.75g,12mmol.)、1-(4-溴苯基)吡咯烷(2.26g,10mmol)制备标题化合物以产生标题化合物(379mg,13%产率)。lc-ms m/z[m+h]
+
,c
13h14
brn3的计算值:292;实测值:292。
[0663]
步骤2:如实施例a19的步骤2中所述从3-溴-1-(4-(吡咯烷-1-基)苯基)-1h-吡唑(292mg,1.0mmol)和3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(532mg,2.0mmol)制备标题化合物以产生呈黄色固体状的标题化合物(77mg,22%产率)。1h nmr(dmso-d6,400mhz)δ:11.05(br,1h),10.34(s,1h),8.34(s,1h),8.02(m,2h),7.66(m,2h),6.98(s,1h),6.63(m,2h),3.27(m,4h),1.98(m,4h);lc-ms m/z[m+h]
+
,c
20h18
fn3o2的计算值:352;实测值:352。
[0664]
实施例a28:3-氟-2-羟基-5-(1-(4-(哌啶-1-基)苯基)-1h-吡唑-3-基)苯甲醛(化合物编号a28)
[0665][0666]
步骤1:1-(4-(3-溴-1h-吡唑-1-基)苯基)哌啶
[0667]
如实施例a19的步骤1中所述从3-溴-1h-吡唑(1.75g,12mmol.)、1-(4-溴苯基)哌啶(2.40g,10mmol)制备标题化合物以产生标题化合物(1.01g,33%产率)。lc-ms m/z[m+h]
+
,c
14h16
brn3的计算值:306;实测值:306。
[0668]
步骤2:如实施例a19的步骤2中所述从1-(4-(3-溴-1h-吡唑-1-基)苯基)哌啶(306mg,1.0mmol)和3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(532mg,2.0mmol)制备标题化合物以产生呈黄色固体状的标题化合物(92mg,25%产率)。1h nmr(dmso-d6,400mhz)δ:11.06(br,1h),10.34(s,1h),8.40(s,1h),8.02(m,2h),7.70(d,j=8.8hz,2h),7.03(m,3h),3.18(m,4h),1.64(m,4h),1.55(m,2h);lc-ms m/z[m+h]
+
,c
21h20
fn3o2的计算值:366;实测值:366。
[0669]
实施例a29:3-氟-2-羟基-5-(1-(4-吗啉代苯基)-1h-吡唑-3-基)苯甲醛(化合物
编号a29)
[0670][0671]
步骤1:4-(4-(3-溴-1h-吡唑-1-基)苯基)吗啉
[0672]
如实施例a19的步骤1中所述从3-溴-1h-吡唑(1.75g,12mmol.)、4-(4-溴苯基)吗啉(2.42g,10mmol)制备标题化合物以产生标题化合物(585mg,19%产率)。lc-ms m/z[m+h]
+
,c
13h14
brn3o的计算值:308;实测值:308。
[0673]
步骤2:如实施例a19的步骤2中所述从4-(4-(3-溴-1h-吡唑-1-基)苯基)吗啉(308mg,1.0mmol)和3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(532mg,2.0mmol)制备标题化合物以产生呈黄色固体状的标题化合物(118mg,32%产率)。1h nmr(dmso-d6,400mhz)δ:11.07(br,1h),10.33(s,1h),8.43(s,1h),8.02(m,2h),7.74(d,j=8.8hz,2h),7.07(d,j=8.8hz,2h),7.01(s,1h),3.76(m,4h),3.16(m,4h);lc-ms m/z[m+h]
+
,c
20h18
fn3o3的计算值:368;实测值:368。
[0674]
实施例a30:3-氟-2-羟基-5-(1-(3-(吡咯烷-1-基)苯基)-1h-吡唑-3-基)苯甲醛(化合物编号a30)
[0675][0676]
步骤1:3-溴-1-(3-(吡咯烷-1-基)苯基)-1h-吡唑
[0677]
如实施例a19的步骤1中所述从3-溴-1h-吡唑(1.75g,12mmol.)、1-(3-溴苯基)吡咯烷(2.26g,10mmol)制备标题化合物以产生标题化合物(584mg,20%产率)。lc-ms m/z[m+h]
+
,c
13h14
brn3的计算值:292;实测值:292。
[0678]
步骤2:如实施例a19的步骤2中所述从3-溴-1-(3-(吡咯烷-1-基)苯基)-1h-吡唑(292mg,1.0mmol)和3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(532mg,2.0mmol)制备标题化合物以产生呈淡黄色固体状的标题化合物(67mg,19%产率)。1h nmr(cdcl3,400mhz)δ:10.99(s,1h),10.02(s,1h),7.94(m,3h),7.31(m,1h),6.97(m,2h),6.70(s,1h),6.55(m,1h),3.39(m,4h),2.07(m,4h);lc-ms m/z[m+h]
+
,c
20h18
fn3o2的计算值:352;实测值:352。
[0679]
实施例a31:3-氟-2-羟基-5-(1-(3-(哌啶-1-基)苯基)-1h-吡唑-3-基)苯甲醛(化合物编号a31)
[0680][0681]
步骤1:1-(3-(3-溴-1h-吡唑-1-基)苯基)哌啶
[0682]
如实施例a19的步骤1中所述从3-溴-1h-吡唑(1.75g,12mmol.)、1-(3-溴苯基)哌啶(2.40g,10mmol)制备标题化合物以产生标题化合物(370mg,12%产率)。lc-ms m/z[m+h]
+
,c
14h16
brn3的计算值:306;实测值:306。
[0683]
步骤2:如实施例a19的步骤2中所述从1-(3-(3-溴-1h-吡唑-1-基)苯基)哌啶(306mg,1.0mmol)和3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(532mg,2.0mmol)制备标题化合物以产生呈淡黄色固体状的标题化合物(83mg,27%产率)。1h nmr(dmso-d6,400mhz)δ:11.10(br,1h),10.34(s,1h),8.57(s,1h),8.04(m,2h),7.39(s,1h),7.28(m,2h),7.05(s,1h),6.89(m,1h),3.24(m,4h),1.65(m,4h),1.57(m,2h);lc-ms m/z[m+h]
+
,c
21h20
fn3o2的计算值:366;实测值:366。
[0684]
实施例a32:3-氟-2-羟基-5-(1-(3-吗啉代苯基)-1h-吡唑-3-基)苯甲醛(化合物编号a32)
[0685][0686]
步骤1:4-(3-(3-溴-1h-吡唑-1-基)苯基)吗啉
[0687]
如实施例a19的步骤1中所述从3-溴-1h-吡唑(1.75g,12mmol.)、4-(3-溴苯基)吗啉(2.42g,10mmol)制备标题化合物以产生标题化合物(524mg,17%产率)。lc-ms m/z[m+h]
+
,c
13h14
brn3o的计算值:308;实测值:308。
[0688]
步骤2:如实施例a19的步骤2中所述从4-(3-(3-溴-1h-吡唑-1-基)苯基)吗啉(308mg,1.0mmol)和3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(532mg,2.0mmol)制备标题化合物以产生呈白色固体状的标题化合物(114mg,31%产率)。1h nmr(cdcl3,400mhz)δ:11.01(br,1h),10.03(s,1h),7.98(s,1h),7.93(m,2h),7.55(m,1h),7.40(m,1h),7.29(m,1h),7.02(m,1h),6.73(s,1h),3.99(m,4h),3.33(m,4h);lc-ms m/z[m-h]-,c
20h18
fn3o3的计算值:366;实测值:366。
[0689]
实施例a33:(e)-2-氟-6-(((4-甲基哌嗪-1-基)亚氨基)甲基)-4-(1-苯基-1h-吡唑-3-基)苯酚(化合物编号a33)
[0690][0691]
在20ml密封盖玻璃小瓶中,将3-氟-2-羟基-5-(1-苯基-1h-吡唑-3-基)苯甲醛(85mg,0.3mmol)和4-甲基哌嗪-1-胺(65mg,0.3mmol)悬浮于乙醇(5ml)中,并且添加三氟乙酸(3滴)并使混合物升温以得到澄清溶液。接着在室温下搅拌2小时,通过真空过滤收集所得粉碎产物,并且用少量乙醇洗涤产物以产生呈白色固体状的标题产物(85mg,75%产率)。1h nmr(500mhz,氯仿-d)δ11.86(s,1h),7.94(d,j=2.5hz,1h),7.77
–
7.70(m,3h),7.53(d,j=2.7hz,1h),7.50
–
7.42(m,3h),7.29(td,j=7.3,1.3hz,2h),6.67(d,j=2.5hz,1h),3.23(t,j=5.1hz,4h),2.77
–
2.50(m,4h),2.37(s,3h);lc-ms m/z[m-h]-,c
21h22
fn5o的计算值:380;实测值:380。
[0692]
实施例a34:2-(1,3-二氧杂环己烷-2-基)-6-氟-4-(1-(4-(吡咯烷-1-基)苯基)-1h-吡唑-4-基)苯酚(化合物编号a34)
[0693][0694]
使3-氟-2-羟基-5-(1-(4-(吡咯烷-1-基)苯基)-1h-吡唑-4-基)苯甲醛(35mg,0.1mmol)、丙烷-1,3-二醇(30mg,0.4mmol)和tsoh(5mg,0.03mmol)于甲苯中的溶液回流2小时。移除大部分溶剂,并且将残余物通过制备型tlc来纯化以产生呈白色固体状的所需产物(13mg,32%产率)。1h nmr(cdcl3,300mhz)δ:7.95(s,1h),7.86(s,1h),7.74(m,1h),7.55(d,j=9.0hz,2h),7.22(m,1h),6.71(m,2h),4.36(m,2h),4.08(m,2h),3.37(m,4h),2.23(m,1h),2.08(m,5h);lc-ms m/z[m+h]
+
,c
23h24
fn3o3的计算值:411;实测值:411。
[0695]
用于实施例a35至实施例a41的一般性程序:
[0696]
将3-氟-2-羟基-5-(1-(4-(吡咯烷-1-基)苯基)-1h-吡唑-4-基)苯甲醛(1当量)和胺化合物(2当量)溶解于乙醇或甲醇中。使反应回流2小时。移除大部分溶剂,并且将残余物过滤。将滤饼用乙醇洗涤,并且在真空中干燥以产生所需产物。
[0697]
实施例a35:(e)-2-氟-6-(((4-甲基哌嗪-1-基)亚氨基)甲基)-4-(1-(4-(吡咯烷-1-基)苯基)-1h-吡唑-4-基)苯酚(化合物编号a35)
[0698][0699]
如以上一般性程序中所述从3-氟-2-羟基-5-(1-(4-(吡咯烷-1-基)苯基)-1h-吡唑-4-基)苯甲醛(100mg,0.28mmol)和4-甲基哌嗪-1-胺(64mg,0.56mmol)制备标题化合物以产生呈白色固体状的标题化合物(80mg,63%产率)。1h nmr(cdcl3,400mhz)δ:11.60(br,1h),7.93(s,1h),7.85(s,1h),7.72(s,1h),7.52(d,j=8.4hz,2h),7.21(d,j=11.6hz,1h),7.12(s,1h),6.61(d,j=8.4hz,2h),3.33(m,8h),2.80(m,4h),2.49(s,3h),2.04(m,4h);lc-ms m/z[m+h]
+
,c
25h29
fn6o的计算值:449;实测值:449。
[0700]
实施例a36:(e)-2-(((4-环丙基哌嗪-1-基)亚氨基)甲基)-6-氟-4-(1-(4-(吡咯烷-1-基)苯基)-1h-吡唑-4-基)苯酚(化合物编号a36)
[0701][0702]
除将乙酸钠(5mg,0.06mmol)碱添加至反应混合物中,并且最终用水和乙醇洗涤残余物之外,如以上一般性程序中所述从3-氟-2-羟基-5-(1-(4-(吡咯烷-1-基)苯基)-1h-吡唑-4-基)苯甲醛(20mg,0.06mmol)和4-环丙基哌嗪-1-胺二盐酸盐(12mg,0.06mmol)制备标题化合物以产生呈灰白色固体状的标题化合物(11mg,41%产率)。1h nmr(dmso-d6,400mhz)δ:11.52(br,1h),8.69(s,1h),8.01(s,1h),7.90(m,1h),7.62(d,j=8.8hz,2h),7.51(m,2h),6.63(d,j=8.8hz,2h),3.27(m,4h),3.13(m,4h),2.75(m,4h),1.98(m,4h),1.73(m,1h),0.45(m,2h),0.36(m,2h);lc-ms m/z[m+h]
+
,c
27h31
fn6o的计算值:475;实测值:475。
[0703]
实施例a37:(e)-2-氟-6-((吗啉代亚氨基)甲基)-4-(1-(4-(吡咯烷-1-基)苯基)-1h-吡唑-4-基)苯酚(化合物编号a37)
[0704][0705]
如以上一般性程序中所述从3-氟-2-羟基-5-(1-(4-(吡咯烷-1-基)苯基)-1h-吡唑-4-基)苯甲醛(100mg,0.28mmol)和吗啉-4-胺(57mg,0.56mmol)制备标题化合物以产生呈白色固体状的标题化合物(85mg,69%产率)。1h nmr(dmso-d6,400mhz)δ:11.42(br,1h),8.70(s,1h),8.00(m,2h),7.62(m,2h),7.53(m,2h),6.63(d,j=8.8hz,2h),3.80(m,4h),3.27(m,4h),3.16(m,4h),1.97(m,4h);lc-ms m/z[m+h]
+
,c
24h26
fn5o2的计算值:436;实测值:436。
[0706]
实施例a38:n'-(3-氟-2-羟基-5-(1-(4-(吡咯烷-1-基)苯基)-1h-吡唑-4-基)苯亚甲基)乙酰肼(化合物编号a38)
[0707][0708]
如以上一般性程序中所述从3-氟-2-羟基-5-(1-(4-(吡咯烷-1-基)苯基)-1h-吡唑-4-基)苯甲醛(100mg,0.28mmol)和乙酰肼(41mg,0.56mmol)制备标题化合物以产生呈白色固体状的标题化合物(55mg,47%产率)。1h nmr(dmso-d6,400mhz)δ:11.87(br,0.6h),11.56(br,0.6h),11.45(br,0.4h),10.34(br,0.4h),8.75(s,1h),8.36(s,0.6h),8.29(s,0.4h),8.08(s,1h),7.64(m,4h),6.64(d,j=8.4hz,2h),3.27(m,4h),2.25(s,1h),1.97-2.02(m,6h);lc-ms m/z[m+h]
+
,c
22h22
fn5o2的计算值:408;实测值:408。
[0709]
实施例a39:(e)-2-氟-6-((苯基亚氨基)甲基)-4-(1-(4-(吡咯烷-1-基)苯基)-1h-吡唑-4-基)苯酚(化合物编号a39)
4-(4-(吡咯烷-1-基)苯基)-1h-1,2,3-三唑
[0718][0719]
将2-(5-叠氮基-3-氟-2-(4-甲氧基苯甲基氧基)苯基)-1,3-二硫杂环己烷(0.3g,0.77mmol)(如实施例a43中所制备)、cuso4(21mg,0.13mmol)和l-抗坏血酸钠盐(65mg,0.39mmol)于meoh/水(20ml/2ml)中的混合物用氮气吹扫三次,接着将1-(4-乙炔基苯基)吡咯烷(112mg,0.77mmol)添加至反应混合物中。在50℃下将反应加热1小时。使混合物冷却至室温,用水(40ml)稀释,并且用乙酸乙酯(40mlx3)萃取。将有机萃取物合并,用盐水(40mlx2)洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯=20:1至2:1)来纯化以产生所需标题产物(203mg,47%产率)。lc-ms m/z[m+h]
+
,c
30h31
fn4o2s2的计算值:563;实测值:563。
[0720]
步骤2:在40℃下将以上获得的步骤1产物(150mg,0.27mmol)、mei(3.8g,26.8mmol)和nahco3(448mg,5.3mmol)于乙腈/水(15ml/3ml)中的溶液搅拌过夜。将溶液用水稀释,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物溶解于4n hcl(5ml)中,并且在室温下将反应搅拌1小时。将溶液倾倒至冰冷的饱和碳酸氢钠中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过制备型tlc(dcm/meoh=20:1)来纯化以产生呈黄色固体状的所需产物(7mg,7%产率)。1h nmr(cdcl3,400mhz)δ:11.07(s,1h),10.03(s,1h),8.01(s,1h),7.84(m,2h),7.75(m,2h),6.68(m,2h),3.36(m,4h),2.05(m,4h);lc-ms m/z[m+h]
+
,c
19h17
fn4o2的计算值:353;实测值:353。
[0721]
实施例a42:3-氟-2-羟基-5-(1-(4-(吡咯烷-1-基)苯基)-1h-1,2,3-三唑-4-基)苯甲醛(化合物编号a43)
[0722][0723]
步骤1:5-乙炔基-3-氟-2-羟基苯甲醛
[0724][0725]
在氮气保护下将起始物料pdcl2(pph)2(0.3g,0.25mmol)、cui(0.03g,0.1mmol)和
乙炔基三甲基甲硅烷(1.47g,15.0mmol)添加至5-溴-3-氟-2-羟基苯甲醛(2.19g,10.0mmol)、三乙胺(2.02g,20.0mmol)和三苯基膦(0.045g,0.125mmol)于thf(20ml)中的溶液中,回流60小时。使混合物冷却至室温,用水/乙酸乙酯稀释,并且过滤。将滤饼用乙酸乙酯洗涤。将滤液和洗涤液合并,分离,并且将水相用乙酸乙酯再萃取又两次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯=500:1至300:1)来纯化以产生3-氟-2-羟基-5-((三甲基甲硅烷基)乙炔基)苯甲醛(1.1g,47%产率)。将3-氟-2-羟基-5-((三甲基甲硅烷基)乙炔基)苯甲醛(1.0g,4.2mmol)溶解于thf(15ml)中,并且添加tbaf(2.2g,8.4mmol)。在室温下将反应搅拌1小时。在真空中移除溶剂,并且将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯=500:1至300:1)来纯化以产生标题产物(0.31g,45%产率)。1h nmr(cdcl3,400mhz)δ:10.96(br,1h),9.89(d,j=8.4hz,1h),7.49(m,2h),3.08(s,1h)。
[0726]
步骤2:1-(4-叠氮基苯基)吡咯烷
[0727][0728]
在50ml干燥圆底烧瓶中,在-78℃下将buli(4ml,10.0mmol,2.5m,于thf中)添加至1-(4-溴苯基)吡咯烷(0.5g,2.2mmol)于thf(5ml)中的溶液中。将反应搅拌30分钟。添加tsn3(1.3g,6.7mmol)。在室温下将反应搅拌5小时。将反应用饱和氯化铵(20ml)淬灭,并且用etoac(20mlx3)萃取。将有机层合并,用盐水(20ml)洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯=500:1至400:1)来纯化以产生标题产物(150mg,36%产率)。lc-ms m/z[m+h]
+
,c
10h12
n4的计算值:189;实测值:189。
[0729]
步骤3:将1-(4-叠氮基苯基)吡咯烷(100mg,0.53mmol)、cuso4(8.5mg,0.053mmol)和l-抗坏血酸钠盐(52.7mg,0.27mmol)于t-buoh/水(5ml/5ml)中的混合物用氮气吹扫三次,并且将5-乙炔基-3-氟-2-羟基苯甲醛(131mg,0.80mmol)添加至反应混合物中。在40℃下将反应加热过夜。使混合物冷却至室温,用水(20ml)稀释,并且用乙酸乙酯(20mlx3)萃取。将有机萃取物合并,用盐水(20mlx2)洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯=20:1至5:1)和制备型hplc来纯化以产生呈淡黄色固体状的所需最终产物(12mg,6%产率)。1h nmr(dmso-d6,400mhz)δ:11.17(br,1h),10.37(s,1h),9.15(s,1h),8.04(m,2h),7.68(d,j=8.8hz,2h),6.70(d,j=9.2hz,2h),3.30(m,4h),2.00(m,4h);lc-ms m/z[m+h]
+
,c
19h17
fn4o2的计算值:353;实测值:353。
[0730]
实施例a43:3-氟-2-羟基-5-(4-(3-(吡咯烷-1-基)苯基)-1h-1,2,3-三唑-1-基)苯甲醛(化合物编号a44)
[0731][0732]
步骤1:2-(5-溴-3-氟-2-(4-甲氧基苯甲基氧基)苯基)-1,3-二硫杂环己烷
[0733][0734]
在100ml干燥圆底烧瓶中,在氮气保护下将bf3.oet2(3.41g,24.0mmol)添加至5-溴-3-氟-2-羟基苯甲醛(4.36g,20.0mmol)和丙烷-1,3-二硫醇(2.6g,24.0mmol)于dcm(20ml)中的溶液中。在室温下将反应搅拌3小时。将溶液倾倒至冰水中,并且用乙酸乙酯(50mlx3)萃取。将有机萃取物合并,用盐水(30ml)洗涤,经无水硫酸钠干燥,并且浓缩。将粗物质溶解于dmf(20ml)中,接着添加pmbcl(6.24g,40.0mmol)和碳酸钾(8.28g,60mmol)。在90℃下将反应搅拌2小时。使混合物冷却至室温,用水(100ml)稀释,并且用乙酸乙酯(100mlx3)萃取。将有机萃取物合并,用盐水(50mlx2)洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯=500:1至400:1)来纯化以产生标题产物(6.37g,74%产率)。1h nmr(cdcl3,400mhz)δ:7.51(s,1h),7.42(m,2h),7.24(m,1h),6.94(m,2h),5.48(s,1h),5.07(s,2h),3.84(s,3h),2.98(m,2h),2.88(m,2h),2.15(m,1h),1.90(m,1h)。
[0735]
步骤2:2-(5-叠氮基-3-氟-2-(4-甲氧基苯甲基氧基)苯基)-1,3-二硫杂环己烷
[0736][0737]
在100ml干燥圆底烧瓶中,在-78℃下将buli(6.6ml,10.5mmol,1.6m,于thf中)添加至2-(5-溴-3-氟-2-(4-甲氧基苯甲基氧基)苯基)-1,3-二硫杂环己烷(1.0g,2.3mmol)和tsn3(1.38g,7.0mmol)于thf(10ml)中的溶液中。在室温下将反应搅拌2.5小时。将反应用饱和氯化铵(30ml)淬灭,并且用etoac(30mlx3)萃取。将有机层合并,用盐水(30ml)洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯=100:1至50:1)来纯化以产生标题产物(0.71g,78%产率,内部含有约55%脱溴副产物)。lc-ms m/z[m+h]
+
,c
18h18
fn3o2s2的计算值:392;实测值:392。
[0738]
步骤3:5-叠氮基-3-氟-2-(4-甲氧基苯甲基氧基)苯甲醛
[0739][0740]
将dmp(2.4g,5.6mmol)添加至2-(5-叠氮基-3-氟-2-(4-甲氧基苯甲基氧基)苯基)-1,3-二硫杂环己烷(1.1g,2.8mmol)于乙腈/dcm/水(16ml/2ml/2ml)中的溶液中。在45℃下将反应搅拌过夜。将混合物用乙酸乙酯(50ml)稀释并过滤。将滤液用饱和碳酸氢钠(50ml)洗涤。将有机层经无水硫酸钠干燥并浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯=100:1至50:1)来纯化以产生标题产物(0.79g,93%产率,内部含有约55%脱溴副产物)。lc-ms m/z[m+h]
+
,c
15h12
fn3o3的计算值:302;实测值:302。
[0741]
步骤4:3-(吡咯烷-1-基)苯甲醛
[0742][0743]
在-78℃下将buli(20.6ml,33.2mmol,1.6m,于thf中)添加至1-(3-溴苯基)吡咯烷(5g,22.1mmol)于thf(25ml)中的溶液中。在这个温度下将反应搅拌1小时。添加dmf(2.4g,33.2mmol)于thf(5ml)中的溶液。在室温下将反应搅拌2小时。将反应用饱和氯化铵(50ml)淬灭,并且用etoac(50mlx3)萃取。将有机层合并,用盐水(50ml)洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯=500:1至300:1)来纯化以产生所需产物(2.85g,74%产率)。1h nmr(cdcl3,400mhz)δ:9.97(s,1h),7.79(t,j=8.0hz,1h),7.16(d,j=7.2hz,1h),7.04(s,1h),6.83(dd,j=8.4hz,2.0hz,1h),3.36(m,4h),2.06(m,4h)。
[0744]
步骤5:1-(3-乙炔基苯基)吡咯烷
[0745][0746]
在-78℃下将buli(4.3ml,6.9mmol,1.6m,于thf中)添加至3-(吡咯烷-1-基)苯甲醛(1.0g,5.7mmol)于thf(10ml)中的溶液中。将反应搅拌30分钟。添加tmsn2(3.4ml,6.9mmol,2m,于thf中)。在-78℃下将反应搅拌1小时。将反应用饱和氯化铵(30ml)淬灭,并且用etoac(30mlx3)萃取。将有机层合并,用盐水(30ml)洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯=500:1至400:1)来纯化以产生所需1-(3-乙炔基苯基)吡咯烷(0.63g,64%产率)。
[0747]
步骤6:3-氟-2-(4-甲氧基苯甲基氧基)-5-(4-(3-(吡咯烷-1-基)苯基)-1h-1,2,3-三唑-1-基)苯甲醛
[0748][0749]
将5-叠氮基-3-氟-2-(4-甲氧基苯甲基氧基)苯甲醛(0.4g,1.3mmol)、cuso4(20mg,0.13mmol)和l-抗坏血酸钠盐(150mg,0.75mmol)于t-buoh/水(5ml/5ml)中的混合物用氮气吹扫三次,接着将1-(3-乙炔基苯基)吡咯烷(0.2g,1.2mmol)添加至反应混合物中。在40℃下将反应加热过夜。使混合物冷却至室温,用水(20ml)稀释,并且用乙酸乙酯(20mlx3)萃取。将有机萃取物合并,用盐水(20ml x 2)洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯=20:1至2:1)来纯化以产生经pmb保护的所需产物(120mg,22%产率)。lc-ms m/z[m+h]
+
,c
27h25
fn4o3的计算值:473;实测值:473。
[0750]
步骤7:在室温下将3-氟-2-(4-甲氧基苯甲基氧基)-5-(4-(3-(吡咯烷-1-基)苯
基)-1h-1,2,3-三唑-1-基)苯甲醛(120mg,0.25mmol)和tfa(86mg,0.76mmol)于dcm(5ml)中的溶液搅拌过夜。将溶液用dcm(10ml)稀释,并且用饱和碳酸氢钠(10ml)洗涤。将有机层经无水硫酸钠干燥并浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯/dcm=20:1:1至5:1:1)来纯化以产生呈淡黄色固体状的最终所需产物(30mg,34%产率)。1h nmr(dmso-d6,400mhz)δ:11.51(s,1h),10.40(s,1h),9.31(s,1h),8.21(dd,j=11.2hz,2.8hz,1h),8.03(m,1h),7.26(m,1h),7.17(m,1h),7.11(m,1h),6.56(m,1h),3.31(m,4h),2.00(m,4h););lc-ms m/z[m+h]
+
,c
19h17
fn4o2的计算值:353;实测值:353。
[0751]
实施例a44:3-氟-2-羟基-5-(1-(3-(吡咯烷-1-基)苯基)-1h-1,2,3-三唑-4-基)苯甲醛(化合物编号a45)
[0752][0753]
步骤1:1-(3-叠氮基苯基)吡咯烷
[0754][0755]
使3-(吡咯烷-1-基)苯胺(0.5g,3.1mmol)于乙腈(10ml)中的溶液冷却至0℃。添加亚硝酸叔丁酯(0.96g,9.3mmol)和tmsn3(0.86g,7.4mmol)。在室温下将反应搅拌过夜。将反应用水(20ml)稀释,并且用etoac(20mlx3)萃取。将有机层合并,用盐水(20ml)洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯=300:1至100:1)来纯化以产生所需产物(190mg,33%产率)。lc-ms m/z[m+h]
+
,c
10h12
n4的计算值:189;实测值:189。
[0756]
步骤2:将1-(3-叠氮基苯基)吡咯烷(100mg,0.53mmol)、cuso4(8.5mg,0.053mmol)和l-抗坏血酸钠盐(52.7mg,0.27mmol)于t-buoh/水(5ml/5ml)中的混合物用氮气吹扫三次,接着将5-乙炔基-3-氟-2-羟基苯甲醛(131mg,0.80mmol)(来自实施例a43)添加至反应混合物中。在40℃下将反应加热过夜。使混合物冷却至室温,用水(20ml)稀释,并且用乙酸乙酯(20mlx3)萃取。将有机萃取物合并,用盐水(20mlx2)洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯=20:1至5:1)和制备型tlc来纯化以产生呈白色固体状的最终产物(15mg,7%产率)。1h nmr(cdcl3,400mhz)δ:11.05(br,1h),10.03(s,1h),8.21(s,1h),8.01(s,1h),7.88(d,j=11.2hz,1h),7.44(m,1h),7.34(m,1h),7.19(m,1h),6.92(d,j=7.2hz,1h),3.48(m,4h),2.16(m,4h);lc-ms m/z[m+h]
+
,c
19h17
fn4o2的计算值:353;实测值:353。
[0757]
实施例a45:3-氟-2-羟基-5-(1-(4-(吡咯烷-1-基)苯基)-1h-咪唑-4-基)苯甲醛(化合物a47)
[0758][0759]
步骤1:4-(4-溴-1h-咪唑-1-基)苯胺
[0760]
在80℃下在n2保护下将1-氟-4-硝基苯(1.16g,8.2mmol,1.2当量)、5-溴-1h-咪唑(1g,6.8mmol,1.0当量)和碳酸钾(2.84g,20.4mmol,3.0当量)于dmf(15ml)中的混合物加热2小时。使混合物冷却至室温,倾倒至水中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩以产生粗制4-溴-1-(4-硝基苯基)-1h-咪唑(1.77g,6.63mmol,98%产率)。lc-ms:268.0,270.0(m+h)
+
,c9h6brn3o2。在100ml玻璃小瓶中,将铁粉(2.71g,48.32mmol,10.0当量)添加至4-溴-1-(4-硝基苯基)-1h-咪唑(1.3g,4.83mmol,1.0当量)于acoh(20ml)中的溶液中。在60℃下将反应加热2小时。使反应混合物冷却至室温,倾倒至饱和nahco3中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩以产生4-(4-溴-1h-咪唑-1-基)苯胺(790mg,3.31mmol,68%产率)。
[0761]
步骤2:4-溴-1-(4-(吡咯烷-1-基)苯基)-1h-咪唑
[0762]
在室温下将4-(4-溴-1h-咪唑-1-基)苯胺(500mg,2.1mmol,1.0当量)和二氢呋喃-2,5-二酮(422mg,4.2mmol,2.0当量)于甲苯(15ml)中的溶液搅拌过夜。将溶液倾倒至水中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩以产生粗中间体(710mg)。接着使这个中间体在亚硫酰氯(10ml)中回流1小时,并且在真空中浓缩以得到倒数第二个中间体(690mg)。将这个中间体(600mg,1.88mmol,1.0当量)溶解于thf(10ml)中,并且使溶液冷却至0℃。添加硼烷-二甲基硫醚(1.68ml,10m,9.0当量)。在50℃下将反应搅拌2小时。使体系冷却至室温,倾倒至冰水中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/etoac=20:1至10:1)来纯化以产生4-溴-1-(4-(吡咯烷-1-基)苯基)-1h-咪唑(240mg,0.82mmol,44%产率)。lc-ms m/z[m+h]
+
,c
13h14
brn3的计算值:292;实测值:292。
[0763]
步骤3:在100℃下在氮气氛围下将4-溴-1-(4-(吡咯烷-1-基)苯基)-1h-咪唑(200mg,0.69mmol,1.0当量)、3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(459mg,1.73mmol,2.5当量)、碳酸钾(286mg,2.07mmol,3.0当量)、pdcl2(dppf)(85mg,0.07mmol,0.1当量)于二噁烷/水(10ml/3ml)中的混合物加热3小时。使混合物冷却至室温,并且倾倒至水中。接着将体系的ph调整至4-5,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱(石油醚/etoac=50:1至20:1)来纯化以产生呈黄色固体状的3-氟-2-羟基-5-(1-(4-(吡咯烷-1-基)苯基)-1h-咪唑-4-基)苯甲醛(42mg,0.12mmol,17%产率)。1h nmr(dmso-d6,400mhz)δ:10.87(br,1h),10.33(s,1h),8.14(d,j=10.4hz,2h),7.97-7.92(m,2h),7.45(d,j=8.8hz,2h),6.64(d,j=8.4hz,2h),3.27(m,4h),1.98(m,4h);lc-ms m/z[m+h]
+
,c
20h18
fn3o2的计算值:352;实测值:352。
[0764]
实施例a46:3-氟-2-羟基-5-(5-(4-(吡咯烷-1-基)苯基)噻吩-2-基)苯甲醛(化合物a50)
[0765][0766]
步骤1:1-(4-(噻吩-2-基)苯基)吡咯烷
[0767]
在95℃下在氮气氛围下将噻吩-2-基硼酸(1.7g,13.3mmol,1.5当量)、1-(4-溴苯基)吡咯烷(2g,8.89mmol,1.0当量)、碳酸钾(3.7g,26.8mmol,3.0当量)和pdcl2(dppf)(0.7g,0.89mmol,0.1当量)于二噁烷/水(9ml/3ml)中的混合物加热2小时。使混合物冷却至室温并过滤。将滤饼用乙酸乙酯洗涤。将滤液和洗涤液合并,用水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱(石油醚/etoac=100至300:1)来纯化以产生1-(4-(噻吩-2-基)苯基)吡咯烷(1.2g,5.24mmol,59%产率)。
[0768]
步骤2:1-(4-(5-溴噻吩-2-基)苯基)吡咯烷
[0769]
将1-(4-(噻吩-2-基)苯基)吡咯烷(950mg,4.15mmol,1当量)和nbs(1.11g,6.23mmol,1.5当量)于chcl3(20ml)中的溶液搅拌2小时。将溶液倾倒至饱和碳酸氢钠中,并且用ch2cl2萃取三次。将有机萃取物合并,用水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱(纯石油醚)来纯化以产生1-(4-(5-溴噻吩-2-基)苯基)吡咯烷(350mg,1.13mmol,27%产率)。1h nmr(dmso-d6,400mhz)δ:7.39(dd,j=6.8hz,2.0hz,2h),7.14(d,j=4.0hz,1h),7.08(d,j=4.0hz,1h),6.54(d,j=8.8hz,2h),3.25(m,4h),1.96(m,4h)。
[0770]
步骤3:在95℃下在氮气氛围下将1-(4-(5-溴噻吩-2-基)苯基)吡咯烷(340mg,1.10mmol,1.0当量)、3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(322mg,1.21mmol,1.1当量)、碳酸钾(456mg,3.30mmol,3.0当量)和pdcl2(dppf)(90mg,0.11mmol,0.1当量)于二噁烷/水(9ml/3ml)中的混合物加热2小时。使混合物冷却至室温,并且倾倒至水中。接着将体系的ph调整至4-5,并且用乙酸乙酯萃取。将有机萃取物合并,用水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱(石油醚/etoac=100:1至20:1)来纯化以产生3-氟-2-羟基-5-(5-(4-(吡咯烷-1-基)苯基)噻吩-2-基)苯甲醛(110mg,0.30mmol,27%产率)。1h nmr(dmso-d6,400mhz)δ:11.10(br,1h),10.31(s,1h),7.90(dd,j=12.0hz,1.6hz,1h),7.65(s,1h),7.47(m,3h),7.26(d,j=3.6hz,1h),6.57(d,j=8.8hz,2h),3.36(m,4h),1.96(m,4h)。lc-ms m/z[m+h]
+
,c
21h18
fno2s的计算值:368;实测值:368。
[0771]
实施例a47:3-氟-2-羟基-5-(4-(4-(吡咯烷-1-基)苯基)噻吩-2-基)苯甲醛(化合物a51)
[0772][0773]
步骤1:5-(4-溴噻吩-2-基)-3-氟-2-羟基苯甲醛
[0774]
在100℃下在氮气氛围下将2,4-二溴噻吩(1g,4.1mmol,1.0当量)、3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(1.2g,4.51mmol,1.08当量)、磷酸钾(4.4g,20.8mmol,5.0当量)、pd(pph3)4(0.48g,0.41mmol,0.1当量)于二噁烷/水(20ml/6ml)中的混合物加热3小时。使混合物冷却至室温,并且倾倒至水中。接着将体系的ph调整至4-5,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱(石油醚/etoac=100:1至20:1)来纯化以产生5-(4-溴噻吩-2-基)-3-氟-2-羟基苯甲醛(390mg,1.29mmol,31%产率)。lc-ms m/z[m+h]
+
,c
11
h6brfo2s的计算值:301;实测值:301。
[0775]
步骤2:在100℃下在氮气氛围下将5-(4-溴噻吩-2-基)-3-氟-2-羟基苯甲醛(302mg,1mmol,1.0当量)、1-(4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)吡咯烷(295mg,1.08mmol,1.08当量)、磷酸钾(1.06g,5.0mmol,5.0当量)、pd(pph3)4(116mg,0.1mmol,0.1当量)于二噁烷/水(10ml/3ml)中的混合物加热3小时。使混合物冷却至室温,并且倾倒至水中。接着将体系的ph调整至4-5,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱(石油醚/etoac=100:1至20:1)来纯化以产生呈黄色固体状的3-氟-2-羟基-5-(4-(4-(吡咯烷-1-基)苯基)噻吩-2-基)苯甲醛(60mg,0.16mmol,16%产率)。1h nmr(dmso-d6,400mhz)δ:11.13(br,1h),10.32(s,1h),8.00(dd,j=12.4hz,2.4hz,1h),7.93(d,j=1.2hz,1h),7.72(s,1h),7.61-7.55(m,3h),6.57(d,j=8.8hz,2h),3.26(m,4h),1.97(m,4h)。lc-ms m/z[m+h]
+
,c
21h18
fno2s的计算值:368;实测值:368。
[0776]
实施例a48:3-氟-2-羟基-5-(5-(4-(吡咯烷-1-基)苯基)噻吩-3-基)苯甲醛(化合物a52)
[0777][0778]
步骤1:1-(4-(4-溴噻吩-2-基)苯基)吡咯烷
[0779]
在100℃下在氮气氛围下将2,4-二溴噻吩(1g,4.1mmol,1.0当量)、1-(4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)吡咯烷(1.22g,4.51mmol,1.08当量)、磷酸钾(4.4g,20.8mmol,5.0当量)、pd(pph3)4(0.48g,0.41mmol,0.1当量)于二噁烷/水(20ml/6ml)中的混合物加热3小时。使混合物冷却至室温,并且倾倒至水中。接着将体系的ph调整至4-5,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱(石油醚/etoac=100至500:1)来纯化以产生1-(4-(4-溴噻吩-2-基)苯基)吡咯烷(260mg,0.84mmol,21%产率),其用于下一步骤中。
[0780]
步骤2:使用与如实施例a47中所述的方法类似的方法从1-(4-(4-溴噻吩-2-基)苯基)吡咯烷(230mg,0.74mmol,1.0当量)和3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(214mg,0.80mmol,1.08当量)制备标题化合物以产生呈黄色固体状的最终标题化合物(110mg,0.30mmol,41%产率)。1h nmr(dmso-d6,400mhz)δ:10.98(br,1h),10.32(s,1h),8.00(dd,j=12.4hz,2.0hz,1h),7.87(d,j=1.2hz,1h),7.75(d,j=1.2hz,1h),7.70(d,j=1.2hz,1h),7.54(d,j=8.8hz,2h),6.58(d,j=8.8hz,2h),3.27(m,4h),1.97(m,4h)。lc-ms m/z[m+h]
+
,c
21h18
fno2s的计算值:368;实测值:368。
[0781]
实施例a49:3-氟-2-羟基-5-(2-(4-(吡咯烷-1-基)苯基)噻唑-4-基)苯甲醛(化合物a57)
[0782][0783]
步骤1:4-溴-2-(4-(吡咯烷-1-基)苯基)噻唑
[0784]
在100℃下在氮气保护下将2,4-二溴噻唑(500mg,2.06mmol,1.0当量)、1-(4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)吡咯烷(620mg,2.26mmol,1.1当量)、碳酸钾(850mg,6.18mmol,3.0当量)和pdcl2(dppf)(170mg,0.21mmol,0.1当量)于二噁烷/水(10ml/5ml)中的混合物加热1小时。使混合物冷却至室温,倾倒至水中,并且用乙酸乙酯
萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱(石油醚/etoac=100至500:1)来纯化以产生4-溴-2-(4-(吡咯烷-1-基)苯基)噻唑(397mg,1.29mmol,63%产率)。lc-ms m/z[m+h]
+
,c
13h13
brn2s的计算值:311;实测值:311。
[0785]
步骤2:使用与如实施例a47中所述的方法类似的方法从3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(415mg,1.56mmol,1.2当量)和4-溴-2-(4-(吡咯烷-1-基)苯基)噻唑(400mg,1.30mmol,1.0当量)制备标题化合物以产生呈黄色固体状的最终标题化合物(110mg,0.30mmol,41%产率)。1h nmr(dmso-d6,400mhz)δ:11.12(br,1h),10.35(s,1h),8.14(dd,j=10.0hz,2.4hz,2h),7.97(s,1h),7.82(d,j=8.8hz,2h),6.63(d,j=8.8hz,2h),3.31(m,4h),1.98(m,4h)。lc-ms m/z[m-h]-,c
20h17
fn2o2s的计算值:367;实测值:367。
[0786]
实施例a50:3-氟-2-羟基-5-(5-(4-(吡咯烷-1-基)苯基)-1,2,4-噻二唑-3-基)苯甲醛(化合物a61)
[0787][0788]
步骤1:3-溴-5-(4-(吡咯烷-1-基)苯基)-1,2,4-噻二唑
[0789]
在80℃下在氮气氛围下将3-溴-5-氯-1,2,4-噻二唑(0.5g,2.5mmol,1.0当量)、1-(4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)吡咯烷(0.75g,2.75mmol,1.1当量)、磷酸钾(1.59g,7.5mmol,3.0当量)、pdcl2(dppf)(204mg,0.25mmol,0.1当量)于dmf/水(6ml/2ml)中的混合物加热2.5小时。使混合物冷却至室温,并且倾倒至水中。接着将体系的ph调整至4-5,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱(石油醚/etoac=20:1至50:1)来纯化以产生3-溴-5-(4-(吡咯烷-1-基)苯基)-1,2,4-噻二唑(203mg,0.66mmol,26%产率)。lc-ms m/z[m+h]
+
,c
12h12
brn3s的计算值:312;实测值:312。
[0790]
步骤2:使用与如实施例a47中所述的方法类似的方法从3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(133mg,0.50mmol,1.1当量)和3-溴-5-(4-(吡咯烷-1-基)苯基)-1,2,4-噻二唑(140mg,0.45mmol,1.0当量)制备标题化合物以产生呈黄色固体状的最终标题化合物(30mg,0.08mmol,18%产率)。1h nmr(dmso-d6,400mhz)δ:11.54(br,1h),10.37(s,1h),8.38(d,j=1.2hz,1h),8.24(dd,j=11.6hz,2.0hz,1h),7.89(d,j=8.8hz,2h),6.67(d,j=8.8hz,2h),3.35(m,4h),1.99(t,j=6.6hz,4h)。lc-ms m/z[m+h]
+
,c
19h16
fn3o2s的计算值:370;实测值:370。
[0791]
实施例a51:3-氟-2-羟基-5-(3-(4-(吡咯烷-1-基)苯基)-1,2,4-噻二唑-5-基)苯甲醛(化合物a62)
[0792][0793]
使用与如实施例a47中所述的方法类似的方法从1-(4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)吡咯烷(258mg,0.94mmol,1.1当量)和5-(3-溴-1,2,4-噻二唑-5-基)-3-氟-2-羟基苯甲醛(260mg,0.86mmol,1当量)(如实施例a47中所制备)制备标题化合物以产生呈黄色固体状的最终标题化合物(87mg,0.24mmol,27%产率)。1h nmr(dmso-d6,400mhz)δ:11.88(br,1h),10.36(s,1h),8.22(dd,j=11.2hz,2.4hz,1h),8.15(s,1h),8.13(d,j=8.8hz,2h),6.65(d,j=9.2hz,2h),3.32(t,j=6.8hz,4h),1.98(m,4h)。lc-ms m/z[m+h]
+
,c
19h16
fn3o2s的计算值:370;实测值:370。
[0794]
实施例a52:3-氟-2-羟基-5-(2-苯基噁唑-5-基)苯甲醛(化合物a88)
[0795][0796]
使用与如实施例a47中所述的方法类似的方法从5-溴-2-苯基噁唑(223mg,1mmol,1当量)和3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(244mg,1.08mmol,1.08当量)制备标题化合物以产生呈黄色固体状的最终标题化合物(120mg,0.42mmol,42%产率)。1h nmr(dmso-d6,400mhz)δ:11.35(br,1h),10.35(s,1h),8.12-8.06(m,3h),7.92(s,1h),7.86(s,1h),7.57(m,3h)。lc-ms m/z[m+h]
+
,c
16h10
fno3的计算值:284;实测值:284。
[0797]
实施例a53:3-氟-2-羟基-5-(5-苯基噁唑-2-基)苯甲醛(化合物a89)
[0798][0799]
以与由ji等人(rsc adv.,2018,8,13643-13648.)所述的方式类似的方式合成3-氟-2-羟基-5-(5-苯基噁唑-2-基)苯甲醛。
[0800]
步骤1a:将5-溴-3-氟-2-羟基苯甲醛(131mg,0.6mmol)、双(频哪醇合)二硼(253mg,0.66mmol)、磷酸三钾(254.7mg)、xphos pd g3(50.8mg)和xphos(28.6mg)放置在具有搅拌棒的5ml微波小瓶中。添加二噁烷(2.4ml),并且将小瓶用氩气脱气并密封。在biotage微波中将反应加热至130℃,持续60分钟。
[0801]
步骤1b:将来自步骤1a的反应混合物的等分试样(0.8ml)添加至含有2-溴-5-苯基噁唑(44.8mg,0.2mmol)、xphos pd g3(8.5mg)和xphos(4.8mg)的微波小瓶中。将反应用氩气脱气,并且在微波中加热至130℃,持续30分钟。将反应混合物用dcm稀释,用柠檬酸酸化至ph=3,并且用dcm萃取3次。将合并的有机相用盐水洗涤,并且经无水na2so4干燥,过滤并
蒸发。将粗产物通过快速柱色谱法(0-10%meoh/dcm)来纯化。产率(6.6mg,12%)。1h nmr(500mhz,cdcl3)δ11.22(s,1h),10.04(d,j=1.7hz,1h),8.19(dd,j=2.0,1.2hz,1h),8.10(dd,j=11.0,2.0hz,1h),7.98(s,1h),7.85
–
7.77(m,2h),7.48
–
7.41(m,2h),7.40
–
7.33(m,1h)。ms m/z[m+h]
+
,c
16h10
fno3的计算值:284;实测值:284。
[0802]
实施例a54:3-氟-2-羟基-5-(4-苯基噁唑-2-基)苯甲醛(化合物a90)
[0803][0804]
利用可商购获得的2-溴-4-苯基噁唑,使用与如实施例a53中所述的方法类似的方法制备标题化合物。产率:14%。1h nmr(500mhz,cdcl3)δ11.22(s,1h),10.04(d,j=1.7hz,1h),8.19(dd,j=2.0,1.2hz,1h),8.10(dd,j=11.0,2.0hz,1h),7.98(s,1h),7.84
–
7.78(m,2h),7.49
–
7.41(m,2h),7.40
–
7.32(m,1h)。ms m/z[m+h]
+
,c
16h10
fno3的计算值:284;实测值:284。
[0805]
实施例a55:3-氟-2-羟基-5-(2-苯基噻唑-5-基)苯甲醛(化合物a91)
[0806][0807]
利用可商购获得的5-溴-2-苯基噻唑,使用与如实施例a53中所述的方法类似的方法制备标题化合物。产率9%。1h nmr(500mhz,cdcl3)δ11.15(s,1h),10.03(d,j=1.8hz,1h),8.03(dd,j=2.1,1.2hz,1h),8.01(s,1h),7.97(dd,j=11.1,2.1hz,1h),7.62
–
7.59(m,2h),7.47
–
7.43(m,2h),7.40
–
7.35(m,1h)。ms m/z[m+h]
+
,c
16h10
fno2s的计算值:300;实测值:300。
[0808]
实施例a56:5-(2-(4-氯苯基)噻唑-4-基)-3-氟-2-羟基苯甲醛(化合物a92)
[0809][0810]
利用可商购获得的4-溴-2-(4-氯苯基)噻唑,使用与如实施例a53中所述的方法类似的方法制备标题化合物。产率:14%。1h nmr(500mhz,氯仿-d)δ11.03(s,1h),10.04(d,j=1.8hz,1h),8.06(dd,j=2.1,1.2hz,1h),8.00
–
7.95(m,3h),7.47
–
7.43(m,3h)。ms m/z[m+h]
+
,c
16
h9clfno2s的计算值:334;实测值:334。
[0811]
实施例a57:3-氟-2-羟基-5-(4-苯基噻唑-2-基)苯甲醛(化合物a93)
[0812]
[0813]
利用可商购获得的2-溴-4-苯基噻唑,使用与如实施例a53中所述的方法类似的方法制备标题化合物。产率:30%。1h nmr(500mhz,cdcl3)δ11.16(s,1h),10.04(d,j=1.8hz,1h),8.08
–
8.04(m,1h),8.07(s 1h),7.99
–
7.97(m,2h),7.50(s,1h),7.49
–
7.44(m,2h),7.40
–
7.36(m,1h)。ms m/z[m+h]
+
,c
16h10
fno2s的计算值:300;实测值:300。
[0814]
实施例a58:3-氟-2-羟基-5-(5-苯基-1,3,4-噻二唑-2-基)苯甲醛(化合物a94)
[0815][0816]
利用可商购获得的2-溴-5-苯基-1,3,4-噻二唑,使用与如实施例a53中所述的方法类似的方法制备标题化合物。产率:20%。1h nmr(500mhz,氯仿-d)δ11.26(s,1h),10.04(d,j=1.7hz,1h),8.08(dd,j=2.0,1.2hz,1h),8.02(tt,j=7.4,2.1hz,3h),7.55
–
7.49(m,3h)。ms m/z[m+h]
+
,c
15
h9fn2o2s的计算值:301;实测值:301。
[0817]
实施例a59:3-氟-2-羟基-5-(3-苯基-1,2,4-噻二唑-5-基)苯甲醛(新化合物a95)
[0818][0819]
使用与如实施例a53中所述的方法类似的方法制备标题化合物。然而,根据dimauro等人(j.org.chem,2006,71(10),359-3962.)的程序合成和分离中间体3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛。
[0820]
步骤1:向5ml微波小瓶中添加5-溴-3氟-水杨醛(329mg,1.5mmol)、双(频哪醇合)二硼(419mg,1.65mmol)、乙酸钾(295mg,3mmol)和pd(dppf)cl2(109mg,0.15mmol),随后添加5ml二噁烷。将混合物用氩气吹扫,并且在微波中在140℃下加热45分钟。使混合物冷却,转移至圆底烧瓶,浓缩至干燥,并且再悬浮于dcm中。在经硅藻土过滤以及再次浓缩之后,将产物通过快速柱色谱法来纯化,使用0-100%dcm/己烷作为洗脱剂,以提供在静置后固化的呈无色油状的3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(237mg,59%产率)。1h nmr(500mhz,dmso-d6)δ11.35(s,1h),10.27(s,1h),7.82(dd,j=1.6,0.7hz,1h),7.59(dd,j=11.1,1.5hz,1h),1.29(s,12h)。
[0821]
步骤2:向2ml微波小瓶中添加来自步骤1a的3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(40mg,0.15mmol)、5-溴-3-苯基-1,2,4-噻二唑(36mg,0.15mmol)、xphos pd g3(6.4mg,0.05当量)和xphos(3.6mg,0.05当量)、二噁烷(0.6ml)以及经脱气0.5m k3po4(0.6ml)。将微波容器用氩气吹扫,并且在微波中加热至130℃,持续30分钟。将反应混合物用dcm稀释,用柠檬酸酸化至ph=3,并且用dcm萃取3次。将合并的有机相用盐水洗涤,并且经无水na2so4干燥,过滤并蒸发。将粗产物通过快速柱色谱法(0-10%meoh/dcm)来纯化。产率(8mg,17%)。1h nmr(500mhz,dmso-d6)δ12.02(bs,1h),10.36(s,1h),8.36
–
8.24(m,3h),8.24
–
8.15(m,1h),7.64
–
7.47(m,3h)。ms m/z[m+h]
+
,c
15
h9fn2o2s的计算值:301;实测值:301。
(吡咯烷-1-基)苯基)噻唑的合成。添加二噁烷(8.7ml)和经脱气0.5m k3po4(8.7ml),并且将小瓶用氩气脱气。将密封反应容器加热至140℃,持续4小时,冷却,用dcm稀释,并且用水和饱和nahco3水溶液萃取。将合并的水层用dcm再萃取2次。将合并的有机层用盐水洗涤,经na2so4干燥,过滤并蒸发。使用0-70%dcm/己烷纯化以提供5-溴-2-(4-(吡咯烷-1-基)苯基)噻唑(274mg,51%产率)。1h nmr(500mhz,dmso-d6)δ7.79(s,1h),7.74
–
7.61(m,2h),6.67
–
6.52(m,2h),3.29
–
3.22(m,4h),2.08
–
1.87(m,4h)。
[0831]
通过以与如实施例a59中所述的方法类似的方法使中间体a 3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(94mg,0.35mmol)与中间体b 5-溴-2-(4-(吡咯烷-1-基)苯基)噻唑(109mg,0.35mmol)偶联来合成化合物a55 3-氟-2-羟基-5-(2-(4-(吡咯烷-1-基)苯基)噻唑-5-基)苯甲醛。产率:32mg,25%。1h nmr(500mhz,dmso-d6)δ11.20(bs,1h),10.31(s,1h),8.14(s,1h),7.96(dd,j=11.9,2.3hz,1h),7.82
–
7.72(m,2h),7.64(dd,j=2.3,1.0hz,1h),6.66
–
6.57(m,2h),3.31
–
3.28(m,4h),2.02
–
1.94(m,4h)。ms m/z[m+h]
+
,c
20h17
fn2o2s的计算值:369;实测值:369。
[0832]
实施例a63:3-氟-2-羟基-5-(4-甲基-2-(4-(吡咯烷-1-基)苯基)噻唑-5-基)苯甲醛(化合物a98)
[0833][0834]
利用3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(50mg,0.19mmol)和通过与如对于实施例a62中的中间体b所述的方法类似的方法制备的5-溴-4-甲基-2-(4-(吡咯烷-1-基)苯基)噻唑(58mg,0.19mmol),使用与如实施例a62中所述的方法类似的方法制备标题化合物以制备3-氟-2-羟基-5-(4-甲基-2-(4-(吡咯烷-1-基)苯基)噻唑-5-基)苯甲醛(28mg,40%产率)。1h nmr(500mhz,氯仿-d)δ10.98(s,1h),9.97(d,j=1.8hz,1h),7.88
–
7.73(m,2h),7.50
–
7.43(m,2h),6.57(dd,j=9.1,2.6hz,2h),3.41
–
3.32(m,4h),2.51(s,3h),2.04(ddd,j=6.7,4.2,2.9hz,4h)。ms m/z[m+h]
+
,c
21h19
fn2o2s的计算值:383;实测值:383。
[0835]
实施例a64:5-羟基-2-(2-苯基噻唑-5-基)异烟甲醛(化合物a99)
[0836][0837]
使用与如实施例a59中所述的方法类似的方法,通过使2-溴-5-羟基异烟甲醛(50mg,0.25mmol)与可商购获得的2-苯基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)噻唑(71mg,0.25mmol)偶联来合成5-羟基-2-(2-苯基噻唑-5-基)异烟甲醛。产率:8mg,11%。1h nmr(499mhz,氯仿-d)δ10.35(s,1h),10.11(d,j=0.6hz,1h),8.55(d,j=0.7hz,1h),8.22(s,1h),8.04
–
7.96(m,2h),7.83(d,j=0.7hz,1h),7.52
–
7.42(m,3h)。ms m/z[m+h]
+
,c
15h10
n2o2s的计算值:283;实测值:283。
[0838]
实施例a65:5-(3-(4-(3,3-二甲基吡咯烷-1-基)苯基)-1,2,4-噻二唑-5-基)-3-氟-2-羟基苯甲醛(化合物a100)
[0839][0840]
使用与如实施例a46中所述的方法类似的方法从3,3-二甲基-1-(4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)吡咯烷(176mg,0.58mmol,1.1当量)和5-(3-溴-1,2,4-噻二唑-5-基)-3-氟-2-羟基苯甲醛(162mg,0.53mmol,1.0当量)(如实施例a47中所制备)制备标题化合物以产生呈黄色固体状的最终标题化合物(22mg,0.06mmol,10%产率)。1h nmr(dmso-d6,400mhz)δ:11.87(br,1h),10.36(s,1h),8.23(m,1h),8.16(s,1h),8.10(d,j=8.8hz,2h),6.61(d,j=8.8hz,2h),3.41(t,j=6.8hz,2h),3.11(s,2h),1.80(t,j=6.8hz,2h),1.13(s,6h)。lc-ms m/z[m+h]
+
,c
21h20
fn3o2s的计算值:398;实测值:398。
[0841]
实施例a66:3-氟-2-羟基-5-(2-(3-(吡咯烷-1-基)苯基)噻唑-5-基)苯甲醛(化合物a101)
[0842][0843]
以3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(11mg,0.04mmol)和通过与如对于实施例a62中的中间体b所述的方法类似的方法制备的5-溴-2-(3-(吡咯烷-1-基)苯基)噻唑(14mg,0.17mmol)作为起始物料,使用与如实施例a62中所述的方法类似的方法来合成3-氟-2-羟基-5-(2-(3-(吡咯烷-1-基)苯基)噻唑-5-基)苯甲醛。产率:8mg,51%。1h nmr(500mhz,dmso-d6)δ11.28(s,1h),10.32(s,1h),8.28(s,1h),8.02(dd,j=11.8,2.3hz,1h),7.78
–
7.67(m,1h),7.29(t,j=7.9hz,1h),7.15(dt,j=7.6,1.1hz,1h),7.07(t,j=2.1hz,1h),6.67(dd,j=8.2,2.5hz,1h),3.30
–
3.27(m,4h),2.03
–
1.95(m,4h)。ms m/z[m+h]
+
,c
20h17
fn2o2s的计算值:369;实测值:369。
[0844]
实施例a67:3-氟-2-羟基-5-(2-(6-(吡咯烷-1-基)吡啶-3-基)噻唑-5-基)苯甲醛(新化合物a102)
[0845][0846]
从3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(25mg,0.09mmol)和通过与如对于实施例a62中的中间体b所述的方法类似的方法制备的5-溴-2-(6-(吡咯烷-1-基)吡啶-3-基)噻唑(29mg,0.09mmol)起始,使用与如实施例a62中所述的方法类似的方法制备标题化合物。产率:31mg,89%。1h nmr(500mhz,dmso-d6)δ11.24(s,1h),10.31(s,1h),8.65(dd,j=2.5,0.7hz,1h),8.19(s,1h),8.01
–
7.94(m,2h),7.65
(dd,j=2.4,1.0hz,1h),6.56(dd,j=9.0,0.8hz,1h),3.45(d,j=6.4hz,4h),2.01
–
1.93(m,4h)。ms m/z[m+h]
+
,c
19h16
fn3o2s的计算值:370;实测值:370。
[0847]
实施例a68:3-氟-2-羟基-5-(4-甲基-2-(3-(吡咯烷-1-基)苯基)噻唑-5-基)苯甲醛(化合物a103)
[0848][0849]
利用3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(46mg,0.17mmol)和以与实施例a62中的中间体b类似的方式制备的5-溴-4-甲基-2-(3-(吡咯烷-1-基)苯基)噻唑(55mg,0.17mmol),使用与如实施例a62中所述的方法类似的方法制备标题化合物。产率:31mg,47%。1h nmr(500mhz,dmso-d6)δ11.26(s,1h),10.32(s,1h),7.74(dd,j=11.7,2.3hz,1h),7.59(dd,j=2.3,1.0hz,1h),7.31
–
7.22(m,1h),7.14
–
7.07(m,1h),7.03(t,j=2.1hz,1h),6.65(ddd,j=8.3,2.5,0.9hz,1h),3.31
–
3.25(m,4h),2.48(s,3h),2.02
–
1.93(m,4h)。ms m/z[m+h]
+
,c
21h19
fn2o2s的计算值:383;实测值:383。
[0850]
实施例a69:3-氟-2-羟基-5-(4-甲基-2-(6-(吡咯烷-1-基)吡啶-3-基)噻唑-5-基)苯甲醛(化合物a104)
[0851][0852]
从3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(49mg,0.18mmol)和以与实施例a62中的中间体b类似的方式制备的5-溴-4-甲基-2-(6-(吡咯烷-1-基)吡啶-3-基)噻唑(59mg,0.18mmol)起始,使用与如实施例a62中所述的方法类似的方法制备标题化合物。产率:62mg,89%。1h nmr(499mhz,dmso-d6)δ11.23(s,1h),10.32(s,1h),8.61(d,j=2.4hz,1h),7.96(dd,j=8.9,2.5hz,1h),7.71(dd,j=11.7,2.3hz,1h),7.56(dd,j=2.3,1.0hz,1h),6.54(dd,j=11.2,8.9hz,1h),3.45(d,j=6.5hz,4h),2.44(s,3h),1.96(h,j=3.3hz,4h)。ms m/z[m+h]
+
,c
20h18
fn3o2s的计算值:384;实测值:384。
[0853]
实施例a70:5-(4-(4-(3,3-二甲基吡咯烷-1-基)苯基)噻唑-2-基)-3-氟-2-羟基苯甲醛(化合物a105)
[0854][0855]
使用与如实施例a46中所述的方法类似的方法从3,3-二甲基-1-(4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)吡咯烷(153mg,0.51mmol,1.1当量)和5-(4-溴
噻唑-2-基)-3-氟-2-羟基苯甲醛(140mg,0.46mmol,1.0当量)(如实施例a47中所制备)制备标题化合物以产生呈黄色固体状的最终标题化合物(48mg,0.12mmol,26%产率)。1h nmr(dmso-d6,400mhz)δ:11.51(br,1h),10.35(s,1h),8.11(dd,j=11.2hz,2.0hz,1h),8.05(s,1h),7.84(d,j=8.8hz,2h),7.79(s,1h),6.56(d,j=8.8hz,2h),3.38(m,2h),3.07(s,2h),1.78(d,j=6.8hz,2h),1.12(s,6h)。lc-ms m/z[m-h]-,c
22h21
fn2o2s的计算值:395;实测值:395。
[0856]
实施例a71:3-氟-2-羟基-5-(2-(6-(吡咯烷-1-基)吡啶-3-基)噻唑-4-基)苯甲醛(化合物a123)
[0857][0858]
步骤1:4-溴-2-(6-(吡咯烷-1-基)吡啶-3-基)噻唑
[0859]
在100℃下在氮气保护下将2,4-二溴噻唑(486mg,2.0mmol,1.0当量)、2-(吡咯烷-1-基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)吡啶(603mg,2.2mmol,1.1当量)、碳酸钾(828mg,6.0mmol,3.0当量)和pdcl2(dppf)(146mg,0.2mmol,0.1当量)于二噁烷/水(10ml/5ml)中的混合物加热1小时。使混合物冷却至室温,倾倒至水中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱来纯化,使用己烷-etoac(0-100%),以产生4-溴-2-(6-(吡咯烷-1-基)吡啶-3-基)噻唑(520mg,84%产率)。lc-ms m/z[m+h]
+
,c
12h12
brn3s的计算值:311;实测值:311。
[0860]
步骤2:在30ml密封盖玻璃小瓶中,将3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(266mg,1.0mmol,1.0当量)、4-溴-2-(6-(吡咯烷-1-基)吡啶-3-基)噻唑(310mg,1.30mmol,1.0当量)、碳酸钠(318mg,3.0mmol,3.0当量)在1:1二噁烷-水(10ml)中组合,接着持续2分钟使氮气通过混合物并添加pd(pph3)4(112mg,0.1mmol,0.1当量),并且将盖子密封并在105℃下继续8小时。接着冷却至室温,并且添加水并用etoac(2x 25ml)萃取,并且用盐水洗涤并经硫酸钠干燥,并且蒸发。将所得粗产物通过柱色谱法来纯化,使用己烷-etoac(0-100%)洗脱剂,以产生呈黄色固体状的最终标题化合物(108mg,29%产率)。1h nmr(500mhz,氯仿-d)δ11.00(s,1h),10.02(d,j=1.8hz,1h),8.77(d,j=2.4hz,1h),8.11
–
8.02(m,2h),7.94(dd,j=11.7,2.0hz,1h),7.29(s,1h),6.43(d,j=8.9hz,1h),3.54(m,4h),2.10
–
2.01(m,4h)。lc-ms m/z[m+h]
+
,c
19h16
fn3o2s的计算值:370;实测值:370。
[0861]
实施例a72:3-氟-2-羟基-5-(2-(3-(吡咯烷-1-基)苯基)噻唑-4-基)苯甲醛(化合物a124)
[0862][0863]
步骤1:4-溴-2-(3-(吡咯烷-1-基)苯基)噻唑
[0864]
使用与如实施例a71中所述的方法类似的方法从1-(3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)吡咯烷(601mg,2.2mmol,1.1当量)和2,4-二溴噻唑(486mg,2.0mmol,1.0当量)制备标题化合物以产生呈灰白色固体状的所需产物(540mg,87%产率)。lc-ms m/z[m+h]
+
,c
13h13
brn2s的计算值:310;实测值:310。
[0865]
步骤2:使用与如实施例a46中所述的方法类似的方法从3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(133mg,0.5mmol,1.0当量)和4-溴-2-(3-(吡咯烷-1-基)苯基)噻唑(155mg,0.5mmol,1.0当量)制备标题化合物以产生呈黄色固体状的最终标题化合物(110mg,41%产率)。1h nmr(500mhz,氯仿-d)δ11.01(s,1h),10.04(d,j=1.9hz,1h),8.06(t,j=1.6hz,1h),7.97(dd,j=11.6,2.1hz,1h),7.40(s,1h),7.33
–
7.27(m,2h),7.20(t,j=2.0hz,1h),6.66(dt,j=8.2,1.6hz,1h),3.39m,4h),2.15
–
1.96(m,4h)。lc-ms m/z[m+h]
+
,c
20h17
fn2o2s的计算值:369;实测值:369。
[0866]
实施例a73:3-氟-2-羟基-5-(2-(6-(吡咯烷-1-基)-5-(三氟甲基)吡啶-3-基)噻唑-5-基)苯甲醛(化合物a114)
[0867][0868]
利用3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(69mg,0.35mmol)与使用与对于实施例a62中的中间体b所述的方法类似的方法合成的5-溴-2-(6-(吡咯烷-1-基)-5-(三氟甲基)吡啶-3-基)噻唑(97mg,0.35mmol),使用与如实施例a62中所述的方法类似的方法合成3-氟-2-羟基-5-(2-(6-(吡咯烷-1-基)-5-(三氟甲基)吡啶-3-基)噻唑-5-基)苯甲醛。产率:50mg,45%。1h nmr(499mhz,dmso-d6)δ11.28(s,1h),10.31(s,1h),8.85(d,j=2.3hz,1h),8.33(d,j=2.3hz,1h),8.27(s,1h),8.00(dd,j=11.9,2.3hz,1h),7.67(dd,j=2.3,1.0hz,1h),3.60(d,j=6.3hz,4h),1.98
–
1.88(m,4h)。lc-ms m/z[m-h]
+
,c
20h15
f4n3o2s的计算值:438,实测值:438。
[0869]
实施例a74:3-氟-2-羟基-5-(5-(3-(吡咯烷-1-基)苯基)-1,2,4-噻二唑-3-基)苯甲醛(化合物a125)
[0870][0871]
步骤1:3-溴-5-(3-(吡咯烷-1-基)苯基)-1,2,4-噻二唑
[0872]
使用与如实施例a71中所述的方法类似的方法从1-(3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)吡咯烷(601mg,2.2mmol,1.1当量)和3-溴-5-氯-1,2,4-噻二唑(310mg,2.0mmol,1.0当量)制备标题化合物以产生呈黄色固体状的所需产物(351mg,57%产率)。lc-ms m/z[m+h]
+
,c
12h12
brn3s的计算值:311;实测值:311。
[0873]
步骤2:使用与如实施例a46中所述的方法类似的方法从3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(200mg,0.75mmol,1.5当量)和3-溴-5-(3-(吡咯烷-1-基)苯基)-1,2,4-噻二唑(155mg,0.5mmol,1.0当量)制备标题化合物以产生呈黄色固体状的最终标题化合物(42mg,49%产率)。1h nmr(500mhz,氯仿-d)δ11.21(s,1h),10.06(d,j=1.8hz,1h),8.46(t,j=1.6hz,1h),8.39(dd,j=11.4,2.0hz,1h),7.34(t,j=7.9hz,1h),7.28
–
7.23(m,1h),7.17(t,j=2.1hz,1h),6.74(dd,j=8.3,2.5hz,1h),3.45
–
3.28(m,4h),2.07(m,4h)。lc-ms m/z[m+h]
+
,c
19h16
fn3o2s的计算值:370;实测值:370。
[0874]
实施例a75:3-氟-2-羟基-5-(2-(6-(哌啶-1-基)吡啶-3-基)噻唑-4-基)苯甲醛(化合物a126)
[0875][0876]
步骤1:4-溴-2-(6-(哌啶-1-基)吡啶-3-基)噻唑
[0877]
使用与如实施例a71中所述的方法类似的方法从2-(哌啶-1-基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)吡啶(634mg,2.2mmol,1.1当量)和2,4-二溴噻唑(486mg,2.0mmol,1.0当量)制备标题化合物以产生呈黄色固体状的所需产物(352mg,54%产率)。lc-ms m/z[m+h]
+
,c
13h14
brn3s的计算值:325;实测值:325。
[0878]
步骤2:使用与如实施例a46中所述的方法类似的方法从3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(200mg,0.75mmol,1.5当量)和4-溴-2-(6-(哌啶-1-基)吡啶-3-基)噻唑(162mg,0.5mmol,1.0当量)制备标题化合物以产生呈黄色固体状的最终标题化合物(21mg,11%产率)。1h nmr(500mhz,氯仿-d)δ11.00(s,1h),10.03(d,j=1.9hz,1h),8.76(d,j=2.5hz,1h),8.07(dd,j=9.0,2.5hz,1h),8.04(t,j=1.6hz,1h),7.94(dd,j=11.7,2.1hz,1h),7.30(s,1h),6.69(d,j=9.0hz,1h),3.74
–
3.40(m,4h),
1.74
–
1.63(m,6h)。lc-ms m/z[m+h]
+
,c
20h18
fn3o2s的计算值:384;实测值:384。
[0879]
实施例a76:3-氟-2-羟基-5-(2-(6-(哌啶-1-基)吡啶-3-基)噻唑-5-基)苯甲醛(化合物a127)
[0880][0881]
步骤1:5-溴-2-(6-(哌啶-1-基)吡啶-3-基)噻唑
[0882]
使用与如实施例a71中所述的方法类似的方法从2-(哌啶-1-基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)吡啶(634mg,2.2mmol,1.1当量)和2,5-二溴噻唑(486mg,2.0mmol,1.0当量)制备标题化合物以产生呈黄色固体状的所需产物(225mg,35%产率)。lc-ms m/z[m+h]
+
,c
13h14
brn3s的计算值:325;实测值:325。
[0883]
步骤2:使用与如实施例a46中所述的方法类似的方法从3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(80mg,0.3mmol,1.2当量)和5-溴-2-(6-(哌啶-1-基)吡啶-3-基)噻唑(81mg,0.25mmol,1.0当量)制备标题化合物以产生呈黄色固体状的最终标题化合物(78mg,81%产率)。1h nmr(500mhz,氯仿-d)δ10.98(s,1h),9.99(d,j=1.8hz,1h),8.70(d,j=2.5hz,1h),8.00(dd,j=9.0,2.5hz,1h),7.87(s,1h),7.62
–
7.53(m,2h),6.69(d,j=9.0hz,1h),3.77
–
3.48(m,4h),1.75
–
1.63(m,6h)。lc-ms m/z[m+h]
+
,c
20h18
fn3o2s的计算值:384;实测值:384。
[0884]
实施例a77:5-(2-(4-(2-氮杂螺[3.3]庚烷-2-基)苯基)噻唑-5-基)-3-氟-2-羟基苯甲醛。(化合物a116)
[0885][0886]
步骤1:从3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛(175mg,0.66mmol)和可商购获得的5-溴-2-(4-氯苯基)噻唑(181mg,0.66mmol)起始,来自实施例a95的程序用于制备化合物a130 5-(2-(4-氯苯基)噻唑-5-基)-3-氟-2-羟基苯甲醛(68mg,31%产率)。lc-ms m/z[m-h]
+
,c
16
h9clfno2s的计算值:334;实测值:334。
[0887]
步骤2:与如实施例a61中所述的方法类似的方法用于制备5-(2-(4-(2-氮杂螺[3.3]庚烷-2-基)苯基)噻唑-5-基)-3-氟-2-羟基苯甲醛,产率是11%。1h nmr(500mhz,dmso-d6)δ11.22(s,1h),10.31(d,j=3.0hz,1h),8.15(s,1h),7.97
–
7.92(m,1h),7.74(d,j=6.7hz,1h),7.73(s,1h),7.64(dd,j=2.3,1.0hz,1h),6.50
–
6.44(m,2h),3.87(s,4h),2.19(t,j=7.6hz,4h),1.87
–
1.75(m,2h)。lc-ms m/z[m-h]
+
,c
22h19
fn2o2s的计算值:395;实测值:395。
[0888]
实施例a78:5-羟基-2-(2-(4-(吡咯烷-1-基)苯基)噻唑-5-基)异烟甲醛(化合物a112)
[0889][0890]
步骤1:使用如实施例a62中所述的类似方法合成起始物料中间体b。使用用于制备实施例a59中的3-氟-2-羟基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯甲醛的类似方法制备中间体c2-(4-(吡咯烷-1-基)苯基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)噻唑。然而,在下一反应中使用之前,不对中间体c进行纯化。在反应完成之后,将粗混合物溶解于dcm中,经硅藻土过滤,并且浓缩至干燥。
[0891]
步骤2:使用如实施例a59中所述的类似方法,粗中间体c2-(4-(吡咯烷-1-基)苯基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)噻唑(123mg)和2-溴-5-羟基异烟甲醛(70mg,0.35mmol)用于制备5-羟基-2-(2-(4-(吡咯烷-1-基)苯基)噻唑-5-基)异烟甲醛(12mg,产率:10%)。1h nmr(500mhz,dmso-d6)δ11.29(bs,1h),10.39(s,1h),8.44(s,1h),8.31(s,1h),7.99(s,1h),7.83
–
7.73(m,2h),6.67
–
6.55(m,2h),3.32-3.29(m,4h),2.36
–
1.61(m,4h)。lc-ms m/z[m+h]
+
,c
19h17
n3o2s的计算值:352;实测值:352。
[0892]
实施例b1:3-氟-2-羟基-5-((4-(吡咯烷-1-基)苯基)乙炔基)苯甲醛(化合物编号b1)
[0893][0894]
步骤1:1-(4-乙炔基苯基)吡咯烷
[0895][0896]
在-78℃下向tms-重氮甲烷(17.14ml,34.29mmol)于thf(50ml)中的溶液中添加buli(13.72ml,34.29mmol,2m,于thf中)。在-78℃下将反应搅拌30分钟。接着添加4-(吡咯烷-1-基)苯甲醛(5g,28.57mmol)。在-78℃下将反应再搅拌1小时。将混合物用饱和nh4cl(150ml)淬灭,接着用乙酸乙酯(100mlx3)萃取。将有机萃取物合并,经无水硫酸钠干燥,并且浓缩。将粗物质通过硅胶柱色谱法(石油醚/乙酸乙酯=200:1至100:1)来纯化以产生呈白色固体状的所需产物(2.1g,43%产率)。1h nmr(cdcl3,400mhz)δ:7.35(d,j=8.4hz,2h),6.46(d,j=8.4hz,2h),3.29(t,j=6.2hz,4h),2.98(s,1h),2.01(t,j=6.2hz,4h)。
[0897]
步骤2:在80℃下将5-溴-3-氟-2-(4-甲氧基苯甲基氧基)苯甲醛(988mg,2.92mmol)、1-(4-乙炔基苯基)吡咯烷(600mg,3.51mmol)、tbaf.3h2o(5.5g,17.54mmol)和
pd(pph3)2cl2(62mg,0.09mmol)于thf(20ml)中的混合物加热2小时。使混合物冷却至室温,用水(100ml)稀释,接着用乙酸乙酯(100mlx3)萃取。将有机萃取物合并,用盐水(80ml)洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯=20:1至10:1)来纯化以产生经pmb保护的倒数第二个产物(417mg,33%产率)。将经pmb保护的中间体(100mg,0.23mmol)溶解于二氯甲烷(5ml)中,并且添加tfa(3ml)。在室温下将反应搅拌30分钟。在真空中移除溶剂,并且将残余物通过制备型tlc(石油醚/乙酸乙酯=5:1)来纯化以提供呈黄色固体状的标题化合物(23mg,32%产率)。1h nmr(cdcl3,400mhz)δ:11.00(s,1h),9.90(s,1h),7.52(s,1h),7.46(d,j=11.2hz,1h),7.37(d,j=8.4hz,2h),6.51(d,j=8.4hz,2h),3.31(m,4h),2.02(m,4h);lc-ms m/z[m-h]-,c
19h16
fno2的计算值:308;实测值:308。
[0898]
实施例b2:3-氟-2-羟基-5-((4-(哌啶-1-基)苯基)乙炔基)苯甲醛(化合物编号b2)
[0899][0900]
步骤1:1-(4-乙炔基苯基)哌啶
[0901][0902]
在-78℃下向tms-重氮甲烷(6.3ml,12.6mmol)于thf(20ml)中的溶液中添加buli(6.3ml,12.6mmol,2m,于thf中)。在-78℃下将反应搅拌30分钟。接着添加处于thf中的4-(哌啶-1-基)苯甲醛(1.89g,10mmol)。在-78℃下将反应再搅拌1小时。将混合物用饱和nh4cl(100ml)淬灭,接着用乙酸乙酯(100mlx3)萃取。将有机萃取物合并,经无水硫酸钠干燥,并且浓缩。将粗物质通过硅胶柱色谱法来纯化以产生所需产物(1.42g,77%产率)。
[0903]
步骤2:使用与如实施例b1中所述的方法类似的方法从5-溴-3-氟-2-羟基苯甲醛(219mg,1.0mmol)和1-(4-乙炔基苯基)哌啶(185mg,1.0mmol)制备标题化合物以产生呈黄色固体状的标题化合物(91mg,28%产率)。1h nmr(dmso-d6,400mhz)δ11.33(br,1h),10.26(s,1h),7.67(d,j=11.2hz,1h),7.57(s,1h),7.35(d,j=8.4hz,2h),6.93(d,j=8.4hz,2h),3.24(m,4h),1.57(m,6h);lc-ms m/z[m+h]
+
,c
20h18
fno2的计算值:324;实测值:324。
[0904]
实施例b3:3-氟-2-羟基-5-((4-吗啉代苯基)乙炔基)苯甲醛(化合物编号b3)
[0905][0906]
步骤1:4-(4-乙炔基苯基)吗啉
[0907][0908]
在-78℃下向tms-重氮甲烷(6.3ml,12.6mmol)于thf(20ml)中的溶液中添加buli(6.3ml,12.6mmol,2m,于thf中)。在-78℃下将反应搅拌30分钟。接着添加4-吗啉代苯甲醛(2g,10.5mmol)。在-78℃下将反应再搅拌1小时。将混合物用饱和nh4cl(100ml)淬灭,接着用乙酸乙酯(100mlx3)萃取。将有机萃取物合并,经无水硫酸钠干燥,并且浓缩。将粗物质通过硅胶柱色谱法(石油醚/乙酸乙酯=200:1至100:1)来纯化以产生呈白色固体状的所需产物(1.1g,56%产率)。
[0909]
步骤2:在80℃下将5-溴-3-氟-2-(4-甲氧基苯甲基氧基)苯甲醛(561mg,3.0mmol)、4-(4-乙炔基苯基)吗啉(1.01g,3.0mmol)、tbaf.3h2o(5.68g,18.0mmol)和pd(pph3)2cl2(63mg,0.09mmol)于thf(20ml)中的混合物加热3小时。使混合物冷却至室温,用水(100ml)稀释,接着用乙酸乙酯(100mlx3)萃取。将有机萃取物合并,用盐水(80ml)洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯=5:1至1:1)来纯化以产生呈黄色固体状的经pmb保护的倒数第二个产物(410mg,31%产率)。将经pmb保护的中间体(100mg,0.22mmol)溶解于二氯甲烷(5ml)中,并且添加tfa(3ml)。在室温下将反应搅拌30分钟。在真空中移除溶剂,并且将残余物通过制备型tlc(石油醚/乙酸乙酯=1:1)来纯化以提供呈黄色固体状的标题产物(27mg,37%产率)。1h nmr(dmso-d6,400mhz)δ:10.20(s,1h),7.43-7.46(m,2h),7.36(d,j=8.4hz,2h),6.95(d,j=8.4hz,2h),3.73(m,4h),3.17(m,4h);lc-ms m/z[m+h]
+
,c
19h16
fno3的计算值:326;实测值:326。
[0910]
实施例b4:2-氟-6-羟基-4-((4-(吡咯烷-1-基)苯基)乙炔基)苯甲醛(化合物编号b4)
[0911][0912]
在氮气氛围下使4-溴-2-氟-6-羟基苯甲醛(900mg,4.1mmol)、1-(4-乙炔基苯基)吡咯烷(847mg,5.0mmol)、pdcl2(pph3)2(290mg,0.4mmol)和tbaf.3h2o(7.8g,24.8mmol)于thf(30ml)中的混合物回流3小时。使混合物冷却至室温,用水(100ml)稀释,并且用乙酸乙酯(100mlx3)萃取。将有机萃取物合并,用盐水(50mlx2)洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯=100:1至20:1)来纯化以产生呈黄色固体状的标题产物(900mg,71%产率)。1h nmr(cdcl3,400mhz)δ:11.53(s,1h),10.18(s,1h),7.40(d,j=8.8hz,2h),6.83(s,1h),6.71(m,1h),6.51(d,j=8.4hz,2h),3.32(m,4h),2.03(m,4h);lc-ms m/z[m+h]
+
,c
19h16
fno2的计算值:310;实测值:310。
[0913]
实施例b5:2-氟-6-羟基-4-((4-(哌啶-1-基)苯基)乙炔基)苯甲醛(化合物编号b5)
[0914][0915]
使用与如实施例b1中所述的方法类似的方法从4-溴-2-氟-6-羟基苯甲醛(219mg,1.0mmol)和1-(4-乙炔基苯基)哌啶(185mg,1.0mmol)制备标题化合物以产生呈黄色固体状的标题化合物(181mg,56%产率)。1h nmr(dmso-d6,400mhz)δ11.37(br,1h),10.22(s,1h),7.39(d,j=8.8hz,2h),6.93(m,2h),6.88(m,2h),3.28(m,4h),1.58(m,6h);lc-ms m/z[m+h]
+
,c
20h18
fno2的计算值:324;实测值:324。
[0916]
实施例b6:2-氟-6-羟基-4-((4-吗啉代苯基)乙炔基)苯甲醛(化合物编号b6)
[0917][0918]
使用与如实施例b1中所述的方法类似的方法从4-溴-2-氟-6-羟基苯甲醛(219mg,1.0mmol)和4-(4-乙炔基苯基)吗啉(187mg,1.0mmol)制备标题化合物以产生呈黄色固体状的标题化合物(134mg,41%产率)。1h nmr(dmso-d6,400mhz)δ11.38(br,1h),10.22(s,1h),7.45(d,j=8.4hz,2h),6.99(d,j=8.4hz,2h),6.91(m,2h),3.73(m,4h),3.22(m,4h);lc-ms m/z[m+h]
+
,c
19h16
fno3的计算值:326;实测值:326。
[0919]
实施例b7:2-羟基-6-甲氧基-4-((4-(吡咯烷-1-基)苯基)乙炔基)苯甲醛(化合物编号b7)
[0920][0921]
在氮气氛围下使4-溴-2-羟基-6-甲氧基苯甲醛(462mg,2.0mmol)、1-(4-乙炔基苯基)吡咯烷(340mg,2.0mmol)、pdcl2(pph3)2(140mg,0.2mmol)和tbaf.3h2o(3.78g,12.0mmol)于thf(30ml)中的混合物回流2小时。使混合物冷却至室温,用水(100ml)稀释,并且用乙酸乙酯(100mlx3)萃取。将有机萃取物合并,用盐水(50mlx2)洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯/二氯甲烷=300:1:1至200:1:20)来纯化以产生呈黄色固体状的标题产物(320mg,50%产率)。1h nmr(cdcl3,400mhz)δ12.03(s,1h),10.26(s,1h),7.41(d,j=8.0hz,2h),6.64(s,1h),6.47-6.53(m,3h),3.60(s,3h),3.31(m,4h),2.03(m,4h);lc-ms m/z[m+h]
+
,c
20h19
no3的计算值:322;实测值:322。
[0922]
实施例b8:2-羟基-3-甲氧基-5-((4-吗啉代苯基)乙炔基)苯甲醛(化合物编号b8)
[0923][0924]
在80℃下将5-溴-3-甲氧基-2-(4-甲氧基苯甲基氧基)苯甲醛(1.3g,3.74mmol)、
4-(4-乙炔基苯基)吗啉(700mg,3.74mmol)、tbaf.3h2o(7g,22.44mmol)和pd(pph3)2cl2(79mg,0.11mmol)于thf(20ml)中的混合物加热2小时。使混合物冷却至室温,用水(100ml)稀释,接着用乙酸乙酯(100mlx3)萃取。将有机萃取物合并,用盐水(80ml)洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯=5:1至1:1)来纯化以产生经pmb保护的倒数第二个产物(880mg,51%产率)。将经pmb保护的中间体(100mg,0.22mmol)溶解于二氯甲烷(5ml)中,并且添加tfa(3ml)。在室温下将反应搅拌30分钟。在真空中移除溶剂,并且将残余物通过制备型tlc(石油醚/乙酸乙酯=1:1)来纯化以提供呈黄色固体状的标题产物(31mg,42%产率)。1h nmr(cdcl3,400mhz)δ:11.23(s,1h),9.90(s,1h),7.44(m,2h),7.38(s,1h),7.22(s,1h),6.89(m,2h),3.93(s,3h),3.88(m,4h),3.23(m,4h);lc-ms m/z[m+h]
+
,c
20h19
no4的计算值:338;实测值:338。
[0925]
实施例b9:n-(3-氟-5-甲酰基-4-羟基苯基)苯甲酰胺(化合物编号b9)
[0926][0927]
步骤1:3-氟-2-羟基-5-硝基苯甲醛
[0928]
在125ml圆底烧瓶中,在0℃下将含hno3(2.23ml,50.0mmol)的tfa(20ml)添加至3-氟-2-羟基苯甲醛(2g,14.3mmol)于乙酸(10ml)中的溶液中。在0℃下将反应搅拌1小时。将溶液倾倒至冰水中,并且将所得沉淀过滤并用石油醚洗涤以产生3-氟-2-羟基-5-硝基苯甲醛(1.8g,68%产率),其不经进一步纯化即用于下一反应。1h nmr(cdcl3,400mhz)δ:11.67(s,1h),10.05(s,1h),8.45(s,1h),8.27(dd,j=10.0hz,2.8hz,1h)。
[0929]
步骤2:2-(3-氟-2-(4-甲氧基苯甲基氧基)-5-硝基苯基)-1,3-二硫杂环己烷
[0930]
将bf3.et2o(4.9ml,18.2mmol)添加至3-氟-2-羟基-5-硝基苯甲醛(2.8g,15.1mmol)和丙烷-1,3-二硫醇(1.82ml,18.2mmol)于二氯甲烷(30ml)中的混合物中。在室温下将反应搅拌过夜。将混合物倾倒至冰水中,并且将所得沉淀过滤并用石油醚/二氯甲烷(10:1)洗涤。将滤饼干燥以产生呈黄色固体状的中间体(3.9g,94%产率)。1h nmr(dmso-d6,400mhz)δ:12.01(br,1h),8.09(m,2h),5.73(s,1h),3.17(m,2h),2.91(m,2h),2.13(m,1h),1.77(m,1h)。将中间体(2.75g,10.0mmol)溶解于dmf(20ml)中,接着将pmbcl(3.12g,20.0mmol)和碳酸钾(4.1g,30.0mmol,3当量)添加至反应混合物中。在90℃下将反应加热3小时。将混合物倾倒至水中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩以产生粗制2-(3-氟-2-(4-甲氧基苯甲基氧基)-5-硝基苯基)-1,3-二硫杂环己烷(3.3g,84%产率),其不经进一步纯化即用于下一反应。
[0931]
步骤3:3-(1,3-二硫杂环己烷-2-基)-5-氟-4-(4-甲氧基苯甲基氧基)苯胺
[0932]
在60℃下将2-(3-氟-2-(4-甲氧基苯甲基氧基)-5-硝基苯基)-1,3-二硫杂环己烷(2.1g,5.3mmol)和铁(3g,53.2mmol)于乙酸(20ml)中的混合物加热3小时。将混合物用乙酸乙酯稀释并过滤。将滤液用碳酸氢钠中和至ph 8-9,并且分离有机层。将水相用乙酸乙酯再萃取又两次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩以产生粗制3-(1,3-二硫杂环己烷-2-基)-5-氟-4-(4-甲氧基苯甲基氧基)苯胺(1.2g,62%产率),其不经进一步纯化即用于下一反应。1h nmr(dmso-d6,400mhz)δ:7.38(d,j=8.4hz,2h),6.96(d,j
=8.0hz,2h),6.50(s,1h),6.34(d,j=13.2hz,1h),5.42(s,1h),5.31(br,2h),4.81(s,2h),3.77(s,3h),3.02(m,2h),2.89(m,2h),2.12(m,1h),1.69(m,1h)。
[0933]
步骤4:n-(3-(1,3-二硫杂环己烷-2-基)-5-氟-4-(4-甲氧基苯甲基氧基)苯基)苯甲酰胺
[0934]
在室温下将3-(1,3-二硫杂环己烷-2-基)-5-氟-4-(4-甲氧基苯甲基氧基)苯胺(500mg,1.37mmol)、苯甲酰氯(289mg,2.05mmol)和三乙胺(415mg,4.11mmol)于二氯甲烷(20ml)中的溶液搅拌过夜。移除溶剂,并且将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯=20:1至5:1)来纯化以产生n-(3-(1,3-二硫杂环己烷-2-基)-5-氟-4-(4-甲氧基苯甲基氧基)苯基)苯甲酰胺(620mg,96%产率)。lc-ms m/z[m+h]
+
,c
25h24
fno3s2的计算值:470;实测值:470。
[0935]
步骤5:n-(3-氟-5-甲酰基-4-羟基苯基)苯甲酰胺
[0936]
在45℃下将n-(3-(1,3-二硫杂环己烷-2-基)-5-氟-4-(4-甲氧基苯甲基氧基)苯基)苯甲酰胺(620mg,1.32mmol)和dmp(1.12g,2.64mmol)于乙腈/二氯甲烷/水(16ml/2ml/2ml)中的混合物搅拌过夜。将混合物过滤,并且将滤饼用二氯甲烷洗涤。将滤液和洗涤液用5%碳酸氢钠溶液洗涤。将水相用二氯甲烷再萃取又两次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯/二氯甲烷=50:1:1至20:1:1)来纯化以产生经pmb保护的n-(3-氟-5-甲酰基-4-羟基苯基)苯甲酰胺(250mg,50%产率)。将经pmb保护的n-(3-氟-5-甲酰基-4-羟基苯基)苯甲酰胺(250mg,0.66mmol)溶解于二氯甲烷(5ml)中,并且将tfa(230mg,1.98mmol)添加至混合物中。在室温下将反应搅拌1小时。在真空中移除溶剂,并且将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯/二氯甲烷=20:1:1至10:1:1)来纯化以产生呈白色固体状的n-(3-氟-5-甲酰基-4-羟基苯基)苯甲酰胺(60mg,0.23mmol,35%产率)。1h nmr(dmso-d6,400mhz)δ:10.74(s,1h),10.39(s,1h),10.32(s,1h),7.90-8.04(m,4h),7.52-7.61(m,3h);lc-ms m/z[m+h]
+
,c
14h10
fno3的计算值:260;实测值:260。
[0937]
实施例b10:1-(3-氟-5-甲酰基-4-羟基苯基)-3-苯基脲(化合物编号b10)
[0938][0939]
步骤1:1-(3-(1,3-二硫杂环己烷-2-基)-5-氟-4-(4-甲氧基苯甲基氧基)苯基)-3-苯基脲
[0940]
将dppa(1.1g,4mmol)和三乙胺(0.42g,4mmol)添加至苯甲酸(0.35g,2.9mmol)于二噁烷(10ml)中的溶液中。在室温下将反应搅拌30分钟。接着,将3-(1,3-二硫杂环己烷-2-基)-5-氟-4-(4-甲氧基苯甲基氧基)苯胺(0.5g,1.4mmol,1当量)添加至反应混合物中,并且在90℃下将反应加热3小时。移除溶剂,并且将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯/二氯甲烷=30:1:1至10:1:1)来纯化以产生1-(3-(1,3-二硫杂环己烷-2-基)-5-氟-4-(4-甲氧基苯甲基氧基)苯基)-3-苯基脲(610mg,92%产率)。lc-ms m/z[m+h]
+
,c
25h25
fn2o3s2的计算值:485;实测值:485。
[0941]
步骤2:1-(3-氟-5-甲酰基-4-羟基苯基)-3-苯基脲
[0942]
在50℃下将1-(3-(1,3-二硫杂环己烷-2-基)-5-氟-4-(4-甲氧基苯甲基氧基)苯基)-3-苯基脲(300mg,0.62mmol)、mei(1.76g,12.4mmol)和nahco3(1g,12.4mmol)于乙腈/水(15ml/3ml)中的溶液搅拌过夜。将溶液用水稀释,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯/二氯甲烷=10:1:1至5:1:1)来纯化以产生经pmb保护的1-(3-氟-5-甲酰基-4-羟基苯基)-3-苯基脲(170mg,70%产率)。将经pmb保护的1-(3-氟-5-甲酰基-4-羟基苯基)-3-苯基脲(80mg,0.20mmol)溶解于6n hcl/二噁烷(5ml)中,并且在室温下将反应搅拌30分钟。将溶液倾倒至冰冷的饱和碳酸氢钠中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过制备型tlc(ch2cl2/meoh=20:1)来纯化以产生呈灰白色固体状的1-(3-氟-5-甲酰基-4-羟基苯基)-3-苯基脲(30mg,0.23mmol,54%产率)。1h nmr(dmso-d6,400mhz)δ:10.50(s,1h),10.28(s,1h),8.78(s,1h),8.70(s,1h),7.74(m,1h),7.46(m,3h),7.27(m,2h),6.97(m,1h);lc-ms m/z[m+h]
+
,c
14h11
fn2o3的计算值:275;实测值:275。
[0943]
实施例b11:3-氟-5-甲酰基-4-羟基-n-苯基苯甲酰胺(化合物编号b11)
[0944][0945]
步骤1:3-氟-5-甲酰基-4-羟基苯甲酸
[0946]
将hmpa(28g,0.2mol,2当量)于tfa(20ml)中的溶液添加至3-氟-4-羟基苯甲酸(15.6g,0.1mol)于tfa(30ml)中的溶液中。在100℃下将反应搅拌过夜。使溶液冷却至室温,并且倾倒至3m hcl(200ml)中。将混合物搅拌30分钟,并且将所得沉淀过滤并干燥以产生3-氟-5-甲酰基-4-羟基苯甲酸,其不经进一步纯化即用于下一反应。lc-ms m/z[m-h]-,c8h5fo4的计算值:183;实测值:183。
[0947]
步骤2:3-氟-5-甲酰基-4-羟基-n-苯基苯甲酰胺
[0948]
将hatu(0.63g,1.7mmol)和n-甲基吗啉(0.67g,6.6mmol)添加至3-氟-5-甲酰基-4-羟基苯甲酸(0.2g,1.1mmol)和苯胺盐酸盐(0.43g,3.3mmol)于二氯甲烷(30ml)中的混合物中。在室温下将混合物搅拌过夜。移除溶剂,并且将残余物溶解于乙醚(6ml)和4m hcl(6ml)的混合物中。在室温下将混合物搅拌过夜。将混合物用水(20ml)稀释,并且用乙酸乙酯(20mlx3)萃取。将有机萃取物合并,用盐水(20ml)洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯/二氯甲烷=10:1:1至2:1:1)来纯化以产生呈淡黄色固体状的所需3-氟-5-甲酰基-4-羟基-n-苯基苯甲酰胺产物(4%产率)。1h nmr(dmso-d6,400mhz)δ:11.67(br,1h),10.36(s,1h),10.30(s,1h),8.20(s,1h),8.11(dd,j=12.0hz,2.4hz,1h),7.75(d,j=7.2hz,1h),7.35(m,2h),7.11(m,1h);lc-ms m/z[m-h]-,c
14h10
fno3的计算值:258;实测值:258。
[0949]
实施例b12:3-氟-5-甲酰基-4-羟基-n-(4-(吡咯烷-1-基)苯基)苯甲酰胺(化合物编号b12)
[0950][0951]
以如对于实施例b11中的3-氟-5-甲酰基-4-羟基-n-苯基苯甲酰胺所述的类似方式合成标题化合物以获得呈绿色固体状的所需产物(67%产率)。1h nmr(dmso-d6,400mhz)δ:11.57(br,1h),10.35(s,1h),10.03(br,1h),8.18(s,1h),8.09(dd,j=12.0hz,2.4hz,1h),7.53(d,j=8.8hz,2h),6.55(d,j=8.0hz,2h),3.22(m,4h),1.95(m,4h);lc-ms m/z[m+h]
+
,c
18h17
fn2o3的计算值:329;实测值:329。
[0952]
实施例b13:3-氟-5-甲酰基-4-羟基-n-(4-(三氟甲基)苯基)苯甲酰胺(化合物编号b13)
[0953][0954]
步骤1:3-氟-5-甲酰基-4-甲氧基苯甲酸
[0955]
在50℃下将3-氟-5-甲酰基-4-羟基苯甲酸(0.5g,2.7mmol)、mei(1.16g,8.2mmol)和碳酸钾(1.13g,8.2mmol)于dmf(5ml)中的混合物加热3小时。使混合物冷却至室温,用水(20ml)稀释,并且用乙酸乙酯(20mlx3)萃取。将有机萃取物合并,用盐水(10mlx2)洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯=100:1至20:1)来纯化以产生甲基醚中间体(0.58g,定量产率)。将甲基醚中间体(0.58g,2.7mmol)溶解于thf/水(2ml/2ml)中,并且添加lioh.h2o(0.57g,13.5mmol)。在室温下将反应搅拌1小时。将反应体系的ph调整至4-5,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩以产生粗制3-氟-5-甲酰基-4-甲氧基苯甲酸(0.5g,94%产率),其不经进一步纯化即用于下一反应。
[0956]
步骤2:3-氟-5-甲酰基-4-甲氧基-n-(4-(三氟甲基)苯基)苯甲酰胺
[0957]
将一滴dmf添加至3-氟-5-甲酰基-4-甲氧基苯甲酸(0.2g,1.0mmol)和草酰氯(0.39g,3.0mmol)于dcm(5ml)中的溶液中。在室温下将反应搅拌1小时。在真空中移除溶剂,并且将残余物与二氯甲烷共蒸发两次。接着将残余物溶解于二氯甲烷(5ml)中。添加4-三氟甲基苯胺(0.5g,3.0mmol)、dmap(0.02g,0.1mmol)和三乙胺(0.5g,5.0mmol)。将反应搅拌1小时。lc-ms显示了所需产物的形成。移除溶剂,并且将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯/二氯甲烷=20:1:1至5:1:1)来纯化以产生3-氟-5-甲酰基-4-甲氧基-n-(4-(三氟甲基)苯基)苯甲酰胺(130mg,38%产率),内部含有在同一斑点处的4-三氟甲基苯胺。lc-ms m/z[m+h]
+
,c
16h11
f4no3的计算值:342;实测值:342。
[0958]
步骤3:3-氟-5-甲酰基-4-羟基-n-(4-(三氟甲基)苯基)苯甲酰胺
[0959]
在-78℃下将bbr3(191mg,0.76mmol)添加至3-氟-5-甲酰基-4-甲氧基-n-(4-(三氟甲基)苯基)苯甲酰胺(130mg,0.38mmol)于二氯甲烷(5ml)中的溶液中。在室温下将反应搅拌30分钟。将溶液用二氯甲烷稀释,并且用饱和碳酸氢钠洗涤。分离有机层,经无水硫酸钠干燥,并且浓缩。在真空中移除残余物,并且将残余物与二氯甲烷共蒸发两次。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯/二氯甲烷=20:1:1至5:1:1)来纯化以产生3-氟-5-甲酰基-4-羟基-n-(4-(三氟甲基)苯基)苯甲酰胺(50mg,40%产率)。1h nmr(dmso-d6,400mhz)δ:11.77(br,1h),10.62(s,1h),10.36(s,1h),8.22(s,1h),8.13(dd,j=12.0hz,2.0hz,1h),8.00(d,j=8.8hz,2h),7.74(d,j=8.4hz,2h);lc-ms m/z[m+h]
+
,c
15
h9f4no3的计算值:328;实测值:328。
[0960]
实施例b14:n-(3-氯-4-(三氟甲基)苯基)-3-氟-5-甲酰基-4-羟基苯甲酰胺(化合物编号b14)
[0961][0962]
以如对于实施例b13中的3-氟-5-甲酰基-4-羟基-n-(4-(三氟甲基)苯基)苯甲酰胺所述的类似方式合成标题产物。步骤3的产率:22%,棕色固体。1h nmr(dmso-d6,400mhz)δ:11.84(br,1h),10.74(s,1h),10.37(s,1h),8.20(m,2h),8.11(dd,j=11.6hz,2.0hz,1h),7.92(m,2h);lc-ms m/z[m+h]
+
,c
15
h8clf4no3的计算值:362;实测值:362。
[0963]
实施例b15:3-氟-5-甲酰基-4-羟基-n-(4-(吡咯烷-1-基)苯基)苯磺酰胺(化合物b17)
[0964][0965]
步骤1:3-氟-5-甲酰基-4-羟基苯-1-磺酰氯
[0966]
在0℃下将氯磺酸(1.66g,14.3mmol,10当量)逐滴添加至3-氟-2-羟基苯甲醛(200mg,1.4mmol,1.0当量)于二氯甲烷(10ml)中的溶液中。在室温下将反应搅拌过夜。将反应混合物倾倒至冰水(30ml)中,并且用二氯甲烷萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩以产生粗制3-氟-5-甲酰基-4-羟基苯-1-磺酰氯(390mg,定量产率),其不经进一步纯化即用于下一反应中。lc-ms m/z[m-hcl]-,c7h4clfo4s的计算值:219;实测值:219。
[0967]
步骤2:将3-氟-5-甲酰基-4-羟基苯-1-磺酰氯(390mg,1.64mmol,1.0当量)、4-(吡咯烷-1-基)苯胺(664mg,4.10mmol,2.5当量)和n-甲基吗啉(497mg,4.92mmol,3.0当量)于二氯甲烷(10ml)中的溶液搅拌5小时。将反应混合物倾倒至4n hcl中。将反应搅拌3小时,接着用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将
残余物通过硅胶柱色谱法和制备型tlc来纯化以产生呈黄色固体状的3-氟-5-甲酰基-4-羟基-n-(4-(吡咯烷-1-基)苯基)苯磺酰胺(23mg,0.06mmol,4%产率)。1h nmr(dmso-d6,400mhz)δ:12.03(br,1h),10.26(br,1h),9.57(s,1h),7.75(s,1h),7.62(dd,j=10.4hz,2.4hz,1h),6.82(d,j=8.8hz,2h),6.38(d,j=8.0hz,2h),3.13(m,4h),1.90(m,4h)。lc-ms m/z[m+h]
+
,c
17h17
fn2o4s的计算值:365;实测值:365。
[0968]
实施例b16:3-氟-5-甲酰基-4-羟基-n-(2-(吡咯烷-1-基)嘧啶-5-基)苯甲酰胺(化合物b59)
[0969][0970]
步骤1:5-硝基-2-(吡咯烷-1-基)嘧啶
[0971]
在室温下将2-氯-5-硝基嘧啶(2g,12.6mmol,1.0当量)、吡咯烷(1.3g,18.9mmol,1.5当量)和碳酸钾(3.5g,25.2mmol,2.0当量)于dmf(10ml)中的混合物搅拌5小时。将混合物倾倒至水(100ml)中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩以产生5-硝基-2-(吡咯烷-1-基)嘧啶(2.3g,94%产率),其不经进一步纯化即用于下一反应。lc-ms m/z[m+h]
+
,c8h
10
n4o2的计算值:195;实测值:195。
[0972]
步骤2:2-(吡咯烷-1-基)嘧啶-5-胺
[0973]
将5-硝基-2-(吡咯烷-1-基)嘧啶(2.3g,11.9mmol,1.0当量)和pd/c(0.2g)于甲醇(10ml中的混合物氢化2小时。滤除pd/c,并且用甲醇洗涤。将滤液和洗涤液合并,并且浓缩以产生2-(吡咯烷-1-基)嘧啶-5-胺(1.63g,84%产率),其不经进一步纯化即用于下一反应。lc-ms m/z[m+h]
+
,c8h
12
n4的计算值:165;实测值:165。
[0974]
步骤3:将hatu(0.71g,1.87mmol,1.5当量)和n-甲基吗啉(0.4g,3.74mmol,3.0当量)添加至3-氟-5-甲酰基-4-羟基苯甲酸(0.23g,1.25mmol,1.0当量)和2-(吡咯烷-1-基)嘧啶-5-胺(0.5g,3.05mmol,2.5当量)于二氯甲烷(30ml)中的混合物中。在30℃下将混合物搅拌过夜。移除溶剂,并且将残余物溶解于二噁烷(6ml)和4n hcl(6ml)的混合物中。在55℃下将混合物搅拌2小时。将混合物用水(20ml)稀释,并且用乙酸乙酯(30ml)洗涤。丢弃洗涤液。将水相用碳酸氢钠中和,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水(20ml)洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/丙酮=20:1至5:1)来纯化以产生呈浅黄色固体状的3-氟-5-甲酰基-4-羟基-n-(2-(吡咯烷-1-基)嘧啶-5-基)苯甲酰胺(15mg,0.05mmol,4%产率)。1h nmr(dmso-d6,400mhz)δ:11.70(br,1h),10.35(s,1h),10.22(br,1h),8.59(s,2h),8.20(s,1h),8.07(dd,j=11.6hz,2.0hz,1h),3.48(m,4h),1.94(m,4h)。lc-ms m/z[m+h]
+
,c
16h15
fn4o3的计算值:331;实测值:331。
[0975]
实施例b17:3-氟-5-甲酰基-4-羟基-n-(6-(吡咯烷-1-基)吡啶-3-基)苯甲酰胺(化合物b61)
m/z[m-h]-,c
19h19
fo4s2的计算值:393;实测值:393。
[0993]
步骤2:1-(3-(1,3-二硫杂环己烷-2-基)-5-氟-4-(4-甲氧基苯甲基氧基)苯基)-3-(4-氟苯基)脲
[0994]
在室温下将3-(1,3-二硫杂环己烷-2-基)-5-氟-4-(4-甲氧基苯甲基氧基)苯甲酸(0.3g,0.76mmol,1.0当量)、dppa(251mg,0.91mmol,1.2当量)和tea(231mg,2.28mmol,3.0当量)于二噁烷(10ml)中的溶液搅拌30分钟,并且添加4-氟苯胺(169mg,1.52mmol,2.0当量)。接着在90℃下将反应加热过夜。使反应混合物冷却至室温,倾倒至水中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/etoac=20:1至3:1)来纯化以产生1-(3-(1,3-二硫杂环己烷-2-基)-5-氟-4-(4-甲氧基苯甲基氧基)苯基)-3-(4-氟苯基)脲(240mg,63%产率)。lc-ms m/z[m+h]
+
,c
25h24
f2n2o3s2的计算值:503;实测值:503。
[0995]
步骤3:将mei(6.5g,45.8mmol,100当量)添加至1-(3-(1,3-二硫杂环己烷-2-基)-5-氟-4-(4-甲氧基苯甲基氧基)苯基)-3-(4-氟苯基)脲(230mg,0.46mmol,1.0当量)和nahco3(770mg,9.17mmol,20.0当量)于乙腈/水(30ml/6ml)中的混合物中。在40℃下将反应加热6小时。使反应混合物冷却至室温,倾倒至水中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物于二氯甲烷(3ml)中搅拌,并且收集固体以产生中间体(约100mg)。将中间体(约100mg)溶解于二噁烷(2ml)中,并且添加6n hcl/二噁烷(3ml)。在室温下将反应搅拌1小时。将溶液倾倒至冰冷的饱和nahco3中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将固体于二氯甲烷(3ml)中搅拌10分钟并过滤。收集滤饼,并且干燥以产生呈灰白色固体状的1-(3-氟-5-甲酰基-4-羟基苯基)-3-(4-氟苯基)脲(45mg,0.15mmol,34%产率)。1h nmr(dmso-d6,400mhz)δ:10.51(br,1h),10.27(s,1h),8.77(d,j=14.4hz,2h),8.69(dd,j=12.8hz,2.4hz,1h),7.45(m,3h),7.12(m,2h)。lc-ms m/z[m+h]
+
,c
14h10
f2n2o3的计算值:293;实测值:293。
[0996]
实施例b20:1-(3-氟-5-甲酰基-4-羟基苯基)-3-(4-(吡咯烷-1-基)苯基)脲(化合物b65)
[0997][0998]
将4-(吡咯烷-1-基)苯胺(176mg,1.09mmol,1.0当量)添加至3-氟-5-甲酰基-4-羟基苯甲酸(200mg,1.09mmol,1.0当量)于二噁烷(5ml)中的溶液中。在室温下将反应搅拌10分钟。将所得混合物浓缩,并且将残余物于二氯甲烷(20ml)中搅拌10分钟,接着过滤。将滤饼干燥,并且再悬浮于二噁烷(30ml)中。添加dppa(448mg,1.63mmol,1.5当量)和tea(329mg,3.26mmol,3.0当量)。在室温下将反应搅拌30分钟。接着添加4-(吡咯烷-1-基)苯胺(176mg,1.09mmol,1.0当量),并且在90℃下将反应加热3小时。使混合物冷却至室温,并且倾倒至4n hcl/水(50ml)中。在室温下搅拌1小时之后,将混合物用乙酸乙酯萃取三次,并且用二氯甲烷萃取4次。将有机萃取物合并,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶
柱色谱法(石油醚/etoac=20:1至3:1)和制备型tlc来纯化以产生呈绿色固体状的1-(3-氟-5-甲酰基-4-羟基苯基)-3-(4-(吡咯烷-1-基)苯基)脲(25mg,0.07mmol,7%产率)。1h nmr(dmso-d6,400mhz)δ:10.45(br,1h),10.27(s,1h),8.63(br,1h),8.57(br,1h),7.71(dd,j=13.2hz,2.4hz,1h),7.46(s,1h),7.31(m,2h),6.74(m,2h),3.93(m,4h),1.99(m,4h)。lc-ms m/z[m+h]
+
,c
18h18
fn3o3的计算值:344;实测值:344。
[0999]
实施例b21:3-氟-5-甲酰基-4-羟基-n-(4-(哌啶-1-基)苯基)苯甲酰胺(新化合物b66)
[1000][1001]
在50ml玻璃小瓶中,在室温下将3-氟-5-甲酰基-4-羟基苯甲酸(200mg,1.09mmol,1.0当量)、4-(哌啶-1-基)苯胺(478mg,2.73mmol,2.5当量)、hatu(619mg,1.63mmol,1.5当量)和n-甲基吗啉(329mg,3.26mmol,3.0当量)于thf(10ml)中的溶液搅拌过夜。将反应混合物倾倒至4n hcl中。将反应搅拌30分钟,接着用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法和制备型tlc来纯化以产生呈黄色固体状的3-氟-5-甲酰基-4-羟基-n-(4-(哌啶-1-基)苯基)苯甲酰胺(23mg,0.04mmol,4%产率)。1h nmr(cdcl3,400mhz)δ:11.30(br,1h),10.02(s,1h),8.03(s,1h),7.89(d,j=10.0hz,1h),7.74(br,1h),7.51(m,2h),7.02(m,2h),3.16(m,4h),1.76(m,6h)。lc-ms m/z[m+h]
+
,c
19h19
fn2o3的计算值:343;实测值:343。
[1002]
实施例b22:n-(4-(3,3-二氟吡咯烷-1-基)苯基)-3-氟-5-甲酰基-4-羟基苯甲酰胺(化合物b67)
[1003][1004]
步骤1:3,3-二氟吡咯烷盐酸盐
[1005]
将dast(4.03g,67.6mmol,2.5当量)添加至3-氧代吡咯烷-1-甲酸叔丁酯(5g,27.0mmol,1.0当量)于二氯甲烷(30ml)中的溶液中。在室温下将反应搅拌5小时。将反应混
合物倾倒至冰冷的饱和nahco3溶液(100ml)中,并且用二氯甲烷萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩以产生粗制boc-3,3-二氟吡咯烷(5.9g,定量产率),接着将其用6n hcl二噁烷溶液处理以产生3,3-二氟吡咯烷盐酸盐(4.1g,定量产率)。lc-ms m/z[m+h]
+
,c4h8clf2n的计算值:110;实测值:110。
[1006]
步骤2:3,3-二氟-1-(4-硝基苯基)吡咯烷
[1007]
在95℃下将3,3-二氟吡咯烷盐酸盐(1.43g,1.0mmol,1.0当量)、1-溴-4-硝基苯(2.01g,1.0mmol,1当量)、binap(0.94g,0.15mmol,0.15当量)、cs2co3(8.15g,2.5mmol,2.5当量)和pd(oac)2(0.23g,0.1mmol,0.1当量)于甲苯(20ml)中的混合物加热过夜。使反应混合物冷却至室温,倾倒至水(100ml)中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法来纯化以产生3,3-二氟-1-(4-硝基苯基)吡咯烷(1.5g,66%产率)。lc-ms m/z[m+h]
+
,c
10h10
f2n2o2的计算值:229;实测值:229。
[1008]
步骤3:4-(3,3-二氟吡咯烷-1-基)苯胺
[1009]
将铁粉(3.7g,66.1mmol,10.0当量)添加至3,3-二氟-1-(4-硝基苯基)吡咯烷(1.5g,6.6mmol,1.0当量)于acoh(30ml)中的溶液中。在60℃下将反应加热2小时。使反应混合物冷却至室温,倾倒至饱和nahco3中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩以产生粗制4-(3,3-二氟吡咯烷-1-基)苯胺(1.1g,84%产率),其不经进一步纯化即用于下一反应。lc-ms m/z[m+h]
+
,c
10h12
f2n2的计算值:199;实测值:199。
[1010]
步骤4:在室温下将3-氟-5-甲酰基-4-羟基苯甲酸(200mg,1.09mmol,1.0当量)、4-(3,3-二氟吡咯烷-1-基)苯胺(430mg,2.17mmol,2.0当量)、hatu(619mg,1.63mmol,1.5当量)和n-甲基吗啉(329mg,3.26mmol,3.0当量)于thf(10ml)中的溶液搅拌过夜。将反应混合物倾倒至4n hcl中。将反应搅拌30分钟,接着用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法和制备型tlc来纯化以产生呈黄色固体状的n-(4-(3,3-二氟吡咯烷-1-基)苯基)-3-氟-5-甲酰基-4-羟基苯甲酰胺(50mg,0.13mmol,12%产率)。1h nmr(dmso-d6,400mhz)δ:11.61(br,1h),10.35(s,1h),10.10(br,1h),8.18(s,1h),8.09(dd,j=12.0hz,2.0hz,1h),7.59(d,j=8.8hz,2h),6.63(d,j=9.2hz,2h),3.68(t,j=9.6hz,2h),3.43(m,4h)。lc-ms m/z[m+h]
+
,c
18h15
f3n2o3的计算值:365;实测值:365。
[1011]
实施例b23:n-(4-(4,4-二氟哌啶-1-基)苯基)-3-氟-5-甲酰基-4-羟基苯甲酰胺(新化合物b68)
[1012][1013]
在室温下将3-氟-5-甲酰基-4-羟基苯甲酸(200mg,1.09mmol,1.0当量)、4-(4,4-二氟哌啶-1-基)苯胺(460mg,2.17mmol,2.0当量)(如实施例b22中所制备)、hatu(619mg,1.63mmol,1.5当量)和n-甲基吗啉(329mg,3.26mmol,3.0当量)于thf(10ml)中的溶液搅拌过夜。将反应混合物倾倒至4n hcl中。将反应搅拌30分钟,接着用乙酸乙酯萃取三次。将有
机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法和制备型tlc来纯化以产生呈黄色固体状的n-(4-(4,4-二氟哌啶-1-基)苯基)-3-氟-5-甲酰基-4-羟基苯甲酰胺(13mg,0.03mmol,3%产率)。1h nmr(dmso-d6,400mhz)δ:11.63(br,1h),10.35(s,1h),10.15(br,1h),8.18(s,1h),8.09(d,j=11.6hz,1h),7.61(d,j=8.8hz,2h),7.01(d,j=8.8hz,2h),3.29(m,4h),2.05(m,4h)。lc-ms m/z[m+h]
+
,c
19h17
f3n2o3的计算值:379;实测值:379。
[1014]
实施例b24:n-(4-(4-环丙基哌嗪-1-基)苯基)-3-氟-5-甲酰基-4-羟基苯甲酰胺(化合物b69)
[1015][1016]
在室温下将3-氟-5-甲酰基-4-羟基苯甲酸(200mg,1.09mmol,1.0当量)、4-(4-环丙基哌嗪-1-基)苯胺(590mg,2.73mmol,2.5当量)(如实施例b22中所制备)、hatu(619mg,1.63mmol,1.5当量)和n-甲基吗啉(329mg,3.26mmol,3.0当量)于thf(10ml)中的溶液搅拌过夜。将反应混合物倾倒至4n hcl中。将反应搅拌30分钟,接着用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法和制备型tlc来纯化以产生呈浅黄色固体状的n-(4-(4-环丙基哌嗪-1-基)苯基)-3-氟-5-甲酰基-4-羟基苯甲酰胺(25mg,0.03mmol,6%产率)。1h nmr(dmso-d6,400mhz)δ:11.65(br,1h),10.36(s,1h),10.21(s,1h),8.19(s,1h),8.10(dd,j=11.6hz,2.0hz,1h),7.65(d,j=9.2hz,2h),7.01(d,j=8.8hz,2h),3.77(m,2h),3.54(m,2h),3.36(m,2h),3.06(m,2h),2.93(m,1h),1.10(m,2h),0.82(m,2h)。lc-ms m/z[m+h]
+
,c
21h22
fn3o3的计算值:384;实测值:384。
[1017]
实施例b25:n-(4-(4-环丙基-1,4-二氮杂环庚烷-1-基)苯基)-3-氟-5-甲酰基-4-羟基苯甲酰胺(新化合物b70)
[1018][1019]
步骤1:1-环丙基-4-(4-硝基苯基)-1,4-二氮杂环庚烷
[1020]
在100ml玻璃小瓶中,在50℃下将1-氟-4-硝基苯(1.1g,7.80mmol,1.1当量)、1-环丙基-1,4-二氮杂环庚烷(1g,7.14mmol,1.0当量)和k2co3(4.9g,35.5mmol,5.0当量)于dmf(20ml)中的混合物加热7小时。将混合物倾倒至水中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(纯dcm)来纯化以产生呈黄色油状的1-环丙基-4-(4-硝基苯基)-1,4-二氮杂环庚烷(1.57g,
6.01mmol,84%产率)。lc-ms m/z[m+h]
+
,c
14h19
n3o2的计算值:262;实测值:262。
[1021]
步骤2:4-(4-环丙基-1,4-二氮杂环庚烷-1-基)苯胺
[1022]
在100ml玻璃小瓶中,将铁粉(794mg,14.18mmol,10当量)添加至1-环丙基-4-(4-硝基苯基)-1,4-二氮杂环庚烷(370mg,1.42mmol,1.0当量)于acoh(10ml)中的溶液中。在60℃下将反应加热2小时。使反应混合物冷却至室温,倾倒至饱和nahco3中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩以产生4-(4-环丙基-1,4-二氮杂环庚烷-1-基)苯胺(290mg,1.26mmol,88%产率)。lc-ms m/z[m+h]
+
,c
14h21
n3的计算值:232;实测值:232。
[1023]
步骤3a:3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸
[1024]
在100ml玻璃小瓶中,在90℃下将3-氟-5-甲酰基-4-羟基苯甲酸(2g,10.9mmol,1.0当量)、2,2-二甲基丙烷-1,3-二醇(2.26g,21.8mmol,2.0当量)和p-tsoh.h2o(414mg,2.18mmol,0.2当量)于甲苯(30ml)中的溶液加热3小时。在真空中移除溶剂,并且将残余物溶解于水/etoac中。接着将混合物用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩以产生粗制3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(2.97g,定量产率)。lc-ms m/z[m+h]
+
,c
13h15
fo5的计算值:271;实测值:271。
[1025]
步骤3:在100ml玻璃小瓶中,在室温下将3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(193mg,0.71mmol,1.0当量)、4-(4-环丙基-1,4-二氮杂环庚烷-1-基)苯胺(180mg,0.79mmol,1.1当量)、hatu(324mg,0.85mmol,1.2当量)和nmm(215mg,2.13mmol,3.0当量)于thf(10ml)中的溶液搅拌4小时。将溶液倾倒至饱和nahco3中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(ch2cl2/meoh=300:1至150:1)和制备型tlc来纯化以产生中间体(40mg,0.08mmol,12%产率)。将中间体(30mg,0.06mmol,1.0当量)溶解于thf/4n hcl(2ml/4ml)中,并且在室温下将反应搅拌30分钟。将体系的ph调整至7-7.5,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过制备型tlc来纯化以产生呈黄色固体状的n-(4-(4-环丙基-1,4-二氮杂环庚烷-1-基)苯基)-3-氟-5-甲酰基-4-羟基苯甲酰胺(7mg,0.02mmol,29%产率)。1h nmr(dmso-d6,400mhz)δ:10.32(s,1h),9.96(s,1h),8.14(s,1h),8.00(d,j=12.0hz,1h),7.50(d,j=8.8hz,2h),6.68(d,j=9.2hz,2h),3.49(m,4h),2.92(m,2h),2.75(m,2h),2.01(m,1h),1.89(m,2h),0.47(m,2h),0.38(m,2h)。lc-ms m/z[m+h]
+
,c
22h24
fn3o3的计算值:398;实测值:398。
[1026]
实施例b26:3-氟-5-甲酰基-4-羟基-n-(3-(吡咯烷-1-基)苯基)苯甲酰胺(化合物b71)
[1027][1028]
在100ml玻璃小瓶中,在室温下将3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(300mg,1.11mmol,1.0当量)、3-(吡咯烷-1-基)苯胺(180mg,1.11mmol,
1.0当量)、hatu(633mg,1.67mmol,1.5当量)和nmm(336mg,3.33mmol,3.0当量)于thf(10ml)中的溶液搅拌过夜。将溶液倾倒至饱和nahco3中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/etoac=20:1至5:1)来纯化以产生中间体(110mg,0.27mmol,24%产率)。将中间体(100mg,0.24mmol,1.0当量)溶解于thf/4n hcl(2ml/4ml)中,并且在室温下将反应搅拌30分钟。将混合物用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/etoac=10:1至5:1)来纯化以产生呈黄色固体状的3-氟-5-甲酰基-4-羟基-n-(3-(吡咯烷-1-基)苯基)苯甲酰胺(65mg,0.20mmol,83%产率)。1h nmr(dmso-d6,400mhz)δ:11.62(br,1h),10.35(s,1h),10.07(s,1h),8.19(s,1h),8.10(dd,j=11.6hz,1.6hz,1h),7.08(m,2h),7.00(d,j=2.0hz,1h),6.29(m,1h),3.22(m,4h),1.97(m,4h)。lc-ms m/z[m+h]
+
,c
18h17
fn2o3的计算值:329;实测值:329。
[1029]
实施例b27:3-氟-5-甲酰基-4-羟基-n-(3-(哌啶-1-基)苯基)苯甲酰胺(化合物b72)
[1030][1031]
使用与如实施例b25中所述的方法类似的方法从3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(250mg,0.93mmol,1当量)和3-(哌啶-1-基)苯胺(163mg,0.93mmol,1当量)制备标题化合物以产生呈淡黄色固体状的标题化合物3-氟-5-甲酰基-4-羟基-n-(3-(哌啶-1-基)苯基)苯甲酰胺(7mg,0.02mmol,11%产率)。1h nmr(dmso-d6,400mhz)δ:11.66(br,1h),10.35(s,1h),10.11(s,1h),8.19(s,1h),8.10(dd,j=11.6hz,2.0hz,1h),7.36(m,1h),7.22(m,1h),7.15(m,1h),6.69(m,1h),3.14(m,4h),1.62(m,4h),1.55(m,2h)。lc-ms m/z[m+h]
+
,c
19h19
fn2o3的计算值:343;实测值:343。
[1032]
实施例b28:n-(4-(3,3-二甲基吡咯烷-1-基)苯基)-3-氟-5-甲酰基-4-羟基苯甲酰胺(化合物b73)
[1033][1034]
使用与如实施例b25中所述的方法类似的方法从3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(270mg,1.0mmol,1.0当量)和4-(3,3-二甲基吡咯烷-1-基)苯胺(190mg,1mmol,1.0当量)(如实施例b25中所制备)制备标题化合物以产生呈黄色固体状的标题化合物(130mg,0.37mmol,74%产率)。1h nmr(dmso-d6,400mhz)δ:11.60(br,1h),10.34(s,1h),9.99(s,1h),8.16(d,j=1.2hz,1h),8.06(dd,j=11.6hz,2.0hz,1h),7.50(d,j=8.8hz,2h),6.47(d,j=9.2hz,2h),3.35-3.28(m,2h),3.00(s,2h),1.75(t,j=10.8hz,2h),1.11(s,6h)。lc-ms m/z[m+h]
+
,c
20h21
fn2o3的计算值:357;实测值:357。
[1035]
实施例b29:n-(4-(3-氮杂双环[3.1.0]己烷-3-基)苯基)-3-氟-5-甲酰基-4-羟基苯甲酰胺(化合物b74)
[1036][1037]
使用与如实施例b25中所述的方法类似的方法从3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(310mg,1.15mmol,1.0当量)和4-(3-氮杂双环[3.1.0]己烷-3-基)苯胺(200mg,1.15mmol,1.0当量)(如实施例b25中所制备)制备标题化合物以产生标题化合物(60mg,0.18mmol,39%产率)。1h nmr(dmso-d6,400mhz)δ:11.62(br,1h),10.34(s,1h),10.01(s,1h),8.16(d,j=1.6hz,1h),8.06(dd,j=12.0hz,2.0hz,1h),7.50(d,j=8.8hz,2h),6.53(d,j=9.2hz,2h),3.48(d,j=9.2hz,2h),3.12(m,2h),1.67(m,2h),0.70(m,1h),0.27(m,1h)。lc-ms m/z[m+h]
+
,c
19h17
fn2o3的计算值:341;实测值:341。
[1038]
实施例b30:3-氟-5-甲酰基-4-羟基-n-(4-((3ar,6as)-四氢-1h-呋喃并[3,4-c]吡咯-5(3h)-基)苯基)苯甲酰胺(化合物b75)
[1039][1040]
使用与如实施例b25中所述的方法类似的方法从3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(270mg,1.0mmol,1.0当量)和4-((3ar,6as)-二氢-1h-呋喃并[3,4-c]吡咯-5(3h,6h,6ah)-基)苯胺(204mg,1.0mmol,1.0当量)(如实施例b25中所制备)制备标题化合物以产生标题化合物(60mg,0.16mmol,36%产率)。1h nmr(dmso-d6,400mhz)δ:11.59(br,1h),10.34(s,1h),10.06(s,1h),8.17(s,1h),8.08(dd,j=12.0hz,2.0hz,1h),7.54(d,j=8.8hz,2h),6.63(d,j=8.8hz,2h),3.85(m,2h),3.54(m,2h),3.31(m,2h),3.15(m,2h),2.98(m,2h)。lc-ms m/z[m+h]
+
,c
20h19
fn2o4的计算值:371;实测值:371。
[1041]
实施例b31:3-氟-5-甲酰基-n-(4-((3ar,6as)-六氢环戊二烯并[c]吡咯-2(1h)-基)苯基)-4-羟基苯甲酰胺(化合物b76)
[1042][1043]
使用与如实施例b25中所述的方法类似的方法从3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(270mg,1.0mmol,1.0当量)和4-((3ar,6as)-六氢环戊二烯并[c]吡咯-2(1h)-基)苯胺(202mg,1.0mmol,1.0当量)(如实施例b25中所制备)制备标题化合物以产生标题化合物(220mg,0.60mmol,62%产率)。1h nmr(dmso-d6,400mhz)δ:11.60(br,1h),10.34(s,1h),10.04(s,1h),8.17(d,j=1.6hz,1h),8.08(dd,j=12.0hz,2.0hz,1h),7.52(d,j=9.2hz,2h),6.60(d,j=9.2hz,2h),3.36(m,2h),2.94(m,2h),2.74(m,2h),
1.79(m,2h),1.54(m,1h),1.49(m,1h),1.45(m,2h)。lc-ms m/z[m+h]
+
,c
21h21
fn2o3的计算值:369;实测值:369。
[1044]
实施例b32:n-(4-(2-氮杂螺[3.3]庚烷-2-基)苯基)-3-氟-5-甲酰基-4-羟基苯甲酰胺(化合物b77)
[1045][1046]
使用与如实施例b25中所述的方法类似的方法从3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(270mg,1.0mmol,1.0当量)和4-(2-氮杂螺[3.3]庚烷-2-基)苯胺(188mg,1mmol,1.0当量)(参考:如zhang,hui等人,pct国际申请2013013504,2013年1月31日中制备的2-氮杂螺[3.3]庚烷盐酸盐)(如实施例b25中所制备)制备标题化合物以产生呈黄色固体状的标题化合物(140mg,0.40mmol,53%产率)。1h nmr(dmso-d6,400mhz)δ:11.60(br,1h),10.34(s,1h),10.05(s,1h),8.16(d,j=1.6hz,1h),8.07(dd,j=11.6hz,2.0hz,1h),7.51(d,j=8.8hz,2h),6.39(d,j=8.8hz,2h),3.74(s,4h),2.16(t,j=5.0hz,4h),1.84-1.80(m,2h)。lc-ms m/z[m+h]
+
,c
20h19
fn2o3的计算值:355;实测值:355。
[1047]
实施例b33:3-氟-5-甲酰基-4-羟基-n-(4-(6-氧代-5-氮杂螺[2.4]庚烷-5-基)苯基)苯甲酰胺(化合物b78)
[1048][1049]
使用与如实施例b25中所述的方法类似的方法从3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(281mg,1.04mmol,1.0当量)和5-(4-氨基苯基)-5-氮杂螺[2.4]庚烷-6-酮(210mg,1.04mmol,1.0当量)(如实施例b22中所制备)制备标题化合物以产生呈白色固体状的标题化合物(100mg,0.27mmol,49%产率)。1h nmr(dmso-d6,400mhz)δ:11.68(br,1h),10.36(s,1h),10.33(s,1h),8.20(s,1h),8.11(dd,j=11.6hz,2.0hz,1h),7.75(d,j=8.8hz,2h),7.62(d,j=9.2hz,2h),3.75(s,2h),2.56(s,2h),0.70(s,4h)。lc-ms m/z[m+h]
+
,c
20h17
fn2o4的计算值:369;实测值:369。
[1050]
实施例b34:n-(4-(5-氮杂螺[2.4]庚烷-5-基)苯基)-3-氟-5-甲酰基-4-羟基苯甲酰胺(化合物b79)
[1051]
[1052]
步骤1:4-(5-氮杂螺[2.4]庚烷-5-基)苯胺
[1053]
将5-(4-硝基苯基)-5-氮杂螺[2.4]庚烷-6-酮(300mg,1.29mmol,1.0当量)溶解于thf(10ml)中,并且使溶液冷却至0℃。添加硼烷-二甲基硫醚(0.26ml,10m,于dms中,2.58mmol,2.0当量)。在50℃下将反应搅拌1小时。使体系冷却至室温,倾倒至冰水中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩以产生粗制5-(4-硝基苯基)-5-氮杂螺[2.4]庚烷(305mg,定量产率)。在100ml玻璃小瓶中,将铁粉(770mg,13.75mmol,10当量)添加至5-(4-硝基苯基)-5-氮杂螺[2.4]庚烷(305mg,1.29mmol,1.0当量)于acoh(20ml)中的溶液中。在60℃下将反应加热2小时。使反应混合物冷却至室温,倾倒至饱和nahco3中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩以产生粗制4-(5-氮杂螺[2.4]庚烷-5-基)苯胺(180mg,0.96mmol,74%产率),其不经进一步纯化即用于下一反应。
[1054]
步骤2:使用与如实施例b25中所述的方法类似的方法从3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(284mg,1.05mmol,1.0当量)和4-(5-氮杂螺[2.4]庚烷-5-基)苯胺(180mg,0.96mmol,1当量)制备标题化合物以产生呈黄色固体状的标题化合物(70mg,0.20mmol,44%产率)。1h nmr(dmso-d6,400mhz)δ:10.34(br,1h),10.00(br,1h),8.16(s,1h),8.06(d,j=11.6hz,1h),7.53(d,j=8.8hz,2h),6.49(d,j=8.8hz,2h),3.36(m,2h),3.15(s,2h),1.91(t,j=6.4hz,2h),0.62(d,j=8.0hz,4h)。lc-ms m/z[m+h]
+
,c
20h19
fn2o3的计算值:355;实测值:355。
[1055]
实施例b35:n-环丙基-4-((3-氟-5-甲酰基-4-羟基苯基)乙炔基)苯甲酰胺(化合物b80)
[1056][1057]
步骤1:4-(碘乙炔基)苯甲酸甲酯
[1058]
在100ml玻璃小瓶中,将phi(oac)2(3.66g,11.4mmol,1.0当量)添加至4-乙炔基苯甲酸甲酯(1.82g,11.4mmol,1.0当量)和tbai(5.04g,13.7mmol,1.2当量)于乙腈(20ml)中的溶液中。在室温下将反应搅拌5小时。将混合物倾倒至水(50ml)中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩以产生呈黄色固体状的粗制4-(碘乙炔基)苯甲酸甲酯(3.64g,定量产率),其不经进一步纯化即用于下一反应。
[1059]
步骤2:n-环丙基-4-(碘乙炔基)苯甲酰胺
[1060]
在50ml玻璃小瓶中,将lioh.h2o(1.34g,28.4mmol,2.5当量)添加至4-(碘乙炔基)苯甲酸甲酯(粗物质,3.64g,11.4mmol,1.0当量)于水/thf(10ml/10ml)中的溶液中。在室温下将反应搅拌2小时。将溶液用水稀释,并且用石油醚萃取两次。丢弃石油醚层。接着将水相的ph用5%khso4调整至3-4,然后将混合物用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩以产生呈白色固体状的酸(2.36g,76%产率)。在50ml
基)苯胺(350mg,1.56mmol,1.0当量)(如实施例b25中所制备)制备标题化合物以产生标题化合物(130mg,0.33mmol,51%产率)。1h nmr(dmso-d6,400mhz)δ:11.66(br,1h),10.35(s,1h),10.10(s,1h),8.17(s,1h),8.07(dd,j=11.6hz,1.6hz,1h),7.61(d,j=8.8hz,2h),7.23-7.16(m,4h),7.01(d,j=8.8hz,2h),4.36(s,2h),3.51(t,j=5.6hz,2h),2.91(d,j=5.6hz,2h)。lc-ms m/z[m+h]
+
,c
23h19
fn2o3的计算值:391;实测值:391。
[1068]
实施例b38:3-氟-5-甲酰基-4-羟基-n-(4-(4-苯基哌嗪-1-基)苯基)苯甲酰胺(化合物b83)
[1069][1070]
使用与如实施例b25中所述的方法类似的方法从3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(373mg,1.38mmol,1.0当量)和4-(4-苯基哌嗪-1-基)苯胺(350mg,1.38mmol,1.0当量)(如实施例b25中所制备)制备标题化合物以产生标题化合物(4mg,0.01mmol,2%产率)。1h nmr(dmso-d6,400mhz)δ:11.60(br,1h),10.35(br,1h),10.14(br,1h),8.19(s,1h),8.10(d,j=10.0hz,1h),7.63(m,2h),7.24(m,2h),7.02(m,2h),6.81(m,1h),3.27(m,8h)。lc-ms m/z[m+h]
+
,c
24h22
fn3o3的计算值:420;实测值:420。
[1071]
实施例b39:3-氟-5-甲酰基-4-羟基-n-(4-(4-(吡咯烷-1-基)哌啶-1-基)苯基)苯甲酰胺(化合物b84)
[1072][1073]
使用与如实施例b25中所述的方法类似的方法从3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(170mg,0.63mmol,1.0当量)和4-(4-(吡咯烷-1-基)哌啶-1-基)苯胺(140mg,0.57mmol,1.0当量)(如实施例b25中所制备)制备标题化合物以产生标题化合物(47mg,0.11mmol,48%产率)。1h nmr(dmso-d6,400mhz)δ:10.14(s,1h),9.51(s,1h),7.86(d,j=2.8hz,1h),7.55(d,j=9.2hz,2h),7.45(d,j=13.6hz,2.4hz,1h),6.88(d,j=9.2hz,2h),3.60(d,j=12.4hz,2h),2.75(m,4h),2.641(t,j=11.6hz,2h),2.54(m,1h),1.97(d,j=12.0hz,2h),1.75(m,4h),1.55(m,2h)。lc-ms m/z[m+h]
+
,c
23h26
fn3o3的计算值:412;实测值:412。
[1074]
实施例b40:3-氟-5-甲酰基-4-羟基-n-(4-(4-(吡咯烷-1-基)哌啶-1-基)苯基)苯甲酰胺(化合物b85)
[1075][1076]
使用与如实施例b25中所述的方法类似的方法从3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(283mg,1.05mmol,1.1当量)和4-(吲哚啉-1-基)苯胺
(200mg,0.95mmol,1当量)(如实施例b25中所制备)制备标题化合物以产生标题化合物(7mg,0.02mmol,7%产率)。1h nmr(dmso-d6,400mhz)δ:11.63(br,1h),10.36(s,1h),10.25(s,1h),8.20(d,j=1.6hz,1h),8.11(dd,j=12.0hz,2.0hz,1h),7.73(d,j=8.8hz,2h),7.23(dd,j=8.8hz,2.8hz,2h),7.16(d,j=7.2hz,1h),7.04(m,2h),6.71(m,1h),3.92(d,j=8.4hz,2h),3.09(d,j=8.4hz,2h)。lc-ms m/z[m+h]
+
,c
22h17
fn2o3的计算值:377;实测值:377。
[1077]
实施例b41:3-氟-5-甲酰基-4-羟基-n-(6-(异吲哚啉-2-基)吡啶-3-基)苯甲酰胺(化合物b86)
[1078][1079]
使用与如实施例b25中所述的方法类似的方法从3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(637mg,2.37mmol,1.0当量)和6-(异吲哚啉-2-基)吡啶-3-胺(500mg,2.37mmol,1.0当量)(如实施例b16中所制备)制备标题化合物以产生标题化合物(47mg,0.12mmol,15%产率)。1h nmr(dmso-d6,400mhz)δ:11.81(br,1h),10.76(br,1h),10.36(s,1h),8.65(s,1h),8.37(d,j=7.2hz,1h),8.24-8.21(m,2h),7.45(m,2h),7.39(m,2h),7.20(d,j=7.2hz,1h),4.95(s,4h)。lc-ms m/z[m+h]
+
,c
21h16
fn3o3的计算值:378;实测值:378。
[1080]
实施例b42:n-(6-(3,3-二甲基吲哚啉-1-基)吡啶-3-基)-3-氟-5-甲酰基-4-羟基苯甲酰胺(化合物b87)
[1081][1082]
使用与如实施例b25中所述的方法类似的方法从3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(475mg,1.76mmol,1.0当量)和6-(3,3-二甲基吲哚啉-1-基)吡啶-3-胺(420mg,1.76mmol,1.0当量)(如实施例b16中所制备)制备标题化合物以产生标题化合物(87mg,0.21mmol,25%产率)。1h nmr(dmso-d6,400mhz)δ:11.67(br,1h),10.36(s,1h),10.34(s,1h),8.63(d,j=2.8hz,1h),8.22(d,j=1.6hz,1h),8.18-8.04(m,3h),7.20(dd,j=7.6hz,1.2hz,1h),7.14(m,1h),6.89(m,1h),6.85(m,1h),3.78(s,2h),1.35(s,6h)。lc-ms m/z[m+h]
+
,c
23h20
fn3o3的计算值:406;实测值:406。
[1083]
实施例b43:3-氟-n-(6-(5-氟-3,3-二甲基吲哚啉-1-基)吡啶-3-基)-5-甲酰基-4-羟基苯甲酰胺(化合物b99)
[1084][1085]
步骤1:5-氟-3,3-二甲基-1-(5-硝基吡啶-2-基)吲哚啉
[1086]
在95℃下将5-氟-3,3-二甲基吲哚啉(1g,6.1mmol,1.0当量)、2-氯-5-硝基吡啶(1.44g,9.1mmol,1.5当量)、碳酸铯(4.94g,15.2mmol,2.5当量)、binap(566mg,0.91mmol,0.15当量)和pd(oac)2(136mg,0.61mmol,0.1当量)于甲苯(30ml)中的混合物加热30分钟。使混合物冷却至室温,倾倒至水中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/etoac=300:1至100:1)来纯化以产生5-氟-3,3-二甲基-1-(5-硝基吡啶-2-基)吲哚啉(910mg,52%产率),用于下一步骤中。
[1087]
步骤2:6-(5-氟-3,3-二甲基吲哚啉-1-基)吡啶-3-胺
[1088]
遵循按照实施例b25的用于获得4-(3,3-二甲基吡咯烷-1-基)苯胺的类似程序,从5-氟-3,3-二甲基-1-(5-硝基吡啶-2-基)吲哚啉(900mg,3.1mmol,1.0当量)和fe(1.76g,31.4mmol,10当量)制备6-(5-氟-3,3-二甲基吲哚啉-1-基)吡啶-3-胺(690mg,2.7mmol,87%产率)。lc-ms m/z[m+h]
+
,c
15h16
fn3的计算值:258;实测值:258。
[1089]
步骤3:3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-n-(6-(5-氟-3,3-二甲基吲哚啉-1-基)吡啶-3-基)-4-羟基苯甲酰胺
[1090]
遵循按照实施例b25的用于获得3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-n-(4-(3,3-二甲基吡咯烷-1-基)苯基)-5-氟-4-羟基苯甲酰胺的类似程序,从6-(5-氟-3,3-二甲基吲哚啉-1-基)吡啶-3-胺(600mg,2.3mmol,1.0当量)和3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(630mg,2.3mmol,1.0当量)制备3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-n-(6-(5-氟-3,3-二甲基吲哚啉-1-基)吡啶-3-基)-4-羟基苯甲酰胺(550mg,47%产率)。lc-ms m/z[m+h]
+
,c
28h29
f2n3o4的计算值:510;实测值:510。
[1091]
步骤4:遵循如实施例b25中的类似程序从3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-n-(6-(5-氟-3,3-二甲基吲哚啉-1-基)吡啶-3-基)-4-羟基苯甲酰胺(550mg,1.08mmol,1.0当量)以黄色固体形式制备3-氟-n-(6-(5-氟-3,3-二甲基吲哚啉-1-基)吡啶-3-基)-5-甲酰基-4-羟基苯甲酰胺(80mg,18%产率)。正性lc-ms:423.9(m+h)
+
,c
23h19
f2n3o3。1h nmr(dmso-d6,400mhz)δ:11.67(br,1h),10.36(br,1h),10.33(br,1h),8.62(br,1h),8.22(m,2h),8.13-8.06(m,2h),7.11(m,1h),6.95-6.89(m,2h),3.80(s,2h),1.35(s,6h)。lc-ms m/z[m+h]
+
,c
23h19
f2n3o3的计算值:424;实测值:424。
[1092]
实施例b44:n-(4-(2,3-二氢-4h-苯并[b][1,4]噁嗪-4-基)苯基)-3-氟-5-甲酰基-4-羟基苯甲酰胺(化合物b90)
[1093][1094]
步骤1:4-(4-硝基苯基)-3,4-二氢-2h-苯并[b][1,4]噁嗪
[1095]
遵循按照实施例b25的用于获得3,3-二甲基-1-(4-硝基苯基)吡咯烷的类似程序,从3,4-二氢-2h-苯并[b][1,4]噁嗪(1.35g,10.0mmol,1.0当量)和1-氟-4-硝基苯(1.7g,12.0mmol,1.1当量)制备4-(4-硝基苯基)-3,4-二氢-2h-苯并[b][1,4]噁嗪(1.43g,5.6mmol,56%产率)。未对这个化合物进行lcms。
[1096]
步骤2:4-(2h-苯并[b][1,4]噁嗪-4(3h)-基)苯胺
[1097]
遵循按照实施例b25的用于获得4-(3,3-二甲基吡咯烷-1-基)苯胺的类似程序,从4-(4-硝基苯基)-3,4-二氢-2h-苯并[b][1,4]噁嗪(1.43g,5.59mmol,1.0当量)和fe(3.13g,55.9mmol,10当量)制备4-(2h-苯并[b][1,4]噁嗪-4(3h)-基)苯胺(847mg,3.75mmol,67%产率)。lc-ms m/z[m+h]
+
,c
14h14
n2o的计算值:227;实测值:227。
[1098]
步骤3:n-(4-(2h-苯并[b][1,4]噁嗪-4(3h)-基)苯基)-3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酰胺
[1099]
遵循按照实施例b25的用于获得3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-n-(4-(3,3-二甲基吡咯烷-1-基)苯基)-5-氟-4-羟基苯甲酰胺的类似程序,从4-(2h-苯并[b][1,4]噁嗪-4(3h)-基)苯胺(420mg,1.86mmol,1当量)和3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(502mg,1.86mmol,1.0当量)制备n-(4-(2h-苯并[b][1,4]噁嗪-4(3h)-基)苯基)-3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酰胺(403mg,0.84mmol,45%产率)。lc-ms m/z[m+h]
+
,c
27h27
fn2o5的计算值:479;实测值:479。
[1100]
步骤4:遵循用于实施例b25的类似程序从n-(4-(2h-苯并[b][1,4]噁嗪-4(3h)-基)苯基)-3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酰胺(400mg,0.84mmol,1.0当量)以黄色固体形式制备n-(4-(2h-苯并[b][1,4]噁嗪-4(3h)-基)苯基)-3-氟-5-甲酰基-4-羟基苯甲酰胺(110mg,0.28mmol,33%产率)。1h nmr(dmso-d6,400mhz)δ:11.67(br,1h),10.36(s,1h),10.31(s,1h),8.20(d,j=1.6hz,1h),8.10(dd,j=11.6hz,2.8hz,1h),7.76(d,j=8.8hz,2h),7.24(d,j=8.8hz,2h),6.81-6.69(m,4h),4.25(t,j=4.0hz,2h),3.67(d,j=4.0hz,2h)。lc-ms m/z[m+h]
+
,c
22h17
fn2o4的计算值:393;实测值:393。
[1101]
实施例b45:3-氟-5-甲酰基-4-羟基-n-(4-(甲基(新戊基)氨基)苯基)苯甲酰胺(化合物b94)
[1102][1103]
步骤1:n-甲基-n-新戊基-4-硝基苯胺
[1104]
遵循按照实施例b25的用于获得3,3-二甲基-1-(4-硝基苯基)吡咯烷的类似程序,从n,2,2-三甲基丙-1-胺盐酸盐(500mg,3.64mmol,1.1当量)和1-氟-4-硝基苯(466mg,3.30mmol,1.0当量)制备n-甲基-n-新戊基-4-硝基苯胺(670mg,3.02mmol,91%产率)。未对这个化合物进行lcms。
[1105]
步骤2:n1-甲基-n1-新戊基苯-1,4-二胺
[1106]
遵循按照实施例b25的用于获得4-(3,3-二甲基吡咯烷-1-基)苯胺的类似程序,从n-甲基-n-新戊基-4-硝基苯胺(670mg,3.02mmol,1.0当量)和fe(1.69g,30.2mmol,10当量)制备n1-甲基-n1-新戊基苯-1,4-二胺(320mg,1.66mmol,55%产率)。lc-ms m/z[m+h]
+
,c
12h20
n2的计算值:193;实测值:193。
[1107]
步骤3:3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基-n-(4-(甲基(新戊基)氨基)苯基)苯甲酰胺
[1108]
遵循按照实施例b25的用于获得3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-n-(4-(3,3-二甲基吡咯烷-1-基)苯基)-5-氟-4-羟基苯甲酰胺的类似程序,从n1-甲基-n1-新戊基苯-1,4-二胺(100mg,0.52mmol,1当量)和3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(155mg,0.57mmol,1.1当量)制备3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基-n-(4-(甲基(新戊基)氨基)苯基)苯甲酰胺(170mg,0.38mmol,74%产率)。lc-ms m/z[m+h]
+
,c
25h33
fn2o4的计算值:445;实测值:445。
[1109]
步骤4:遵循用于实施例b25的类似程序从3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基-n-(4-(甲基(新戊基)氨基)苯基)苯甲酰胺(170mg,0.38mmol,1当量)以黄色固体形式制备3-氟-5-甲酰基-4-羟基-n-(4-(甲基(新戊基)氨基)苯基)苯甲酰胺(60mg,0.17mmol,44%产率)。1h nmr(cdcl3,400mhz)δ:11.26(br,1h),10.00(br,1h),7.97(s,1h),7.85(d,j=10.8hz,1h),7.56(br,1h),7.39(d,j=8.4hz,2h),6.74(br,2h),3.14(s,2h),3.00(s,3h),1.00(s,9h)。lc-ms m/z[m+h]
+
,c
20h23
fn2o3的计算值:359;实测值:359。
[1110]
实施例b46:n-(4-(7-氮杂双环[2.2.1]庚烷-7-基)苯基)-3-氟-5-甲酰基-4-羟基苯甲酰胺(化合物b95)
[1111][1112]
步骤1:(1s,4s)-7-(4-硝基苯基)-7-氮杂双环[2.2.1]庚烷
[1113]
遵循按照实施例b25的用于获得3,3-二甲基-1-(4-硝基苯基)吡咯烷的类似程序,从(1s,4s)-7-氮杂双环[2.2.1]庚烷盐酸盐(500mg,3.73mmol,1.1当量)和1-氟-4-硝基苯(480mg,3.40mmol,1.1当量)制备(1s,4s)-7-(4-硝基苯基)-7-氮杂双环[2.2.1]庚烷(710mg,3.26mmol,96%产率)。未对这个化合物进行lcms。
[1114]
步骤2:4-((1s,4s)-7-氮杂双环[2.2.1]庚烷-7-基)苯胺
[1115]
遵循按照实施例b25的用于获得4-(3,3-二甲基吡咯烷-1-基)苯胺的类似程序,从(1s,4s)-7-(4-硝基苯基)-7-氮杂双环[2.2.1]庚烷(710mg,3.26mmol,1当量)和fe(1.8g,32.6mmol,10当量)制备4-((1s,4s)-7-氮杂双环[2.2.1]庚烷-7-基)苯胺(490mg,
2.61mmol,80%产率)。lc-ms m/z[m+h]
+
,c
12h16
n2的计算值:189;实测值:189。
[1116]
步骤3:n-(4-((1s,4s)-7-氮杂双环[2.2.1]庚烷-7-基)苯基)-3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酰胺
[1117]
遵循按照实施例b25的用于获得3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-n-(4-(3,3-二甲基吡咯烷-1-基)苯基)-5-氟-4-羟基苯甲酰胺的类似程序,从4-((1s,4s)-7-氮杂双环[2.2.1]庚烷-7-基)苯胺(420mg,2.23mmol,1当量)和3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(660mg,2.44mmol,1.1当量)制备n-(4-((1s,4s)-7-氮杂双环[2.2.1]庚烷-7-基)苯基)-3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酰胺(360mg,0.82mmol,37%产率)。lc-ms m/z[m+h]
+
,c
25h29
fn2o4的计算值:441;实测值:441。
[1118]
步骤4:遵循用于实施例b25的类似程序从n-(4-((1s,4s)-7-氮杂双环[2.2.1]庚烷-7-基)苯基)-3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酰胺(160mg,0.36mmol,1当量)以淡黄色固体形式制备n-(4-((1s,4s)-7-氮杂双环[2.2.1]庚烷-7-基)苯基)-3-氟-5-甲酰基-4-羟基苯甲酰胺(75mg,0.21mmol,59%产率)。1h nmr(cdcl3,400mhz)δ:11.28(br,1h),9.98(d,j=1.2hz,1h),7.96(s,1h),7.84(d,j=10.8hz,1h),7.65(s,1h),7.41(d,j=8.4hz,2h),6.89(d,j=8.8hz,2h),4.16(t,j=2.0hz,2h),1.80(t,j=3.2hz,4h),1.44(d,j=6.8hz,4h)。lc-ms m/z[m+h]
+
,c
20h19
fn2o3的计算值:355;实测值:355。
[1119]
实施例b47:n-(4-(8-氮杂双环[3.2.1]辛烷-8-基)苯基)-3-氟-5-甲酰基-4-羟基苯甲酰胺(化合物b96)
[1120][1121]
步骤1:(1r,5s)-8-(4-硝基苯基)-8-氮杂双环[3.2.1]辛烷
[1122]
遵循按照实施例b25的用于获得3,3-二甲基-1-(4-硝基苯基)吡咯烷的类似程序,从(1r,5s)-8-氮杂双环[3.2.1]辛烷盐酸盐(500mg,3.39mmol,1.05当量)和1-氟-4-硝基苯(455mg,3.23mmol,1.0当量)制备(1r,5s)-8-(4-硝基苯基)-8-氮杂双环[3.2.1]辛烷(740mg,3.19mmol,98%产率)。未对这个化合物进行lcms。
[1123]
步骤2:4-((1r,5s)-8-氮杂双环[3.2.1]辛烷-8-基)苯胺
[1124]
遵循按照实施例b25的用于获得4-(3,3-二甲基吡咯烷-1-基)苯胺的类似程序,从(1r,5s)-8-(4-硝基苯基)-8-氮杂双环[3.2.1]辛烷(740mg,3.19mmol,1.0当量)和fe(1.8g,31.9mmol,10当量)制备4-((1r,5s)-8-氮杂双环[3.2.1]辛烷-8-基)苯胺(610mg,3.02mmol,95%产率)。未对这个化合物进行lcms。
[1125]
步骤3:n-(4-((1r,5s)-8-氮杂双环[3.2.1]辛烷-8-基)苯基)-3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酰胺
[1126]
遵循按照实施例b25的用于获得3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-n-(4-(3,3-二甲基吡咯烷-1-基)苯基)-5-氟-4-羟基苯甲酰胺的类似程序,从4-((1r,5s)-8-氮杂双环[3.2.1]辛烷-8-基)苯胺(400mg,1.98mmol,1当量)和3-(5,5-二甲基-1,3-二氧杂环
己烷-2-基)-5-氟-4-羟基苯甲酸(588mg,2.18mmol,1.1当量)制备n-(4-((1r,5s)-8-氮杂双环[3.2.1]辛烷-8-基)苯基)-3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酰胺(420mg,0.93mmol,47%产率)。lc-ms m/z[m+h]
+
,c
26h31
fn3o4的计算值:455;实测值:455。
[1127]
步骤4:遵循用于实施例b25的类似程序从n-(4-((1r,5s)-8-氮杂双环[3.2.1]辛烷-8-基)苯基)-3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酰胺(420mg,0.93mmol,1当量)以黄色固体形式制备n-(4-((1r,5s)-8-氮杂双环[3.2.1]辛烷-8-基)苯基)-3-氟-5-甲酰基-4-羟基苯甲酰胺(190mg,0.52mmol,56%产率)。正性lc-ms:369.0(m+h)
+
,c
21h21
fn2o3。1h nmr(cdcl3,400mhz)δ:11.26(br,1h),10.00(s,1h),7.96(s,1h),7.98(s,1h),7.86(d,j=10.8hz,1h),7.63(br,1h),7.43(d,j=8.0hz,2h),7.77(br,2h),4.18(br,2h),2.09(m,2h),1.98-1.81(m,4h),1.56(m,2h),1.23(m,2h)。lc-ms m/z[m+h]
+
,c
21h21
fn2o3的计算值:369;实测值:369。
[1128]
实施例b48:3-氟-5-甲酰基-4-羟基-n-(4-(吡咯烷-1-基)-3-(三氟甲基)苯基)苯甲酰胺(化合物b91)
[1129][1130]
步骤1:1-(4-硝基-2-(三氟甲基)苯基)吡咯烷
[1131]
遵循按照实施例b25的用于获得3,3-二甲基-1-(4-硝基苯基)吡咯烷的类似程序,从吡咯烷(357mg,5.0mmol,1.05当量)和1-氟-4-硝基-2-(三氟甲基)苯(1g,4.8mmol,1.0当量)制备1-(4-硝基-2-(三氟甲基)苯基)吡咯烷(930mg,3.6mmol,75%产率)。未对这个化合物进行lcms。
[1132]
步骤2:4-(吡咯烷-1-基)-3-(三氟甲基)苯胺
[1133]
遵循按照实施例b25的用于获得4-(3,3-二甲基吡咯烷-1-基)苯胺的类似程序,从1-(4-硝基-2-(三氟甲基)苯基)吡咯烷(900mg,3.5mmol,1.0当量)和fe(1.94g,34.6mmol,10当量)制备4-(吡咯烷-1-基)-3-(三氟甲基)苯胺(790mg,3.4mmol,98%产率)。lc-ms m/z[m+h]
+
,c
11h13
n3o2的计算值:231;实测值:231。
[1134]
步骤3:4-(苯甲基氧基)-3-(1,3-二硫杂环己烷-2-基)-5-氟-n-(4-(吡咯烷-1-基)-3-(三氟甲基)苯基)苯甲酰胺
[1135]
将苯甲基溴(bnbr)(3.62g,21.2mmol,2.0当量)添加至3-(1,3-二硫杂环己烷-2-基)-5-氟-4-羟基苯甲酸(2.9g,10.6mmol,1.0当量)和碳酸钾(2.9g,21.0mmol,2.0当量)于dmf(25ml)中的溶液中。在室温下将混合物搅拌3小时,并且倾倒至水中。接着将混合物用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩以产生呈淡黄色固体状的粗制经双bn保护的酯(3.1g,6.8mmol,64%产率)。将酯(3.1g,6.8mmol,1.0当量)与lioh.h2o(833mg,20.5mmol,3当量)在thf/水(5ml/5ml)中混合。在室温下将反应搅拌2小时。接着将反应体系的ph酸化至3-4,并且将混合物用乙酸乙酯萃取三次。将有机萃取
物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。使残余物在乙酸乙酯/石油醚中结晶以产生呈白色固体状的4-(苯甲基氧基)-3-(1,3-二硫杂环己烷-2-基)-5-氟苯甲酸(1.5g,4.1mmol,60%产率)。将所得4-(苯甲基氧基)-3-(1,3-二硫杂环己烷-2-基)-5-氟苯甲酸(445mg,1.2mmol,1.0当量)溶解于二氯甲烷(10ml)和草酰氯(311mg,2.4mmol,2.0当量)中,并且添加dmf(1滴)。在室温下将反应搅拌2小时。在真空中移除溶剂,并且将残余物与二氯甲烷共蒸发两次。接着将残余物溶解于二氯甲烷中,并且使溶液冷却至0℃。接着,相继添加4-(吡咯烷-1-基)-3-(三氟甲基)苯胺(309mg,1.3mmol,1.1当量)和tea(369mg,3.6mmol,3.0当量)。在室温下将反应搅拌3小时。将溶液倾倒至水中,并且用二氯甲烷萃取两次。将有机萃取物用1%khso4洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/乙酸乙酯=20:1至5:1)来纯化以产生呈黄色粉末状的4-(苯甲基氧基)-3-(1,3-二硫杂环己烷-2-基)-5-氟-n-(4-(吡咯烷-1-基)-3-(三氟甲基)苯基)苯甲酰胺(370mg,0.64mmol,53%产率)。lc-ms m/z[m+h]
+
,c
29h28
f4n2o2s2的计算值:577;实测值:577。
[1136]
步骤4:在40℃下将4-(苯甲基氧基)-3-(1,3-二硫杂环己烷-2-基)-5-氟-n-(4-(吡咯烷-1-基)-3-(三氟甲基)苯基)苯甲酰胺(350mg,0.61mmol,1.0当量)、mei(12.3g,60.8mmol,100当量)和碳酸氢钠(1.46g,12.2mmol,20当量)于乙腈/水(25ml/5ml)中的混合物加热2小时。使混合物冷却至室温,倾倒至水中,并且用乙酸乙酯萃取三次。将有机萃取物合并,用盐水洗涤,经无水硫酸钠干燥,并且浓缩。将残余物通过硅胶柱色谱法(石油醚/etoac=100:1至20:1)来纯化以产生呈黄色固体状的中间体(290mg,0.60mmol,98%产率)。将中间体(190mg,0.39mmol,1.0当量)溶解于二氯甲烷(10ml)中,并且添加无水alcl3(208mg,1.56mmol,4.0当量)。在室温下将反应搅拌过夜。将混合物倾倒至冰水和二氯甲烷中。滤除不溶物,并且将滤液用dcm萃取三次。将有机萃取物合并,经无水硫酸钠干燥,并且浓缩。将残余物通过制备型tlc来纯化以产生呈黄色固体状的4-(苯甲基氧基)-3-氟-5-甲酰基-n-(4-(吡咯烷-1-基)-3-(三氟甲基)苯基)苯甲酰胺(80mg,0.20mmol,52%产率)。1h nmr(dmso-d6,400mhz)δ:10.34(s,1h),10.30(s,1h),8.19(s,1h),8.07(m,2h),7.88(dd,j=9.2hz,2.0hz,1h),7.20(d,j=9.2hz,1h),3.20(m,4h),1.89(m,4h)。lc-ms m/z[m+h]
+
,c
19h16
f4n2o3的计算值:397;实测值:397。
[1137]
实施例b49:3-氟-5-甲酰基-4-羟基-n-(6-(4-苯基哌嗪-1-基)吡啶-3-基)苯甲酰胺(化合物b102)
[1138][1139]
步骤1:1-(5-硝基吡啶-2-基)-4-苯基哌嗪
[1140]
遵循按照实施例b25的用于获得3,3-二甲基-1-(4-硝基苯基)吡咯烷的类似程序,从1-苯基哌嗪盐酸盐(1.78g,11.0mmol,1.1当量)、碳酸钾(4.4g,31.89mmol,3.0当量)和2-氯-5-硝基吡啶(1.58g,10.0mmol,1.0当量)制备1-(5-硝基吡啶-2-基)-4-苯基哌嗪(2.1g,
7.4mmol,74%产率)。未对这个化合物进行lcms。
[1141]
步骤2:6-(4-苯基哌嗪-1-基)吡啶-3-胺
[1142]
遵循按照实施例b25的用于获得4-(3,3-二甲基吡咯烷-1-基)苯胺的类似程序,从1-(5-硝基吡啶-2-基)-4-苯基哌嗪(1g,3.52mmol,1.0当量)和fe(1.97g,35.2mmol,10当量)制备6-(4-苯基哌嗪-1-基)吡啶-3-胺(750mg,2.95mmol,84%产率)。未对这个化合物进行lcms。
[1143]
步骤3:3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基-n-(6-(4-苯基哌嗪-1-基)吡啶-3-基)苯甲酰胺
[1144]
遵循按照实施例b25的用于获得3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-n-(4-(3,3-二甲基吡咯烷-1-基)苯基)-5-氟-4-羟基苯甲酰胺的类似程序,从6-(4-苯基哌嗪-1-基)吡啶-3-胺(254mg,1.0mmol,1.0当量)和3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(270mg,1.0mmol,1.0当量)制备3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基-n-(6-(4-苯基哌嗪-1-基)吡啶-3-基)苯甲酰胺(270mg,0.53mmol,53%产率)。lc-ms m/z[m+h]
+
,c
28h31
fn4o4的计算值:507;实测值:507。
[1145]
步骤4:遵循用于实施例b25的类似程序,从3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基-n-(6-(4-苯基哌嗪-1-基)吡啶-3-基)苯甲酰胺(270mg,0.53mmol,1当量)以黄色固体形式制备3-氟-5-甲酰基-4-羟基-n-(6-(4-苯基哌嗪-1-基)吡啶-3-基)苯甲酰胺(120mg,0.29mmol,54%产率)。1h nmr(dmso-d6,400mhz)δ:11.69(br,1h),10.35(br,1h),10.21(s,1h),8.47(d,j=2.0hz,1h),8.19(s,1h),8.08(dd,j=11.6hz,1h),7.93(dd,j=8.8hz,2.0hz,1h),7.24(m,2h),6.99(m,2h),6.96(d,j=8.8hz,1h),6.81(m,1h),3.61(m,4h),3.25(m,4h)。lc-ms m/z[m+h]
+
,c
23h21
fn4o3的计算值:421;实测值:421。
[1146]
实施例b50:3-氟-5-甲酰基-n-(6-((3ar,6as)-六氢环戊二烯并[c]吡咯-2(1h)-基)吡啶-3-基)-4-羟基苯甲酰胺(化合物b103)
[1147][1148]
步骤1:(3ar,6as)-2-(5-硝基吡啶-2-基)八氢环戊二烯并[c]吡咯
[1149]
遵循按照实施例b25的用于获得3,3-二甲基-1-(4-硝基苯基)吡咯烷的类似程序,从(3ar,6as)-八氢环戊二烯并[c]吡咯盐酸盐(0.5g,3.4mmol,1.0当量)、碳酸钾(1.4g,10.2mmol,3.0当量)和2-氯-5-硝基吡啶(0.53g,3.7mmol,1.1当量)制备(3ar,6as)-2-(5-硝基吡啶-2-基)八氢环戊二烯并[c]吡咯(680mg,2.9mmol,86%产率)。未对这个化合物进行lcms。
[1150]
步骤2:6-((3ar,6as)-六氢环戊二烯并[c]吡咯-2(1h)-基)吡啶-3-胺
[1151]
遵循按照实施例b25的用于获得4-(3,3-二甲基吡咯烷-1-基)苯胺的类似程序,从(3ar,6as)-2-(5-硝基吡啶-2-基)八氢环戊二烯并[c]吡咯(0.5g,2.1mmol,1.0当量)和fe(1.2g,21.5mmol,10当量)制备6-((3ar,6as)-六氢环戊二烯并[c]吡咯-2(1h)-基)吡啶-3-胺(410mg,2.0mmol,94%产率)。未对这个化合物进行lcms。
[1152]
步骤3:3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-n-(6-((3ar,6as)-六氢
环戊二烯并[c]吡咯-2(1h)-基)吡啶-3-基)-4-羟基苯甲酰胺
[1153]
遵循按照实施例b25的用于获得3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-n-(4-(3,3-二甲基吡咯烷-1-基)苯基)-5-氟-4-羟基苯甲酰胺的类似程序,从6-((3ar,6as)-六氢环戊二烯并[c]吡咯-2(1h)-基)吡啶-3-胺(240mg,1.18mmol,1.1当量)和3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-4-羟基苯甲酸(290mg,1.07mmol,1.0当量)制备3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-n-(6-((3ar,6as)-六氢环戊二烯并[c]吡咯-2(1h)-基)吡啶-3-基)-4-羟基苯甲酰胺(160mg,0.35mmol,33%产率)。lc-ms m/z[m+h]
+
,c
25h30
fn3o4的计算值:456;实测值:456。
[1154]
步骤4:遵循用于实施例b25的类似程序从3-(5,5-二甲基-1,3-二氧杂环己烷-2-基)-5-氟-n-(6-((3ar,6as)-六氢环戊二烯并[c]吡咯-2(1h)-基)吡啶-3-基)-4-羟基苯甲酰胺(160mg,0.35mmol,1当量)以黄色固体形式制备3-氟-5-甲酰基-n-(6-((3ar,6as)-六氢环戊二烯并[c]吡咯-2(1h)-基)吡啶-3-基)-4-羟基苯甲酰胺(70mg,0.19mmol,54%产率)。1h nmr(cdcl3,400mhz)δ:10.01(br,1h),8.78(br,1h),8.39(s,1h),8.26(s,1h),8.17(m,1h),8.03(d,j=10.8hz,1h),6.50(d,j=9.2hz,1h),3.72(m,2h),3.32(m,2h),2.84(m,2h),1.92(m,2h),1.78(m,1h),1.65(m,1h),1.53(m,2h)。lc-ms m/z[m+h]
+
,c
20h20
fn3o3的计算值:370;实测值:370。
[1155]
生物学实施例1:体外测定
[1156]
i.tlr2测定
[1157]
合成二酰化脂蛋白(pam2csk4,tlr2/6激动剂)和合成三酰化脂蛋白(pam3csk4,tlr1/2激动剂)从invivogen获得,并且将其溶解于无内毒素水中以达到1mg/ml浓度,涡旋直至完全溶解,并且以等分试样在-20℃下储存。在添加至细胞之前,简短地涡旋经溶解配体的等分试样,接着于培养基中稀释至25ng/ml pam2csk4或1000ng/ml pam3csk4。通过使用每种激动剂的从以下起始浓度开始的3倍稀释液来确定每个测定操作的激动剂ec
50
:对于pam2csk4是5ng/ml,并且对于pam3csk4是200ng/ml。
[1158]
将测试化合物于dmso中新鲜溶解成10-20mm储备物,并且在水浴声波仪中进行声波处理5-10分钟。于dmso中制备连续稀释液,接着于培养基中稀释。用于测定中的最终dmso浓度是1%。
[1159]
hek-blue htlr2报告细胞(invivogen)是稳定表达人tlr2基因与在nfκb启动子位点的下游的分泌型胚胎碱性磷酸酶(seap)报告构建体两者的hek-293细胞。使用含有1x glutamax(gibco)、10%热失活胎牛血清(gibco)、青霉素-链霉素(50u/ml青霉素,50μg/ml链霉素,gibco)、100μg/ml normocin(invivogen)和选择性抗生素1x hek-blue selection(invivogen)的杜贝卡氏改良依格氏培养基(dulbecco’s modified eagle medium,dmem;gibco),根据制造商方案培养hek-blue htlr2报告体。将用于检测和定量分泌型碱性磷酸酶的quanti-blue试剂(invivogen)溶解于100ml无内毒素水中,升温至37℃,持续30分钟,接着使用0.2μm膜来过滤。
[1160]
ii.tlr9测定
[1161]
合成odn(odn 2006(odn7909),b类cpg寡核苷酸,tlr9激动剂)从invivogen获得,并且将其溶解于无内毒素水中以达到500μm浓度,涡旋直至完全溶解,并且以等分试样在-20℃下储存。在添加至细胞之前,简短地涡旋经溶解配体的等分试样,接着于培养基中稀释
至50μm。通过使用从起始浓度10μm开始的3倍稀释液来确定每个测定操作的激动剂ec
50
。
[1162]
将测试化合物于dmso中新鲜溶解成10-20mm储备物,并且在水浴声波仪中进行声波处理5-10分钟。于dmso中制备连续稀释液,接着于培养基中稀释。用于测定中的最终dmso浓度是1%。
[1163]
hek-blue htlr9报告细胞(invivogen)是稳定表达人tlr9基因与在nfκb启动子位点的下游的分泌型胚胎碱性磷酸酶(seap)报告构建体两者的hek-293细胞。使用含有1x glutamax(gibco)、10%热失活胎牛血清(gibco)、青霉素-链霉素(50u/ml青霉素,50μg/ml链霉素,gibco)、100μg/ml normocin(invivogen)以及选择性抗生素10μg/ml杀稻瘟素(blasticidin)(invivogen)和100μg/ml吉欧霉素(zeocin)(invivogen)的杜贝卡氏改良依格氏培养基(dmem;gibco),根据制造商方案培养hek-blue htlr9细胞。将用于检测和定量分泌型碱性磷酸酶的quanti-blue试剂(invivogen)溶解于100ml无内毒素水中,升温至37℃,持续30分钟,接着使用0.2μm膜来过滤。
[1164]
生物学实施例2:hek blue htlr2拮抗测定
[1165]
i.tlr2测定
[1166]
在第1天,将50μl的每种测试化合物稀释液(一式两份)或媒介物对照添加至96孔板的每个孔中,随后添加150μl的hek-blue htlr2细胞悬液(1x105个细胞/孔),并且在37℃/5%co2下孵育2小时。接着,将50μl的约3x ec
50
浓度的每种激动剂(pam2csk4或pam3csk4)添加至含有测试化合物或媒介物对照的孔中。接着在37℃/5%co2下将板孵育18小时。对于每个测定操作,将非处理hek-blue htlr2细胞用激动剂的连续稀释液处理以确定相应操作的ec
50
值。
[1167]
在第2天,检测细胞培养上清液中的分泌型碱性磷酸酶(seap)活性。简要来说,从每个孔收集20μl,并且转移至96孔板中。接着,将200μl的quanti-blue检测试剂添加至每个孔中。在室温下将板孵育15分钟,并且通过在655nm下进行分光光度计od读取来评估seap活性。表a和表b显示使用pam2csk4和pam3csk4作为激动剂在hek细胞中测试的化合物的活性。将化合物的对抗pam2csk4和pam3csk4的活性呈现为ic
50
值,其定义为当对由激动剂诱导的信号的抑制百分比等于50时的化合物浓度。对于每种化合物,基于8点稀释计算ic
50
值。
[1168]
ii.tlr9测定
[1169]
在第1天,将50μl的每种测试化合物稀释液(一式两份)或媒介物对照添加至96孔板的每个孔中,随后添加150μl的hek-blue htlr9细胞悬液(1x105个细胞/孔),并且在37℃/5%co2下孵育2小时。接着,将50μl的约3x ec
50
浓度的tlr9激动剂odn 2006添加至含有测试化合物或媒介物对照的孔中。接着在37℃/5%co2下将板孵育18小时。对于每个测定操作,将经媒介物处理的hek-blue htlr9细胞用激动剂的连续稀释液处理以确定相应操作的ec
50
值。
[1170]
在第2天,检测细胞培养上清液中的分泌型碱性磷酸酶(seap)活性。简要来说,从每个孔收集30μl,并且转移至96孔板中。接着,将200μl的quanti-blue检测试剂添加至每个孔中。在37℃下将板孵育60分钟,并且通过在655nm下进行分光光度计od读取来评估seap活性。表a和表b显示在hek-blue htlr9细胞中测试的化合物的对抗odn 2006的活性。将化合物的对抗odn 2006的活性呈现为ic
50
值,其定义为当对由激动剂诱导的信号的抑制百分比等于50时的化合物浓度。对于每种化合物,基于8点稀释计算精确ic
50
值。对于每种化合物,
基于4点稀释计算近似ic
50
值(约或《)。
[1171]
表a.
[1172]
[1173]
[1174][1175]
nd=未测出
[1176]
表b.
[1177]
[1178][1179]
nd=未测出
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1