包含二氢和厚朴酚的制剂的制作方法
包含二氢和厚朴酚的制剂
1.相关申请的交叉引用
2.本公开要求于2019年8月6日提交的美国专利申请号62/883,453的申请日的权益,其公开内容在此通过引用整体并入本文。
背景技术:
3.迄今为止,焦虑症被认为是神经疾病的类型。焦虑症的代表性症状的示例包括神经障碍、情绪障碍、人格障碍、行为障碍和睡眠障碍。已知用于治疗上述症状的药物制品有大约50种产品,例如苯二氮卓类、噻吩二氮卓类和氨基甲酸酯制品。
4.由于需要长期施用此类药物制品以改善症状,不利的是,因此使用此类药物制品会导致严重的副作用,例如药物依赖、运动障碍和意识模糊,或轻微的副作用,例如如嗜睡、头晕、食欲不振和虚弱。因此,一直在等待开发可以作为现有抗焦虑剂的替代品的新型抗焦虑制剂。
技术实现要素:
5.本公开的一个方面是包含二氢和厚朴酚-b(dhh-b)或其衍生物或类似物的制剂(下文称为“dhh-b制剂”)。在一些实施例中,dhh-b制剂可以是糊剂、粉末、油、液体、悬浮液、溶液或其他形式。在一些实施例中,dhh-b制剂适合施用于哺乳动物。在一些实施例中,提供dhh-b制剂以施用于人类受试者。在其他实施例中,提供dhh-b制剂供兽医使用。在一些实施例中,dhh-b制剂适用于治疗焦虑或焦虑相关病症。
6.在一些实施例中,dhh-b制剂作为用于口服给药的液体制剂提供,例如用于向人和/或兽药受试对象口服给药。在一些实施例中,包括dhh-b的液体制剂可以采取例如溶液、糖浆或悬浮液的形式,或者它们可以作为干燥产品提供,用于在给药前用水或其他合适的载体重构并且可以施用于人类和/或兽药受试对象。此类液体制剂可以通过常规方法与药学上可接受的如下添加剂一起制备:例如悬浮剂(例如山梨糖醇糖浆、甲基纤维素或氢化食用脂肪);乳化剂(例如卵磷脂或阿拉伯胶);非水载体(例如杏仁油、油性酯或乙醇);防腐剂(例如对羟基苯甲酸甲酯或丙酯或山梨酸);粘合剂、崩解剂、填充剂、络合剂、润滑剂和/或人造或天然色素或甜味剂。液体制剂可以在本领域技术人员已知的药物载体中施用于人类或兽药受试对象。此类药物载体包括但不限于胶囊、锭剂、糖浆、喷雾剂、漱洗剂和漱口水。
7.在一些实施例中,dhh-b制剂可用作膳食补充剂、营养品或可用于预防、减轻、减缓发作或治疗各种人类疾病(例如,焦虑症)的此类其他制剂。应当认识到,与药物组合物相比,包括dhh-b在内的膳食补充剂可能不使用相同的配方成分或不具有相同的无菌和其他fda要求。膳食补充剂可以是液体形式,例如溶液、糖浆或悬浮液,或者可以是在使用前用水或任何其他合适的液体重构的产品形式。此类液体制品可通过常规方法制备,例如茶、保健饮料、膳食奶昔、液体浓缩物或液体可溶性片剂、胶囊、丸剂或粉末,从而可通过溶解液体可溶性片剂、胶囊、药丸或液体中的粉末来制备饮料并饮用所得饮料。或者,如上所述,包括dhh-b的膳食补充剂可以采取片剂或胶囊剂的形式,例如软胶囊,通过常规方式制备并且任
选地包括其他膳食补充剂,包括维生素、矿物质、其他草药补充剂、粘合剂、填充剂、润滑剂、崩解剂或润湿剂。片剂可通过本领域熟知的方法包衣以提供延迟释放和/或延长释放。
8.本公开的第一方面是包含二氢和厚朴酚-b(“dhh-b”)和至少一种药学上可接受的载体的组合物,其中dhh-b以按组合物的总重量计约0.5%至约25%之间的量存在。在一些实施例中,dhh-b与增溶剂复合。在一些实施例中,增溶剂是环糊精。在一些实施例中,环糊精是羟丙基-β-环糊精。在一些实施例中,所述组合物还包含稀释剂、粘合剂、甜味剂、崩解剂、填充剂和润滑剂中的至少三种。在一些实施例中,所述组合物还包含按组合物的总重量计约0.4%至约65%的量的交联聚维酮。
9.在一些实施例中,组合物包含按组合物总重量计约39%至约80%的量的微晶纤维素。在一些实施例中,dhh-b的存在量为占组合物总重量的约0.75%至约2.5%。
10.在一些实施例中,组合物进一步包含油和表面活性剂。在一些实施例中,油包含甘油三酯。在一些实施例中,表面活性剂包含平均分子量为约1500g/mol的聚乙二醇。在一些实施例中,该组合物进一步包含二甘醇单乙醚。
11.本公开的第二方面是包含二氢和厚朴酚-b(“dhh-b”)和至少一种药学上可接受的载体的组合物,其中dhh-b的存在量在按组合物总重量计约0.000001%至约5%之间。权利要求13的组合物,进一步包含d-ɑ-生育酚聚乙二醇琥珀酸酯。在一些实施例中,所述组合物还包含调味剂。在一些实施例中,dhh-b存在于量为组合物总重量的约0.000008%至约1%。
12.在一些实施例中,所述组合物还包含润湿剂。在一些实施例中,所述润湿剂是丙二醇,并且其中所述丙二醇以按组合物总重量计约0.0005%至约6%的量存在。
13.本公开的第三方面是治疗焦虑或其症状的方法,包括向有需要的受试者施用包含二氢和厚朴酚-b(“dhh-b”)和至少一种药学上可接受的载体的组合物,其中dhh-b以组合物总重量的约0.5%至约25%的量存在。在一些实施例中,施用制剂使得每天向受试者施用至少5mg的dhh-b。在一些实施例中,该方法进一步包括向受试者共同施用第二活性药物成分,其中第二活性药物成分是抗焦虑剂。
14.本公开的第四方面是治疗焦虑或其症状的方法,包括向有需要的受试者施用包含二氢和厚朴酚-b(“dhh-b”)和至少一种药学上可接受的载体的组合物,其中dhh-b以组合物总重量的约0.000001%至约5%的量存在。
15.本公开的第五方面是治疗原发性震颤障碍、帕金森病震颤、张力障碍性震颤、小脑震颤、心因性震颤、直立性震颤、生理性震颤的方法,包括向有需要的受试者施用包含二氢和厚朴酚-b的组合物(“dhh-b”)和至少一种药学上可接受的载体,其中dhh-b以组合物总重量的约0.000001%至约5%的量存在。
16.本公开的第六方面是治疗原发性震颤障碍、帕金森病震颤、张力障碍性震颤、小脑震颤、心因性震颤、直立性震颤、生理性震颤的方法,包括向有需要的受试者施用包含二氢和厚朴酚-b的组合物(“dhh-b”)和至少一种药学上可接受的载体,其中dhh-b以组合物总重量的约0.5%至约25%的量存在。在一些实施例中,施用制剂使得每天向受试者施用至少5mg的dhh-b。
具体实施方式
17.定义
18.还应该理解的是,除非有明确的相反指示,否则在本文要求保护的包括一个以上步骤或动作的任何方法中,该方法的步骤或动作的顺序不一定限于叙述该方法的步骤或动作的顺序。
19.如本文所用,单数术语“一”、“一个”和“该”包括复数指示物,除非上下文另有明确指示。类似地,除非上下文另有明确说明,否则“或”一词旨在包括“和”。术语“包括”具有包容性定义,因此“包括a或b”是指包括a、b或者a和b。
20.如本文所用,术语“约”在本文中用于表示大约、在该区域中、大致或大约。当术语“约”与数值范围结合使用时,它通过在所述数值之上和之下扩展边界来修改该范围。一般而言,术语“约”或“大约”在本文中用于将数值修改为高于和低于所述值20%的方差。
21.如本文在说明书和权利要求书中使用的,“或”应理解为与如上定义的“和/或”具有相同的含义。例如,当分隔列表中的项目时,“或”或“和/或”应被解释为具有包容性,即包括至少一个,但也包括多个或多个元素列表,以及(可选)其他未列出的项目。只有明确指出相反的术语,例如“仅一个或“恰好一个”,或者当在权利要求中使用时,“由...组成”将指包含一个元素数量或元素列表中的一个元素。一般而言,此处使用的术语“或”仅应解释为表示排他性的替代方案(即“一个或另一个但不是两者”),如果前面带有排他性术语,例如“任一”、“其中一个”、“仅一个”或“恰好一个”。“基本上由
……
组成”在权利要求中使用时,应具有专利法领域中使用的普通含义。
22.术语“包括”、“包括”、“具有”等可互换使用并且具有相同的含义。类似地,“包括”、“包括”、“具有”等可互换使用并且具有相同的含义。具体而言,每个术语的定义与美国专利法中“包含”的通用定义一致,因此被解释为开放术语,意思是“至少以下”,并且也被解释为不排除附加特征、限制、因此,例如,“具有组件a、b和c的设备”意味着该设备至少包括组件a、b和c。类似地,短语:“涉及步骤a、b和c的方法”是指该方法至少包括步骤a、b和c。此外,虽然步骤和过程可以在本文中以特定顺序概述,但本领域技术人员将认识到排序步骤和过程可以变化。
23.如本文在说明书和权利要求书中使用的,短语“至少一个”在提及一种或多种元素的列表时,应理解为表示选自以下任何一种或多种元素的至少一种元素。元素列表中的元素,但不一定包括元素列表中具体列出的每个元素中的至少一个,并且不排除元素列表中的元素的任何组合。该定义还允许除了在短语“至少一个”所指的元素列表中具体标识的元素之外的元素可以可选地存在,无论是否与那些具体标识的元素相关或不相关。因此,作为非限制性示例,“a和b中的至少一个”(或等效地,“a或b中的至少一个”,或等效地“a和/或b中的至少一个”)可以指,在一个实施例中,至少一种,任选地包括多于一种的a,不存在b(并且任选地包括除b之外的元素);在另一个实施例中,至少一个,任选地包括多于一个的b,不存在a(并且任选地包括除a之外的元素);在又一个实施例中,至少一种,任选地包括多于一种的a,和至少一种,任选地包括多于一种的b(并且任选地包括其它元素);等等。
24.本文使用的术语“抗焦虑作用”或“抗焦虑效果”是指例如治疗、缓解或预防焦虑症病症,例如神经障碍、情绪障碍、人格障碍、行为障碍和睡眠障碍。
25.如本文所用,术语“施用”是指向需要治疗的受试者提供组合物、制剂或特定试剂,包括本文所述的那些。
26.短语“药学上可接受的”或“药学上可接受的”是指当给予动物或人时不产生不利、
过敏或其他不良反应的分子实体和组合物。如本文所用,“药学上可接受的载体”包括溶剂、缓冲剂、溶液、分散介质、包衣、抗菌剂和抗真菌剂、等渗剂和吸收延迟剂等,其可用于配制药物,例如适合施用于人的药物。将此类介质和试剂用于药物活性物质在本领域中是众所周知的。除非任何常规介质或试剂与本公开的表达载体不相容,否则考虑其在治疗组合物中的用途。
27.如本文所用,术语“受试者”是指哺乳动物,例如人、小鼠、马、狗或灵长类动物。通常,哺乳动物是人类(智人)。人类受试者可以是成年患者或儿科患者。
28.如本文所用,术语“治疗有效剂量”或“剂量量(dose amount)”是指组合物或组合物的组分的量,其有效实现受试者或其生理系统的改善,包括但不限于改善或消除症状、延迟疾病发作、症状进展较慢和本领域技术人员酌情选择的其他指标。
29.如本文所用,关于特定病症的术语“治疗(treatment)”、“治疗(treating)”或“治疗(treat)”是指获得所需的药理学和/或生理学效果。就完全或部分预防疾病或其症状而言,该效果可以是预防性的和/或就疾病的部分或完全治愈和/或归因于该疾病的副作用而言可以是治疗性的。如本文所用,“治疗”涵盖对受试者,特别是人类的疾病的任何治疗,并且包括:(a)防止疾病在可能易患但尚未被诊断患有该疾病的受试者中发生;(b)抑制疾病,即阻止其发展;(c)缓解疾病,即导致疾病消退和/或缓解一种或多种疾病症状。“治疗”还可以包括药剂的递送或治疗的施用以提供药理作用,即使在没有疾病或病症的情况下。术语“治疗”在一些实施例中用于指施用本公开的化合物以减轻宿主、优选哺乳动物受试者、更优选人类的疾病或病症。因此,术语“治疗”可以包括:防止疾病在宿主中发生,特别是当宿主易患该疾病但尚未被诊断出患有该疾病时;抑制疾病;和/或减轻或逆转疾病。就本公开的方法涉及预防疾病而言,应理解术语“预防”并不要求疾病状态被完全阻止。相反,如本文所用,术语预防是指技术人员识别易患疾病的群体,使得本公开的化合物的施用可以在疾病发作之前发生的能力。该术语并不意味着必须完全避免疾病状态。
30.dhh-b制剂
31.本公开内容涉及适合施用于哺乳动物的dhh-b制剂。在一些实施例中,提供dhh-b制剂以施用于人类受试者。在其他实施例中,提供dhh-b制剂供兽医使用。
32.二氢和厚朴酚-b
33.二氢和厚朴酚,3'-(2-丙烯基)-5-丙基-(1,1'-联苯)-2,4'-二醇(“dhh-b”),是一种有效的抗焦虑化合物,具有如苯二氮卓的副作用。
34.在一些实施例中,任何制剂中的dhh-b的量为组合物总重量的约0.5%至约30%。在其他实施例中,任何组合物中的dhh-b的量为组合物的总重量的约1%至约30%之间。在又一些实施例中,任何组合物中的dhh-b的量为组合物总重量的约1%至约25%。在进一步的实施例中,任何组合物中的dhh-b的量为组合物总重量的约1%至约20%。在更进一步的实施例中,任何组合物中dhh-b的量为组合物总重量的约1%至约15%。在更进一步的实施例中,任何组合物中的dhh-b的量为组合物总重量的约1%至约10%。在更进一步的实施例中,任何组合物中的dhh-b的量为组合物总重量的约1%至约5%。
35.在一些实施例中,任何制剂中dhh-b的量在组合物总重量的约0.000001%至约5%之间。在其他实施例中,任何组合物中dhh-b的量为组合物总重量的约0.000001%至约3%。在其它实施例中,任何组合物中的dhh-b的量按组合物的总重量计在约0.000001%至约
2.5%之间。在进一步的实施例中,任何组合物中的dhh-b的量为组合物总重量的约0.00001%至约2.5%。在更进一步的实施例中,任何组合物中的dhh-b的量为组合物总重量的约0.0001%至约2.5%。在更进一步的实施例中,任何组合物中的dhh-b的量为组合物总重量的约0.001%至约2.5%。在更进一步的实施例中,任何组合物中的dhh-b的量为组合物总重量的约0.01%至约2.5%。在更进一步的实施例中,任何组合物中的dhh-b的量为组合物总重量的约0.01%至约2%。在更进一步的实施例中,任何组合物中的dhh-b的量为组合物总重量的约0.01%至约1.5%。在更进一步的实施例中,任何组合物中的dhh-b的量为组合物总重量的约0.1%至约1.5%。在更进一步的实施例中,任何组合物中的dhh-b的量为组合物总重量的约0.1%至约1%。在更进一步的实施例中,任何组合物中的dhh-b的量为组合物总重量的约0.1%至约0.5%。
36.在一些实施例中,任何制剂中dhh-b的量在约1mg至约20mg dhh-b之间。在一些实施例中,任何制剂中dhh-b的量在约2mg至约20mg dhh-b之间。在一些实施例中,任何制剂中dhh-b的量在约3mg至约18mg dhh-b之间。在一些实施例中,任何制剂中dhh-b的量在约3mg至约16mg dhh-b之间。在一些实施例中,任何制剂中dhh-b的量在约3mg至约15mg dhh-b之间。在一些实施例中,任何制剂中的dhh-b的量在约4mg至约14mg dhh-b之间。在一些实施例中,任何制剂中dhh-b的量在约4mg至约12mg dhh-b之间。在一些实施例中,任何制剂中dhh-b的量在约5mg至约10mg dhh-b之间。
37.在一些实施例中,任何制剂中的dhh-b的量为约4mg。在一些实施例中,任何制剂中dhh-b的量为约4.5mg。在一些实施例中,任何制剂中dhh-b的量为约5mg。在一些实施例中,任何制剂中dhh-b的量为约5.5mg。在一些实施例中,任何制剂中dhh-b的量为约6mg。在一些实施例中,任何制剂中的dhh-b的量为约6.5mg。在一些实施例中,任何制剂中的dhh-b的量为约7mg。在一些实施例中,任何制剂中的dhh-b的量为约7.5mg。在一些实施例中,任何制剂中dhh-b的量为约8mg。在一些实施例中,任何制剂中的dhh-b的量为约8.5mg。在一些实施例中,任何制剂中的dhh-b的量为约9mg。在一些实施例中,任何制剂中的dhh-b的量为约9.5mg。在一些实施例中,任何制剂中的dhh-b的量为约10mg。在一些实施例中,任何制剂中的dhh-b的量为约10.5mg。在一些实施例中,任何制剂中的dhh-b的量为约11mg。在一些实施例中,任何制剂中的dhh-b的量为约11.5mg。在一些实施例中,任何制剂中dhh-b的量为约12mg。在一些实施例中,任何制剂中的dhh-b的量为约12.5mg。在一些实施例中,任何制剂中dhh-b的量为约13mg。在一些实施例中,任何制剂中的dhh-b的量为约15mg。
38.在一些实施例中,dhh-b的日剂量范围在约0.08mg/kg至约3mg/kg之间。在一些实施例中,dhh-b的日剂量范围在约0.09mg/kg至2.8mg/kg之间。在一些实施例中,dhh-b的日剂量范围在约0.1mg/kg至约2.6mg/kg之间。在一些实施例中,dhh-b的日剂量范围在约0.11mg/kg至约2.4mg/kg之间。在一些实施例中,dhh-b的日剂量范围在约0.12mg/kg至约2.2mg/kg之间。在一些实施例中,dhh-b的日剂量范围在约0.13mg/kg至约2mg/kg之间。在一些实施例中,dhh-b的日剂量范围在约0.14mg/kg至约1.8mg/kg之间。在一些实施例中,dhh-b的日剂量为约0.15mg/kg。
39.药学上可接受的赋形剂、载体和添加剂
40.本公开的制剂可以进一步包含一种或多种药学上可接受的赋形剂,包括但不限于稀释剂、粘合剂、润滑剂、崩解剂、调味剂、掩味剂、着色剂、ph调节剂、稳定剂、吸收剂增强
剂、粘度调节剂、成膜聚合物、填充剂、表面活性剂、助流剂、增塑剂、防腐剂、精油和甜味剂。在一些实施例中,药学上可接受的赋形剂、载体和/或添加剂可以是可引入本文所述制剂中的食物组合物或食物产品。
41.本领域技术人员将能够为所需制剂选择合适的赋形剂或赋形剂混合物。通常,包含在任何制剂中的任何药学上可接受的赋形剂、载体和/或添加剂的量可以根据所需的效果、给药途径、最终组合物的形式而变化。然而,一般而言,用本公开的制剂配制的药学上可接受的赋形剂、载体和/或添加剂的总量可以占制剂总重量的约1%至约99%。在一些实施例中,用本公开的制剂配制的药学上可接受的赋形剂、载体和/或添加剂的总量可以占制剂总重量的约1%至约98%。在一些实施例中,用本公开的制剂配制的药学上可接受的赋形剂、载体和/或添加剂的总量可以占制剂总重量的约1%至约97%。在一些实施例中,用本公开的制剂配制的药学上可接受的赋形剂、载体和/或添加剂的总量可以占制剂总重量的约1%至约96%。在一些实施例中,用本公开的制剂配制的药学上可接受的赋形剂、载体和/或添加剂的总量可以占制剂总重量的约1%至约95%。在一些实施例中,用本公开的制剂配制的药学上可接受的赋形剂、载体和/或添加剂的总量可以占制剂总重量的约1%至约94%。在一些实施例中,用本公开的制剂配制的药学上可接受的赋形剂、载体和/或添加剂的总量可以占制剂总重量的约1%至约93%。在一些实施例中,用本公开的制剂配制的药学上可接受的赋形剂、载体和/或添加剂的总量可以占制剂总重量的约1%至约92%。在一些实施例中,用本公开的制剂配制的药学上可接受的赋形剂、载体和/或添加剂的总量可以占制剂总重量的约1%至约91%。
42.在其他实施例中,用本公开的制剂配制的药学上可接受的赋形剂、载体和/或添加剂的总量可以在按制剂总重量计约1%至约90%的范围内。在一些实施例中,用本公开的制剂配制的药学上可接受的赋形剂、载体和/或添加剂的总量可以占制剂总重量的约1%至约88%。在一些实施例中,用本公开的制剂配制的药学上可接受的赋形剂、载体和/或添加剂的总量可以占制剂总重量的约1%至约86%。在一些实施例中,用本公开的制剂配制的药学上可接受的赋形剂、载体和/或添加剂的总量可以占制剂总重量的约1%至约84%。在一些实施例中,用本公开的制剂配制的药学上可接受的赋形剂、载体和/或添加剂的总量可以占制剂总重量的约1%至约82%。在其他实施例中,用本公开的制剂配制的药学上可接受的赋形剂、载体和/或添加剂的总量可以占制剂总重量的约1%至约80%。在一些实施例中,用本公开的制剂配制的药学上可接受的赋形剂、载体和/或添加剂的总量可以占制剂总重量的约1%至约78%。在一些实施例中,用本公开的制剂配制的药学上可接受的赋形剂、载体和/或添加剂的总量可以占制剂总重量的约1%至约76%。在一些实施例中,用本公开的制剂配制的药学上可接受的赋形剂、载体和/或添加剂的总量可以占制剂总重量的约1%至约74%。在一些实施例中,用本公开的制剂配制的药学上可接受的赋形剂、载体和/或添加剂的总量可以占制剂总重量的约1%至约72%。在其他实施例中,用本公开的制剂配制的药学上可接受的赋形剂、载体和/或添加剂的总量可以占制剂总重量的约1%至约70%。
43.在一些实施例中,dhh-b的量与药学上可接受的赋形剂或载体的量之比为约100:1至约1:100。在一些实施例中,dhh-b的量与药学上可接受的赋形剂或载体的量之比为约90:1至约1:90。在一些实施例中,dhh-b的量与药学上可接受的赋形剂或载体的量之比为约80:1至约1:80。在一些实施例中,dhh-b的量与药学上可接受的赋形剂或载体的量之比为约70:
1至约1:70。在一些实施例中,dhh-b的量与药学上可接受的赋形剂或载体的量之比为约60:1至约1:60。在一些实施例中,dhh-b的量与药学上可接受的赋形剂或载体的量之比为约50:1至约1:50。在一些实施例中,dhh-b的量与药学上可接受的赋形剂或载体的量之比为约40:1至约1:40。在一些实施例中,dhh-b的量与药学上可接受的赋形剂或载体的量之比为约30:1至约1:30。在一些实施例中,dhh-b的量与药学上可接受的赋形剂或载体的量之比为约20:1至约1:20。在一些实施例中,dhh-b的量与药学上可接受的赋形剂或载体的量之比为约10:1至约1:10。在一些实施例中,dhh-b的量与药学上可接受的赋形剂或载体的量之比为约5:1至约1:5。
44.水
45.在一些实施例中,载体是水。在一些实施例中,组合物中存在的水的量为组合物总重量的约80%至约99%、组合物总重量的约80%至约98%、组合物总重量的约85%至约97%、组合物总重量的约85%至约95%、组合物总重量的约88%至约95%、组合物总重量的约90%至约95%、组合物总重量的约90%至约94%、以及组合物总重量的约90%至约93%。仅举例来说,制剂可以包含活性剂(例如dhh-b)和药学上可接受的赋形剂、载体和/或添加剂的50:50混合物。
46.稀释剂
47.稀释剂可以选自例如碳酸钙、磷酸氢钙、磷酸三钙、硫酸钙、微晶纤维素、微晶硅化纤维素、粉状纤维素、葡萄糖、葡萄糖、果糖、乳糖醇、无水乳糖、乳糖一水合物、乳糖二水合物、乳糖三水合物、甘露醇、山梨糖醇、淀粉、预胶化淀粉、蔗糖、滑石粉、木糖醇、麦芽糖、麦芽糊精、麦芽糖醇。在一些实施例中,稀释剂选自淀粉、乳糖、纤维素衍生物、糖果糖等。不同等级的乳糖包括但不限于乳糖一水合物、乳糖dt(直接压片)、无水乳糖等。不同的淀粉包括但不限于玉米淀粉、马铃薯淀粉、大米淀粉、小麦淀粉、预糊化淀粉等。可以使用的不同纤维素包括结晶纤维素,例如微晶纤维素,和粉末纤维素。其他有用的稀释剂包括但不限于羧甲纤维素、糖醇如甘露醇、山梨糖醇和木糖醇、碳酸钙、碳酸镁、磷酸氢钙和磷酸三钙。
48.粘合剂
49.粘合剂可以选自例如阿拉伯胶、海藻酸、卡波姆、羧甲基纤维素钙、羧甲基纤维素钠、微晶纤维素、粉状纤维素、乙基纤维素、明胶液体葡萄糖、瓜尔豆胶、羟乙基纤维素、羟丙基纤维素、羟丙基甲基纤维素、麦芽糖糊精、甲基纤维素、聚葡萄糖、聚环氧乙烷、聚维酮、海藻酸钠、淀粉糊、预胶化淀粉、蔗糖、黄蓍胶、低取代羟丙基纤维素、葡萄糖、山梨糖醇。
50.填料
51.合适的填充剂可以选自例如淀粉衍生物,例如玉米淀粉、马铃薯淀粉或大米淀粉,多糖例如糊精、麦芽糖糊精、糊精、微晶纤维素、粉状纤维素、微晶纤维素和瓜尔豆胶的混合物,微晶纤维素的共加工混合物;和多元醇,例如木糖醇和山梨糖醇。
52.崩解剂
53.崩解剂可以选自例如海藻酸、二氧化碳、羧甲基纤维素钙、羧甲基纤维素钠、微晶纤维素、粉状纤维素、交联羧甲基纤维素钠、交聚维酮、多库酯钠、野牛胶、羟丙基纤维素、甲基纤维素、波拉克林钾、泊洛沙姆、聚维酮、海藻酸钠、甘氨酸碳酸钠、十二烷基硫酸钠、羟基乙酸淀粉钠、淀粉、预糊化淀粉、低取代羟丙基纤维素。
54.助流剂
55.助流剂可以选自例如硅酸钙、粉状纤维素、淀粉、滑石、胶体二氧化硅。
56.润滑剂
57.润滑剂可以选自例如硬脂酸镁、硬脂酸、硬脂富马酸钠、十二烷基硫酸镁、滑石、聚乙二醇和山嵛酸甘油酯、单硬脂酸甘油酯、棕榈酸、滑石、巴西棕榈蜡、硬脂酸钙钠、十二烷基硫酸钠或镁、钙皂、硬脂酸锌、聚氧乙烯单硬脂酸酯、硅酸钙、二氧化硅、氢化植物油和脂肪、硬脂酸及其任何组合。
58.精油
59.合适的精油可以选自佛手柑油(从citrus aurantium l.subsp.bergamia wright et arn.中提取);依兰依兰油(从cananga odorata hook.f.和thoms.中提取);茉莉精油(从jasminum officinale l.中提取)。在一个实施例中,精油混合物包含等份,总计为组合物总量的约0.01%至约1%w/w,优选约0.1%w/w。其他精油是可能的。
60.甜味剂/调味剂
61.合适的甜味剂可以选自诸如蔗糖、乳糖和葡萄糖的糖;甜蜜素及其盐;糖精及其盐;和阿斯巴甜。
62.可掺入组合物中的调味剂可选自合成调味油和调味芳香剂、天然油、植物提取物。实例包括肉桂油、冬青油、薄荷油、丁香油、月桂油、茴香油、桉树油、百里香油、雪松叶油、肉豆蔻油、鼠尾草油或杏仁油。调味剂的实例包括但不限于杏仁、苹果、香蕉、浆果、泡泡糖、焦糖、柑橘、樱桃、巧克力、椰子、葡萄、绿茶、蜂蜜、柠檬、甘草、酸橙、芒果、枫树、薄荷、橙子、桃子、菠萝、葡萄干、草莓、香草、西瓜及其组合。调味剂可以以制剂总重量的约0.001001%至约5%的量存在。在一些实施例中,调味剂可以选自天然或合成香料,例如草莓香料、野樱桃香料、青苹果香料、留兰香香料和薄荷香料。在一些实施例中,调味剂选自薄荷醇、薄荷、冬青、橙、樱桃和其他水果、香草、杏仁和其他坚果等。在一些实施例中,dhh-b制剂包括两种或更多种调味剂的混合物。
63.吸收增强剂
64.用于根据本公开的某些实施例使用的吸收增强剂包括,例如,gelucire 44/14;gelucire 50/13;tagat to;tween 80;肉豆蔻酸异丙酯、聚山梨醇酯、脱水山梨糖醇酯、泊洛沙姆嵌段共聚物、peg-35蓖麻油、peg-40氢化蓖麻油、辛基聚乙二醇8甘油酯、peg-8辛酸/癸酸甘油酯、月桂基硫酸钠、磺基琥珀酸二辛酯、聚月桂基醚、乙氧基二甘醇、丙二醇单二辛酸酯、甘油单辛酸酯、甘油脂肪酸(c8-c18)乙氧基化、油酸、亚油酸、甘油辛酸酯/癸酸酯、甘油单油酸酯、甘油单月桂酸酯、辛酸/癸酸甘油三酯、乙氧基化壬基酚、peg-(8-50)硬脂酸盐、橄榄油peg-6酯、三油精peg-6酯、卵磷脂、d-α生育酚聚乙二醇1000琥珀酸酯、聚碳酸酯、甘胆酸钠、牛磺胆酸钠、环糊精、柠檬酸、柠檬酸钠、甘油三乙酸酯、组合其等。在某些优选的实施例中,吸收促进剂是甘油三乙酸酯。
65.增溶剂
66.dhh-b制剂可以包括一种或多种增溶剂或络合剂。在一些实施例中,增溶剂或络合剂是环糊精。环糊精是由环状α-(1
→
4)连接的d-吡喃葡萄糖单元组成的环状寡糖。具有六到八个单元的环糊精分别被命名为α-、β-和γ-环糊精。单元的数量决定了锥形空腔的大小,该空腔是环糊精的特征,药物可以包含在其中以形成稳定的复合物。α-、β-和γ-环糊精的许多衍生物是已知的,其中一个或多个羟基被醚基或其他基团取代。因此,这些化合物是
已知的络合剂,并且之前已在制药领域用于与水不溶性药物形成包合络合物,从而将它们溶解在水性介质中。
67.本公开范围内的环糊精包括天然环糊精α、β和γ-环糊精及其衍生物,特别是其中一个或多个羟基被例如烷基取代的衍生物,羟基烷基、羧基烷基、烷基羰基、羧基烷氧基烷基、烷基羰基氧基烷基、烷氧基羰基烷基或羟基-(单或多烷氧基)烷基;并且其中每个烷基或亚烷基部分优选包含最多六个碳。取代的环糊精通常可以以不同的取代度获得,例如1至14,优选4至7;取代度是环糊精分子上取代基的近似平均数,例如,在羟丙基-β-环糊精分子的情况下,羟丙基的近似数,并且所有这些变化都在本公开的范围内。可用于本公开内容的取代的环糊精包括聚醚,例如,如美国专利3,459,731号中所述。
68.取代的环糊精的其他实例包括醚,其中一个或多个环糊精羟基的氢被c
1-6
烷基、羟基-c
1-6
烷基、羧基-c
1-6
烷基或c
1-6
烷氧基羰基-c
1-6
烷基或其混合醚取代。特别地,此类取代的环糊精是其中一个或多个环糊精羟基的氢被c
1-3
烷基、羟基-c
2-4
烷基或羧基-c
1-2
烷基或更特别地被甲基、乙基、羟乙基、羟丙基取代的醚、羟丁基、羧甲基或羧乙基。术语“c
1-6
烷基”意在包括直链和支链饱和烃基,具有1至6个碳原子,例如甲基、乙基、1-甲基乙基、1,1-二甲基乙基、丙基、2-甲基丙基、丁基、戊基、己基等。考虑用于本文的其他环糊精包括葡糖基-β-环糊精和麦芽糖基-β-环糊精。
69.在本公开中特别有用的是β-环糊精醚例如二甲基-β-环糊精,如cyclodextrins of the future,vol.9,no.8,p.577-578by m.nogradi(1984)中描述的,随机甲基化的β-环糊精和聚醚,例如羟丙基-β-环糊精、羟乙基-β-环糊精、羟丙基-γ-环糊精和羟乙基-γ-环糊精,以及磺丁基醚,特别是β-环糊精磺丁基醚。除了简单的环糊精外,还可以使用支链环糊精和环糊精聚合物。其他环糊精描述于,例如,chemical and pharmaceutical bulletin 28:1552-1558(1980);yakugyo jiho no.6452(28mar.1983);angew.chem.int.ed.engl.19:344-362(1980);美国专利3,459,731和4,535,152号;欧洲专利号ep 0 149 197a和ep 0 197 571a;pct国际专利公开号wo90/12035;和英国专利公开gb 2,189,245。
70.描述用于根据本公开的组合物的环糊精并且为环糊精的制备、纯化和分析提供指南的其他参考文献包括以下:cyclodextrin technology by jozsef szejtli,kluwer academic publishers(1988)in the chapter cyclodextrins in pharmaceuticals;cyclodextrin chemistry by m.l.bender et al.,springer-verlag,berlin(1978);advances in carbohydrate chemistry,vol.12,ed.by m.l.wolfrom,academic press,new york in the chapter"the schardinger dextrins"by dexter french,pp.189-260;cyclodextrins and their inclusion complexes by j.szejtli,akademiai kiado,budapest,hungary(1982);i.tabushi,acc.chem.research,1982,15,pp.66-72;w.sanger,angewandte chemie,92,p.343-361(1981);a.p.croft et.al.,tetrahedron,39,pp.1417-1474(1983);irie et.al.,pharmaceutical research,5,pp.713-716(1988);pitha et.al.,int.j.pharm.29,73(1986);美国专利第4,659,696和4,383,992号;德国专利号de 3,118,218和de-3,317,064;和欧洲专利号ep 0 094 157a。描述β-和γ-环糊精的羟烷基化衍生物的专利包括pitha的美国专利4,596,795和4,727,064号,m
ü
ller的美国专利4,764,604和4,870,060号,以及m
ü
ller等人的美国专利6,407,079号。
71.用于与dhh-b络合的特别感兴趣的环糊精包括:γ-环糊精;羟烷基,例如羟乙基或羟丙基,β-和γ-环糊精的衍生物;羧基烷基,例如羧甲基或羧乙基,β-或γ-环糊精的衍生物;β-环糊精磺丁基醚;二甲基-β-环糊精;和随机甲基化的β-环糊精。2-羟丙基-β-环糊精(hpβcd)、2-羟丙基-γ-环糊精(hpγcd)、随机甲基化β-环糊精、二甲基-β-环糊精、β-环糊精磺丁基醚、羧甲基-β-环糊精(cmβcd)、羧甲基-γ-环糊精(cmγcd)和γ-环糊精(γcd)本身特别受关注,尤其是γ-环糊精和羟丙基-,β-环糊精,特别尤其是γ-环糊精。
72.表面活性剂
73.在一些实施例中,表面活性剂是阴离子表面活性剂。阴离子表面活性剂通常基于硫酸盐、磺酸盐、磷酸盐或羧酸盐并含有水溶性阳离子。磺酸盐的代表性分子式是r
–
so3–
m,其中r是约5至22个碳原子的烃基,可通过烷氧基或氧烷氧基连接到磺酸盐官能团,其中m是水溶性阳离子,例如碱金属。在一些实施例中,阴离子表面活性剂包括烷基醚硫酸盐、烷基硫酸盐和磺酸盐、烷基羧酸盐、烷基苯基醚硫酸盐、烷基聚(氧乙烯)磺酸钠盐、烷基苄基磺酸钠盐,例如十二烷基苄基磺酸钠和钠盐月桂基醚硫酸盐。在一些实施例中,阴离子表面活性剂还包括阴离子磷酸酯。
74.在一些实施例中,阴离子表面活性剂包括但不限于聚氧乙烯烷基醚,其中烷基是(ch2)s并且氧乙烯是(c2h4o)
t
,其中s是5至16,8至14,或10至12的整数;t是10至40、15至30或20至28的整数。在一个实施例中,阴离子表面活性剂是具有式(c2h4o)
23c12h25
oh的聚氧乙烯月桂基醚。在另一个实施例中,阴离子表面活性剂是聚氧乙烯(20)脱水山梨糖醇单烷基化物,该单烷基化物包含8至14个碳。在另一个实施例中,阴离子表面活性剂是具有式c
12-14h25-29
o(ch2ch2o]
x
的直链仲醇聚氧乙烯,其中x是介于2和12之间的整数。在又一个实施例中,阴离子表面活性剂是聚氧乙烯辛基。示例性表面活性剂以以下名称出售:tergitol
tm
、triton
tm
、ecosurf
tm
、dowfax
tm
、聚山梨醇酯80
tm
、bigchap、deoxy bigchap、saponin、pluronic f-68、洋地黄皂苷、脱氧胆酸盐等。在一些实施例中,阴离子表面活性剂选自tergitol
tm
、triton
tm
。
75.在一些实施例中,表面活性剂是阳离子表面活性剂。可以用于本公开的制剂的阳离子表面活性剂包括氨基或季铵部分。可用于本文的那些阳离子表面活性剂公开于以下文件中:m.c.publishing co.,mccutcheon's,detergents&emulsifiers,(north american edition 1979);schwartz,et al.;surface active agents,their chemistry and technology,new york:interscience publishers,1949;1964年11月3日颁布的hilfer的3,155,591号美国专利;1975年12月30日颁布的laughlin等人的3,929,678号美国专利;美国专利1976年5月25日颁布的bailey等人的3,959,461号;以及1983年6月7日颁布的bolich,jr.的4,387,090号美国专利,。
76.在一些实施例中,可用于本文的含季铵阳离子表面活性剂材料是具有以下通式的那些:
[0077][0078]
其中r
1-r4各自独立地为具有约1至约22个碳原子的脂肪族基团或具有约1至约22
个碳原子的芳族、烷氧基、聚氧化烯、烷基酰胺基、羟烷基、芳基或烷芳基;x是成盐阴离子,例如选自卤素(例如氯离子、溴离子)、乙酸根、柠檬酸根、乳酸根、乙醇酸根、硝酸磷酸根、硫酸根和烷基硫酸根的阴离子。在一些实施例中,脂族基团除了碳和氢原子之外还可以包括醚键和其他基团,例如氨基。在一些实施例中,较长链的脂肪族基团,例如约12个或更多碳的那些,可以是饱和的或不饱和的。在一些实施例中,阳离子表面活性剂是单长链(例如单c
12
至c
22
、或c
12
至c
18
)双短链(例如c1至c3烷基)季铵盐。
[0079]
在一些实施例中,伯、仲和叔脂肪胺的盐也是合适的阳离子表面活性剂材料。在一些实施例中,此类胺的烷基具有约12至约22个碳原子并且可以是取代的或未取代的。此类胺包括但不限于硬脂酰氨基丙基二甲基胺、二乙基氨基乙基硬脂酰胺、二甲基硬脂胺、二甲基大豆胺、大豆胺、肉豆蔻胺、十三烷基胺、乙基硬脂胺、n-牛脂丙烷二胺、乙氧基化(与5摩尔环氧乙烷)硬脂胺、二羟乙基硬脂胺和花生基山嵛胺。合适的胺盐包括卤素、乙酸盐、磷酸盐、硝酸盐、柠檬酸盐、乳酸盐和烷基硫酸盐。这样的盐包括但不限于硬脂胺盐酸盐、大豆胺氯化物、硬脂胺甲酸盐、n-牛脂丙烷二胺二氯化物、硬脂酰胺丙基二甲胺柠檬酸盐、十六烷基三甲基氯化铵和二十六烷基二氯化铵。在一些实施例中,阳离子表面活性剂是十六烷基三甲基氯化铵、硬脂基三甲基氯化铵、十四烷基三甲基氯化铵、二十六烷基二甲基氯化铵、二椰油二甲基氯化铵及其混合物。在其他实施例中,阳离子表面活性剂是十六烷基三甲基氯化铵。
[0080]
在一些实施例中,表面活性剂是非离子表面活性剂。合适的非离子表面活性剂包括c
8-c
30
醇与糖或淀粉聚合物的缩合产物。这些化合物可由式(s)
n-o-r表示,其中s是糖部分,例如葡萄糖、果糖、甘露糖和半乳糖;n为约1至约1000的整数,且r为c
8-c
30
烷基。可衍生r基团的合适c
8-c
30
醇的实例包括癸醇、鲸蜡醇、硬脂醇、月桂醇、肉豆蔻醇、油醇等。这种表面活性剂的合适实例包括癸基聚葡糖苷和月桂基聚葡糖苷。
[0081]
其他合适的非离子表面活性剂包括烯化氧与脂肪酸的缩合产物(即脂肪酸的烯化氧酯)。这些材料具有通式rco(x)noh,其中r是c
10-c
30
烷基,x是-och2ch
2-(衍生自环氧乙烷)或-och2chch
3-(衍生自环氧丙烷),其中n是约1至约200的整数。
[0082]
其他合适的非离子表面活性剂是烯化氧与脂肪酸的缩合产物(即脂肪酸的烯化氧二酯),具有式rco(x)noocr,其中r是c
10-c
30
烷基,x是-och2ch
2-(衍生自环氧乙烷)或-och2chch
3-(衍生自环氧丙烷),其中n是约1至约200的整数。还有其他非离子表面活性剂是环氧烷与脂肪醇的缩合产物(即环氧烷醚),具有通式r(x)nor'的脂肪醇),其中r是c
10-c
30
烷基,其中n是约1至约200的整数,并且r'是h或c
10-c
30
烷基。
[0083]
其他的非离子表面活性剂是具有式rco(x)nor'的化合物,其中r和r'是c
10-c
30
烷基,x是-och2ch
2-(衍生自环氧乙烷)或-och2chch
3-(衍生自环氧丙烷),n为约1至约200的整数。衍生自环氧烷的非离子表面活性剂的实例包括ceteth-1、ceteth-2、ceteth-6、ceteth-10、ceteth-12、ceteraeth-2、ceteareth6、ceteareth-10、ceteareth-12、steareth-1、steareth-2、steareth-6、steareth-10、steareth-12、peg-2硬脂酸酯、peg4硬脂酸酯、peg6硬脂酸酯、peg-10硬脂酸酯、peg-12硬脂酸酯、peg-20硬脂酸甘油酯、peg-80牛油酸甘油酯、ppg-10硬脂酸甘油酯、peg-30椰油酸甘油酯、peg-80椰油酸甘油酯、peg-200牛油酸甘油酯、peg-8二月桂酸酯、peg-10二硬脂酸酯及其混合物。其他有用的非离子表面活性剂包括例如在美国专利号2,965,576、2,703,798和1,985,424中公开的多羟基脂肪酸酰胺,通过引用将
这些专利并入本文。
[0084]
表面活性剂的非限制性实例包括tomadol 1200(air products)、tomadol 900(air products)、tomadol 91-8(air products)、tomadol 1-9(air products)、tergitol 15-s-9(sigma)、tergitol 15-s-12(sigma)、masurf nrw-n(pilot chemical)、bio-soft n91-6(stepan)和brij-35(聚乙二醇十二烷基醚)(sigma)。
[0085]
在一些实施例中、表面活性剂选自聚羟乙基烷氧基环氧烷、聚氧乙烯-聚氧丙烯嵌段共聚物、醚化聚氧乙烯-聚氧丙烯嵌段共聚物、改性烷基化多元醇、改性/甲基封端嵌段共聚物、非离子型多元醇、非离子表面活性剂、烷氧基化多元醇、烷基多苷、葡糖醚、烷氧基化醇、醇乙氧基化物、聚氧乙烯、阴离子共混物、环氧乙烷、壬基酚聚氧乙烯醚、月桂基聚醚硫酸钠、月桂基聚醚硫酸酯、月桂基聚醚硫酸铵、tea月桂基硫酸盐、二乙基己基钠磺基琥珀酸盐、月桂酰肌氨酸钠、硬脂酸钠、烯烃磺酸钠、月桂基醚磺基琥珀酸二钠、油胺磺基琥珀酸二钠、二辛基磺基琥珀酸钠椰油基羟乙基磺酸钠、辛酰羟乙基磺酸钠、己酰羟乙基磺酸钠、月桂酰羟乙基磺酸钠、棕榈酰羟乙基磺酸钠、丙烯酸酯/硬脂酸-羟乙基磺酸钠共聚物、辛酸铵leth硫酸盐、ammonium pareth-25硫酸盐、ammonium myreth硫酸盐、ceteareth-20、椰油酰胺丙基甜菜碱、disteareth-75ipdi、-100ipdi、乳化蜡nf、isosteareth-20、steareth
–
2,-4,10,16,-20,21、isosteareth-2,-10,-20、月桂醇聚醚硫酸镁、oleth硫酸镁、聚乙二醇、peg-20、peg-40、苯氧乙醇、聚氧乙烯、polysorbate-20,-40,-60,-80、steareth-2,-4,-10,-16,-20,-21、椰油醇硫酸钠、十二烷基醚硫酸钠、醇醚硫酸钠、月桂基聚醚硫酸钠、丁香醚硫酸钠、十三烷基硫酸钠、椰油醇硫酸锌、2-十二烷基苯磺酸、4-十二烷基苯磺酸、烷基苯磺酸盐、葡萄糖庚酸盐、葡萄糖庚酸钠、葡萄糖庚酸钾、葡萄糖庚酸钙、葡萄糖庚酸镁、葡萄糖庚酸硼、葡萄糖庚酸氯、葡萄糖庚酸铜、葡萄糖庚酸铁、葡萄糖庚酸锰、葡萄糖庚酸钼、甲庚酸锌、丙酸、b丁酸、戊酸、己酸、庚酸、辛酸、壬酸、癸酸、十一烷酸、十二烷酸、十三烷酸、十四烷酸、十五烷酸、十六烷酸、十七烷酸、十八烷酸、十九烷酸、二十烷酸、1,2,3-三羟基丙烷、二甘醇、烷基酚乙氧基化物、3-oxapentane-1,5-二醇、丙烷-1,2,3-三醇、烷基酚乙氧基化物、聚二甲基硅氧烷、1,2-丙二醇、二甲基聚硅氧烷、脂肪醇和丁氧基乙醇、丁氧基乙醇、磷酸酯表面活性剂、烷基芳基烷氧基化物、羟基羧酸、柠檬酸、酒石酸、葡萄糖酸、草酸、丙酸、磷酸酯、硫酸铵、乙氧基化表面活性剂、氢氧化钠、防腐蚀化合物、多价螯合剂、非离子和离子表面活性剂、羟基羧酸盐、聚丙烯酸酯、糖丙烯酸酯、氨基羧酸碱、磷酸盐、膦酸盐、六偏磷酸钠、多磷酸钠、三聚磷酸钠、三偏磷酸钠、焦磷酸钠、磷酸氨基多羧酸盐、氨基多羧酸盐、edtmp、detmp、atmp、hedp、dtpmp、聚醚-聚甲基硅氧烷共聚物、乙氧基化烷基磷酸酯、c
16-c
28
链烷酸酯、石蜡基石油、农业石蜡油、链烷醇酰胺表面活性剂、烷基芳基聚乙氧基乙醇硫酸盐、烷基芳基聚氧乙二醇磷酸酯表面活性剂、磷酸酯表面活性剂、石油油、多元醇脂肪酸酯、甲基化种子油、石蜡油、羰基二酰胺聚氧烷基化二醇加合物、羰基二胺、聚氧乙烯-聚氧丙烯聚合物、甲基化植物油、玉米衍生表面活性剂、游离脂肪酸、异丙醛、烷基芳基聚氧乙烯二醇、硫酸氢、脂肪烃油、聚丙烯酸盐、聚硅氧烷聚醚共聚物、聚环氧烷改性聚二甲基硅氧烷、妥尔油脂肪酸、有机硅表面活性剂、聚亚烷基改性七甲基三硅氧烷、改性链烷酸酯、聚脂肪酸酯、碳酸盐、聚硅氧烷、柠檬烯、烯丙氧基聚乙二醇甲醚、植物油基础油、二甲基聚硅氧烷、矿物油、聚醚聚甲基硅氧烷共聚物、非离子碳水化合物表面活性剂、聚氧乙烯聚氧乙烯-聚氧丙二醇、单脲硫酸二氢盐、消泡剂、作物基弹性聚合物、二铵盐、以及它们的任何组合。
[0086]
在一些实施例中,表面活性剂是聚羟乙基烷氧基环氧烷。在一些实施例中,表面活性剂是聚氧乙烯-聚氧丙烯嵌段共聚物。在一些实施例中,表面活性剂是醚化的聚氧乙烯-聚氧丙烯嵌段共聚物。在一些实施例中,表面活性剂是改性烷基化多元醇。在一些实施例中,表面活性剂是改性的/甲基封端的嵌段共聚物。在一些实施例中,表面活性剂是非离子多元醇。在一些实施例中,表面活性剂是烷氧基化多元醇。在一些实施例中,表面活性剂是烷基多糖苷。在一些实施例中,表面活性剂是葡糖醚。在一些实施例中,表面活性剂是烷氧基化醇。在一些实施例中,表面活性剂是醇乙氧基化物。在一些实施例中,表面活性剂是聚氧乙烯。在一些实施例中,表面活性剂是阴离子共混物。
[0087]
给药途径和剂型
[0088]
可以通过任何常见途径向受试者施用根据本公开的制剂,只要靶组织可通过该途径获得。制剂可以方便地以剂量单位形式存在并且可以通过药学领域众所周知的任何方法制备。在一些实施例中,制剂通过使活性组分与液体载体或细碎的固体载体或两者均匀且紧密地结合,然后(如果需要)将产品成型为所需剂型来制备。当然,本领域技术人员将认识到活性成分(例如dhh-b)的含量足以产生所需的药理作用。
[0089]
在一些实施例中,本公开的dhh-b制剂可以以离散单元的形式提供,例如硬胶囊或软胶囊、片剂、锭剂或锭剂,每个都包含预定量的活性成分;以可分散的粉末或颗粒的形式;在水性液体或非水性液体中的溶液或悬浮液形式;以糖浆或酏剂的形式;或以水包油乳剂或油包水乳剂的形式。在其他实施例中,本公开的dhh-b制剂可以制备成例如用于口服给药或肠胃外给药(例如,静脉内、动脉内、腹膜内、经直肠、皮下、肌内、舌下、鼻内或经阴道给药)。其非限制性实例包括溶液、片剂、散剂、颗粒剂、胶囊剂、栓剂、喷雾剂、控释剂、混悬剂和饮料。
[0090]
例如,在固体剂型中,制剂可以与至少一种药学上可接受的赋形剂或载体例如柠檬酸钠或磷酸二钙和/或a)填充剂或增量剂例如淀粉、乳糖、蔗糖、葡萄糖、甘露醇、二元钙和硅酸,b)粘合剂例如微晶纤维素、羧甲基纤维素、藻酸盐、明胶、聚乙烯吡咯烷酮、蔗糖和阿拉伯胶,c)保湿剂例如甘油,d)崩解剂例如琼脂、碳酸钙、马铃薯或木薯淀粉、海藻酸、某些硅酸盐、交聚维酮和碳酸钠,e)溶液阻滞剂,例如石蜡,f)吸收促进剂,例如季铵化合物,g)润湿剂,例如,乙酰基醇和单硬脂酸甘油酯,h)吸收剂,例如高岭土和膨润土,i)润滑剂,例如滑石、硬脂酸钙、硬脂酸镁、固体聚乙二醇、钠脲基硫酸盐,和j)增溶剂或络合剂,例如环糊精及其混合物。
[0091]
口服剂型
[0092]
dhh-b制剂通常可以以离散单元的形式提供,例如硬胶囊或软胶囊、片剂、锭剂或锭剂,每一个都含有预定量的dhh-b,如本文所述;以可分散的粉末或颗粒的形式;在水性液体或非水性液体中的溶液或悬浮液形式;以糖浆或酏剂的形式;或以水包油乳剂或油包水乳剂的形式。
[0093]
在一些实施例中,用于口服给药的dhh-b液体剂型包括但不限于药学上可接受的乳剂、溶液剂、混悬剂、糖浆剂和酏剂。除了dhh-b,任何液体剂型都可以包含本领域常用的惰性稀释剂。例如,液体dhh-b制剂可以包括水、酒精、聚乙二醇醚或任何其他药学上可接受的溶剂。增溶剂(例如环糊精)和乳化剂,例如乙醇、异丙醇、碳酸乙酯、乙酸乙酯、苯甲醇、苯甲酸苄酯、丙二醇、1,3-丁二醇、二甲基甲酰胺、油类(特别是棉籽、花生、玉米、胚芽、橄榄、
蓖麻和芝麻油)、甘油、四氢糠醇、聚乙二醇和脱水山梨糖醇的脂肪酸酯,以及它们的混合物也可以存在于所公开的dhh-b制剂中。此外,口服dhh-b制剂可以包括佐剂,例如润湿剂、乳化剂和悬浮剂、甜味剂、调味剂和芳香剂。当配制成悬浮液时,所公开的dhh-b制剂包括dhh-活性剂和悬浮剂,例如乙氧基化异硬脂醇、聚氧乙烯山梨醇、山梨糖醇酯、微晶纤维素、偏氢氧化铝、膨润土、琼脂、黄蓍胶和其混合物。
[0094]
在一些实施例中,水性悬浮液包括在混合液(admixture)中dhh-b与适用于制造水性悬浮液的赋形剂的混合物。这样的赋形剂可以是(a)悬浮剂,例如羟乙基纤维素、羧甲基纤维素钠、甲基纤维素、羟丙基甲基纤维素、海藻酸钠、聚乙烯吡咯烷酮、黄蓍胶和阿拉伯树胶;(b)分散剂或润湿剂,可以是(b.1)天然存在的磷脂如卵磷脂,(b.2)环氧烷与脂肪酸的缩合产物,例如聚氧乙烯硬脂酸酯,(b.3)环氧乙烷与长链脂肪醇的缩合产物,例如十七亚乙基氧十六醇,(b.4)环氧乙烷与衍生自脂肪酸和己糖醇的偏酯例如聚氧乙烯山梨糖醇单油酸酯的缩合产物,或(b.5)环氧乙烷与衍生自脂肪酸和己糖醇酐的偏酯的缩合产物,例如聚氧乙烯脱水山梨糖醇单油酸酯。
[0095]
在一些实施例中,dhh-b水性混悬剂还可包含一种或多种防腐剂,例如对羟基苯甲酸乙酯或正丙酯;一种或多种着色剂;一种或多种调味剂;和一种或多种甜味剂,例如蔗糖或糖精。
[0096]
在一些实施例中,可以通过将dhh-b悬浮在植物油(例如花生油、橄榄油、芝麻油或椰子油)或矿物油(例如液体石蜡)中来配制dhh-b油性混悬剂。在一些实施例中,油性悬浮液可包含增稠剂,例如蜂蜡、硬石蜡或鲸蜡醇。在一些实施例中,可以添加甜味剂和调味剂以提供可口的口服制剂。
[0097]
在一些实施例中,dhh-b制剂可以包括至少一种抗氧化剂,用于增强药物的稳定性。抗氧化剂可以作为制剂的一部分或作为包装组分存在。抗氧化剂可以以有效延缓易受氧化的药物分解的量存在。在一些实施例中,dhh-b制剂中抗氧化剂的含量为dhh-b制剂总重量的约0.001至10。抗氧化剂的非限制性实例包括抗坏血酸及其盐、生育酚、亚硫酸盐如焦亚硫酸钠或亚硫酸钠、硫化钠、丁基化羟基茴香醚、丁基化羟基甲苯、抗坏血酸棕榈酸酯和没食子酸丙酯中的一种或多种。本领域技术人员将容易地认识到其他合适的抗氧化剂。
[0098]
在一些实施例中,dhh-b制剂可以包括乳化剂。乳化剂可以是本领域普通技术人员已知的任何乳化剂。在一些实施例中,乳化剂是含有聚氧乙烯嵌段的嵌段共聚物,即由重复的环氧乙烷部分组成的嵌段。这种类型的合适乳化剂是泊洛沙姆,即聚氧乙烯-聚氧丙烯嵌段共聚物,例如poloxamer 188。参见the handbook of pharmaceutical excipients,p.352,2nd edn.pharmaceutical press,london,1994,eds,wade and weller。
[0099]
在一些实施例中,乳化剂是磷乳化剂。这可以是衍生自大豆或鸡蛋的任何药学上可接受的材料,例如大豆或鸡蛋卵磷脂。鸡蛋卵磷脂,例如由lipoid(germany)提供的称为lipoid e80的材料是优选的,它包含磷脂酰胆碱和磷脂酰乙醇碱,然而也可以使用其他磷脂材料,包括磷脂-聚乙二醇(peg)缀合物(peg化磷脂)已被描述用于脂质体系统,例如在litzinger et al,biochembiophys acta,1190(1994)99-107中被描述的。
[0100]
适用于口服剂型的示例性磷脂包括:50pg;53mct;75sa、80;90g;90h;和90ng。适用于皮肤剂型的示例性磷脂包括:50pg;
50sa;75sa;80;80h;85g;90ng;90ng;90h;和100h。适用于肠胃外剂型的示例性磷脂包括:90g;和适用于肺部药物制剂的磷脂包括:90g;9.0h和
[0101]
在一些实施例中,乳化剂可包含多糖。多糖可以是直链或支链、硫酸化或非硫酸化的。在一些实施例中,组合物包含一种或多种称为“角叉菜胶”的直链硫酸化多糖。
[0102]
在一些实施例中,乳化剂是角叉菜胶,例如λ-角叉菜胶、κ-角叉菜胶、iota-角叉菜胶以及角叉菜胶的任何混合物中的一种或多种。角叉菜胶是从食用海藻中提取的线性硫酸化多糖家族,广泛用于食品工业。uspnf 23将角叉菜胶描述为通过用水或碱水溶液从红藻科(红海藻)的少数成员中提取和纯化获得的水胶体。它主要由半乳糖和3,6-脱水半乳糖共聚物的钾、钠、钙镁和铵硫酸酯组成。这些己糖在聚合物中的α-1,3和β-1,4位点交替连接。
[0103]
角叉菜胶根据硫酸根的位置和脱水半乳糖的存在分为三个家族。λ-角叉菜胶(λ-角叉菜胶)是一种非胶凝聚合物,含有约35%重量的硫酸酯,不含3,6-脱水半乳糖。ι-角叉菜胶(t-角叉菜胶)是一种胶凝聚合物,含有约32%重量的硫酸酯和约30%的3,6-脱水半乳糖。kappa角叉菜胶(κ-角叉菜胶)是一种强胶凝聚合物,具有允许胶凝的螺旋三级结构。它含有25%重量的硫酸酯和大约34%的3,6-脱水半乳糖。在三种角叉菜胶中,λ-角叉菜胶是唯一的非胶凝聚合物。
[0104]
在一些实施例中,乳化剂选自由甘油单酯、甘油二酯及其任何混合物组成的组。术语“甘油单酯”是指其中甘油部分通过酯键共价键合到脂肪酸链的分子。术语“甘油二酯”是指其中甘油部分通过酯键与两条脂肪酸链共价键合的分子。在一些实施例中,乳化剂包括甘油单酯和甘油二酯的混合物。在一些实施例中,乳化剂包括甘油单酯和甘油二酯的混合物以及角叉菜胶。
[0105]
在一些实施例中,乳化剂是卵磷脂(其是指存在于动植物组织中的由磷酸、胆碱、脂肪酸、甘油、糖脂、甘油三酯和磷脂(例如,磷脂酰胆碱、磷脂酰乙醇胺和磷脂酰肌醇))。在一些实施例中,甘油三酯包括植物油、鱼油、动物脂肪、氢化植物油、部分氢化植物油、中链和长链甘油三酯以及结构化甘油三酯。在一些实施例中,乳化剂可以是油,包括植物油,例如大豆油、橄榄油、棉籽油、花生油、芝麻油和蓖麻油,优选芝麻油和蓖麻油。
[0106]
在一些实施例中,乳化剂是聚氧乙烯脱水山梨醇的脂肪酸酯(例如,等)。
[0107]
在一些实施例中,dhh-b制剂可以以可分散的粉末和/或颗粒的形式提供,例如适合于制备水性悬浮液的那些。在一些实施例中,dhh-b以与分散剂或润湿剂、悬浮剂和一种或多种防腐剂的混合物形式提供。合适的分散剂或润湿剂和悬浮剂以本文已经描述的那些为例。也可以存在另外的赋形剂,例如上述那些甜味剂、调味剂和着色剂,包括本文所述的那些中的每一种。着色剂可用于对组合物进行颜色编码,例如以指示其中治疗剂的类型和剂量。着色剂也可用于区分包含在诸如胶囊的单位剂型中的多颗粒的不同部分。合适的着色剂包括但不限于一种或多种天然和/或人造着色剂,例如fd&c着色剂、天然果汁浓缩物、颜料(例如氧化钛、二氧化硅、氧化铁、氧化锌等)。
[0108]
本公开的dhh-b制剂也可以是水包油乳液的形式。在一些实施例中,油相可以是植物油例如橄榄油或花生油,或矿物油例如液体石蜡或其混合物。合适的乳化剂可以是(a)天然存在的树胶,例如阿拉伯树胶,(b)天然存在的磷脂,例如大豆和卵磷脂,(c)衍生自脂肪酸和己糖醇酐的酯或偏酯,例如脱水山梨糖醇单油酸酯,(d)所述偏酯与环氧乙烷的缩合产物,例如聚氧乙烯脱水山梨糖醇单油酸酯。乳液还可以含有甜味剂和调味剂。
[0109]
在一些实施例中,dhh-b制剂可以以糖浆剂的形式提供,酏剂可以与甜味剂一起配制,例如甘油、丙二醇、山梨糖醇或蔗糖。这样的制剂还可以包含防腐剂和调味剂和着色剂。
[0110]
在一些实施例中,适合口服给药的固体剂型包括胶囊剂、片剂、丸剂、散剂、口腔崩解片剂和颗粒剂。在一些实施例中,dhh-b固体剂型也可以配制成糖果、棒棒糖、糖锭等。在这样的固体剂型中,dhh-b可以与至少一种药学上可接受的赋形剂或载体(例如柠檬酸钠或磷酸二钙)和/或以下进行混合:a)填充剂或增量剂例如淀粉、乳糖、蔗糖、葡萄糖、甘露醇和硅酸,b)粘合剂,例如羧甲基纤维素、藻酸盐、明胶、聚乙烯吡咯烷酮、蔗糖和阿拉伯胶,c)保湿剂,例如甘油,d)崩解剂,例如琼脂、碳酸钙、马铃薯或木薯淀粉、海藻酸、某些硅酸盐和碳酸钠,e)溶液阻滞剂,例如石蜡,f)吸收促进剂,例如季铵化合物,g)润湿剂,例如,乙酰基醇和单硬脂酸甘油酯,h)吸收剂,例如高岭土和膨润土,以及i)润滑剂,例如滑石粉、硬脂酸钙、硬脂酸镁、固体聚乙二醇、十二烷基硫酸钠及其混合物。对于胶囊、片剂和丸剂,剂型还可以包含缓冲剂。
[0111]
下面提供了口服溶解片剂制剂的一个示例:
[0112][0113][0114]
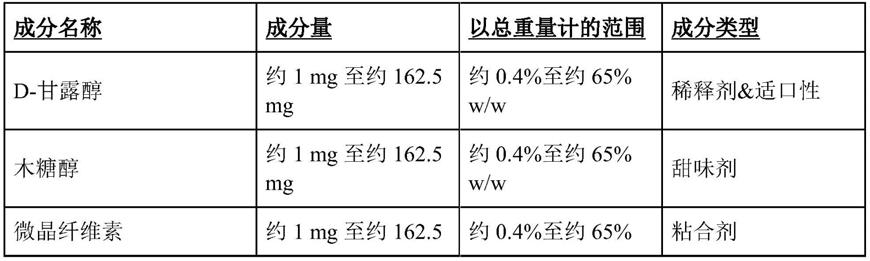
下面提供了口服片剂制剂的一个示例(例如用于人类受试者):
[0115][0116]
替代润滑剂包括三硬脂酸甘油酯、poem(tr-fb)和poem(tr-hb)。替代粘合剂包括甘露醇、葡萄糖、蔗糖、乙基纤维素、甲基纤维素、羟丙基甲基纤维素、羧甲基纤维素钠、聚乙烯吡咯烷酮。
[0117]
下面提供了口服片剂制剂的一个示例(例如用于犬科动物):
[0118]
成分名称成分量以总重量计的范围成分类型dhh-b约12mg约0.5至约1.0%w/w活性剂乳清干约1000mg约70至约80%w/w粘合剂微晶纤维素约200mg约10至约20%w/w粘合剂鸡肉或肝脏调味料达到配方规格约0.1至约10%w/w增味剂硬脂酸镁约6mg约0.5%w/w润滑剂
[0119]
在一些实施例中,片剂可具有约20牛顿至约150牛顿的硬度。在其他实施例中,片剂可具有约20牛顿至约120牛顿的硬度。在一些实施例中,片剂可具有约20牛顿至约150牛顿的硬度。在一些实施例中,片剂可具有约20牛顿至约10牛顿的硬度。在一些实施例中,片剂可具有约20牛顿至约80牛顿的硬度。在一些实施例中,片剂可具有约20牛顿至约60牛顿的硬度。在一些实施例中,片剂可具有约20牛顿至约150牛顿的硬度。
[0120]
在一些实施例中,用于口服的dhh-b制剂可以是硬明胶或hpmc胶囊的形式,其中活性成分与惰性固体稀释剂(例如预胶化淀粉、碳酸钙、磷酸钙或高岭土)混合,或通过颗粒配方分配。在其他实施例中,它们也可以是软明胶胶囊的形式,其中活性成分与水或油介质(例如花生油、液体石蜡、中链甘油三酯或橄榄油)混合。
[0121]
在一些实施例中,片剂、胶囊剂或丸剂可以是未包衣的,或者它们可以通过已知技术进行包衣以延迟在胃肠道中的崩解和吸收,从而在较长时间内提供延迟作用或持续作用。例如,可以使用诸如乙酸邻苯二甲酸纤维素或乙酸琥珀酸羟丙基纤维素之类的延时材料或诸如乙基纤维素或甲基丙烯酸铵共聚物(b型)之类的缓释材料。
[0122]
栓剂制剂
[0123]
本公开范围内的栓剂制剂通过将治疗有效量的dhh-b与为栓剂制剂提供长期稳定性的栓剂基质混合并通过任何公认的方法由混合物形成栓剂来制备。通常,此类栓剂基质是亲脂性的,更优选地,栓剂基质是非质子亲脂性基质,例如甘油三酯亲脂性基质或包含烃混合物的链烷烃基质。栓剂基质应具有确保栓剂在插入后的合理时间内熔化的熔化温度。通常,栓剂基质可包括熔点范围为约32℃至36℃的烃(石蜡)混合物或熔点范围为约32℃至36℃的脂肪酸甘油三酯混合物。烃的混合物可以优选地是熔点范围为约32至36℃的硬石蜡
(约50-60%)和液体石蜡(约40-50%)的混合物。栓剂的优选基质是witepsol s55、witepsol s58、这些产品的混合物,或者两者之一或两者与witepsol w35和/或witepsol h15的混合物。栓剂基质witepsol为甘油单酯、甘油二酯和甘油三酯的混合物,它们是源自棕榈籽油(例如椰子油)的植物衍生脂肪酸混合物的甘油酯。
[0124]
在一些实施例中,栓剂基质具有常规制剂并且可以包含可可脂、甘油明胶、氢化植物油、各种分子量的聚乙二醇的混合物、聚乙二醇脂肪酸酯以及甘油单酯、甘油二酯、和甘油三酯的混合物,它们是植物来源的脂肪酸混合物的甘油酯,例如衍生自棕榈仁油(如椰子油和棕榈仁油),表面活性剂含量低于polysorbate 80或cetomacrogol1000的0.5%。dhh-b栓剂本公开的制剂还可以包括其他常规成分,例如用于在栓剂/水基乳液中提供约4至约8.5的ph胺中和剂,以及溶解水胶体(例如聚丙烯酸)。
[0125]
任何甘油酯,包括甘油三酯、甘油二酯和/或甘油单酯都可以用于本公开的dhh-b制剂中。在一些实施例中,甘油三酯是lll、oll、ool、ooo、pll、pol、poo或sol中的一种。在一个实施例中,甘油三酯还可以包括ssl、sls、lls、lsl、mml、mlm、mml、llm、ssm、sms、mmm、sss和lll。可以使用长链、中链、短链和混合长度链甘油三酯。甘油三酯还包括包含任何已知脂肪酸或任何其他较短链饱和或不饱和酸的残基的任何甘油三酯。脂肪酸包括肉豆蔻油酸、棕榈油酸、皂角酸、油酸、反油酸、异油酸、亚油酸、亚油酸、α-亚麻酸、花生四烯酸、二十碳五烯酸、芥酸、二十二碳六烯酸、辛酸、癸酸、月桂酸、肉豆蔻酸、棕榈酸、硬脂酸、花生酸、山嵛酸、二十烷酸和/或蜡酸。虽然脂肪酸主要作为甘油三酯、甘油二酯或甘油单酯的残基部分存在于本文所述的制剂中,但独立的脂肪酸也可以是制剂的一部分。
[0126]
下面提供了dhh-b栓剂制剂的一个示例:
[0127][0128]
局部给药
[0129]
用于局部给药的剂型包括但不限于软膏、乳膏、乳剂、洗剂、凝胶、防晒剂和有利于渗透到表皮内的试剂。本领域技术人员已知的各种添加剂可以包括在本公开的局部制剂中。添加剂的实例包括但不限于增溶剂、皮肤渗透促进剂、防腐剂(例如抗氧化剂)、保湿剂、胶凝剂、缓冲剂、表面活性剂、乳化剂、润肤剂、增稠剂、稳定剂、保湿剂、分散剂和药物载体。
保湿剂的示例包括荷荷巴油和月见草油。
[0130]
合适的皮肤渗透促进剂在本领域是众所周知的并且包括低级烷醇,例如甲醇乙醇和2-丙醇;烷基甲基亚砜,例如二甲基亚砜(dmso)、癸基甲基亚砜(c10 mso)和十四烷基甲基亚砜;吡咯烷酮,尿素;n,n-二乙基间甲苯甲酰胺;c
2-c6烷二醇;二甲基甲酰胺(dmf)、n,n-二甲基乙酰胺(dma)和四氢糠醇。其他合适的渗透促进剂可以包括脂肪酸,例如油酸、月桂酸、癸酸、肉豆蔻酸、棕榈酸、硬脂酸、亚油酸、亚麻酸、二癸酸、斜酸、单油酸、二月桂酸、辛酸、花生四烯酸、甘油1-单癸酸酯、甘油单酯和甘油二酯及其生理学上可接受的盐。
[0131]
增溶剂的实例包括但不限于亲水性醚,例如二甘醇单乙醚(乙氧基二甘醇,可作为商购)和二甘醇单乙醚油酸酯(可作为商购);聚氧35蓖麻油、聚氧40氢化蓖麻油、聚乙二醇(peg),特别是低分子量peg,例如peg 300和peg 400,以及聚乙二醇衍生物,例如peg-8辛酸/癸酸甘油酯(可作为商购获得);烷基甲基亚砜,例如dmso;吡咯烷酮、dma及其混合物。
[0132]
在一些实施例中,dhh-b局部制剂还可以包括一种或多种润湿剂。有用的润湿剂包括例如但不限于明胶、酪蛋白、卵磷脂(磷脂)、阿拉伯树胶、胆固醇、西黄蓍胶、硬脂酸、苯扎氯铵、硬脂酸钙、单硬脂酸甘油酯、鲸蜡硬脂醇、西多聚醇乳化蜡、脱水山梨糖醇酯、聚氧乙烯烷基醚(例如聚乙二醇醚,例如聚乙二醇1000)、聚氧乙烯蓖麻油衍生物、聚氧乙烯脱水山梨糖醇脂肪酸酯或聚山梨醇酯(例如,)、聚乙二醇、聚氧乙烯硬脂酸酯、磷酸盐、十二烷基硫酸钠、泊洛沙姆、十二烷基硫酸钠,羧甲基纤维素钙、羧甲基纤维素钠、甲基纤维素、羟乙基纤维素、羟丙基纤维素、羟丙基甲基纤维素邻苯二甲酸酯、非晶纤维素、硅酸铝镁、三乙醇胺、聚乙烯醇和聚乙烯吡咯烷酮(或pvp)。tyloxapol(烷基芳基聚醚醇类型的非离子液体聚合物,也称为superinone或triton)是另一种有用的润湿剂,其与其他此类材料的组合对于本领域普通技术人员是已知的。
[0133]
下面提供了dhh-b局部制剂的一个示例:
[0134][0135]
肠胃外制剂
[0136]
用于肠胃外给药的dhh-b制剂包括水性和非水性无菌注射溶液,其可以含有抗氧化剂、缓冲剂、抑菌剂和使制剂与预期接受者的血液等渗的溶质。用于肠胃外给药的制剂还包括水性和非水性无菌混悬剂,其可以包括助悬剂和增稠剂。制剂可以存在于单位剂量或多剂量容器中,例如密封的安瓿和小瓶中,并且可以在使用前储存在冷冻干燥(冻干)条件
下,仅需要添加无菌液体载体,例如盐水、磷酸盐-缓冲盐水(pbs)等。临时注射溶液和悬浮液可以由下述种类的无菌粉末制备。
[0137]
下面提供了可注射制剂的一个示例:
[0138]
1升制剂:
[0139]
25,000mg/l=25mg/ml dhh-b
[0140][0141]
固体和液体食品
[0142]
可以将有效量的任何一种dhh-b制剂添加到基本上不含二氢和厚朴酚或其衍生物或类似物的任意食品或饮料产品或功能性食品中。因此,可以将本公开的任何一种dhh-b制剂制备成食品或饮料产品或功能性食品的形式。食品或饮料产品和功能性食品的示例包括但不限于糖果、蒸煮袋食品、果汁、茶和乳制品。另外,在饮食品或功能性食品中,可以根据需要添加甜味剂、调味剂、乳化剂、悬浮剂、防腐剂等。此外,本发明的抗焦虑组合物可用作食品添加剂。
[0143]
根据本公开的食品、膳食组合物或补充剂是包含与食品或膳食补充剂组合物混合的本公开的天然产物组合物的任何可摄取制剂。食品可以干燥、煮熟、煮沸、冻干或烘烤。食物组合物或食物产品可以包括烘焙产品,包括但不限于面包、糕点、核仁巧克力饼、蛋糕、馅饼、甜甜圈、薄脆饼干和松饼。食物组合物或食物产品可以包括乳制品,包括但不限于牛奶、发酵乳、凝乳、乳清、酸奶、奶油、奶酪、黄油、澄清黄油、酥油和冰淇淋。食物组合物或食物产品可以包含坚果酱或种子酱,包括但不限于花生酱、杏仁酱、腰果酱、榛子酱、澳洲坚果酱、山核桃酱、开心果酱、核桃酱、南瓜籽酱、芝麻种子黄油、大豆黄油和葵花籽黄油。食物组合物或食物产品可以包含油(例如,食用油),包括但不限于橄榄油、椰子油、植物油、菜籽油、玉米油、花生油、葵花籽油、杏仁油、鳄梨油、米糠油、棉籽油、亚麻籽油、亚麻籽油、葡萄籽油、大麻油、芥末油、澳洲坚果油、棕榈油、茶籽油、核桃油、人造黄油、猪油、黄油、澄清黄油、酥油或牛油。食物组合物或食物产品可以包括运动食物产品,例如能量凝胶、运动饮料、能量粉、能量棒、能量注射剂、蛋白质粉末和蛋白质饮料(例如蛋白质奶昔)。食物组合物或食物产品可以包括饮料,包括但不限于水、电解质饮料、苏打水、椰子水、茶(例如jun茶、红茶、绿茶、白茶、凉茶)、咖啡、软饮料、酒精饮料(例如鸡尾酒、烈酒、烈酒、啤酒、葡萄酒、麦芽饮料)、水、果汁(例如苹果汁、橙汁、番茄汁、蔬菜汁、蔓越莓汁)、运动饮料、电解质-浓缩水、维生素强化水、牛奶(例如乳基奶(dairy-based milk)、椰奶、杏仁奶、豆奶、大麻奶、米浆、燕麦奶、腰果奶、榛子奶)和酸奶。
[0144]
食物组合物或食物产品可包括在明胶基产品(例如)或明胶基甜点中的本文公开的天然产品组合物。在一些实施例中,食物组合物或食物产品包含天然产品组合物和胶凝剂。胶凝剂的合适实例包括角叉菜胶、琼脂、海藻酸钠、结冷胶、黄原胶、羧甲基纤维素钠、瓜尔胶、大豆蛋白和结晶纤维素。食品组合物或食品中所含的胶凝剂的量不受限制,
只要获得本发明的效果即可。食品组合物中胶凝剂的比例例如为食品组合物或食品产品总重量的约0.5至约3。不希望受任何特定理论的束缚,据信所含胶凝剂的量影响塑炼中的硬度。如果胶凝剂的量按食品组合物或食品产品的总重量计小于约0.5,则食品组合物或食品产品趋于变得过软并且不能达到适合咀嚼的硬度。另一方面,如果该量按食品组合物或食品产品的总重量计大于约3,则食品组合物或食品往往不能达到可以进行咀嚼的硬度,即使该数量的咀嚼次数增加。
[0145]
下面提供了dhh-b液体或饮料制剂的一个示例:
[0146][0147][0148]
给药和给药时间表
[0149]
普通技术人员将理解,在本公开的方法中使用的任何制剂中dhh-b的有效量可以凭经验确定。应当理解,当施用于受试者(人或兽药的)时,本公开的制剂的总每日使用量将由主治医师或其他医学专业人员在合理的医学判断范围内决定。任何受试者的具体治疗有效剂量水平将取决于多种因素:要达到的反应的类型和程度;所用特定组合物的活性;患者的年龄、体重、一般健康状况、性别和饮食;治疗的持续时间;患者的严重程度;与本公开的方法组合或同时使用的药物;以及医学领域中众所周知的类似因素。
[0150]
根据需要,这样的剂量可以分几次给药,例如2次或3次。此外,本公开的任何dhh-b制剂可以与另一种抗焦虑剂组合施用于患者。
[0151]
此外,可以将有效量的本公开的任何dhh-b制剂添加到用于家畜动物(例如马、牛或猪)或宠物动物(例如猫或狗)的基本上不含类胡萝卜素的任何形式的饲料中。因此,本公开的任何dhh-b制剂可以以饲料的形式制备。动物的焦虑症可以通过摄入这种饲料来预防
或治疗。因此,这种形式的饲料对于动物饲养是有效的。
[0152]
在一些实施例中,任何dhh-b制剂每天施用一次。在其他实施例中,任何dhh-b制剂每天两次施用一次。在其他实施例中,任何dhh-b制剂每天至少施用3次。在一些实施例中,任何dhh-b制剂可以每12小时施用。在其他实施例中,任何dhh-b制剂可以每8小时施用。在其他实施例中,任何dhh-b制剂可以每4小时施用。在更进一步的实施例中,任何dhh-b制剂可以根据需要施用,但其中24小时期间的给药次数不超过每种活性成分的预定给药次数或预定量。在一些实施例中,任何dhh-b制剂与食物一起施用。在其他实施例中,任何dhh-b制剂在禁食状态下给药。
[0153]
本文所述的任何dhh-b制剂可以以单位剂型提供。单位剂量可以是每小时剂量。单位剂量可以是日剂量。单位剂量可为有需要的受试者提供一种或多种组合物的约1/24、1/12、1/8、1/6、1/4、1/3、1/2或全部每日剂量。如本文所述,单位剂量可采取包装用于一次性消费或给药的片剂、凝胶、液体、食品、食品棒、限定体积的液体容器或本文所述的其他形式。
[0154]
治疗方法
[0155]
在某些实施例中,本公开涉及一种降低由焦虑症引起的焦虑的方法,所述焦虑症例如伴有或不伴有广场恐惧症的恐慌症,没有恐慌症病史的广场恐怖症,动物恐惧症和包括社交恐惧症的其他恐惧症,强迫症、应激障碍(包括创伤后和急性应激障碍),以及全身性或物质诱发的焦虑症;神经症;抽搐;偏头痛;抑郁或双相情感障碍,例如单发或复发性重度抑郁障碍、心境恶劣障碍、双相i和双相ii躁狂障碍和循环性障碍;精神疾病,包括精神分裂症;脑缺血引起的神经变性;注意缺陷多动障碍;抽动秽语综合征;言语障碍,包括口吃;和昼夜节律紊乱,例如在遭受时差或轮班工作影响的受试者中的。
[0156]
在一些实施例中,可以将任何dhh-b制剂施用于受试者以治疗焦虑和相关病症,包括改善焦虑和相关症状。在一些实施例中,本公开涉及用于治疗和/或预防焦虑的方法,包括单独或与药学上可接受的载体或赋形剂组合施用治疗有效量的dhh-b。在一些实施例中,该方法包括施用本文所述的任何dhh-b制剂。在一些实施例中,该方法包括施用如本文所指的dhh-b以及药学上可接受的赋形剂、载体和/或添加剂。在一些实施例中,该方法包括施用嵌入食物组合物或食物产品中的本文公开的任何dhh-b制剂的dhh-bor。
[0157]
在一些实施例中,本文公开的任何dhh-b制剂可以在联合疗法中施用,即,以单一或单独的剂型同时或以彼此间隔数小时或数天的单独剂型施用。用于治疗焦虑症的此类联合疗法中的化合物/药物的实例包括但不限于西酞普兰、度洛西汀、依他普仑、氟西汀、氟伏沙明、帕罗西汀、舍曲林、曲唑酮、文拉法辛、氯米帕明、地西帕明、多塞平、丙咪嗪、异卡波肼、苯乙肼、司来吉兰、反苯环丙胺、阿普唑仑、氯氮卓、氯硝西泮、地西泮、劳拉西泮、奥沙西泮、双丙戊酸钠、加巴喷丁、普瑞巴林、阿替洛尔、纳多洛尔、普萘洛尔、莫林酮、奥氮平、喹硫平和利培酮。在一些实施例中,本文公开的组合物可以在联合疗法中施用,即,以单一剂型或单独剂型同时施用,或彼此在数小时或数天内以单独剂型施用。用于治疗抑郁症的此类联合疗法中的化合物/药物的示例包括但不限于选择性血清素再摄取抑制剂(ssri)、血清素和去甲肾上腺素再摄取抑制剂(snri)、三环抗抑郁药(tca)、四环抗抑郁药、多巴胺再摄取阻滞剂、5-ht1a受体拮抗剂、5-ht2受体拮抗剂、5-ht3受体拮抗剂、单胺氧化酶抑制剂(maoi)和去甲肾上腺素能拮抗剂。抗抑郁药的具体实例包括但不限于去甲文拉法辛、度洛
西汀、左旋米那普仑、文拉法辛、阿米替林、阿莫沙平、氯米帕明、地昔帕明、多塞平、丙咪嗪、去甲替林、普罗替林、曲米帕明、安非他酮、马普替林、维拉佐酮、奈法唑酮、曲唑酮、沃替西汀、异卡波肼、苯乙肼、司来吉兰、反苯环丙胺和米氮平。
[0158]
在一些实施例中,本文所述的任何dhh-b制剂可以施用于受试者,以治疗颤抖障碍、原发性颤抖障碍、帕金森氏颤抖、张力障碍性颤抖、小脑颤抖、心因性颤抖、直立性颤抖、生理性颤抖和类似。在一些实施例中,本公开涉及用于治疗颤抖障碍、特发性颤抖障碍、帕金森氏颤抖、张力障碍性颤抖、小脑性颤抖、心因性颤抖、直立性颤抖、生理性颤抖等的方法,包括单独或与药学上可接受的载体或赋形剂组合施用治疗有效量dhh-b。在一些实施例中,该方法包括施用本文所述的任何dhh-b制剂。在一些实施例中,该方法包括施用如本文所指的dhh-b以及药学上可接受的赋形剂、载体和/或添加剂。在一些实施例中,该方法包括施用嵌入食物组合物或食物产品中的dhh-b或本文公开的任何dhh-b制剂。
[0159]
稳定性
[0160]
在一些实施例中,本公开的任何dhh-b制剂的单独组分不会降解到不可接受的程度,使得最终产品具有至少约2年的保质期。如前所述,这意味着剂型中的活性成分在剂型的期望(例如标记的)保质期(例如至少为剂型生产日期后约2年)期间保持其在剂量中的初始量的90%至110%。在一些实施例中,本文所述的组合物可具有至少约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、110、120、130、140、150、160、170、180、190、200、210、240、270、300、330或360天的保质期。在一些情况下,本文所述的组合物可具有至少约1、2、3、4或5年的保质期。
[0161]
示例
[0162]
示例1-二氢和厚朴酚-b-环糊精络合过程:
[0163]
向250ml烧杯中加入90ml去离子水。将烧杯放在搅拌板上并加热至70℃。将磁力搅拌棒放入烧杯中并设定在水中产生涡流的速度。向水中加入45g羟丙基-β环糊精(hpbcd)。环糊精迅速溶解。向水溶液中缓慢加入5g二氢和厚朴酚-b。
[0164]
示例2-水溶性片剂制剂
[0165]
对于水溶性片剂成分的制造,将溶液转移到真空烘箱中并在真空下加热过夜以从二氢和厚朴酚环糊精复合物中除去水。这种材料已用于饮料、片剂和口服溶解片剂(odt)。
[0166]
250mg口服溶解片剂示例
[0167]
75mg hpbcd复合的dhh-b
[0168]
35mg d-甘露醇
[0169]
35mg木糖醇
[0170]
35mg微晶纤维素
[0171]
35mg交聚维酮
[0172]
35mg无水磷酸氢钙
[0173]
示例3-栓剂制剂
[0174]
基础材料在50℃下熔化以形成均匀的脂质混合物。通过机械混合将二氢和厚朴酚-b(15mg)溶解在该混合物中。将得到的熔融sedds共混物倒入1g容量的栓剂模具中。让栓剂在室温下放置5-10分钟,然后在10℃下进一步硬化30分钟。评估最终sedds产品的外观、
室温下的稳定性以及从模具中取出的难易程度。
[0175]
1,000mg栓剂实施例
[0176]
15mg dhh-b
[0177]
110mg油混合物
[0178]
800mg peg-32混合物
[0179]
50mg二甘醇单乙醚
[0180]
示例4
–
液体或饮料制剂
[0181]
在250ml玻璃烧杯中加入9g d-ɑ-生育酚聚乙二醇琥珀酸酯(tpgs)。将搅拌棒添加到烧杯中,并将其放置在设定为60℃的加热搅拌板上,以缓慢的搅拌速度进行搅拌。在tpgs熔融液化后,加入1.5g二氢和厚朴酚-b。搅拌10分钟后,加入150ml70℃的水并增加搅拌速度。将该溶液再加热15分钟。让溶液静置过夜,如果需要,加入0.5%聚山梨醇酯80以使溶液澄清。将溶液进一步稀释成合适的配方。
[0182]
制剂的示例包括浓度为每毫升7.5mg dhh-b的30ml酊剂瓶到每份15mg的12盎司饮料。
[0183]
15mg液体示例
[0184]
15mg dhh-b
[0185]
90mg tpgs
[0186]
50ml水
[0187]
100mg粉状樱桃调味剂
[0188]
示例5-透皮制剂
[0189]
二氢和厚朴酚-b和润湿剂丙二醇首先被掺入到磷脂基质中。然后将制剂与electronic mortar and pestle(emp)(technology,e/s型号)在设置为7下混合3分钟,使用软膏磨(exakt technologies,inc.,50型号)剪切两次(一次设置为2,一次设置为1),并与emp重新混合(在设置为5下持续1分钟)以实现内容物均匀性。
[0190]
透皮示例
[0191]
15mg dhh-b
[0192]
885mg丙二醇
[0193]
49ml plo-凝胶
[0194]
示例6
–
可注射制剂
[0195]
向1500ml erlenmeyer烧瓶中加入450ml去离子水。将烧杯放在搅拌板上并加热至70℃。将磁力搅拌棒放入烧杯中并设置为在水中产生涡流的速度。向水中加入225g羟丙基-β环糊精(hpbcd)。环糊精迅速溶解。向水溶液中缓慢加入25g二氢和厚朴酚-b。冷却至室温后,加入小于5.0%的苯甲醇。将该溶液的ph调节至7.10。使溶液达到足够量(qs)以使其达到1000ml。该溶液通过无菌0.22um过滤器过滤到单独的多用途无菌小瓶中。
[0196]
可注射示例
[0197]
75mg dhh-b
[0198]
675mg hpbcd
[0199]
3ml无菌水
[0200]
0.15ml苯甲醇
[0201]
在该示例中,可以为440kg纯种马注射2ml至4ml。5ml的体积适合紧张的马。10ml 25mg/ml的量不会引起任何不良事件。
[0202]
示例7-口服片剂制剂
[0203]
250mg口服片剂示例
[0204]
75mg hpbcd复合的dhh-b
[0205]
1.25mg硬脂酸镁
[0206]
162.5mg微晶纤维素
[0207]
尽管已经参考多个说明性实施例描述了本公开,但是应当理解,本领域技术人员可以设计出许多其他修改和实施例,这些修改和实施例将落入本公开原理的精神和范围内。更具体地,在前述公开、附图和所附权利要求的范围内,在不脱离本公开的精神的情况下,可以对主题组合布置的组成部分和/或布置进行合理的变化和修改。除了部件和/或布置的变化和修改之外,替代用途对于本领域技术人员来说也是显而易见的。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1