一种小儿用对乙酰氨基酚泡腾片及其制备工艺的制作方法
1.本发明涉及药物制剂技术领域,特别是涉及一种小儿用对乙酰氨基酚泡腾片及其制备工艺。
背景技术:
2.对乙酰氨基酚,通常为白色结晶性粉末,由对硝基酚钠经还原成对氨基酚,再酰化制得。它是最常用的非甾体抗炎解热镇痛药,解热作用与阿司匹林相似,是乙酰氨基类药物中最好的品种,特别适合于不能应用羧酸类药物的病人。此外,用于关节痛、神经痛、偏头痛、癌痛及手术后止痛等。
3.泡腾片是一种较新的药物剂型,与普通片剂不同,泡腾片利用有机酸和碱式碳酸 (氢)盐作为泡腾崩解剂,置入水中,即刻发生泡腾反应,生成并释放大量的二氧化碳气体,加速泡腾片的崩解和融化,有利于提高药物生物利用度,质量较好的口服泡腾片泡腾完毕后即为一杯酸甜可口的饮品,非常适用于小孩、老人和不能吞服的患者。
4.但是现有的泡腾片一般采用大量的单一的碱源与酸源反应,继而保证的二氧化碳的量,得到的泡腾颗粒的崩解速度较差。
5.将市场上对乙酰氨基泡腾片溶解在水、果汁、碳酸饮料、牛奶中,不能达到药物充分溶解,且难以保持药物稳定性,影响药效发挥。
技术实现要素:
6.针对现有技术中存在的缺陷或不足,本发明提供一种可充分溶解于水、果汁、碳酸饮料、牛奶中且可以长时间保证药物稳定性、适用于小孩、老人和不能吞服的患者的对乙酰氨基泡腾片及其制备工艺。
7.为了达到上述效果,本发明采用如下技术方案,本发明小儿用对乙酰氨基酚泡腾片的片芯组成按重量配比为:以10万片计,对乙酰氨基酚9 kg~11 kg,无水枸橼酸26.154 kg~31.966 kg,柠檬酸一钠8.721kg~10.659 kg,碳酸氢钠23.796 kg~29.084 kg,无水碳酸钠10.197 kg~12.463 kg,苯甲酸钠0.99 kg~1.21 kg,甘露醇4.5 kg~5.5 kg,甘氨酸4.5 kg~5.5 kg,聚乙二醇6000 2.07 kg~2.53 kg,二甲硅油0.072 kg~0.088 kg 。
8.作为一种优选方案,本发明所述对乙酰氨基酚10kg,无水枸橼酸29.06kg,柠檬酸一钠9.69kg,碳酸氢钠26.44kg,无水碳酸钠11.33kg,苯甲酸钠1.1kg,甘露醇5kg,甘氨酸5kg,聚乙二醇6000 2.3kg,二甲硅油0.08kg。
9.本发明小儿用对乙酰氨基酚泡腾片的制备工艺包括以下具体操作步骤:(1)原料粒度控制原料通过气流粉碎微粉化方式加工成200目;(2)称量按照相应的比例称取各物料,封口保存,以待备用;3)沸腾制粒
ꢀ
取无水枸橼酸、枸橼酸一钠、碳酸氢钠、无水碳酸钠和聚乙二醇6000放入沸腾干燥机内,控制沸腾干燥机流化床温度和混合时间,进行沸腾制粒。卸料,冷却至室温,过24目筛,封口保存,标记为制粒a物料,以待备用;4)预混合 将对乙酰氨基酚、苯甲酸钠、甘露醇、甘氨酸、二甲硅油放入混合机中,混合后过24目筛,封口,标记为混合b物料备用;5)总混合将上述制粒a物料与混合b物料按处方量放入混合机中,混合至均匀,过24目筛,封口待用;6)压片将混合后得到的物料通过压片机进行压片,用φ15mm圆形平冲压制;7)内包装按批次采用聚酯/铝/聚乙烯药品包装用复合膜包装或口服固体药用聚丙烯瓶包装;8)外包装、入库进行外包装后寄库,抽样进行全检,全检合格后入库。
10.作为一种优选方案,本发明所述步骤(3)沸腾制粒干燥机流化床温度和混合时间,沸腾温度控制在55℃-65℃之间,混合20分钟;其次,本发明所述步骤(4)混合机采用三维运动混合机,预混合转速为900r/min,混合时间为 30min;另外,本发明所述步骤(5)采用三维运动混合机,混合转数600r/min,混合时间30min;此外,本发明所述步骤(6)压片采用压片机用φ15mm圆形平冲压制,转数控制在14转/分~16转/分,压片开始,崩解时限≤5分钟,10片片重范围按
±
4%控制。
11.与现有技术相比,本发明具有如下显著性有益效果:本发明制备的所述小儿用对乙酰氨基酚泡腾片,将其投入水中时发生泡腾反应从而生成并释放大量的二氧化碳气体,促进制剂的崩解和融化,无粘冲现象,增加了对乙酰氨基酚药物溶解度,有助于药物吸收,有助于提高对乙酰氨基酚生物利用度且药效稳定;通过本工艺制备的对乙酰氨基酚泡腾片可以提高用药方便性和患者服药的依从性,有助于提高患者特别是儿童用药的依从性;经稳定性试验表明,按本发明方法制成的泡腾片质量稳定。
具体实施方式
12.以下将对本发明的优选实施例进行详细描述。按照常规条件,所举实施例仅是为了更好地对本发明的内容进行说明。但不应将此理解为本发明的内容仅限于所举实施例,凡基于本发明的上述内容对实施方案进行非本质的改进和调整,仍属于本发明的保护范围。
13.本发明小儿用对乙酰氨基酚泡腾片为了达到上述效果,本发明采用如下技术方案,本发明小儿用对乙酰氨基酚泡腾片的片芯组成按重量配比为:以10万片计,对乙酰氨基酚9 kg~11 kg,无水枸橼酸26.154 kg~31.966 kg,柠檬酸一钠8.721kg~10.659 kg,碳
酸氢钠23.796 kg~29.084 kg,无水碳酸钠10.197 kg~12.463 kg,苯甲酸钠0.99 kg~1.21 kg,甘露醇4.5 kg~5.5 kg,甘氨酸4.5 kg~5.5 kg,聚乙二醇6000 2.07 kg~2.53 kg,二甲硅油0.072 kg~0.088 kg 。
14.所述对乙酰氨基酚10 kg,无水枸橼酸29.06 kg,柠檬酸一钠9.69 kg,碳酸氢钠26.44 kg,无水碳酸钠11.33 kg,苯甲酸钠1.1 kg,甘露醇5 kg,甘氨酸5 kg,聚乙二醇6000 2.3 kg,二甲硅油0.08 kg。
15.本发明小儿用对乙酰氨基酚泡腾片的制备工艺包括以下具体操作步骤:1)原料粒度控制原料通过气流粉碎微粉化方式加工成200目;2)称量根据处方,按照相应的比例精确称取各物料,封口保存,以待备用;3)沸腾制粒 按比例称取无水枸橼酸、枸橼酸一钠、碳酸氢钠、无水碳酸钠和聚乙二醇6000放入沸腾干燥机内,控制沸腾干燥机流化床温度和混合时间,进行沸腾制粒。卸料,冷却至室温,过24目筛,封口保存,标记为制粒a物料,以待备用;4)预混合将对乙酰氨基酚、苯甲酸钠、甘露醇、甘氨酸、二甲硅油放入混合机中,混合后过24目筛,封口,标记为混合b物料备用;5)总混合将上述制粒a物料与混合b物料按处方量放入三维混合机中,混合至均匀,过24目筛,封口待用;6)压片将混合后得到的物料通过压片机进行压片,用φ15mm圆形平冲压制;7)内包装按批次采用聚酯/铝/聚乙烯药品包装用复合膜包装或口服固体药用聚丙烯瓶包装;8)外包装、入库进行外包装后寄库,抽样进行全检,全检合格后入库。
16.作为一种优选方案,本发明所述步骤(3)沸腾制粒干燥机流化床温度和混合时间,沸腾温度控制在55℃-65℃之间,混合20分钟;其次,本发明所述步骤(4)混合机采用三维运动混合机,预混合转速为900r/min,混合时间为 30min;另外,本发明所述步骤(5)采用三维运动混合机,混合转数600r/min,混合时间30min;此外,本发明所述步骤(6)压片采用压片机用φ15mm圆形平冲压制,转数控制在14转/分~16转/分,压片开始,崩解时限≤5分钟,10片片重范围按
±
4%控制。
17.实施例11)原料粒度控制原料通过气流粉碎微粉化方式加工成200目;
2)称量根据处方,按照相应的比例精确称取各物料,封口保存,以待备用;3)沸腾制粒 按比例称取无水枸橼酸29.06 kg、枸橼酸一钠9.69kg、碳酸氢钠26.44kg、无水碳酸钠11.33kg和聚乙二醇6000 2.3kg放入fl-60沸腾制粒干燥机内,控制fl-60沸腾制粒干燥机流化床温度和混合时间,沸腾温度控制在55℃,混合20分钟后停机出料进行沸腾制粒。卸料,冷却至室温,通过yk-160a摇摆制粒机用24目筛网整粒,标记为制粒a物料,封口保存,以待备用;4)预混合将对乙酰氨基酚10.00kg、苯甲酸钠1.10kg、甘露醇5.00kg、甘氨酸5.00kg和二甲硅油0.08kg按处方量放入gh-500三维混合机中,混合条件:900r/min,混合时间:30分钟。混合后通过yk-160a摇摆制粒机用24目筛网整粒,封口,标记为混合b物料备用;5)总混合将上述制粒a物料与混合b物料按处方量放入gh-500三维混合机中,混合至均匀,混合条件:600r/min,混合时间:30分钟,混合后通过yk-160a摇摆制粒机用24目筛网整粒,封口待用;6)压片安装相应的冲具(φ15mm平冲),调节压片机的压力,在片厚4.05
±
0.10毫米,硬度为5-10 kn范围内调整填充量,成型良好后,转数控制在14转/分~16转/分,调试压片开始,由中控员检查崩解时限≤5分钟,10片片重范围按
±
4%控制,各指标合格后,开始正式压片,操作员每隔1小时对片重进行抽检,并记录在批记录中;7)内包装按批次采用聚酯/铝/聚乙烯药品包装用复合膜包装或口服固体药用聚丙烯瓶包装。将dsl-160b自动双铝包装机升温至预热:100℃
±
5℃,加热a:165℃
±
5℃;加热b:165℃
±
5℃,调节裁切频率:25hz。然后调试批号打印位置,直至批号打印清晰、位置准确,板面整齐、热封良好(以双手不轻易撕开为准),设备调试结束后,打开加料器进行加料,操作过程中操作人员要注意观察药板有无缺药以及表面无折皱、复合情况是否良好;8)外包装、入库进行外包装后寄库,抽样进行全检,全检合格后入库。
18.实施例2:1)原料粒度控制原料通过气流粉碎微粉化方式加工成200目;2)称量根据处方,按照相应的比例精确称取各物料,封口保存,以待备用;3)沸腾制粒 按比例称取无水枸橼酸26.154 kg、枸橼酸一钠8.721 kg、碳酸氢钠23.796kg、无水碳酸钠10.197 kg和聚乙二醇6000 2.07 kg放入fl-60沸腾制粒干燥机内,控制fl-60沸腾制粒干燥机流化床温度和混合时间,沸腾温度控制在55℃,混合20分钟后停机出料进行沸腾制粒。卸料,冷却至室温,通过yk-160a摇摆制粒机用24目筛网整粒,标记为制粒a物料,
封口保存,以待备用;4)预混合 将对乙酰氨基酚9kg、苯甲酸钠0.99kg、甘露醇4.5kg、甘氨酸4.5kg和二甲硅油0.072kg按处方量放入gh-500三维混合机中,混合条件:900r/min,混合时间:30分钟。混合后通过yk-160a摇摆制粒机用24目筛网整粒,封口,标记为混合b物料备用;5)总混合将上述制粒a物料与混合b物料按处方量放入gh-500三维混合机中,混合至均匀,混合条件:600r/min,混合时间:30分钟,混合后通过yk-160a摇摆制粒机用24目筛网整粒,封口待用;6)压片安装相应的冲具(φ15mm平冲),调节压片机的压力,在片厚4.05
±
0.10毫米,硬度为5-10 kn范围内调整填充量,成型良好后,转数控制在14转/分~16转/分,调试压片开始,由中控员检查崩解时限≤5分钟,10片片重范围按
±
4%控制,各指标合格后,开始正式压片,操作员每隔1小时对片重进行抽检,并记录在批记录中;7)内包装按批次采用聚酯/铝/聚乙烯药品包装用复合膜包装或口服固体药用聚丙烯瓶包装。将dsl-160b自动双铝包装机升温至预热:100℃
±
5℃,加热a:165℃
±
5℃;加热b:165℃
±
5℃,调节裁切频率:25hz。然后调试批号打印位置,直至批号打印清晰、位置准确,板面整齐、热封良好(以双手不轻易撕开为准),设备调试结束后,打开加料器进行加料,操作过程中操作人员要注意观察药板有无缺药以及表面无折皱、复合情况是否良好;8)外包装、入库进行外包装后寄库,抽样进行全检,全检合格后入库。
19.实施例3:1)原料粒度控制原料通过气流粉碎微粉化方式加工成200目;2)称量根据处方,按照相应的比例精确称取各物料,封口保存,以待备用;3)沸腾制粒按比例称取无水枸橼酸31.966 kg、枸橼酸一钠10.659 kg、碳酸氢钠29.084kg、无水碳酸钠12.463 kg和聚乙二醇6000 2.53 kg放入fl-60沸腾制粒干燥机内,控制fl-60沸腾制粒干燥机流化床温度和混合时间,沸腾温度控制在55℃,混合20分钟后停机出料进行沸腾制粒。卸料,冷却至室温,通过yk-160a摇摆制粒机用24目筛网整粒,标记为制粒a物料,封口保存,以待备用;4)预混合 将对乙酰氨基酚11kg、苯甲酸钠1.21kg、甘露醇5.5kg、甘氨酸5.5kg和二甲硅油0.088kg按处方量放入gh-500三维混合机中,混合条件:900r/min,混合时间:30分钟。混合后通过yk-160a摇摆制粒机用24目筛网整粒,封口,标记为混合b物料备用;5)总混合将上述制粒a物料与混合b物料按处方量放入gh-500三维混合机中,混合至均匀,
混合条件:600r/min,混合时间:30分钟,混合后通过yk-160a摇摆制粒机用24目筛网整粒,封口待用;6)压片安装相应的冲具(φ15mm平冲),调节压片机的压力,在片厚4.05
±
0.10毫米,硬度为5-10 kn范围内调整填充量,成型良好后,转数控制在14转/分~16转/分,调试压片开始,由中控员检查崩解时限≤5分钟,10片片重范围按
±
4%控制,各指标合格后,开始正式压片,操作员每隔1小时对片重进行抽检,并记录在批记录中;7)内包装按批次采用聚酯/铝/聚乙烯药品包装用复合膜包装或口服固体药用聚丙烯瓶包装。将dsl-160b自动双铝包装机升温至预热:100℃
±
5℃,加热a:165℃
±
5℃;加热b:165℃
±
5℃,调节裁切频率:25hz。然后调试批号打印位置,直至批号打印清晰、位置准确,板面整齐、热封良好(以双手不轻易撕开为准),设备调试结束后,打开加料器进行加料,操作过程中操作人员要注意观察药板有无缺药以及表面无折皱、复合情况是否良好;8)外包装、入库进行外包装后寄库,抽样进行全检,全检合格后入库。
20.实施例4:泡腾崩解剂种类的考察本实验考察以l-(+)-酒石酸、无水枸橼酸和枸橼酸一钠为酸源,以碳酸氢钠、碳酸氢钾和无水碳酸钠为碱源,考察酸源、碱源的种类及用量的配比变化对制剂的成型性及泡腾过程的影响。考察指标:颗粒成型性、流动性、可压性、崩解时限、沉淀物等,见表1和表2。
21.表1.酸源、碱源的处方考察(1000片用量)处方号123456对乙酰氨基酚(g)100.0100.0100.0100.0100.0100.0碳酸氢钠(g)357.0——237.0——碳酸氢钾(g)—425.0——282.0—无水碳酸钠(g)——224.0——149.0枸橼酸一钠(g)——————无水枸橼酸(g)272.0272.0272.0———l-(+)-酒石酸(g)———211.0211.0211.0聚乙二醇6000(g)23.023.023.023.023.023.0甘露醇(g)50.050.050.050.050.050.0甘氨酸(g)50.050.050.050.050.050.0苯甲酸钠(g)11.011.011.011.011.011.0二甲硅油(g)0.80.80.80.80.80.8表2.酸源、碱源的考察结果
处方号123456制粒a物料颗粒成型性颗粒硬度适中、成型性好颗粒硬度适中、成型性好颗粒硬度适中、成型性好颗粒硬度适中、成型性好颗粒硬度适中、成型性好颗粒硬度适中、成型性好颗粒休止角(
°
)353435363434片剂情况不黏冲、无脱盖、无缺角、片面光洁,无花斑不黏冲、无脱盖、无缺角、片面光洁,无花斑不黏冲、无脱盖、无缺角、片面光洁,无花斑不黏冲、无脱盖、无缺角、片面光洁,无花斑不黏冲、无脱盖、无缺角、片面光洁,无花斑不黏冲、无脱盖、无缺角、片面光洁,无花斑硬度(kg)6.936.517.365.906.145.70崩解时限(秒)92.1562.2686.16482.15415.3665.48
泡腾后ph值5.755.705.735.775.715.80超声后ph值5.785.755.815.835.795.85沉淀物0.26%2.31%0.23%2.51%2.72%2.81%
结果表明,l-(+)-酒石酸晶型较大,硬度较高,不易快速溶解,采用l-(+)-酒石酸为酸源的泡腾效果不及无水枸橼酸和枸橼酸一钠,泡腾时间较长,导致不能有效崩解;碳酸氢钾为碱源的上浮时间较长,泡腾剧烈,但泡腾时间太短,导致主成分不能充分溶解,沉淀物较多;优选的泡腾崩解剂为无水碳酸钠或碳酸氢钠为碱源,无水枸橼酸或枸橼酸一钠为酸源。
22.实施例5:泡腾崩解剂单独使用和混合使用的考察泡腾崩解剂为无水碳酸钠或碳酸氢钠为碱源,无水枸橼酸或枸橼酸一钠为酸源;本实施例主要考察单独使碳酸氢钠作为碱源,无水枸橼酸作为酸源,还是无水碳酸钠和碳酸氢钠混合作为碱源,无水枸橼酸和枸橼酸一钠混合作为酸源的崩解效果,见表3。
23.表3.泡腾崩解剂单独使用和混合使用的处方考察(1000片用量)处方号12对乙酰氨基酚(g)100.0100.0碳酸氢钠(g)357.0264.4无水碳酸钠(g)—113.3枸橼酸一钠(g)—96.9无水枸橼酸(g)272.0290.6聚乙二醇6000(g)23.023.0甘露醇(g)50.050.0甘氨酸(g)50.050.0苯甲酸钠(g)11.011.0二甲硅油(g)0.80.8试验结果:混合使用能起到缓冲作用,对处方的稳定性较好,能有效避免空气湿度对处方稳定性的影响,故最终采用碳酸氢钠和无水碳酸钠为碱源,无水枸橼酸和枸橼酸一钠为酸源。
24.实施例6:泡腾崩解剂混合使用的用量考察,见表4。
25.表4.泡腾崩解剂用量考察表(1000片用量)处方号123456对乙酰氨基酚(g)100.0100.0100.0100.0100.0100.0无水枸橼酸(g)219.9290.6265.4290.6290.6290.6无水碳酸钠(g)11011011085.696.9107.5枸橼酸一钠(g)100100100124.6113.3102.7碳酸氢钠(g)335.1264.4289.6264.4264.4264.4聚乙二醇6000(g)23.023.023.023.023.023.0甘露醇(g)50.050.050.050.050.050.0甘氨酸(g)50.050.050.050.050.050.0苯甲酸钠(g)11.011.011.011.01111二甲硅油(g)0.80.80.80.80.80.8
ꢀ
试验结果:泡腾崩解剂:无水枸橼酸的用量为290.6g;碳酸氢钠的用量为264.4g ,泡腾稳定剂:枸橼酸一钠的用量为96.9g,无水碳酸钠的用量为113.3g,在以上处方条件下,生产出来的片子更加稳定,崩解时间以及ph值均适合。
26.实施例7:原料粒度对制剂的影响本品为泡腾制剂,原辅料的粒径对崩解时间及泡腾后剩余物的影响较大,现对100目的原料、150目原料和200目的原料制成的泡腾片剂的崩解时间、残渣量进行考察,结果见表5。
27.表5.原料粒度对制剂的影响原辅料粒度123原料粒度100目150目200目崩解时间(秒)86.2572.1249.32残渣量0.12%0.08%0.03%由结果可知,原料粒度对崩解时间及残渣量的影响较大,200目的原料崩解时间和残渣量最为理想,故后续购买的原料加工成200目。
28.实施例8: 对乙酰氨基酚泡腾片加速试验考察条件:温度40℃
±
2℃湿度rh75%
±
5%,结果见表6。
29.表6. 对乙酰氨基酚泡腾片加速试验
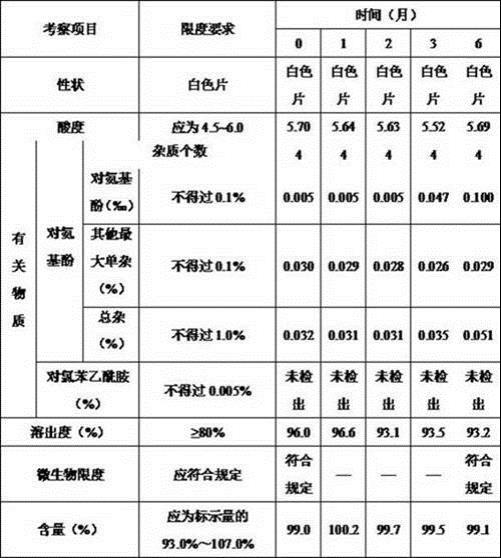
实施例9: 对乙酰氨基酚泡腾片长期试验考察条件:温度25℃
±
2℃湿度rh60%
±
10%,结果见表7。
30.表7. 对乙酰氨基酚泡腾片长期试验结果
结论:通过加速试验和长期稳定性试验可看出通过本工艺生产的对乙酰氨基酚泡腾片质量稳定。
31.实施例10:压片情况和崩解性能试验调节片重、硬度以及观察压片情况,结果见表10。
32.表10:压片结果表
序号运转速度下料情况片子硬度(kg)压片情况片重差异崩解时限(秒)片子厚度(mm)114~16良好8.02流畅不粘冲,片面光滑
±
3.0%59.263.958214~16良好8.11流畅不粘冲,片面光滑
±
2.6%55.453.955314~16良好8.10流畅不粘冲,片面光滑
±
3.1%57.644.002
结果表明:以14~16转/分钟的转速压片,片重差异均良。
33.实施例11:对乙酰氨基酚泡腾片溶解状态研究将本工艺制得的制剂加入到25ml的水、雪碧、可乐、水蜜桃汁和牛奶中各1片,分别在20
±
5℃和40
±
5℃两个温度条件下记录崩解时限,观察5分钟内溶解情况,若未完全溶解测定其残渣量,在每种温度条件下各不同溶液中分别做6次平行试验,结果见表11和表12。
34.表11.20
±
5℃各溶液溶解试验结果
表12.40
±
5℃各溶液溶解试验结果
结果表明:通过溶解现象看出本工艺生产的对乙酰氨基酚泡腾片溶解性能较好;通过外标法计算:残渣中对乙酰氨基酚的含量为99.5%。
35.实施例13:配伍稳定性试验本品为泡腾片剂,使用时溶解后服用,目前上市的泡腾片剂均为用温开水溶解后服用,我公司生产的对乙酰氨基酚泡腾片的用药人群为儿童,儿童具有依从性差,服药期间很难避免饮用奶粉、饮料等,故我公司对生产的泡腾片,用奶粉(不同厂家)、饮料(可乐、雪碧、水蜜桃汁)溶解的配伍稳定性进行考察。
36.取对乙酰氨基酚泡腾片,分别投入奶粉(不同厂家)、饮料(可乐、雪碧、水蜜桃汁)中溶解后,摇匀,在室温条件下放置1h,测定其含量和有关物质的变化,结果见表13。
37.表13. 对乙酰氨基酚泡腾片的配伍稳定性由上述结果可以看出本品与奶粉(不同厂家)、饮料(可乐、雪碧、橙汁)配伍稳定性良好。
38.实施例14:原辅料相容性研究结果将原料、混合辅料、原料+混合辅料分别放置在高湿(25℃、rh90%
±
5%)、高温(60℃)、光照(4500lx
±
500lx)条件下10天,考察原料和混合辅料之间是否存在相互作用,重点考察性状、有关物质、含量,试验结果见表14。
39.表14. 相容性试验结果
试验结果:上述不同配比的原辅料放置在高湿(25℃、rh90%
±
5%)、高温(60℃)、光照(4500lx
±
500lx)条件下10天,原辅料相容性样品与原料的稳定性基本一致,表明选用的原辅料之间无相互作用。
40.以下实验例中所说明的实验方法如无特别说明,均为常规方法。以上实验例中的所用的试剂、材料等,如无特殊说明,均可从商业途径得到。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1