一种基于介电电泳效应的细胞多级过滤装置的制作方法
本发明属于细胞过滤分选技术领域,涉及一种基于介电电泳效应的细胞多级过滤装置。
背景技术:
细胞分离是生物研究和分析诊断中一个重要的纯化过程。传统的多种分离方法大致可以分为两类:第一类是基于细胞本身的特性,如尺寸、重力特性等进行分离;另一类则是通过外加电场或者磁场对细胞进行分离。这些分离方法都有一些缺陷,如第一类分离的精度较差,作用时间长,操作复杂,对细胞活性影响较大;而第二类方法需要对细胞进行预处理使细胞间接带电或者表面附着磁性物质,操作复杂,成本昂贵。
由电泳技术发展而来的介电电泳技术打破了前者要求微粒带电的限制,是微流控系统中较为常用的一种电操作方式。1951年,HerbertPohl首先发现了介电电泳这一现象,将介电电泳定义为中性粒子(电介质)在电场作用下的定向移动。生物细胞或者微粒在非均匀电场中,被电场极化形成偶极子,该偶极子在非均匀电场作用中会受到特定的力而发生定向迁移,即介电电泳。介电电泳分为正向介电电泳效应和负向介电电泳效应。当粒子复介电常数大于缓冲液的复介电常数时,粒子往电场强的方向运动,称为正向介电电泳(positive DEP);相反,当粒子复介电常数小于缓冲液的复介电常数时,粒子往电场弱的方向运动,称为负向介电泳(negative DEP)。正向介电电泳效应被广泛用于细胞分离,负向介电电泳的应用还较少,但是利用正向介电电泳效应分离细胞时,需要选取电导率较低的缓冲液;而负向介电电泳效应可以直接在细胞培养液中产生,因为细胞培养液具有相对较高的电导率和介电常数。因此采用负向介电电泳效应可以直接在细胞培养液中进行细胞分离,分离之后的细胞可以直接进行培养,无需换液以及避免影响细胞活性。同时,介电电泳分离方法还可与其它方法结合使用,以达到最佳的细胞分离检测效果。
细胞过滤芯片是指利用MEMS技术在芯片上加工一些柱状、弯曲沟道、梳状、堰状及筛等微结构,根据不同颗粒(或细胞)尺寸进行分离的一种方法,要求不同颗粒间有明显的尺寸差异。但是这些微过滤芯片在细胞分离后期易出现芯片阻塞问题。
技术实现要素:
有鉴于此,本发明的目的在于提供一种基于介电电泳效应的细胞多级过滤装置,该装置借助介电电泳效应和芯片上加工的微孔阵列,实现不同尺寸细胞的分离;微孔阵列使尺寸小于微孔的细胞通过微孔,大于微孔的细胞停留在微孔处,实现不同大小细胞的选择性过滤。同时,为了避免阻塞微孔,结合介电电泳效应使细胞向低电场区域移动(微孔处为高电场区域),防止细胞在微孔处聚集造成阻塞。
为达到上述目的,本发明提供如下技术方案:
一种基于介电电泳效应的细胞多级过滤装置,包括一面加工有多条微电极的透明硬质基底层,所述微电极为相距约1cm的平板电极;另外还包括一面加工有多级微孔阵列以及微通道的透明弹性橡胶层,微通道两端通过进、出样口与外界管道连接;所述微孔阵列为不同尺寸的矩形微孔,用于过滤不同大小的细胞。
进一步,所述透明硬质基底层采用硬质芯片加工材料玻璃、硅或有机玻璃。
进一步,所述透明弹性橡胶层采用聚二甲基硅氧烷PDMS制成。
进一步,两微孔阵列之间设有一微通道与出样口相连接,每条微电极与每条出样微通道一一对应,以实现微电极与微孔阵列交错分布。
进一步,在该装置中,采用介电电泳效应使细胞向低电场区域移动,防止细胞在微孔处聚集造成阻塞。
本发明的有益效果在于:本发明提出的一种基于介电电泳效应的细胞多级过滤装置的核心点在于利用微加工技术加工集成了大量微孔的微孔阵列,一方面可使直径小于微孔的细胞通过微孔,直径大于微孔的细胞停留,实现细胞的选择性过滤;另一方面利用微孔结构改变两电极板之间电场分布,使得微孔中央区域为整个通道中电场最高区域,可利用负向介电电泳效应操控细胞向低电场区运动,解决细胞在微孔处的阻塞问题,并且利用培养液做缓冲液,分离之后的细胞可以直接进行培养,无需换液以及避免影响细胞活性。
附图说明
为了使本发明的目的、技术方案和有益效果更加清楚,本发明提供如下附图进行说明:
图1为本发明的细胞过滤芯片的平面示意图;
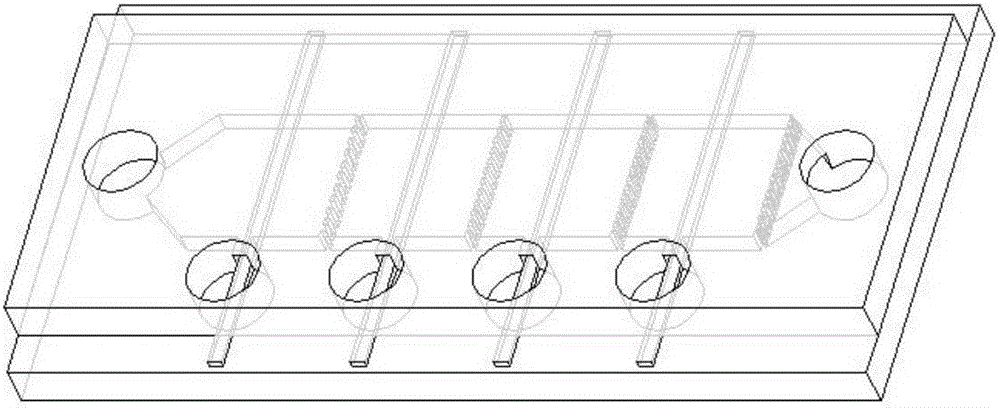
图2为本发明的细胞过滤芯片的总体示意图(结合后);
图3为微孔阵列示意图。
具体实施方式
下面将结合附图,对本发明的优选实施例进行详细的描述。
本发明利用微加工技术加工集成了大量不同大小微孔的多级微孔阵列芯片,用以过滤不同大小的细胞。同时,两级微孔之间施加交流信号,利用介电电泳效应一方面吸附细胞,另一方面防止细胞阻塞微孔。微孔可以改变两电极板之间的电场分布,微孔处为整个通道电场最高的区域。所以细胞会在负向介电电泳的作用下,远离微孔运动,因此不会阻塞微孔。通过调整电场的大小和流速之间的关系,使尺寸不一样的细胞逐级分离。
实施例1:
参见图1、图2和图3,微流控芯片由两层组成,第I层是透明硬质基底层1,采用有机玻璃,第II层是透明弹性橡胶层2,采用PDMS制成。透明硬质基底层1层的导电面刻蚀现成四条平行的平板微电极3。透明弹性橡胶层2的一面加工有多级微孔阵列和微通道,微通道两端有进样口4和出样口5,两微孔阵列之间有出样口6、7、8、9。微孔的直径可根据应用目的的不同有所区别。在微型泵的驱动下,样品液体从进样口进入微通道。结合前,把透明硬质基底层1表面清洁干净,水平放置。将透明弹性橡胶层2用氧等离子体处理30秒钟,微通道朝下覆盖在硬质基底层上。两层基片通过物理作用紧密结合在一起。
整个芯片的尺寸为60(长)×20(宽)×5(高)mm,微孔的直径分别为10μm、20μm、30μm、40μm,两微孔阵列之间的间隔为1cm。微电极的宽度100μm,相邻微电极的间隔为1cm。两微电极之间的电压根据需求来调整。所有进样口4和出样口5、6、7、8、9的直径为0.3~0.5mm。
实施例2:
基于介电电泳效应的细胞多级过滤装置,其细胞过滤实施过程如下:
从实施例1中所述的芯片的进样口4加入细胞悬浮液,不同直径大小(5~50μm)的细胞悬浮于细胞培养液中。通过微型泵在进样口设置进样流速,出口压力为0。
在透明硬质基底层1与透明弹性橡胶层2结合时,保证每条微电极在两微孔阵列之间的中间处。微孔的直径从进样口到出样口依次为40μm、30μm、20μm、10μm,因此40~50μm之间的细胞不能通过第一级微孔阵列,30~40μm的细胞不能第二级微孔阵列,依次类推。加载正弦交流信号与电极板3上,由于微孔阵列改变了两电极板3间的电场分布,使微孔内的电场强度最高,在负向介电电泳效应的作用下,细胞将向低电场区(两微孔阵列之间)运动,因此细胞不会在微孔处聚集,造成阻塞。完成分离后,施加负压于出样口5、6、7、8,收集分离的细胞,完成整个分离过程。
最后说明的是,以上优选实施例仅用以说明本发明的技术方案而非限制,尽管通过上述优选实施例已经对本发明进行了详细的描述,但本领域技术人员应当理解,可以在形式上和细节上对其作出各种各样的改变,而不偏离本发明权利要求书所限定的范围。
- 还没有人留言评论。精彩留言会获得点赞!