生长诱导系统、生长诱导控制装置、生长诱导控制方法和生长诱导控制程序与流程
本发明涉及一种生长诱导系统、生长诱导控制装置、生长诱导控制方法和生长诱导控制程序。
背景技术:
目前,以长时间的脏器功能维持或生长为目的,开发有各种各样的培养装置或培养方法。例如,在专利文献1中公开有如下方法:其为对从哺乳动物中摘除的脏器或组织进行灌注培养的方法,其中,与在生物体内连接于第一脏器或组织的第二脏器或组织一起摘除,通过将第二脏器或组织进行固定而悬挂第一脏器或组织,使灌注液灌注于第一脏器或组织的血管。
另外,在专利文献2中公开有如下方法:将人干细胞、人造血祖细胞或人间质细胞在连续地或周期地交替或灌注的液体培养基中进行培养,一边在生理学上可接受的条件下保持培养,一边补充营养素,由此在体外(exvivo)得到人祖细胞。
另外,在专利文献3中公开了:为了使组织或脏器生长,构建具有包括1个以上的流入口、流出口、传感器、脏器安装部位和/或脏器识别子的生长室的生物反应器,生物反应器具有响应1个以上因素的生长条件的监视、变更、脏器生长、功能优化、灭菌、生长环境的提供、脏器/组织起源的追踪等功能。
现有技术文献
专利文献
专利文献1:日本专利第5881422号公报
专利文献2:日本特开2001-120261号公报
专利文献3:日本特表2013-510590号公报
技术实现要素:
发明所要解决的技术问题
但是,以往的培养装置或培养方法存在如下各种问题。
例如,弥补专利文献1的灌注培养方法的缺点,在专利文献2的含人干细胞的组合物的培养方法中,虽然公开了通过使血液或培养液在脏器中回流,可以除去从活的脏器中排出的废物,能够在保持脏器的功能的状态下进行长期培养,但是以脏器的功能维持为目的,作为使脏器生长的方法使用并不充分。
另外,专利文献3的脏器形成方法存在如下问题:虽然对脏器的生长分化进行了公开,但是只是公开配置于上游的特定的细胞因子分泌细胞对下游的脏器提供细胞因子,存在如下问题,即不能适用于根据脏器的每个生长阶段所需要的细胞因子(激素或生长因子等)发生变化的情况。
本发明是鉴于上述的问题而完成的,提供一种不需要添加每个生长阶段的细胞因子而能够诱导生长的生长诱导系统、生长诱导控制装置、生长诱导控制方法和生长诱导控制程序。
用于解决问题的技术方案
为了实现这样的目的,本发明的生长诱导系统的特征在于,为具有向源自生物体的生长诱导对象灌注培养液的第一培养槽、向分泌细胞因子的分泌体灌注培养液的第二培养槽、和具有检测部、存储部和控制部的生长诱导控制装置,其中,上述存储部存储规定生长诱导步骤的生长诱导方案,上述控制部具有:生长状况检测单元,其经由上述检测部检测上述生长诱导对象的生长状况;和流量控制单元,其基于上述生长诱导方案,根据上述生长诱导对象的生长状况,控制将含有上述分泌体所分泌的细胞因子的培养液供给至上述生长诱导对象的流量。
另外,本发明的生长诱导系统的特征在于,在上述的生长诱导系统中,还具有向分泌其他细胞因子的分泌体灌注培养液的第三培养槽,上述流量控制单元还将上述第二培养槽的上述分泌体作为上述生长诱导对象,控制将含有从第三培养槽的上述分泌体所分泌的细胞因子的培养液供给至该生长诱导对象的流量。
另外,本发明的生长诱导系统的特征在于,在上述的生长诱导系统中,还具有向分泌其他细胞因子的分泌体灌注培养液的第四培养槽,上述流量控制单元还基于上述生长诱导方案,根据上述生长诱导对象的生长状况,由从上述第二培养槽的上述分泌体所分泌的细胞因子切换为从上述第四培养槽的上述分泌体所分泌的细胞因子,进行将上述培养液供给至上述生长诱导对象的切换控制。
另外,本发明的生长诱导系统的特征在于,在上述的生长诱导系统中,上述第一培养槽中灌注于上述生长诱导对象的上述培养液以向至少包括上述第二培养槽的其它上述培养槽回流的方式进行流体连接。
另外,本发明的生长诱导系统的特征在于,在上述的生长诱导系统中,上述流量控制单元还将上述第一培养槽的上述生长诱导对象作为分泌体,控制将含有从该分泌体所分泌的细胞因子的培养液供给至其它上述培养槽的流量。
另外,本发明的生长诱导系统的特征在于,在上述的生长诱导系统中,上述流量控制单元经由设置于上述培养槽之间的流路的阀控制上述流量。
另外,本发明的生长诱导系统的特征在于,在上述的生长诱导系统中,上述流量控制单元经由使液体在上述培养槽之间移动的自动装置(robot)控制上述流量。
另外,本发明的生长诱导系统的特征在于,在上述的生长诱导系统中,上述生长诱导方案规定诱导上述生长诱导对象的增殖和/或分化的步骤。
另外,本发明的生长诱导系统的特征在于,在上述的生长诱导系统中,上述细胞因子为激素、淋巴因子、趋化因子、单核因子、肌肉因子、白细胞介素、干扰素、造血因子、细胞生长因子、肿瘤坏死因子(tnf)、脂肪细胞因子、神经营养因子、抗体、体液配体、神经传递物质、信号传递物质、趋化性引诱物质和/或其它的体液因子。
另外,本发明的生长诱导系统的特征在于,在上述的生长诱导系统中,上述生长诱导对象和/或上述分泌体为细胞、组织或器官。
另外,本发明的生长诱导控制装置的特征在于,至少连接于向源自生物体的生长诱导对象灌注培养液的第一培养槽、和向分泌细胞因子的分泌体灌注培养液的第二培养槽,且上述生长诱导控制装置具有存储部、检测部和控制部,上述存储部存储规定生长诱导步骤的生长诱导方案,上述控制部具有:生长状况检测单元,其经由上述检测部检测上述生长诱导对象的生长状况;和流量控制单元,其基于上述生长诱导方案,根据上述生长诱导对象的生长状况,控制将含有上述分泌体所分泌的细胞因子的培养液供给至上述生长诱导对象的流量。
另外,本发明的生长诱导控制方法的特征在于,其在电脑中实行,该电脑至少连接于向源自生物体的生长诱导对象灌注培养液的第一培养槽、和向分泌细胞因子的分泌体灌注培养液的第二培养槽,且该电脑具有存储规定生长诱导步骤的生长诱导方案的存储部、检测部和控制部,该生长诱导控制方法包括在上述控制部中所实行的生长状况检测步骤和流量控制步骤,上述生长状况检测步骤经由上述检测部检测上述生长诱导对象的生长状况,上述流量控制步骤基于上述生长诱导方案,根据上述生长诱导对象的生长状况,控制将含有上述分泌体所分泌的细胞因子的培养液供给至上述生长诱导对象的流量。
另外,本发明的生长诱导控制程序的特征在于,其用于在电脑中实行,该电脑至少连接于向源自生物体的生长诱导对象灌注培养液的第一培养槽、和向分泌细胞因子的分泌体灌注培养液的第二培养槽,且该电脑具有存储规定生长诱导步骤的生长诱导方案的存储部、检测部和控制部,在上述控制部中,实行如下步骤:经由上述检测部检测上述生长诱导对象的生长状况的生长状况检测步骤;和基于上述生长诱导方案,根据上述生长诱导对象的生长状况,控制将含有上述分泌体所分泌的细胞因子的培养液供给至上述生长诱导对象的流量的流量控制步骤。
发明效果
根据本发明,发挥能够抑制在每个生长阶段添加细胞因子的成本而诱导生长的效果。更具体而言,根据本发明,可以提供一种系统、或其方法、装置、程序、记录介质等,该系统通过在作为生长诱导对象的脏器等之外,将分泌细胞因子的多种细胞、组织等分泌体进行共培养,并与该分泌体相互作用,控制遍布于生长诱导对象的细胞因子的种类、量,由此能够诱导将生长诱导对象向脏器分化/增殖等的生长。进而,通过将生长诱导对象设为细胞,使可用于细胞治疗的细胞进行增殖、分化,形成组织,也可以作为生长、分化成细胞组织片等的方法提供。
附图说明
图1是表示本发明的实施方式的生长诱导系统的整体概要的构成图。
图2是表示培养槽40的串联配置的例子的图。
图3是表示培养槽40的并联配置的例子的图。
图4是表示培养槽40的回流配置的例子的图。
图5是表示本实施方式的生长诱导系统中的生长诱导控制装置100的生长诱导控制处理的一例的流程图。
图6是表示实施例1和2的构成的图。
图7是本实施例的控制部设备90的系统框图。
图8是培养步骤数据和激素分泌细胞的配置信息的例子。
图9是表示阀开闭操作步骤的流程图的一例。
图10是表示使用本实施方式培养脏器、在其过程中实施了阀的开闭操作的情况下在脏器的生长过程中各因子的培养液中浓度的图。
图11是表示实施例2中的培养步骤数据和激素分泌细胞的配置信息的例子的图表。
图12是用流程图表示本实施例中的阀开闭操作步骤书的图。
图13是表示实施例2的成肌细胞的培养过程中的各因子的培养液中浓度的按时间顺序变化的图。
图14是表示本实施例2的结果得到的利用胎盘细胞培养上清液的肝脏细胞的增殖的图。
图15是表示利用肝脏细胞培养上清液的成肌细胞的增殖的图。
图16是实施例3的构成图。
图17是实施例4的构成图。
图18是实施例5和实施例6的构成图。
图19是实施例7的构成图。
图20是表示实施例7中的细胞间作用的循环的图。
图21是表示本实施例7的利用成肌细胞上清液的胎盘细胞的增殖的图。
图22是实施例8的构成图。
具体实施方式
以下,基于附图详细地说明本发明的本实施方式的生长诱导系统、生长诱导控制装置、生长诱导控制方法、及生长诱导控制程序、以及记录介质的实施方式。予以说明,该发明并不受其实施方式限定。特别是在以下的实施方式中,以将培养槽之间用管连接、使用阀(阀门)控制在管内流动的培养液的流量或切换的方式构成,但本发明并不限于此。例如,各培养槽也可以在独立的槽中不相互连结,但通过在培养槽之间往来的移液自动装置等设备搬运培养槽之间的液体,进行流量控制或切换控制。
[生长诱导系统的构成]
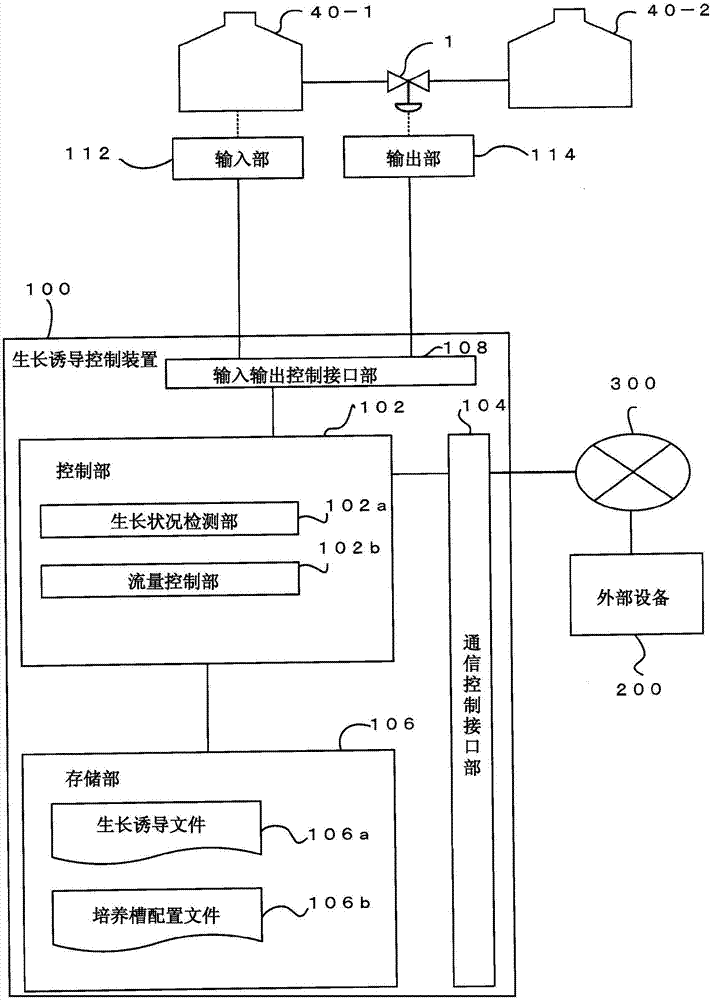
首先,以下对本发明的本实施方式的生长诱导系统的构成进行说明,之后,对本实施方式的处理等详细地进行说明。在此,图1是表示本发明的实施方式的生长诱导系统的整体概要的构成图。
如图1所示,本实施方式的生长诱导系统具有生长诱导控制装置100和至少2个培养槽40而构成。
图1中,第一培养槽40-1为向源自生物体的生长诱导对象灌注培养液的培养槽。在此,生长诱导对象可以为细胞、组织、器官(脏器)等。生长诱导对象为细胞或组织的情况下,可以通过使培养液遍布于培养层而进行灌注。另外,生长诱导对象为器官(脏器)的情况下,可以通过使培养液遍布于培养脏器的血管而进行灌注。更具体而言,可以将套管等管连结于脏器等的血管,与血流同样地使培养液流入和流出而培养脏器等。予以说明,为了回流,可以每个培养槽40具有另行的培养液回流机构。
另外,第二培养槽40-2为向分泌细胞因子的分泌体灌注培养液的第二培养槽。在此,分泌体可以为细胞、组织、器官(脏器)等。分泌体所分泌的细胞因子可以为各种激素、淋巴因子、趋化因子、单核因子、肌肉因子(myokine)、白细胞介素(il)、干扰素(ifn)、造血因子(csf)、细胞生长因子、肿瘤坏死因子(tnf)、脂肪细胞因子、神经营养因子(ngf)、抗体(激动剂抗体等)、体液配体、神经传递物质、信号传递物质、趋化性引诱物质、此外可以为与细胞或组织、器官(脏器)等的生长有关的体液因子。予以说明,在本实施方式中,“生长”包含增殖、分化、凋亡、坏死等。
在此,如图1所示,在本实施方式中,第一培养槽40-1和第二培养槽40-2构成为由在流路上具有阀1的管进行流体连接,通过将该阀1进行开闭而能够控制流量。作为阀的结构,可以使用凸缘式、螺纹式等公知的阀(阀门),作为阀的调整方法,可以使用空气驱动式、电动式、油压式等公知的调整阀。另外,为了防止逆流,也可以具有止逆阀。
予以说明,图1中,生长诱导系统图示有2个培养槽40,但并不限定于此,也可以将3个以上的培养槽40以串联、并联、和/或回流配置进行流体连接。在此,图2是表示培养槽40的串联配置的例子的图。
串联配置的情况下,如图2所示,生长诱导系统作为一例,还具有向分泌与第二培养槽40-2的分泌体不同的细胞因子的分泌体灌注培养液的第三培养槽40-3,后述的控制部102(流量控制部102b等)进而将第二培养槽40-2的分泌体作为生长诱导对象,以能够控制将含有从第三培养槽40-3的分泌体所分泌的细胞因子的培养液供给至第二培养槽40-2的生长诱导对象的流量的方式配置。这样,通过控制从第三培养槽40-3向第二培养槽40-2的流量,能够诱导第二培养槽40-2的分泌体(从第三培养槽40-3的分泌体来看的生长诱导对象)的增殖、分化等的生长,因此,能够使从第二培养槽40-2的分泌体所分泌的细胞因子的分泌量或种类等变化,即使为相同的流量,也可以间接地控制向第一培养槽40-1的生长诱导对象供给的细胞因子的作用量和作用内容。在此,图3是表示培养槽40的并联配置的例子的图。
并联配置的情况下,如图3所示,生长诱导系统作为一例,具有向分泌与第二培养槽40-2的分泌体不同的细胞因子的分泌体灌注培养液的第四培养槽40-4,后述的控制部102(流量控制部102b等)进而根据第一培养槽40-1的生长诱导对象的生长状况,以由从第二培养槽40-2的分泌体所分泌的细胞因子切换为从第四培养槽40-4的分泌体所分泌的细胞因子、能够进行将培养液供给至该生长诱导对象的切换控制的方式构成。通过这样从第二培养槽40-2向第四培养槽40-4的切换控制,能够使向第一培养槽40-1的生长诱导对象供给的细胞因子的种类、作用量等发生变化。在此,图4是表示培养槽40的回流配置的例子的图。
回流配置的情况下,如图4所示,生长诱导系统作为一例,以将在第一培养槽40-1中灌注于生长诱导对象的培养液向其它培养槽40(例如第二培养槽40-2)回流的方式进行连结。在此,第一培养槽40-1的生长诱导对象可以作为分泌体分泌细胞因子,将培养液通过灌注而供给至作为其它第二培养槽40-2等的生长诱导对象的分泌体。通过这样从第一培养槽40-1向其它培养槽40的回流流量控制,能够诱导第二培养槽40-2的分泌体(从第一培养槽40-1的分泌体来看的生长诱导对象)的增殖、分化等生长,因此,能够使从第二培养槽40-2等的分泌体所分泌的细胞因子的分泌量或种类等发生变化,结果,能够自然而然地间接控制向第一培养槽40-1的生长诱导对象供给的细胞因子的作用量或作用内容。
予以说明,以上的串联配置、并联配置、回流配置可以任意地以多个加以组合。例如,生长诱导系统可以在多阶段将培养槽40串联配置,也可以将并联配置和回流配置组合,还可以切换控制含有从第一培养槽40-1的分泌体所分泌的细胞因子的培养液的通过回流的供给目标。予以说明,虽然没有图示,但是在阀1或流路上可以具有过滤功能、热失活功能、各种过滤器。另外,在回流系统中,可以具有气体交换部和透析部。予以说明,回流系统可以将培养槽40的培养液返回到相同的培养槽40。
[生长诱导控制装置100的构成]
再回到图1,对本实施方式的生长诱导控制装置100等的构成进行说明。如图1的框图所示,适用本实施方式的生长诱导控制装置100的构成仅概念性地表示该构成中与本实施方式有关的部分。
图1中,生长诱导控制装置100概略性地具有全面控制生长诱导控制装置100的整体的cpu等控制部102、与连接于通信线路等的路由器等通信装置(未图示)连接的通信控制接口部104、与传感器或接触面板等输入部112或输出部114连接的输入输出控制接口部108、以及贮藏各种数据库或表格等的存储部106而构成,这些各个部分经由任意的通信路径而可通信地连接。在此,生长诱导控制装置100可以为微型计算机、或个人电脑、服务器用电脑等。
存储部106所贮藏的各种数据库或表格(例如生长诱导文件106a或培养槽配置文件106b等)为使用sram(staticrandomaccessmemory,静态随机存取存储器)等所构成的小容量高速存储器(例如、高速缓冲存储器)等、或hdd(harddiskdrive,硬盘驱动器)或ssd(solidstatedrive,固态硬盘)等的固定磁盘装置等存储单元,贮藏用于各种处理的各种程序、表格、文件和/或数据库等。
其中的生长诱导文件106a为存储规定生长诱导步骤的生长诱导方案的生长诱导信息存储单元。作为一例,生长诱导方案可以根据分化期或生长阶段等,关联所需要的细胞因子的种类或供给量的阈值并贮藏。在此,生长诱导文件106a可以作为蓄积有各种培养步骤数据等的生长诱导方案的数据库构成。
另外,培养槽配置文件106b为存储培养槽40的配置信息的配置信息存储单元。例如,培养槽配置文件106b可以存储:培养槽40的并联/串联/回流配置等的配置信息、贮藏细胞因子的分泌体或生长诱导对象的培养槽40的配置信息、阀1或管道等的配置信息或控制信息(例如开闭信号与流量的对应表格)等。
另外,图2中,输入输出控制接口部108进行传感器或开关等的输入部112或输出部114的控制。作为输入部112,可以使用检测生长诱导对象的生长状况等的传感器或照相机、阀开闭的输入设备等。另外,作为输出部114,可以使用阀开闭驱动器、或泵等。
作为传感器等的检测部,输入部112对作为培养的对象的细胞、细胞组织、器官、脏器检测其状态。作为一例,传感器等的输入部112检测培养槽40内部的环境、例如脏器的状态。输入部112可以具有多个传感器。
关于检测脏器等的状态的方法,已知脏器等作为表示目前状态的信号传递物质,会分泌蛋白质、激素或细胞因子。作为一例,输入部112的传感器通过检测该信号传递物质而探测脏器的状态。更具体而言,输入部112的传感器作为探测脏器等的状态的指标,可以检测ph、盐分浓度、钠离子浓度、钾离子浓度、钙离子浓度、温度、糖度、压力、信号传递物质浓度、信号传递蛋白质浓度、特定波长下的吸光度等。
作为检测信号物质传递物质浓度、或信号蛋白质浓度的方法,可以采用使用抗体的测定法(enzyme-linkedimmunesorbentassay,酶联免疫吸附测定:elisa法)或吸光度计。elisa法通过以脏器等的生长诱导对象的状态选择性地检测特征性的蛋白质或信号物质,来确定生长诱导对象的状态(参照专利文献1)。信号传递物质或信号传递蛋白质在构成其的芳香属氨基酸特定的波长区域280nm内显示大的吸光度(参照专利文献2),因此,输入部112可以通过测量λabs附近的吸光度而检测生长诱导对象的状态。
另外,输入部112除上述的生长状况的检测之外,可以同时具有按钮、控制杆、接触面板、网络设备等其它输入单元。另外,作为输出部114,除上述的阀开闭驱动器或泵等之外,可以使用液晶监视器等显示装置。
另外,图1中,控制部102具有os(operatingsystem,操作系统)等控制程序、规定各种处理步骤等的程序、及用于贮藏所需要数据的内存储器,控制部102为利用这些程序等而进行用于实行各种处理的信息处理的cpu等的处理器。控制部102在功能概念性上具有生长状况检测部102a和流量控制部102b而构成。
其中的生长状况检测部102a为经由作为检测单元(传感器等)的输入部112而检测生长诱导对象的生长状况的生长状况检测单元。作为一例,生长状况检测部102a可以基于利用输入部112的传感器所检测的信息,将利用elisa法补充的抗原的信号物质传递物质浓度等进行定量化。作为其它例,生长状况检测部102a可以基于由输入部112的传感器所检测的激发波长λabs附近的吸光度,进行含有芳香属氨基酸的蛋白质的定量。此外,生长状况检测部102a可以基于经由照相机等的输入部112拍摄的显微镜图像信息,进行形态识别,判断分化期、或发育期、或发生期等的生长状况。
另外,流量控制部102b为按照存储于生长诱导文件106a的生长诱导方案,根据生长状况检测部102a所检测的生长诱导对象的生长状况,控制将含有分泌体所分泌的细胞因子的培养液供给至生长诱导对象的流量的流量控制单元。例如,流量控制部102b可以基于所检测的生长诱导对象的生长状况的生长阶段,参照生长诱导方案,判定所需的细胞因子的种类和作用量等,接着,基于培养槽配置文件106b的配置信息,为了将所需的细胞因子的种类和作用量的培养液供给至该生长对象,经由输出部114进行阀1的切换控制和流量控制。予以说明,流量控制部102b为了抑制所需要的细胞因子以外的体液因子产生影响,可以以不通过不需要的细胞因子的过滤器、或不需要的细胞因子被热失活的方式控制输出部114。
在此,生长诱导控制装置100可以构成为与提供生长诱导方案的数据库、或提供生长诱导控制程序或图像形态识别程序等外部程序等的外部设备200,经由网络300以能够通信的方式连接。该情况下,生长诱导控制装置100可以经由路由器等通信装置及专用线等有线或无线的通信线路而与网络300以能够通信的方式连接。
而且,图1中,通信控制接口部104为进行生长诱导控制装置100和互连网等的网络300(或路由器等通信装置)之间的通信控制的装置。即,通信控制接口部104具有与其它终端或电台经由通信线路(不论有线、无线)而通信数据的功能。外部设备200经由网络300与生长诱导控制装置100相互连接,具有提供:提供对各终端提供生长诱导方案的数据库等的外部数据库、或实行生长诱导控制程序或图像形态识别程序等外部程序等的网址等的功能。
在此,外部设备200例如可以由个人电脑或服务器用的电脑等硬件要素与操作系统、应用程序、其它的数据等软件要素来实现。例如,外部设备200可以作为web服务器或asp服务器等构成,其硬件构成可以由一般所市售的工作站、个人电脑等的信息处理装置及其附属装置构成。另外,外部设备200的各功能由外部设备200的硬件构成中的cpu等的处理器、磁盘装置、存储器装置、输入装置、输出装置、通信控制装置等及控制这些装置的程序等来实现。
以上,结束本实施方式的生长诱导系统的各构成的说明。
[生长诱导控制处理]
下面,对这样构成的本实施方式的生长诱导系统中的生长诱导控制装置100的生长诱导控制处理的一例,以下参照图5详细地进行说明。图5是表示本实施方式的生长诱导系统中的生长诱导控制装置100的生长诱导控制处理的一例的流程图。
首先,生长状况检测部102a经由传感器或照相机等输入部112,检测培养槽40内的生长诱导对象的生长状况(步骤sa-1)。例如,生长状况检测部102a经由输入部112检测ph、或盐分浓度、钠离子浓度、钾离子浓度、钙离子浓度、温度、糖度、压力、信号传递物质浓度、信号传递蛋白质浓度、特定波长下的吸光度等,由此可以判定脏器等的生长诱导对象的生长状况。作为一例,生长状况检测部102a可以基于利用elisa法被抗体捕捉的抗原的有无或量而判定生长状况,也可以由芳香属氨基酸特定的波长区域280nm的吸光度将蛋白量进行定量而判定生长状况,还可以通过基于用照相机等拍摄的图像进行形态识别而判定生长状况。
然后,流量控制部102b读取存储于生长诱导文件106a的生长诱导方案(步骤sa-2)。例如,流量控制部102b可以从生长诱导方案的数据库提取生长诱导对象的生长诱导方案。
然后,流量控制部102b参照读取的生长诱导方案,确定与由生长状况检测部102a所检测的生长诱导对象的生长状况相应的、含有细胞因子的培养液的供给量(步骤sa-3)。予以说明,流量控制部102b不需要在严格的意义上确定至供给量的数值。例如,如果细胞因子以阈值以上的浓度对生长诱导对象诱导生长,则供给量为其阈值以上即可。进而,流量控制部102b即使在生长诱导方案中没有阈值的数据,且在培养液中所含的细胞因子的量不清楚的情况下,通过关联由阀开闭控制的供给量的历史信息与其供给的结果、由生长状况检测部102b所判定的生长诱导对象的生长状况的变化,能够学习细胞因子的作用量。而且,从下一次开始,参照学习数据库,流量控制部102b可以估算供给量。
接着,流量控制部102b基于培养槽配置文件106b的配置信息,为了将所需的细胞因子的种类或供给量的培养液供给至该生长对象,经由输出部114进行阀1的切换控制或流量控制(步骤sa-4)。
以上为本实施方式的生长诱导系统中的生长诱导控制装置100的生长诱导控制处理的一例。予以说明,生长诱导控制装置100可以重复进行上述的步骤sa-1~sa-4的处理。
[实施例]
以下,对本发明的实施方式的各种各样的实施例进行说明。
本发明的本实施方式提供培养多种分泌细胞因子的细胞、组织或脏器并使其相互作用,诱导生长诱导对象的增殖或分化等的生长的系统、装置和方法等。另外,本发明的实施方式的目的在于提供所分泌的细胞因子在作用于其它细胞因子分泌体时,控制其顺序,或使细胞因子作用于生长诱导对象的系统、装置和方法等。以下,一边参照附图,一边说明本实施例1~8。
<实施例1>
使用图6,说明本实施例的脏器生长诱导装置的方式。将表示本发明的实施例1的构成图示于图6。图6是表示实施例1和2的构成的图。
实施例1的细胞组织41为作为生长诱导对象的细胞、细胞组织或脏器等。作为生长诱导对象41,可以为细胞、细胞块、脏器、连结多个脏器的对象等。
容器(培养槽)40保存进行培养的生长诱导对象41。容器40具有能够贮藏生长诱导对象41的大小,保护生长诱导对象41免受来自外部的冲击或接触。进而,容器40可以具有遮光性、耐冲击性、隔热性等功能。
作为在容器40内的生长诱导对象41的保存方法,通过将培养液流入的管连接于动脉,将流出的管连接于静脉,可以使培养液灌注于脏器。作为赋予用于使培养液在期望的方向流动的压力的方法,考虑在流路上使用泵的方法、利用重力的方法、利用渗透压的方法等。除此之外,如专利文献1(日本专利第5881422号公报)所记载的那样,也可以用在被横隔膜包裹的状态下悬挂等公知的方法载持。
细胞因子分泌组织贮藏装置60保存细胞因子分泌组织50。作为细胞因子分泌组织50,除所摘除或培养的肾上腺、甲状腺、脑垂体之外,还可以为具有分泌细胞因子的功能的导入有基因重组体的细胞。作为细胞因子的种类,可列举:生长激素或性激素、作为细胞因子的上皮生长因子(epidermalgrowthfactor(egf))、成纤维细胞生长因子(fibroblastgrowthfactor(fgf))、肝细胞生长因子(hepatocytogrowthfactor(hgf))或趋化因子等。
在经由阀1-00或阀1-11流入的培养液中,用细胞因子分泌组织贮藏装置60添加细胞因子,经由阀1-20流出。
同样地,在细胞因子分泌组织贮藏装置61中,贮藏有细胞因子分泌组织51。另外,关于贮藏装置61,也可以其中不贮藏细胞因子分泌组织51而设为空的状态,仅作为培养液的流路使用。
阀1-00、1-01、1-11、1-20、1-21控制回流培养液的流量。作为阀的结构,既可以由油压、空气压、水压等物理的力进行驱动,也可以使用电磁力。
在此,如果将阀1-00、1-11、1-21开放,将阀1-01和1-20关闭,则流路系统就以透析部30、阀1-00、贮藏装置60、阀1-11、贮藏装置61、阀1-21、容器40的顺序连接。
在此,如果将阀1-01、1-11、1-20开放,将阀1-00和1-21关闭,则流路系统就以透析部30、阀1-00、贮藏装置61、阀1-11、贮藏装置60、阀1-21、容器40的顺序连接,贮藏装置60和贮藏装置61在流路上的顺序相对于前面的例子相反。
另外,如果将阀1-00和1-20开放,将阀1-01、1-11、1-21关闭,则仅贮藏装置60装载于流路系统上。
作为输入部112的一部分功能,传感器70检测容器40内部的环境、例如脏器的状态。由传感器70所检测的与脏器的状态有关的信息向输入输出控制接口108等的输入设备80发送,输入控制设备90。此外也可以具有多个传感器。
图7是本实施例的控制部设备90的系统框图。本实施例的控制设备90相当于上述实施方式的控制部102或存储部106,具有图7所示的软件、或与其类似的系统,基于来自输入设备80的信号,控制阀1-00、1-01、1-11、1-20、1-21的开闭。图8是培养步骤数据和激素分泌细胞的配置信息的例子。图9是表示阀开闭操作步骤的流程图的一例。
本实施例的控制设备90具有相当于上述实施方式的生长诱导文件106a的培养步骤数据901和贮藏其的培养步骤数据库902。另外,控制设备90具有相当于上述实施方式的生长诱导文件106b的、记述在哪个贮藏装置中贮藏哪个细胞因子分泌组织的激素分泌细胞的配置信息903(参照图8)。
另外,控制设备90具有:由培养步骤数据库902和激素分泌细胞配置信息903生成阀开闭操作步骤书的阀开闭步骤制作部904(参照图9,相当于上述的流量控制部102b)、和按照阀开闭操作步骤书实施阀1-00、1-01、1-11、1-20、1-21的开闭操作的阀开闭控制部905(相当于上述的流量控制部102b)。作为阀的开闭控制的单元,考虑利用电信号的单元、利用无线的单元、利用机械作用的单元等各种各样的机构。图10是表示使用本实施方式培养脏器、在其过程中实施了阀的开闭操作的情况下在脏器的生长过程中各因子的培养液中浓度的图。
根据以上的构成和其动态,细胞组织41受到如图10那样随时间变化的浓度的细胞因子的化学暴露,细胞组织41的生长和分化得到控制。
<实施例2>
实施例2中,使用实施例1的构成(参照图6),将胎盘细胞设为50,将肝脏细胞设为51,将成肌细胞设为生长诱导对象41,参照流程图说明在容器40中使肌肉组织生长的情况下的本发明的实施方式。
专利文献3中,胎盘细胞分泌的增殖因子hgf作用于肝脏细胞,使肝脏细胞进行分裂、分化。另外在专利文献4(日本特表2008-513013)中,报道有肝脏细胞分泌的因子作用于成肌细胞,使其在未分化的状态下进行增殖,之后报道了该因子为tgfβ(专利文献5:参照日本专利第5797113号)。
根据这种情况,本实验中,从妊娠第12.5天的小鼠胚胎中回收胎盘、肝脏、成肌细胞,分别用在memα中添加有10%fbs的培养液中进行1周培养。其间,进行将胎盘细胞50的培养上清液向肝脏细胞51的移动,将肝脏细胞51的培养上清液向成肌细胞41的移动。作为培养液的移动量,设置整体的50%、25%、10%和0%的未移动的处理区。最终对培养的细胞数或按照大小对细胞数计数。图11是表示实施例2中的培养步骤数据和激素分泌细胞的配置信息的例子的图表。
作为使装置工作的准备,输入图11的培养步骤书和激素分泌细胞的配置信息,生成阀开闭操作步骤书。图12是用流程图表示本实施例中的阀开闭操作步骤书的图。
按照所生成的阀开闭操作步骤书开始培养操作时,在初期状态下,阀1-00、1-11、1-21开放,阀1-01和1-20关闭。在该构成中,胎盘细胞50位于肝脏细胞51的上游,胎盘细胞50分泌的生长因子作用于肝脏细胞51。
胎盘细胞50一定程度增殖,传感器70检测出为阈值的100ng/ml以上的生长因子时,为了阻断从贮藏胎盘细胞50的贮藏装置60向贮藏肝脏细胞51的贮藏装置61的流路,阀1-01和1-21打开,阀1-00、1-11、1-20被关闭。通过该操作,仅贮藏装置61残留在流路系统上,向成肌细胞41连续供给适当的量的血清成分,成肌细胞41分化为肌肉组织。
接着,肝脏细胞51进一步增殖,传感器70检测出为阈值以上的血清成分时,为了阻断从贮藏肝脏细胞51的贮藏装置61向贮藏成肌细胞41的容器40的流路,阀1-00和1-20打开,阀1-01、1-11、1-21被关闭。通过该操作,对成肌细胞41的血清成分的暴露停止,成肌细胞41的向现有程度以上的肌肉组织的分化停止。
之后,从成肌细胞中分化的肌肉组织进一步生长,如果传感器70检测出肌肉组织放出的信号物质的浓度超过阈值的0.2ng/l,则判断可得到足够量的肌肉组织,培养操作结束。
该一系列的操作期间,传感器70检测的生长因子、血清成分和信号物质的时间变化如图13所示。图13是表示实施例2的成肌细胞的培养过程中的各因子的培养液中浓度的按时间顺序变化的图。
图14是表示本实施例2的结果得到的利用胎盘细胞培养上清液的肝脏细胞的增殖的图,图15是表示利用肝脏细胞培养上清液的成肌细胞的增殖的图。如图14和图15所示,确认到:通过本实施例,胎盘细胞50作用于肝脏细胞51,细胞增殖,肝脏细胞51作用于细胞组织41,细胞增殖。
<实施例3>
将表示本实施方式的实施例3的构成图示于图16。图16是实施例3的构成图。本实施例中,可以使3种细胞因子分泌组织相互作用。
例如通过将阀1-00、1-10、1-12和1-21开放,将其以外的阀1-01、1-02、1-11、1-20、1-22关闭,流路系统以贮藏装置60、62、61的顺序连接。
与此相对,如果将阀1-01、1-11、1-10、1-22开放,将其以外的阀1-00、1-02、1-12、1-20、1-21关闭,则流路系统以贮藏装置61、60、62的顺序连接。
如果将阀1-02、1-10、1-20开放,将其以外的阀1-00、1-01、1-11、1-12、1-21、1-22关闭,则流路系统以贮藏装置62、60的顺序连接,贮藏装置61从流路系统中脱离。
这样,通过将阀开闭而控制流路系统的顺序或构成要素来控制细胞因子分泌组织的活动的方法,在将4种以上的细胞因子分泌组织在相同数量的贮藏装置中每个装置中各贮藏1种的构成中也可以适用。
<实施例4>
将表示本实施方式的实施例4的构成图示于图17。图17是实施例4的构成图。本实施例中,提供一种通过阀1-00、1-01、1-11、1-20、1-21的操作,在贮藏装置60或61的任一个或两者独立于流路系统情况下,细胞因子分泌组织50和51或其一方不死亡而被保存的单元。
本实施例中,在图1所示的第1实施例的基础上,贮藏装置60具有包括泵601、气体交换部602、透析部603的流路系统。
例如,将阀1-01和1-21开放,将阀1-00、1-11、1-20关闭的情况下,贮藏装置61装载于从透析部30至容器40的流路系统,但贮藏装置60独立。该情况下,经过长时间时,通过细胞因子分泌组织50的活动,引起废物的蓄积及氧和营养素的缺乏,细胞因子分泌组织50死亡。因此,通过泵611、气体交换部612、透析部613使培养液回流,维持细胞因子分泌组织50的生命活动。
通过在贮藏装置60中也具有与对于贮藏装置61的泵611、气体交换部612、透析部613同样的装置,贮藏装置60独立于流路系统的情况下,也能够维持细胞因子分泌组织50的生命活动。
<实施例5>
实施例5中,提供一种防止气泡、细胞或细胞碎片、其它的垃圾等异物侵入图1所示的贮藏装置60、61和容器40、以及连接它们的流路中的单元。图18是实施例5和实施例6的构成图。
例如,在贮藏装置60中侵入气泡或垃圾等异物的情况下,由于异物粘接于细胞或组织而不能在该细胞部位遍布培养液,引起营养素的缺乏和干燥,细胞因子分泌组织50局部地死亡。细胞或细胞侵入的情况下,在细胞或组织中引起堵塞或粘接,改变细胞或组织的形态或诱导死亡。
本实施例中,阀1-00、1-01、1-11、1-20、1-21具有除去异物的柱、过滤器、收集器、支流装置等的机构。利用该机构,例如在流路系统上产生的异物流入贮藏装置60之前,利用具有除去异物的机构的阀1-00除去异物,细胞因子分泌组织50能够维持生命活动。
作为除去异物的机构,过滤器、柱、收集器在继续使用中会发生堵塞,妨碍流路系统,因此,需要定期的清洁。作为不需要定期的清洁的单元,既可以使用bd公司或贝克曼库尔特公司等出售的细胞分选仪(cellsorter),也可以采用使用层流的on-chipbiotechnologies拥有的专利(日本专利第4601423号公报(日本特愿2004-379327))所公开的分选技术。
<实施例6>
实施例6中,提供从图1所示的贮藏装置60、61和容器40、及连接它们的流路中除去特定的蛋白质或化合物等成分,或使其生理学的效果灭失的单元。
本实施例中,阀1-00、1-01、1-11、1-20、1-21具有用于除去特定的蛋白质或化合物等成分或者使其生理学的效果灭失的加热装置、uv照射装置、激光照射装置、化合物或其溶液的注入装置等机构。通过该机构,作为除去对象的特定的蛋白质或化合物等成分例如在流入贮藏装置60之前,可以利用阀1-00除去该成分。
作为例子,报道有作为血清成分的肝脏分泌的白蛋白从超过60℃的附近开始形态迅速地变化,丧失生理活性。另一方面,即使作为乳蛋白质的酪蛋白超过60℃,也比较稳定(katoa,osakoy,matsudomiay,kobayashiak,“changesintheemulsifyingandfoamingpropertiesofproteinsduringheatdenaturation”,agriculturalandbiologicalchemistry,1983,47卷33-37:社团法人日本农艺化学会)。如此,因蛋白质的结构的特性而热耐性不同,能够利用它们的差而使特定的蛋白质的生理学的效果丧失。
<实施例7>
将表示本发明的实施例7的构成图示于图19。图19是实施例7的构成图。实施例7中,流路系统成为环状,培养液进行循环而被再利用。
泵10供给使培养液从脏器贮藏容器40在气体交换部20的方向回流的压力。泵可以为稳流泵,也可以为脉动泵,但更优选脉动泵。另外,泵10的位置在气体交换部20和透析部30之间、或贮藏装置60或保存的容器40之间等连结气体交换部20、透析部30、容器40的流路上,只要是对培养液施加回流压力的位置,则在哪里都可以,也可以设置多个。
气体交换部20从培养液中除去二氧化碳,加入氧。该功能与人工心肺等所使用的氧/二氧化碳交换功能等同。
透析部30从流入的培养液的一部分或全部除去废物。作为除去的方法,既可以使用半透膜,也可以将废物进行凝结沉淀,还可以与新的培养液进行交换。
本实施例中,由于培养液进行回流,因此,如图19所示,相互作用循环,细胞组织41分泌的物质也可得到对细胞因子分泌组织50或51起作用的效果。
在此,图20是表示实施例7中的细胞间作用的循环的图。图20中,在细胞组织41为成肌细胞、细胞因子分泌组织50为胎盘细胞的情况下,成肌细胞显示促进胎盘细胞的增殖的结果。在此,认为成肌细胞分泌的efg和fgf作用于胎盘细胞。图21是表示本实施例7的利用成肌细胞上清液的胎盘细胞的增殖的图。如图21所示,确认到:由本实施例7利用回流机构使含有各种细胞因子的培养液循环,使生长诱导对象相互作用,可得到所期望的细胞或组织。
<实施例8>
将表示本实施方式的实施例8的构成图示于图22。图22是实施例8的构成图。
本实施例中,提供防止气泡、细胞、细胞碎片、其它的垃圾等异物侵入容器40及泵10、气体交换部20、透析部30及连接它们的流路的单元。
在贮藏装置40中侵入异物的情况下,在细胞或组织中引起堵塞或粘接,改变细胞或组织41的形态或者诱导死亡,或引起流路的堵塞。异物为细胞或细胞碎片的情况下,有时会引起细胞的污染,抑制正常的增殖、分化。
因此,本实施例中,贮藏装置40在其上游具有柱、过滤器、收集器、支流装置等除去异物的机构130。
以上,结束包括实施例1~8的本实施方式的说明。
[其它实施方式]
目前为止对本发明的实施方式进行了说明,本发明除上述的实施方式以外,也可以在权利要求书中记载的技术思想的范围内根据各种不同的实施方式实施。
例如,对生长诱导控制装置100以独立的形态进行处理的方式作为一体构成的例子进行了说明,但并不限定于此,也可以根据来自外部设备200等的客户终端的要求进行处理,将其处理结果返还到该客户终端。
另外,也可以手动地进行实施方式中说明的各处理中说明为自动进行的处理的全部或一部分,或者,也可以用公知的方法自动地进行说明为手动进行的处理的全部或一部分。
此外,对包含上述文献中或附图中所示的处理步骤、控制步骤、具体的名称、各处理的注册数据或检索条件等的参数的信息、画面例、数据库构成,除了特殊说明的情况,可以任意地变更。
另外,关于包含生长诱导控制装置100或培养槽40的生长诱导系统或外部设备200,图示的各构成要素是功能概念性的表示,不一定需要在物理上如图示那样构成。
例如,关于生长诱导控制装置100的各装置具有的处理功能、特别是由控制部102进行的各处理功能,可以以将其全部或任意的一部分用cpu(centralprocessingunit,中央处理器)等处理器及由该处理器解释实行的程序来实现,另外,也可以作为利用接线逻辑的硬件处理器实现。另外,程序被记录于后述的包含用于在电脑中实行本发明的方法的程序化了的命令的、非暂时性电脑可读取的记录介质,根据需要机械性地读取至生长诱导控制装置100或外部设备200。即,在rom或hdd(harddiskdrive,硬盘驱动器)等存储部106等中,与os(operatingsystem)协作而对cpu给予命令,记录用于进行各种处理的电脑程序。该电脑程序通过载入于ram而实行,与cpu协作而构成控制部。
另外,该电脑程序可以存储于经由任意的网络300连接于生长诱导控制装置100或外部设备200的应用程序服务器,也可以根据需要下载其全部或一部分。
另外,可以将本发明的程序贮藏于电脑可读取的记录介质,另外,也可以构成为程序产品。在此,该“记录介质”包括:存储卡、usb存储器、sd卡、软盘、光盘、rom、eprom、eeprom、cd-rom、mo、dvd和blu-ray(注册商标)disc(蓝光光盘)等任意的“便携式物理介质”。
另外,“程序”为用任意的语言或记述方法所记述的数据处理方法,不论源代码或二进制代码等的形式。予以说明,“程序”不一定限于单一构成的程序,也包含作为多个模块或库分散构成的程序、或与以os(operatingsystem)为代表的另一个程序协作而实现其功能的程序。予以说明,关于在实施方式所示的各装置中用于读取记录介质的具体的构成、读取步骤、或者读取后的安装步骤等,可以使用公知的构成或步骤。程序也可以作为被记录于非暂时性电脑可读取的记录介质的程序产品构成本发明。
被贮藏于存储部106的各种数据库等(生长诱导文件106a,培养槽配置文件106b等)为ram、rom等存储器装置、硬盘等的固定盘装置、软盘和光盘等的存储单元,贮藏用于各种处理或提供网址的各种程序、表格、数据库和网页用文件等。
另外,生长诱导控制装置100或外部设备200可以作为已知的个人电脑、工作站等的信息处理装置构成,另外,也可以将任意的周边装置连接于该信息处理装置而构成。另外,生长诱导控制装置100或外部设备200也可以通过在该信息处理装置安装实现本发明的方法的软件(包含程序、数据等)而实现。
进而,装置的分散、合并的具体形态并不限于图示,可以将其全部或一部分根据各种附加等或根据功能负荷,以任意的单位,功能性或物理性地进行分散、合并而构成。即,可以任意地组合上述的实施方式而实施,也可以选择性地实施实施方式。
<现有技术的说明和对比>
予以说明,作为对现有技术的补充,进行现有技术的构成、工作的说明。专利文献2(日本特开2001-120261)中,提供一种使造血细胞祖细胞进行分化、控制造血的手段。具体而言,将人干细胞进行回流培养,以含有造血增殖因子的培养液从设置于旁边的人造血祖细胞的回流培养系统流入人干细胞的回流培养系统的方式进行设定。其结果,来自人干细胞的造血被促进。
专利文献3(日本特表2013-510590)中,提供一种用于使用生物反应器或其它装置及构成要素使组织和脏器生长或进行分析的物品和方法。该专利文献3中,(专利文献2中的人造血祖细胞那样的)细胞因子分泌细胞和人干细胞那样的生长诱导对象的组织配置于同一回流培养系统,所分泌的细胞因子随着培养液而达到生长诱导对象的组织,使生长诱导对象的组织生长、分化。
专利文献4(日本特表2008-513013)中,公开有将分泌细胞因子的多种细胞同时进行培养,适当变更流路而任意地使特定种类的生长分化细胞因子作用于观察对象的细胞和组织的方法。
<现有技术和本实施方式的比较>
相对于专利文献2,本实施方式中,细胞因子分泌细胞和生长诱导对象的组织串联地配置于相同的回流培养系统(環流培養形)上,生长、分化的结构和控制方法不同。
相对于专利文献3,本实施方式中,成为多种细胞因子分泌细胞能够作用于生长诱导对象的组织的结构,实现更复杂的细胞因子的控制。
相对于专利文献4,本实施方式中,成为不仅多种细胞因子分泌细胞能够作用于生长诱导对象的组织,而且细胞因子分泌细胞彼此能够相互作用的结构,实现更复杂的细胞因子代谢。由此,对于生长诱导对象的组织,能够进行更细致的利用细胞因子的控制。
在细胞的增殖、分化、或者组织或脏器的发育中,在不同的阶段中需要不同的细胞因子,但本实施方式中,能够提供根据阶段而得到不同的细胞因子的手段。更具体而言,多种细胞因子分泌细胞a和b串联地配置在可变更顺序的流路上,进行回流培养。在此,配置于下游的细胞因子分泌细胞b响应配置于上游的细胞因子分泌细胞a所分泌的细胞因子a,切换为能够不分泌本来的b而分泌另一种细胞因子c的构成。
通过细胞因子分泌的控制,能够控制未分化的细胞的增殖或分化、未成熟的组织或脏器的生长或分化。作为应用上的利用,也可以进行对脏器的长期保存、或脏器对外在原因的反应等的观察。细胞因子分泌细胞的切换通过利用各种传感器的自动或手动的方式变更培养液的流路来控制。
<参考专利文献>
1.专利第5881422号“脏器或组织的灌注培养方法和灌注培养装置”
2.日本特开2001-120261号公报“含人干细胞的组合物的培养方法和形态切换方法”
3.日本特表2013-510590号公报“用于形成和/或分析脏器的生物反应器、系统及方法”
4.日本特表2008-513013号公报“细胞培养用的灌注生物反应器”
5.日本专利第5797113号“生物人工脏器制作方法”
(附记1)
一种生长诱导装置,其特征在于,具有:第一单元,其中,生长诱导对象为细胞或组织的情况下,使培养液遍布于培养层,将该生长诱导对象进行长期培养,生长诱导对象为脏器的情况下,使培养液遍布于培养脏器的血管,将该生长诱导对象进行长期间培养;
第二单元,其使培养液遍布于分泌细胞因子的细胞种,将培养脏器进行长期培养;
第三单元,其使分泌细胞因子的细胞种分泌细胞因子;
第四单元,其使细胞因子所含的培养液遍布于上述生长诱导对象的培养层或培养脏器;和
第五单元,其控制细胞因子所含的培养液的流量。
(附记2)
一种生长诱导装置,其为细胞、组织或脏器的生长诱导装置,其特征在于,具有:
第一种细胞因子分泌细胞或组织(50)、
保存细胞因子分泌细胞或组织(50)的细胞因子分泌组织贮藏装置(60)、
第二种细胞因子分泌细胞或组织(51)、
保存细胞因子分泌脏分泌细胞或组织(61)的细胞因子分泌细胞或组织贮藏装置(61)、
调节培养液向贮藏装置(60)的流入量的阀(1-00)、
调节培养液向贮藏装置(61)的流入量的阀(1-01)、
调节贮藏装置(60)和贮藏装置(61)之间的培养液的流量的阀(1-11)、
调节培养液从贮藏装置(60)的流出量的阀(1-20)、
调节培养液从贮藏装置(61)的流出量的阀(1-21)、
在其下游设为生长诱导对象的细胞、组织或脏器(41)、
保存细胞、组织或脏器(41)的容器(40)、
检测细胞、组织或脏器41的状态的传感器部(70)、
接受传感器(70)的信号等来自外部的输入的输入部(80)、和
基于来自输入部(80)的信号控制阀(1-00、1-01、1-11、1-20、1-21)的开闭的阀开闭控制部(90)。
(附记3)
如附记2所述的生长诱导装置,其特征在于,还具有:
第三种细胞因子分泌细胞或组织(52)、
保存细胞因子分泌细胞或组织(52)的细胞因子分泌细胞或组织贮藏装置(62)、
调节培养液向贮藏装置(62)的流入量的阀(1-02)、
调节贮藏装置(60)和贮藏装置(62)之间的培养液的流量的阀(1-10)、
调节贮藏装置(61)和贮藏装置(62)之间的培养液的流量的阀(1-12)、和
调节培养液从贮藏装置(62)的流出量的阀(1-22)。
(附记4)
如附记2或3所述的生长诱导装置,其特征在于:
细胞因子分泌细胞或组织(50)的贮藏装置(60)还具有包括泵(611)、气体交换部(612)、透析部(613)的回流系统。
(附记5)
如附记2~4中任一项所述的生长诱导装置,其特征在于,还具有:
在流路上的阀(1-00、1-01、1-02、1-10、1-11、1-12、1-20、1-21、1-22)的位置上将具有柱、过滤器、阀的流路分支点等的气泡、细胞或细胞碎片、其它的垃圾等异物从流路系统中除去的机构。
(附记6)
如附记2~5中任一项所述的生长诱导装置,其特征在于,具有:
在流路上的阀(1-00、1-01、1-02、1-10、1-11、1-12、1-20、1-21、1-22)的任意个或全部的位置上通过加热、过滤、吸附、选择性化学反应等将特定的有机化合物、无机化合物、蛋白质等化合物利用分解、除去、失活等方法使其生理学的活性丧失的机构。
(附记7)
如附记2~6中任一项所述的生长诱导装置,其特征在于,还具有:
将氧供给至培养液,排出二氧化碳的气体交换部(20)、和
从培养液中除去废物的透析部(30),
该生长诱导装置将培养液进行回流并再使用。
(附记8)
如附记2~7中任一项所述的生长诱导装置,其特征在于,
保存细胞、组织或脏器(40)的容器(41)具有不使细胞或细胞碎片或其它垃圾通过的过滤器或除去装置(130)。
(附记9)
一种生长诱导方法,其特征在于,包括用于实现附记2~8中任一项所述的生长诱导装置的功能的各步骤。
(附记10)
一种生长诱导方法,其特征在于,包括:
第一步骤,生长诱导对象为细胞或组织的情况下,使培养液遍布于培养层,将该生长诱导对象进行长期培养,生长诱导对象为脏器的情况下,使培养液遍布于培养脏器的血管,将该生长诱导对象进行长期培养;
第二步骤,使培养液遍布于分泌细胞因子的细胞种,将培养脏器进行长期培养;
第三步骤,使分泌细胞因子的细胞种分泌细胞因子;
第四步骤,使细胞因子所含的培养液遍布于上述生长诱导对象的培养层或培养脏器;和
第五步骤,控制细胞因子所含的培养液的流量。
(附记11)
一种生长诱导程序,其用于在电脑中实行如下方法,该方法包括:
第一步骤,生长诱导对象为细胞或组织的情况下,使培养液遍布于培养层,将该生长诱导对象进行长期培养,生长诱导对象为脏器的情况下,使培养液遍布于培养脏器的血管,将该生长诱导对象进行长期培养;
第二步骤,使培养液遍布于分泌细胞因子的细胞种,将培养脏器进行长期培养;
第三步骤,使分泌细胞因子的细胞种分泌细胞因子;
第四步骤,使细胞因子所含的培养液遍布于上述生长诱导对象的培养层或培养脏器;和
第五步骤,控制细胞因子所含的培养液的流量。
工业上的可利用性
如以上详述中说明的那样,根据本发明,能够提供不需要在脏器的每个生长阶段添加生长因子而能够抑制成本地进行培养的生长诱导装置、生长诱导方法和生长诱导程序。
符号说明
1阀
10泵
20气体交换部
30透析部
40培养槽(容器)
41细胞组织
50、51分泌组织
60、61、62分泌组织贮藏装置
70传感器
80输入设备
90控制部
100生长诱导控制装置
102控制部
102a生长状况检测部
102b流量控制部
104通信控制接口部
106存储部
106a生长诱导文件
106b培养槽配置文件
108输入输出控制接口
112输入部
114输出部
130异物除去机构
200外部设备
300网络
601泵
602气体交换部
603透析部
901培养步骤数据
902培养步骤数据库
903配置信息
904阀开闭步骤制作部
905阀开闭控制部
- 还没有人留言评论。精彩留言会获得点赞!