人多能干细胞来源的外泌体、基于该外泌体的制剂及用途的制作方法
本发明属于细胞生物学、分子生物学及药物研发技术领域,尤其是涉及人多能干细胞来源的外泌体、基于该外泌体的制剂及其用途。
背景技术:
随着年龄的增长,人体各器官机能均会出现逐渐衰老,并引发相关疾病的发生。随着我国社会老龄化加剧,心脑血管疾病、骨与关节疾病、神经系统疾病以及代谢性疾病等的发病率显著上升,老年性疾病的危害日益突出。目前全世界有超过2亿的骨质疏松患者,而年龄超过50岁的女性中有1/3发生骨质疏松骨折,有很高的致残、致死率,严重威胁大众健康,带来极大的社会经济负担。此外,骨关节炎是一种在临床上非常常见的慢性退行性疾病,被列为老年人行动能力下降的首要病因,严重影响人们的生活质量。研发能有效防治骨退行性疾病发生与发展的技术显得尤为重要。
干细胞再生医学技术是当前最有可能防治这些退行性疾病的技术,研究表明,移植成体干细胞或诱导人多能干细胞分化来的组织前体细胞治疗相关疾病具有明显疗效。但是,直接移植干细胞始终面临着细胞变异、致瘤风险、运输保存困难、难以产业化等问题。近年人们发现,干细胞产生的外泌体,具有与干细胞高度类似的功能,也可以促进组织再生,因此引起了广大学者的极大关注,为干细胞再生医学技术的转化应用带来了新的希望。
外泌体是一类由细胞分泌的直径约30-150nm的细胞外囊泡,其携带供体细胞来源的多种生物活性物质包括dna、rna、蛋白等进入效应细胞,有效调控机体细胞信号转导。研究表明,干细胞分泌的外泌体通过向效应细胞传递干细胞来源的生物活性物质,生理性修复或者清除机体损伤、病变和衰老的细胞,发挥抗炎、调节免疫、促进效应细胞增殖、迁移和分化、促进血管新生等功能。
由于诱导人多能干细胞具有与胚胎干细胞相似的全能性,其分泌的外泌体可能包裹了与多能性相关的因子、转录因子、mrna、microrna等,表现出比成体组织干细胞外泌体更强大的功能。人多能干细胞产生的外泌体,可以抑制细胞衰老过程,改变靶细胞表观遗传特征,使效应细胞逆转至低分化状态,从而促进修复组织损伤。同时人多能干细胞来源的外泌体,也可以起到与组织干细胞类似的作用,如修复血管、抑制炎症、促进组织干细胞增殖分化等功能。
胚胎干细胞(embryonicstemcell,escs)与诱导人多能干细胞(inducedpluripotentstemcells,ipscs)具有体外培养无限增殖、自我更新和多向分化的特性。escs和ipscs具有多能性(pluripotency),即escs和ipscs可分化成三胚层的任意细胞,具有发育成多种组织的能力,参与部分组织的形成。而成体干细胞仅具备多种分化潜能(multipotency),即只能分化成为有限的几种细胞。因而escs和ipscs与组织成体干细胞相比在促进组织器官再生更新方面功能更强大。但由于escs或ipscs存在致瘤性,所以不能直接移植用于疾病的防治。而escs或ipscs分泌的外泌体可能包裹了与多能性相关的因子、转录因子、mrna、microrna等,可能表现出比成体组织干细胞外泌体更强大的功能。
虽然已有不少文献及专利报道了干细胞来源的外泌体在修复组织损伤中的应用,如已有报道骨髓间充质干细胞分泌的外泌体具有促进骨再生修复骨缺损的功能,由ipscs定向诱导得到的间充质干细胞(ipscs-mscs)所分泌的外泌体也具有促进骨再生、血管新生、软骨再生,用于修复下肢缺血、皮肤创面、骨折、颅骨缺损、骨性关节炎、骨坏死等的修复治疗。中国授权专利cn101890050a公开了脐带间质干细胞来源膜性囊泡(外泌体)在治疗肝、肾或皮肤损伤疾病方面的功能。以上报道的均属于成体干细胞,由于escs或ipscs属人多能干细胞,具有比成体干细胞更强的促进组织再生和抗衰老功能,其分泌的外泌体也应具有类似的强大功能。但目前尚未见直接应用escs或ipscs分泌的外泌体防治骨退行性疾病的研究报道。
技术实现要素:
本发明的目的就是为了提供一种功能更强大的人多能干细胞(即escs或ipscs)来源的外泌体、其制备方法、基于该外泌体的制剂及其制剂在防治骨科疾病方面的用途。
本发明的目的可以通过以下技术方案来实现:
本发明第一方面:
提供一种人多能干细胞外泌体的制备方法,包括以下步骤:
采用无饲养层培养方法,在无血清培养体系培养人escs或ipscs,收集培养基,收集纯化培养基中的外泌体。
在一种实施方式中,无血清培养体系选择市售的型号为tesrtm-e8tm或mtesr1的培养基。
在一种实施方式中,收集纯化培养基中的外泌体的方法为:通过旋转超滤结合低温超速离心方法收集纯化培养基中的外泌体。
在一种实施方式中,收集外泌体后,通过电镜、粒径分析、免疫印迹等方法对外泌体的特性进行鉴定,结果符合外泌体特征:直径范围50-150nm,透射电子显微镜下呈双层膜囊状结构,其膜结构表面含有cd9,cd63等标志物。
本发明第二方面:
提供一种人多能干细胞外泌体,其采用本发明第一方面的制备方法获得。
所述人多能干细胞外泌体包括人escs外泌体与人ipscs外泌体。
在一种实施方式中,所述人多能干细胞外泌体采用深低温保存,所述深低温保存指-80℃以下保存。
本发明第三方面:
提供基于所述人多能干细胞外泌体的制剂。
a、悬浮剂:所述人多能干细胞外泌体溶于溶剂中,以悬浮剂的形式存在,其溶剂为生理盐水或磷酸盐缓冲液或基础细胞培养基。
基于所述人多能干细胞外泌体的悬浮剂以人多能干细胞外泌体为功效成分。
基于所述人多能干细胞外泌体的悬浮剂可通过口服、静脉注射,或直接在组织损伤部位注射(如关节腔内注射、骨折处注射等)或喷雾等形式进行使用。
b、缓释外泌体的复合物:由人多能干细胞外泌体与载体结合形成缓释外泌体的复合物。
所述载体包括各种水凝胶、生物膜、生物陶瓷材料、纳米结构的生物材料等。
所述缓释外泌体的复合物采用植入组织损伤部位的形式使用。
c、含有人多能干细胞外泌体的添加剂:以人多能干细胞外泌体作为功效成分的添加剂。
含有人多能干细胞外泌体的添加剂可以加入到各种药物中用于疾病的治疗,或加入到各种培养体系用于各种细胞培养。
本发明第四方面:
提供人多能干细胞外泌体的用途。
a、作为体外培养的维持成体干细胞的干性而抑制其衰老的添加剂应用:
所述成体干细胞包括间充质干细胞与组织特异干细胞,所述的间充质干细胞包括各种组织来源的间充质干细胞,如脂肪间充质干细胞、骨髓间充质干细胞、滑膜间充质干细胞、尿液来源的间充质干细胞、牙髓间充质干细胞、脐带间充质干细胞、胎盘间充质干细胞、羊膜间充质干细胞等;所述组织特异干细胞包括肝干细胞、内皮祖细胞、神经干细胞、胰岛干细胞、上皮干细胞、肾脏干细胞、肺上皮干细胞、表皮干细胞、毛囊干细胞、角膜缘干细胞、黑色素干细胞、汗腺干细胞、肌腱干细胞、软骨前体细胞等。
在一种实施方式中,将人多能干细胞外泌体或基于人多能干细胞外泌体的制剂按比例加到体外培养的人成体干细胞的培养基中,观察其对所培养的人成体干细胞的干性维持及抑制老化的效果。
b、作为体外培养的维持各种组织原代培养细胞的增殖活性的添加剂应用:
所述组织原代培养细胞包括血管内皮细胞、皮肤黑色素细胞、表皮细胞、肝上皮细胞、神经细胞、角膜上皮细胞、角膜内皮细胞、成纤维细胞、胰岛β细胞、成骨细胞、软骨细胞和破骨细胞等。
c、在制备治疗骨与软骨退行性病变的药物中的应用,或作为治疗骨与软骨退行性病变的药物应用:
在一种实施方式中,以静脉注射或口服或患处直接局部注射或喷涂人多能干细胞外泌体或基于人多能干细胞外泌体的制剂,观察外泌体对动物骨质疏松、骨关节炎的逆转效果。
实验过程中,以衰老动物为实验模型,静脉注射或口服或患处直接局部注射或喷涂人多能干细胞外泌体或基于人多能干细胞外泌体的制剂,观察外泌体对衰老动物骨质疏松、骨关节炎的逆转效果。
d、在制备预防骨与软骨退行性病变的药物中的应用,或作为预防骨与软骨退行性病变的药物应用:
在一种实施方式中,以静脉注射或口服或患处直接局部注射或喷涂人多能干细胞外泌体或基于人多能干细胞外泌体的制剂,观察外泌体对其骨质疏松、骨关节炎发生的预防效果。
实验过程中,以年轻动物为实验模型,静脉注射或口服或患处直接局部注射或喷涂人多能干细胞外泌体或基于人多能干细胞外泌体的制剂,随着实验动物的年龄增长,观察外泌体对其骨质疏松、骨关节炎发生的预防效果。
e、在制备治疗骨坏死、骨不连、骨折、软骨损伤、肌腱损伤、冰冻肩或肌腱粘连等骨科疾病的药物中的应用,作为治疗骨坏死、骨不连、骨折、软骨损伤、肌腱损伤、冰冻肩、肌腱粘连等骨科疾病的药物应用:
在一种实施方式中,以静脉注射或口服或患处直接局部注射或喷涂人多能干细胞外泌体或基于人多能干细胞外泌体的制剂。
实验过程中,构建骨坏死、骨不连、骨折、软骨损伤、肌腱损伤动物模型,静脉注射或口服或患处直接局部注射或喷涂人多能干细胞外泌体或基于人多能干细胞外泌体的制剂。
本发明第五方面:
提供基于人多能干细胞外泌体的制剂的用途。
a、作为体外培养的维持成体干细胞的干性而抑制其衰老的添加剂应用:
所述成体干细胞包括间充质干细胞与组织特异干细胞,所述的间充质干细胞包括各种组织来源的间充质干细胞,如脂肪间充质干细胞、骨髓间充质干细胞、滑膜间充质干细胞、尿液来源的间充质干细胞、牙髓间充质干细胞、脐带间充质干细胞、胎盘间充质干细胞、羊膜间充质干细胞等;所述组织特异干细胞包括肝干细胞、内皮祖细胞、神经干细胞、胰岛干细胞、上皮干细胞、肾脏干细胞、肺上皮干细胞、表皮干细胞、毛囊干细胞、角膜缘干细胞、黑色素干细胞、汗腺干细胞、肌腱干细胞、软骨前体细胞等。
在一种实施方式中,将人多能干细胞外泌体或基于人多能干细胞外泌体的制剂按比例加到体外培养的人成体干细胞的培养基中,观察其对所培养的人成体干细胞的干性维持及抑制老化的效果。
b、作为体外培养的维持各种组织原代培养细胞的增殖活性的添加剂应用:
所述组织原代培养细胞包括血管内皮细胞、皮肤黑色素细胞、表皮细胞、肝上皮细胞、神经细胞、角膜上皮细胞、角膜内皮细胞、成纤维细胞、胰岛β细胞、成骨细胞、软骨细胞和破骨细胞等。
c、在制备治疗骨与软骨退行性病变的药物中的应用,或作为治疗骨与软骨退行性病变的药物应用:
在一种实施方式中,以静脉注射或口服或患处直接局部注射或喷涂人多能干细胞外泌体或基于人多能干细胞外泌体的制剂,观察外泌体对动物骨质疏松、骨关节炎的逆转效果。
实验过程中,以衰老动物为实验模型,静脉注射或口服或患处直接局部注射或喷涂人多能干细胞外泌体或基于人多能干细胞外泌体的制剂,观察外泌体对衰老动物骨质疏松、骨关节炎的逆转效果。
d、在制备预防骨与软骨退行性病变的药物中的应用,或作为预防骨与软骨退行性病变的药物应用:
在一种实施方式中,以静脉注射或口服或患处直接局部注射或喷涂人多能干细胞外泌体或基于人多能干细胞外泌体的制剂,观察外泌体对其骨质疏松、骨关节炎发生的预防效果。
实验过程中,以年轻动物为实验模型,静脉注射或口服或患处直接局部注射或喷涂人多能干细胞外泌体或基于人多能干细胞外泌体的制剂,随着实验动物的年龄增长,观察外泌体对其骨质疏松、骨关节炎发生的预防效果。
e、在制备治疗骨坏死、骨不连、骨折、软骨损伤、肌腱损伤、冰冻肩或肌腱粘连等骨科疾病的药物中的应用,作为治疗骨坏死、骨不连、骨折、软骨损伤、肌腱损伤、冰冻肩、肌腱粘连等骨科疾病的药物应用:
在一种实施方式中,以静脉注射或口服或患处直接局部注射或喷涂人多能干细胞外泌体或基于人多能干细胞外泌体的制剂。
实验过程中,构建骨坏死、骨不连、骨折、软骨损伤、肌腱损伤动物模型,静脉注射或口服或患处直接局部注射或喷涂人多能干细胞外泌体或基于人多能干细胞外泌体的制剂。
与现有技术相比,本发明具有以下优点及有益效果:
本发明人多能干细胞来源的外泌体是来自escs或ipscs多能干细胞,现有技术主要是研究成体干细胞来源的外泌体;escs和ipscs具有多能性(pluripotency),即escs和ipscs可分化成三胚层的任意细胞,具有发育成多种组织的能力,参与部分组织的形成。而成体干细胞仅具备多种分化潜能(multipotency),即只能分化成为有限的几种细胞。多能干细胞促进组织细胞再生防治衰老的功能明显比成体干细胞强。多能干细胞分泌的外泌体亦具有强大的促进组织细胞再生,防治衰老,治疗骨类疾病的功能,因而显示出更大的应用价值。
附图说明
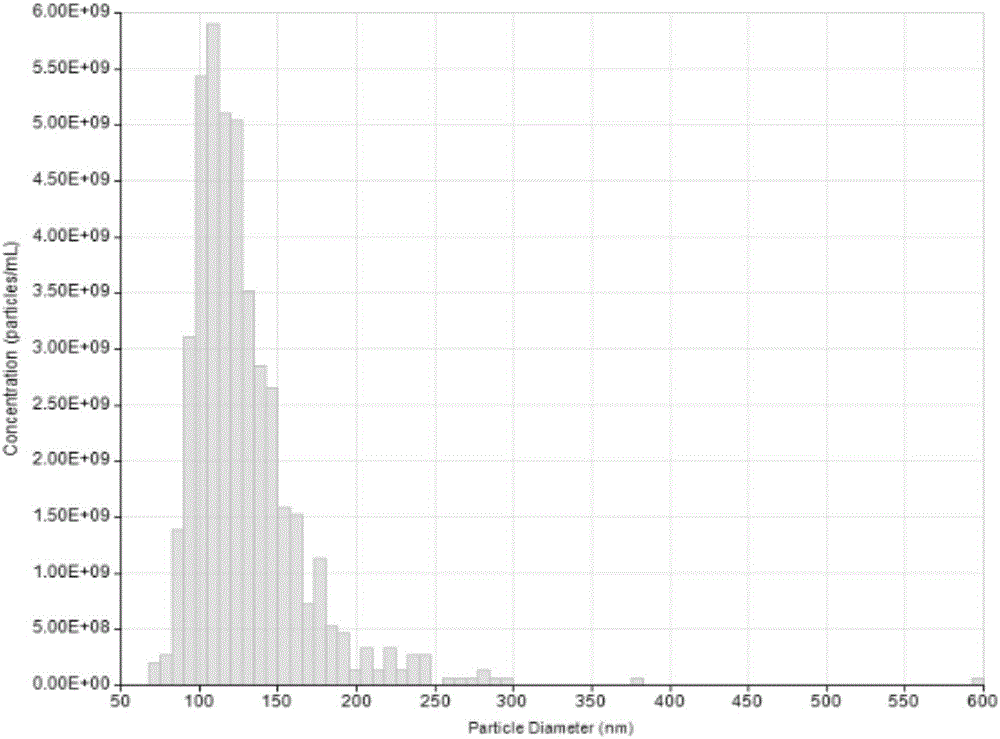
图1人多能干细胞分泌的外泌体(es-exo)粒径分布图;
图2外泌体标志物鉴定;
图3microct扫描结果;a组:对照组;b组:治疗实验组;c组:预防实验组。
a组与b组及c组比较,骨皮质变薄,骨小梁稀疏,骨质疏松较明显;c组与b组比较骨质疏松现象减轻。
图4碱性磷酸酶和抗酒石酸酸性磷酸酶elisa检测结果。
*表示与对照组相比差异显著(p<0.05).
图5runx2、osterix基因pcr检测结果。
*表示与对照组相比差异显著(p<0.05).
图6runx2、osterix蛋白westernblot检测结果。
图7he染色结果。
模型组(a)骨小梁明显变少,形态变薄,骨细胞出现空泡和核固缩;es-exo干预组(b)骨小梁有轻度坏死,少见骨细胞的空泡变性;对照组(c)正常骨组织。
图8microct扫描结果。
模型组(a)的骨小梁显著减少,且出现结构完全消失的区域;es-exo干预组(b)的骨小梁结构保持相对完整;对照组(c)正常骨组织。
图9血管造影结果。
模型组(a)的血管数明显减少;es-exo干预组(b)的血管数目明显多于模型组;对照组(c)正常骨组织。
图10高倍组织学显微镜下观察关节面的照片。
正常对照组(a)和es-exo治疗组(b)可见正常软骨表现,而关节炎模型组(c)可见软骨磨损,软骨下骨暴露,表面纤维组织增生。
图11micro-ct扫描结果。
模型组(c)只有少量的新生骨;β-tcp移植组(b)有新生骨生成,但骨缺损的两端并没有连接;在es-exo/β-tcp组(a)有大量的新生骨,新生的骨痂把缺损部位完全连接。
图12bmscs培养至p10时的镜下形态。
a示常规培养基培养的bmscs;b示在含有es-exo的培养基中培养的bmscs。
图13p10代bmscs在含有es-exo的培养基和常规培养基中培养的生长曲线。
图14衰老细胞染色结果。b中染色部分为β半苷乳糖酶阳性,示衰老细胞。
具体实施方式
下面结合附图和具体实施例对本发明进行详细说明。
实施例1:
人胚胎干细胞(escs)的培养和外泌体的提取与鉴定
在培养皿中铺一层胚胎干细胞基质胶(esc-qualifiedbdmatrigel,bd
es-exo的形态通过透射电镜(tem)观察。将载样铜网(孔径2nm)固定在支架上,将20μl样本滴加到铜网上,室温静置3分钟后,在铜网一侧用滤纸将液体吸去,滴加3%磷钨酸溶液30μl对样本进行负染(室温,5分钟)。用滤纸吸去负染液,将铜网转移至透射电子显微镜下,观察外泌体形态。
es-exo的粒径和浓度通过纳米粒子分析系统(izonqnano,newzealand)进行检测,按照操作说明书调节仪器各项参数:将nanopore(np100)安装到加样孔下方,调节stretch至43cm,向加样孔内加入40μlpbs,使电流稳定在100-120na范围内。吸去pbs,加入40μl1:100稀释的cpc100标准品(粒径70nm),测量粒子数和浓度,通过软件得到标准曲线。吸去标准品,pbs洗3次,加入40μl1:1000稀释的待测样品,测定粒子数和浓度,重复测量3次。通过软件进行数据分析,得出分析报告。结果显示粒径范围为50-150nm,见图1。
通过westernblot检测es-exo特异性表面标志物cd9和cd63的表达。具体步骤:外泌体总蛋白提取,通过bca蛋白分析试剂盒检测样本蛋白浓度,制胶配制10%的分离胶,电泳,转膜,封闭及抗体孵育,化学发光成像分析仪观察条带显影情况。结果所提取的外泌体均表达特异性表面标志物cd9和cd63。见图2。
人诱导人多能干细胞(ipscs)的培养和外泌体的提取与鉴定
在培养皿中铺一层胚胎干细胞基质胶(esc-qualifiedbdmatrigel,bd
ips-exo的形态通过透射电镜(tem)观察。将载样铜网(孔径2nm)固定在支架上,将20μl样本滴加到铜网上,室温静置3分钟后,在铜网一侧用滤纸将液体吸去,滴加3%磷钨酸溶液30μl对样本进行负染(室温,5分钟)。用滤纸吸去负染液,将铜网转移至透射电子显微镜下,观察外泌体形态。
ips-exo的粒径和浓度通过纳米粒子分析系统(izonqnano,newzealand)进行检测,按照操作说明书调节仪器各项参数:将nanopore(np100)安装到加样孔下方,调节stretch至43cm,向加样孔内加入40μlpbs,使电流稳定在100-120na范围内。吸去pbs,加入40μl1:100稀释的cpc100标准品(粒径70nm),测量粒子数和浓度,通过软件得到标准曲线。吸去标准品,pbs洗3次,加入40μl1:1000稀释的待测样品,测定粒子数和浓度,重复测量3次。通过软件进行数据分析,得出分析报告。
通过westernblot检测ips-exo特异性表面标志物cd9和cd63的表达。具体步骤:外泌体总蛋白提取,通过bca蛋白分析试剂盒检测样本蛋白浓度,制胶配制10%的分离胶,电泳,转膜,封闭及抗体孵育,化学发光成像分析仪观察条带显影情况。结果所提取的外泌体均表达特异性表面标志物cd9和cd63。
实施例2
人多能干细胞来源的外泌体对骨质疏松的防治作用
预防实验:选择6月龄samp6快速衰老小鼠模型,实验分二组,每组10只小鼠,实验组每天灌胃给予人2~5×108个的es-exo或ips-exo进行干预,对照组灌胃相同体积的生理盐水。分别于干预后3个月处死老鼠,取材检测。
治疗实验:选择8月龄的samp6快速衰老小鼠模型,实验分二组,每组10只小鼠,实验组每天灌胃给予人2~9×108个的es-exo进行干预,对照组灌胃相同体积的生理盐水。于干预后3个月处死老鼠,取材检测。
老鼠处死前留取血液,elisa法测定血清抗酒石酸酸性磷酸酶和骨碱性磷酸酶水平。留取每只小鼠的股骨,按检测指标的要求分别保存。小动物断层扫描系统(microct)对骨组织进行扫描,检测骨组织显微结构,评估骨组织微结构的参数包括相对骨体积(bv/tv)、连接密度(conn.dn)、骨小梁数量(tb.n)、骨矿物质密度(bmd)、骨小梁厚度(tb.th)和结构模型指数(smi)。通过实时定量荧光pcr技术检测调控骨再生的基因runx2、osterix基因的表达水平。westernblot检测runx2、osterix蛋白表达水平。组织病理学和免疫组化检测:截取股骨,生理盐水冲洗后置于甲醛溶液固定(4℃,24-48h),通过乙二胺四乙酸(edta)脱钙处理,使用乙醇溶液梯度脱水,二甲苯透明,石蜡纵向包埋骨组织,厚度为5um连续切片,用于苏木素一伊红(he)染色、trap染色、masson染色以及免疫组化染色。
通过苏木精-伊红染色结果显示,对照组的骨结构破坏与预防实验组和治疗实验组相比明显严重,预防实验组和治疗实验组的股骨有新生的骨小梁形成,且骨小梁结构完整、数目较多,可见成骨细胞多于对照组。microct检测结果显示,对照组骨皮质变薄,骨小梁稀疏,骨质疏松明显;与对照组相比,预防实验组和治疗实验组的骨皮质较厚,骨小梁较密。见图3。
实验结果显示,与对照组相比,治疗实验组的碱性磷酸酶水平明显升高,抗酒石酸酸性磷酸酶水平明显降低,差异均有显著性意义(p<0.05),见图4。治疗实验组的调控骨形成的runx2、osterix基因水平均显著高于对照组(p<0.05),见图5;治疗实验组的runx2、osterix蛋白表达水平均显著高于对照组(p<0.05),见图6。
以上结果提示,人多能干细胞来源的外泌体对骨质疏松的发生与发展具有明显的防治作用。
实施例3
人胚胎干细胞来源的外泌体对股骨头缺血坏死的防治作用
人胚胎干细胞的培养和外泌体的提取同实施例1。实验采用300-320g的雄性sd大鼠制作激素诱导性股骨头坏死模型:sd大鼠肌注甲泼尼龙(40mg/kg),每周3次,持续3周。实验分组:模型组(激素诱导股骨头坏死,n=10);es-exo干预组(激素诱导的同时静脉给予es-exo进行干预,n=10);正常对照组(给予同等剂量的pbs,n=10)。所有注射完成后,将大鼠置于笼中正常饲养3周。然后取材评估股骨头血管新生情况和骨坏死情况。
通过microct(skyscan,1076scanner,kontich,belgium)检测股骨头骨性结构的变化情况:将股骨头标本置于检测平台,分辨率调节至18mm后进行断层扫描,通过nrecon软件(version1.5.1.4,skyscan)重建股骨头3d图像,并计算骨体积/总体积(bv/tv),骨表面积/骨体积,骨小梁厚度(tb.th)和骨小梁数量(tb.n)。通过微血管造影观察股骨头部位的血管分布和密度改变:将各组大鼠麻醉后,剪开胸腔和腹腔,结扎升主动脉,用静脉输液针穿刺左心室,用肝素生理盐水冲洗心腔,用4%多聚甲醛固定组织和血管,然后向心室输注microfil造影剂(microfilmv-122,flowtech,carver,ma,usa),将灌注好的大鼠置于4℃冰箱过夜,然后将股骨头取下,用4%多聚甲醛固定,用10%edta进行脱钙处理,标本最后进行microct检测。组织学染色:将已脱钙后的标本进行石蜡包埋,切片,每张切片5μm厚,he染色,光学显微镜下观察。
实验结果:he染色结果显示,模型组骨小梁明显变少,形态变薄,骨细胞出现空泡和核固缩;es-exo干预组骨小梁有轻度坏死,少见骨细胞的空泡变性(图7);es-exo干预组的空泡的比例为15.5±2.1%,显著低于模型组的38±4.8%(p<0.05)。microct检测结果显示,模型组的骨小梁显著减少、变薄,且出现骨小梁结构完全消失的区域;es-exo干预组的骨小梁结构保持相对完整(图8),bv/tv、tb.th和tb.n值均显著高于模型组(p<0.05)。血管造影结果显示,es-exo干预组的血管数目明显多于模型组(图9),且血管体积及百分比、血管表面积和血管厚度均明显高于模型组(p<0.05)。
以上实验结果提示,es-exo可以防止股骨头坏死的发生与发展。
实施例4
人胚胎干细胞来源的外泌体防治骨性关节炎
人胚胎干细胞的培养和外泌体的提取同上。选择6-8周龄c57小鼠制作骨性关节炎模型(模型组):小鼠麻醉后置于鼠板上,暴露膝关节,剃毛,碘伏消毒,膝关节正中切开,显微镜下分离出膝关节,微量注射器注入5-10ul胶原酶vii。es-exo治疗组:于造模后第7、14、21天,分别关节腔注射es-exo5-10μl(1~9×1010/ml)。关节炎模型组和正常对照组于关节腔注射相同体积的pbs。于造模后第28天处死各组小鼠,小鼠处死后在膝关节水平离断胫骨。大体观察:于显微镜下分离胫骨平台周围组织及半月板,充分展示胫骨平台关节面,高倍组织学显微镜下观察关节面并拍照。组织学检测:edta溶液脱钙1周,石蜡包埋,胫骨平台冠状位切片,5um厚度,行he染色、番红-固绿染色、免疫组化染色(col-1,col-2)。
实验结果显示,关节炎模型组可见软骨磨损,软骨下骨暴露,表面纤维组织增生;而正常对照组和es-exo治疗组可见正常软骨表现,见图10。组织学检测结果显示,正常对照组和es-exo治疗组可见典型透明软骨外观,软骨面光滑,软骨细胞排列整齐,胶原含量正常;关节炎模型组呈软骨磨损,骨坠形成,胶原含量减少,表面纤维组织增生。icrs评分结果:正常对照组=es-exo治疗组>关节炎模型组;免疫组化染色结果显示,正常对照组和es-exo治疗组col-2呈强阳性(深棕色)、col-1染色呈阴性;而关节炎模型组col-2着色很浅;col-1染色呈强阳性(深棕色)。
以上实验结果提示,es-exo可以防止骨性关节炎的发生与发展
实施例5
人胚胎干细胞来源的外泌体负载于β-tcp修复大段骨缺损
人胚胎干细胞的培养和外泌体的提取同上。选择具有三维多孔纳米结构的磷酸三钙(β-tcp)吸附一定浓度的es-exo。采用sd雄性大鼠(300±50g)构建大段骨缺损模型。实验分三组:模型组(即造模后不做任何干预)、β-tcp移植组(造模后在骨缺损处移植β-tcp)和es-exo/β-tcp移植组(造模后在骨缺损处移植es-exo/β-tcp)。大鼠麻醉固定后,暴露股骨中段,电钻钻孔后,股骨近端与远端各植入一枚螺钉将不锈钢接骨板固定在股骨上,然后采用牙科磨钻磨去股骨中段6mm长骨组织,分别将β-tcp和uscs/β-tcp移植到缺损部位并固定,模型对照组不植入任何材料。术后4和8周进行x线检查,观察材料降解及骨缺损的愈合修复情况。术后12周处死动物,取出手术股骨标本,4%多聚甲醛固定24h,应用小动物micro-ct对股骨标本进行扫描重建,具体扫描参数设置如下:电压600kv,电流300μa,扫描时间900ms,空间分辨率18μm。将股骨手术部位设置为roi,长度为15mm,其纵轴与股骨干纵轴平行。采用ctanalysis分析软件对原始数据进行分析,分析指标包括相对骨体积(bonevolume/tissuevolume,bv/tv)和骨密度(bonemineraldensity,bmd)。骨组织进行常规脱钙,通过常规he染色和masson染色显示骨缺损处新骨生成。
x线检查结果显示,模型组4周和8周都无明显新骨生成;β-tcp移植组在4周无明显新骨生成,在8周后材料逐步降解,可见新生骨生成;es-exo/β-tcp组在4周材料与断端结合部位有新生骨生成,在8周之后材料几乎完全降解,骨缺损部位长满新生骨。micro-ct结果显示,模型组只有少量的新生骨;β-tcp移植组有新生骨生成,但骨缺损的两端并没有连接,仍有大量的β-tcp填充在骨缺损部位;在es-exo/β-tcp组有大量的新生骨,新生的骨痂把缺损部位完全连接,只有少量的β-tcp在骨缺损处,见图11。进一步的骨密度(bonemineraldensity,bmd)分析显示,模型组、β-tcp移植组和es-exo/β-tcp移植组分别为683.1±38.6,844.5±65.7和854.5±68.7mg/cm3。骨体积分数(bonevolumefraction,bv/tv)分析显示模型组、β-tcp和es-exo/β-tcp移植组骨体积分数分别为6.8±2.9%,9.2±3.8%和18.3±3.2%。显示在es-exo/β-tcp移植组有更多的新生骨生成。he染色结果显示三组都无明显的炎症反应。he染色和masson三色染色都显示es-exo/β-tcp移植组有大量的新生骨;β-tcp组同样有新生骨但数量远小于es-exo/β-tcp移植组;在模型组无明显的新生骨,有大量的纤维结缔组织填充。
以上结果表明,es-exo负载生物材料能显著促进骨再生,修复临床棘手的大段骨缺损。
实施例6
人胚胎干细胞来源的外泌体抑制体外培养的骨髓间充质干细胞衰老
人胚胎干细胞的培养和外泌体的提取同上。人骨髓间充质干细胞(bmscs)的培养:经知情同意获得临床手术中废弃的骨组织,生理盐水冲洗松质骨,获得的细胞悬液,细胞经筛过滤后离心弃上清(300g,5分钟),用dmem完全培养基重悬后将其接种到细胞培养瓶中,置于细胞培养箱(37℃,5%co2)内培养。24小时后全量换液,以后每隔3天换液一次。待细胞培养瓶中的细胞克隆融合形成单层贴壁细胞后,用0.25%的胰蛋白酶消化细胞,用含血清的dmem培养基中止消化并离心弃上清(300g,5分钟),用dmem完全培养基重悬细胞并接种到新的细胞培养瓶中进行扩增。取生长良好的第5代细胞进行实验。实验分2组,一组按常规方法继续传代培养(对照组),另一组在细胞培养基中添加1x107/mles-exo,传代培养至对照组出现细胞增殖慢且形态老化时,用cck-8试剂盒检测细胞增殖活性,通过细胞衰老β半苷乳糖酶染色试剂盒检测二组细胞的衰老状况。
实验结果显示,常规培养方法培养的bmscs在传代培养到十代(p10)时细胞出现生长缓慢、颗粒增多、胞体变大等衰老形态,见图12.;cck-8检测结果显示用含有es-exo的培养基培养的细胞增殖能力明显强于对照组,见图13.;β半苷乳糖酶染色结果发现用含有es-exo的培养基培养的细胞胞浆呈蓝色的细胞很少,而常规培养的细胞出现大量胞浆呈蓝色的衰老细胞,见图14。结果表明,es-exo可有效防治体外培养的bmscs衰老。
上述的对实施例的描述是为便于该技术领域的普通技术人员能理解和使用发明。熟悉本领域技术的人员显然可以容易地对这些实施例做出各种修改,并把在此说明的一般原理应用到其他实施例中而不必经过创造性的劳动。因此,本发明不限于上述实施例,本领域技术人员根据本发明的揭示,不脱离本发明范畴所做出的改进和修改都应该在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!