两类3‑位含吡啶取代基团芳炔前体及其制备的制作方法
本发明属于有机化学的技术领域,具体涉及利用非传统1,2-二芳炔前体合成两类3-位含吡啶取代基团的芳炔前体及其制备。
背景技术:
含吡啶基团的多取代芳环结构广泛存在于天然产物、生物活性分子、药物分子和染料等有机化合物中。利用简单、快捷的方法制备含吡啶基团的多取代芳基化合物是合成有机化学中重要的研究方向之一。
本专利提出一种3-位含吡啶取代基团芳炔前体的高效合成方法,该方法使用的原料是非传统1,2-二芳炔前体和吡啶n-氧化物。并且,利用该方法合成的芳炔前体可以发生进一步反应,合成含吡啶取代基团的多取代芳基化合物。这种非传统1,2-二芳炔前体与传统的1,2-二芳炔前体所不同的是:此1,2-二芳炔前体含有一个离去基团,两个活化基团;而一般的1,2-二芳炔前体含有两个离去基团,一个活化基团。
具体实施方式
下面结合实施例对本发明作进一步说明:
本发明的两类3-位含吡啶取代基团芳炔前体的结构通式a,b如下:
由a,b的结构式可以看出两类3-位含吡啶取代基团芳炔前体的不同是:结构式a是3-位含芳炔前体取代基团的吡啶化合物,而结构式b是2-位含芳炔前体取代基团的吡啶化合物。
实施例
本发明的两类3-位含吡啶取代基团芳炔前体的合成路线如下:
3-位含吡啶取代基团芳炔前体a的合成:
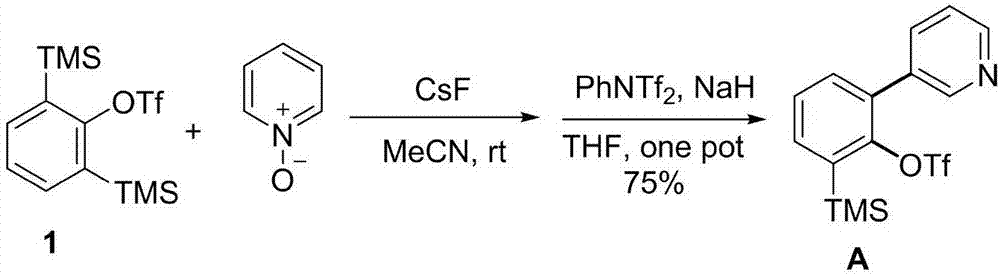
化合物a的合成反应过程如下所示:
i)在手套箱内,将结构式1(370mg,1.0mmol,2.0equiv)溶入乙腈(mecn)(25ml)中,加入吡啶n-氧化合物(47.5mg,0.5mmol,1.0equiv),氟化铯(csf)(302mg,2.0mmol,4.0equiv,从手套箱内移出在氩气保护下室温搅拌约8小时;将反应停止搅拌过滤,旋蒸。将得到的粗品溶于四氢呋喃(thf),(20ml)中,室温下加入氢化钠(nah,60%,0.75mmol,1.5equiv),搅拌半小时后,phntf2(0.75mmol,1.5equiv)加入,室温搅拌10小时,过滤旋蒸得到粗品3-吡啶基芳炔前体a。
ii)粗品经层析柱纯化得到结构式a3-吡啶基芳炔前体(140mg),产率75%。
3-位吡啶取代基团芳炔前体b的合成:
化合物b的合成反应过程如下所示:
i)在手套箱内,将结构式1(370mg,1.0mmol,2.0equiv.)溶入乙腈(mecn)(25ml)中,加入喹啉n-氧化合物(73mg,0.5mmol,1.0equiv),四丁基氟化铵(1mol/ml,在四氢呋喃中),(tbaf),(1.5ml,3.0equiv),从手套箱内移出在氩气保护下室温搅拌约2小时;将反应停止搅拌过滤,旋蒸。将得到的粗品溶于二氯甲烷(dcm)(20ml)中,室温下加入氢化钠(nah,60%,0.75mmol,1.5equiv),搅拌半小时后加入对甲苯磺酰氯(tscl),(0.75mmol,1.5equiv),室温搅拌10小时,过滤旋蒸得到粗品3-吡啶基芳炔前体b。
ii)粗品经层析柱纯化得到结构式3-吡啶基芳炔前体b(154mg),产率69%。
上述的结构式1的1,2-二芳炔前体为已知的化合物,其物理性质及表征数据参见:“anaryne-basedroutetosubstitutedbenzoisothiazoles”(通过2,6二溴苯酚与三甲基氯硅烷,丁基锂,三氟甲磺酸酐合成),yidingchenandmichaelc.willis.org.lett.2015,17,4786-4789.
上述的结构式喹啉n-氧化合物已知的化合物,其物理性质及表征数据参见:“expedientsynthesisofα-(2-azaheteroaryl)acetatesviatheadditionofsilylketeneacetalstoazine-n-oxides”(通过喹啉与间氯过氧苯甲酸合成),allynt.londregan,kristenburford,edwardl.conn,andkevind.hesp.org.lett.2014,16,3336-3339.
本发明3-位含吡啶取代基团芳炔前体的应用实例:
3-位含吡啶取代基团芳炔前体可以合成一系列含吡啶取代基团的多取代芳基化合物c,d,例如下列结构式e,f的合成。
含吡啶取代基团的多取代芳基化合物e的合成:
在手套箱内将3-位含吡啶取代基团芳炔前体a(113mg,0.3mmol,1.0equiv)溶于乙腈(10ml)中,加入2,5-二甲基-呋喃(58mg,0.6mmol,2.0equiv,氟化铯(91mg,0.6mmol,2.0equiv),反应室温搅拌约24h,过滤,旋蒸得到粗品经层析柱纯化得到结构式e含吡啶取代基的多取代芳基化合物58mg,产率78%。
含吡啶取代基团的多取代芳基化合物e的合成:
在手套箱内将3-位含吡啶取代基团芳炔前体b(134mg,0.3mmol,1.0equiv)溶于二氧六环(10ml)中,加入2,5-二甲基-呋喃(58mg,0.6mmol,2.0equiv),氟化铯(91mg,0.6mmol,2.0equiv),18-冠醚-6(80mg,0.3mmol,1.0equiv),移出手套箱反应加热到100摄氏度搅拌约24h,过滤,旋蒸得到粗品经层析柱纯化得到结构式f含吡啶取代基的多取代芳基化合物60mg,产率65%。
附图说明
图1为两类3-位含吡啶取代基团芳炔前体a,b的结构式
图2为3-位含吡啶取代基团芳炔前体a的合成路线
图3为3-位含吡啶取代基团芳炔前体b的合成路线
图4为含吡啶取代基团的多取代芳基化合物c,d的结构式
图5为含吡啶取代基团的多取代芳基化合物e的合成路线
图6为含吡啶取代基团的多取代芳基化合物f的合成路线
图7非传统1,2-二芳炔前体化合物1的合成路线
图8为喹啉n-氧化物的合成路线
化合物性质
所得结构式a的物理性质及表征数据:
1hnmr(500mhz,cdcl3)δ8.67(d,j=1.5hz,1h),8.63-8.62(m,1h),7.77-7.73(m,1h),7.62(dd,j1=1.5,j2=7.5hz,1h),7.47(t,j=7.5hz,1h),7.41(dd,j1=1.5,j2=7.5hz,1h),7.38-7.35(m,1h),0.44(s,9h)ppm;13cnmr(125mhz,cdcl3)δ150.3,149.6,149.4,137.1,137.0,136.6,133.6,133.2,133.1,128.6,123.4,118.2(q,j=318.8hz),0.4ppm;ir(thinfilm)2924,1636,1365,1214,1141,845,754,712,702,644,513,405(cm-1);hrms-maldi(m/z)calcdfor[c15h17f3no3ssi]+,376.0645;found,376.0644.
所得结构式b的物理性质及表征数据:
熔点:55-57℃;1hnmr(400mhz,cdcl3)δ7.90(t,j=7.6hz,2h),7.75(d,j=8.0hz,1h),7.70-7.66(m,3h),7.59-7.49(m,2h),7.42(t,j=8.0hz,1h),7.07(d,j=8.0hz,2h),6.49(d,j=8.0hz,2h),1.91(s,3h),0.53(s,9h)ppm;13cnmr(100mhz,cdcl3)δ156.3,151.2,148.2,144.6,137.5,137.3,135.4,134.7,133.2,132.6,129.6,129.4,128.9,128.2,127.5,127.4,126.9,126.6,123.4,21.5,0.82ppm;ir(thinfilm)2926,1705,1634,1384,1252,1124,1004,772,620,612,519,408(cm-1);hrms-maldi(m/z)calcdfor[c25h25nnao3ssi]+,470.1217;found,470.1216.
所得结构式e的物理性质及表征数据:
1hnmr(500mhz,cdcl3)δ8.63(d,j=3.5hz,1h),8.49(s,1h),7.61(d,j=7.0hz,1h),7.37-7.35(m,1h),7.19(d,j=7.0hz,1h),7.06(t,j=7.0hz,1h),6.90-6.86(m,3h),1.92(s,3h),1.42(s,3h)ppm;13cnmr(125mhz,cdcl3)δ153.6,150.4,149.9,148.9,147.4,146.8,136.3,135.9,131.5,126.9,125.3,123.2,118.3,90.0,88.1,17.9,15.5ppm;ir(thinfilm)2924,1712,1636,1407,1350,1302,1219,1136,684,851,800,760,627(cm-1);hrms-maldi(m/z)calcdfor[c17h16no]+,250.1226;found,250.1230.
所得结构式f的物理性质及表征数据:
1hnmr(400mhz,cdcl3)δ8.24(d,j=8.0hz,1h),8.14(d,j=8.0hz,1h),7.88(d,j=8.0hz,1h),7.76(t,j=8.0hz,1h),7.60-7.56(m,2h),7.22(d,j=8.0hz,1h),7.18-7.08(m,3h),6.87(d,j=5.2hz,1h),1.95(s,3h),1.47(s,3h)ppm;13cnmr(125mhz,cdcl3)δ158.4,153.9,151.8,147.8,147.1,147.1,136.6,134.6,130.1,129.8,127.8,127.1,126.8,126.1,125.2,121.7,118.5,90.8,88.0,17.7,15.6ppm;ir(thinfilm)2824,2653,2371,1637,1384,1218,1092,885,875,852,513,500,402(cm-1);hrms-maldi(m/z)calcdfor[c21h18no]+,300.1383;found,300.1385.
使用的药品:
本发明公开了两类3-位含吡啶取代基团的芳炔前体及其制备。该3-位含吡啶取代基团的芳炔前体的合成方法包括非传统1,2-二芳炔前体的合成、利用非传统1,2-二芳炔前体与吡啶n-氧化物一锅煮进行反应,高效地制备了3-位含吡啶取代基团芳炔前体a,b两个步骤。本发明的技术效果是:首先,实现了两类3-位含吡啶取代基团的芳炔前体a,b的制备,该化合物及其合成方法在有机物合成和药物合成领域具有广阔的应用前景;其次,此方法合成方法简便,能大量制备。
- 还没有人留言评论。精彩留言会获得点赞!