基于RAA荧光法检测乙型肝炎病毒的引物探针组及试剂盒的制作方法
本发明属于分子生物学检测技术领域,尤其涉及基于raa荧光法检测乙型肝炎病毒的引物探针组及试剂盒。
背景技术
乙型肝炎病毒(hepatitisbvirus,hbv)感染仍是威胁着人们健康的全球性问题。目前,全世界受hbv感染者接近20亿,其中有超过3亿的慢性感染者。在亚太地区,慢性hbv感染率超过10%,其中25%~40%患者会因合并或不合并肝细胞癌的肝硬化而死亡。世界卫生组织已将hbv感染列为全球十大死亡原因之一。hbv的感染不仅可以导致急、慢性病毒性肝炎和重型肝炎,而且还与肝硬化和肝细胞癌的发生、发展密切相关。hbv感染导致全球每年50~120万人死亡,其中死于肝细胞癌的约占32万。
乙肝病毒在电子显微镜下可呈3种形态的颗粒结构:直径约42nm的大球形颗粒、直径约22nm的小球形颗粒以及管型颗粒。大球形颗粒(dane颗粒)为完整的病毒颗粒,由包膜和核衣壳组成,包膜含hbsag、糖蛋白和细胞脂肪,核心颗粒内含核心蛋白(hbcag)、环状双股hbv-dna和hbv-dna多聚酶,是病毒的完整形态,有感染性。乙肝病毒利用cccdna转录出3.5kb,2.4kb,2.1kb及约0.8kb的mrna,其中3.5kb为前基因组rna(pgrna),可反转录出基因组dna并作为编码病毒核心蛋白和聚合酶蛋白的模板,hbsag合成后在粗面内质网中多聚化,并转运至高尔基体前腔以包装核心颗粒,装配好的hbv颗粒与亚病毒颗粒转运至高尔基体进行hbsag的糖基化修饰,最后以出芽方式将完整的病毒粒子分泌出宿主细胞而完成生活周期。
我国是hbv感染的高发区,约60%的人群感染过hbv,10%的人群为携带者,多达1.2亿。现有乙型肝炎患者约为1200万,年发病率为158/10万。因此,hbv的快速准确检测对于乙型肝炎病毒的诊断防治具有重要的意义。
目前诊断乙型肝炎病毒的方法有酶联免疫吸附法(elisa)、时间分辨荧光免疫分析技术、胶体金法等。但是这些血清学方法或是操作复杂、费时、费力,或是敏感度不够高。近年来,发展起来的分子生物学方法如聚合酶链式反应(pcr)以及等温核酸技术中的lamp法已经建立起来,在乙型肝炎病毒的检测上已得到较好的应用,大大缩短了检测的时间。以pcr技术为代表如多重pcr、巢式pcr以及实时定量pcr以其高度的特异性及敏感性在乙型肝炎病毒检测方面取得了重大的突破。但是这些方法不仅需要相关的昂贵仪器设备且需要有专业技术人员操作,因此在基层和现场的检测应用受到很大限制;整体实验时间在2~4h。等温核酸技术中的lamp方法克服了pcr技术需要昂贵的设备仪器等缺点,具有操作简便,结果判断简单等优点。但是,lamp技术要求多对引物且对靶基因的要求较高,假阳性率也比较高,容易发生交叉污染。
技术实现要素:
有鉴于此,本发明提供一种基于raa荧光法检测乙型肝炎病毒的引物探针组及试剂盒。本发明提供的引物探针组具有特异性强、灵敏度高、重复性好的特点,具有较大的应用价值;包括上述引物探针组的试剂盒能在15min内检测出乙型肝炎病毒dna。
为了实现上述目的,本发明提供了以下技术方案:基于raa荧光法检测乙型肝炎病毒的引物探针组,包括上游引物、下游引物和探针,所述上游引物的核苷酸序列如seqidno.1所示,所述下游引物的核苷酸序列如seqidno.2所示,所述探针的核苷酸序列如seqidno.3所示;所述探针为荧光报告基团和荧光猝灭基团修饰的探针。
优选的,所述探针核苷酸序列5’至3’方向的第37位碱基修饰荧光报告基团、第38位碱基替换为四氢呋喃残基,并且第39位碱基修饰荧光淬灭基团的物质。
优选的,所述荧光报告基团为fam、hex、tet、joe、vic、rox、cy3或cy5。
优选的,所述荧光淬灭基团为tamra、eclipse、bhq1、bhq2、bhq3或dabcyl。
本发明还提供了基于raa荧光法检测乙型肝炎病毒的试剂盒,包括raa基础荧光通用反应试剂、反应缓冲液、阳性质控品,阴性质控品和上述引物探针组。
优选的,所述的探针的浓度为0.01~0.03mm。
优选的,所述上游引物和下游引物的浓度独立地为0.02~0.05mm。
优选的,所述反应缓冲液包括:使用浓度为500mmph值为7.4的tris-hcl缓冲液、240mm的mgac和质量分数为10%的peg10000。
优选的,所述阳性质控品为乙型肝炎病毒重组dna质粒。
优选的,所述阴性质控品为ddh2o或纯化水。
本发明的有益效果:本发明提供了raa荧光法检测乙型肝炎病毒的引物探针组,本发明提供的引物探针组能够实现乙型肝炎病毒的快速准确鉴定,操作简便,检测时间短,特异性高达100%。试验结果表明,本发明提供的引物探针组只需15min内即可完成乙型肝炎病毒dna的检测,无需通过高温使dna解旋,只需在30~42℃下进行等温扩增即可完成检测,检测快速、灵敏,特异性好,无假阳性;对未来诊断乙型肝炎病毒具有非常重要的意义,具有很大的应用前景。
附图说明
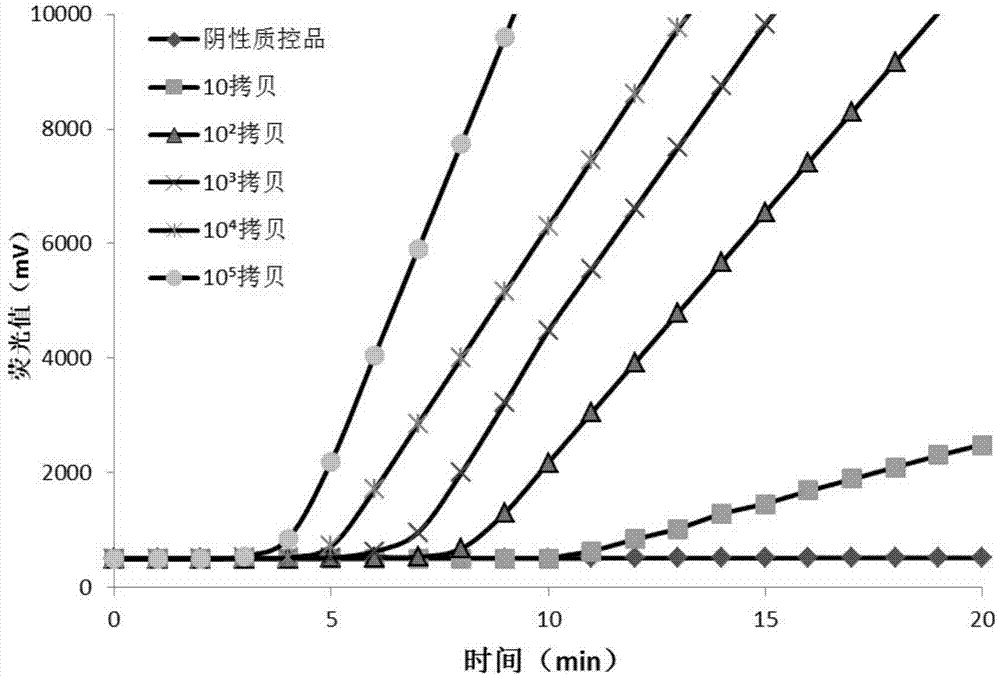
图1为本发明实施例2提供的不同浓度质粒dna灵敏度检测结果图;
图2为本发明实施例3提供的乙型肝炎病毒质粒dna重复性检测结果图;
图3为本发明实施例4提供的乙型肝炎病毒的特异性检测结果图。
具体实施方式
本发明提供了基于raa荧光法检测乙型肝炎病毒的引物探针组,包括上游引物、下游引物和探针,所述上游引物的核苷酸序列如seqidno.1所示,所述下游引物的核苷酸序列如seqidno.2所示,所述探针的核苷酸序列如seqidno.3所示;所述探针为荧光报告基团和荧光猝灭基团修饰的探针。
在本发明中,所述上游引物的核苷酸序列seqidno.1为5’-attcgcatgccccaacctcaatcactcacc-3’;所述下游引物的核苷酸序列seqidno.2为5’-aataccacatcatccatataactgaaagcc-3’;本发明对所述上游引物和下游引物的来源没有特殊的限定,采用本领域技术人员熟知的生物公司进行人工合成即可,如生工生物工程(上海)股份有限公司。
本发明所述探针的核苷酸序列如seqidno.3所示:5’-tatcatcttcctcttcatcctgctgctatgcctcatcttcttgttggttc-3’,本发明中所述探针为荧光报告基团和荧光猝灭基团修饰的探针,优选的,所述探针核苷酸序列5’至3’方向的第37位碱基修饰荧光报告基团、第38位碱基替换为四氢呋喃残基,并且第39位碱基修饰荧光淬灭基团的物质。在本发明中,所述荧光报告基团优选为fam、hex、tet、joe、vic、rox、cy3或cy5,更优选为fam或hex;所述淬灭基团优选为tamra、eclipse、bhq1、bhq2、bhq3或dabcyl,更优选为bhq1或bhq2;本发明对不同的荧光报告基因和淬灭基团的组合没有特殊的限定,上述荧光报告基团和猝灭基团进行组合都可以达到相同的效果,本发明对荧光检测的仪器没有特殊的限定,采用本领域技术人员所熟知的相应荧光检测用仪器即可,如当所述荧光报告基团为fam,所述荧光猝灭基团为bhq1时,采用无锡奇天生物科学仪器有限公司生产的raa-f1620荧光基因检测仪进行检测。本发明所述修饰后得到探针的序列为:5’-tatcatcttcctcttcatcctgctgctatgcctca(fam-dt)(thf)(bhq1-dt)tcttgttggttc-3’,其中,fam为荧光报告基团,bhq1为荧光淬灭基团,thf为四氢呋喃残基。本发明对所述引物和探针的来源没有特殊的限定,采用本领域技术人员熟知的生物公司进行合成即可。
本发明还提供了基于raa荧光法检测乙型肝炎病毒的试剂盒,所述试剂盒包括上述技术方案所述的引物探针组。本发明对所述引物和探针在试剂盒中的储存浓度没有特殊的限定。在本发明中,所述的探针使用浓度为0.01~0.03mm,更优选为0.02mm。在本发明中,所述上游引物和下游引物的使用浓度独立地为0.02~0.05mm,更优选独立地为0.03mm。在本发明中,所述上游引物、下游引物和探针优选的以混合物的形式。
在本发明中,所述试剂盒还包括raa基础荧光通用反应试剂和反应缓冲液。在本发明中,所述raa基础荧光通用反应试剂优选为经过低温冷冻干燥的冻干粉;在本发明的实施例中,所述raa基础荧光通用反应试剂的来源可以为江苏奇天基因生物科技有限公司、商品货号为f00001的市售商品,raa基础荧光通用反应试剂的反应规格为50μl,使用前应用反应缓冲液进行重溶。在本发明中,所述raa基础荧光通用反应试剂也可根据raa荧光法检测方法的原理,选择其他能够作为raa基础荧光通用反应试剂的产品作为替换。本发明对所述反应缓冲液在试剂盒中的储存浓度没有特殊的限定;所述反应缓冲液包括:使用浓度为500mmph值为7.4的tris-hcl缓冲液、240mm的mgac和质量分数为10%的peg10000。本发明中,所述tris-hcl缓冲液、mgac和peg10000的浓度均为终浓度。本发明对所述tris-hcl缓冲液、mgac和peg10000的来源没有特殊限定,采用常规市售产品即可。本发明实施例中所述tris-hcl、和peg10000的购自sigma-aldrich,mgac购自国药沪试。
在本发明中,所述试剂盒还包括阳性质控品;本发明中,所述阳性质控品为乙型肝炎病毒重组dna质粒,所述乙型肝炎病毒重组dna质粒的浓度为1.0×103~1.0×106copies/μl。在本发明中,所述阳性质控品的使用浓度更优选为1.0×104~1.0×105copies/μl,最优选为1.0×105copies/μl。本发明所述阳性质控品优选通过重组质粒转接大肠杆菌培养并提取。本发明所述阳性质控品还能用作灵敏度实验的阳性标准品,通过调节阳性质控品的浓度,实现灵敏度的检测,当所述阳性质控品用作阳性标准品时,所述阳性标准品的浓度优选调整为1.0×100~1.0×1010copies/μl备用。
在本发明中,所述试剂盒还包括阴性质控品,所述阴性质控品为ddh2o或纯化水。
本发明所述试剂盒用于检测乙型肝炎病毒,在本发明中,所述试剂盒的使用方法,优选包括如下步骤:
(1)提取待测样品(疑似乙型肝炎病毒)的dna;本发明所述提取的方法优选采用市售商品化的病毒核酸提取试剂,按说明书进行操作,如西安天隆、qiagen试剂盒、天根试剂盒等,也可采用自动核酸提取仪进行dna提取;提取得到的dna在-80℃保存备用;
(2)将检测仪器raa-f1620接通电源进行预热,对反应参数进行设置,反应参数设置为39℃,反应时间:20min。
(3)在47μl反应缓冲液中加入1μl探针和1μl引物混合或者2μl引物与探针混合物,得到反应混合液将配制好的49μl试剂加入到raa基础荧光通用反应试剂冻干粉中,使其充分溶解并混匀;
(4)将1μl所述步骤(1)中得到的待测dna样品与所述步骤(3)中得到的反应混合液充分混合,得到的反应体系放入检测仪器raa-f1620进行检测荧光信号;
(6)根据raa-f1620检测仪器中的阳性判定方法,将斜率值k≥20时,判定为阳性,斜率值k<20时判定为阴性。
在本发明中,所述待测样品为可能含有乙型肝炎病毒的样本,本发明对待测样本的提取方法没有特殊限定,采用病毒dna的常规提取方法即可。
在本发明中,所述实时raa荧光法反应条件优选为:反应温度30~42℃,反应时间5~20min,针对荧光实时荧光更优选39℃,反应时间20min。
本发明提供的试剂盒检测乙型肝炎病毒时与艾滋病毒和丙型肝炎病毒无交叉反应,特异性强,达100%。灵敏度高,每反应检测灵敏度达到10copies。且本发明提供的试剂盒,不需要大型仪器设备,适用于现场诊断及适用于大规模的筛选。
下面结合实施例对本发明提供的技术方案进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。
实施例1
本发明提取乙型肝炎病毒样本dna进行验证,根据基因名称乙型肝炎病毒(hepatitisbvirus,hbv),在genebank中找到相应的全基因序列(www.ncbi.nlm.nih.gov),运用dnaman软件进行同源性分析和b1ast序列分析,筛出乙型肝炎病毒高度保守序列(nt311-nt751,genbankaccessionno.mh220971.1)。本发明依据高度保守序列作为检测的目的基因,合成乙型肝炎病毒重组dna质粒并设计引物探针。
根据目的基因委托生工生物工程(上海)股份有限公司进行合成乙型肝炎病毒重组dna质粒,质粒大小440bp;
①引物探针设计
根据raa技术引物及探针设计原则进行的设计,通过筛选和评价,最终确定的:
上游引物序列5’-attcgcatgccccaacctcaatcactcacc-3’;
下游引物序列5’-aataccacatcatccatataactgaaagcc-3’;
未修饰的探针为:
5’-tatcatcttcctcttcatcctgctgctatgcctcatcttcttgttggttc-3’。
②选择荧光修饰基团和荧光淬灭基团
根据实验仪器采用的是无锡奇天生物科学仪器有限公司生产的raa-f1620荧光基因检测仪,所检测的荧光为fam荧光,因此荧光报告基团选为fam,荧光淬灭基团选为bhq1。
③所述探针的修饰方法包括:荧光报告基团修饰在探针序列离5'端碱基数37bp的位置上;荧光淬灭基团修饰在探针序列离5'端碱基数39bp的位置上,荧光报告基团与淬灭基团之间间隔1个碱基c,该碱基用四氢呋喃残基替换。经过修饰的探针为:
5’-tatcatcttcctcttcatcctgctgctatgcctca(fam-dt)(thf)(bhq1-dt)tcttgttggttc-3’;
其中,fam为荧光报告基团,bhq1为荧光淬灭基团,thf为四氢呋喃残基。
④引物探针及质粒均委托生工生物工程(上海)股份有限公司进行合成。
⑤乙型肝炎病毒重组dna质粒阳性标准品制备
乙型肝炎病毒重组dna质粒通过转接大肠杆菌培养并提取,得到质粒后用超微量紫外分光光度计进行浓度测定并进行拷贝数计算,按浓度梯度稀释制备成1.0×100copies/μl~1.0×1010copies/μl备用。
⑥组成试剂盒
本发明试剂盒包括raa基础荧光通用反应试剂、反应缓冲液、阳性质控品、阴性质控品,引物和探针;
上游引物和下游引物的浓度独立为0.04mmol/l。
探针的浓度为0.03mmol/l。
raa基础荧光通用反应试剂购自江苏奇天基因生物科技有限公司,货号为f00001。raa基础荧光通用反应试剂的反应规格为50μl,使用前应用反应缓冲液进行重溶。
重溶raa基础荧光通用反应试剂的反应缓冲液包括以下含量的组分:浓度为500mmol/l的tris-hcl(ph7.4)缓冲液、浓度为240mmol/l的mgac和质量分数为10%的peg10000。
阳性质控品:含有乙型肝炎病毒重组dna质粒,所述乙型肝炎病毒重组dna质粒的浓度为1×105copies/μl。
阴性质控品:ddh2o。
实施例2
灵敏度实验
上游引物:
5’-attcgcatgccccaacctcaatcactcacc-3’;
下游引物:
5’-aataccacatcatccatataactgaaagcc-3’。
探针序列为:
5’-tatcatcttcctcttcatcctgctgctatgcctcatcttcttgttggttc-3’
荧光报告基团采用fam,荧光淬灭基团采用bhq1;
修饰后的探针为:
5’-tatcatcttcctcttcatcctgctgctatgcctca(fam-dt)(thf)(bhq1-dt)tcttgttggttc-3’;
试剂盒组成如表1所示:
表1试剂盒成分表
乙型肝炎病毒重组dna质粒阳性标准品制备好的不同浓度的工作标准品,分别为:
工作标准品(阳性质控品)1,含有1.0×105copies/μl乙型肝炎病毒重组dna质粒。
工作标准品(阳性质控品)2,含有1.0×104copies/μl乙型肝炎病毒重组dna质粒。
工作标准品(阳性质控品)3,含有1.0×103copies/μl乙型肝炎病毒重组dna质粒。
工作标准品(阳性质控品)4,含有1.0×102copies/μl乙型肝炎病毒重组dna质粒。
工作标准品(阳性质控品)5,含有1.0×101copies/μl乙型肝炎病毒重组dna质粒。
实施方法:
1反应缓冲液的配制
从试剂盒中反应缓冲液管里吸取280μl反应缓冲液加入预先准备好的1.5mlpe管,再加入16μl探针与引物的混合物(探针的浓度为0.02mmol/,引物的浓度为0.05mmol/l),充分混匀,得混匀后的反应缓冲液。
2raa荧光基础反应试剂重溶
准备6个raa荧光基础反应试剂,吸取步骤1中混匀的反应缓冲液49μl分别加入到准备好的6个raa荧光基础反应试剂管中,使冻干粉充分溶解并混均,成为raa反应体系。
3、加样反应
在以上6个配制好的raa荧光基础反应试剂试管中分别加入1μl阴性质控品、1μl工作标准品5、1μl工作标准品4、1μl工作标准品3、1μl工作标准品2、1μl工作标准品1为模板,加好样后每个反应管进行充分混均,每个反应管总体积为50μl。
将反应管放入raa-f1620荧光检测仪中,设定反应温度为39℃,反应时间20min。检测结果如图1所示。结果显示最快5min明显有扩增,20min内所有标准工作品均有扩增,最低灵敏度可以达到1.0×101copies/μl,表明本发明灵敏度高,检测时间短。
实施例3
重复性实验
引物探针及阳性质控品序列与实施例1相同。
试剂盒组成如表2所示:
表2试剂盒成分表
反应缓冲液配制:
从试剂盒中反应缓冲液管里吸取190μl反应缓冲液加入预先准备好的1.5mlpe管,再加入8μl探针与引物的混合物(探针的浓度为0.02mmol/,引物的浓度为0.04mmol/l),充分混匀,得混匀后的反应缓冲液。
2raa荧光基础反应试剂重溶
准备4个raa荧光基础反应试剂,每次吸取49μl步骤1中混匀的反应缓冲液分别加入到准备好的4个raa荧光基础反应试剂管中,使冻干粉充分溶解并混匀,成为raa反应体系,并做好标记。
3、加样反应
在以上4个配制好的raa荧光基础反应试剂试管中分别加入1μl阴性质控品、其他3个反应管中分别加入1μl阳性质控品;每加好一个样就盖好管盖。加好样后每个反应管进行充分混均,每个反应管总体积为50μl。
将混匀的4个反应管放入raa-f1620荧光检测仪中,设定反应温度为39℃,反应时间20min。检测结果如图2所示。结果显示扩增反应重复性好。
实施例4
特异性实验
引物探针及阳性质控品序列与实施例1相同。
试剂盒组成如表3所示:
表3试剂盒成分表
特异性实验中样本来源:丙型肝炎病毒、艾滋病毒。
其中丙型肝炎病毒、艾滋病毒样本以及乙型肝炎病毒样本由中国疾病预防控制中心提供,丙型肝炎病毒、艾滋病毒样本通过西安天隆全自动核酸提取仪提取病毒rna,乙型肝炎病毒样本通过天根病毒dna提取试剂盒提取病毒dna。丙型肝炎病毒及艾滋病毒rna通过promegam-mlv体外反转录试剂盒反转录为病毒cdna。
实施方法:
1反应缓冲液的配制
从试剂盒中反应缓冲液管里吸取236μl反应缓冲液加入预先准备好的1.5mlpe管,再加入10μl探针与引物的混合物(探针的浓度为0.03mmol/,引物的浓度为0.05mmol/l),充分混匀,得混匀后的反应缓冲液。
2raa荧光基础反应试剂重溶
准备5个raa荧光基础反应试剂,每次吸取49μl步骤1中混匀的反应缓冲液分别加入到准备好的5个raa荧光基础反应试剂管中,使冻干粉充分溶解并混均,成为raa反应体系,并做好标记。
3、加样反应
在以上5个配制好的raa荧光基础反应试剂试管中分别加入1μl阴性质控品、1μl乙型肝炎病毒dna、1μl丙型肝炎病毒cdna、1μl艾滋病毒cdna、1μl阳性质控品;每加好一个样就盖好管盖。加好样后每个反应管进行充分混均,每个反应管总体积为50μl。
将混匀的5个反应管放入raa-f1620荧光检测仪中,设定反应温度为39℃,反应时间20min。检测结果如图3所示。结果显示除阳性质控品外,只有乙型肝炎病毒dna有扩增,为阳性,其他样本丙型肝炎病毒cdna、艾滋病毒cdna及阴性质控品均没有扩增,均为阴性。表明本发明提供的检测方法特异性强。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
序列表
<110>江苏奇天基因生物科技有限公司
中国疾病预防控制中心病毒病预防控制所
<120>基于raa荧光法检测乙型肝炎病毒的引物探针组及试剂盒
<160>3
<170>siposequencelisting1.0
<210>1
<211>30
<212>dna
<213>人工序列(artificialsequence)
<400>1
attcgcatgccccaacctcaatcactcacc30
<210>2
<211>30
<212>dna
<213>人工序列(artificialsequence)
<400>2
aataccacatcatccatataactgaaagcc30
<210>3
<211>50
<212>dna
<213>人工序列(artificialsequence)
<400>3
tatcatcttcctcttcatcctgctgctatgcctcatcttcttgttggttc50
- 还没有人留言评论。精彩留言会获得点赞!