用于致病性大肠埃希氏菌检测的多核苷酸、方法和试剂盒与流程
本发明属于生物
技术领域:
,具体地说,本发明涉及用于致病性大肠埃希氏菌检测的多核苷酸、方法和试剂盒。
背景技术:
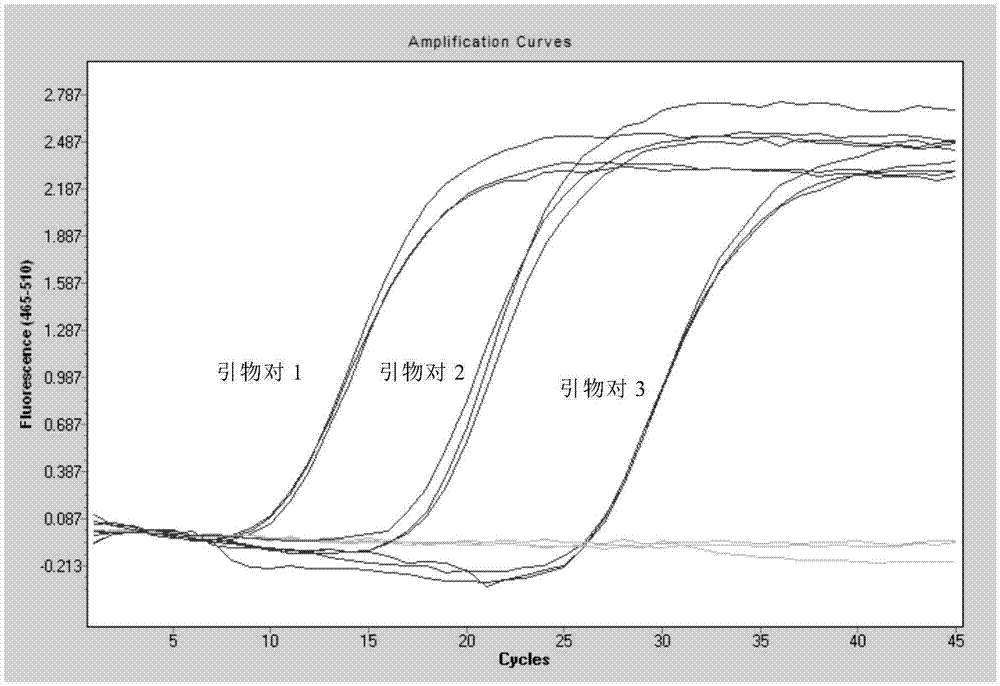
:大肠埃希氏菌(e.coli)通常称为大肠杆菌,一直被当作正常肠道菌群的组成部分,被认为是非致病菌。直到20世纪中叶,才认识到一些特殊血清型的大肠杆菌对人和动物有病原性,尤其对婴儿和幼畜,常引起严重腹泻和败血症,根据不同的生物学特性将可致病的大肠杆菌分为5类:致病性大肠杆菌(epec)、肠产毒性大肠杆菌(etec)、肠侵袭性大肠杆菌(eiec)、肠出血性大肠杆菌(ehec)、肠黏附性大肠杆菌(eaec)。目前,在大肠杆菌检测中常用的检测方法多样,各具特点。传统检测方法需要先分离再培养,然后用经典的方法鉴定,是国际上通用的鉴定细菌的方法。这类培养法耗时长、灵敏度低。免疫学方法简单、方便、迅速,但是交叉反应比较严重、假阳性多、灵敏度偏低。因此,为了有效地检测致病性大肠杆菌,本领域迫切需要开发特异性好、灵敏度高、简单便捷的致病性大肠杆菌检测方法。技术实现要素:本发明的目的在于提供一种用于致病性大肠埃希氏菌检测的多核苷酸、方法和试剂盒。在本发明的第一方面,提供了一种检测致病性大肠埃希氏菌的引物对,所述的引物对选自下组:seqidno.:1和seqidno.:2所示的引物对;seqidno.:3和seqidno.:4所示的引物对;和seqidno.:5和seqidno.:6所示的引物对。在另一优选例中,所述的引物对选自下组:seqidno.:1和seqidno.:2所示的引物对;和seqidno.:3和seqidno.:4所示的引物对。在另一优选例中,所述的引物对为:seqidno.:1和seqidno.:2所示的引物对在另一优选例中,所述引物对用于实时荧光定量pcr。本发明的第二方面,提供了一种检测致病性大肠埃希氏菌的试剂盒,所述试剂盒包括本发明第一方面所述的引物对。在另一优选例中,所述试剂盒还包括探针序列,所述探针序列如seqidno.:11所示。在另一优选例中,所述试剂盒还包括:taq酶、dntp、和/或mg2+。本发明的第三方面,提供了如本发明第一方面所述的引物对、或本发明第二方面所述的试剂盒的用途,用于致病性大肠埃希氏菌的检测。在另一优选例中,所述检测为非诊断或治疗目的的。在另一优选例中,所述检测为荧光定量pcr检测。本发明的第四方面,提供了一种检测致病性大肠埃希氏菌的方法,所述方法包括步骤:(1)提供待检测样本,并从所述待检测样本中提取dna;(2)使用本发明第二方面所述的试剂盒检测步骤(1)提取得到的dna,从而判断所述待检测样本中是否存有致病性大肠埃希氏菌。在另一优选例中,所述方法为荧光定量pcr检测方法。应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。附图说明图1显示了各引物对针对感染血液dna探针检出灵敏度检测结果。图2显示了使用引物对1针对致病性大肠埃希氏菌标准品的灵敏度检测结果。图3显示了使用引物对1针对感染血液样本中致病性大肠埃希氏菌dna模板的灵敏度检测结果。具体实施方式本发明人通过广泛而深入的研究,获得了能够用于致病性大肠埃希氏菌检测的引物对和探针,对目标菌株的dna进行实时荧光pcr检测时,具有极佳的特异性和灵敏度,并且稳定性良好。本发明还提供了用于致病性大肠埃希氏菌检测的试剂盒。在描述本发明之前,应当理解本发明不限于所述的具体方法和实验条件,因为这类方法和条件可以变动。还应当理解本文所用的术语其目的仅在于描述具体实施方案,并且不意图是限制性的,本发明的范围将仅由所附的权利要求书限制。除非另外定义,否则本文中所用的全部技术与科学术语均具有如本发明所属领域的普通技术人员通常理解的相同含义。如本文所用,在提到具体列举的数值中使用时,术语“约”意指该值可以从列举的值变动不多于1%。例如,如本文所用,表述“约100”包括99和101和之间的全部值(例如,99.1、99.2、99.3、99.4等)。虽然在本发明的实施或测试中可以使用与本发明中所述相似或等价的任何方法和材料,本文在此处例举优选的方法和材料。本文所用的术语“引物”具有本领域技术人员常规理解的意义。本发明的引物对在致病性大肠埃希氏菌dna时能够同时具备高灵敏度和高特异性,从而能准确而灵敏地检测产品,例如环境样品、食品、保健品、化妆品中的致病性大肠埃希氏菌含量,或者血液样本、组织样本中是否含有致病性大肠埃希氏菌,从而用于感染性疾病的诊断。本文所用的术语“探针”具有本领域技术人员常规理解的意义,即,一小段单链dna或者rna片段,用于检测与其互补的核酸序列。探针可以处于液相中,也可以固定于固相上。本发明中,致病性大肠埃希氏菌引物探针设计的靶序列如下:1tttttattttttaatgtatttgtacatggagaaaataaagtgaaacaaagcactattgca61ctggcactcttaccgttactgtttacccctgtgacaaaagcccggacaccagaaatgcct121gttctggaaaaccgggctgctcagggcgatattactgcacccggcggtgctcgccgttta181acgggtgatcagactgccgctctgcgtgattctcttagcgataaacctgcaaaaaatatt241attttgctgattggcgatgggatgggggactcggaaattactgccgcacgtaattatgcc301gaaggtgcgggcggcttttttaaaggtatagatgccttaccgcttaccggg(seqidno.10)表1本发明还提供一种检测致病性大肠埃希氏菌基因组dna的检测试剂,所述检测试剂包含本发明的引物对以及探针等实施pcr所需的其它成分,例如taq酶、dntp、mg2+等等。在具体的实施方式中,本发明检测试剂的检测灵敏度达到1fg/μl。在本发明的引物对或检测试剂的基础上,本发明进一步提供一种检测致病性大肠埃希氏菌基因组dna的方法,所述方法包括:利用本发明的引物对或检测试剂,对待测样品进行pcr,并检测pcr扩增产物。在本发明的引物对的基础上,本发明还提供一种pcr试剂盒,所述试剂盒中包括容器以及位于所述容器中的根据本发明的引物对;和/或探针。在具体的实施方式中,所述试剂盒中还装有标准品对照。在本发明的引物对的基础上,本发明提供利用本发明的引物对扩增目标产物的pcr方法。本发明的主要优点在于:本发明获得的一段能够用于致病性大肠埃希氏菌检测的引物对和探针,对目标菌株的dna进行实时荧光pcr检测时,具有极佳的特异性和灵敏度,并且稳定性良好。下面结合具体实施例,进一步详陈本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明详细条件的实验方法,通常按照常规条件如美国sambrook.j等著《分子克隆实验室指南》(黄培堂等译,北京:科学出版社,2002年)中所述的条件,或按照制造厂商所建议的条件。除非另外说明,否则百分比和份数按重量计算。以下实施例中所用的实验材料和试剂如无特别说明均可从市售渠道获得。材料和方法1.样本处理试剂:(柱纯化回收)包括蛋白酶k20mg/ml,革兰氏阳性菌需添加溶菌酶,预处理缓冲液,结合缓冲液,洗涤缓冲液,洗脱缓冲液,结合柱,收集管,1.5ml离心管。2.dna检测体系:2xtaqmanmix:含有taq酶、dntp、mg2+、本发明引物及探针等成分。标准品,阴性质控,dna稀释液3.仪器:roche480ⅱ。4.实验操作及过程4.1基因组dna提取纯化(根据试剂盒说明书操作步骤进行)1)在1.5ml离心管中加入20μlproteinasek(具体体积根据样本大小可调整)。2)加入样本,加入200μl缓冲液gb,抽打混匀或振荡混匀。3)将离心管置于56℃,直至组织完全消化。4)每孔加入200μl无水乙醇,抽打混匀或振荡混匀,室温放置5分钟。5)每孔加入15μl磁珠悬浮液b,抽打混匀或振荡混匀。6)将离心管放置于磁力架上静置30秒,待磁珠完全吸附时小心去除液体。7)将离心管从磁力架上取下,加入500μl缓冲液gd,抽打混匀或振荡混匀。8)将离心管放置于磁力架上静置30秒,待磁珠完全吸附时小心去除液体。9)将离心管从磁力架上取下,加入600μl漂洗液pw,抽打混匀或振荡混匀。10)将离心管放置于磁力架上静置30秒,待磁珠完全吸附时小心去除液体;11)重复操作步骤9、10,液体尽量去除干净。12)离心管于磁力架上,室温晾干10-15分钟。13)将离心管从磁力架上取下,加入50-100μl洗脱液tb,抽打混匀振荡混匀,置于56℃,孵育10分钟。14)将离心管放置于磁力架上静置30秒,待磁珠完全吸附时小心将dna溶液转移至收集板,并于适当条件保存。4.2检测1)根据引物探针浓度,加入适量ddh2o,稀释至100um;2)将引物、探针稀释至10*工作液浓度(工作液浓度:引物0.3-1um,探针0.05-0.2um);3)pcr反应体系4)pcr反应条件根据所获得的标准曲线,计算得到待检样本中致病性大肠埃希氏菌dna的量。实施例1特异性检测针对致病性大肠埃希氏菌的保守dna序列(seqidno.:10),本发明人设计了数十对引物,将设计的引物和探针交由宝生物工程(大连)有限公司合成,mastermix购自roche公司。实验仪器包括:实时荧光定量pcr扩增仪(rocheⅱ)离心机、恒温水浴锅、培养箱、天平等。实时荧光pcr检测:分别使用设计的引物和探针(典型的如表1中所示)进行检测、实时荧光pcr检测体系的方法和条件如上所述。测试菌株包括:致病性大肠埃希氏菌、金黄色葡萄球菌、肺炎链球菌、肺炎克雷白杆菌、铜绿假单胞菌、鲍曼不动杆菌、嗜麦芽窄食单孢菌、粪肠球菌、屎肠球菌、肺炎支原体、军团菌、结核杆菌,使用试剂盒分别提取各菌株的基因组dna后进行实时荧光pcr检测。表2目标菌引物对1引物对2引物对3引物对4引物对5引物对6引物对7引物对8引物对9引物对10致病性大肠埃希氏菌++++++-+-+金黄色葡萄球菌----------肺炎链球菌---------+肺炎克雷白杆菌----------铜绿假单胞菌----------鲍曼不动杆菌-----+--+-嗜麦芽窄食单孢菌----------粪肠球菌----+--+--屎肠球菌----+---+-肺炎支原体----------军团菌----------结核杆菌----------注:“+”表示检测结果为阳性,“-”表示检测结果为阴性。典型的检测结果如表2所示,结果表明所设计的引物和探针中,引物对1、引物对2、引物对3、引物对4的特异性较好,能够检测出致病性大肠埃希氏菌,而且对其它菌株没有阳性反应。菌株培养编号如下:实施例2灵敏度检测针对致病性大肠埃希氏菌标准菌株(购自广东微生物研究所,菌株编号atcc35150)的灵敏度检测:提取致病性大肠埃希氏菌标准菌株的基因组dna,提取后基因组dna浓度调整至1ng/ul,然后进行梯度稀释检测(1ng/uldna,稀释度1/10/100/1000/10000/100000)。表3:大肠杆菌探针检出灵敏度样本稀释度(ng/ul)ct致病性大肠埃希氏菌117.05致病性大肠埃希氏菌0.120.05致病性大肠埃希氏菌0.0123.8致病性大肠埃希氏菌0.00127.43致病性大肠埃希氏菌0.000130.87致病性大肠埃希氏菌0.0000134.39针对感染血液样本中致病性大肠埃希氏菌(病人血液样本来自复旦大学附属中山医院呼吸病研究所)的灵敏度检测:提取感染血液样本中的dna,提取方法如下:1)1.5ml离心管中加入25ulqiagen蛋白酶;2)加入200ul血清或者血浆;3)加入200ulal裂解buffer,涡旋15s;4)56℃温预15min;5)短暂离心后,加入250ul无水乙醇,涡旋15s,室温静置5min;6)短暂离心后,将所有液体转入qiaampminelutecolumn,6,000g,离心1min,弃滤液;7)加入500ulaw1溶液,6,000g离心1min,弃滤液;8)加入500ulaw2溶液,6,000g离心1min,弃滤液;9)加入500ul无水乙醇,6,000g,离心1min,弃滤液;10)换新的2ml离心管,20,000g,离心3min;11)换新的2ml离心管,打开滤柱管盖,将滤膜晾干;12)将滤柱转入1.5ml离心管,加入20ulavebuffer,室温5min,20,000g离心1min;将提取后的基因组dna利用特异性引物进行预扩增(kapa2grobusthotstartreadymixpcrkit),预扩增pcr条件如下:pcr反应条件根据所获得的标准曲线,计算得到待检样本中致病性大肠埃希氏菌dna的量。表4:感染血液dna探针检出灵敏度genenamect引物1感染血液10.18引物1感染血液10.39引物1感染血液10.34引物2感染血液18.2引物2感染血液17.77引物2感染血液17.86引物3感染血液25.79引物3感染血液26.18引物3感染血液26.13引物4感染血液>35引物4感染血液>35引物4感染血液>35实验结果本实例中对特异性较好的引物对1、引物对2、引物对3、引物对4结合探针进行了测试,实验结果表明:引物对1的检测效果最好,检测灵敏度最高,最低可检测1.77copy/μl的目标序列,且没有非特异性的条带出现,对标准菌株和感染血液样本中的致病性大肠埃希氏菌基因组dna均可检测。图1显示了各引物对针对感染血液dna探针检出灵敏度检测结果。图2显示了使用引物对1针对致病性大肠埃希氏菌标准品的灵敏度检测结果。图3显示了使用引物对1针对感染血液样本中致病性大肠埃希氏菌dna模板的灵敏度检测结果。采用大肠杆菌标准株,浓度从1ng/μl,10倍梯度稀释至0.00001ng/μl,引物1扩增ct值呈现出非常好的线性关系。感染血液样本dna线性放大,与标准品(0.00001ng/μl)线性放大ct值接近,说明引物1完全适合感染血液的检测。引物对2的检测灵敏度较低,能够检测到0.0001ng/μl的目标序列。引物对3对标准菌株能够检测到0.001ng/μl的目标序列,但是对感染血液样本的检测灵敏度较差,仅能检测到相当于1000copy/μl的目标序列。引物对4能够检测到0.01ng/μl的目标序列,但是对于感染血液样本的检测观察到非特异性条带出现,对结果的准确判断存在较大干扰。在本发明提及的所有文献都在本申请中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。序列表<110>上海卓立生物科技有限公司<120>用于致病性大肠埃希氏菌检测的多核苷酸、方法和试剂盒<130>00000<160>10<170>siposequencelisting1.0<210>1<211>21<212>dna<213>人工序列(artificialsequence)<400>1tggagaaaataaagtgaaaca21<210>2<211>18<212>dna<213>人工序列(artificialsequence)<400>2atcgctaagagaatcacg18<210>3<211>21<212>dna<213>人工序列(artificialsequence)<400>3tggagaaaataaagtgaaaca21<210>4<211>18<212>dna<213>人工序列(artificialsequence)<400>4atcgctaagagaatcacg18<210>5<211>23<212>dna<213>人工序列(artificialsequence)<400>5ggagaaaataaagtgaaacaaag23<210>6<211>19<212>dna<213>人工序列(artificialsequence)<400>6gtctgatcacccgttaaac19<210>7<211>23<212>dna<213>人工序列(artificialsequence)<400>7ggagaaaataaagtgaaacaaag23<210>8<211>18<212>dna<213>人工序列(artificialsequence)<400>8cagtctgatcacccgtta18<210>9<211>20<212>dna<213>人工序列(artificialsequence)<400>9cctggtagtccacgccgtaa20<210>10<211>351<212>dna<213>大肠埃希氏菌(escherichiacoli)<400>10tttttattttttaatgtatttgtacatggagaaaataaagtgaaacaaagcactattgca60ctggcactcttaccgttactgtttacccctgtgacaaaagcccggacaccagaaatgcct120gttctggaaaaccgggctgctcagggcgatattactgcacccggcggtgctcgccgttta180acgggtgatcagactgccgctctgcgtgattctcttagcgataaacctgcaaaaaatatt240attttgctgattggcgatgggatgggggactcggaaattactgccgcacgtaattatgcc300gaaggtgcgggcggcttttttaaaggtatagatgccttaccgcttaccggg351当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1