AGAP9在制备诊断骨关节炎的产品中的应用的制作方法
本发明涉及疾病诊断领域,更具体地,本发明涉及以检测agap9异常为手段的疾病诊断方法。
背景技术:
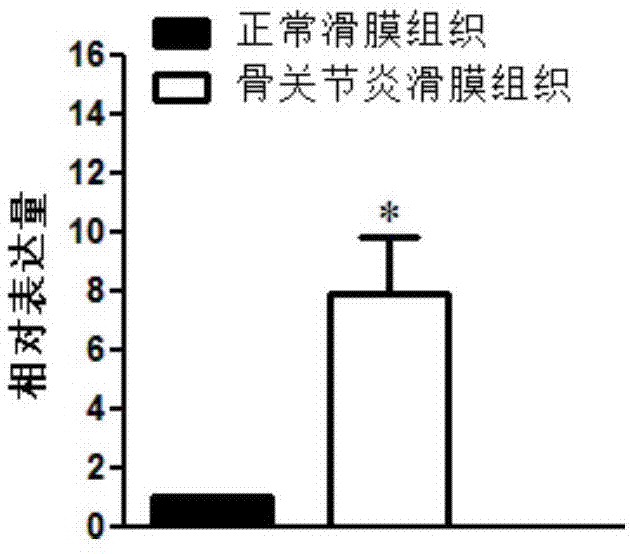
:骨关节炎(oa)作为中老年人较常见的一种慢性、进展性关节疾病,可表现为不同程度的关节肿痛、活动受限等症状,以关节软骨和软骨下骨进行性破坏、关节滑膜炎症反应为主要病理特征,其发病机制迄今尚不完全清楚,早期诊断困难,临床上常用的诊断手段往往针对中晚期患者,早期患者作为一个特殊人群,其早期诊断水平对其健康结局的影响更为直接和明显。骨关节炎被认为是一种慢性疾病,可以长时期保持“沉默”,临床诊断其早期阶段颇为困难;诊断通常是基于临床症状和影像学变化。然而x线有一个可怜的灵敏度和精度,只提供了一个累积损伤,误差相对较大,不能提前检测骨关节炎或监控关节损伤的进展。ct及mri也同样存在一些问题。由于这些工具的局限性,当前可供评估早期阶段的骨关节炎,只有生物标志物:研究集中于软骨基质的结构组件,尤其是ii型胶原降解产物。然而国内外一些学者的实验结果证明单纯检测ii型胶原降解产物,仍不能解决诊断早期阶段骨关节炎的灵敏度和精度问题,这样慢慢就形成这样的共识:单纯检测h型胶原降解产物行不通。近年人们更多关注细胞因子il-1上,特别是,其被认为是骨关节炎发展的核心因素以及单核苷酸多态性基因生物标记物和借助代谢组学等技术,也许有利于检测早期骨关节炎。可能替代的方法,如分子标记,能够量化的,可靠地,敏感地检测骨关节炎的关节在早期阶段的变化。该实验目前还没有走到将来那一步,只是借助目前更成熟更容易普及的临床检测方法,尝试其可行性。在分子水平上尤其是在基因水平上进行骨关节炎的早期诊断已经成为了骨关节炎诊断领域的发展趋势,在诊断方面,申请号为:201510548635.x、2015105495645、2015105486241、201510627048.x、2015107250040、201510724747.6、2015107257552专利文献均披露了可以用于骨关节炎诊断的基因标志物。本申请是在现有技术的启示下寻找新的可以用于骨关节炎诊断的生物标志物。技术实现要素:本发明的目的在于提供一种用于诊断骨关节炎的基因标志物。本发明利用测序和qpcr实验证明了agap9基因在骨关节炎滑膜组织的的表达水平显著高于正常滑膜组织,因此可将agap9基因作为诊断骨关节炎的基因标志物。根据本发明的一个方面,本发明提供了一种用于诊断骨关节炎的产品,所述产品包括检测agap9基因表达的试剂。进一步,所述试剂包括能够定量agap9基因mrna的试剂,和/或能够定量agap9蛋白的试剂。进一步,本发明前面的所述产品包括但不限于芯片、试剂盒、试纸、或高通量测序平台;高通量测序平台是一种特殊的诊断骨关节炎的工具,随着高通量测序技术的发展,对一个人的基因表达谱的构建将成为十分便捷的工作。通过对比疾病患者和正常人群的基因表达谱,容易分析出哪个基因的异常与疾病相关。因此,在高通量测序中获知agap9基因的异常与骨关节炎相关也属于agap9基因的用途,同样在本发明的保护范围之内。本发明的试剂盒包括特异扩增agap9基因的引物。作为本发明的一个具体实施例,所述引物序列如seqidno.1和seqidno.2所示。本发明的试剂盒还可以包括:sybrgreen聚合酶链式反应体系、用于扩增agap9基因和/或管家基因的引物对。优选地,所述sybrgreen聚合酶链式反应体系包含pcr缓冲液、dntps、sybrgreen荧光染料。上述技术方案中,所述pcr缓冲液为本领域技术人员公知的现有技术,优选地,所述pcr缓冲液包含:25mmkcl,2.5mmmgcl2,200mm(nh4)2so4。所述引物对是本领域技术人员可以根据引物设计的常规设计原则设计;在优选的实施方案中,扩增agap9基因的正向序列5’-taagaagaagcaactgta-3’(seqidno.1),反向序列5’-gtgtgatatgatgaggta-3’(seqidno.2);管家基因优选β-actin,扩增该基因的正向引物序列为5’-gtggggcgccccaggcacca-3’(seqidno.3),反向引物序列为5’-ctccttaatgtcacgcacgattt-3’(seqidno.4)。进一步,本发明的试剂盒还可以包含m-mlv逆转录体系,该逆转录体系包含:t重复寡核苷酸oligo(dt)、逆转录反应液、m-mlv逆转录酶、rna酶抑制剂、dntps。优选地,逆转录反应液包含:250mmtris-hcl(ph8.3)、375mmkcl、15mmmgcl2、50mmdtt。rna酶抑制剂可选用本领域常用的rna酶抑制剂,优选为大肠杆菌表达的非竞争性抑制rna酶的重组蛋白酶。优选地,本发明的试剂盒还包含rna提取试剂,rna提取试剂包含trizol、氯仿、异丙醇、75%乙醇。本发明的试剂盒保存于-20℃,尽量减少反复冻融。根据本发明的另一个方面,本发明还提供了检测agap9的试剂在制备诊断骨关节炎的产品中的应用。进一步,所述检测agap9的试剂包括检测agap9基因表达的试剂。更进一步,所述检测agap9基因表达的试剂包括能够定量agap9基因mrna的试剂,和/或能够定量agap9蛋白的试剂。定量agap9基因mrna的试剂包括:如pcr、southern杂交、northern杂交、点杂交、荧光原位杂交(fish)、dna微阵列、aso法、高通量测序平台等定性地、定量地、或半定量地检测基因mrna表达水平的方法中使用的任何试剂。进一步,所述定量agap9基因mrna的试剂包括qpcr中使用的引物,和/或探针。在本发明的具体实施方案中,所述定量agap9基因mrna的试剂包括qpcr中使用的引物,所述引物序列如seqidno.1和seqidno.2所示。上面所述的引物可以通过化学合成来制备,使用本领域技术人员知道的方法参考已知信息来适当地设计,并通过化学合成来制备。前面所述的探针可以通过化学合成来制备,通过使用本领域技术人员知道的方法参考已知信息来恰当设计,并通过化学合成来制备,或者可以通过从生物材料制备含有期望核酸序列的基因,并使用设计用于扩增期望核酸序列的引物扩增它来制备。定量agap9蛋白的试剂包括如elisa、放射免疫测定法、免疫组织化学法、western印迹等能够检测蛋白表达水平的方法中使用的任何试剂。本发明可用于定量agap9蛋白的试剂包括针对agap9蛋白的抗体,所述抗体可以是单克隆抗体、多克隆抗体、多特异性抗体(例如双特异性抗体)。前面所述的本发明的所述产品检测的样本不受特别限制,只要它适于本发明的测定;例如,它可以包括组织、血液、血浆、血清、淋巴液、尿液、浆膜腔液、脊髓液、滑液、房水、泪液、唾液、或其级分或经过处理的材料。在本发明的具体实施方案中,所述样本来自受试者的组织。本发明还提供了一种诊断骨关节炎的方法,所述方法包括如下步骤:(1)获取受试者含有agap9基因表达产物的样本;(2)检测样本中agap9基因或蛋白的表达水平;(3)将测得的agap9基因或蛋白的表达水平与受试者患病与否关联起来;(4)与正常滑膜组织相比,如果agap9基因或蛋白的表达水平升高,则该受试者被诊断为骨关节炎,或判断该受试者患有骨关节炎的风险高。在本发明的上下文中,“诊断骨关节炎”既包括判断受试者是否已经患有骨关节炎、也包括判断受试者是否存在患有骨关节炎的风险。如本文所用,术语”抗体”,意指特异性结合至特定抗原或与特定抗原相互作用的任意抗原-结合分子或分子复合体,其包含至少一个互补决定区(cdr)。术语”抗体”包括含有4个多肽链(即,通过双硫键相互连接的2个重(h)链以及2个轻(l)链)以及其多聚体(例如igm)。每个重链含有重链可变区以及重链恒定区。重链恒定区含有3个结构域ch1、ch2和ch3。每个轻链含有轻链可变区以及轻链恒定区。轻链恒定区含有一个结构域(cl1)。vh与vl区可进一步细分成高变区(称为互补决定区(cdr)),其中散布着较保守的称为框架区(fr)的区域。每个vh和vl均由三个cdr和四个fr组成,从氨基端到羧基端按以下顺序排列:fr1、cdr1、fr2、cdr2、fr3、cdr3和fr4。如本文所用,术语“抗体”还包括整个抗体分子的抗原结合片段。抗体的抗原结合片段可以利用任何适宜的标准技术,例如蛋白水解消化或涉及编码抗体可变区和任选恒定区的dna的操纵和表达的重组基因改造技术,从例如完整的抗体分子衍生。这样的dna是已知的及/或很容易从例如市售来源、dna库(包括例如噬菌体-抗体库)获得,或可以被合成。该dna可以被测序且以化学方法或分子生物学技术加以操纵,从而例如将一个或多个可变区和/或恒定区排列成适宜的构型,或引入密码子、产生半胱氨酸残基、修饰、添加或删除氨基酸等。抗原结合片段的非限制性实例包括:(i)fab片段;(ii)f(ab')2片段;(iii)fd片段;(iv)fv片段;(v)单链fv(scfv)分子;(vi)dab片段;以及(vii)由模拟抗体高变区(例如孤立的互补决定区(cdr),如cdr3肽)的氨基酸残基组成的最小识别单元或约束型fr3-cdr3-fr4肽。抗原结合片段还包括其它工程化的分子,如结构域特异性抗体、单域抗体、结构域缺失的抗体、嵌合抗体、cdr移植的抗体、双抗体、三抗体、四抗体、微抗体、纳米抗体(例如单价纳米抗体、二价纳米抗体等)、小模块免疫药物(smallmodularimmunopharmaceuticals)(smip),以及鲨鱼可变ignar域。“单克隆抗体”是由单克隆的b-淋巴细胞或由已经将编码单个抗体(或其抗原结合片段)的抗体轻链和重链可变区的核酸转染至其中的细胞或其后代产生的抗体。单克隆抗体通过本领域技术人员已知的方法产生,例如通过从骨髓瘤细胞与免疫脾细胞的融合制造杂合抗体形成细胞来进行。这些融合细胞和它们的后代被称为“杂交瘤”。“多特异性抗体”可以是对一个标的多肽的不同表位具有特异性或者可能含有对超过一个标的多肽具有特异性的抗原-结合域。参见例如tutt等,1991,j.immunol.147:60-69;kufer等,2004,trendsbiotechnol.22:238-244。抗体或其片段在功能上可以链接(例如,通过化学偶合、遗传融合、非共价缔合或其他方式)至一或多个其他分子实体,诸如另一个抗体或抗体片段,以产生带有第二种结合特异性的双特异性或多特异性抗体。在本发明的上下文中,“agap9基因”(nc_000010.11(47501854..47523638,complement))序列可在国际公共核酸序列数据库genebank中查询到。附图说明图1显示利用qpcr在mrna水平上检测agap9基因差异表达情况的统计图。具体的实施方式下面结合附图和实施例对本发明作进一步详细的说明。以下实施例仅用于说明本发明而不用于限制本发明的范围。实施例中未注明具体条件的实验方法,通常按照常规条件,例如sambrook等人,分子克隆:实验室手册(newyork:coldspringharborlaboratorypress,1989)中所述的条件,或按照制造厂商所建议的条件。实施例1筛选差异表达基因1、取材:5例oa患者的滑膜组织(oa组)来自于行膝关节置换或滑膜切除术的oa病人。所用病例符合altam提出的关于oa的诊断标准。3例正常滑膜组织(nor组)来自于外伤手术病人关节滑膜组织。本研究中所用临床样本,均对患者进行知情告知并经医院的伦理委员会通过。选择的研究对象的临床信息如表1所示。表1临床信息2、组织rna的获取从组织样品中提取totalrna,利用nanodrop2000对所提rna的浓度和纯度进行检测,琼脂糖凝胶电泳检测rna完整性,agilent2100测定rin值。单次建库要求rna总量5μg,浓度≥200ng/μl,od260/280介于1.8~2.2之间。3、mrna文库构建真核生物mrna3’末端具有ploya尾的结构,用带有oligo(dt)的磁珠富集真核生物mrna。加入fragmentationbuffer将mrna打断成短片段,以mrna为模板,用六碱基随机引物(randomhexamers)合成第一条cdna链,然后加入缓冲液、dntps、rnaseh和dnapolymerasei合成第二条cdna链,在经过qiaquickpcr试剂盒纯化并加eb缓冲液洗脱之后做末端修复并连接测序接头,然后用琼脂糖凝胶电泳进行片段大小选择,最后进行pcr扩增,使用建好的文库上机测序。4、上机测序lluminahiseqx-ten上机测序流程(mrna)(1)文库富集,pcr扩增15个cycles;(2)2%琼脂糖胶回收目的条带(certifiedlowrangeultraagarose);(3)tbs380(picogreen)定量,按数据比例混合上机;(4)cbot上进行桥式pcr扩增,生成clusters;(5)hiseqx-ten测序平台,进行2*100bp/300bp测序。5、生物信息学分析测序数据获得以后的mrna分析过程如下所示:(1)用cutadapt对reads的5’和3’段进行trim,trim掉质量<20的碱基,并且删掉n大于10%的reads(用fastqc看一下测序数据的质量,拿到的数据完成处理时可跳过此步);(2)tophat比对到mrna参考基因组上。mrna所用的参考基因组版本为grch38.p7,fasta和gff文件下载自ncbi;(3)cuffquant定量mrna的表达量并标准化输出;(4)cuffdiff包比较对照组跟疾病组mrna的表达差异。6、结果显著差异mrna筛选条件:p<0.05,|log2fc|>1。用以上标准筛选得到在正常滑膜组织和骨关节炎滑膜组织之间存在差异基因1068个,其中表达上调基因516个,表达下调的基因有552个。实施例2大样本验证筛选出的差异表达基因基于前期测序的结果,根据pvalue的大小,我们选择agap9基因进行验证。1、样本收集按照实施例1的方法收集骨关节炎滑膜组织和正常滑膜组织各42例。2、在mrna水平上进行验证2.1提取组织rna步骤同实施例1。2.2逆转录反转录使用primescript1ststrandcdnasynthesiskit试剂盒,操作步骤如下进行:(1)在微量离心管中加入以下反应液体,如表2所示:表2反应液体(2)70℃孵育5min,迅速冷却至4℃;在微量离心管内加入以下反应试剂,制成反应体系,如表3所示:表3反应体系的配制试剂剂量5x1ststrandsynthesisbuffer4.0μlprimescriptrtase1.0μlrnaseinhibitor1.0μlrnasefreedh2o4.0μl轻轻震荡,快速离心后,42℃反应1h,70℃10min终止反应,4℃冷却,-20℃保存。采用sybppremixextaptmii试剂盒,在eppendorfreal-timepcr分析仪进行,具体操作如下:(1)在冰上配制以下pcr反应液,如表4所示:表4pcr反应液的配制引物序列设计如下:agap9基因:5’-taagaagaagcaactgta-3’(seqidno.1);5’-gtgtgatatgatgaggta-3’(seqidno.2)β-actin:5’-gtggggcgccccaggcacca-3’(seqidno.3);5’-ctccttaatgtcacgcacgattt-3’(seqidno.4)(2)上机,执行下述程序:95℃预变性3min;95℃变性15s。49℃退火20s,72℃延伸20s,共40个循环。结果釆用相对定量法,运用公式2-△△ct计算。实验重复3次。△ct=ct(a)-ct(β-actin)△△ct=△ct(实验组)-△ct(对照组)结果显示,42例骨关节炎滑膜组织中有42例骨关节炎滑膜组织中的agap9基因mrna水平相比正常滑膜组织的平均值显著上调;统计结果如图1所示,与正常滑膜组织相比,骨关节炎滑膜组织中agap9基因的mrna水平明显增加,差异具有统计学意义(p<0.05)。上述实施例的说明只是用于理解本发明的方法及其核心思想。应当指出,对于本领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也将落入本发明权利要求的保护范围内。序列表<110>德阳市人民医院<120>agap9在制备诊断骨关节炎的产品中的应用<160>4<170>siposequencelisting1.0<210>1<211>18<212>dna<213>人工序列(artificialsequence)<400>1taagaagaagcaactgta18<210>2<211>18<212>dna<213>人工序列(artificialsequence)<400>2gtgtgatatgatgaggta18<210>3<211>20<212>dna<213>人工序列(artificialsequence)<400>3gtggggcgccccaggcacca20<210>4<211>23<212>dna<213>人工序列(artificialsequence)<400>4ctccttaatgtcacgcacgattt23当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1