H7N9病毒检测用的核酸组合物和H7N9病毒实时荧光定量检测试剂盒及其应用的制作方法
本发明涉及分子诊断领域,特别是涉及一种h7n9病毒检测用的核酸组合物和h7n9病毒实时荧光定量检测试剂盒及其应用。
背景技术:
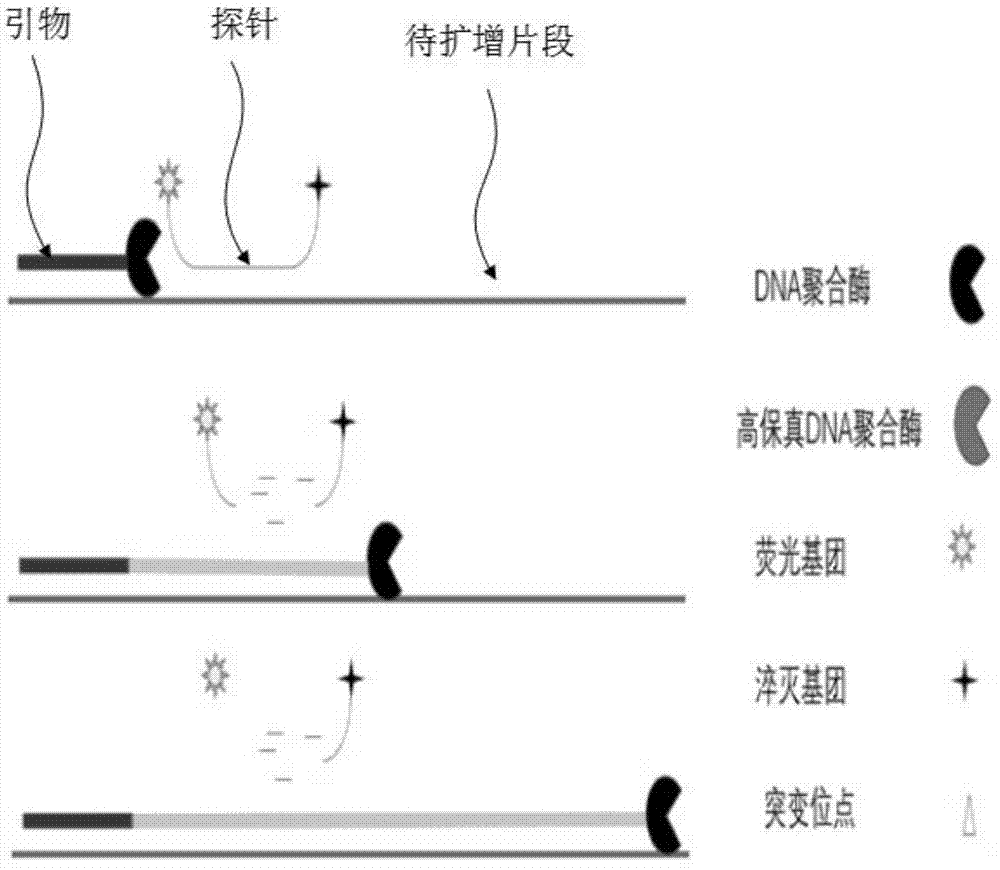
:流感病毒属于正粘病毒科,遗传物质为单股、负链、多节段的核糖核酸(rna)分子。根据流感病毒核蛋白(nuclearprotein,np)抗原性差异,可将流感病毒分为a、b、c三型,其中,a型流感病毒为最常见的流感病毒,宿主范围广泛,可感染大多数哺乳动物、家禽以及野鸟。根据流感病毒表面血凝素(ha,是决定病毒毒力最重要的蛋白)和神经氨酸酶(na,是导致流感炉散的糖蛋白,可以催化唾液酸水解,协助成熟流感病毒脱离宿主细胞而感染新的细胞)氨基酸的差异,又可将a型流感病毒分为18个ha亚型和11个na亚型。h7n9病毒是流感病毒中的一种,其表面有血凝素h7亚型和神经氨酸酶n9亚型。人感染h7n9禽流感是由甲型流感病毒h7n9亚型引起的急性呼吸道传染病。患者一般表现为流感样症状,如发热,咳嗽,少痰,可伴有头痛、肌肉酸痛和全身不适。重症患者病情发展迅速,表现为重症肺炎,体温大多持续在39℃以上,出现呼吸困难,可伴有咯血痰;可快速进展出现急性呼吸窘迫综合征、纵隔气肿、脓毒症、休克、意识障碍及急性肾损伤等。2013年2月,首次报告人感染h7n9禽流感病毒疫情,2013年3月31日,国家卫生和计划生育委员会通报确认,在上海和安徽发现3例第一次发现有人感染h7n9禽流感病例,此前此病毒仅在禽类间有传染。截至2017年2月,中国已发生5次人感染h7n9禽流感病毒疫情,为了防止疫情传染,采取关闭活禽市场、暂停各类活禽交易、严格控制活禽运输等措施,很大程度上制约了相关地区家禽养殖业的发展,对人民群众的生产生活造成较大影响。人感染h7n9禽流感诊疗的实验室检查包括血常规、血生化、病原学检查等。病原学检测是人感染h7n9禽流感的筛查、确认重要的环节。流感病毒检测的“金标准”是病毒培养,但病毒培养操作复杂,实验室硬件要求高,周期长,阳性率低,限制了其应用。近年来,随着分子诊断技术的发展,pcr荧光探针技术以其简便快捷、特异性、敏感性、实时定量等优势而应用于人感染h7n9禽流感的筛查和确认,以克服传统临床诊断的缺陷。然而,传统的pcr荧光探针技术包括了三条核苷酸序列,分别为正向引物、反向引物和探针。引物的平均长度为20bp左右,探针的平均长度为35bp~30bp,则要求保守区域的平均长度足够长,并且该技术的检测灵敏度较低,不能满足实际需求。技术实现要素:基于此,有必要提供一种h7n9病毒检测用的核酸组合物,该h7n9病毒检测用的核酸组合物对保守区域的平均长度要求较低,且检测灵敏度较高。此外,还提供一种h7n9病毒实时荧光定量检测试剂盒及其应用。一种h7n9病毒检测用的核酸组合物,包括:用于扩增血凝素h7基因待扩增片段的第一正向引物与第一反向引物,所述第一正向引物从5’端到3’端包括第一匹配片段和第一连接片段,所述第一匹配片段能够与所述血凝素h7基因待扩增片段互补配对,所述第一正向引物的两端分别结合有第一荧光基团和第一荧光猝灭基团;和/或,用于扩增神经氨酸酶n9基因待扩增片段的第二正向引物与第二反向引物,所述第二正向引物从5’端到3’端包括第二匹配片段和第二连接片段,所述第二匹配片段能够与所述神经氨酸酶n9基因待扩增片段互补配对,所述第二正向引物的两端分别结合有第二荧光基团和第二荧光猝灭基团。上述h7n9病毒检测用的核酸组合物中第一正向引物从5’端到3’端包括第一匹配片段及第一连接片段,第一匹配片段能够与血凝素h7基因待扩增片段互补配对,第一正向引物的两端分别结合有第一荧光基团和第一荧光猝灭基团,使得第一正向引物不仅能够作为引物,还能够作为探针,以提供荧光信号而进行定量检测,从而降低对保守区域的平均长度的要求;第二正向引物从5’端到3’端包括第二匹配片段及第二连接片段,第二匹配片段能够与神经氨酸酶n9基因待扩增片段互补配对,第二正向引物的两端分别结合有第二荧光基团和第二荧光猝灭基团,使得第二正向引物不仅能够作为引物,还能够作为探针,以提供荧光信号而进行定量检测,从而降低对保守区域的平均长度的要求。经试验验证,与采用传统的pcr荧光探针技术进行h7n9病毒的检测相比,采用上述h7n9病毒检测用的核酸组合物的检测灵敏度更高。在其中一个实施例中,所述第一连接片段为polya片段;和/或,所述第二连接片段为polya片段。在其中一个实施例中,所述第一正向引物还包括第一容错片段,所述第一容错片段位于所述第一匹配片段和所述第一连接片段之间,所述第一容错片段针对所述血凝素h7基因待扩增片段的高变区进行设计,且所述第一容错片段能够在所述血凝素h7基因待扩增片段的高变区发生变异时被切断;和/或,所述第二正向引物还包括第二容错片段,所述第二容错片段位于所述第二匹配片段和所述第二连接片段之间,所述第二容错片段针对所述神经氨酸酶n9基因待扩增片段的高变区进行设计,且所述第二容错片段能够在所述神经氨酸酶n9基因待扩增片段的高变区发生变异时被切断。在其中一个实施例中,所述第一容错片段含有2~4个碱基;和/或,所述第二容错片段含有2~4个碱基。在其中一个实施例中,所述第一正向引物的核苷酸序列如seqidno.1所示,所述第一反向引物的核苷酸序列如seqidno.2所示;和/或,所述第二正向引物的核苷酸序列如seqidno.3所示,所述第二反向引物的核苷酸序列如seqidno.4所示。在其中一个实施例中,所述第一正向引物的5’端结合有所述第一荧光基团,所述第一正向引物的3’端结合有所述第一荧光猝灭基团;和/或,所述第二正向引物的5’端结合有所述第二荧光基团,所述第二正向引物的3’端结合有所述第二荧光猝灭基团。在其中一个实施例中,所述第一荧光基团选自fam、hex及vic中的一种,所述第一荧光猝灭基团选自tamara及bhq1中的一种。在其中一个实施例中,所述第二荧光基团选自fam、hex及vic中的一种,所述第二荧光猝灭基团选自tamara及bhq1中的一种。一种h7n9病毒实时荧光定量检测试剂盒,包括上述h7n9病毒检测用的核酸组合物。上述h7n9病毒检测用的核酸组合物在制备h7n9病毒检测试剂中的应用。附图说明图1为传统的荧光探针技术的扩增过程原理示意图;图2为一实施方式的h7n9病毒实时荧光定量检测试剂盒检测未发生变异的h7n9病毒的原理示意图;图3为图2所示实施方式的h7n9病毒实时荧光定量检测试剂盒检测发生变异的h7n9病毒的原理示意图;图4为实施例1的阴性对照的扩增曲线;图5为实施例1的实验组1的扩增曲线;图6为实施例1的实验组2的扩增曲线;图7为实施例1的实验组3的扩增曲线;图8为实施例2的采用试剂盒1与试剂盒2对待测样品进行检测后的扩增曲线对比图;图9为实施例3的采用试剂盒1与试剂盒2对待测样品进行检测后的扩增曲线对比图。具体实施方式为使本发明的上述目的、特征和优点能够更加明显易懂,下面结合具体实施例及附图对本发明的具体实施方式做详细的说明。在下面的描述中阐述了很多具体细节以便于充分理解本发明。但是本发明能够以很多不同于在此描述的其它方式来实施,本领域技术人员可以在不违背本发明内涵的情况下做类似改进,因此本发明不受下面公开的具体实施的限制。未特别说明,序列表中的碱基序列均为从5’端到3’端的顺序。一实施方式的h7n9病毒实时荧光定量检测试剂盒,该试剂盒能够对待测样中h7n9病毒进行检测,特异性较高,灵敏度较高,检测结果的准确性较高,进而能够用于制备h7n9病毒检测装置。上述h7n9病毒实时荧光定量检测试剂盒包括反应液和反应酶。在其中一个实施例中,待测样品为血液或唾液。反应液包括h7n9病毒检测用的核酸组合物。h7n9病毒检测用的核酸组合物对保守区域的平均长度要求较低,且检测灵敏度较高。具体地,h7n9病毒检测用的核酸组合物包括第一正向引物、第一反应引物、第二正向引物及第二反向引物。第一正向引物与第一反应引物用于扩增血凝素h7基因待扩增片段。血凝素是指红血球凝聚素(hemagglutinin,ha),是流感病毒包膜表面的糖蛋白,也是决定病毒毒力的蛋白。红血球凝聚素有18(h1~h18)种形态。其中禽流感病毒h7n9表面的血凝素即为血凝素h7。在其中一个实施例中,第一正向引物从5’端到3’端包括第一匹配片段及第一连接片段。第一匹配片段能够与血凝素h7基因待扩增片段互补配对。第一正向引物的两端分别结合有第一荧光基团和第一荧光猝灭基团。此种设置,使得第一正向引物不仅能够作为引物,还能够作为探针,以提供荧光信号而达到定量检测的目的,从而对保守区域的平均长度要求较低,且检测灵敏度较高。在其中一个具体示例中,第一连接片段为polya片段。进一步地,第一连接片段含有4~6个a碱基。在其中一个实施例中,第一荧光基团选自fam、hex及vic中的一种。第一荧光猝灭基团选自tamara及bhq1中的一种。在其中一个实施例中,第一正向引物的5’端结合有第一荧光基团,第一正向引物的3’端结合有第一荧光猝灭基团。此种设置,将第一荧光猝灭基团连接于第一连接片段的3’端,使得在扩增血凝素h7基因待扩增片段的过程中,第一荧光猝灭基团能够随第一连接片段被切掉,从而使扩增反应能够继续。在其中一个实施例中,第一正向引物还包括第一容错片段。第一容错片段位于第一匹配片段和第一连接片段之间。第一容错片段针对血凝素h7基因待扩增片段的高变区进行设计。且第一容错片段能够在血凝素h7基因待扩增片段的高变区发生变异时被切断。此种设置,使得在扩增血凝素h7基因待扩增片段的过程中,若遇到血凝素h7基因待扩增片段的高变区发生变异,第一容错片段则无法与发生变异的位置互补配对,此时,能够从第一容错片段中与变异位置对应的位置切断第一容错片段,以使扩增反应继续而检测血凝素h7基因,以避免因血凝素h7基因待扩增片段变异无法继续扩增而形成漏检,检测的准确性较高。可选地,第一容错片段能够在血凝素h7基因待扩增片段的高变区发生变异时被pfu酶切断。需要说明的是,血凝素h7基因待扩增片段的高变区发生变异可以为单一碱基的突变,可以为多个碱基的突变。当该变异为一个碱基的突变时,第一容错片段则无法与该变异的碱基互补配对。当该变异为多个碱基的突变时,可以为连续多个碱基突变,也可以为多个间隔的碱基突变。当该变异为多个碱基的突变时,第一容错片段则无法与该多个变异的碱基互补配对。需要说明的是,若遇到血凝素h7基因待扩增片段的高变区中一个碱基发生变异时,能够从第一容错片段中与变异碱基对应的位置切断第一容错片段。若遇到血凝素h7基因待扩增片段的高变区中多个碱基发生变异时,能够从第一容错片段中与最靠近5’端的变异碱基对应的位置切断第一容错片段。在其中一个实施例中,第一正向引物从5’端到3’端包括依次连接的第一匹配片段、第一容错片段和第一连接片段。进一步地,第一容错片段含有2~4个碱基。此时,第一容错片段能够在血凝素h7基因待扩增片段的高变区中对应位置的2~4个碱基中至少一个发生变异时被切断。在其中一个实施例中,第一正向引物与第一反向引物根据h7n9亚型禽流感病毒的血凝素抗原(ha)基因序列(genbank:kc853766)设计。第二正向引物和第二反向引物用于扩增神经氨酸酶n9基因待扩增片段。神经氨酸酶又称唾液酸酶(neuraminidase,na),是分布于流感病毒被膜上的一种糖蛋白,具有抗原性,可以催化唾液酸水解,协助成熟流感病毒脱离宿主细胞感染新的细胞。目前,已知的甲型流感病毒中共有11种不同的神经氨酸酶抗原型(即n1~n11)。其中,禽流感病毒h7n9表面的神经氨酸酶即为神经氨酸酶n9。在其中一个实施例中,第二正向引物从5’端到3’端包括第二匹配片段及第二连接片段。第二匹配片段能够与神经氨酸酶n9基因待扩增片段互补配对。第二正向引物的两端分别结合有第二荧光基团和第二荧光猝灭基团。此种设置,使得第二正向引物不仅能够作为引物,还能够作为探针,以提供荧光信号而达到定量检测的目的,从而对保守区域的平均长度要求较低,且检测灵敏度较高。在其中一个具体示例中,第二连接片段为polya片段。进一步地,第二连接片段含有4~6个a碱基。在其中一个实施例中,第二荧光基团选自fam、hex及vic中的一种。第二荧光猝灭基团选自tamara及bhq1中的一种。在其中一个实施例中,第二正向引物的5’端结合有第二荧光基团,第二正向引物的3’端结合有第二荧光猝灭基团。此种设置,将第二荧光猝灭基团连接于第二连接片段的3’端,使得在扩增神经氨酸酶n9基因待扩增片段的过程中,第二荧光猝灭基团能够随第二连接片段被切掉,从而使扩增反应能够继续。在其中一个实施例中,第二正向引物还包括第二容错片段。第二容错片段位于第二匹配片段和第二连接片段之间。第二容错片段针对神经氨酸酶n9基因待扩增片段的高变区进行设计。且第二容错片段能够在神经氨酸酶n9基因待扩增片段的高变区发生变异时被切断。此种设置,使得扩增神经氨酸酶n9基因待扩增片段的过程中,若遇到神经氨酸酶n9基因待扩增片段的高变区发生变异,第二容错片段则无法与发生变异的位置互补配对,此时,能够从第二容错片段中与变异位置对应的位置切断第二容错片段,使扩增反应继续以检测神经氨酸酶n9基因,以避免检测神经氨酸酶n9基因待扩增片段变异无法继续扩增而形成漏检,检测的准确性较高。可选地,第二容错片段能够在神经氨酸酶n9基因待扩增片段的高变区发生变异时被pfu酶切断。需要说明的是,神经氨酸酶n9基因待扩增片段的高变区发生变异可以为单一碱基的突变,可以为多个碱基的突变。当该变异为一个碱基的突变时,第二容错片段则无法与该变异的碱基互补配对。当该变异为多个碱基的突变时,可以为连续多个碱基突变,也可以为多个间隔的碱基突变。当该变异为多个碱基的突变时,第二容错片段则无法与该多个变异的碱基互补配对。需要说明的是,若遇到神经氨酸酶n9基因待扩增片段的高变区中一个碱基发生变异时,能够从第二容错片段中与变异碱基对应的位置切断第二容错片段。若遇到神经氨酸酶n9基因待扩增片段的高变区中多个碱基发生变异时,能够从第二容错片段中与最靠近5’端的变异碱基对应的位置切断第二容错片段。在其中一个实施例中,第二正向引物从5’端到3’端包括依次连接的第二匹配片段、第二容错片段和第二连接片段。进一步地,第二容错片段含有2~4个碱基。此时,第二容错片段能够在神经氨酸酶n9基因待扩增片段的高变区中对应位置的2~4个碱基中至少一个发生变异时被切断。在其中一个实施例中,第二正向引物与第二反向引物根据h7n9亚型禽流感病毒的神经氨酸酶抗原(na)基因序列(genbank:kc853765)设计。在其中一个具体示例中,第一正向引物的核苷酸序列如seqidno.1所示,第一反向引物的核苷酸序列如seqidno.2所示;第二正向引物的核苷酸序列如seqidno.3所示,第二反向引物的核苷酸序列如seqidno.4所示。采用此h7n9病毒检测用的核酸组合物进行h7n9病毒检测,特异性、灵敏度及准确性均较高。具体地,如seqidno.1所示的核苷酸系列为5’-aaacccggtcaaactaagcagcggctacaaaa-3’,其中,第一匹配片段为aaacccggtcaaactaagcagcgg,第一容错片段为ctac,第一连接片段为aaaa;如seqidno.2所示的核酸序列为5’-ccgaagctaaaccaragtatcaca-3’;如seqidno.3所示的核苷酸序列为5’-aaatcaccgcccacagtgtacaatagcaaaa-3’,其中,第二匹配片段为aaatcaccgcccacagtgtacaa,第二容错片段为tagc,第二连接片段为aaaa;如seqidno.4所示的核苷酸序列为5’-actagtacttgaccamccaatgca-3’。进一步地,第一正向引物的5’端结合有第一荧光基团,第一正向引物的3’端结合有第一荧光猝灭基团,第一荧光基团为fam,第一荧光猝灭基团为tamara。第二正向引物的5’端结合有第二荧光基团,第二正向引物的3’端结合有第二荧光猝灭基团,第二荧光基团为hex,第二荧光猝灭基团为tamara。在其中一个实施例中,反应液包括10μm~20μm的第一正向引物、10μm~20μm的第一反向引物、10μm~20μm的第二正向引物、10μm~20μm的第二反向引物。进一步地,反应液还包括tris-hcl、mg2+、dntp等常见的荧光定量pcr反应试剂。具体地,反应液还包括60mm~150mm的tris-hcl、30mm~50mm的(nh4)2so4、6mm~10mm的mgso4、体积百分含量为5%~10%的甘油、体积百分含量为0.66%~1%的牛血清白蛋白(即bsa)、体积百分含量为0.12%~0.5%的乙基苯基聚乙二醇(即np-40)、体积百分含量为0.1%~0.2%的吐温20、100mm~150mm的kcl、4mm~6mm的mgcl2、1mm~2mm的二硫苏糖醇(即dtt)、体积百分含量为3%~6%的dmso及80μg/ml~100μg/ml的bt。其中,bt为牛凝血酶。更进一步地,反应液还包括0.4mm~0.8mm的dntps。在其中一个实施例中,h7n9病毒实时荧光定量检测试剂盒还包括反应酶,反应酶包括pfu酶。pfu酶即为pfudna聚合酶(pfudnapolymerase),是在嗜热的古核生物火球菌属内发现的、一类能在活体内进行dna复制的酶。该酶同时具有5’-3’聚合酶活性和3’-5’外切核酸酶活性,因此,在聚合反应中能够通过切断错误掺入的碱基以纠正错配。通过在h7n9病毒实时荧光定量检测试剂盒中加入pfu酶,使得在基因扩增过程中,若遇到基因突变,能够通过切断第一容错片或第二容错片段而使扩增反应继续,以到达检测h7n9病毒的目的,提高检测的准确性。在其中一个实施例中,反应酶包括2u/μl~5u/μl的pfu酶。进一步地,pfu酶为neb公司且货号为e0555的pfu酶或qiagen公司的pfu酶。进一步地,反应酶还包括10u/μl~20u/μl的逆转录酶。通过逆转录酶能够将h7n9病毒的rna逆转录成cdna。在其中一个实施例中,反应酶与反应液的体积比为15:5~19:1。在其中一个实施例中,h7n9病毒实时荧光定量检测试剂盒还包括rna提取试剂。rna提取试剂用于提取h7n9病毒的rna。进一步地,rna提取试剂为病毒rna提取试剂盒。更进一步地,rna提取试剂为深圳市刚竹医疗科技有限公司的货号为rv010-50的病毒rna提取试剂盒。需要说明的是,rna提取试剂不限于上指出的病毒rna提取试剂盒,也可以为其他厂家的病毒rna提取试剂盒。在其中一个实施例中,h7n9病毒实时荧光定量检测试剂盒还包括h7n9阳性对照和h7n9阴性对照。进一步地,阳性对照品为含有阳性核苷酸序列的质粒。进一步地,该阳性核苷酸序列与h7n9病毒dna的序列相同。h7n9阴性对照为无核酸水。上述h7n9病毒检测用的核酸组合物中第一正向引物与第二正向引物的设计原理如下:选择并确定待扩增片段的高变区;根据该高变区设计容错片段所在位置,容错片段与未变异的参考序列匹配;再从容错片段的3’端到5’端的方向设计匹配片段,匹配片段与参考序列的上游区域匹配;再于容错片段的3’端加上连接片段,用于连接荧光猝灭基团,从而得到正向引物。上述h7n9病毒实时荧光定量检测试剂盒的操作原理如下:从图1可以看出,传统的pcr荧光探针技术包括三条核苷酸序列,分别为正向引物、反向引物和探针。正向引物与反向引物用于模板链的扩增,探针用于提供荧光源。当探针完整时,荧光基团发射的荧光信号被淬灭基团吸收。当进行扩增时,探针被酶切降解而使荧光基团和荧光淬灭基团分离,此时,荧光监测系统能够接收到荧光信号而实现荧光检测。从图2可以看出,采用上述h7n9病毒实时荧光定量检测试剂盒对未发生突变的h7n9病毒进行检测时,正向引物即作为引物,又作为探针。当正向引物完整时,荧光基团发射的荧光信号被淬灭基团吸收。而在扩增过程中,该正向引物的连接片段被高保真dna聚合酶切断,以使荧光淬灭基团与荧光基团分离,并使扩增反应能够继续,而实现实时荧光定量检测。从图3可以看出,采用上述h7n9病毒实时荧光定量检测试剂盒对发生突变的h7n9病毒进行检测时,正向引物即作为引物,又作为探针。当正向引物完整时,荧光基团发射的荧光信号被淬灭基团吸收。而在扩增过程中,若待扩增片段的高变区发生变异,该正向引物的容错片段中与变异处对应的位置被高保真dna聚合酶切断,以使荧光淬灭基团与荧光基团分离,并使扩增反应能够继续,而实现实时荧光定量检测。上述h7n9病毒实时荧光定量检测试剂盒至少具有如下优点:上述h7n9病毒检测用的核酸组合物中第一正向引物从5’端到3’端包括的第一匹配片段及第一连接片段,第一匹配片段能够与血凝素h7基因待扩增片段互补配对,第一正向引物的两端分别结合有第一荧光基团和第一荧光猝灭基团,使得第一正向引物不仅能够作为引物,还能够作为探针,以提供荧光信号而进行定量检测,从而降低对保守区域的平均长度的要求;第二正向引物从5’端到3’端包括第二匹配片段及第二连接片段,第二匹配片段能够与神经氨酸酶n9基因待扩增片段互补配对,第二正向引物的两端分别结合有第二荧光基团和第二荧光猝灭基团,使得第二正向引物不仅能够作为引物,还能够作为探针,以提供荧光信号而进行定量检测,从而降低对保守区域的平均长度的要求。经试验验证,与采用传统的pcr荧光探针技术进行h7n9病毒的检测相比,采用上述h7n9病毒检测用的核酸组合物的检测灵敏度更高。再者,传统的pcr荧光探针技术包括了三条核苷酸序列,分别为正向引物、反向引物和探针。引物的平均长度为20bp左右,探针的平均长度为35bp~30bp。因此,要求保守区域的平均长度最低为80bp~100bp,在病毒的基因组中,如果选择特别保守的区域,则容易把其他的基因扩增出来,造成交叉扩增或非特异性扩增,如果选择高变区域,则容易在有突变的情况下信号弱或者漏检。同时,h7n9病毒的基因组保守区域较长,但区分度较高的区域较少,适合做引物设计区域的dna序列很有限。上述h7n9病毒检测用的核酸组合物中,通过使第一正向引物与第二正向引物即作为引物又作为探针,从而使得通过较短的保守区域及上述四条核苷酸序列即可进行h7n9病毒的检测,降低对保守区域的序列长度的要求,检测灵敏度更高。最后,上述h7n9病毒检测用的核酸组合物包括第一容错片段和第二容错片段,扩增血凝素h7基因待扩增片段或神经氨酸酶n9基因待扩增片段的过程中,若遇到血凝素h7基因待扩增片段突变或神经氨酸酶n9基因待扩增片段突变,能够通过切断第一容错片段或第二容错片段而使扩增反应继续以检测h7n9病毒,以避免因基因突变无法继续扩增而形成漏检,不仅能够对正常的h7n9病毒进行准确检测,还能够对基因突变的h7n9病毒进行准确检测,检测的准确性较高,检测范围更大。以下为具体实施例部分:实施例中采用试剂和仪器如非特别说明,均为本领域常规选择。实施例中未注明具体条件的实验方法,通常按照常规条件,例如文献、书本中所述的条件或者试剂盒生产厂家推荐的方法实现。实施例中所使用的试剂均为市售。如未特别说明,以下实施例中,逆转录酶为invtrogen公司的货号为c28025的逆转录酶;pfu酶为qiagen公司的pfu酶。第一正向引物与第一反向引物根据h7n9亚型禽流感病毒的血凝素抗原(ha)基因序列(genbank:kc853766)设计。第二正向引物与第二反向引物根据h7n9亚型禽流感病毒的神经氨酸酶抗原(na)基因序列(genbank:kc853765)设计。如未特别说明,以下实施例中,试剂盒1为包括:反应酶与反应液。反应酶包括2u/μl的pfu酶及10u/μl的逆转录酶。反应液包括10μm的第一正向引物、10μm的第一反向引物、10μm的第二正向引物、10μm的第二反向引物、120mm的tris-hcl、33.2mm的(nh4)2so4、6mm的mgso4、体积百分含量为10%的甘油、体积百分含量为0.66%的牛血清白蛋白(即bsa)、体积百分含量为0.12%的乙基苯基聚乙二醇(即np-40)、体积百分含量为0.1%的吐温20、100mm的kcl、4mm的mgcl2、1mm的二硫苏糖醇(即dtt)、体积百分含量为3%的dmso、80μg/mlml的bt及0.8mm的dntps;第一正向引物的核苷酸序列如seqidno.1所示,第一反向引物的核苷酸序列如seqidno.2所示;第二正向引物的核苷酸序列如seqidno.3所示,第二反向引物的核苷酸序列如seqidno.4所示。第一正向引物的5’端结合有fam,第一正向引物的3’端结合有tamara;第二正向引物的5’端结合有hex,第二正向引物的3’端结合有tamara。试剂盒2与试剂盒1大致相同,不同之处在于,试剂盒2的反应液包括10μm的第一正向引物、10μm的第一反向引物及10μm的第一探针,的第一正向引物的核苷酸序列如seqidno.5所示(即为5’-gaggcaatgcaaatagaatacagat-3’),第一反向引物的核苷酸序列如seqidno.6所示(即为5’-ccgaagctaaaccagagtatcaca-3’),第一探针的核苷酸序列如seqidno.7所示(即为5’-acccggtcaaactaagcagcggctayaa-3’);兼并碱基y为c碱基或t碱基,第一探针的5’端结合有fam,第一探针的3’端结合有bhq2。实施例1(1)采用通用型病毒rna提取试剂盒(购于深圳市刚竹医疗科技有限公司)并按照其操作说明提取待测样品中的病毒rna,并将提取的病毒rna保存于-80℃。其中,待测样品包括样品1~3,样品1为武汉病毒研究所保藏中心的h7n9灭活病毒,样品2为武汉病毒研究所保藏中心的h7灭活病毒,样品3为武汉病毒研究所保藏中心的n9灭活病毒。阳性对照品为含有阳性核苷酸序列的质粒,样品1~3均设置相应的阳性对照品。阳性对照品解冻,并于使用前在2000rpm离心20s。阴性对照品为无核酸水。(2)准备试剂盒1。从试剂盒1中取出反应液和反应酶,冰上融化。在使用前于2000rpm离心10s备用。(3)取灭过菌的1.5ml离心管,向每个离心管中加入19μl的反应酶,再加入1μl的反应液,混匀后短暂离心(即2000rpm离心20s)。实验分组为实验组1~3、阳性对照组及阴性对照组,实验组1~3中每组三个离心管,阳性对照组及阴性对照组各1个离心管。向实验组1的每管加入5μl的样品1的病毒rna,向实验组2的每管加入5μl的样品2的病毒rna,向实验组3的每管加入5μl的样品3的病毒rna,阳性对照组及阴性对照组的离心管分别加入5μl的阳性对照品和5μl的阴性对照品,并按照表1的反应条件进行荧光定量pcr反应。荧光信号采集设定在退火温度,h7基因的报告荧光为fam,淬灭基团选none;n9基因的报告荧光为joe,淬灭基团选none。表1荧光定量pcr反应条件(4)对检测结果进行分析。具体地,分析条件设置:根据分析后图像调节基线(baseline)的start值、stop值以及阈值(threshold)的value值(可根据实际情况自行调整,start值可以在3~15、end值可以在5~20,调整阴性对照的扩增曲线平直或低于阈值线),使仪器给出正确的结果。质量控制的标准为:(a)阴性对照品检测后,fam通道/joe通道均无扩增曲线,ct值显示为undet或noct;(b)阳性对照品检测后,fam通道和joe通道均有扩增曲线,ct值均≤30;以上两个要求在同一次实验中同时满足,检测结果有效,否则,本次实验的检测结果无效,需要重新进行实验。结果判读标准为:当fam通道和joe通道均有扩增曲线,且ct值均≤35,可判定h7n9阳性;当fam通道和joe通道均无扩增曲线,可判定h7n9阴性;当fam通道有扩增曲线,且ct值≤35,而joe通道无扩增曲线,可判定h7基因阳性;当joe通道有扩增曲线,且ct值≤35,而fam通道无扩增曲线,可判定n9基因阳性。其中,检测结果详见图4~7。图4为阴性对照品的扩增曲线;图5为实验组1的扩增曲线;图6为实验组2的扩增曲线;图7为实验组3的扩增曲线。从图4~7可以看出,阴性对照品没有扩增曲线,实验组1的h7基因与n9基因均有扩增曲线,说明待样品1为h7n9阳性病毒。实验组2的h7基因有扩增曲线,而n9基因没有扩增曲线,说明样品2为h7阳性病毒。实验组3的n9基因有扩增曲线,而h7基因没有扩增曲线,说明样品3为n9阳性病毒。实施例2(1)实验分组共分为两组,每组三个平行,具体分组如下表2:表2实施例2的实验分组分组试剂盒实验组1试剂盒1实验组2试剂盒2其中,实验组1~2的待测样品均为武汉病毒研究所保藏中心的h7n9灭活病毒。该病毒为a/shanghai/1/2013(h7n9)毒株。(2)按照实施例1的操作对上述各组样品进行实时荧光定量pcr检测,采用试剂盒1对实验组1进行检测,采用试剂盒2对实验组2进行检测。测定结果详见图8。图8为采用试剂盒1与试剂盒2对待测样品进行检测后的扩增曲线对比图。从图8可以看出,采用试剂盒1检测的灵敏度高于试剂盒2,说明上述实施方式的h7n9病毒检测用的核酸组合物具有较高的灵敏度。实施例3(1)实验分组共分为两组,每组三个平行,具体分组如下表3:表3实施例3的实验分组分组试剂盒实验组1试剂盒1实验组2试剂盒2其中,实验组1~2的待测样品均为武汉病毒研究所保藏中心的h7n9灭活病毒。该病毒为a/shanghai/2/2013(h7n9)毒株。(2)按照实施例1的操作对上述各组样品进行实时荧光定量pcr检测,采用试剂盒1对实验组1进行检测,采用试剂盒2对实验组2进行检测。测定结果详见图9。图9为采用试剂盒1与试剂盒2对待测样品进行检测后的扩增曲线对比图。从图9可以看出,采用试剂盒1能够扩增上述待测样品,而采用试剂盒2不能扩增上述待测样品,说明上述实施方式的h7n9病毒检测用的核酸组合物能够对基因突变的h7n9病毒进行准确检测,检测的准确性较高,检测范围更大。以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。序列表<110>深圳市刚竹医疗科技有限公司<120>h7n9病毒检测用的核酸组合物和h7n9病毒实时荧光定量检测试剂盒及其应用<160>7<170>siposequencelisting1.0<210>1<211>32<212>dna<213>人工序列(artificialsequence)<400>1aaacccggtcaaactaagcagcggctacaaaa32<210>2<211>24<212>dna<213>人工序列(artificialsequence)<400>2ccgaagctaaaccaragtatcaca24<210>3<211>31<212>dna<213>人工序列(artificialsequence)<400>3aaatcaccgcccacagtgtacaatagcaaaa31<210>4<211>24<212>dna<213>人工序列(artificialsequence)<400>4actagtacttgaccamccaatgca24<210>5<211>25<212>dna<213>人工序列(artificialsequence)<400>5gaggcaatgcaaatagaatacagat25<210>6<211>24<212>dna<213>人工序列(artificialsequence)<400>6ccgaagctaaaccagagtatcaca24<210>7<211>28<212>dna<213>人工序列(artificialsequence)<400>7acccggtcaaactaagcagcggctayaa28当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1