与水稻白叶枯病抗性基因Xa23紧密连锁的分子标记R112146的制作方法
本发明属于分子生物学领域,涉及一种分子标记,特别是涉及一种与水稻白叶枯病抗性基因xa23紧密连锁的分子标记。本发明还涉及扩增该分子标记的引物、该分子标记和引物在水稻白叶枯病抗性基因xa23定位或水稻遗传育种中的用途。
背景技术:
水稻白叶枯病是世界上分布最广,危害最重的一种细菌病害,目前我国除新疆、西藏和东北的北部地区外,其余各省市和自治区均已发现。该病是由黄单胞杆菌属革兰氏阴性菌稻黄单胞杆菌(xanthomonasoryzaepv.oryzae,xoo)侵染引起的一种寄生性病害,水稻整个生长周期都会受到侵害而发病,通常会减产20%-30%,严重时可达到50%或绝收。
通过前人研究,可以发现控制白叶枯病最经济有效的方式就是培育抗病品种。传统抗病育种是根据分离群体的表现和育种者的经验进行选择,通常受环境条件、显隐性关系、基因上位等因素的影响,费时、费力、不准确。近年来生物技术的发展,尤其是分子标记技术的应用给水稻遗传育种带来了巨大变化。分子标记辅助选择为育种者提供了对目标性状进行选择的有效手段,它大大加速了育种进程,提高了育种选择效率,同时减少了盲目选择和人力、物力的大量浪费,展示出极其广阔的应用前景。
至今为止,经国际注册确认和期刊报道的抗白叶枯病基因共有40个,已被定位的抗性基因有33个。但由于水稻抗白叶枯病的遗传机制较复杂,仍然缺乏足够数量的与抗白叶枯病性相关的qtls及分子标记。随着基因组学和生物信息的发展,开发与抗白叶枯病基因尤其是具有广谱的白叶枯病抗性的xa23基因紧密连锁的分子标记,将为水稻的遗传研究及育种开辟新的思路和方法。
技术实现要素:
本发明的目的是提供一种与水稻白叶枯病抗性基因xa23紧密连锁的分子标记。
本发明的另一目的是提供一种可用于pcr扩增与水稻白叶枯病抗性基因xa23紧密连锁的分子标记的引物对,以及由该引物对扩增获得的分子标记。
本发明的再一目的是提供上述分子标记在水稻白叶枯病抗性基因xa23定位、检测以及水稻辅助育种中的用途以及上述分子标记的检测方法。
本发明的目的还包括提供一种包括上述分子标记的重组载体,以及含有该重组载体的重组细胞;提供一种包括使用上述分子标记的水稻白叶枯病抗性基因xa23的定位方法,和使用所述分子标记的水稻辅助育种方法。
为了实现上述目的,本发明采用了以下技术方案:
本发明公开了一种与水稻白叶枯病抗性基因xa23紧密连锁的分子标记,所述分子标记含有seqidno:1所示核苷酸序列;优选的,所述分子标记为seqidno:1所示核苷酸序列。
其中,需要说明的是,发明人针对xa23基因具有广谱持久抗性的特点,利用分子标记技术,开发出了上述与xa23基因连锁的标记。发明人发现,该分子标记与xa23白叶枯病抗性基因xa23紧密连锁,其将在培育水稻抗白叶枯病新品种中发挥重要的作用。利用该标记白叶枯在抗病育种时能够培育出持久广谱抗性品种。
本发明还公开了一种扩增与水稻白叶枯病抗性基因xa23紧密连锁的分子标记的引物对,所述引物对扩增的目标序列包含seqidno:1所示序列;
在本发明的一个实施方案中,所述引物对的引物1含有seqidno:2所示核苷酸序列,引物2含有seqidno:3所示核苷酸序列。
在本发明的另一实施方案中,所述引物1为seqidno:2所示核苷酸序列,所述引物2为seqidno:3所示核苷酸序列。
本发明还公开了一种与水稻白叶枯病抗性基因xa23紧密连锁的分子标记,所述分子标记是由上述引物对以抗白叶枯病的水稻基因组dna为模板经pcr扩增得到的。
优选的由上述引物对扩增得到的分子标记含有seqidno:1所示核苷酸序列。
在本发明的一个实施方案中,所述分子标记(含有seqidno:1所示核苷酸序列的dna片段)为水稻基因组中seqidno:1所示核苷酸序列的dna片段,即所包含的seqidno:1的5’端和/或3’端以外的核苷酸序列也是水稻基因组中的序列,优选的,为水稻基因组中seqidno:1的5’端和/或3’端的上下游序列。本领域技术人员可以理解,只要扩增或者检测抗白叶病的水稻基因组dna中的该分子标记,必然能够检测或扩增得到含有seqidno:1所示的序列。seqidno:1的5’端和/或3’端的上下游序列的长度为适当长度,并不特别限定,例如,满足分子标记的长度小于10,000bp、小于5,000bp、小于2,000bp、小于1,500bp、小于1,200bp、小于1,000bp、小于800bp、或者小于500bp。
在本发明的一个实施方案中,所述分子标记(含有seqidno:1所示核苷酸序列的dna片段)所包含的seqidno:1的5’端和/或3’端可操作地连接有人工序列和/或控制序列,例如启动子、增强子、终止子、酶切位点、引物序列等等。其中,术语“可操作地”在本发明中定义为一种如下构象,在该构象中,控制序列例如启动子被适当地置于seqidno:1的一个位置上,以致该控制序列指导seqidno:1编码的多肽的产生。
本发明还公开了一种载体,其含有本发明的分子标记。所述载体可以是插入有本发明的分子标记的表达重组载体或者克隆重组载体。获得上述重组载体后,本领域技术人员可以理解,根据不同的需要,将重组载体转化到合适的细胞中,得到含有该重组载体的重组细胞。因此,本发明还公开了一种含有所述重组载体的重组细胞。
本发明还公开了本发明的分子标记的制备方法,包括下述步骤:使用抗白叶枯病的水稻基因组dna作为模板,以上述引物对进行pcr扩增,得到的扩增产物即含有所述分子标记;优选地,还包括将pcr扩增产物进行纯化的步骤。
对本领域技术人员而言,可以理解,也可以dna化学合成的方法得到本发明的分子标记。
本发明还公开了本发明的分子标记的检测方法,包括步骤:根据上述分子标记的核苷酸序列设计引物,以被检测水稻基因组dna为模板进行扩增,并判断扩增产物中是否存在该分子标记。优选的,所述引物为上述分别含有seqidno:2和seqidno:3的引物对。
例如,可以以被检测水稻的基因组dna为模板,以上述引物(seqidno:2和seqidno:3)进行pcr扩增,得到扩增产物。可以将得到的扩增产物进行测序或者凝胶电泳。
本发明还公开所述分子标记或者所述分子标记引物对在水稻白叶枯病抗性基因xa23定位或检测中的用途。
本发明还公开了一种水稻白叶枯病抗性基因xa23定位的方法,所述方法包括使用本发明的分子标记或分子标记引物对的步骤。
本发明还公开了所述的分子标记或者所述分子标记引物对在水稻辅助育种中的用途。
本发明还公开了一种水稻辅助育种方法,所述方法包括检测本发明的分子标记或用本发明的分子标记引物对进行检测的步骤。
本发明的分子标记可用于今后的分子标记辅助育种中,本领域技术人员可以理解,比如通过检测是否存在本发明的分子标记来筛选水稻是否含有白叶枯病抗性基因xa23。所述检测可以是pcr检测的方法,具体地,可以使用上述的本发明的分子标记的引物对。所述检测还可以通过测序方法进行。该水稻辅助育种方法具有简便、快速、高通量的优点。
由于采用以上技术方案,使本发明具备的有益效果在于:
本发明提供了与水稻白叶枯病抗性基因xa23紧密连锁的分子标记,该分子标记将基因组dna序列与水稻白叶枯病抗性基因xa23联系起来,有利于水稻分子标记辅助育种体系的建立;所述分子标记与水稻白叶枯病抗性基因xa23紧密连锁。本发明的分子标记及分子标记扩增引物可以简便、快速、高通量地应用于水稻育种实践和资源及品种鉴定。
附图说明
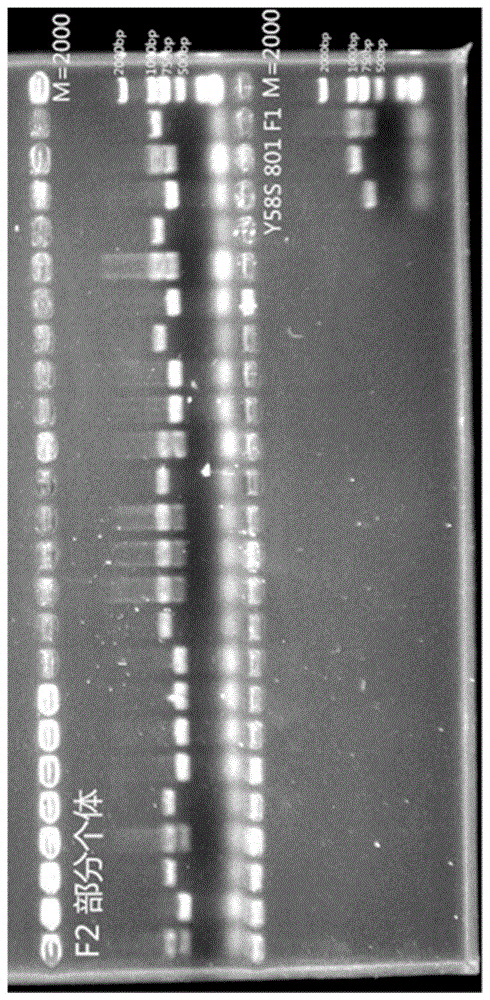
图1:父本、母本、杂交f1代以及部分f2代个体利用分子标记引物(seqidno:2和seqidno:3)扩增的电泳检测结果,其中:父本801扩增片段约为1000bp,母本y58s扩增片段约为600bp,杂交f1代同时含有这两个扩增片段。
具体实施方式
本发明公开了一种引物对以及与水稻白叶枯病抗性基因xa23紧密连锁的分子标记r112146(seqidno:1所示的核酸序列)。利用本发明的引物对,以水稻基因组dna为模板进行pcr,可以得到与水稻白叶枯病抗性基因xa23紧密连锁的分子标记,该分子标记在本发明中命名为分子标记r112146。需要指出的是,本领域技术人员可以理解,除了通过上述pcr扩增获得本发明的分子标记外,还可以通过化学合成获得本发明的分子标记。
本发明的引物对分别含有序列表seqidno:2和seqidno:3所示核苷酸序列。
本领域技术人员熟知,在上述seqidno:2和seqidno:3所示核苷酸序列中,可在其5’端或3’端分别增加1~10个碱基,所增加的碱基类型可根据水稻基因组dna上与seqidno:2和seqidno:3相匹配区域的碱基类型并依据碱基配对原则来确定,由此得到的引物对与seqidno:2和seqidno:3的扩增产物基本相同(上游和下游引物之间的dna序列相同)。因此,上述在seqidno:2和seqidno:3的5’端或3’端分别增加1~10个碱基并能扩增得到基本相同dna片段的引物对,均包括在本发明的引物对中。在本发明具体的实施方式中,本发明的引物对优选为seqidno:2和seqidno:3所示核苷酸序列。
下面通过具体实施例并结合附图对本发明作进一步详细说明。以下实施例仅仅对本发明进行进一步的说明,不应理解为对本发明的限制。实施例中未注明具体技术或条件的,按照本领域内的文献所描述的技术或条件(例如参考j.萨姆布鲁克等著,黄培堂等译的《分子克隆实验指南》,第三版,科学出版社)或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规产品,例如可以采购自illumina公司。
实施例1
1、水稻f2代分离群体的构建
父本为籼型常规稻801,为高抗白叶枯病的水稻品种。
母本为籼型不育系y58s,为具有优质、高光效、优良株叶形态和高配合力等优良性状的广适性水稻光温敏不育系,2005年通过审定,多年种植,抗性鉴定白叶枯病5级为中感白叶枯病。
父本和母本杂交得到f1,f1代自交产生f2代群体,共192个单株。将f2群体种植期间,田间偏施氮肥,使鉴定材料保持常青状态利于鉴定病情。
病菌从当地白叶枯病斑标样分离获得,经过单菌落纯化、培养、柯氏法则验证后,选择其中5个作为试验菌株。
在水稻孕穗期采用剪叶接种法开展菌株致病性测定:接种前2天在psa斜面上划线活化菌株,经28℃生长48h后,挑取单菌落接种到ps培养基中,于28℃下振荡(120r/min)培养48h,用无菌水配成浓度为3×108cfu/ml的菌悬液进行接种,用手术剪蘸取菌液剪去剑叶约2cm,按单株接种各菌系,每个菌系接种4株,每株接种5张叶片。接种过程中,每接种1个菌株要换1把处理过的剪刀。接种后20天,当病斑长度明显且稳定时对每株叶片进行测量,取平均值计算病斑长度。病情分级按照国际标准0-9级分级标准,0-3级判为抗病。记录表型调查数据。
表1:水稻品种抗白叶枯病评价分级表
表型数据显示:在192个f2后代中,其中142个个体植株白叶枯病评价分级在0-3之间,具有白叶枯病抗性性状;另外50个个体植株白叶枯病评价分级在5-9之间,不具有白叶枯病抗性。经卡方检测可知,f2白叶枯病抗性性状分离比为3:1,符合单基因控制性状的孟德尔遗传规律,可知在此群体中稻瘟病抗性是显性单基因位点控制质量性状。
表2:水稻f2群体白叶枯病抗性分离比例
2、父母本以及f1代、f2代个体基因组dna的提取
用改良的ctab法分别提取父母本、f1代以及f2代个体的基因组dna,具体方法如下:
1)取样:取幼嫩的叶片1g左右,置于2ml离心管中。
2)样品冷冻抽干:取好的样品家研磨珠,打开管盖放入真空冷冻抽干机,-50℃条件下持续冷冻抽干12小时以上(一般冷冻抽干过夜)。
3)样品研磨:将冷冻抽干的样品置于高通量机械研磨仪中,启动程序研磨,将样品粉碎。机械研磨仪程序运行需5分钟,通量为96份样品/5分钟。
4)样品研磨充分后,在管内加入65℃预热1h的ctab提取液,混匀,65℃水浴40分钟,期间每隔5分钟颠倒混匀一次。
5)将水浴后的样品从水浴锅内拿出,冷却至室温后,加入与ctab等体积的氯仿(三氯甲烷/异戊醇按照24:1比例混合),轻轻混匀10分钟,至下层液体变为深绿色。(本步骤需在通风厨内操作)
6)混匀后将离心管转入高速离心机内离心,转速12000rpm,离心15分钟。离心后样品上层为清夜。
7)抽取适量的上清液于1.5ml离心管中,并加等体积的异丙醇,轻轻混匀(此时可以看到有絮状沉淀析出),然后将样品置于-20℃的冰柜30分钟,以沉淀dna。
8)样品冷冻30分钟后转移至高速离心机内离心,转速12000rmp,离心10分钟。
9)弃掉清夜,dna沉淀用75%乙醇洗涤2次,洗涤后将乙醇倒掉,敞开管口放置于通风厨内晾干。
10)待乙醇完全挥发后,加入50微升te缓冲液(加rna酶)溶解dna,并于-20℃保存。
3、遗传图谱构建和基因定位
(1)遗传图谱构建
针对步骤2中获得的f2代个体的基因组dna,基于rad-seq的基因分型技术对f2群体的个体进行基因分型,获得f2群体的基因型数据。
用mapmaker3.0软件(constructinggeneticmapswithmapmaker/exp3.0,slincoln,mdaly,elander-cambridge,ma:whiteheadinstitute,1992)进行遗传连锁图谱绘制,得到遗传连锁图。
(2)基因定位
由于父母本在白叶枯病抗性表现上有明显的差异(父本广谱抗病,母本低抗白叶枯病),对f2个体进行性状分析,并根据性状与分子标记之间的连锁关系将源自于父本的抗白叶枯病基因定位在遗传图谱上。
具体地,根据步骤1获得的f2群体的表型数据,结合群体基因型以及遗传连锁图,通过winqtlcart2.5软件进行qtl定位。结果显示,其中一个水稻抗白叶枯病基因xa23定位在11号染色体21804679至22420133区间内,长度约615bp。根据目前xa23基因克隆后的定位信息,可以确定本次f2群体中所定位区间包含xa23基因位点。。
4、分子标记的开发
根据rad-seq的测序结果,利用华大自主开发的soap软件比对测序reads,然后用soapsv寻找片段差异较大的分子标记,便于用凝胶电泳区分鉴别。选择靠近抗白叶枯病基因xa23所在区段的标记r112146作为候选。所述分子标记表现为seqidno:1所示核苷酸序列的插入/缺失长度多态性。根据本发明的实施例,seqidno:1所示核苷酸序列如下(269bp):
ggccattcccaaccaaaaacactagacatggttttcacaaactccacatcatcaagaaactagtactagacactcctcttccaatgcaaacactactattccatacttaaatttaatgcttcttatctcacatgatgtcttggatattgtgtagaaaccatgtctccttctctttcctcatttattcacttgccacataatttttcatcctatgtgacatcttatttaatgttatggacaccatcctagtcattggattgggaatggtc(seqidno:1)。
5、候选分子标记验证
对步骤4中确定的水稻抗白叶枯病候选分子标记r112146(seqidno:1所示的核酸序列)进行验证,具体如下:
针对上述候选分子标记设计引物,引物序列如下所示:
正向引物:5’-ggtttgctccacattgatgt-3’(seqidno:2)
反向引物:5’-atgccttcagatctctgcat-3’(seqidno:3)
利用上述引物,通过pcr扩增和琼脂糖凝胶电泳检测来验证该候选分子标记的多态性和扩增稳定性。
具体地,以步骤3中提取的父母本、f1代、f2代的基因组dna为模板,利用上述扩增引物进行pcr扩增,其中,
pcr反应体系如下:
pcr反应程序如下:
94℃预变性5分钟;94℃变性30秒,60℃退火30秒,72℃延伸40秒,运行35个循环;最后72℃延伸3分钟。pcr扩增产物经纯化后于4℃下保存。
经上述扩增过程得到分子标记,取部分pcr扩增产物,用1%琼脂糖凝胶电泳检测,得到多态性电泳条带,结果见图1。
图1为父本、母本、杂交f1代以及部分f2代个体利用分子标记引物(seqidno:2和seqidno:3)扩增的电泳检测结果。如图1所示,父本扩增片段约为1000bp,母本扩增片段约为600bp,杂交f1代同时含有这两个扩增片段,并且,针对f2代,凡是扩增条带为1000bp或者同时含有两个扩增片段的个体,其植株具有白叶枯病抗性;凡扩增条带为600bp的个体,其植株不具有白叶枯病抗性。由此证明该分子标记r112146(seqidno:1所示的核苷酸序列)在父母本之间具有多态性,并与抗白叶枯病性状紧密连锁。
然后,利用3730测序仪对各扩增产物进行测序,结果,父本及f2代中抗白叶枯病的单株扩增条带,与母本及f2代中不抗白叶枯病的单株扩增条带相比增加了一些序列,即为候选分子标记r112146。由此,证明该候选分子标记r112146在父母本之间具有多态性,该候选分子标记与水稻抗白叶枯病性状紧密相关,且具有与白叶枯病抗性基因xa23连锁遗传的稳定性。
因为候选分子标记具有多态性、与白叶枯病抗性基因xa23连锁遗传的稳定性,所以该候选分子标记可作为白叶枯病抗性基因xa23的分子标记使用。多态性指的是:分子标记在抗白叶枯病和不抗白叶枯病水稻基因组中的序列不同,可以区分。
尽管本发明的具体实施方式已经得到详细的描述,本领域技术人员将会理解。根据已经公开的所有教导,可以对那些细节进行各种修改和替换,这些改变均在本发明的保护范围之内。本发明的全部范围由所附权利要求及其任何等。
序列表
<110>深圳市华大农业应用研究院
深圳华大生命科学研究院
中国农业科学院深圳生物育种创新研究院
<120>与水稻白叶枯病抗性基因xa23紧密连锁的分子标记r112146
<130>p2018-1-0113.cn
<160>3
<170>siposequencelisting1.0
<210>1
<211>269
<212>dna
<213>水稻(oryzasativa)
<400>1
ggccattcccaaccaaaaacactagacatggttttcacaaactccacatcatcaagaaac60
tagtactagacactcctcttccaatgcaaacactactattccatacttaaatttaatgct120
tcttatctcacatgatgtcttggatattgtgtagaaaccatgtctccttctctttcctca180
tttattcacttgccacataatttttcatcctatgtgacatcttatttaatgttatggaca240
ccatcctagtcattggattgggaatggtc269
<210>2
<211>20
<212>dna
<213>人工合成(artificial)
<400>2
ggtttgctccacattgatgt20
<210>3
<211>20
<212>dna
<213>人工合成(artificial)
<400>3
atgccttcagatctctgcat20
- 还没有人留言评论。精彩留言会获得点赞!