模拟脑脊液生物力学环境构建组织工程骨组织的装置的制作方法
本实用新型属于生物医学技术领域,具体涉及一种模拟脑脊液生物力学环境构建组织工程骨组织的装置。
背景技术:
全椎板、半椎板切除减压术能够切实有效地扩大椎管容量、解除神经压迫,作为临床常规术式已广泛应用于治疗因脊柱病变、外伤等原因导致的椎管狭窄、脊髓和神经根受压等疾病。对于严重的椎管狭窄症、创伤及椎管内肿瘤等,椎板切除术仍为首选治疗。然而椎板切除术后椎板缺损导致的脊柱不稳和硬膜粘连等并发症严重影响其术后效果,加速脊柱退行性变,增加再次手术难度,而修复椎板缺损可有效预防以上并发症,因此重建椎板极为重要。
目前国内外已在椎板重建对于恢复脊柱稳定性和预防硬膜粘连的重要性方面达成共识,并在该方面做了多种尝试,如采用自体骨移植、异体骨移植、单纯人工骨替代、钛板替代等重建椎板。尽管研究报道以上方法均可有效恢复脊柱稳定性、预防硬膜粘连,但仍难以回避以上椎板重建方法存在的诸多不足,如自体骨移植取材有限,且存在取骨区疼痛,增加患者痛苦等;大量同种异体骨移植易产生免疫排斥反应并造成某些疾病的传播;单纯人工骨降解缓慢且难以固定,易造成新的压迫;钛板替代造成二次手术困难等。而我们前期研究已证实采用骨髓间充质干细胞复合β-磷酸三钙或胶原蛋白海绵支架构建组织工程骨,能够在兔椎板缺损模型上成功重建椎板,并且新生椎板可有效修复脊柱后柱结构,隔离硬膜外瘢痕组织。由此可见,利用组织工程技术生理性重建椎板具有独特优势。
尽管组织工程重建椎板的优势已充分证实,但该技术在临床应用中仍存在诸多犹疑,其中最为突出的是组织工程重建椎板是否会对脊髓造成新的压迫。然而分析前期实验结果,发现一个重要的现象:利用组织工程骨重建的新生椎板不会压迫脊髓,但其发生机制尚不清楚。前期试验结果还发现新生椎板骨小梁的方向与脑脊液搏动的力学方向一致。根据Wolf定律:骨小梁总是沿反复承受应力的方向排列,推测脑脊液搏动产生的持续性力学刺激在新生椎板发生上述变化的过程中起着极为重要的作用,如能阐明该作用机制将为组织工程重建椎板技术的临床应用奠定极为重要的理论基础。但是目前有关脑脊液搏动如何调控新生椎板的成骨与塑形,国内外尚未见相关报道。
脑脊液搏动是动物基本生命活动(心跳以及呼吸)的产物,可以分为动脉搏动引起的脉搏波和呼吸引起的呼吸波。当前关于腰椎段脑脊液搏动来源有两种理论:一种是腰椎段脑脊液搏动来源于脊髓内血管的搏动,另一种是脑内血管搏动所引起的颅内脑脊液搏动经过蛛网膜下腔传递下来。当前的主流观点认为腰椎段脑脊液搏动主要来源于脊髓内血管的搏动。
力学刺激在组织再生和重塑过程中具有重要的调控作用,如周期性张力可以促进肌腱组织的再生和修复;动态压力、静态水压、剪切应力可促进干细胞向软骨细胞分化,进而促进软骨组织的再生;剪切应力对血管内皮细胞的形态结构、生长和功能具有重要影响;静态水压和剪切应力对成骨细胞的增殖分化均具有重要的调控作用。机械性力学信号是调节成骨与塑形不可或缺的影响因素,这些信号在细胞和分子层面通过力传导和力回馈机制感应骨骼承受的机能负荷,以此来刺激骨骼不断的重塑和维持,以应对外界环境的刺激。因此,脑脊液搏动力同样也可促进脊椎骨椎板的成骨与塑形。因此,体外构建脑脊液搏动力学模型,有利于进一步探究脑脊液搏动性张力刺激在椎板成骨与塑形过程中的调控作用及力学传导机制。
目前应用于骨组织再生领域的组织工程技术包括自体骨祖细胞与三维多孔支架材料的结合使用。骨组织工程技术包括四个部分:成骨诱导、成骨细胞、成骨生长因子、特定的力学环境。成骨细胞已被广泛应用于在体外构建矿化的细胞支架结构。但由于成骨细胞更趋于成熟,其相对于骨祖细胞的分化增殖能力有所减弱。相较而言,骨髓间充质干细胞有着更强的增殖分化能力。其可取材于骨髓穿刺液,也可取自脂肪组织或者脐带血。骨髓间充质干细胞具有向不同细胞系分化的潜能,其可分化为成骨细胞、软骨细胞、脂肪细胞和肌细胞。其缺点在于体外不易获取且经体外传代后增殖分化能力会相应减弱。骨祖细胞的三维立体培养具有一定的挑战性,例如:多孔支架内部细胞的营养供给,氧气输送,代谢废物排出等。理想的细胞支架应该拥有类似于人体正常骨骼的机械性能,并且易于以理想的形状生产。适用于制造矿化的细胞支架结构的支架材料应具备以下优势:支持细胞附着;支持细胞沿孔隙网络向支架内部生长;可生物降解以促进本体骨的生成与塑形。支架材料构成了骨组织工程的基本框架,目前用于修复骨缺损的支架材料种类很多,大体分为两种:天然生物衍生材料、人工合成材料。天然生物衍生材料是一种经过物理和化学方法处理得到的天然生物组织,一种为类骨、异种骨和同种异体骨等,是将其他个体的骨组织无机部分作为支架材料采用直接或完全代替的方法修复骨缺损;另一种是根据间接或部分替代的原理,寻找类似细胞外基质的物质。目前研究较多的支架材料有:胶原、明胶、氨基多糖、纤维蛋白等,这类材料具有良好的生物相容性,有利于骨髓间充质干细胞的的粘附、分化、增殖,但其具有较高的降解率,且降解速度快。在合成材料中,骨组织工程常用的支架材料主要有:(1)无机材料-生物陶瓷类,如:羟基磷灰石(HA)、磷酸三钙生物陶瓷、生物活性玻璃陶瓷、双相钙磷陶瓷等;(2)高分子有机合成材料,如聚羟基乙酸(PGA)、聚乳酸(PLA)及两者的共聚物(PLGA)等;(3)复合材料,如HA/PLGA的复合,HA/胶原的复合,生物陶瓷/骨形态发生蛋白(BMP)的复合等。人工合成材料的优势在于可通过调整材料的分子量、组成比例及组分进行调配,根据不同的组织工程需求对细胞支架的性能加以调配。根据大量体内实验表明,适宜成骨细胞生长的理想的支架空隙直径为200-400μm。除此之外,细胞支架相互连通的孔隙网络还要适宜成骨血管化。细胞支架内部的孔隙结构可以影响流体剪切力的分布,机械刺激范围以及骨祖细胞的增殖分化。细胞支架中的骨祖细胞不仅受生物物理性刺激,而且受体内特殊的细胞生长因子的调控。许多在体外调控成骨细胞成骨分化的调控因子是可获得的。其中骨成形蛋白(BMPs)与骨成形密切相关,它们同属于广泛存在于生物体内的转化生长因子家族(TGF-β)。目前,只有BMP-2和BMP-7被允许应用于临床。重组人BMP-2被应用于椎间融合术、新鲜胫骨骨折、上颌骨骨折的骨移植手术。重组人BMP-7被应用于长骨骨折、骨折不愈合、椎间融合的治疗。
鉴于生物反应器可以提供对于组织工程结构的物理性刺激,是构建组织工程骨不可或缺的技术组成部分,其将成为骨组织工程技术的核心。大量研究人员已研发出各种各样的动态3D生物反应器来模仿骨组织的原始微环境,包括转瓶、旋转壁式容器、流体灌流生物反应器等,这些生物反应器能够予以骨细胞支架复合体不同形式的机械性力学刺激。但目前尚没有一款生物反应器可模拟脑脊液搏动性张力刺激,还原椎板成骨塑形的力学微环境。
基于上述内容,为有效预防椎板切除术后椎板缺损导致的脊柱不稳和硬膜粘连等严重并发症的发生,研究脑脊液搏动性张力刺激对新生椎板成骨与塑形的调控作用及力学传导机制,进而利用组织工程技术生理性重建椎板极为关键。因此,我们迫切需要一种能够动态培养骨祖细胞且能模拟脑脊液搏动性张力刺激,还原椎板成骨与塑形的力学微环境的生物反应器弥补该领域生物反应器研究的空白。
技术实现要素:
本实用新型要解决的技术问题是提供一种模拟脑脊液生物力学环境构建组织工程骨组织的装置,用于模拟脑脊液搏动力学环境,在体外构建一个参数可以设定动态培养环境,并实施记录实验数据,便于探究脑脊液搏动如何调控新生椎板的成骨与塑形作用及其力学传导机制,弥补该领域生物反应器研究的空白。
为解决上述技术问题,本实用新型采用如下的技术方案:
一种模拟脑脊液生物力学环境构建组织工程骨组织的装置,包括主控制箱、细胞培养箱、培养室以及连接主控制箱和培养室的硅胶连接管和连接头,所述培养室置于细胞培养箱内,所述主控制箱位于细胞培养箱上方,主控制箱通过设置所搭载的硅胶连接管内液体的力学参数控制培养室力学环境。
优选地,所述主控制箱包括主控制器模块、蠕动泵驱动控制模块、电磁阀驱动控制模块、液压采集模块、触摸式显示屏、电源模块,所述主控制器模块包括STM32F103RCT6系列单片机,第一去耦电容,第二去耦电容,第三去耦电容,第四去耦电容,复位按钮,第一旁路电容,第一上拉电阻,STC脱机下载模块,第二上拉电阻,第三上拉电阻,第四上拉电阻,第五上拉电阻,第一下拉电阻,第二旁路电容,第一跨接电阻器,第二跨接电阻器,第三跨接电阻器,第四跨接电阻器,第六上拉电阻,第一发光二极管,STM32F103RCT6单片机上第19引脚接VCC 3.3后接第一去耦电容,第一去耦电容另一脚接第18引脚后回接GND;第32引脚接VCC 3.3后接第二去耦电容,第二去耦电容另一脚接第31引脚后回接GND;第48引脚接VCC 3.3后接第三去耦电容,第三去耦电容另一脚接第47引脚后回接GND;第64引脚接VCC 3.3后接第四去耦电容,第四去耦电容另一脚接第63引脚后回接GND,复位键S1并联第一旁路电容,一端接GND,再与第一上拉电阻R45串联并接至VCC 3.3,BOOT0引脚连接至VCC 3.3并接入第二跨接电阻器和第一跨接电阻器,第一跨接电阻器另一端接GND,BOOT1引脚接VCC 3.3后连第四跨接电阻器和第三跨接电阻器,第三跨接电阻器另一端接GND,第一发光二极管阳极端先连第六上拉电阻R36后连VCC 3.3,LED1阴极接GND,JTAG下载接口电路由STC脱机下载模块完成,STC脱机下载模块第1引脚连接VCC 3.3,第3引脚连第二上拉电阻,第5引脚连第三上拉电阻,第7引脚连第四上拉电阻,且第二上拉电阻、第三上拉电阻、第四上拉电阻、第一下拉电阻并联后接VCC 3.3,另一端连第五上拉电阻后回接第13引脚,第9引脚连第一下拉电阻后接GND,STC脱机下载模块第2引脚接VCC后连第二旁路电容,第二旁路电容另一端连第4引脚,第8、10、12、14、16、18、20引脚接GND,第11、17、19引脚悬空。
优选地,所述蠕动泵驱动模块包括三个蠕动泵以及相应驱动电路,其中,第一蠕动泵,第二蠕动泵,第三蠕动泵排布于主控制箱前面板右侧,第一蠕动泵,第二蠕动泵为培养液灌流蠕动泵,第三蠕动泵为搏动压控制蠕动泵,在蠕动泵头部分别搭载硅胶连接管,用于培养液灌流及脑脊液搏动模拟。
优选地,所述蠕动泵驱动电路包括DRV8825芯片,第四旁路电容,第五旁路电容,第六旁路电容,第七旁路电容,第八旁路电容,第九旁路电容,第十旁路电容,第七上拉电阻,第八上拉电阻,第九上拉电阻,第十上拉电阻,第一采样电阻,第二采样电阻,第二下拉电阻,第三下拉电阻,第一滑动变阻器,第二发光二极管,第三发光二极管,DRV8825芯片第1引脚连接第五旁路后连第2引脚,第六旁路电容和第九上拉电阻并联后一端连第3引脚,一端连第11引脚,第4引脚连第十旁路电容并接VCC,第十旁路电容另一端接GND,第11引脚接第九旁路电容,第九旁路电容另一端接地,第14、28、29引脚都接GND,第5引脚和第7引脚分别连接步进电机A+、A-,为电机的A线圈供电,第8引脚和第10引脚连接步进电机的B+、B-,为电机的B线圈供电,第6引脚接第二采样电阻后接GND,第9引脚接第二下拉电阻后接GND,第23引脚悬空不接,第15引脚接VCC,第四旁路电容一端接VCC,一端接GND,第一滑动变阻器和第八旁路电容并联后一端接GND,另一端接第八上拉电阻后接第12引脚和第13引脚,第七上拉电阻一端接VCC,一端接第16引脚的同时并联第七旁路电容后接地,第17引脚接第十上拉电阻后接VCC 5,第19引脚接步进电机DECAY,第20、21、22引脚为控制步进电机工作的方向、使能以及转速脚,第24、25、26引脚分别接拨码开关的3、4、5引脚,第27引脚接第二下拉电阻和第二发光二极管阴极,第18引脚接第三下拉电阻后接第三发光二极管阴极,第二发光二极管和第三发光二极管阳极全都接VCC5。
优选地,所述电磁阀驱动模块包括电磁阀和电磁阀驱动电路,所述电磁阀驱动模块采用场效应管搭配光耦隔离芯片PC817来驱动电磁阀和保证电磁阀正常工作,PC817芯片的第1引脚连接STM32F103RCT6单片机的输入脚,第2引脚连接第一限流电阻后接地,第4引脚连接第十一上拉电阻后接VCC 12,第4引脚在串联第二限流电阻R3后,连MOS管的栅极的同时并联第四下拉电阻,第四下拉电阻另一端接地,第3引脚接GND,MOS管源极接第一反向二极管至VCC 24,漏极直接接地,所述电磁阀与第一反向二极管并联。
优选地,所述触摸式显示屏采用电阻式触摸屏,串口电路采用MAX232ACPE芯片完成,所述芯片的第1引脚和第3引脚之间接第十一旁路电容,第4引脚和第5引脚之间接第十二旁路电容,第2引脚和第6引脚分别接第十三旁路电容、第十四旁路电容至GND,第16引脚接VCC 5,并接第十五旁路电容到地,第11引脚接STM32F103RCT6单片机的PA9脚,第12引脚接单片机的PA10脚,第14引脚接串口插座的第2引脚,第13引脚接串口插座的第3引脚,串口插座第5引脚接地。
优选地,所述液压采集模块包括扩散硅压力变送器传感器,即为液压传感器和液压采集驱动电路,所述液压传感器内嵌于支架内部,可灵敏检测管道的力学变化,所述液压驱动电路J4端子为液压采集传感器信号输入端,第1引脚连接VCC 24,第2引脚接STM32F103RCT6单片机ADC输入脚PA1,同时,第2引脚连接第三采样电阻后接地。
优选地,所述电源模块由降压电路和交流转直流电路组成,进一步地,降压电路主要由LM2596芯片和ASM1117芯片构成,所述LM2596芯片上第1引脚接VCC 24,第十六旁路电容和第十七旁路电容并联后一端接VCC 24,一端接GND,LM2596芯片的第2引脚接第二反向二极管后接GND,并接一个电感及第十八旁路电容至GND,二极管、电感和电容构成输出端的充放电回路,芯片的第4引脚为信号反馈脚,其接第三限流电阻到地,并连接一个滑动变阻器至VCC 5,VCC 5输出接第一滤波电容到地,第3、5引脚直接接GND;芯片ASM1117的第1引脚接VCC 5,第2引脚接GND,第3引脚为电源输出脚,第二滤波电容、第三滤波电容并联后接至第1引脚和第2引脚之间,为输入电压进行滤波处理;第四滤波电容,第十九旁路电容并联后接至第3引脚和第2引脚之间,为输出电压进行滤波处理。J2端子接220V交流电,第22脚接保险丝再接变压器后回接第1引脚,由此可形成变压器的输入回路;变压器的输出回路首先接一个桥式整流电路,整流桥后接并联的第二十旁路电容和第二十一旁路电容,最终接输出端子J1;其中T1输出电源的为24V的交流电,桥式整流电路输出的电源为整流以后的直流电源。
优选地,所述细胞培养箱设有四个网状隔板,含有温度控制单元并能够完全密封;进一步地,细胞培养箱后侧面板开有孔,并在开孔处设有橡胶塞,允许选择通入培养液的数量或者气体交换通道是否打开,在保证细胞培养室能够处于完全密封状态的同时,允许模拟脑脊液搏动以及培养液循环的硅胶连接管能够伸入细胞培养箱并连接培养室。
优选地,进一步地,所述培养室为长方体结构,上/下面板为透明材质面板,侧面为一整体部件,由无毒性非透明材质制成,所述侧面板中的前后面板各有三个开孔,并安装有三个一号连接头;所述一号连接头上可连接一带有空气过滤网和密封夹的硅胶连接管,为气体交换通道;或者连接一带有密封夹的长硅胶连接管,为培养液循环通道;进一步地,所述一号连接头与开孔的连接处设有硅胶圈以保证密封良好,左/右面板各有两个开孔,内部均连接有二号连接头;开孔外部一处直接连接密封塞,该开孔内部连接头上连有硅胶连接管,为空白对照管;另一开孔外侧有二号连接头,为脑脊液模拟液循环入口或出口,内侧二号连接头连有硅胶连接管,为脑脊液搏动模拟管。
采用本实用新型具有如下的有益效果:本实用新型与现有技术相比,具有的有益效果是:在骨细胞培养的过程中添加了骨细胞生长所必须的力学环境,并且,该力学环境的参数是精确可控的。本实用新型可以调节脑脊液搏动的频率和脑脊液循环时候的流速,可以至多并行独立控制6个电磁阀。在触摸式显示屏上可以切换观察到不同培养室的脑脊液模拟液压强情况。本实用新型将脑脊液对骨细胞生长情况的影响因素有了较为全面的考虑且做到了量化控制或显示。
附图说明
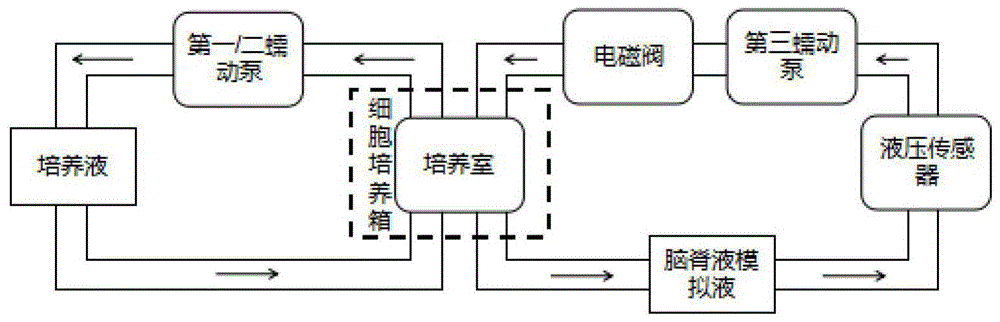
图1为本实用新型一种脑脊液生物反应器的系统结构示意图;
图2为本实用新型一种脑脊液生物反应器的实体结构示意图;
图3为本实用新型一种脑脊液生物反应器培养室并行排布;
图4为本实用新型一种脑脊液生物反应器培养室结构示意图;
图5为本实用新型主控制机箱系统整体方案设计框图;
图6为本实用新型主控制箱主控及外围电路原理图;
图7为本实用新型主控制箱JTAG下载接口电路原理图;
图8为本实用新型主控制箱电源指示灯及BOOT模式选择电路原理图;
图9为本实用新型主控制箱DRV8825驱动电路图;
图10为本实用新型主控制箱电磁阀驱动电路图;
图11为本实用新型主控制箱U5模块232串口电路图;
图12为本实用新型主控制箱液压采集模块电路图;
图13为本实用新型主控制箱LM2596电路原理图;
图14为本实用新型主控制箱ASM1117电路原理图;
图15为本实用新型主控制箱交流转直流电路原理图。
图中附图标记说明如下:
1、主控制箱;2、第一蠕动泵;3、第二蠕动泵;4、第三蠕动泵;5、触摸式显示屏;6、信号采集单元接口;7、支架;8、复位按钮;9、细胞培养箱;10、网状隔板;11、培养室;12、培养室上/下面板;13、固定螺丝;14、一号连接头;15、二号连接头;16、硅胶连接管;17、左/右面板;18、前/后面板;19、电磁阀;20、密封帽盖;21、培养液储存瓶;22、脑脊液循环瓶;23、液压传感器;24、空气过滤网;25、密封夹;26、导气管;27、脑脊液搏动管;28对照管;29贴壁生长细胞;30、密封螺帽;31、一号密封圈。
具体实施方式
下面将结合本实用新型实施例中的附图,对本实用新型实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本实用新型一部分实施例,而不是全部的实施例。基于本实用新型中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本实用新型保护的范围。
如图1所示,本实用新型一种脑脊液生物反应器装置用于体外并行动态培养骨细胞,处理后得到的细胞用于骨手术治疗、脊椎置换手术等。该脑脊液生物反应器装置包括:主控制箱1,细胞培养箱9,培养室11。
其中主控制箱1包括主控制器模块、蠕动泵驱动控制模块、电磁阀驱动控制模块、液压采集模块、触摸式显示屏模块、电源模块。主控制器模块包括STM32F103RCT6系列单片机,去耦电容第一去耦电容C19、第二去耦电容C24、第三去耦电容C18、第四去耦电容C7;复位按钮S1,第一旁路电容C31,第一上拉电阻R45;STC脱机下载模块U8,第二上拉电阻R40,第三上拉电阻R41,第四上拉电阻R42,第五上拉电阻R43,第一下拉电阻R44,第二旁路电容C30;第一跨接电阻器R32,第二跨接电阻器R33,第三跨接电阻器R34,第四跨接电阻器R35,第六上拉电阻R36,第一发光二极管LED1。
STM32F103RCT6单片机上第19引脚接VCC 3.3后接第一去耦电容C19,C19另一脚接第18引脚后回接GND;第32引脚接VCC 3.3后接第二去耦电容C24,C24另一脚接第31引脚后回接GND;第48引脚接VCC 3.3后接第三去耦电容C18,C18另一脚接第47引脚后回接GND;第64引脚接VCC 3.3后接第四去耦电容C7,C7另一脚接第63引脚后回接GND。复位键S1并联第一旁路电容C31,一端接GND,再与第一上拉电阻R45串联并接至VCC 3.3。BOOT0引脚连接至VCC 3.3并接入第二跨接电阻器R33和第一跨接电阻器R32,R32另一端接GND。BOOT1引脚接VCC 3.3后连第四跨接电阻器R35和第三跨接电阻器R34,R34另一端接GND。第一发光二极管LED1阳极端先连第六上拉电阻R36后连VCC 3.3,LED1阴极接GND。JTAG下载接口电路由STC脱机下载模块U8完成,U8第1引脚连接VCC 3.3,第3引脚连第二上拉电阻R40,第5引脚连第三上拉电阻R41,第7引脚连第四上拉电阻R42,且R40、R41、R42、R44并联后接VCC 3.3,另一端连第五上拉电阻R43后回接第13引脚。第9引脚连第一下拉电阻R44后接GND。U8第2引脚接VCC后连第二旁路电容C30,C30另一端连第4引脚。第8、10、12、14、16、18、20引脚接GND。第11、17、19引脚悬空。
蠕动泵驱动模块包括三个润泽流体公司YZ1515X系列步进整机蠕动泵以及相应驱动电路。其中,第一蠕动泵2,第二蠕动泵3,第三蠕动泵4排布于主控制箱前面板右侧,第一蠕动泵2,第二蠕动泵3为培养液灌流蠕动泵,第三蠕动泵为搏动压控制蠕动泵,在蠕动泵头部分别搭载硅胶连接管,用于培养液灌流及脑脊液搏动模拟。蠕动泵驱动电路包括DRV8825芯片,第四旁路电容CC1,第五旁路电容CC2,第六旁路电容CC3,第七旁路电容CC4,第八旁路电容CC5,第九旁路电容CC6,第十旁路电容CC7,第七上拉电阻CR1,第八上拉电阻CR2,第九上拉电阻CR3,第十上拉电阻CR4,第一采样电阻CR5,第二采样电阻CR6,第二下拉电阻CR7,第三下拉电阻CR8,第一滑动变阻器,第二发光二极管DS1,第三发光二极管DS2。
DRV8825第1引脚连接第五旁路CC2后连第2引脚。第六旁路电容CC3和第九上拉电阻CR3并联后一段连第3引脚,一端连第11引脚。第4引脚连第十旁路电容CC7并接VCC,CC7另一端接GND。第11引脚接第九旁路电容CC6,CC6另一端接地。第14、28、29引脚都接GND。第5引脚和第7引脚分别连接步进电机A+、A-,为电机的A线圈供电。第8引脚和第10引脚连接步进电机的B+、B-,为电机的B线圈供电。第6引脚接第二采样电阻CR6后接GND,第9引脚接第二下拉电阻后接GND,第23引脚悬空不接。第15引脚接VCC,第四旁路电容CC1一端接VCC,一端接GND。第一滑动变阻器和第八旁路电容CC5并联后一端接GND,另一端接第八上拉电阻CR2后接第12引脚和第13引脚。第七上拉电阻CR1一端接VCC,一端接第16引脚的同时并联第七旁路电容CC4后接地。第17引脚接第十上拉电阻CR4后接VCC 5。第19引脚接步进电机DECAY。第20、21、22引脚为控制步进电机工作的方向、使能以及转速脚。第24、25、26引脚分别接拨码开关的3、4、5引脚。第27引脚接第二下拉电阻CR7和第二发光二极管DS1阴极。第18引脚接第三下拉电阻CR8后接第三发光二极管DS2阴极,DS1和DS2阳极全都接VCC 5。
电磁阀驱动模块由SMC公司VDW31-5G-3-02型号电磁阀19和电磁阀驱动电路构成。电磁阀驱动模块采用IRF3205PBF场效应管搭配光耦隔离芯片PC817来驱动电磁阀和保证电磁阀正常工作。PC817芯片的第1引脚连接STM32F103RCT6单片机的输入脚,第2引脚连接第一限流电阻R1后接地。第4引脚连接第十一上拉电阻R2后接VCC 12,第4引脚在串联第二限流电阻R3后,连MOS管的栅极的同时并联第四下拉电阻R4,R4另一端接地。第3引脚接GND。MOS管源极接第一反向二极管D1至VCC 24,漏极直接接地。电磁阀与D1并联。
触摸式显示屏采用昆仑通态的TP第四去耦电容C7062电阻式触摸屏,串口电路采用MAX232ACPE芯片完成。芯片的第1引脚和第3引脚之间接第十一旁路电容C25,第4引脚和第5引脚之间接第十二旁路电容C29,第2引脚和第6引脚分别接第十三旁路电容C27、第十四旁路电容C28至GND。第16引脚接VCC 5,并接第十五旁路电容C26到地。第11引脚接STM32F103RCT6单片机的PA9(U1_TX)脚,第12引脚接单片机的PA10(U1_RX)脚,第14引脚接串口插座的第2引脚,第13引脚接串口插座的第3引脚,串口插座第5引脚接地。
液压采集模块包括美控公司开发的扩散硅压力变动器传感器,即为液压传感器23和液压采集驱动电路。液压传感器内嵌于支架7内部,可灵敏检测管道的力学变化。液压驱动电路,J4端子为液压采集传感器信号输入端,第1引脚连接VCC 24,第2引脚接STM32F103RCT6单片机ADC输入脚PA1,同时,第2引脚连接第三采样电阻R39后接地。
电源模块由降压电路和交流转直流电路组成。进一步地,降压电路主要由LM2596芯片和ASM1117芯片构成。LM2596芯片上第1引脚接VCC 24,第十六旁路电容C12和第十七旁路电容C14并联后一端接VCC 24,一端接GND。芯片的第2引脚接第二反向二极管D3后接GND,并接一个电感及第十八旁路电容C13至GND。二极管、电感和电容构成输出端的充放电回路。芯片的第4引脚为信号反馈脚,其接第三限流电阻R40到地,并连接一个滑动变阻器至VCC 5,VCC 5输出接第一滤波电容C10到地,第3、5引脚直接接GND。芯片ASM1117的第1引脚接VCC 5,第2引脚接GND,第3引脚为电源输出脚。第二滤波电容C16、第三滤波电容C17并联后接至第1引脚和第2引脚之间,为输入电压进行滤波处理。第四滤波电容C8,第十九旁路电容C15并联后接至第3引脚和第2引脚之间,为输出电压进行滤波处理。J2端子接220V交流电,第22脚接保险丝F1再接变压器T1后回接第1引脚,由此可形成变压器的输入回路。变压器的输出回路首先接一个桥式整流电路D1Bridge,整流桥后接并联的第二十旁路电容C2和第二十一旁路电容C3,最终接输出端子J1。其中T1输出电源的为24V的交流电,D1Bridge输出的电源为整流以后的直流电源。
本实用新型能够允许6个培养室11但不仅限于6个培养室同时并行培养实验,培养室排列方式如图3所示,其与单个实验情况相似,故不再赘述。培养室11为一长方体结构,培养室上/下面板12为无毒高分子透明材料,可直接观察到细胞的生长情况。侧面板也是由生物无毒性材料制成,通过在培养室上/下面板12各设10个开孔,再由不锈钢固定螺丝13将上/下面板与侧片版固定为一整体。进一步地,培养室上/下面板12和侧面板的连接处有一号密封圈31保证培养室11的密封性良好。固定螺丝13和培养室上/下面板12的连接处有二号密封圈27保证培养室11的密封性良好。培养室前/后面板18各有3个开孔,开孔处可装有一号连接头14,可连接一带有密封夹25和空气过滤网24的导气管26便于培养室11进行气体交换;或者连接硅胶连接管16进行培养液更换。若不需要用到该开孔,有密封帽盖20可保证一号连接头14被密封。进一步地,一号连接头14和前/后面板18有二号密封圈27保证培养室11的密封性良好。侧面板的左/右面板17各开2孔,孔的内部都装有二号连接头15,安装有两根硅胶连接管分别为脑脊液搏动管27和静态对照管28。进一步地,脑脊液搏动管27为培养室11提供脑脊液搏动力学环境,其两端在外侧安装都有二号连接头15与控制装置相连。进一步地,所培养的细胞与生物材料复合物固定在固定支架29内部,保证培养的样品能受到均匀和稳定的力学刺激。静态对照管28两端外侧不可连通,采用密封螺帽30密封,脑脊液搏动管27和静态对照管28上可同时放置多个固定支架29,用于培养多个样品。
具体地,本实用新型脑脊液生物反应器的结构和功能可划分为两个互不干扰的全封闭循环部分,即为一个脑脊液力学参数模拟循环通路和一个培养液更换通路。一个脑脊液力学参数模拟循环通路,该通路是由第三蠕动泵4搭载硅胶连接管16,接入支架7中液压传感器23,再通过电磁阀19联合模拟控制脑脊液搏动作用力的产生。其中该作用力的频率、压强可通过触摸式显示屏进行相关参数设置。然后,再由硅胶连接管16接入脑脊液循环瓶22,脑脊液循环瓶22盖子上有3个开孔,孔1为液体流出口,孔2为液体流入口,孔3为气体排出口,并且在孔3位置设有空气过滤网24,打开与否保证循环环境无菌无污染。最后,硅胶连接管16穿过细胞培养箱9后面板开孔接入培养室左面板17外侧二号连接头15,右面板17外侧二号连接头15连接一硅胶连接管16再次穿过细胞培养箱9后面板开孔连接至脑脊液循环瓶22孔2处,完成整个脑脊液力学参数模拟循环通路。
培养液更换通路,包括培养液储存瓶21顶部开口1处连接一根硅胶连接管16,由第一蠕动泵2或第二蠕动泵3搭载该硅胶连接管16,穿过细胞培养箱9后后部的开孔,连接至培养室11前面板18上的一号连接头14,再将后面板18上的一号连接头14连接硅胶连接管16,穿过细胞培养箱9后面板开孔,最后连接至培养液储存瓶21顶部开口2,完成整个培养液更换通路。
该脑脊液搏动生物反应器能模拟脑脊液的生物力学环境,能在体外设置不同的参数环境构建组织工程骨组织,能形成封闭无菌的环境培养细胞和生物材料的复合物,在培养过程中,各种参数能实时显示并能以表格的形式存储在电脑中便于后续的分析,构建的组织工程骨组织具有良好的生物力学性能、生物相容性和生物活性,为骨科的临床研究与应用提供了构建组织工程骨的一种新的方法。本实用新型提出的脑脊液生物反应器具备基本的温度、二氧化碳浓度、湿度控制,可确保无菌的操作环境,并且能够方便地根据需要,对环境参数进行设置更改。基于本实用新型在体外环境中动态培养椎板成骨细胞,可以研究脑脊液的搏动频率、压强等因素对于骨细胞成长的影响,并且提供一种信号分析处理及数据保存方法便于后期数据处理分析。整套设备实现自动化智能控制,相较传统的静态培养方法具有明显优势。
上述脑脊液搏动装置正常工作时候,信号分析处理及数据保存方法。
具体的,通过数据采集卡将脑脊液实验信号采集并传输到电脑端,选择物理通道并设置合适的采样频率、采样点数,最大输入电压、最小输入电压。最小(大)输入电压和液压传感器选择相关;采样频率和采样点数根据脑脊液搏动频率的大小有较严格选择范围。通过多次实验,本实用新型中最终得到能够较好采集到压强信号的多组参数。选择目标文件夹的位置,便于实验结束后找到数据保存位置。
上述基本设置完成后,开始采集信号。系统通过将采样点离散信号拟合成模拟信号,将信号通过滤波处理,减少噪音干扰。通过波峰和波谷的提取方法,将峰/谷值显示,对于同一滤波后信号,实时显示同时并写入目标文件夹保存。还具有信号分析处理及数据保存方法还具备计时功能,获取本地时间后,通过对获取波形成分,即时间轴数值,折算成相应运行时间。
本实用新型又一技术方案提供了一种模拟脑脊液生物力学环境构建组织工程骨组织的方法,使用如上述的模拟脑脊液生物力学环境构建组织工程骨组织的装置进行操作,包括以下步骤:
将培养室、硅胶连接管等采用环氧乙烷充分消毒,将脑脊液循环瓶和培养液储存瓶在高温高压环境下充分消毒;
无菌环境下,在培养室的脑脊液搏动模拟管和空白对照管上涂抹一层胶原等支架材料,便于椎板成骨细胞的贴壁生长,检查培养室前后侧面板上连接头是否安装良好,确认后在培养室内放入适量培养液,并将上面板密封好;
无菌环境下,用硅胶连接管将主控制箱上支架内液压传感器和脑脊液循环瓶盖子上孔连接,液压传感器与第三蠕动泵连接,第三蠕动泵与电磁阀连接,再将硅胶连接管穿过细胞培养箱后部开孔,将电磁阀和培养室左面板上二号连接头连接,右面板二号连接头上的硅胶连接管穿过细胞培养箱后面板开孔与培养液储存瓶盖子上孔1连接,构建脑脊液循环通路;
无菌环境下,用硅胶连接管将培养液储存瓶盖子上孔和第一蠕动泵连接,将硅胶连接管穿过细胞培养箱后面板上开孔后连接第一蠕动泵和培养室前面板上一号连接头,同样将硅胶连接管穿过细胞培养箱后面板开孔后连接培养室后面板上一号连接头和培养液储存瓶盖子上孔,构建完成培养液循环通路;
在培养液储存瓶中装入培养液,在脑脊液循环瓶中装入水;
将电磁阀上信号采集数据线与主控制箱信号采集单元接口连接,打开主控制箱电源总开关,按动主控制箱上复位按钮,在触摸式显示屏上可对脑脊液搏动频率、流速等参数进行设计,并且切换至压强动态实时显示界面,直观看到模拟脑脊液搏动时候系统压强的实时变化;或将电磁阀上信号采集数据线与采集卡相连,打开主控制箱电源总开关,按动主控制箱上复位按钮,在触摸式显示屏上可对脑脊液搏动频率、流速等参数进行设计,电脑端选择文件保存位置后,点击屏幕上“开始”按钮,开始显示信号波形和在目标文件夹内保存数据。
应当理解,本文所述的示例性实施例是说明性的而非限制性的。尽管结合附图描述了本实用新型的一个或多个实施例,本领域普通技术人员应当理解,在不脱离通过所附权利要求所限定的本实用新型的精神和范围的情况下,可以做出各种形式和细节的改变。
- 还没有人留言评论。精彩留言会获得点赞!