用于急性移植物抗宿主病的供体选择和预后的组合物和方法与流程
交叉引用的申请
本申请要求于2018年4月19日提交的美国临时申请号62/659,807的权益,其全部内容通过引用并入本文。
序列表
本申请包含已通过efs-web以ascii格式提交并其全部内容通过引用并入本文的序列表。所述ascii副本,创建于2019年4月19日,名为du6176pct_seq_listing_st25.txt并且大小为2,186字节。
关于联邦资助研究的声明
本发明是在nih/niaid授予的联邦资助号ai119707的政府支持下完成的。联邦政府对本发明享有某些权利。
提供了用于受试者中急性移植物抗宿主病的供体选择、诊断、预后和确定风险的组合物和方法。
发明背景
同种异体骨髓干细胞移植(bmt)是一种用于治疗白血病以及其他非恶性疾病的有效治疗性方法。但是,植入的t细胞可能攻击受体中的许多器官,从而在bmt后100天内诱发急性移植物抗宿主病(agvhd)。目前,人白细胞抗原(hla)是用于骨髓或脐带血移植的供体与受体匹配的主要考虑因素。供体和受体之间紧密的hla匹配降低了受体将发展agvhd的机会。但是,还需要其他生物学标志物来确定与gvhd的发展有关的风险。
发明概述
本公开内容部分上提供了用于受试者中急性移植物抗宿主病的供体选择和预后的组合物和方法。
提供了如下方法,其中包括(a)从处于gvhd风险的第一受试者获得第一生物学样品,和(b)检测所述样品中的mir-142-3p水平。在一些方面,该样品与不处于gvhd风险的第二受试者获得的第二生物学样品相比具有降低水平的mir-142-3p。在一些方面,第一受试者需要骨髓干细胞移植。一些方面包括将从第一受试者获得的样品中的mir-142-3p水平与从第二受试者获得的mir-142-3p水平进行比较。一些方面包括确定第一受试者中gvhd的风险、预后或诊断。一些方面包括对第一受试者执行干细胞移植。
还提供了用于选择干细胞移植供体的方法,包括:(a)从第一受试者获得第一生物学样品和从第二受试者获得第二生物学样品,(b)检测第一生物学样品和第二生物学样品中的mir-142-3p水平;(c)确定(i)第二生物学样品中的mir-142-3p水平与(ii)第一生物学样品中的mir-142-3p水平的比率;和(d)基于所述比率确定第一受试者将发展gvhd的可能性。一些方面包括基于该比率选择移植供体。
一些方面包括基于所述比率不选择移植供体。一些方面包括:如果(i)∶(ii)的比率是至少约2∶1,则将来自第二受试者的干细胞移植到第一受试者。在一些方面,所述比率是约2.5∶1、约3∶1、约3.5∶1、约4∶1、约4.5∶1或约5∶1。
在一些方面,所述方法包括从一个或多个另外的受试者获得一个或多个另外的生物学样品,其中(i)第二生物学样品中的mir-142-3p水平与(ii)第一生物学样品中的mir-142-3p水平的比率高于(i)所述一个或多个另外的生物学样品中的mir-142-3p水平与(ii)第一生物学样品中的mir-142-3p水平的比率;和将来自第二受试者的干细胞移植到第一受试者。
在一些方面,所述第一受试者和第二受试者是hla匹配的。在其他方面,所述第一受试者和第二受试者是hla不匹配的。
还提供了确定受试者是否将发展gvhd的方法,包括:(a)从已经经历干细胞移植的第一受试者获得第一生物学样品;(b)检测第一生物学样品中的mir-142-3p水平;(c)从第一受试者获得第二生物学样品,其中在从受试者获得第一生物学样品之后,从所述受试者获得第二生物学样品;(d)确定第二生物学样品中的mir-142-3p水平;(e)确定(i)第二生物学样品中的mir-142-3p水平与(ii)第一生物学样品中的mir-142-3p水平的比率;和(f)基于所述比率确定第一受试者将发展gvhd的可能性。一些方面包括对受试者治疗gvhd。在一些方面,治疗包括施用免疫抑制药、化疗、类固醇、抗真菌剂、和抗病毒剂或抗生素中的一种或多种。在一些方面,免疫抑制药包括环孢霉素、他克莫司、甲氨蝶呤、西罗莫司、霉酚酸和利妥昔单抗中的一种或多种;化疗包括甲氨蝶呤;类固醇包括泼尼松或甲基泼尼松龙;抗真菌剂包括泊沙康唑;抗病毒剂包括阿昔洛韦或伐昔洛韦;和抗生素包括磺胺甲恶唑。
还提供了确定gvhd治疗的功效的方法,包括:(a)从已经用抗gvhd疗法治疗的第一受试者获得第一生物学样品;(b)检测第一生物学样品中的mir-142-3p水平;(c)从第一受试者获得第二生物学样品,其中在从受试者获得第一生物学样品之后,从所述受试者获得第二生物学样品;(d)确定第二生物学样品中的mir-142-3p水平;(e)确定(i)第二生物学样品中的mir-142-3p水平与(ii)第一生物学样品中的mir-142-3p水平的比率;和(f)基于所述比率确定抗gvhd疗法的功效。一些方面包括,如果所述比率低于约2∶1,则改变gvhd的治疗。在一些方面,抗gvhd疗法包括免疫抑制药、化疗、类固醇、抗真菌剂、和抗病毒剂或抗生素中的一种或多种。在一些方面,免疫抑制药包括环孢霉素、他克莫司、甲氨蝶呤、西罗莫司、霉酚酸和利妥昔单抗中的一种或多种;化疗包括甲氨蝶呤;类固醇包括泼尼松或甲基泼尼松龙;抗真菌剂包括泊沙康唑;抗病毒剂包括阿昔洛韦或伐昔洛韦;和抗生素包括磺胺甲恶唑(sulfamethoxazole)。
在一些方面,所述第一受试者和/或第二受试者是哺乳动物,例如人。
在一些方面,所述第一生物学样品和/或第二生物学样品选自组织、细胞、活组织检查、血液、淋巴液、血清、血浆、尿液、唾液、粘液和眼泪。在特定方面,所述样品包括血液或血浆。
还提供了用于实施所提供的方法的组合物。在一些方面,所述组合物包含用于确定生物学样品中的mir-142-3p水平的探针阵列,所述阵列包含与mir-142-3p杂交的多个探针。在一些方面,所述组合物包含用于确定生物学样品中的mir-142-3p水平的试剂盒,包括用于进行生物学样品中的mir-142-3p表达水平的确定的探针阵列和说明书。在一些方面,所述探针阵列包括具有与其附着的多个探针的固相支持物。
还提供了确定受试者中gvhd的风险、预后和/或诊断的方法,包括定量衍生自所述受试者的生物学样品中存在的至少一种生物学标志物的量、由其组成或基本上由其组成,其中所述生物学标志物包含与gvhd有关的mirna、由其组成或基本上由其组成。
一些方面包括对移植受体选择供体的方法,包括以下、由以下组成或基本上由以下组成:(a)从所述供体获得生物学样品;(b)确定所述生物学样品中与gvhd有关的一种或多种mirna生物学标志物的表达水平;(c)比较所述生物学样品中所述一种或多种mirna生物学标志物的表达水平与对照的表达水平,其中mirna表达低于对照指示匹配差;和(d)不选择所述供体用于移植。
在一些方面,所述方法还包括匹配供体-受体hla匹配,其中(a)供体-受体hla不匹配和低mirna表达导致不选择所述供体用于移植,和(b)供体-受体hla匹配和低mirna表达导致不选择所述供体用于移植。
还提供了确定受试者在移植事件后发展或已经发展gvhd的预后的方法,包括以下、由以下组成或基本上由以下组成:(a)从受试者获得生物学样品;(b)确定所述生物学样品中与gvhd有关的一种或多种mirna生物学标志物的表达水平;比较所述生物学样品中mirna生物学标志物的表达水平与对照的表达水平,其中mirna表达低于对照指示预后不良,和(c)如果一种或多种所述生物学标志物物以低水平表达,则施用适当的抗gvhd疗法或改变已经施用的抗gvhd疗法。
还提供了用于确定受试者中gvhd治疗方案的功效的方法,包括以下、由以下组成或基本上由以下组成:(a)确定表达与gvhd有关的一种或多种mirna生物学标志物的基线值;(b)向受试者施用抗gvhd疗法方案;和(c)重新确定所述受试者中一种或多种生物学标志物的表达水平,其中观察到一种或多种所述mirna生物学标志物表达水平的增加与所述疗法方案的功效相关联。
附图的简要说明
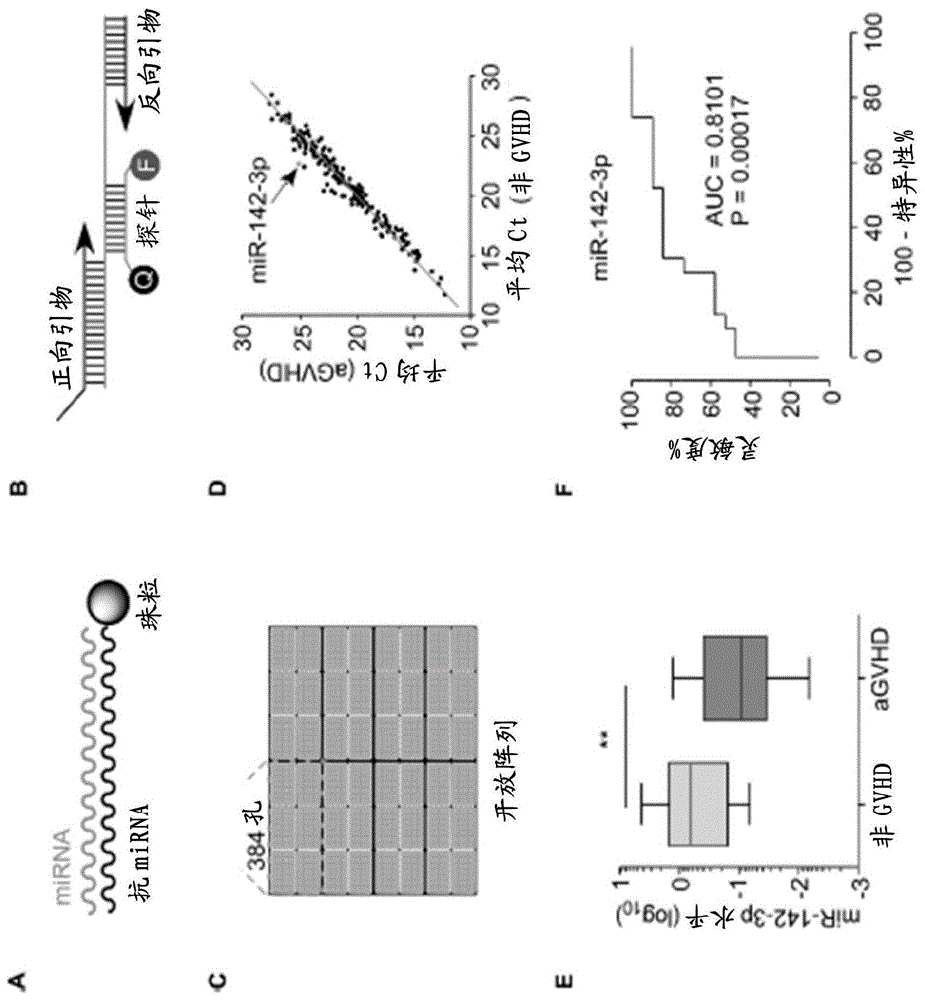
图1a-f涉及使用高通量平台对候选mirna进行谱分析。图1a描绘了使用抗mirna珠捕获方法的rna提取的示意图。图1b描绘了taqmanmirna实时pcr测定法的示意图;图1c描绘了taqmanmicrorna开放阵列芯片的示意图;图1d提供了从杜克医院的agvhd发病前1-3天(n=19)和时间点匹配的非gvhd(n=23)取得的发病前样品的血浆microrna的taqman开放阵列谱分析结果;图1e提供了来自非gvhd(n=23)和agvhd(n=19)患者的血浆中的mir-142-3p相对表达水平,其显著性通过两尾曼恩-惠特尼检验(**p≤0.01)来确定;图1f提供了血浆mir-142-3p的roc分析。
图2a和2b描绘了显示血浆mir-142-3p比率与agvhd发展有关的图。图2a描述了agvhd(n=53)和非gvhd患者(n=56)的供体和受体之间血浆mir-142-3p水平的比率。图2b描述了来自同一agvhd(n=52)或非gvhd(n=56)患者的第28天和第0天之间血浆mir-142-3p水平的比率;图2a和2b两者中的显著性通过两尾学生t检验确定(***p≤0.001)。
详细说明
除非另外定义,否则本文中使用的技术和科学术语具有本主题所属领域的普通技术人员通常理解的含义。本文参考了本领域普通技术人员已知的各种方法学。本领域普通技术人员已知的任何合适的材料和/或方法可以用于进行本文提供的方面。但是,描述了特定的材料和方法。除非另有说明,在以下说明书和实施例中参考的材料、试剂等可以从商业来源获得。阐述供参考的这些已知方法学的出版物和其他材料通过引用全文并入本文中,如同在全文中完整提供。
如本文所使用的,单数形式“一个”、“一种”和“该”既表示单数也表示复数,除非明确指出仅表示单数。
术语“约”表示所理解的数字不限于在此阐述的确切数字,并且旨在是指基本上围绕所述数字而不背离所公开的主题的范围的数字。如本文中所使用的,“约”将被本领域普通技术人员理解并且将在使用它的上下文中在某种程度上变化。如果在其给定使用上下文的情况下存在本领域普通技术人员不清楚的术语使用,则“约”将表示该特定术语的多至正负10%。
本文中术语“包括”、“包含”或“具有”及其变体的使用意在涵盖其后列出的要素及其等同物以及另外的要素。阐述为“包括”、“包含”或“具有”某些要素的方面也被认为是“基本上由这些要素组成”和“由这些要素组成”。
除非本文另外指出,否则本文中对数值范围的记载仅旨在用作单独指代落入该范围内的每个独立数值的简写方法,并且每个独立数值都被并入说明书中,如同其在本文中被单独记载一样。例如,如果将浓度范围陈述为1%至50%,则意图在本说明书中明确列出了诸如2至40%,10%至30%或1%至3%等的数值。这些仅是具体意图的示例,并且在所列举的最小数值和最大数值之间(包括所列举的所述最小数值和所述最大数值)的数值的所有可能组合被认为在本公开内容中明确地提及。
如本文所用,术语“mirna”或“mir”或“microrna”是指长度在10至30个核苷酸的非编码rna,其与编码rna杂交并调节其表达(参见zeng和cullen,rna,9(1):112-123,2003;kidnerandmartienssentrendsgenet,19(1):13-6,2003;dennisc,nature,420(6917):732,2002;couzinj,science298(5602):2296-7,2002,其中每一篇通过引用并入本文)。可以通过自然加工方式(例如,使用完整的细胞或细胞裂解液)或通过合成加工路线(例如,使用分离的加工酶,例如分离的dicer、argonaut或rnaseiii)从mirna前体获得10至30个核苷酸的mirna分子。应当理解,也可以直接地或者通过生物学或化学合成来产生10至30个核苷酸的rna分子,而无需从mir前体进行加工。
在该定义中包括天然mirna分子、pre-mirna、pri-mirna、在核酸序列上与天然形式相同的mirna分子以及核酸序列,其中一个或多个核酸已经被或被一个或更多的dna核苷酸和/或核酸类似物取代或代表。本说明书中的mirna分子有时被称为编码mirna的核酸分子或简称为核酸分子。
如本文所用,术语“生物学标志物”是指以变化的浓度存在于受试者中的天然存在的生物学分子,其可以用于预测疾病或病况例如gvhd的风险或发生率。例如,所述生物学标志物可以是以较高或较低量存在于有gvhd风险的受试者中的mirna。所述生物学标志物可以包括用作细胞、组织或受试者中gvhd的指示剂或标志物的核酸、核糖核酸或多肽。在某些方面,所述生物学标志物是mirna,例如mir-142-3p。
如本文所用,术语“急性移植物抗宿主病”、“agvhd”和“gvhd”可以互换使用并且是指通常在移植后的头100天内观察到的gvhd的急性或暴发性形式。例如在nassereddine,anticancerresearch,37(4):1547-1555(2017)中讨论了gvdh。
如本文所用,“治疗”、“疗法”和/或“疗法方案”是指响应于由患者表现出的或患者可能易感的疾病、病症或生理状况而进行的临床干预。治疗的目的包括症状的减轻或预防,减慢或停止疾病、病症或病况的发展或恶化和/或疾病、病症或病况的缓解。“治疗”是指治疗性处理和预防性或防备性措施中的一种或两种。需要治疗的那些患者包括已经受疾病或病症或者不期望的生理状况影响的那些患者以及要预防所述疾病或病症或者不期望的生理状况的那些患者。对于每个受试者而言治疗/疗法方案将有所不同,取决于几个因素,包括受试者的年龄/健康状况,疾病阶段等,并且可以由主治医生容易地确定。例如,可能的治疗/疗法包括但不限于免疫抑制药的施用,同种异体反应性t淋巴细胞的选择性耗尽,单克隆抗体(例如抗cd3、抗cd5、il-2抗体)的使用等。在本文中使用的术语“预防性治疗”是指用于防止诸如gvhd的病况发生的那些疗法。合适的预防性治疗可以包括使用免疫抑制药的预防性治疗,使用脐带血作为供体细胞的来源,供体与患者之间更紧密的hla匹配等。
术语“有效量”或“治疗有效量”是指足以实现有益或期望的生物学和/或临床结果的量。
如本文所用,术语“受试者”和“患者”可以互换使用并且是指人和非人动物。术语“非人动物”包括所有脊椎动物,例如哺乳动物和非哺乳动物,例如非人灵长类动物、绵羊、狗、猫、马、奶牛、鸡、两栖动物、爬行动物等。在某些方面,受试者是人。在某些方面,受试者是有gvhd风险的人。受试者可以是但不限于移植受体、移植供体、潜在的移植受体或潜在的移植供体。
如本文所用,术语“生物学样品”包括但不限于含有从受试者分离的组织、细胞和/或生物学流体的样品。生物学样品的例子包括组织、细胞、活组织检查、血液、淋巴液、血清、血浆、尿液、唾液、粘液和眼泪。在某些方面,生物学样品是血液样品(例如血浆样品)。生物学样品可以直接从受试者获得(例如,通过血液或组织采样)或从第三方获得(例如,从诸如医疗保健提供者或实验室技术员的中间人那里获得)。
如本文所用,术语“移植事件”是指从供体向受体移植器官、血液、骨髓或其他生物学材料的行为。在一些方面,移植事件包括骨髓移植(bonemarrowtransfer,bmt)。
i.引言
可以基于本方法评估与gvhd有关的任何mircorna。具体方面涉及基于生物学样品中的mir-142-3p水平评估发展gvhd的风险。mir-142-3p是被认为在造血发育中起作用的microrna并且其具有示例性序列uguaguguuuccuacuuuaugga(seqidno:1)。
ii.移植物抗宿主病
gvhd是同种异体干细胞移植的潜在严重并发症。在一些方面,gvhd起因于受试者接受来自供体或捐赠的脐带血的干细胞。来自供体的t细胞可以攻击受体中的健康细胞、组织或器官,从而损害细胞、组织或器官的功能或导致其衰竭。不受理论的束缚,据信gvhd是由以下一种或多种引起的:对受体施用具有活力和功能性免疫细胞的免疫活性移植物;在与供体免疫学上不同的受体(即组织不相容性)中执行移植;并在免疫受损的受体中执行移植。
在某些方面,gvhd与肝脏、皮肤、粘膜和胃肠道中的一种或多种的损害有关。在一些方面,gvhd影响免疫系统(例如造血系统,例如骨髓和/或胸腺)和肺(例如,以免疫介导的肺炎的形式)之一或二者。与gvhd有关的症状包括但不限于肠道炎症、粘膜脱落、腹泻、腹痛、恶心、呕吐、高胆红素水平、红斑丘疹和粘膜损害中的一种或多种。
经历同种异体干细胞移植或脐带血移植的受试者有发展gvhd的风险。其他风险因素包括供体和受体之间人白细胞抗原(hla)差异的程度(例如hla不匹配对比hla匹配,参见kanda,int.j.hematol.,98(3):300-308(2013)),供体和受体性别差异(例如,女性供体对于男性受体之间或男性供体对于女性受体),移植调理方案的强度,所用的gvhd预防性方案,移植物的来源(例如,外周血、骨髓或脐带血),受体的年龄,供体和受体的巨细胞病毒状况,供体爱泼斯坦-巴尔病毒敏感性,无菌环境的存在(例如肠道去污染)和具体的hla单倍型。可以考虑hla以将受体与供体匹配用于骨髓或脐带血移植。供体和受体之间的紧密hla匹配降低了发展agvhd的机会。hla匹配或不匹配可以涉及hla-a、-b、-c、-drb1、-dqb1和-dpb1基因座。
已经开发了几种用于对急性gvhd进行分级的系统。两个这样的系统是glucksberg级(i-iv)和国际骨髓移植注册机构(ibmtr)分级系统(ad)(glucksberg,transplantation,18(4):295-304(1974);rowlings,br.j.haemotol.,97:855-864(1997))。急性gvhd的严重程度可以通过评估皮肤、肝脏和胃肠道的受累程度来确定。单个器官受累的阶段与患者的表现状态组合(glucksberg)或不组合(ibmtr)得到总体分级。i(a)级gvhd的特征为轻度疾病,ii(b)级gvhd的特征为中度,iii(c)级为严重,并且iv(d)级危及生命。
ibmtr分级系统将急性gvhd的严重程度定义如下:a级–阶段1只有皮肤受累(身体上<25%有乳头状皮疹),无肝脏或胃肠道受累;b级–阶段2皮肤受累;阶段1至2肠道或肝脏受累;c级–阶段3任何器官系统受累(泛发性红皮病;胆红素6.1至15.0mg/dl;腹泻1500至2000ml/天);d级–阶段4任何器官系统受累(泛发性红皮病伴大疱形成;胆红素>15mg/dl;腹泻>2000ml/天或疼痛或肠梗阻)。
iii.检测mir-142-3p的方法
提供了检测mirna,例如mir-142-3p的方法。在一些方面,在生物学样品例如从受试者获得的生物学样品中检测mirna。在一些方面,mirna是细胞外mirna。在一些方面,mirna是循环mirna,例如在血液中的循环mirna。
一些方面涉及从受试者获得超过一个样品,例如两个或更多个样品,例如三个样品、四个样品或更多样品。在一些方面,所述样品从同一受试者获得。在某些方面,所述样品从不同的受试者获得。一些方面包括在所述两个或更多个样品之间在存在或不存在至少一种核酸的表达和/或所述至少一种核酸的表达水平进行相对比较。备选地,可以将单个样品与“标准化的”样品进行比较,这样的样品包括来自多个样品,优选地还来自几个个体的材料或数据。
在一些方面,在分析样品之前对样品执行一个或多个样品制备操作。这样的样品制备操作包括但不限于这样的操作,例如从组织/整个细胞样品中细胞内物质例如核酸的浓缩、悬浮、提取等,核酸的扩增,片段化,转录,标记和/或延伸反应。
可以使用本领域已知的任何技术分离核酸,尤其是rna并特别是mirna,例如基于苯酚的提取和基于硅胶基质或基于玻璃纤维过滤器(gff)的结合。基于苯酚的试剂包含变性剂和rnase抑制剂的组合,用于细胞和组织破坏和随后从污染物中分离rna。基于苯酚的分离程序可以回收10-200个核苷酸范围内的rna种类,例如mirna、5srrna、5.8srrna和ulsnrna。如果通过常规硅胶基质柱或gff程序纯化“总”rna的样品,则可能耗尽小rna。然而,诸如使用trizol或trireagent的提取程序将纯化所有大小的rna,并可以用于从将含有mirna/sirna的生物学样品中分离总rna。
通过本文所述的任何方法在检测之前处理样品所需的任何方法均落入本公开内容的范围内。
提供用于检测mirna的方法在本公开内容的一般范围内。一些方面涉及在本文包含的附图的绘图和图象中描述的mirna序列的检测。如本文所用,术语“检测”或“确定...的存在”是指对一种或多种生物学标志物如核酸、核糖核酸或多肽以及其他生物学分子的不可检测、低、正常或高浓度的定性测量。
检测可以包括1)基于一种或多种mirna的存在与否的意义上的检测,以及2)一种或多种mirna的表达水平或表达程度的登记/定量,这取决于所采用的检测方法。术语“定量”或“量化”可以互换使用,并且是指确定样品中物质(例如,生物学标志物)的量或丰度的过程,包括相对的或绝对的。例如,可以通过包括但不限于微阵列分析、qrt-pcr、northern或western印迹上的条带强度的方法或通过本领域中的各种其他方法来确定量化。
一种或多种核酸分子的检测允许对诸如gvhd的病况进行分类、诊断和预后。此类病况的分类在医学和科学上均具有相关性并且可以提供对病况的诊断、预后和治疗有用的重要信息。如本公开的目的,对病况例如gvhd的诊断是对疾病存在的确证,是本公开内容的目的,基于在本文中也称为核酸分子的至少一种mirna的表达。预后是对病况例如gvhd的可能结果的估计或预测,并且通过增加具体病况的信息量可以大大促进这种预后。
任何检测方法都落入本公开内容的一般范围内。检测方法可以是用于检测核酸(例如,rna)的通用方法,或者可以被优化用于检测小rna种类(例如,成熟的和/或前体mirna),或者被设计用于检测mirna种类。检测方法可以针对一种或多种核酸分子的存在或不存在进行评分,或者可以用于表达水平的检测。
检测方法可以分为两类,在本文中称为原位方法或筛选方法。术语原位方法是指检测其中样品结构得到保留的样品中的核酸分子。因此,这可以是其中组织结构得到保留的活组织检查。原位方法通常是组织学的,即本质上是微观的,并且包括但不限于诸如以下的方法:原位杂交技术和原位pcr方法。
筛选方法通常采用分子生物学技术并且通常涉及样品材料的制备,以便接近待检测的核酸分子。筛选方法包括但不限于诸如以下方法:阵列系统、亲和基质、northern印迹和pcr技术,例如实时定量rt-pcr。
本公开内容的一个方面是提供可以用于检测本文所定义的核酸分子的探针。本文所定义的探针是用于通过杂交检测核酸的核酸的特定序列。核酸可以包括天然的或合成的核酸,例如dna、rna、lna或pna。根据所选择的检测方法的要求,可以对探针进行标记、加标签、固定化或其他修饰。标记或标签可以用于鉴定与之缔合的化合物。一些方面采用通过本领域中任何方式标记或加标签的探针,方式例如但不限于:放射性标记、荧光标记和酶标记。此外,可以基于选择的检测方法对标记或未标记的探针固定化以促进检测。
原位杂交(ish)应用并外推核酸杂交技术到单细胞水平,并且与细胞化学、免疫细胞化学和免疫组织化学相组合,允许维持形态并鉴定待维持和鉴定的细胞标志物,将序列定位于群体例如组织和血液样品中的特定细胞。ish是一种杂交类型,使用互补核酸将一个或多个特定核酸序列定位在组织的部分或区段(原位),或者如果组织足够小,则定位在整个组织中(整体ish)。dnaish可以用于确定染色体的结构和单个基因的定位以及任选地它们的拷贝数。荧光dnaish(fish)可以例如用于医学诊断以评估染色体完整性。rnaish用于测定组织/跨细胞中的表达和基因表达模式,例如本文所述的mirna/核酸分子的表达。可以处理样品细胞以增加其渗透性从而允许探针进入细胞,可以将探针添加到处理过的细胞中,允许在相关温度下杂交,然后可以洗掉多余的探针。可以用放射性、荧光或抗原标签标记互补探针,以便可以分别使用放射自显影、荧光显微镜或免疫测定法确定探针在组织中的位置和数量。样品可以是本文所述的任何样品。探针同样是根据基于本文提及的mirna的任何探针的探针。
原位pcr是在ish之前对靶核酸序列的基于pcr的扩增。为了检测rna,可以在原位pcr之前引入细胞内反转录(rt)步骤以从rna模板生成互补dna。这使得能够检测低拷贝rna序列。
在原位pcr之前,细胞或组织样品可以被固定并透化以保留形态,并且允许pcr试剂接近待扩增的细胞内序列。然后可以在悬浮的完整细胞中或者直接在载玻片上的细胞离心制备物或组织切片中执行靶序列的pcr扩增。在前一种方法中,可以使用常规热循环仪对悬浮在pcr反应混合物中的固定的细胞进行热循环。pcr后,将细胞进行细胞离心至载玻片上,通过ish或免疫组织化学可视化细胞内pcr产物。可以通过在盖玻片下用pcr混合物覆盖样品,在载玻片上执行原位pcr,其中盖玻片可以密封以防止反应混合物的蒸发。通过将载玻片直接放置在常规或专门设计的热循环仪的加热块顶部上或通过使用热循环炉,可以实现热循环。细胞内pcr产物的检测可以通过多种技术来完成,例如使用pcr产物特异性探针的ish进行间接原位pcr,或通过没有ish的直接原位pcr,其通过直接检测标记的核苷酸(例如洋地黄毒苷11-dutp、荧光素-dutp,h-ctp或生物素-16-dutp),所述标记的核苷酸已在热循环过程中掺入pcr产物中。
在一些方面,通过微阵列进行检测。微阵列是核酸、蛋白质、小分子、细胞或其他物质的微观有序阵列,能够对复杂的生化样品进行并行分析。dna微阵列具有不同的核酸探针,称为捕获探针,其化学附着至固体基质上,该固体基质可以是微芯片、载玻片或微球尺寸的珠子。可以使用微阵列,例如以同时测量大量mrna/mirna的表达水平。
可以使用多种技术来制造微阵列,包括使用尖头针在载玻片上打印,使用预制掩模的光刻,使用动态微镜装置的光刻,喷墨打印或在微电极阵列上的电化学。
一些方面涉及使用微阵列用于在诸如gvhd的病况中mirna的表达谱分析。举例来说,可以从细胞或组织样品中提取rna,并且可以使用变性聚丙烯酰胺凝胶电泳(page)从总rna中从以尺寸选择小rna(18-26个核苷酸的rna)。然后,可以将寡核苷酸接头附着至小rna的5'和3'末端,并且所得连接产物可以用作模板进行10个扩增循环的rt-pcr反应。有义链pcr引物可以具有附着至其5'末端的cy3荧光团,从而荧光标记pcr产物的有义链。可以使pcr产物变性,然后与微阵列杂交。与阵列上的相应mirna捕获探针序列互补的称为靶核酸的pcr产物将通过碱基配对与捕获探针所固定的斑点杂交。当使用微阵列激光扫描仪激发时,斑点将发出荧光。然后,可以使用多种阳性和阴性对照以及阵列数据归一化方法,就特定mirna的拷贝数来评估每个斑点的荧光强度,这将导致对具体mirna的表达水平的评估。
可以使用几种类型的微阵列,例如斑点寡核苷酸微阵列、预制的寡核苷酸微阵列或斑点长寡核苷酸阵列。
在斑点寡核苷酸微阵列中,捕获探针可以是与mirna序列互补的寡核苷酸。这种类型的阵列可以与来自用两种不同的荧光团标记的两个待比较样品的尺寸选择的小rna的扩增的pcr产物杂交。备选地,可以从上述两个样品中提取包含小rna级分(包括mirna)的总rna并直接使用而无需尺寸选择小rna,以及使用t4rna连接酶和用两个不同的荧光团标记的短rna接头进行3’末端标记。可以将样品混合并杂交到可以扫描的单个微阵列上,以观察上调和下调的mirna基因。在一些方面,可以使用通用参考,包括大量的荧光团标记的寡核苷酸,与阵列捕获探针互补。
在预制的寡核苷酸微阵列或单通道微阵列中,可以设计探针以匹配已知的或预测的mirna的序列。来自例如affymetrix或agilent的公司的市售设计可以覆盖完整的基因组。这些微阵列提供了基因表达的绝对值的估计并因此两种条件的比较可以使用两个单独的微阵列。
斑点长寡核苷酸阵列由50到70聚体的寡核苷酸捕获探针组成,可以通过喷墨或自动印刷来生产。短寡核苷酸阵列由20-25聚体的寡聚核苷酸探针组成,可以通过光刻合成(affymetrix)或通过自动印刷来生产。最近,nimblegensystems的无掩模阵列合成将灵活性与大量探针相组合。通过定制阵列设计,阵列可以包含多至390,000个斑点。
术语“pcr反应”、“pcr扩增”、“pcr”、“pre-pcr”、“q-pcr”、“实时定量pcr”和“实时定量rt-pcr”是可互换的术语,用于表示使用核酸扩增系统,该系统扩增被检测的靶核酸。这种系统的例子包括聚合酶链反应(pcr)系统和连接酶链反应(lcr)系统。一些方面涉及使用基于核酸序列的扩增和qbeta复制酶系统。由所述扩增反应形成的产物可以实时监测或不实时监测,或仅在反应之后作为终点测量。
实时定量rt-pcr是聚合酶链反应的一种改进,用于快速测量聚合酶链反应产物的量。优选地,它是实时进行的,因此它是用于定量地测量dna,互补dna或核糖核酸(rna)的起始量的间接方法。这可用于确定样品中是否存在遗传序列,以及是否存在一定数量的拷贝。该过程可以用于使用热循环和热稳定的dna聚合酶扩增dna样品。
聚合酶链反应可以通过琼脂糖凝胶电泳,使用sybrgreen,双链dna染料和/或荧光报告探针来执行。在琼脂糖凝胶电泳中,可以用已知浓度的靶dna相似尺寸的片段来制备未知样品和已知样品,用于扩增。两个反应可以在相同条件下进行相同的时间长度(优选地使用相同的引物,或至少使用相似退火温度的引物)。琼脂糖凝胶电泳可以用于将反应产物与其原始dna和多余引物区分开。可以测量已知样品和未知样品的相对量,以确定未知样品的量。
sybrgreen染料是结合所有新合成的双链(ds)dna的dna结合染料,并且测量荧光强度的增加,从而可以确定初始浓度。可以通过添加荧光dsdna染料运行反应,并可以监测荧光水平,当染料与dsdna结合时发出荧光。通过参考标准样品或标准曲线,可以确定pcr中的dsdna浓度。
荧光报告分子探针使用基于序列特异性核酸的探针来定量探针序列而不是全部的双链dna。可以使用基于dna的探针(带有荧光报告分子和处于相邻位置的淬灭剂),所谓的双标记探针。报道分子与淬灭剂非常接近,防止其发出荧光;当探针破裂时,可以检测到荧光。这个过程取决于所涉及的聚合酶的5'至3'核酸外切酶活性。实时定量pcr反应可以通过添加双标记探针进行制备。在双链dna模板变性时,探针能够结合在模板dna的目标区域中的其互补序列(引物也是如此)。当加热pcr反应混合物以激活聚合酶时,聚合酶开始合成互补链至引发的单链模板dna。随着聚合反应的继续,它到达与其互补序列结合的探针,该探针由于聚合酶的5'-3'核酸外切酶活性而被水解,从而将荧光报告分子与猝灭剂分子分开。这导致荧光的增加,可以检测到。在实时pcr反应的热循环期间,可以监测在每个pcr循环中从水解的双标记探针释放的荧光的增加,从而可以准确确定dna的最终量,进而初始量。
可以确定本文定义的核酸分子的表达的任何pcr方法都落入本公开内容的范围内。一些方面包括实时定量rt-pcr方法,基于根据本文所述使用sybrgreen染料或双标记探针用于核酸的检测和定量。
本公开内容的一个方面包括通过诸如northern印迹分析的技术检测本文公开的核酸分子。
本公开内容的另一方面包括用于预测受试者中gvhd的试剂盒,所述试剂盒包括:用于反转录衍生自受试者的生物学样品中用于gvhd的一种或多种mirna生物学标志物的引物,其中所述mirna生物学标志物中包括mir-142-3p以及说明书,所述说明书用于定量生物学样品中的mirna生物学标志物表达水平,以及如果衍生自受试者的生物学样品中的mirna生物学标志物的表达水平低于参考样品,预测受试者有发展gvhd的风险增加。
本公开的一个方面包括用于诊断受试者中gvhd的试剂盒,所述试剂盒包括:用于反转录衍生自受试者的生物学样品中用于gvhd的一种或多种mirna生物学标志物的引物,其中所述mirna生物学标志物由mir-142-3p组成,以及说明书,其用于定量生物学样品中的mirna生物学标志物表达水平,以及如果衍生自受试者的生物学样品中mirna生物学标志物的表达水平低于参考对照,则诊断受试者具有gvhd。
本公开内容的一个方面包括用于确定受试者发展或已经发展gvhd的预后的试剂盒,所述试剂盒包括:用于反转录衍生自受试者的生物学样品中用于gvhd的一种或多种mirna生物学标志物的引物,其中所述mirna生物学标志物由mir-423、mir-142-3p组成,以及说明书,其用于定量生物学样品中的mirna生物学标志物表达水平,以及如果衍生自受试者的生物学样品中所述mirna生物学标志物的表达水平低于参考对照,则鉴定所述受试者gvhd存活的机会差。
本公开内容的一个方面包括用于确定受试者发展或已经发展gvhd的预后的试剂盒,所述试剂盒包括:用于反转录衍生自受试者的生物学样品中用于gvhd的一种或多种mirna生物学标志物的引物,其中所述mirna生物学标志物由mir-142-3p组成,以及说明书,其用于定量生物学样品中所述mirna生物学标志物的表达水平,以及如果衍生自受试者的生物学样品中所述mirna生物学标志物的表达水平低于参考对照,则鉴定所述受试者的gvhd存活的机会差
本公开内容的还另一个方面提供了物质的组合物,其包括以下、由以下组成或基本上由以下组成:(a)用于确定样品中的mirna水平的探针阵列,所述阵列包括与和gvhd有关的一种或多种mirna杂交的多个探针;或(b)用于确定样品中mirna水平的试剂盒,其中包括探针阵列和用于进行确定样品中的mirna表达水平的说明书。在一些方面,所述探针阵列还包括具有与其附着的多个探针的固相支持物。
iv.风险确定
令人惊讶地,确定可以基于从受试者获得的生物学样品中的mir-142-3p水平(例如表达水平)来评估gvhd的风险。此类mir-142-3p水平也可以用于诊断gvhd或监测gvhd的进程。
例如,在一些方面,从受试者获得的生物学样品中的mir-142-3p水平降低与受试者将发展gvhd的风险增加有关或关联。在一些方面,供体(或潜在供体)中的mir-142-3p水平增加与受体(或潜在受体)将发展gvhd的风险降低有关或关联。
在某些方面,比较了来自两个或更多个受试者(例如3、4、5、6、7、8、9或10个或更多个受试者)的mir-142-3p水平,并基于mir-142-3p的水平确定gvhd的相对风险。
在一些方面,基于(i)从一个受试者(例如,移植供体或潜在供体)获得的生物学样品中的mir-142-3p水平与(ii)从不同受试者(例如移植受体或潜在受体)获得的生物学样品中的mir-142-3p水平的比率(例如log2比率)进行风险确定。示例性比率(例如,log2比率)包括约0.5∶1、约1∶1、约1.5∶1、约2∶1、约2.5∶1、约3∶1、约3.5∶1、约4∶1、约4.5∶1和约5∶1,例如0.5∶1、1∶1、1.5∶1、2∶1、2.5∶1、3∶1、3.5∶1、4∶1、4.5∶1和5∶1。
在一些方面,确定受试者有发展gvhd的风险是比率小于约2∶1、小于约1.5∶1、小于约1∶1或小于约0.5∶1,例如小于2∶1、小于1.5∶1、小于1∶1或小于0.5.1。
在一些方面,风险确定是相对风险确定。例如,与具有更低供体∶受体mir-142-3p比率的供体-受体(或潜在的供体-潜在受体对)相比,具有更高供体∶受体mir-142-3p比率的供体-受体对(或潜在的供体-潜在受体对)可能有降低的gvhd风险。因此,一些方面包括检测一个或多个潜在受体和一个或多个潜在供体中的mir-142-3p水平,以及基于所述潜在供体和潜在受体之间的供体∶受体mir-142-3p比率来确定gvhd的风险。一些方面包括基于所确定的比率来选择供体和/或受体。一些方面包括基于所确定的比率来阻止或延迟移植。
一些方面包括确定已经经历干细胞移植的受试者将发展gvhd的风险。其他方面包括确定gvhd治疗的功效。可以通过检测mir-142-3p水平随时间的变化来确定这种风险。例如,在受试者接受移植或gvhd治疗后约100天的时间段内,可以检测并比较从受试者获得的生物学样品中的mir-142-3p水平。可以每天、每周或每月获得此类样品。因此,在一些方面,在接受移植或gvhd治疗后每天获得生物学样品。在一些方面,在接受移植或gvhd治疗后,每周至少一次从受试者获得生物学样品。在一些方面,在接受移植或gvhd治疗后每月至少一次获得生物学样品。在一些方面,在接受移植或gvhd治疗后1天、2天、3天、4天、5天、6天、7天、8天、9天、10天、11天、12天、13天、14天、15天、16天、17天、18天、19天、20天、21天、22天、23天、24天、25天、26天、27天、28天、29天、30天或31天获得生物学样品。在一些方面,在接受移植或gvhd治疗后立即或一天内获得所述生物学样品。
在一些方面,发展gvhd的风险基于(i)在较晚时间点获得的生物学样品中的mir-142-3p水平与(ii)在较早的时间点获得的生物学样品中的mir-142-3p水平的比率来确定。在一些方面,比率(例如log2比率)小于约3∶1,小于约2∶5.1,小于约2∶1,小于约1.5∶1,小于约1∶1,小于约0.5∶1,或小于约-0.1∶1,或小于约-1∶1指示了发展gvhd的风险。例如,在某些方面,比率小于3∶1,小于2∶5.1,小于2∶1,小于1.5∶1,小于1∶1,小于0.5∶1,或小于-0.1∶1,或小于-1∶1指示了发展gvhd的风险。
如上所述,一些方面涉及基于mir-142-3p水平随时间的变化确定gvhd治疗的功效。因此,在一些方面,mir-142-3p水平随时间的增加指示了有效的gvhd治疗。备选地,在一些方面,mir-142-3p水平随时间的降低指示了无效的gvhd治疗。一些方面涉及基于(i)在较晚时间点获得的生物学样品中的mir-142-3p水平与(ii)在较早时间点获得的生物学样品中的mir-142-3p水平的比率来确定gvhd治疗的功效。在一些方面,比率(例如log2比率)小于约3∶1,小于约2∶5.1,小于约2∶1,小于约1.5∶1,小于约1∶1,小于约0.5∶1,或小于约-0.1∶1,或小于约-1∶1指示了持续或恶化的gvhd的风险。例如,在某些方面,比率小于3∶1,小于2∶5.1,小于2∶1,小于1.5∶1,小于1∶1,小于0.5∶1,或小于-0.1∶1,或小于-1∶1指示了存在gvhd持续或恶化的风险。
在一些方面,基于检测mir-142-3p水平与其他指标的组合来评估发展gvhd的风险或gvhd治疗的功效。此类其他指标包括,例如,hla匹配或不匹配,和/或检测升高或降低水平的生物学标志物,例如mir-423、mir-199a-3p、mir-93*和mir-377中的一个或多个。因此,在一些方面,hla不匹配以及mir-423、mir-199a-3p、mir-93*和mir-377中的一种或多种的升高水平指示发展gvhd的风险。
因此,除其他指标(例如hla)外还有或与其他指标(例如hla)无关:(1)供体血浆中的低mir-142-3p水平是供体选择和骨髓移植后发展agvhd的风险因素;和/或(2)骨髓移植后受体中的血浆mir-142-3p水平可以用于监测agvhd的发展。
一些方面包括匹配供体和受体,其中(a)供体-受体hla不匹配和低mir-142-3p表达导致不选择所述供体用于移植和/或(b)供体-受体hla匹配和低mir-142-3p表达导致不选择供体用于移植。一些方面包括匹配供体和受体,其中(a)供体-受体hla不匹配和高mir-142-3p表达导致选择所述供体用于移植和/或(b)供体-受体hla匹配和高mir-142-3p表达导致选择所述供体用于移植。
在一些方面,基于与对照或阈值的比较,mir-142-3p表达水平被分类为高或低。可以参照gvhd或非gvhd受试者中的mir-142-3p表达水平来确定此类对照或阈值,或参照gvhd或非gvhd受试者的群体来确定。
v.gvhd治疗
一些方面包括治疗具有gvhd或有发展gvhd风险的受试者。在一些方面,对诊断或预后具有gvhd的受试者施用治疗。在一些方面,可以在确定治疗的功效或确定gvhd进展的风险时修改受试者的治疗。
一些方面涉及预防性治疗,这是指预防gvhd发生的疗法。合适的预防性治疗可以包括使用免疫抑制药的预防性治疗,使用脐带血作为供体细胞的来源以及寻求供体和受体之间更紧密的hla匹配。
一些方面包括启动或施用,监测和/或修改治疗方案。gvhd治疗的非限制性实例包括免疫抑制药(例如霉酚酸酯莫非替尔(mofetil)、阿仑单抗[campath]、atg、西罗莫司、环孢霉素、他克莫司、甲氨蝶呤、西罗莫司、霉酚酸和利妥昔单抗中的一种或多种);选择性耗尽同种反应性t淋巴细胞;单克隆抗体(例如抗cd3、抗cd5和/或il-2抗体);化疗(例如甲氨蝶呤);类固醇(例如强的松和甲基强的松龙中的一种或两种);抗真菌剂(例如泊沙康唑);抗病毒剂(例如阿昔洛韦或伐昔洛韦中的一种或两种);和抗生素(例如磺胺甲恶唑)。gvhd的示例性治疗在nassereddine,anticancerresearch,37(4):1547-1555(2017)中进行了阐述。
包括以下实施例作为本文所述组合物的举例说明。这些实施例决不旨在限制本发明的范围。对于本发明所属领域的技术人员而言,本发明的其他方面将是显而易见的。
实施例
实施例1:
样品收集、rna提取、反转录、实时pcr和pcr产物测序
使用由来自多中心的经历同种异体hct的192名人受试者和114个相应供体组成的群体进行了研究。从杜克大学医学中心、达纳法伯癌症研究所以及血液和骨髓移植临床试验网络收集血浆样品。mirna谱分析集由杜克大学医学中心的已经发展agvhd的19名hct患者和从未发展agvhd(非gvhd)的23名hct患者组成。来自达纳法伯癌症研究所的15个非gvhd和agvhd发作前的15个agvhd样品的另一个群组用于执行独立的开放阵列测定法,以验证从杜克样品中鉴定出的候选mirna。mir-142-3p鉴定集包括6名agvhd和6名非gvhd患者,以及来自达纳法伯癌症研究所的每位受体的对应供体。mir-142-3p验证集包括来自临床试验网络的52名agvhd和56名非gvhd患者,以及每个受体的对应供体。从患者中抽取edta抗凝血液并使用两步离心方案(2000rpm进行10分钟,12000rpm进行3分钟)从所有血液样品中分离无细胞血浆,以防止细胞核酸的污染。agvhd的诊断基于临床标准并通过活组织检查在靶器官中进行组织学证实。基于靶器官受累的严重度对agvhd进行分级。
使用taqmanabcmirna纯化试剂盒(thermofisher)从50μl血浆中提取总rna。来自拟南芥的合成的micrornaath-mir159a用作加标对照(单链rna,序列:uuuggauugaagggagcucua(seqidno:2))。简而言之,将100ulabc缓冲液添加到50ul血浆中,涡旋30秒以混合,然后短暂离心。将2μl的1nm外部对照mirna(ath-mir159a)添加到制备的样品中,涡旋以混合,短暂离心,然后按照制造商的说明书纯化mirna。最后,将microrna在100μl不含dnase和rnase的水中洗脱。
对于反转录和预扩增,使用真空离心冷凝器(speedvacplus,sc110a,savant)在室温以低速将总microrna从100μl浓缩到20μl。使用taqmanmicrorna反转录试剂盒(cat#:4366596,thermofisher)根据制造商的方案合成cdna。使用taqmanpreampmastermix(cat#:4391128,thermofisher)和megaplexpreamp引物(cat#:4399233和4444303,thermofisher)根据制造商的方案预扩增rt产物。表1中列出了所用的引物和探针以及检测的mirna序列,其中“fam”表示荧光染料荧光素,“mgb”表示小沟结合分子。
表1:用于检测mirna的引物和探针
为了进行开放阵列实时pcr,将预扩增反应产物用0.1xteph8.0以1:10稀释。将40μl稀释的预扩增a池(或b池)混合物与40μl2xpcr主混合物混合。使用自动系统,用xstream移液器(eppendorf)将每个池的5μl放入8个孔中,并用石蜡油覆盖开放阵列。阵列使用quantstudio12kflex(thermofisher)运行。
为了验证来自taqman测定法的micrornapcr产物的特异性,使用ta克隆试剂盒(cat#231124,qiagen)克隆了pcr产物并转化入感受态dh5α大肠杆菌(cat#c2987h,neb)中。用杜克大学dna分析设施对来自每个mirna的20个克隆的质粒进行测序。dna序列比对通过dnastarlasergenestructuralbiologysuite(dnastar)执行。
实施例2:
使用高通量平台对候选mirna进行谱分析
microrna序列特异性抗mirna珠捕获方法用于从血浆中纯化microrna(图1a)。从最终洗脱液中洗掉血液相关样品中常见的rt-pcr抑制剂和降解的rna片段。此外,基于探针的实时pcr方法(图1b)和开放阵列pcr芯片(图1c)用于改善特异性和通量。通过对来自健康供体的血浆microrna的五个随机micrornapcr产物进行测序来验证平台。测序结果表明平台可以有效地和特异性地检测来自血浆样品的microrna(92%<特异性≤100%)。使用来自19名已经发展gvhd的患者和23名时间点匹配的非gvhd受试者的血浆在平台执行microrna分析。
大多数血浆microrna在疾病和非疾病之间显示相似的表达模式(图1d)。广义线性模型分析用于分析可以区分agvhd和非gvhd的microrna。
结果显示,与来自非gvhd患者的血浆相比,来自agvhd患者的血浆中的mirna-142-3p差异表达。使用来自达纳法伯癌症研究所的另一个群组血浆样品,在独立的开放阵列中进一步验证了mir-142-3p的表达水平。与来自非gvhd的血浆相比,在来自agvhd的血浆中的mir-142-3p表达水平显著更低(图1d,1e)。auc分析指示mir-142-3p在检测agvhd方面具有高灵敏度和特异性(图1f)。
实施例3:
供体和受体血浆mir-142-3p比率与agvhd发展有关
测定了来自agvhd患者的血浆中的mir-142-3p表达水平更低(图1d,1e)。与来自非gvhd组相比,agvhd组中供体与受体之间血浆mir-142-3p的比率平均低4倍。还使用bmt后第0天和第28天获得的血浆样品确定mir-142-3p的表达水平。在这两种情况下,bmt之前血浆中的mir-142-3p水平的低比率与agvhd有关(图2a)。此外,bmt后第0天和第28天之间的mir-142-3p比率在agvhd组和非gvhd组之间显示出相似的模式(图2b)。这些数据表明供体血浆中的低mir-142-3p水平是供体选择和bmt后agvhd发展的风险因素。此外,bmt后受体的血浆mir-142-3p水平可以用于监测agvhd的发展。
本说明书中提到的任何专利或出版物都指示了本发明所属领域的技术人员的水平。这些专利和出版物通过引用并入本文,程度如同每个单独的出版物被明确地和单独地指出通过引用并入。
在有冲突的情况下,以本说明书包括定义为准。本领域技术人员将容易理解本发明非常适合于进行目标并获得所提及的目的和优点以及其中固有的那些。本文描述的本公开内容目前代表优选的方面,是示例性的,并且不意图作为对本发明范围的限制。本领域技术人员将想到其中的改变和其他用途,这包括在由权利要求的范围所限定的本发明的精神内。
序列表
<110>dukeuniversity
<120>用于急性移植物抗宿主病的供体选择和预后的组合物和方法
<130>d1181240wo/du6176pct
<150>62/659,807
<151>2018-04-19
<160>10
<170>patentinversion3.5
<210>1
<211>23
<212>rna
<213>人工序列
<220>
<223>mirnahsa-mir-142-3p
<400>1
uguaguguuuccuacuuuaugga23
<210>2
<211>21
<212>rna
<213>人工序列
<220>
<223>ath-mir159a
<400>2
uuuggauugaagggagcucua21
<210>3
<211>49
<212>dna
<213>人工序列
<220>
<223>rt引物159art
<400>3
gtcgtatccagtgcagggtccgaggtattcgcactggatacgactagag49
<210>4
<211>17
<212>dna
<213>人工序列
<220>
<223>探针159ap
<400>4
ctggatacgactagagc17
<210>5
<211>21
<212>dna
<213>人工序列
<220>
<223>qpcr5p引物159af
<400>5
gccgtttggattgaagggagc21
<210>6
<211>16
<212>dna
<213>人工序列
<220>
<223>qpcr3p引物upr
<400>6
gtgcagggtccgaggt16
<210>7
<211>51
<212>dna
<213>人工序列
<220>
<223>rt引物142-3prt
<400>7
gtcgtatccagtgcagggtccgaggtattcgcactggatacgactccataa51
<210>8
<211>18
<212>dna
<213>人工序列
<220>
<223>探针142-3pp
<400>8
ctggatacgactccataa18
<210>9
<211>24
<212>dna
<213>人工序列
<220>
<223>qpcr5p引物142-3pf
<400>9
cgccgctgtagtgtttcctacttt24
<210>10
<211>16
<212>dna
<213>人工序列
<220>
<223>qpcr3p引物upr
<400>10
gtgcagggtccgaggt16
- 还没有人留言评论。精彩留言会获得点赞!