单萜基双香豆素类化合物、药物组合物及其制备方法和用途与流程
本发明涉及天然药物化学领域,具体涉及一种单萜基双香豆素类化合物、药物组合物及其制备方法和用途。
背景技术:
中枢神经系统退行性病变是一类慢性、退行性神经系统疾病,临床上对于这类疾病尚无有效控制病程进展的措施,患者最终将丧失生活能力甚至死亡,例如,阿尔兹海默症,占痴呆症中60%-70%的成因,现在已成为21世纪人类健康最大的威胁之一。最新统计表明,全世界年龄超过60岁的人数约有4000万患有ad,另外每年有770万新增病例,因此已经成为全球一个重要的公共健康问题。但ad的病因至今仍然不明确。因此寻找有效的防治ad的药物十分迫切。胆碱能神经系统功能紊乱是ad发病机制之一,针对胆碱能神经系统的调控可能可以成为防治ad的途径之一。
三叉苦(学名evodialepta(spreng.)merr.)是芸香科(rutaceae)吴茱萸属(evodia)植物,主要分布于我国南部诸省及东南亚地区,是岭南常用中草药。《中药大辞典》记载其味苦,性寒,有清热解毒、祛风除湿的功效,主治咽喉肿痛、虫蛇咬伤、脑炎、风湿骨痛、湿疹、皮炎和疮疡等,也是广东地区凉茶的重要组分之一。
目前,三叉苦化学成分的研究报道较多,主要包括色稀、生物碱、黄酮等。在前人的研究基础之上,我们对三叉苦茎部进行了抗老年痴呆活性先导化合物的研究,发现了一种具有显著活性的单萜基双香豆素类化合物。
技术实现要素:
因此,本发明的其中一个目的在于提供单萜基双香豆素类化合物,其对映异构体、非对映异构体、顺反异构体、外消旋体、药学上可接受的盐或它们的混合物。
所述单萜基双香豆素类化合物具有式(i)所示的结构,
其中,与r1、r2、r3和r4连接的
带“*”碳原子和带“#”碳原子为手性碳原子,带“*”碳原子为r构型、s构型,或其组合,带“#”碳原子为r构型、s构型,或其组合;
x1、x2、x3和x4独立地选自碳原子或者氧原子;
r1-r4独立地选自h、羟基、氧原子、c1-c6的烷基、c3-c6的环烷基、c1-c6的烷氧基;
r5、r6独立地选自h、羟基、c1-c5的烷基、c3-c5的环烷基、c1-c5的烷氧基。
进一步地,r1、r2、r3、r4独立地选自h、羟基、氧原子、甲基、乙基、正丙基、异丙基、正丁基、异丁基、叔丁基、环丙基、环丁基、环戊基、环己基、甲氧基、乙氧基、正丙氧基、异丙氧基中的一种;
当r1、r2、r3或者r4为氧原子时,与所述氧原子连接的
r5、r6独立地选自h、羟基、甲基、乙基、正丙基、异丙基、正丁基、异丁基、叔丁基、环丙基、环丁基、环戊基、甲氧基、乙氧基、正丙氧基、异丙氧基中的一种。
进一步地,x1和x2中有一个为氧原子,另一个为碳原子;x3和x4中有一个为氧原子,另一个为碳原子;
r1和r2中有一个为氧原子,另一个为羟基;r3和r4有一个为氧原子,另一个为羟基;
x1和r1同时为氧原子,或者同时不为氧原子;x2和r2同时为氧原子,或者同时不为氧原子;x3和r3同时为氧原子,或者同时不为氧原子;x4和r4同时为氧原子,或者同时不为氧原子。
进一步地,所述单萜基双香豆素类化合物具有如下(ii)-(v)结构:
进一步地,所述单萜基双香豆素类化合物如下所示的结构:
本发明的另一个目的在于提供所述的单萜基双香豆素类化合物的制备方法,包括如下步骤:
1)取三叉苦茎,用有机溶剂经一次或多次提取,得到有机溶剂提取物;
2)将有机溶剂提取物用水分散后,依次用石油醚、乙酸乙酯、正丁醇萃取,回收乙酸乙酯提取物;
3)将乙酸乙酯提取物经硅胶色谱柱分离,以环己烷/乙酸乙酯为洗脱剂梯度洗脱,得到粗组分,再将所得粗组分经一次mci柱层析、一次反向ods柱层析、一次sephadexlh-20柱层析,得到单萜基双香豆素类化合物的柱层析组分;
4)将含单萜基双香豆素类化合物的柱层析组分用hplc分离精制,即得。
进一步地,所述制备方法,还满足如下的(1)-(8)项中的至少一项;
(1)步骤1)中,所述有机溶剂选自正己烷、二氯甲烷、乙酸乙酯、正丁醇、甲醇、50%-95%的甲醇水溶液、乙醇、50-95%的乙醇水溶液中的至少一种;
(2)步骤1)中,所述提取为回流提取或者超声提取,优选回流提取,回流提物的时间为1-3h,次数为2-5次;
(3)步骤1)中,加入8-12倍体积的有机溶剂;
(4)步骤1)中,所述有机溶剂提取物优选为三叉苦茎提取后经蒸干得到的浸膏;
(5)步骤3)中,一次mci柱层析分离过程中,柱层析采用体积比为2∶3→1∶0的甲醇和水进行梯度洗脱;一次反向ods柱层析采用体积比为3∶2→1∶0的甲醇和水进行梯度洗脱;
(6)步骤3)中,硅胶色谱柱分离过程中,采用体积比为100∶1→0∶1环己烷和乙酸乙酯为洗脱剂梯度洗脱;
(7)步骤3)中,sephadexlh-20柱层析分离过程中,采用甲醇或乙醇为洗脱剂进行洗脱;
(8)步骤4)中,分离精制过程中,采用体积百分数50-75%的乙腈或者甲醇水溶液为流动相;分离精制之后再采用手性hplc柱进行拆分。
本发明还提供了一种药物组合物,所述药物组合物包含上述任一所述的单萜基双香豆素类化合物,其对映异构体、非对映异构体、顺反异构体、外消旋体、药学上可接受的盐或它们的混合物,以及任选的药学可接受的载体。
进一步地,以药物组合物的总质量计,所述药学上可接受的载体选自药学上可接受的溶剂、增溶剂、助溶剂、乳化剂、着色剂、粘合剂、崩解剂、填充剂、润滑剂、润湿剂、渗透压调节剂、稳定剂、助流剂、矫味剂、防腐剂、助悬剂、包衣材料、芳香剂、抗粘合剂、整合剂、渗透促进剂、ph值调节剂、缓冲剂、增塑剂、表面活性剂、增稠剂、包合剂、保湿剂、吸收剂、稀释剂、絮凝剂与反絮凝剂、助滤剂、释放阻滞剂、高分子骨架材料和成膜材料中的至少一种;
所述药物组合物为凝胶剂、乳霜剂、片剂、胶囊剂、散剂、合剂、丸剂、颗粒剂、溶液剂、糖浆剂、煎膏剂、栓剂、气雾剂、贴膏剂、软膏剂、注射剂、喷剂、搽剂、酊剂、湿敷剂、糊剂、洗剂或者缓控释制剂。
所述的单萜基双香豆素类化合物,其对映异构体、非对映异构体、顺反异构体、外消旋体、药学上可接受的盐或它们的混合物,或者所述的药物组合物在制备乙酰胆碱酯酶抑制剂中的用途。
所述的单萜基双香豆素类化合物,其对映异构体、非对映异构体、顺反异构体、外消旋体、药学上可接受的盐或它们的混合物,或者所述的药物组合物在制备用于预防或治疗神经退行性疾病的药物中的用途。
进一步地,所述神经退行性疾病是老年痴呆、记忆力减退、脑组织退行性病变症候群或胆碱能神经退行性病变。
本发明技术方案,具有如下优点:
本发明所提供的单萜基双香豆素类化合物,具有显著的改善东莨菪碱诱导的神经细胞损伤的作用,而且能够显著抑制乙酰胆碱酯酶的活性,具有抗炎、抗氧化的作用,可用于包括老年痴呆症(又称为阿尔茨海默症),胆碱能神经退行病变,学习记忆能力减退等神经系统退行性疾病的预防和治疗。
附图说明
为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
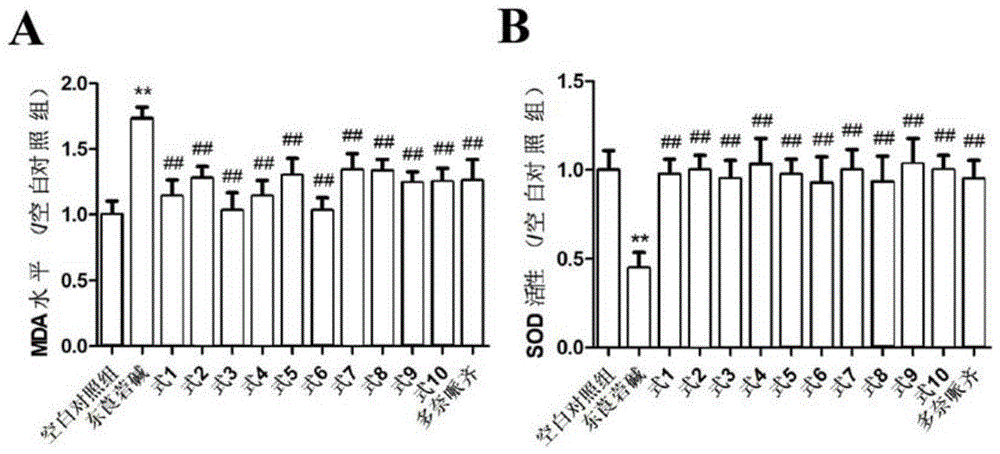
图1是本发明实验例1中氧化应激测试的结果图,a为mda水平,b为sod活性水平;
图2是本发明实验例1中神经炎症测试的结果图,a为il-1β,b为il-6水平;
图3是本发明实施例1中外消旋体1的高分辨质谱(hr-esi-ms)图谱;
图4是本发明实施例1中外消旋体1的1h-nmr图谱(400mhz);
图5是本发明实施例1中外消旋体1的13c-nmr图谱(100mhz);
图6是本发明实施例1中外消旋体1的二维相核磁共振(cosynmr)图谱;
图7是本发明实施例1中外消旋体1的异核单量子相干核磁共振(hsqcnmr)图谱;
图8是本发明实施例1中外消旋体1的1h的异核多碳相关谱核磁共振(hmbcnmr)图谱;
图9是本发明实施例1中外消旋体1的旋转坐标系noe(roesynmr)图谱;
图10是本发明实施例1中化合物1的气相ecd检测图谱。
图11是本发明实施例1中化合物2的气相ecd检测图谱。
图12是本发明实施例1中外消旋体2的高分辨质谱(hr-esi-ms)图谱;
图13是本发明实施例1中外消旋体2的1h-nmr图谱(400mhz);
图14是本发明实施例1中外消旋体2的13c-nmr图谱(100mhz);
图15是本发明实施例1中外消旋体2的二维相核磁共振(cosynmr)图谱;
图16是本发明实施例1中外消旋体2的异核单量子相干核磁共振(hsqcnmr)图谱;
图17是本发明实施例1中外消旋体2的1h的异核多碳相关谱核磁共振(hmbcnmr)图谱;
图18是本发明实施例1中外消旋体2的旋转坐标系noe(roesynmr)图谱;
图19是本发明实施例1中外消旋体3的高分辨质谱(hr-esi-ms)图谱;
图20是本发明实施例1中外消旋体3的1h-nmr图谱(400mhz);
图21是本发明实施例1中外消旋体3的13c-nmr图谱(100mhz);
图22是本发明实施例1中外消旋体3的二维相核磁共振(cosynmr)图谱;
图23是本发明实施例1中外消旋体3的异核单量子相干核磁共振(hsqcnmr)图谱;
图24是本发明实施例1中外消旋体3的1h的异核多碳相关谱核磁共振(hmbcnmr)图谱;
图25是本发明实施例1中外消旋体3的旋转坐标系noe(roesynmr)图谱;
图26是本发明实施例1中外消旋体4的高分辨质谱(hr-esi-ms)图谱;
图27是本发明实施例1中外消旋体4的1h-nmr图谱(400mhz);
图28是本发明实施例1中外消旋体4的13c-nmr图谱(100mhz);
图29是本发明实施例1中外消旋体4的二维相核磁共振(cosynmr)图谱;
图30是本发明实施例1中外消旋体4的异核单量子相干核磁共振(hsqcnmr)图谱;
图31是本发明实施例1中外消旋体4的1h的异核多碳相关谱核磁共振(hmbcnmr)图谱;
图32是本发明实施例1中外消旋体4的旋转坐标系noe(roesynmr)图谱;
图33是本发明实施例1中外消旋体5的高分辨质谱(hr-esi-ms)图谱;
图34是本发明实施例1中外消旋体5的1h-nmr图谱(400mhz);
图35是本发明实施例1中外消旋体5的13c-nmr图谱(100mhz);
图36是本发明实施例1中外消旋体5的二维相核磁共振(cosynmr)图谱;
图37是本发明实施例1中外消旋体5的异核单量子相干核磁共振(hsqcnmr)图谱;
图38是本发明实施例1中外消旋体5的1h的异核多碳相关谱核磁共振(hmbcnmr)图谱;
图39是本发明实施例1中外消旋体5的旋转坐标系noe(roesynmr)图谱。
具体实施方式
下面对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例中未注明具体实验步骤或条件者,按照本领域内的文献所描述的常规实验步骤的操作或条件即可进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规试剂产品。下述实验用三叉苦[evodialepta(spreng.)merr.]茎采自广东省茂名市。
实验例1
一、实验目的
采用造模剂东莨菪碱诱导的sh-sy5y细胞模型,研究化合物的神经保护作用,以及氧化应激和炎症的影响,考察本发明化合物1-10的抗老年痴呆作用。
二、实验方法
1.实验材料
被测样品溶液的配制:受试样品为下述实施例1分离精制的纯品化合物1-10,分别精密称取化合物1-10溶解于dmso中,配制得分别含化合物1-10浓度均为30mm的母液,其中mm为mmol/l,将各化合物的母液分别用dmso稀释成如下浓度梯度的溶液,0.1nm、1nm、10nm、100nm,其中nm为nmol/l。
阳性对照溶液(多奈哌齐溶液)的配制:精密称取多奈哌齐溶解于dmso中,配制得含有多奈哌齐30mm的母液,分别用dmso稀释成如下浓度梯度的溶液,0.1nm、1nm、10nm、100nm。
2.细胞系及细胞的传代培养
人神经母细胞瘤细胞sh-sy5y细胞购自atcc细胞库。细胞的复苏:从液氮中取出冻存管,立即放入37℃水浴锅中迅速摇动至冻存液完全溶解,在5min内完成复温;在超净台中移入离心管,加入5mldmem培养液,混匀;400g,离心5min,弃上清;再在细胞沉淀中加入新的dmem完全培养液,轻轻混匀,移入培养瓶内加足量dmem培养液,放置37℃,5%的co2的培养箱中培养。
细胞的传代:用含10%灭活fbs的dmem培养液在环境为37℃,含5%的co2细胞培养箱中培养sh-sy5y细胞。
3.活力测试方法
样品对东莨菪碱诱导的细胞损伤的保护作用采用mtt方法测定,将对数期的sh-sy5y细胞重悬后以5×103个/孔接种于96孔板中培养24h,每孔200μl,随机分为化合物1-10组、阳性对照组、空白对照组和东莨菪碱模型组。化合物1-10组每孔加入上述配制的分别含化合物1-10的不同浓度的被测样品溶液20μl,阳性对照组每孔分别加入上述配制的不同浓度的多奈哌齐溶液20μl,空白对照组和东莨菪碱模型组则每孔加入dmso各20μl,继续37℃培养24h,化合物1-10组、东莨菪碱模型组和阳性对照组细胞每孔均加入含东莨菪碱2mmol/l的东莨菪碱水溶液20μl,在37℃,5%co2的二氧化碳培养箱中继续培养24h,每孔加入mtt14μl,再孵育3h,然后除去培养液,每孔加150μldmso在振荡器上振荡10min,使结晶物充分溶解。在振荡器上振荡混匀让还原产物充分溶解。选择570nm波长,在酶联免疫监测仪上测定各孔光吸收值(a值),实验中样品和空白对照组均分别设六个平行孔,取a值平均值,按公式细胞抑制率(%)=[1-(化合物1-10组a值/空白对照组a值)]×100%计算细胞抑制率,然后计算ec50。每次实验重复三次。
4.乙酰胆碱酯酶活性测定:按照上述步骤1制备化合物1-10的浓度为0.1nm、1nm、10nm、100nm的待测样品溶液,按照步骤2和3的方法处理sh-sy5y细胞,并收集空白对照组、东莨菪碱模型组、阳性对照组和化合物1-10组细胞在上述步骤3中加入mtt之前的细胞及细胞培养液,离心,取细胞培养液上清液,使用ache试剂盒(南京建成生物工程研究所)按照试剂盒说明书中的方法测试各组细胞培养液上清液中乙酰胆碱酯酶的活性。
5.氧化应激测定、白细胞介素1β(il-1β)和白细胞介素-6(il-6)的测定:根据细胞活力测定结果,参照步骤1中“被测样品溶液的配制”分别制备化合物1-10的ec50浓度的样品溶液及ec50浓度的多奈哌齐溶液,具体为将各化合物浓度为30mm的母液分别用dmso稀释成如下浓度的样品溶液,20.9nm(化合物1)、18.6nm(化合物2)、10.7nm(化合物3)、13.1nm(化合物4)、15.4nm(化合物5)、15.6nm(化合物6)、17.7nm(化合物7)、17.1nm(化合物8)、16.3nm(化合物9)、15.9nm(化合物10);将多奈哌齐浓度为30mm的母液用dmso稀释成16.9nm。按照步骤2的方法培养sh-sy5y细胞,将对数期的sh-sy5y细胞重悬后以5×103个/孔接种于96孔板中培养24h,每孔200μl,随机分为化合物1-10组、阳性对照组、空白对照组和东莨菪碱模型组。化合物1-10组每孔加入分别上述配制的ec50浓度的样品溶液20μl,阳性对照组每孔分别加入上述配制的16.9nm的多奈哌齐溶液20μl,空白对照组和东莨菪碱模型组则每孔加入dmso各20μl,继续37℃培养24h,化合物1-10组、东莨菪碱模型组和阳性对照组细胞每孔均加入2mmol/l的东莨菪碱水溶液20μl,在37℃,5%co2的二氧化碳培养箱中继续培养24h,收集细胞及细胞培养液,离心,取细胞培养液上清液。
分别取细胞培养液上清液使用mda试剂盒(南京建成生物工程研究所)按照试剂盒说明书记载的方法测试各组细胞培养液上清液中丙二醛(mda)的含量;使用sod酶活性试剂盒(南京建成生物工程研究所)按照试剂盒说明书记载的方法测试各组细胞培养液上清液中超氧化物歧化酶(sod)活性;使用il-1β,il-6elisa试剂盒(thermofisherscientific),采用elasa测定法,按照试剂盒说明书记载的方法分别测试各组细胞培养液上清液中il-1β,il-6含量。
6.统计分析:上述检测结果用平均值±sem表示,待测样品组和空白对照组数据进行统计数据学分析,p<0.05表示具有显著性差异。
二、实验结果
1.细胞活力测试结果
表1细胞活力测试结果表
1ec50:半最大效应浓度。
结果见表1所示,表明化合物化合物1-10能够保护东莨菪碱诱导的细胞损伤,其ec50浓度最小为13.1±0.7μm。表明该化合物具有神经保护的作用。
2.乙酰胆碱酯酶活性测试结果
结果见表2所示,以上实验结果表明,相比于东莨菪碱模型组,化合物化合物1-10能够抑制东莨菪碱诱导的乙酰胆碱酯酶活性明显上升,其ic50浓度最小为7.3±0.7nm,表明该化合物具有抑制乙酰胆碱酯酶活性的作用。
表2乙酰胆碱酯酶活性的结果表
1ic50:半抑制浓度。
3.氧化应激测试结果
结果见图1所示,式1-式10对应于化合物1-10,实验结果表明相比于东莨菪碱模型组,化合物化合物1-10能够明显缓解东莨菪碱诱导的mda水平的升高程度,同时能够提升东莨菪碱诱导的抗氧化酶sod活性的下降程度。表明该化合物具有提高抗氧化能力的作用。
4.神经炎症测试结果
结果见图2所示,式1-式10对应于化合物1-10,实验结果表明,相比于东莨菪碱模型组,化合物化合物1-10能够明显缓解东莨菪碱诱导的il-1β和il-6水平的升高程度。表明该化合物具有抗炎的作用。
图1-2中,**表示与空白对照组相比具有显著性差异,p<0.01,##表示与东莨菪碱模型组相比具有显著性差异,p<0.01。
综上所述,本发明所提供的化合物化合物1-10对于东莨菪碱诱导的老年性痴呆模型的神经细胞具有保护用,能够抑制乙酰胆碱酯酶活性,而且具有抗炎、抗氧化的作用。
实施例1化合物1-10的制备
(1)取三叉苦茎,加入三叉苦茎重量的12倍的体积比为70%的乙醇水溶液回流提取一次,在92℃下热回流时间2h,收集乙醇提取液;残留的药渣加入三叉苦根重量的10倍的体积比为70%的乙醇水溶液回流提取一次,在92℃下热回流时间2h,收集乙醇提取液;残留的药渣加入三叉苦根重量的8倍的体积比为70%的乙醇水溶液回流提取一次,热回流时间2h,收集乙醇提取液;合并乙醇提取液,减压浓缩至无醇味,得乙醇浸膏4kg。
(2)将乙醇浸膏4kg用蒸馏水溶解后,依次用石油醚、乙酸乙酯、正丁醇萃取,回收乙酸乙酯萃取物(即本发明的提取物)。
(3)将乙酸乙酯萃取物上硅胶色谱柱分离,以环己烷/乙酸乙酯的体积比为100∶1、5∶1、10∶1、20∶1、50∶1、0∶1六个梯度进行洗脱,每500ml接受一个流份,共接收10个流份,分别记为fr-1到fr-10。取fr-4(为环己烷/乙酸乙酯的体积比为5∶1的流份)进行mci柱层析分离,以甲醇/水的体积比为2∶3、1∶1、3∶2、1∶0四个梯度进行洗脱,每500ml接受一个流份,共接收7个流份,分别记为fr-4-1到fr-4-7。取fr-4-5(为甲醇/水的体积比为1∶1的流份)进行反向ods柱层析分离,以甲醇/水的体积比为3∶2、7∶3、8∶2、0∶1四个梯度进行洗脱,每400ml接受一个流份,共接收8个流份,分别记为fr-4-5-1到fr-4-5-8。取流份fr-4-5-5(为甲醇/水的体积比为8∶2的流份)经过一次sephadexlh-20柱层析分离,以甲醇为洗脱剂洗脱,每500ml接受一个流份,共接收5个流份,分别记为fr-4-5-5-1到fr-4-5-5-5。
(4)取fr-4-5-5-4用hplc分离精制,采用体积份数为70%的乙腈水溶液为流动相,流速为7.0ml/min,检测波长为210nm,得到外消旋体1~外消旋体5,经旋光测定,外消旋体1~外消旋体5均为外消旋体。
(5)取外消旋体1用手性hplc柱进行拆分,采用体积份数为70%的乙腈水溶液为流动相,流速为7.0ml/min,检测波长为210nm,得到化合物1(12mg)和化合物2(17mg);取外消旋体2用手性hplc柱进行拆分,采用体积份数为70%的乙腈水溶液为流动相,流速为7.0ml/min,检测波长为210nm,得到化合物3(14mg)和化合物4(28mg);取外消旋体3用手性hplc柱进行拆分,采用体积份数为90%的乙腈水溶液为流动相,流速为7.0ml/min,检测波长为210nm,得到化合物5(39mg)和化合物6(15mg);取外消旋体4用手性hplc柱进行拆分,采用体积份数为90%的乙腈水溶液为流动相,流速为7.0ml/min,检测波长为210nm,得到化合物7(18mg)和化合物8(19mg);取外消旋体5用手性hplc柱进行拆分,采用体积份数为70%的乙腈水溶液为流动相,流速为7.0ml/min,检测波长为210nm,得到化合物9(26mg)和化合物10(33mg)。
实施例2外消旋体1-5以及化合物1-10的表征
外消旋体1为白色无定形粉末,hr-esi-ms图谱给出准分子离子峰m/z457.1649[m+h]+(calcd.for457.1651),结合13cnmr谱推断化合物1与化合物2的分子式为c28h24o6。紫外光谱(uv)显示有香豆素特征吸收(λmax202nm,246nm,333nm);红外光谱(ir)显示有羟基吸收(3647cm-1),羰基吸收(1716cm-1)。
1h-nmr谱中,在低场区观察到一组香豆素母核的特征氢信号:δh6.10(1h,d,j=9.4hz,h-3)与δh7.79(1h,d,j=9.4hz,h-4);一组e构型的双键质子信号:δh5.96(1h,d,j=16.4hz,h-9′)与δh6.71(1h,d,j=16.4hz,h-10′);此外,低场区还存在两个烯氢质子信号:δh5.30(1h,brs,h-10)和δh7.56(1h,s,h-4′);及一组苯环为abx系统的质子信号:δh7.38(1h,d,j=8.5hz,h-5′),6.75(1h,dd,j=8.5,2.3hz,h-6′)和6.64(1h,d,j=2.3hz,h-8′)。13c-nmr谱显示有28个碳信号,包括2个甲基,2个亚甲基,12个次甲基,14个季碳,进一步分析hsqc谱数据,提示可能存在两个香豆素单元。
在1h-1hcosynmr谱中,存在五组质子耦合系统:h-3与h-4,h-5′与h-6,h-9与h-10,h-5′与h-6′,h-12与h-12′,结合hmbc中多个相关信号:h-3、h-8与c-4a,h-4与c-2、c-8a,h-8与c-6,确定了该化合物中其中一个香豆素单元(unita)结构单元;根据另外几个hmbc中相关信号:h-3′、h-8′与c-4a′,h-4′与c-2′、c-8a′,h-8′与c-6′,亦确定了该化合物的另一香豆素单元(unitb)。依据三组质子耦合系统:h-9与h-10,h-9′与h-10′,h-12与h-12′;以及hmbc谱中的四组相关信号:h-9和c-11,h3-13和c-10,c-12,h-9′和c-11′,h-10′和c-12′,c-13′,提示该化合物存在可能存在一个六元环,且分别在c-11′和c-11连有一个甲基,c-11′连有一个乙烯基,从而确定了另一结构单元(unitc)。最后,通过hmbc谱中的两组相关信号:h-5和c-9,h-9′与c-11′、c-4′,最终确定了三个结构单元的连接方式,既unita与unitc通过c-6与c-9形成的一个碳单键相连,而unitb与unitc通过c-3′与c-9′形成的一个碳单键相连。
在roesynmr谱中观察到一组相关信号:h-9与h3-13′,从而确定了化合物1与化合物2的相对构型(9r,11′r或9s,11′s),最后通过实施例1步骤(5)的手性柱对外消旋体1进行手性拆分,得到一对对映异构体,并通过比较它们ecd的实验值和计算值(图10和11)确定了绝对构型:化合物1为9r,11'r[(+)-化合物1],化合物2为9s,11's[(–)-化合物2],分别将它们命名为(+)-dievodialetinc,(–)-dievodialetinc。
表3外消旋体1-3的1hnmr和13cnmr数据(cd3od,j=hz)
表4外消旋体4-5的1hnmr和13cnmr数据(cd3od,j=hz)
外消旋体2为白色无定形粉末,hr-esi-ms给出准分子离子峰m/z457.1648[m+h]+(calcd.for457.1651),结合13cnmr谱推断分子式为c28h24o6,提示其与化合物1和2互为同分异构体。紫外光谱(uv)显示有香豆素特征吸收(λmax244nm和328nm);红外光谱(ir)显示有羟基吸收(3647cm-1),羰基吸收(1716cm-1)。
1h-nmr谱中,低场区观察到两个烯氢质子信号:δh5.29(1h,brs,h-10)和δh7.69(1h,s,h-4′);及两组苯环为abx系统的质子信号:δh7.42(1h,d,j=8.5hz,h-5′)、6.76(1h,dd,j=8.5,2.3hz,h-6′)、6.65(1h,d,j=2.2hz,h-8′),和δh7.38(1h,d,j=8.5hz,h-5)、6.71(1h,dd,j=8.5,2.3hz,h-6)、6.60(1h,d,j=2.3hz,h-8)。13c-nmr谱显示该化合物有28个碳,有2个甲基,2个亚甲基,12个次甲基,14个季碳。
在1h-1hcosynmr谱中,存在5组质子耦合系统:h-5与h-6,h-5′与h-6′,h-9与h-10,h-9′与h-10′,h-12与h-12′;结合hmbc谱确定了unita和unitb两个结构单元。依据hmbc中四组相关信号:h-9和c-11,h3-13和c-10,c-12,h-9′和c-11′,h-10′和c-12′,c-13′,确定了unitc结构单元;以上nmr信息进一步证明了,外消旋体2与外消旋体1互为同分异构体,都含有unita、unitb和unitc三个结构单元,但是它们的连接方式不同,最后根据hmbc中两组相关信号:h-4和c-9,h-9′和c-4′与c-2′,最终确定了三个结构单元的连接方式。
同样,在roesynmr谱中,存在一组相关信号:h-9与h3-13′,即化合物3和化合物4的相对构型与化合物1和化合物2一样(9r,11′r或9s,11′s),分别将它们命名为(+)-dievodialetind,(–)-dievodialetind。
外消旋体3为白色无定形粉末,hr-esi-ms给出准分子离子峰m/z457.1642[m+h]+(calcd.for457.1642),结合13cnmr谱推断分子式为c28h24o6,提示提示其与化合物1-4互为同分异构体。紫外光谱(uv)显示有香豆素特征吸收(λmax201nm,255nm,329nm);红外光谱(ir)显示有羟基吸收(3647cm-1)及羰基吸收(1716cm-1)。
1h-nmr谱中,低场区有一组香豆素母环的特征质子信号:δh6.18(1h,d,j=9.4hz,h-3′)与δh7.89(1h,d,j=9.4hz,h-4′);两个烯氢质子信号:δh5.31(1h,d,h-10)和δh7.55(1h,s,h-4);一组苯环abx系统的质子信号:δh7.44(1h,d,j=8.5hz,h-5)、6.77(1h,dd,j=8.5,2.3hz,h-6)、6.67(1h,d,j=2.3hz,h-8)。13c-nmr谱显示该化合物亦有28个碳,有2个甲基,2个亚甲基,12个次甲基,14个季碳。
在1h-1hcosy谱中,存在5组质子耦合系统:h-5与h-6,h-3′与h-4′,h-9与h-10,h-9′与h-10′,h-12与h-12′;结合hmbc谱确定了unita和unitb两个结构单元。依据hmbc中四组相关信号:h-9和c-11,h3-13和c-10,c-12,h-9′和c-11′,h-10′和c-12′,c-13′,确定了unitc结构单元;以上nmr信息也进一步证明了提示其与外消旋体1互为同分异构体,且含有unita、unitb和unitc三个单元,也是在连接方式存在差异,最后据hmbc中两组相关信号:h-4和c-9,h-9′和c-2′、c-4′,最终确定了三个结构单元的连接方式。
在roesynmr谱中的一组相关信号(h-9与h3-13′),亦提示化合物5和化合物6相对构型与化合物1和化合物2一样(9r,11′r或9s,11′s),分别将它们命名为(+)-dievodialetine,(–)-dievodialetine。
外消旋体4为白色无定形粉末,hr-esi-ms给出准分子离子峰m/z457.1642[m+h]+(calcd.for457.1651),13cnmr谱推断分子式为c28h24o6,提示其与化合物1-6互为同分异构体。紫外光谱(uv)显示有香豆素特征吸收(λmax201nm,299nm,327nm);红外光谱(ir)显示有羟基吸收(3647cm-1)及羰基吸收(1716cm-1)。
1h-nmr谱中,低场区显示存在一组香豆素母环的特征质子信号:δh6.11(1h,d,j=9.4hz,h-3′)与7.58(1h,d,j=9.4hz,h-4′);一组烯氢质子信号:δh6.26(1h,d,j=12.8hz,h-9′)与5.76(1h,d,j=12.8hz,h-10′);两个烯氢质子信号:δh5.13(1h,brs,h-10)和7.43(1h,s,h-4);及一组苯环为abx系统的质子信号:δh7.39(1h,d,j=8.5hz,h-5)、6.76(1h,dd,j=8.5,2.3hz,h-6)和6.72(1h,d,j=2.3hz,h-8)。13c-nmr谱显示该化合物有28个碳,有2个甲基,2个亚甲基,12个次甲基,14个季碳。
在1h-1hcosy谱中,观察到5组质子耦合系统:h-5与h-6,h-3′与h-4′,h-9与h-10,h-9′与h-10′,h-12与h-12′,结合hmbc谱确定了unita和unitb两个结构单元。依据hmbc中三组相关信号:h-9和c-11,h3-13和c-10,c-12,h-10′和c-12′,c-9,确定了unitc结构单元。综上nmr信息可知,化合物7与化合物8也是由unita、unitb和unitc三个结构单元组成,最后据hmbc中两组相关信号:h-4和c-9,h-9′和c-5′,确定了三个结构单元的连接方式与外消旋体3相同,唯一的区别是外消旋体4的h-9′与h-10′的耦合常数(j=12.8hz),提示该位置为z构型,因此,它们是一对互为z/e异构(或顺反异构)的香豆素二聚体。
roesynmr谱中的一组相关信号(h-9与h3-13′)亦提示化合物7与化合物8的相对构型与化合物1与化合物2一样,同为9r,11′r或9s,11′s,分别将它们命名为(+)-dievodialetinf,(–)-dievodialetinf。
外消旋体5为白色无定形粉末,hr-esi-ms图谱给出准分子离子峰m/z457.1647[m+h]+(calcd.for457.1651),结合13cnmr谱推断分子式为c28h24o6,提示化合物9与化合物10和化合物1-8均互为同分异构体。紫外光谱(uv)显示有香豆素特征吸收(λmax203nm,300nm,329nm);红外光谱(ir)显示有羟基吸收(3647cm-1)及羰基吸收(1716cm-1)。
1hnmr谱中,低场观察到两组香豆素母环的特征质子信号:δh6.20(1h,d,j=9.4hz,h-3)、7.88(1h,d,j=9.4hz,h-4),和δh6.13(1h,d,j=9.4hz,h-3)、7.46(1h,d,j=9.4hz,h-4);一组烯氢质子信号:δh6.04(1h,d,j=12.8hz,h-9)和5.78(1h,d,j=12.8hz,h-10),其h-9和h-10的耦合常数(j=12.8hz)提示外消旋体5与外消旋体4同为z构型。13c-nmr谱显示该化合物有28个碳,有2个甲基,2个亚甲基,12个次甲基,14个季碳。
在1h-1hcosy谱中,存在5组质子耦合系统:h-3与h-4,h-3与h-4,h-9与h-10,h-9与h-10,h-12与h-12;结合hmbc谱确定了unita和unitb两个结构单元。依据hmbc中三组相关信号:h-9和c-11,h3-13和c-10,c-12,h-10和c-12,c-9,从而确定了c结构单元,以上nmr信息进一步证明了外消旋体5与外消旋体1互为同分异构体,且都含有unita、unitb和unitc三个结构单元,最后据hmbc中两组相关信号:h-5和c-9,h-9和c-5,最终确定了三个结构单元的连接方式。
roesynmr谱中存在的一组相关信号(h-9与h3-13),提示化合物9与化合物10相对构型与化合物1和化合物2一样,亦为9r,11'r或9s,11's,分别将它们命名为(+)-dievodialetinf,(–)-dievodialetinf。
其中,外消旋体1-5的13c-nmr图谱上有1个或者2个数据被峰遮挡,该峰为溶剂峰,对本申请技术内容无影响。
制剂实验例1(注射剂的制备)
取1000mg上述实施例1得到的化合物1-10,分别加1000ml的注射用水,用碳酸钠调ph值至7,搅拌使溶解,除菌滤过,灌封,经100℃15分钟流通蒸汽灭菌,分别制成每支分别含1mg/ml的化合物1-10的注射液供注射使用。
制剂实验例2:(胶囊剂的制备)
化合物可以选用实施例1制得的化合物1-10中的一种或者多种,本实施例采用化合物3,按上述配方的重量称量实施例1制得的化合物3,分别称量微晶纤维素、羧甲基淀粉钠、十二烷基硫酸钠混合,采用辊压法进行干法制粒,再与硬脂酸镁混匀,填充入3#空心胶囊,分别制成含实施例制得的化合物100mg/粒的胶囊剂,供口服使用。
制剂实验例3:(片剂的制备)
化合物可以选用实施例1制得的化合物1-10中的一种或者多种,本实施例采用化合物1,按上述配方的重量称量实施例1得到的化合物1、淀粉、交联pvp、羧甲基淀粉钠、硬脂酸镁混合,加入5%pvp-乙醇溶液(乙醇与水的体积百分数为75∶25),制软材,以18目筛制粒,60℃干燥后1h,20目整粒后加入滑石粉,混匀,压片,制成规格为含化合物1100mg/片的片剂,供口服使用。
显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本发明创造的保护范围之中。
- 还没有人留言评论。精彩留言会获得点赞!