基于CLEC9A的嵌合蛋白复合物的制作方法
基于clec9a的嵌合蛋白复合物
1.相关申请的交叉引用
2.本技术要求2019年9月26日提交的美国临时专利申请号62/906,442和2019年3月28日提交的美国临时专利申请号62/825,584的权益和优先权,所述申请的内容特此以引用方式整体并入。
技术领域
3.本发明部分地涉及嵌合蛋白复合物,所述嵌合蛋白复合物包括片段可结晶结构域(fc)、作为靶向部分的clec9a vhh和作为信号传导剂的经修饰的干扰素α2(ifnα2)。还公开了这些嵌合蛋白复合物作为治疗剂的用途。
4.序列表
5.本技术包含已通过efs
‑
web以ascii格式提交的序列表,所述序列表特此以引用方式整体并入。所述ascii副本创建于2020年3月26日,名称为orn
‑
063pc_st25.txt且大小为139,264字节。
背景技术:
6.具有效应功能的生物制剂是一类具有许多潜在治疗应用的生物制剂。在一些情况下,这些生物制剂,例如细胞因子,在施用至人体时编码一种效应功能,这种效应功能可能会产生全身毒性。因此,使这些生物制剂在人体中的耐受性和治疗指数最大化至关重要,以便可降低人体或受试者的全身毒性。
7.通常,需要将这些生物制剂以高精度且以调控方式递送至受试者体内的其一个或多个靶标处以便使这些生物制剂有效。因此,需要具有高固有安全特性、能够以高精度到达受试者体内靶标并能够以调控方式发挥功能的工程化生物分子。
8.此类生物制剂的一个实例是具有连接至靶向元件(能够以高精度寻找其靶标)的信号传导剂(具有效应功能,例如细胞因子)的嵌合蛋白。在这些生物制剂中,信号传导剂可以是野生型信号传导剂或经修饰的信号传导剂(例如通过突变)。经修饰的信号传导剂一般经过修饰以引起信号传导剂的活性的减弱(例如,基本上降低其与其受体相互作用/接合的能力),以这样的方式使得信号传导剂的效应功能可以在靶向元件与其靶标(例如靶细胞上的抗原)结合后得以恢复。
9.然而,此类嵌合蛋白仅在某些条件得到满足时才适合治疗用途,例如能够大规模生产,体内半衰期确保有足够的时间暴露于药物以引发治疗有益效果,大小适当以避免快速清除或有限的组织穿透性和生物分布,以及有确保足够的溶解性、稳定性和储存特性的其他特性而不显著丧失功能。重要的是,上述特性中的全部或基本上大部分应当在不丧失效应功能的条件性靶向并保持经修饰的信号传导剂与其受体的条件性接合的情况下实现。通常,用由单一连续多肽链编码或表现的嵌合蛋白很难实现所有这些目标。在本领域中需要在维持生物制剂的耐受性和治疗指数的同时实现生物制剂的此类期望特性。
技术实现要素:
10.本发明技术提供了嵌合蛋白复合物,所述嵌合蛋白复合物包括生物治疗剂,所述生物治疗剂的效应功能可以高度精确的方式递送至所选择的靶标,交叉反应性有限或无,且系统性不良事件有限或无,同时还提供了赋予药物特性的功能,使得能够生产具有所期望的体内暴露时间(例如半衰期)、尺寸(例如,用于生物分布和清除特征),以及供商业生产的大生产和/或纯化规模的治疗剂(例如,具有足够的溶解性、稳定性和储存特性)。
11.在一方面,本发明涉及一种异源二聚体蛋白复合物及其个别多肽链亚基(组分),并且其中所述蛋白复合物包括特异性地结合至c型凝集素结构域家族9成员a(clec9a)的靶向部分、经修饰的人ifnα2和经修饰的fc结构域。
12.在一方面,本发明涉及一种嵌合蛋白复合物,所述嵌合蛋白复合物包含:(i)特异性地结合至c型凝集素结构域家族9成员a(clec9a)的靶向部分,(ii)经修饰的人ifnα2,和(iii)经修饰的fc结构域。
13.在一方面,本发明涉及一种嵌合蛋白复合物,其中所述嵌合蛋白复合物包括特异性地结合至c型凝集素结构域家族9成员a(clec9a)的靶向部分、经修饰的人ifnα2和经修饰的fc结构域。
14.在一些实施方案中,所述嵌合蛋白复合物包含与seq id no:1
‑
4和43中的任一者具有至少95%同一性或与seq id no:1
‑
4和43中的任一者具有至少98%同一性或与seq id no:1
‑
4和43中的任一者具有至少99%同一性的多肽。在一些实施方案中,所述嵌合蛋白复合物包含seq id no:1
‑
4和43中的任一者的多肽,任选地具有0个、或1个、或2个、或3个、或4个、或5个突变。在一些实施方案中,所述嵌合蛋白复合物包含seq id no:1
‑
4和43中的任一者的多肽。
15.在一些实施方案中,所述嵌合蛋白复合物包含并入与seq id no:1
‑
4和43中的任一者具有至少95%同一性或与seq id no:1
‑
4和43中的任一者具有至少98%同一性的连续氨基酸序列的多肽。
16.在另一方面,本发明涉及一种治疗或预防癌症的方法,所述方法包括向有需要的患者施用有效量的如本文所公开的嵌合蛋白复合物。
17.本发明的另一方面涉及一种包含如本文所公开的嵌合蛋白复合物和药学上可接受的载体的药物组合物。在另一方面,本发明涉及一种用于治疗或预防癌症的方法,所述方法包括向有需要的患者施用有效量的如本文所公开的药物组合物。在另一方面,本发明涉及一种重组核酸组合物,所述重组核酸组合物编码本文所公开的嵌合蛋白复合物的一个或多个多肽链亚基。在另一方面,本发明涉及一种宿主细胞,所述宿主细胞包含编码本文所公开的一种或多种嵌合蛋白复合物的核酸组合物。
附图说明
18.图1示出了本发明的嵌合蛋白复合物的各个非限制性说明性示意图。在多个实施方案中,每个示意图是本发明的组合物。此处“ifn”是指如本文所描述的ifnα2;“vhh”是指如本文所描述的抗clec9avhh;是如本文所描述的任选的“接头”;并且两个长平行矩形(其中一个具有突出部,另一个具有低凹部)是来自igg1的人fc结构域,具有如本文所描述的旋钮入孔洞突变,并且任选地具有同样如本文所描述的效应子敲除和/或稳定化突变。
尽管示出了seq id no,但这些仅是说明性的,例如如果使用如本文所描述的除r149a之外的替代突变,它们将改变。
19.图2示出了在小鼠中静脉内施用后的fc
‑
afn的血浆浓度。绘制每个时间点时间的3个单独样品的平均值(+sem)。
20.图3示出了在小鼠中静脉内施用后的clec9a afn(缺乏fc的构建体)的血浆浓度。绘制每个时间点时间的3个单独样品的平均值(+sem)。
21.图4a至图4d示出了与对照细胞(hl116和hek293t)相比,clec9a
‑
afn fc构建体与表达人clec9a(hl116
‑
hclec9a)的细胞的特异性结合。
22.图5示出了用缓冲液或四种不同的clec9a
‑
afn fc构建体治疗后的人源化小鼠中的肿瘤生长曲线。绘制了每个时间点时间的5只动物的平均值(mm3)(+sem)。
23.图6示出了用缓冲液或增加剂量的单一clec9a
‑
afn fc构建体治疗后的人源化小鼠中的肿瘤生长曲线。绘制了每个时间点时间的5只动物的平均值(mm3)(+sem)。
24.图7示出了本发明所涵盖的各种二价取向和/或构型。实现二价的第二vhh部分加阴影显示并与连接的接头一起形成图中提到的seq id的n端或c端延伸。尽管示出了seq id no,但这些仅是说明性的,例如如果使用如本文所描述的除r149a之外的替代突变,它们将改变。此外,vhh可以是相同的。有关说明参见图1描述。
25.图8a示出了ifna2在clec9a
‑
/cd141
‑
和clec9a+/cd141+pbmc中的pstat1磷酸化的结果。
26.图8b示出了具有a145g或m148a突变的afn在clec9a
‑
/cd141
‑
和clec9a+/cd141+pbmc中的pstat1磷酸化的结果。
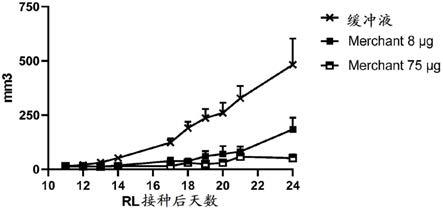
27.图9示出了用缓冲液或7.5μg剂量的两种不同的clec9a
‑
afn fc构建体治疗后的人源化小鼠中的肿瘤生长曲线。绘制每个时间点时间的6只动物的肿瘤大小(mm3)的平均值(+sem)。
28.图10a至图10c示出了用具有ifna2中的t106 o
‑
糖基化的clec9a靶向的afn(图10a)和没有ifna2中的t106 o
‑
糖基化的clec9a靶向的afn(图10b)以及未靶向变体(图10c)治疗后clec9a
‑
/cd141
‑
和clec9a+/cd141+pbmc中的pstat1活性。
29.图11示出了具有ifnα2的a145g突变的clec9a靶向的afn fc的抗肿瘤活性。
具体实施方式
30.在一方面,本发明涉及一种嵌合蛋白复合物,其中所述嵌合蛋白复合物包括特异性地结合至c型凝集素结构域家族9成员a(clec9a)的靶向部分、经修饰的人ifnα2和经修饰的fc结构域。在多个实施方案中,所述嵌合蛋白复合物包含与seq id no:1
‑
4和43中的任一者具有至少95%同一性的多肽。在多个实施方案中,所述嵌合蛋白复合物包含与seq id no:1
‑
4和43中的任一者具有至少98%同一性或与seq id no:1
‑
4和43中的任一者具有至少99%同一性的多肽。在多个实施方案中,所述嵌合蛋白复合物包含seq id no:1
‑
4和43的多肽,其中与所选序列相比,所述序列具有少于10个突变。在多个实施方案中,所述嵌合蛋白复合物包含seq id no:1
‑
4和43的多肽,其中与所选序列相比,所述序列具有少于5个突变。
31.在多个实施方案中,所述嵌合蛋白复合物包含具有氨基酸序列seq id no:1的多肽。该序列包括针对clec9a的单结构域抗体(vhh)(即,r1chcl50(opt4))、接头(即,5*ggs)
和具有lala
‑
kq突变的fc孔洞ridgway序列(即,fc孔洞ridgway(lala
‑
kq),参见ridgway等人,protein engineering 1996;9:617
‑
621,所述文献以引用方式整体并入)。具有序列seq id no:1的这种构建体表示如下:变型1vhh
‑
fc r1chcl50(opt4)
‑
5*ggs
‑
fc孔洞ridgway(lala
‑
kq)。
32.在多个实施方案中,所述嵌合蛋白复合物包含具有氨基酸序列seq id no:2的多肽。该序列包括针对clec9a的单结构域抗体(vhh)(即,r1chcl50(opt4))、接头(即,5*ggs)和具有lala
‑
kq突变的fc孔洞merchant序列(即,fc孔洞merchant(lala
‑
kq),参见merchant等人,nature biotechnology 1998;16:677
‑
681,所述文献以引用方式整体并入)。具有seq id no:2的这种构建体表示如下:vhh
‑
fc:r1chcl50(opt4)
‑
5*ggs
‑
fc孔洞merchant(lala
‑
kq)。
33.在多个实施方案中,所述嵌合蛋白复合物包含具有氨基酸序列seq id no:3的多肽。该序列包括针对clec9a的单结构域抗体(vhh)(即,3lec89(opt4))、接头(即,5*ggs)和具有lala
‑
kq突变的fc孔洞ridgway序列(即,fc孔洞ridgway(lala
‑
kq),参见ridgway等人,protein engineering 1996;9:617
‑
621,所述文献以引用方式整体并入)。具有seq id no:3的这种构建体表示如下:vhh
‑
fc:3lec89(opt4)
‑
5*ggs
‑
fc孔洞ridgway(lala
‑
kq)。
34.在多个实施方案中,所述嵌合蛋白复合物包含具有氨基酸序列seq id no:4的多肽。该序列包括针对clec9a的单结构域抗体(vhh)(即,3lec89(opt4))、接头(即,5*ggs)和具有lala
‑
kq突变的fc孔洞merchant序列(即,fc孔洞merchant(lala
‑
kq),参见merchant等人,nature biotechnology 1998;16:677
‑
681,所述文献以引用方式整体并入)。具有seq id no:4的这种构建体表示如下:vhh
‑
fc:3lec89(opt4)
‑
5*ggs
‑
fc孔洞merchant(lala
‑
kq)。
35.在多个实施方案中,所述嵌合蛋白复合物包含具有氨基酸序列seq id no:43的多肽。该序列包括针对clec9a的单结构域抗体(vhh)(即,r1chcl50(opt4))、接头(即,5*ggs)和具有lala
‑
kq突变且无c端赖氨酸的fc孔洞merchant序列(即,fc孔洞merchant(lala
‑
kq),参见merchant等人,nature biotechnology1998;16:677
‑
681,所述文献以引用方式整体并入)。
36.本发明的嵌合蛋白复合物还可以包括与seq id no:5
‑
8、29
‑
36或41
‑
42中的任一者具有至少95%同一性的氨基酸序列。在多个实施方案中,所述嵌合蛋白复合物包含具有与seq id no:5
‑
8、29
‑
36或41
‑
42中的任一者具有至少98%同一性或与seq id no:5
‑
8、29
‑
36或41
‑
42中的任一者具有至少99%同一性的氨基酸序列的多肽。在多个实施方案中,所述嵌合蛋白复合物包含具有选自seq id no:5
‑
8、29
‑
36或41
‑
42的氨基酸序列的多肽,其中与所选序列相比,所述序列具有少于10个突变。在多个实施方案中,所述嵌合蛋白复合物包含具有选自seq id no:5
‑
8、29
‑
36或41
‑
42的氨基酸序列的多肽,其中与所选序列相比,所述序列具有少于5个突变。
37.在多个实施方案中,所述嵌合蛋白复合物包含具有氨基酸序列seq id no:5的多肽。该序列包括具有r149a突变的经修饰的人干扰素α2b(即,huifna2b_r149a)、接头(即,10*ggs
‑
g)和具有lala
‑
kq突变的fc旋钮ridgway序列(即,fc旋钮ridgway(lala
‑
kq),参见ridgway等人,protein engineering 1996;9:617
‑
621,所述文献以引用方式整体并入)。具有seq id no:5序列的这种构建体表示如下:变型1fc
‑
afn:fc旋钮ridgway(lala
‑
kq)
‑
10*
ggs
‑
g
‑
huifna2b_r149a。
38.在多个实施方案中,所述嵌合蛋白复合物包含具有氨基酸序列seq id no:6的多肽。该序列包括具有r149a和t106e突变的经修饰的人干扰素α2b(即huifna2b_r149a_t106e)、接头(即,10*ggs
‑
g)和具有lala
‑
kq突变的fc旋钮ridgway序列(即,fc旋钮ridgway(lala
‑
kq),参见ridgway等人,protein engineering 1996;9:617
‑
621,所述文献以引用方式整体并入)。具有seq id no:6序列的这种构建体表示如下:变型2fc
‑
afn:fc旋钮ridgway(lala
‑
kq)
‑
10*ggs
‑
g
‑
huifna2b_r149a_t106e。
39.在多个实施方案中,所述嵌合蛋白复合物包含具有氨基酸序列seq id no:7的多肽。该序列包括具有r149a突变的经修饰的人干扰素α2b(即,huifna2b_r149a)、接头(即,10*ggs
‑
g)和具有lala
‑
kq突变的fc旋钮merchant序列(即,fc旋钮merchant(lala
‑
kq),参见merchant等人,nature biotechnology1998;16:677
‑
681,所述文献以引用方式整体并入)。具有seq id no:7序列的这种构建体表示如下:变型3fc
‑
afn:fc旋钮merchant(lala
‑
kq)
‑
10*ggs
‑
g
‑
huifna2b_r149a。
40.在多个实施方案中,所述嵌合蛋白复合物包含具有氨基酸序列seq id no:8的多肽。该序列包括具有r149a和t106e突变的经修饰的人干扰素α2b(即,huifna2b_r149a_t106e)、接头(即,10*ggs
‑
g)和具有lala
‑
kq突变的fc旋钮merchant序列(即,fc旋钮merchant(lala
‑
kq),参见merchant等人,nature biotechnology1998;16:677
‑
681,所述文献以引用方式整体并入)。具有seq id no:8序列的这种构建体表示如下:变型4fc
‑
afn:fc旋钮merchant(lala
‑
kq)
‑
10*ggs
‑
g
‑
huifna2b_r149a_t106e。
41.在多个实施方案中,所述嵌合蛋白复合物包含具有氨基酸序列seq id no:41的多肽。该序列包括具有a145g突变的经修饰的干扰素α2b、接头(即,10*ggs
‑
g)和具有lala
‑
kq突变的fc旋钮merchant序列(即,fc旋钮merchant(lala
‑
kq),参见merchant等人,nature biotechnology 1998;16:677
‑
681,所述文献以引用方式整体并入)。具有序列seq id no:41的这种构建体表示如下:fc4
’‑
ifna2b_a145g。
42.在多个实施方案中,所述嵌合蛋白复合物包含具有氨基酸序列seq id no:42的多肽。该序列包括具有t106a和a145g突变的经修饰的干扰素α2b、接头(即,10*ggs
‑
g)和具有lala
‑
kq突变的fc旋钮merchant序列(即,fc旋钮merchant(lala
‑
kq),参见merchant等人,nature biotechnology 1998;16:677
‑
681,所述文献以引用方式整体并入)。具有序列seq id no:42的这种构建体表示如下:fc4
’‑
ifna2a_t106e_a145g。
43.在一个实施方案中,所述嵌合蛋白复合物包括:(i)与seq id no:1或3中的任一者具有至少95%同一性的氨基酸序列和(ii)与seq id no:5或6中的任一者具有至少95%同一性的氨基酸序列。在另一个实施方案中,所述嵌合蛋白复合物包括:(i)与seq id no:1或3中的任一者具有至少98%同一性的氨基酸序列和(ii)与seq id no:5或6中的任一者具有至少98%同一性的氨基酸序列。在另一个实施方案中,所述嵌合蛋白复合物包括:(i)与seq id no:1或3中的任一者具有至少99%同一性的氨基酸序列和(ii)与seq id no:5或6中的任一者具有至少99%同一性的氨基酸序列。在一个实施方案中,所述嵌合蛋白复合物包括:(i)与seq id no:2或4中的任一者具有至少95%同一性的氨基酸序列和(ii)与seq id no:7或8中的任一者具有至少95%同一性的氨基酸序列。在一个实施方案中,所述嵌合蛋白复合物包括:(i)与seq id no:2或4中的任一者具有至少98%同一性的氨基酸序列和(ii)与
seq id no:7或8中的任一者具有至少98%同一性的氨基酸序列。在另一个实施方案中,所述嵌合蛋白复合物包括:(i)与seq id no:2或4中的任一者具有至少99%同一性的氨基酸序列和(ii)与seq id no:7或8中的任一者具有至少99%同一性的氨基酸序列。
44.在一些实施方案中,所述嵌合蛋白复合物包含:(i)具有与seq id no:2具有至少95%同一性的氨基酸序列的多肽和(ii)具有与seq id no:31或32中的任一者具有至少95%同一性的氨基酸序列的多肽。在一些实施方案中,所述嵌合蛋白复合物包含:(i)具有与seq id no:2具有至少98%同一性的氨基酸序列的多肽和(ii)具有与seq id no:31或32中的任一者具有至少98%同一性的氨基酸序列的多肽。在多个实施方案中,所述嵌合蛋白复合物包含:(i)具有与seq id no:2具有至少99%同一性的氨基酸序列的多肽和(ii)具有与seq id no:31或32中的任一者具有至少99%同一性的氨基酸序列的多肽。在一些实施方案中,所述嵌合蛋白复合物包含:(i)具有与seq id no:43具有至少95%同一性的氨基酸序列的多肽和(ii)具有与seq id no:41或42中的任一者具有至少95%同一性的氨基酸序列的多肽。在一些实施方案中,所述嵌合蛋白复合物包含:(i)具有与seq id no:43具有至少98%同一性的氨基酸序列的多肽和(ii)具有与seq id no:41或42中的任一者具有至少98%同一性的氨基酸序列的多肽。在多个实施方案中,所述嵌合蛋白复合物包含:(i)具有与seq id no:43具有至少99%同一性的氨基酸序列的多肽和(ii)具有与seq id no:41或42中的任一者具有至少99%同一性的氨基酸序列的多肽。
45.在一些实施方案中,所述嵌合蛋白复合物包含:(i)具有与seq id no:1或3中的任一者具有至少95%同一性的氨基酸序列的多肽和(ii)具有与seq id no:5或6中的任一者具有至少95%同一性的氨基酸序列的多肽。
46.在一些实施方案中,所述嵌合蛋白复合物包含:(i)具有与seq id no:1或3中的任一者具有至少98%同一性的氨基酸序列的多肽和(ii)具有与seq id no:5或6中的任一者具有至少98%同一性的氨基酸序列的多肽。
47.在一些实施方案中,所述嵌合蛋白复合物包含:(i)具有与seq id no:1或3中的任一者具有至少99%同一性的氨基酸序列的多肽和(ii)具有与seq id no:5或6中的任一者具有至少99%同一性的氨基酸序列的多肽。
48.在一些实施方案中,所述嵌合蛋白复合物包含:(i)具有与seq id no:2或4中的任一者具有至少95%同一性的氨基酸序列的多肽和(ii)具有与seq id no:7或8中的任一者具有至少95%同一性的氨基酸序列的多肽。
49.在多个实施方案中,所述嵌合蛋白复合物包含:(i)具有与seq id no:2或4中的任一者具有至少98%同一性的氨基酸序列的多肽和(ii)具有与seq id no:7或8中的任一者具有至少98%同一性的氨基酸序列的多肽。
50.在多个实施方案中,所述嵌合蛋白复合物包含:(i)具有与seq id no:2或4中的任一者具有至少99%同一性的氨基酸序列的多肽和(ii)具有与seq id no:7或8中的任一者具有至少99%同一性的氨基酸序列的多肽。
51.在多个实施方案中,所述嵌合蛋白复合物包含:(i)具有与seq id no:2具有至少95%同一性的氨基酸序列的多肽和(ii)具有与seq id no:31或32中的任一者具有至少95%同一性的氨基酸序列的多肽。
52.在多个实施方案中,所述嵌合蛋白复合物包含:(i)具有与seq id no:2具有至少
98%同一性的氨基酸序列的多肽和(ii)具有与seq id no:31或32中的任一者具有至少98%同一性的氨基酸序列的多肽。
53.在多个实施方案中,所述嵌合蛋白复合物包含:(i)具有与seq id no:2具有至少99%同一性的氨基酸序列的多肽和(ii)具有与seq id no:31或32中的任一者具有至少99%同一性的氨基酸序列的多肽。
54.在多个实施方案中,所述嵌合蛋白复合物包含:(i)具有与seq id no:43具有至少95%同一性的氨基酸序列的多肽和(ii)具有与seq id no:41或42中的任一者具有至少95%同一性的氨基酸序列的多肽。
55.在多个实施方案中,所述嵌合蛋白复合物包含:(i)具有与seq id no:43具有至少98%同一性的氨基酸序列的多肽和(ii)具有与seq id no:41或42中的任一者具有至少98%同一性的氨基酸序列的多肽。
56.在一些实施方案中,所述嵌合蛋白复合物包含:(i)具有与seq id no:43具有至少99%同一性的氨基酸序列的多肽和(ii)具有与seq id no:41或42中的任一者具有至少99%同一性的氨基酸序列的多肽。
57.在一些实施方案中,本发明涉及一种多价或二价嵌合蛋白复合物,所述嵌合蛋白复合物包含:具有与氨基酸序列seq id no:17至少95%、或97%、或98%、或99%同一的序列的多肽和具有与氨基酸序列seq id no:7至少95%、或97%、或98%、或99%同一的序列的多肽;具有与氨基酸序列seq id no:2至少95%、或97%、或98%、或99%同一的序列的多肽和具有与氨基酸序列seq id no:19至少95%、或97%、或98%、或99%同一的序列的多肽;具有与氨基酸序列seq id no:18至少95%、或97%、或98%、或99%同一的序列的多肽和具有与氨基酸序列seq id no:7至少95%、或97%、或98%、或99%同一的序列的多肽;具有与氨基酸序列seq id no:20至少95%、或97%、或98%、或99%同一的序列的多肽和具有与氨基酸序列seq id no:7至少95%、或97%、或98%、或99%同一的序列的多肽;具有与氨基酸序列seq id no:2至少95%、或97%、或98%、或99%同一的序列的多肽和具有与氨基酸序列seq id no:22至少95%、或97%、或98%、或99%同一的序列的多肽;或具有与氨基酸序列seq id no:21至少95%、或97%、或98%、或99%同一的序列的多肽和具有与氨基酸序列seq id no:7至少95%、或97%、或98%、或99%同一的序列的多肽。在一些实施方案中,本发明涉及一种用于治疗或预防癌症的方法,所述方法包括向有需要的患者施用有效量的本文所描述的多价或二价嵌合蛋白复合物。
58.在一些实施方案中,本发明涉及一种嵌合蛋白复合物,所述嵌合蛋白复合物包含具有与seq id no:1
‑
43中的任一者的氨基酸序列至少95%、或97%、或98%、或99%、或100%同一的序列的至少两个多肽。在多个实施方案中,本发明涉及一种用于治疗或预防癌症的方法,所述方法包括向有需要的患者施用有效量的嵌合蛋白复合物,所述嵌合蛋白复合物包含具有与seq id no:1
‑
43中的任一者的氨基酸序列至少95%、或97%、或98%、或99%、或100%同一的序列的至少两个多肽。
59.在一些实施方案中,所述嵌合蛋白复合物包含经修饰的人干扰素α2。在多个实施方案中,所述经修饰的ifn
‑
α2剂对ifn
‑
α/β受体(ifnar),即ifnar1和/或ifnar2链具有降低的亲和力和/或活性。在一些实施方案中,所述经修饰的ifn
‑
α2剂对ifn
‑
α/β受体(ifnar),即ifnar1和/或ifnar2链具有基本上降低或消除的亲和力和/或活性。在一些实施方案中,
如本文所公开的经修饰的人干扰素α2具有与seq id no:9或10具有至少95%同一性的氨基酸序列。在其他实施方案中,所述经修饰的人ifnα2具有与seq id no:9或10具有至少98%或至少99%同一性的氨基酸序列。在一些实施方案中,相对于氨基酸序列seq id no:9或10,所述经修饰的人ifnα2具有1
‑
3个突变。在一个实施方案中,相对于seq id no:9或10,所述经修饰的人ifnα2包含r149a突变。在一个实施方案中,相对于seq id no:9或10,所述经修饰的人ifnα2包含a145g突变。
60.在一些实施方案中,本文所公开的嵌合蛋白复合物的靶向部分包含重组的只有重链的抗体(vhh)。在一些实施方案中,所述vhh具有与seq id no:11或12中的一者具有至少95%同一性的氨基酸序列。在其他实施方案中,所述vhh包含具有与seq id no:11或12中的一者具有至少98%同一性或与seq id no:11或12中的一者具有至少99%同一性的氨基酸序列。在一些实施方案中,所述vhh具有seq id no:11和12中的任一者的氨基酸序列。
61.在一些实施方案中,本文所公开的嵌合蛋白复合物包含两个靶向部分。在一些实施方案中,本文所公开的嵌合蛋白复合物包含两个相同的靶向部分。在多个实施方案中,这些二价模式的取向如图7中所示。
62.在一些实施方案中,本文所公开的嵌合蛋白复合物包含两个靶向部分。在一些实施方案中,本文所公开的嵌合蛋白复合物包含两个不同的靶向部分。在多个实施方案中,这些二价模式的取向如图7中所示。举例来说,在一些实施方案中,本文所公开的嵌合蛋白复合物包含针对clec9a和pd
‑
l1的靶向部分(但不限于,vhh)。
63.在多个实施方案中,r149a突变存在于ifn
‑
α2中。
64.在多个实施方案中,r149a突变不存在于ifn
‑
α2中,而是存在另一个突变。举例来说,这种替代突变可能是在位置r33、r144、a145、m148和l153中的一者处。在多个实施方案中,所述替代突变是r33a、r144a、r144i、r144l、r144s、r144t、r144y、a145d、a145g、a145h、a145k、a145y、m148a和l153a中的一者。为清楚起见,在多个实施方案中,本文中对r149a的任何引用可替换为r33a、r144a、r144i、r144l、r144s、r144t、r144y、a145d、a145g、a145h、a145k、a145y、m148a和l153a中的一者。在多个实施方案中,本文中对r149a的任何引用可替换为a145g。
65.在一些实施方案中,本文所公开的嵌合蛋白复合物包括至少一个fc结构域。在一些实施方案中,所述嵌合蛋白复合物包括经修饰的fc结构域,其中相对于seq id no:13
‑
16中的任一者,所述经修饰的fc结构域包括以下突变中的一者或多者:p329g、k322q、k322a或p331s。在其他实施方案中,相对于人igg1 fc,所述经修饰的fc结构域包括以下突变中的一者或多者:p329g、k322q、k322a或p331s。
66.在一些实施方案中,所述嵌合蛋白复合物包括具有与seq id no:13
‑
16具有至少90%同一性的氨基酸序列的经修饰的fc结构域。在其他实施方案中,所述经修饰的fc结构域具有与seq id no:13
‑
16具有至少93%同一性的氨基酸序列。在其他实施方案中,所述经修饰的fc结构域具有与seq id no:13
‑
16具有至少95%同一性的氨基酸序列。
67.在另一方面,本发明涉及一种治疗或预防癌症的方法,所述方法包括向有需要的患者施用有效量的如本文所公开的嵌合蛋白复合物。所述方法可用于治疗或预防选自以下一项或多项的癌症:基底细胞癌;胆道癌;膀胱癌;骨癌;脑和中枢神经系统癌症;乳腺癌;腹膜癌;宫颈癌;绒毛膜癌;结肠和直肠癌;结缔组织癌;消化系统癌症;子宫内膜癌;食道癌;
眼癌;头颈癌;胃癌(包括胃肠癌);成胶质细胞瘤;肝癌;肝细胞瘤;上皮内赘瘤;肾脏癌或肾癌;喉癌;白血病;肝癌;肺癌(例如,小细胞肺癌、非小细胞肺癌、肺腺癌和肺鳞状细胞癌);黑素瘤;骨髓瘤;成神经细胞瘤;口腔癌(唇、舌、口和咽);卵巢癌;胰腺癌;前列腺癌;成视网膜细胞瘤;横纹肌肉瘤;直肠癌;呼吸系统癌症;唾液腺癌;肉瘤(例如卡波西肉瘤);皮肤癌;鳞状细胞癌;胃癌;睾丸癌;甲状腺癌;子宫或子宫内膜癌;泌尿系统癌症;外阴癌;淋巴瘤,包括霍奇金氏淋巴瘤和非霍奇金氏淋巴瘤,以及b细胞淋巴瘤(包括低级/滤泡性非霍奇金氏淋巴瘤(nhl);小淋巴细胞性(sl)nhl;中级/滤泡性nhl;中级弥漫性nhl;高级成免疫细胞性nhl;高级成淋巴细胞性nhl;高级小非核裂细胞nhl;巨大肿块性nhl;套细胞淋巴瘤;aids相关淋巴瘤;和瓦尔登斯特伦巨球蛋白血症;慢性淋巴细胞性白血病(cll);急性成淋巴细胞性白血病(all);毛细胞性白血病;慢性成髓细胞性白血病;以及其他癌瘤和肉瘤;和移植后淋巴组织增生性病症(ptld),以及与斑痣性错构瘤相关的异常血管增生;水肿(例如与脑肿瘤相关的水肿);和梅格斯氏综合征。
68.本发明的另一方面涉及一种包含如本文所公开的嵌合蛋白复合物和药学上可接受的载体的药物组合物。在一些实施方案中,本发明有关于包含本发明的嵌合蛋白复合物的药物组合物。
69.本发明的另一方面涉及一种用于治疗或预防癌症的方法,所述方法包括向有需要的患者施用有效量的如本文所公开的药物组合物。所述药物组合物可用于治疗或预防选自以下一项或多项的癌症:基底细胞癌;胆道癌;膀胱癌;骨癌;脑和中枢神经系统癌症;乳腺癌;腹膜癌;宫颈癌;绒毛膜癌;结肠和直肠癌;结缔组织癌;消化系统癌症;子宫内膜癌;食道癌;眼癌;头颈癌;胃癌(包括胃肠癌);成胶质细胞瘤;肝癌;肝细胞瘤;上皮内赘瘤;肾脏癌或肾癌;喉癌;白血病;肝癌;肺癌(例如,小细胞肺癌、非小细胞肺癌、肺腺癌和肺鳞状细胞癌);黑素瘤;骨髓瘤;成神经细胞瘤;口腔癌(唇、舌、口和咽);卵巢癌;胰腺癌;前列腺癌;成视网膜细胞瘤;横纹肌肉瘤;直肠癌;呼吸系统癌症;唾液腺癌;肉瘤(例如卡波西肉瘤);皮肤癌;鳞状细胞癌;胃癌;睾丸癌;甲状腺癌;子宫或子宫内膜癌;泌尿系统癌症;外阴癌;淋巴瘤,包括霍奇金氏淋巴瘤和非霍奇金氏淋巴瘤,以及b细胞淋巴瘤(包括低级/滤泡性非霍奇金氏淋巴瘤(nhl);小淋巴细胞性(sl)nhl;中级/滤泡性nhl;中级弥漫性nhl;高级成免疫细胞性nhl;高级成淋巴细胞性nhl;高级小非核裂细胞nhl;巨大肿块性nhl;套细胞淋巴瘤;aids相关淋巴瘤;和瓦尔登斯特伦巨球蛋白血症;慢性淋巴细胞性白血病(cll);急性成淋巴细胞性白血病(all);毛细胞性白血病;慢性成髓细胞性白血病;以及其他癌瘤和肉瘤;和移植后淋巴组织增生性病症(ptld),以及与斑痣性错构瘤相关的异常血管增生;水肿(例如与脑肿瘤相关的水肿);和梅格斯氏综合征。
70.在另一方面,本发明涉及一种重组核酸组合物,所述重组核酸组合物编码本文所公开的一种或多种嵌合蛋白复合物,例如编码整个嵌合蛋白复合物或其组成多肽。在另一方面,本发明涉及一种宿主细胞,所述宿主细胞包含本文所公开的重组核酸组合物复合物。
71.定义
72.如本文所使用,“一个/一种(a/an)”或“所述(the)”可以意指一个或多于一个。
73.此外,术语“约”当与引用的数值指示结合使用时意指所引用的数值指示加或减所述引用的数值指示的至多10%。举例来说,语言“约50”覆盖45至55的范围。
74.如本文所使用,术语“有效量”是指足以实现所期望的治疗和/或预防效果的量,例
如使得疾病或病症或与疾病或病症相关的一种或多种征象或症状得以预防或减少的量。在治疗或预防应用的情形中,施用至受试者的组合物的量将取决于疾病的程度、类型和严重程度,以及个体的特征(诸如总体健康状况、年龄、性别、体重和耐药性)。技术人员将能够根据这些和其他因素确定适当的剂量。所述组合物还可以与一种或多种其他治疗性化合物组合施用。在本文所描述的方法中,可以将所述治疗性化合物施用至患有疾病或病症的一种或多种征象或症状的受试者。如本文所使用,如果活性和/或效应的读出在剂或刺激物存在下相对于不存在此类调节降低了显著量,诸如降低了至少约10%、至少约20%、至少约30%、至少约40%、至少约50%、至少约60%、至少约70%、至少约80%、至少约90%、至少约95%、至少约97%、至少约98%或更多、多达并且包括至少约100%,那么某性质“降低”。如本领域普通技术人员所理解,在一些实施方案中,活性降低并且一些下游读出将降低但其他下游读出可以增加。
75.相反地,如果活性和/或效应的读出在剂或刺激物存在下相对于不存在此类剂或刺激物增加了显著量,例如增加了至少约10%、至少约20%、至少约30%、至少约40%、至少约50%、至少约60%、至少约70%、至少约80%、至少约90%、至少约95%、至少约97%、至少约98%或更多、多达并且包括至少约100%或更多、至少约2倍、至少约3倍、至少约4倍、至少约5倍、至少约6倍、至少约7倍、至少约8倍、至少约9倍、至少约10倍、至少约50倍、至少约100倍,那么活性“增加”。
76.尽管开放性的术语“包含”作为术语诸如包括、含有或具有的同义词在本文中用以描述和要求本发明,但本发明或其实施方案可以可选地使用替代性术语如“由
……
组成”或“基本上由
……
组成”加以描述。
77.用于实现治疗效果所需要的本文所描述的组合物的量可以出于特定目的根据常规程序凭经验确定。一般来说,对于出于治疗目的而施用治疗剂而言,治疗剂是以药理学有效剂量给予。“药理学有效量”、“药理学有效剂量”、“治疗有效量”或“有效量”是指足以产生所期望的生理效应的量或能够实现所期望的结果、特别是用于治疗病症或疾病的量。如本文所使用,有效量将包括足以例如延迟病症或疾病的症状的发展、改变病症或疾病的症状的过程(例如,减缓疾病的症状的进展)、减少或消除病症或疾病的一种或多种症状或表现形式,以及逆转病症或疾病的症状的量。治疗益处还包括中断或减缓潜在疾病或病症的进展,无关于是否实现了改善。
78.如本文所使用,“治疗方法”同样适用于组合物用于治疗本文所描述的疾病或病症的用途和/或组合物用于制造用以治疗本文所描述的疾病或病症的药物的一种和/或多种用途。
79.如本文所使用,fc结构域突变是根据eu公约(edelman等人,pnas 1969;63(1)78
‑
85,所述文献以引用方式整体并入)编号。如本文所使用,术语“lala”突变是指具有l234a突变和l235a突变的双突变fc结构域。如本文所使用,术语“kq”突变是指具有k322q突变的突变fc结构域。
80.旋钮入孔洞突变体是ridgway等人,protein engineering1996;9:617
‑
621(其以引用方式整体并入)中描述的那些,即y407t/t366y。
81.或者,旋钮入孔洞突变体是merchant等人,nature biotechnology1998;16:677
‑
681(其以引用方式整体并入)中描述的那些,即s354c:t366w/y349c:t366s:l368a:y407v。
82.除非另外指明,否则fc来自人igg1。
83.序列
84.seq id no:1变型1 vhh
‑
fc:r1chcl50(opt4)
‑
5*ggs
‑
fc孔洞ridgway(lala
‑
kq)
[0085][0086]
seq id no:2变型2 vhh
‑
fc:r1chcl50(opt4)
‑
5*ggs
‑
fc孔洞merchant(lala
‑
kq)
[0087][0088]
seq id no:3变型3 vhh
‑
fc:3lec89(opt4)
‑
5*ggs
‑
fc孔洞ridgway(lala
‑
kq)
[0089]
d
[0090][0091]
seq id no:4变型4vhh
‑
fc:3lec89(opt4)
‑
5*ggs
‑
fc孔洞merchant(lala
‑
kq)
[0092][0093]
seq id no:5变型1fc
‑
afn:fc旋钮ridgway(lala
‑
kq)
‑
10*ggs
‑
g
‑
huifna2b_r149a
[0094][0095]
seq id no:6变型2fc
‑
afn:fc旋钮ridgway(lala
‑
kq)
‑
10*ggs
‑
g
‑
huifna2b_r149a_t106e
[0096][0097]
seq id no:7变型3fc
‑
afn:fc旋钮merchant(lala
‑
kq)
‑
10*ggs
‑
g
‑
huifna2b_r149a
[0098][0099]
seq id no:8变型4fc
‑
afn:fc旋钮merchant(lala
‑
kq)
‑
10*ggs
‑
g
‑
huifna2b_r149a_t106e
[0100][0101]
seq id no:9人ifnα2a(氨基酸序列)
[0102][0103]
seq id no:10人ifnα2b(氨基酸序列)
[0104][0105]
seq id no:11r1chcl50_opt4(抗人clec9a vhh)
[0106][0107]
seq id no:12 3lec89_opt4(抗人clec9a vhh)
[0108][0109]
seq id no:13fc(人igg1)的氨基酸序列—具有lala突变和ridgway孔洞
[0110][0111]
seq id no:14fc(人igg1)的氨基酸序列—具有lala突变和ridgway旋钮
[0112][0113]
seq id no:15fc(人igg1)的氨基酸序列—具有lala突变和merchant孔洞
[0114][0115]
seq id no:16fc(人igg1)的氨基酸序列—具有lala突变和merchant旋钮
[0116][0117]
其他序列在文本的其他地方标识。
[0118]
实施例
[0119]
在一些实施例中,使用了旋钮入孔洞技术的两个变体:ridgway(来源于ridgway等人,protein engineering 1996;9:617
‑
621)和merchant(来源于merchant等人,nature biotechnology1998;16:677
‑
681)。
[0120]
ridgway构建体中的“标准”效应子突变为lala
‑
pg(p329g),这在本文中有说明。merchant构建体中的“标准”效应子突变为lala
‑
kq(k322q),这在本文中有说明。
[0121]
术语“actaferon(afn)”或“actakine”在本文中偶尔用于指代本文所描述的嵌合蛋白(在实施例中提供了关于嵌合蛋白形式的详细信息)。
[0122]
实施例1:基于fc的actaferon
[0123]
为了增加clec9a特异性(clec9a是一种高度特异性的cdc1标记物)actaferon的半衰期,将人clec9a
‑
vhh_huifna2融合蛋白转化成fc融合物。为此,将人igg1
‑
fc经由20*ggs接头融合至actaferon(vhh 3lec89
‑
20*ggs
‑
huifna2_r149)。在第二种型式中,将fc域构建在vhh与ifn部分之间。通过引入lala
‑
p329g突变降低人igg1
‑
fc的效应功能。
[0124]
用于在哺乳动物细胞中表达的相关序列是:
[0125]
p
‑
956:pcdna3.4
‑
小鼠轻链κ
‑
higg1
‑
lala
‑
pg
‑
20*ggs
‑
3lec89
‑
20*ggs+g
‑
ifna2 r149a
[0126][0127]
p
‑
957:pcdna3.4
‑
小鼠ig重链
‑
3lec89
‑
20*ggs
‑
higg1
‑
lala
‑
pg
‑
20*ggs+g
‑
ifna2 r149a
[0128][0129]
通过geneart(thermo fisher)制备这些构建体,并根据制造商的指南在expicho表达系统(thermo fisher)中瞬时表达这些构建体。转染后十天,收集上清液并通过离心除去细胞。根据制造商的指南,使用rprotein a sepharose fast flow树脂(ge healthcare)从培养基中纯化重组蛋白。出乎意料的是,以70
‑
170mg/l表达的蛋白质显示出严重的溶解性问题,即使浓度低于1mg/ml,当储存在4℃下或经历单次冻
‑
融循环后,它们也倾向于聚集和沉淀。当将vhh 3lec89替换为对人pd
‑
l1具有特异性的无关vhh 2lig99时,类似的观察结果表明基于fc的actakine形式具有可制造性。
[0130]
令人惊讶的是,通过设计不同类型的fc构建体解决了溶解性问题。在这种新形式中,通过使用旋钮入孔洞突变y407t/t366y或s354c:t366w/y349c:t366s:l368a:y407v将vhh
‑
fc融合物与fc
‑
ifn融合物结合产生异源二聚体fc复合物。其他变体包括通过t106e突变选择性敲除huifna2中的o
‑
糖基化位点。基于2个不同的人源化人clec9a特异性vhh,总共设计了8个构建体。为了降低igg1
‑
fc蛋白的效应功能,使用了突变lala
‑
k322q。成熟蛋白质的序列由seq id no:1
‑
8表示。这产生总共8个不同的fc复合物,这些复合物可以如图1中所示通过组合旋钮和孔洞结构产生。
[0131]
为了在哺乳动物细胞中表达,将序列连接至前导序列并通过geneart(thermo fisher)制备构建体。如上文所描述,在expicho细胞中进行生产。在hitrap protein a hp(ge healthcare)上从上清液中纯化重组蛋白,中和后将洗脱的蛋白在g25柱(ge healthcare)上脱盐,之后进行最终0.22μm过滤。蛋白质在至少10mg/ml的浓度下在4℃下或经历重复冻/融循环后显示仍可溶。
[0132]
实施例2:有或无fc的嵌合体的pk效应
[0133]
使用基于r1chcl50的fc蛋白的4种不同变体在小鼠中进行的pk(药代动力学)研究。
[0134]
将每种构建体以1mg/kg静脉内给予总共9只小鼠。在5分钟、8小时和6天时从第一
组3只小鼠中抽取k
‑
edta血液,在15分钟、1天和10天时从第二组3只小鼠中抽取血液,并且在2小时、3天和14天时从第三组3只小鼠中抽取血液。通过elisa测量完整的clec9a
‑
afn fc的浓度。简单来说,将maxisorp nunc免疫板(thermo scientific)用pbs中0.5μg/ml的抗人干扰素αmab(克隆mmha
‑
13;pbl assay science)包被过夜。用pbs+0.05%tween
‑
20洗涤板四次后,在室温下用0.1%酪蛋白的pbs封闭至少1小时。随后,将稀释的样品和标准品在0.1%酪蛋白的pbs中于室温下孵育2小时。在另一个洗涤循环后,将定制的兔抗vhh(在0.1%酪蛋白的pbs中以1/20000稀释)在室温下孵育2小时,然后进行另一个洗涤循环,并与hrp缀合的山羊抗兔(jackson
‑
111
‑
035
‑
144;1:5000,0.1%酪蛋白)一起在室温下孵育1小时。在最后的洗涤循环后,根据制造商的说明使用kpl底物(5120
‑
0047;seracare)测量过氧化物酶活性。使用graphpad prism计算样品中的浓度。测得的浓度绘制在图2中,显示所有4种构建体均具有相似的pk曲线,只是在最后一个采样时间点,基于ridgway的fc构建体的清除速度更快。据估计,ridgway构建体的终末半衰期平均约为3天,而merchant构建体的终末半衰期平均约为4.5天。
[0135]
使用无fc融合体的clec9a actaferon在小鼠中进行的pk研究.
[0136]
在单独的研究中,评估无fc的afn(3lec89
‑
20*ggs
‑
huifna2_r149a
‑
his6)在小鼠中的pk。该嵌合体的序列为:
[0137]
p
‑
602序列
[0138][0139]
对九只动物以3mg/kg静脉内给药。在5分钟和1小时时从第一组3只小鼠中抽取k
‑
edta血液,在15分钟和3小时时从第二组3只小鼠中抽取血液,最后在8小时时从最后一组小鼠中抽取血液。使用与如针对fc融合蛋白所描述相同的elisa测量血浆样品中的浓度。所测量的浓度(图3)显示了这种类型的分子的快速清除,导致在8小时时间点的浓度低于检测极限(0.12μg/ml)。估计的终末半衰期在仅2小时的范围内,清楚地证明了基于fc的actakine的优越半衰期特性。
[0140]
实施例3:构建体的结合和体内效应
[0141]
为了测量相对结合亲和力,将如实施例2中所示的相同4个分子与连续稀释的clec9a
‑
afn fc构建体在hl116
‑
hclec9a细胞上一起孵育。为了评定结合特异性,还将亲本hl116细胞和亲本hek293t细胞(均缺乏可检测的clec9a表达)与相同的连续稀释的clec9a
‑
afn fc构建体一起孵育。通过随后与fitc偶联的抗人次级ab一起孵育,在macsquant x仪器(miltenyi biotech)上测量并使用flowlogic软件(miltenyi biotech)进行分析来检测结合。图4中的数据显示基于fc的afn对hl116
‑
hclec9a细胞具有相似的结合ec50,而在不表达clec9a的细胞系上未检测到结合。
[0142]
为了评估基于fc的afn的功效,在人源化小鼠的肿瘤模型中测试这些分子。简单来说,对新生nsg小鼠(1
‑
2天大)进行100cgy亚致死照射,然后肝内递送1x105个cd34+人干细
胞(来自hla
‑
a2阳性脐带血)。在干细胞转移后第13周,给小鼠皮下接种25x105个人rl滤泡性淋巴瘤细胞(atcc crl
‑
2261;对ifn的直接抗增殖效应不敏感)。从肿瘤接种后的第10天至第19天,每天用30μg的人flt3l蛋白腹膜内治疗小鼠。在肿瘤接种后第11天,当可见可触知的肿瘤时,开始每周一次用缓冲液或fc
‑
afn(8或75μg)静脉注射(n=5只小鼠/组)。每天评定肿瘤大小(卡尺测量)、体重和温度。图5和图6中的数据示出了直至第二次治疗后6天的肿瘤生长。图5表明,所有构建体在较低的8μg剂量下都诱导相似的肿瘤生长抑制水平。图6示出了更高剂量的merchant构建体导致肿瘤生长抑制增加的结果。体重和温度的数据未显示缓冲液治疗与afn治疗之间有任何重大差异,这确证所有afn治疗都具有良好的耐受性。
[0143]
实施例4:二价和双特异性变体
[0144]
为了进一步提高分子的靶向能力,添加额外的vhh部分从而产生了构建体,其非限制性构型实例示于图7中。这些新型构建体以二价模式靶向clec9a或者共同靶向例如clec9a和pd
‑
l1两者。作为实例,以下构建体是基于针对clec9a的r1chcl50(opt4)vhh和/或针对pd
‑
l1和huifna2b_r149a的2lig99 vhh。通过将r1chcl50(opt4)替换为3lec89(opt4),可产生类似的系列。或者,可将huifna2b_r149a替换为huifna2b_r149a_t106e。最后,以下实例是基于含有基于merchant的旋钮入孔洞突变的fc部分,其可与具有基于ridgway的旋钮入孔洞突变的fc部分交换。
[0145]
新型构建体
[0146]
a.fc(merchant)的n端的额外vhh的二价clec9a靶向的孔洞链
[0147]
vhh
‑
vhh
‑
fc:r1chcl50(opt4)
‑
5*ggs
‑
r1chcl50(opt4)
‑
5*ggs
‑
fc(lala
‑
kq)
[0148][0149]
b.fc(merchant)的c端的额外vhh的二价clec9a靶向的孔洞链
[0150]
vhh
‑
fc
‑
vhh:r1chcl50(opt4)
‑
5*ggs
‑
fc(lala
‑
kq)
‑
5*ggs
‑
r1chcl50(opt4)
[0151]
[0152]
c.fc(merchant)的n端的额外vhh的二价clec9a靶向的旋钮链
[0153]
vhh
‑
fc
‑
afn:r1chcl50(opt4)
‑
5*ggs
‑
fc(lala
‑
kq)
‑
10*ggs
‑
g
‑
hulfna2b_r149a
[0154][0155]
d.fc(merchant)的n端的额外vhh的双特异性clec9a
‑
pdl1靶向的孔洞链
[0156]
vhh
‑
vhh
‑
fc:2lig99
‑
5*ggs
‑
r1chcl50(opt4)
‑
5*ggs
‑
fc(lala
‑
kq)
[0157][0158]
e.fc(merchant)的c端的额外vhh的双特异性clec9a
‑
pd
‑
l1靶向的孔洞链
[0159]
vhh
‑
fc
‑
vhh:r1chcl50(opt4)
‑
5*ggs
‑
fc(lala
‑
kq)
‑
5*ggs
‑
2lig99
[0160][0161]
f.fc(merchant)的n端的额外vhh的双特异性clec9a
‑
pd
‑
l1靶向的旋钮链
[0162]
vhh
‑
fc
‑
afn:2lig99
‑
5*ggs
‑
fc(lala
‑
kq)
‑
10*ggs
‑
g
‑
hulfna2b_r149a
[0163]
[0164]
为了在哺乳动物细胞中表达,将序列连接至前导序列并通过geneart(thermo fisher)制备表达构建体。如上文所描述,在expicho细胞中进行生产。在hitrap protein a hp(ge healthcare)上从上清液中纯化重组蛋白,中和后将洗脱的蛋白在g25柱(ge healthcare)上脱盐,之后进行最终0.22μm过滤。更具体地说,组合以下表达构建体以产生基于fc的actaferon。
[0165]
·
含有seq id no:17的构建体+含有seq id no:7的构建体
[0166]
·
含有seq id no:2的构建体+含有seq id no:19的构建体
[0167]
·
含有seq id no:18的构建体+含有seq id no:7的构建体
[0168]
·
含有seq id no:20的构建体+含有seq id no:7的构建体
[0169]
·
含有seq id no:2的构建体+含有seq id no:22的构建体
[0170]
·
含有seq id no:21的构建体+含有seq id no:7的构建体
[0171]
实施例5:a145g和m148a afn突变
[0172]
在该实施例中,评估了ifn变异a145g和m148a作为afn突变(即导致生物活性丧失的弹头突变,可在靶向弹头后恢复)的潜力。
[0173]
在异源二聚体的“旋钮入孔洞”fc afn情形中评估突变。此处,clec9a vhh r1chcl50序列经由柔性20*ggs接头且在pcdna3.4表达载体中融合至含有l234a_l235a_k322q效应子突变和“孔洞”修饰y349c_t366s_l368a_y407v的人igg1 fc序列(参见下文序列r1chcl50
‑
fc3)。第二afn配偶体(也克隆到pcdna3.4载体中),由含有l234a_l235a_k322q效应子突变和“旋钮”修饰s354c_t366w的人igg1 fc序列与具有afn突变a145g或m148a和o
‑
糖基化突变t106e的hifna2序列之间的融合物组成(参见下文序列)。
[0174]
为了产生这些“旋钮入孔洞”fc afn,根据制造商的说明,将“孔洞”和“旋钮”质粒的组合转染到expicho
tm
细胞(thermofisher)中。转染后七天,使用蛋白a旋转板(thermofisher)纯化重组蛋白,定量,并使用sds
‑
page进行纯度测试。
[0175]
与其他pbmc群体相比,在原代cdc1细胞(表达clec9a,afn的靶标)中测试所得a145g和m148 afn的stat1磷酸化。简单来说,使用lymphoprep
tm
(stemcell technologies)进行密度梯度离心,从健康供体的血沉棕黄层中分离出pbmc。将细胞用facs缓冲液(2%fbs,1mm edta的pbs)洗涤两次,并在4℃下用抗clec9a和抗cd141 ab(均来自miltenyi)染色20分钟以鉴定cdc1群体。两次洗涤后,将细胞用连续稀释的野生型ifna2或两种afn在37℃下刺激15分钟。在固定(10分钟,37℃,固定缓冲液i;bd biosciences)、透化(30分钟,在冰上,perm iii缓冲液i;bd biosciences)以及洗涤后,将细胞用抗stat1 py701 ab(bd biosciences)染色。使用x仪器(miltenyi biotec)采集样品,并使用flowlogic
tm
软件(miltenyi biotec)进行分析。图8a至图8b中的数据清楚地说明(i)clec9a
‑
/cd141
‑
和clec9a+/cd141+细胞对野生型ifna2的敏感性相当,并且(ii)a145g和m148a突变均消除非cdc1 pbmc(clec9a
‑
/cd141
‑
)中的大部分信号传导,但靶向clec9a阳性细胞(clec9a+/cd141+)在很大程度上恢复了这种信号传导。这导致a145g或m148a突变的afn效应至少为100倍,并说明了这些突变在afn设计中的潜力。
[0176]
序列:
[0177]
p
‑
1451:
‑
20*ggs
‑
hlgg1 fc_l234a_l235a_k322q_y349c_t366s_l368a_y407v(简称:r1chcl50
‑
fc3)
[0178][0179]
p
‑
1846:hlgg1 fc_l234a_l235a_k322q_s354c_t366w
‑
20*ggs
‑
[0180]
(简称:fc4
‑
hlfna2_a145g)
[0181][0182]
p
‑
1850:hlgg1 fc_l234a_l235a_k322q_s354c_t366w
‑
20*ggs
‑
[0183]
(简称:fc4
‑
hlfna2_m148a)
[0184][0185]
实施例6:体内a145g和m148a afn突变
[0186]
为了评估基于fc的afn的功效,在人源化小鼠的肿瘤模型中测试这些分子。简单来说,对新生nsg小鼠(1
‑
2天大)进行100 cgy亚致死照射,然后肝内递送1x105个cd34+人干细胞(来自hla
‑
a2阳性脐带血)。在干细胞转移后第13周,给小鼠皮下接种25x105个人rl滤泡性淋巴瘤细胞(atcc crl
‑
2261;对ifn的直接抗增殖效应不敏感)。从肿瘤接种后的第9天至第22天,用30μg的人flt3l蛋白腹膜内治疗小鼠。在肿瘤接种后第9天,当可见可触知的肿瘤时,开始每周一次用缓冲液或如实施例5中所述的fc
‑
afn(7.5μg)构建体静脉注射(n=6只小鼠/组)。每天评定肿瘤大小(卡尺测量)、体重和温度。图9中的数据示出了直至第三次治疗后一周的肿瘤生长,并表明两种构建体均诱导强肿瘤生长抑制水平。体重和温度的数据未显示缓冲液治疗与afn治疗之间有任何重大差异,这确证所有afn治疗都具有良好的耐受性。
[0187]
实施例7:基于a145g和m148a突变的另外的fc
‑
afn构建体产生了以下具有减弱人干扰素α2的另外的fc构建体:
[0188]
a.hlgg1 fc_l234a_l235a_k322q_s354c_t366w
‑
10*ggs
‑
g
‑
hlfna2_t106e_m148a
[0189][0190]
b.hlgg1 fc_l234a_l235a_k322q_s354c_t366w
‑
10*ggs
‑
g
‑
hlfna2_m148a
[0191][0192][0193]
c.hlgg1 fc_l234a_l235a_k322q_s354c_t366w
‑
10*ggs
‑
g
‑
hlfna2_t106e_a145g
[0194][0195]
d.hlgg1 fc_l234a_l235a_k322q_s354c_t366w
‑
10*ggs
‑
g
‑
hlfna2_a145g
[0196][0197]
e.hlgg1 fc
‑
l234a
‑
l235a_k322q_t366y
‑
10*ggs
‑
g
‑
hlfna2_t106e
‑
m148a
[0198][0199]
f.hlgg1 fc_l234a_l235a_k322q_t366y
‑
10*ggs
‑
g
‑
hlfna2_m148a
[0200][0201][0202]
g.hlgg1 fc_l234a_l235a_k322q_t366y
‑
10*ggs
‑
g
‑
hlfna2_t106e_a145g
[0203][0204]
h,hlgg1 fc_l234a_l235a_k322q_t366y
‑
10*ggs
‑
g
‑
hlfna2_a145g
[0205][0206]
为了产生人clec9a靶向的afn,将任何上述构建体a
‑
d与seq id 2或4的clec9a vhh
‑
fc融合物组合,产生8个新型构建体。此外,将任何上述构建体e
‑
h与seq id 1或3的clec9a vhh
‑
fc融合物组合,产生另外一组8个新型构建体。如实施例5中所述表达和纯化蛋白质。
[0207]
实施例8:a145g突变加或无t106o
‑
糖基化
[0208]
在该实验中,比较在ifna2中有或无t106o
‑
糖基化的clec9a靶向的afn(r1chcl50
‑
fc3+fc4
‑
ifna2_a145g与r1chcl50
‑
fc3+fc4
‑
ifna2_t106e_a145g)与非靶向变体(fc3+fc4
‑
ifna2_a145g)。如实施例5中所述产生蛋白质,并先后通过蛋白a色谱法和尺寸排阻进行纯化。
[0209]
为了评估效力,如实施例5中所述,在人pbmc中的原代cdc1(clec9a+/cd141+)和非cdc1(clec9a
‑
/cd141
‑
)群体中测试构建体的stat1磷酸化。图10示出了有或无t106o
‑
糖基化的clec9a靶向构建体的特异性,显示相比非cdc1细胞,该构建体在cdc1细胞中更有效地激活ifn信号传导,并且相比经非靶向变体处理的cdc1细胞,对cdc1细胞更有效。
[0210]
为了评估前述异源二聚体的“旋钮入孔洞”fc afn构建体的体内功效,在人源化小鼠的肿瘤模型中对其进行测试。简单来说,对新生nsg小鼠(1
‑
2天大)进行100cgy亚致死照射,然后肝内递送1x105个cd34+人干细胞(来自hla
‑
a2阳性脐带血)。在干细胞转移后第13周,给小鼠皮下接种25x105个人rl滤泡性淋巴瘤细胞(atcc crl
‑
2261;对ifn的直接抗增殖效应不敏感)。从肿瘤接种后的第7天至第17天,用30μg的人flt3l蛋白腹膜内治疗小鼠。在肿瘤接种后第9天,当可见可触知的肿瘤时,开始每周一次用缓冲液或fc
‑
afn(2.5μg)构建
体静脉注射(n=5只小鼠/组)。每天评定肿瘤大小(卡尺测量)、体重和温度。图11中的数据示出了直至第三次治疗后一周的肿瘤生长,并表明两种靶向afn均诱导强肿瘤生长水平,而对未靶向变体未观察到显著效应。体重和温度的数据未显示缓冲液治疗与afn治疗之间有任何重大差异,这确证所有afn治疗都具有良好的耐受性。
[0211]
序列
[0212]
1.p
‑
1479:r1chcl50
‑
fc3
[0213][0214]
2.p
‑
1542:fc3
[0215][0216]
3.p
‑
2157:fc4
‑
ifna2_
[0217][0218]
4.p
‑
2158:fc4
‑
ifna2_
[0219][0220]
实施例9:fc
‑
afn构建体
[0221]
质谱分析表明,在几乎所有成熟蛋白质中,r1chcl50
‑
fc3链中的c端赖氨酸k残基都被切割掉了。因此,构建了其中两条fc链中的该赖氨酸残基被除去的变体。所得蛋白质将被称为fc
′
蛋白质。作为实例,下文示出r1chcl50
‑
fc3
′
与fc4
′‑
afn融合物的嵌合蛋白组合的序列,其中ifna2b中的残基a145突变为g,或者其中ifna2a中的残基t106和a145分别突变为e和g。
[0222]
序列:
[0223]
p
‑
2379:fc4
′‑
ifna2b
‑
a145g
[0224][0225]
p
‑
2380:fc4
′‑
ifna2a_t106e_a145g
[0226][0227]
p
‑
1479b:r1chcl50
‑
fc3
″
[0228]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1