一种全共轭的螺稠环梯形有机分子及其制备方法与应用
本发明属光电材料和应用技术领域,涉及一种全共轭的螺稠环梯形有机分子及其制备方法与应用。该材料体系可以作为有机发光增益介质应用于光泵浦有机激光和电泵浦有机激光器件;可以作为上转换发光体应用于非线性发光和激光;也可以作为有机发光材料应用于有机电致发光器件;以及作为空穴传输材料应用于钙钛矿有机无机杂化太阳能电池等。
背景技术:
π-有机共轭分子由于出色的光电性能和易于加工的特性,在有机发光二极管(oled),有机场效应晶体管(ofet),有机太阳能电池(opv)及有机激光(organiclasers)等领域有着越来越广泛的应用。有机激光作为新的发展方向,是半导体激光未来一个非常重要的发展领域。七十年代,美国贝尔实验室成功研制异质结固态激光器,大大降低阈值电流密度,为半导体激光的应用开启了大门。但是,使用化学气相沉积等方法在gaas、蓝宝石等衬底上制造的半导体激光器,有发射波长范围窄和面积小等缺点。近年来,oled的发光强度已经达到实用化的程度,外部量子效率已经接近或超过理论的水平。更重要的是,oled器件制作工艺简单,利用喷墨打印技术制造的优点是无机半导体所无法替代的。而且,oled器件的发射光谱范围广,在380-900nm的可见光和近红外波段均有报道。随着oled技术的日趋成熟,有机半导体激光和有机非线性光学逐渐引起科研工作者的广泛关注。但是,现有的有机发光材料体系仍存在明显不足,比如,迁移率低、光热稳定性差、激光增益系数低、激光转换效率差、上转换效率低等,限制了其在有机半导体激光和有机非线性光学领域中的广泛应用。如何设计和开发具有应用潜力的有机材料体系是发展有机半导体激光和有机非线性光学面临的关键问题。
梯形分子由于其大的分子共轭平面、高的荧光量子效率、高迁移率、优异的电化学/热稳定性,是一类非常重要的有机激光材料体系。但梯形聚合物有着明显的结构缺陷,限制了其作为发光体在有机半导体激光和有机非线性光学中的应用。于此同时,具备多个活性位从而形成全共轭稠环梯形结构的前驱体选择较少。因此,设计合成结构明确的全共轭稠环梯形结构,有望融合梯形分子的所有优点,从而开发出优异光电性能的有机激光增益介质和有机非线性光学材料。
本专利通过巧妙的分子结构设计,发明了一种全新的全共轭的螺稠环梯形有机分子。通过采用suzuki偶联、傅克酰化/烃化反应、环化反应等反应类型,实现了材料的高效制备;得到了结构明确、发光稳定、光热稳定性好、荧光量子效率高的有机发光材料体系;同时通过选用不同电活性的官能团封端,可以调节材料的发光特性、多光子吸收特性和电学性能,改善载流子迁移率,使得这类材料有了更加广阔的应用;制备的激光器件显示,该材料体系具备极高的激光增益特性、优异的激光热稳定性和超低的ase/激光阈值,有效解决了目前有机激光增益介质材料体系材料种类缺乏、光热稳定性差、增益低、阈值高等技术难题,是一类具有重要应用潜力的有机激光材料。非线性测试结果表明,该材料体系具有极高的多光子吸收截面,具备应用于高阶非线性光学中的潜质。同时,该材料体系可以获得良好的蓝光发射,可以实现高效的蓝光和白光oled器件,具有良好的产业化应用潜力;也可以作为空穴传输材料应用于钙钛矿有机无机杂化太阳能电池等领域。
技术实现要素:
技术问题:
本发明公开了一种全共轭的螺稠环梯形有机分子及其制备方法与应用。该材料体系化学结构明确、纯度高、热稳定性能好、玻璃化转变温度高、易于形成均匀的无定形薄膜;同时该材料体系具备高的荧光量子效率、很好的光热稳定性、极高的多光子吸收截面。有效解决了目前有机激光增益介质材料体系材料种类缺乏、光热稳定性差、增益低、阈值高等技术难题,是一类具有重要应用潜力的有机发光/激光材料。材料体系极高的多光子吸收截面有利于解决有机非线性光学材料体系匮乏的问题,作为上转换发光体在非线性发光和激光领域具有广阔的应用前景。
技术方案:本发明提供了一种全共轭的螺稠环梯形有机分子,该全共轭的螺稠环梯形有机分子体系是以螺芴为核,梯形芴为臂,选用二苯胺进行封端的螺稠环梯形有机分子化合物,具有如下结构通式:
其中,r1、r2、r3为c0-c30烷基、烷氧基、烷苯基、烷基苯基中的一种。
进一步的,全共轭的螺稠环梯形有机分子的r1、r2、r3选自c0-c20烷基、烷氧基、烷苯基、烷基苯基中的一种。
本发明的另一个目的,是提供一种全共轭的螺稠环梯形有机分子的制备方法,该制备方法包括以下步骤:
(1)合成前驱体1、前驱体2、前驱体3:以三苯胺硼酸酯或者单体
(2)以单体
(3)将步骤(2)所得化合物加入溴代柔性链r2的有机溶剂中,相应的合成化合物spl(1)-1、spl(1)-2、spl(1)-3、spl(2)-1、spl(2)-2、spl(2)-3、spl-1、spl-2、spl-3。
进一步的,所述步骤(1)合成前驱体1
以三苯胺硼酸酯或者单体
以三苯胺硼酸酯、单体
进一步的,所述步骤(2)合成化合物
以单体
以单体
以单体
进一步的,所述步骤(3)合成通式中化合物spl(1)-1
在氮气保护下,将溴代柔性链r2加入无水四氢呋喃溶剂中,冷却至-78℃,滴加丁基锂溶液,反应0.5-2小时后,将化合物sp(1)-1
本发明的另一个目的,本发明同时提供了该全共轭的螺稠环梯形有机分子的应用,该材料体系作为有机激光增益介质应用于光泵浦有机激光和电泵浦有机激光器件;作为上转换发光体应用于非线性发光和激光;作为有机发光材料应用于有机电致发光(oled)器件;作为空穴传输材料应用于钙钛矿有机无机杂化太阳能电池器件中。
有益结果:本发明提供一种全共轭的螺稠环梯形有机分子材料体系,具体是以螺芴为核,梯形芴为臂,选用二苯胺进行封端的螺稠环梯形有机分子化合物。该材料结构明确、发光稳定、光热稳定性好、荧光量子效率高;同时通过选用不同电活性的官能团封端,可以调节材料的发光特性、非线性特征和电学性能,改善载流子迁移率,使得这类材料有了更加广阔的应用;制备的激光器件具备极高的激光增益特性、优异的激光热稳定性和超低的ase/激光阈值,有效解决了目前有机激光增益介质材料体系材料种类缺乏、光热稳定性差、增益低、阈值高等技术难题,是一类具有重要应用潜力的有机发光/激光材料。非线性测试结果也表明,该材料体系具有极高的多光子吸收截面,具备应用于高阶非线性光学中的潜质。同时,该材料体系可以获得良好的蓝光发射,可以实现高效的蓝光和白光oled器件,具有良好的产业化应用潜力;也可以作为空穴传输材料应用于钙钛矿有机无机杂化太阳能电池等领域。
附图说明
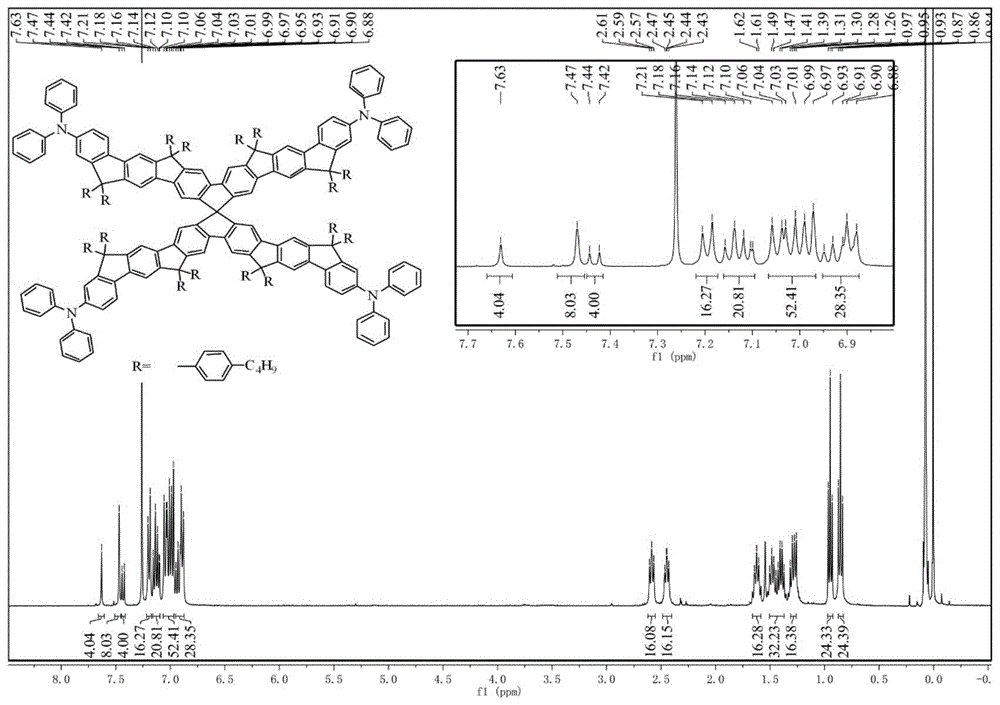
图1.化合物a的1hnmr谱图。
图2.化合物a的13cnmr谱图。
图3.化合物b的1hnmr谱图。
图4.化合物b的13cnmr谱图。
图5.化合物c的1hnmr谱图。
图6.化合物c的13cnmr谱图。
图7.化合物a的溶液和薄膜uv光谱。
图8.化合物a的溶液和薄膜pl光谱。
图9.化合物a的溶液和薄膜uv光谱。
图10.化合物b的溶液和薄膜pl光谱。
图11.化合物c的溶液和薄膜uv光谱。
图12.化合物c的溶液和薄膜pl光谱。
图13.化合物a、b、c的热失重曲线。
图14.化合物a的半峰宽和ase输出斜率随激光强度变化图。
图15.化合物a、b、c的增益系数随激光强度变化图。
图16.化合物c的双光子吸收截面随激光波长变化图。
图17.化合物c的上转化受激辐射能量随激光强度变化图。
图18.实施例1中反应路线图一。
图19.实施例2中反应路线图二。
图20.实施例3中反应路线图三。
图21.实施例4中反应路线图四。
具体实施方式
本发明提供一种全共轭的螺稠环梯形有机分子材料体系,具体是以螺芴为核,梯形芴为臂,选用不同活性官能团如二苯胺进行封端的螺稠环梯形有机分子化合物,具有如下结构通式:
其中,r1、r2、r3为c0-c30烷基、烷氧基、烷苯基、烷基苯基中的一种。
为了更好地理解本发明专利的内容,下面通过具体的实施例来进一步说明本发明的技术方案。具体包括材料合成、性能测试和器件制备。但实施例不限制本发明的涵盖范围。
实施例1:实现前驱体1、2、3的合成
我们从简单原料开始合成目标前驱体1、2、3,如反应路线图一。其中,步骤(i)通过对溴苯二甲酸实现傅克酰化和傅克烃化反应,得到重要单体4;步骤(ii)通过重要单体4跟三苯胺硼酸酯进行suzuki偶联反应得到前驱体1;步骤(iii)由原料2,7-二溴甲基芴和二苯胺在叔丁醇钠、l-脯氨酸作用下二氧六环做溶剂100℃条件下实现乌尔曼偶联反应得到单体5;;步骤(iv)由单体5通过联硼酸频那醇酯、二价钯催化、二氧六环溶剂条件下得到其硼酸酯单体6;步骤(v)由单体6和重要单体4进行suzuki偶联反应得到前驱体2;步骤(vi)由对苯二硼酸酯和重要单体4进行suzuki偶联反应得到单体7;步骤(vii)由单体7和三苯胺硼酸酯进行suzuki偶联反应得到前驱体3。至此,三个目标前驱体都已完成。
【反应路线图一】如图18所示。
实施例2:化合物a的合成
【反应路线图二】如图19所示。
根据反应路线图,四溴螺芴通过联硼酸频那醇酯、二价钯催化、二氧六环溶剂条件下得到螺芴四硼酸酯单体;螺芴四硼酸酯、前驱体1进行suzuki偶联反应得到四臂螺芴前驱体;通过丁基锂实现溴代丁基苯的锂化,锂基丁基苯进攻羰基活性位,最后通过三氟化硼乙醚实现环化过程。具体实验过程如下:
步骤ⅰ:在氮气条件下,将2,2',7,7'-四溴螺芴(1.26g,2.0mmol),联硼酸频那醇酯(3.05g,12.0mmol),乙酸钾(1.88g,18.0mmol)和1,4-二氧六环(30ml)加入100ml反应瓶中,随后加入pd(dppf2)2(0.30g,0.4mmol)催化剂,在100℃条件下反应过夜。冰水淬灭反应,用二氯甲烷萃取有机相,去离子水洗两三次后,无水硫酸镁干燥,抽滤。真空减压浓缩粗产物,柱层析(淋洗液为dcm)纯化,得到螺芴四硼酸酯白色固体0.95g,产率58%。
步骤ⅱ:在氮气条件下,将前驱体1(318mg,0.44mmol),四丁基溴化铵(80mg,0.25mmol),螺芴四硼酸酯(60mg,0.07mmol),四三苯基膦钯(3mg,0.003mmol),nahco3(47mg,0.56mmol)和四氢呋喃(15ml)、水(8ml)加入100ml反应瓶中。85℃反应48小时。冰水淬灭反应,用二氯甲烷萃取有机相,去离子水洗两三次后,无水硫酸镁干燥,抽滤。真空减压浓缩粗产物,柱层析(淋洗液为dcm:pe=4:1)纯化,得到黄色四臂螺芴前驱体152mg,产率73%。
步骤ⅲ:在氮气条件下,将对溴丁基苯(554mg,2.60mmol)、干燥的四氢呋喃溶液(20ml)加入100ml反应瓶中,冷却至-78℃,滴加1ml丁基锂(2.5minhexane),反应1个小时后,将溶解于5ml四氢呋喃中的四臂螺芴前驱体150mg滴加入反应瓶,反应缓慢升温过夜。冰水淬灭反应,用二氯甲烷萃取有机相,去离子水洗两三次后,无水硫酸镁干燥,抽滤。真空减压浓缩粗产物,柱层析(淋洗液为dcm:pe=1:1)纯化,得到黄色透明胶体120mg。将黄色胶体溶解于20ml二氯甲烷溶液中,然后滴加0.2ml三氟化硼乙醚,室温条件下反应搅拌30分钟。冰水淬灭反应,用二氯甲烷萃取有机相,去离子水洗两三次后,无水硫酸镁干燥,抽滤。真空减压浓缩粗产物,柱层析(淋洗液为dcm:pe=4:1)纯化,得到绿色梯形化合物105mg,产率53%。
1hnmr(400mhz,cdcl3,δ):7.63(s,4h),7.47(s,8h),7.43(d,j=8.3hz,4h),7.19(d,j=8.2hz,16h),7.16–7.10(m,20h),7.06–6.96(m,52h),6.95–6.87(m,28h),2.63–2.54(m,16h),2.45(d,j=6.0hz,16h),1.67–1.58(m,16h),1.44(d,j=7.5hz,32h),1.29(d,j=7.2hz,16h),0.95(t,j=7.3hz,24h),0.86(t,j=7.3hz,24h).13cnmr(100mhz,cdcl3,δ):153.55,152.06,152.03,150.93,148.87,147.65,146.86,143.62,143.17,141.67,140.81,140.65,140.58,139.44,139.35,135.16,129.02,128.63,128.32,128.23,128.09,128.00,123.78,123.42,122.42,120.42,117.81,117.09,117.01,116.67,64.60,64.56,64.32,35.48,35.26,33.67,33.51,22.72,22.45,14.06,13.96.maldi-tofms(m/z):calcdforc289h276n4,exactmass:m+3805.31;found:3804.648(m+).
实施例3:化合物b的合成
【反应路线图三】如图20所示。
化合物b的合成方法与化合物a的合成方法类似。
1hnmr(400mhz,cdcl3,δ):7.66(s,4h),7.60(d,j=5.5hz,8h),7.51(d,j=12.9hz,8h),7.46(d,j=8.3hz,4h),7.27(s,4h),7.25(d,j=2.5hz,8h),7.21(d,j=7.6hz,12h),7.11(d,j=16.1hz,56h),7.03–6.87(m,36h),2.68–2.59(m,16h),2.43(d,j=8.2hz,16h),1.72–1.63(m,16h),1.50–1.39(m,56h),1.27(t,j=7.2hz,16h),0.99(t,j=7.3hz,24h),0.83(t,j=7.3hz,24h).13cnmr(100mhz,cdcl3,δ):155.44,152.98,152.17,151.94,151.76,151.72,148.89,148.22,148.00,146.99,143.74,143.65,141.80,140.84,140.71,140.61,140.07,139.80,139.03,138.49,134.54,129.17,128.75,128.35,128.16,128.06,123.89,123.55,122.47,120.51,118.86,117.77,117.30,117.15,116.80,114.02,64.63,64.38,64.35,46.48,35.54,35.30,33.71,33.52,27.35,22.76,22.51,14.09,13.95.maldi-tofms(m/z):calcdforc325h308n4,exactmass:m+4269.95;found:4268.824(m+).
实施例4:化合物c的合成
【反应路线图四】如图21所示。
化合物c的合成方法与化合物a的合成方法类似。
1hnmr(400mhz,cdcl3,δ):7.52(d,j=8.4hz,28h),7.27–7.14(m,56h),7.14–6.87(m,128h),2.67–2.38(m,64h),1.70–1.58(m,64h),1.50–1.32(m,64h),0.89(d,j=8.1hz,96h).13cnmr(100mhz,cdcl3,δ):153.55,152.24,152.23,152.03,151.84,151.75,151.36,150.71,148.81,147.85,147.67,147.00,143.65,143.54,143.49,143.13,141.79,140.97,140.80,140.71,140.68,140.46,140.09,140.01,139.92,139.58,139.47,134.99,129.07,128.75,128.46,128.24,128.14,126.72,123.89,123.73,123.67,123.38,123.36,123.35,123.32,122.53,122.42,122.13,122.11,120.53,117.76,117.64,117.46,117.22,64.61,64.36,64.29,64.21,58.19,35.49,35.24,35.17,33.58,33.46,33.27,22.75,22.56,22.46,14.06,13.97,13.90.maldi-tofms(m/z):calcdforc505h500n4,exactmass:m+6625.40;found:6625.429(m+).
实施例4:有机激光器件的制备
石英片经过超声波清洗,采用甲苯做溶剂,发光主体采用化合物中任意一种,制备20mg/ml的溶液。采用旋凃的方式制作,旋涂条件为1000转/min,膜厚100nm。其中,化合物a的pl光谱的发射峰454nm和478nm,fwhm大约为90nm。ase峰在483nm;fwhm在4.0nm左右;ase阈值0.62kw/cm2(3.11μj/cm2)。材料a光学增益参数随激光能量有一定幅度的变化,在136cm-1-178cm-1之间,最大增益参数178cm-1;材料b光学增益参数在117cm-1-179cm-1之间,最大增益参数179cm-1;材料c光学增益参数在149cm-1-192cm-1之间,最大增益参数192cm-1;是目前有机激光半导体中得到最好结果的材料体系之一。
实施例5:有机非线性光学测试
制备化合物a、b、c的5×10-5mol/l甲苯溶液,将其置于比色皿中。用波长可调节的飞秒激光进行泵浦,并采用饶丹宁6g作为参照样,通过发光强度的变化得到化合物a、b、c的双光子吸收截面。其中材料a的最大双光子吸收截面为1154gm,材料b的最大双光子吸收截面为3856gm,材料c的最大双光子吸收截面为9188gm。材料c的双光子吸收截面是目前有机上转化体系中最理想的结果之一。
实施例6:上转换受激辐射测试
制备化合物a、b、c的3×10-3mol/l甲苯溶液,将其置于比色皿中。用波长可调节的飞秒激光进行泵浦,观测上转换受激辐射现象。其中材料a的双光子受激辐射阈值为0.19μj,发光波长为477nm,发光半宽为7.0nm;材料b的双光子受激辐射阈值为0.16μj,发光波长为485nm,发光半宽为6.9nm;材料c的双光子受激辐射阈值为0.08μj,发光波长为489nm,发光半宽为6.9nm。化合物a、b、c的上转换受激辐射效率分别为6.0%,8.7%和3.7%。
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所做的改进和变换,均应为等效的置换方式,都包含在本发明的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!