经由动态光学投影的无分层生物打印及其用途的制作方法
本申请要求2014年5月20日提交的美国临时申请号62/001,025的权益,该临时申请通过引用以其全文结合在此。
政府权利
本发明是在由美国国立卫生研究院授予的基金号EB012597下的政府支持下进行的。政府对本发明具有某些权利。
发明领域
本发明涉及一种用于微制造光聚合物的三维结构和用于制造具有平滑(无分层)轮廓的生物支架的方法。
发明背景
传统的细胞培养通常在培养皿中进行,并且更普遍使用的细胞生物技术依赖于培养的细胞在2D平台上的使用。众所周知,细胞基底的机械特性影响细胞的分化、生长和能动性。因此,当设计细胞支架时,材料的机械特性是重要考虑的。为了模拟实际的细胞环境,有必要使用3D生物制造方法而非2D图案化方法创建3D功能组织模型。此外,制造过程和/或材料必须是细胞友好型的。用于生物支架的目前制造系统利用了诸如生物喷墨打印和光栅激光投影的方法,这些方法在可扩缩性和速度方面是受限的,并且不能创建复杂结构和可扩缩的组织构建体。浇铸方法可以实现基本几何结构,但不能复制具有复杂仿生特征和纵横比的复杂3D几何结构。激光微光固化快速成型(激光-μSL)技术已因它们创建3D支架的能力而变得流行[马皮力(Mapili)等人,2005;甘赛尔(Gansel)等人,2009]。然而,使用激光-μSL的支架制造通常由于逐点的激光扫描而较慢。许多现有的逐层式光固化快速成型方法的特征不在于动态变化的掩模和同时发生的载物台移动,并且因此产生不希望的层伪影(artifacts),这些层伪影可以改变细胞应答并且不反映出真实的天然生理学。
一种已被碳3D公司(Carbon3D,Inc.)(雷德伍德城(Redwood City),加利福尼亚州(CA))商业化用于浸没式打印聚合物纳米结构的方法涉及将图像投影通过液体树脂贮存池的透明底板,同时当树脂固化在基底的底部上时逐渐地将浸没的基底抬离底板。池的透氧透明底板使得溶解氧的“死区”抑制池底板处的聚合。碳3D系统中使用的技术描述在授予约瑟夫·德西蒙尼(Joseph M.DeSimon)等人的许多美国专利(公布的和等待审批的)中,包括号8,263,129,该专利通过引用结合在此。碳3D系统的贮存池和基底保持静止,其中仅浸没的基底在z轴线内移动以在打印行进时将打印的对象抬离底板,这限制了可以创建的形状的多样性。此外,技术对浸没的依赖性限制了可以使用的材料的类型和组合。
常规的光固化快速成型方法并不非常适于复杂的细胞支持性3D微结构的高通量制造,特别是在生命科学中普遍使用的基底诸如多孔板内尤其如此。这些缺点严重限制了3D打印细胞培养方法的广泛采用,因为研究者常常依赖于被配置成与已建立的实验工作流程成为一体的普遍使用的实验仪器接口的产品。多孔细胞培养板(除显微载片、培养皿、细胞培养烧瓶等之外)常常用作在上面设计专门培养环境的事实标准。在多孔板内,许多3D水凝胶细胞培养平台特征在于生物相容性和/或生物衍生的材料,这些材料是已聚合的或以其他方式制造的,但是典型地作为非图案化的体结构。类似地,还在多孔或标准显微载玻片形式上开发了具有集成的微流体或多电极阵列的高通量细胞培养系统。
能够直接打印到多孔板中的商业3D生物打印机可以从许多公司购得,包括来自Advanced Solutions公司(路易斯维尔(Louisville),肯塔基州(KY),美国(US))的BioAssemblyBotTM生物打印机、来自Cyfuse生物医学公司(东京(Tokyo),日本(JP))的生物打印机、以及来自Invetech公司(墨尔本(Melbourne),澳大利亚(AU))的NovoGen MMXTM生物打印机。这些系统使用光栅扫描方法(即“喷墨样”)经由生物材料的挤出来制造3D构建体,并且因此遭受可扩缩性、分辨率以及材料选择方面上的固有局限性。
高度限定的3D细胞培养微环境可以用于宽范围的生理情境中,包括体外的神经元培养。研究分离的神经培养物的目标是检验并探查可以代表生理相关模型的简单的体外系统。分离的神经培养物是神经科学研究的基石,但是它们反映天然生理学的实用性由于它们固有的不确定的连通性而受限。虽然详述单层神经元的功能的大量神经生理学数据广泛可得,但是用于这些培养物的条件与天然组织中存在的条件是显著不同的。因此,可合理地假定2D培养物的行为不是体内神经生理学的复杂系统的良好代表。
近期工作证明,与2D培养物中生长的神经网络相比,具有掺入的神经胶质的3D支架中生长的神经元提供了显著的形态学和电生理学差异。这归因于以下事实:3D神经支架更类似于体内存在的复杂神经环境。
神经回路的体外复制可以有助于说明神经环境的基本部分并且有利于对较高水平的过程有影响的连通性模型的测试。此外,当针对体外疾病模型而采用患者特异性诱导性多能干细胞(iPSC)时,控制神经群体的功能排布可能对重建相对于病理性神经回路的正常神经回路是关键的。用于神经元图案化的常规装置常常限制于2D情境并且使用未反映出天然机械化学特性的基底。另一方面,产生软的3D支架的方法可能是昂贵、费时或受限于简单的几何特征的。考虑到目前平台的局限性,需要建立用于在更具有生理代表性的软的3D环境中确定性地控制和系统性地调查基本神经回路的网络动态的高通量装置。
针对系统性增加的复杂度将简化的神经回路工程化成具有适应性提供了用于研究神经布线(wiring)和功能连通性的有吸引力的模型。经由体外的表面微电极阵列的电流高密度记录和刺激提供了关于网络状态的丰富信息,并且鉴于它的高通量性质,体外模型的实用性还延伸至药物筛选。培养神经元和导向神经生长的近期创新对网络连通性、细胞密度以及神经表型提供一些控制以便实现网络的某种次序和简明性。值得注意地,其中神经元生长在水凝胶支架(具有至少10个细胞直径的厚度)内的3D培养的出现已经用于通过以下项解决了2D模型的局限性:1)维持更相关的细胞-细胞/细胞-基质相互作用,2)使神经元免受培养基pH变化的影响,3)采用比2D培养中的硬基底更反映出天然生理学的机械上较软的界面,以及4)为生长和迁移提供了高表面积。因此,3D构建体对分离的神经网络的研究进展和生理相关的“大脑芯片(brain-on-a-chip)”系统的发展是必要的。此领域的新进展证明了在3D支架中维持神经元数周同时导向神经生长呈可控的几何图案的可能性。然而,在以下方面仍存在挑战:1)在记录和刺激方面实现高空间分辨率和高密度,2)简化昂贵且费力的制造技术,以及3)产生神经元和神经胶质的非均质共培养物,已证明这对神经元的正常功能是关键的。
发明的简要概述
在一个示例性实施例中,提供了一种用于快速产生具有高度指定的3D几何结构的聚合物支架的方法和系统。本发明的生物制造方法在此称之为“经由动态光学投影的无分层3D打印”或“L3PDOP”。本发明的L3PDOP 3D打印系统和方法可以接收包括一种3D计算机产生的模型的一个输入并且由此模型产生具有高分辨率的多种可光聚合材料的结构。本发明的3D打印系统使用一种动态控制的DMD(数字微镜设备)来反映出UV光在一种可光聚合基底上的一种高分辨率图案。与定制计算机软件的集成允许对投影图像和线性载物台的同时且连续的控制,该线性载物台控制基底相对于投影光的焦平面的位置。由于载物台的连续移动,制造的3D结构在Z(垂直)方向上具有平滑(即无分层)轮廓。通过控制预聚合物溶液的组成,例如通过包含天然衍生的和/或合成生物材料、生物活性分子、非均质的细胞群体,模拟天然组织环境的3D结构可以在数秒内产生。此外,微镜阵列的快速控制经由遍及聚合物的瞬时UV暴露的时空图案化提供了局部材料特性(诸如孔隙率和材料刚度)的微米级和亚微米级的变化。
根据本发明的实施例,用于3D微制造的一种系统和一种方法通过以下方式提供:将能够引发光聚合的光朝向一个空间光调制器投影,该空间光调制器调制响应于对应于结构的层的数字掩模的光。投影光学器件将调制光聚焦在支持于一个载物台上的一种可光聚合材料内的一个光学平面上。一种计算机控制器使得该空间光调制器投影出对应于这些数字掩模的一种图像序列,同时协调该载物台的移动以移动该光学平面在该可光聚合材料内的位置以依序投影出该序列的每个图像从而通过逐渐地光聚合该可光聚合材料产生该结构。
本发明的方法和系统经由对一种微镜阵列(DMD)以及一个线性载物台的动态连续控制提供了一种新型光固化快速成型方法。确切地,该设备由于它的速度、可扩缩性和无分层Z分辨率而实现对当今技术水平的改善。通过提供无分层分辨率,制造的结构未表现出使用涉及该线性载物台向一个新高度位置的离散移动的传统的逐层制造方法产生的平面伪影。此外,本发明的L3PDOP 3D打印平台提供了高度指定的仿生结构的快速且可扩缩的制造。此方法提供了使用采用基于光栅的打印方法或软平板印刷术技术的现有技术不能较好实现的在速度和可扩缩性方面的能力。此外,因为L3PDOP系统几乎可以接受任何一组高清晰度图像,此平台提供了一种用于产生不仅在细胞类型方面具有特异性而且具有整个组织形态的模型的方法。平台的适应性允许复杂3D构建体的不同组件的模块添加和随后的去偶合,从而提供一种用于确定材料类型、共培养物群体、空间细胞排布以及仿生几何结构的单独贡献的手段。用于该装置的操作模式包括生物基底经由动态光固化快速成型的3D微米级生物打印,和具有高的时空分辨率的神经元的光遗传学控制,以及伴随着的同时发生电生理学和荧光成像的集成能力。光固化快速成型的3D生物打印允许多种生物相容性材料(例如PEGDA、MeHA、GelMA)的光聚合并且有利于这些结构内的细胞封装。此外,这些材料-以及它们的掺入的细胞类型-可以非均质地用于相同支架中以提供3D图案化的共培养基底,从而有利于研究多种细胞表型之间的相互作用,例如神经元/神经胶质相互作用。
因为该微镜阵列的单个像素可以在整个制造过程中进行快速地开启和关闭,聚合物结构在孔隙率或材料刚度方面的高度局部化(例如亚微米)的变化可以通过像素水平的UV暴露的时空控制来实现。此平台通过以下方式解决了本领域中的局限性:允许对支架组成、微结构、和较大尺度的3D几何结构的同时控制以及提供速度和可扩缩性的改善。
在本发明的一个方面,使用含有用于抑制光激活的自由基聚合/交联的自由基吸收剂的一种预聚合物溶液来限制固化深度。可以对可由蓝宝石或玻璃(或任何其他足够刚硬的光学透明材料)组成的窗口施加一种表面处理以防止该结构聚合/粘附在浸没的窗口上。这与碳3D方法相反,其中使用本发明平台的打印直接发生在池的底板上,这与直接发生在浸没探针上相反。这使得3D结构快速打印在多孔板的每个孔内,因为该板在X-Y轴线内平移以进行孔至孔之间的移动。通过不依赖于单个大型池的浸没,每个孔可以含有一种不同的聚合物组成并且可以最终保持一种不同的3D结构。
在本发明的另一个方面,该方法和该设备可操作用于记录多个域上的网络活动。例如:1)多个电极阵列(MEA)-在它的上面打印3D神经元网络结构(或任何电活性的细胞类型)-允许与光遗传学刺激同时发生的电活动的正交记录;并且2)电压敏感的染料和蛋白质的荧光成像(这提供了提高的网络活动中的单个细胞分辨率)可以通过采用用于生物打印的相同或类似光源来同时进行。
在本发明的3D打印方法和系统的一个应用中,通过集成3D非均质神经培养物、光遗传学-激活的高分辨率刺激、以及并行的神经活动的电记录和基于图像的记录来产生一种大脑芯片。本平台中利用的制造方法提供对神经环境的形貌复杂度和细胞及材料组成的控制,从而允许系统控制的复杂度增加的可能性。
在本发明的一个方面,一种用于一种结构的3D微制造的系统包括一个光源,该光源被配置成用于将光投影在一条光学路径内,该光源发射被配置成用于引发光聚合的一种波长下的光;一个空间光调制器,该空间光调制器设置在该光学路径内并且被配置成响应于对应于该结构的层的一组数字掩模来调制来自该光源的光;投影光学器件,这些投影光学器件被配置成用于将该调制光聚焦至一个光学平面;一个载物台,该载物台被配置成用于支持与该光学平面内的可光聚合材料接触的一个基底,其中该载物台被配置成沿至少一个轴线移动;以及一个计算机处理器,该计算机处理器可操作用于:控制该空间光调制器以投影出对应于该组数字掩模的一种图像序列;并且协调该载物台的移动以移动该光学平面在该可光聚合材料内的位置以依序投影出该序列的每个图像,从而通过沿该至少一个轴线逐渐地光聚合该可光聚合材料产生该结构。在一些实施例中,该空间光调制器可以是一种数字微镜设备。该可光聚合材料可以是包含在一个容器内的一种预聚合物溶液,并且该系统进一步包括被配置成与该预聚合物溶液接触的一个透明窗口,其中该窗口与该预聚合物溶液之间的一个界面与该光学平面基本上是重合的。在一个实施例中,该载物台朝向该光学平面移动,使得该结构的连续层穿过先前聚合的层而突出。在另一个实施例中,该窗口被密封至一个管的一个末端以便浸没在该预聚合物溶液中并且该载物台远离该光学平面移动使得连续层聚合在先前聚合的层之上。该窗口可以进行处理以抑制该可光聚合材料的粘附并且可以由选自下组的一种材料形成,该组由以下各项组成:二氧化硅、蓝宝石、聚二甲基硅氧烷(PDMS)、透明陶瓷以及透明塑料。在一些实施例中,该容器包括在一个多孔板内的一个孔。该多孔板可以包括多个容器,其中这些容器的至少一部分含有不同的预聚合物溶液。
在其他实施例中,该基底包括一个电极或一个多电极阵列。在这些实施例中,该可光聚合材料可以是一种导电聚合物并且该图像序列的至少一部分对应于与一个或多个电极对准的互连结构。
该可光聚合材料可以是选自下组的一种可光交联的水凝胶,该组由以下各项组成:明胶甲基丙烯酸酯[GelMA]、甲基丙烯酸酯化的透明质酸[MeHA]以及聚乙二醇二丙烯酸酯[PEGDA]。
该系统可以包括设置在该光学路径内的一个第二光源,该第二光源发射被配置成用于刺激一种光活性生物材料的波长下的光。该系统还可以包括设置在该光学路径内的一个图像采集设备。
在一些实施例中,这些数字掩模的至少一部分可以被配置成使得该空间光调制器在该结构的所选择层内产生子图案。
在本发明的另一方面,一种用于一种结构的3D微制造的方法包括控制一个空间光调制器以投影出来自具有一条光学路径的至少一个光源的光的一种图案序列并且将被配置成用于引发光聚合的一定波长下的光发射在一种可光聚合基底上,其中该基底安装在被配置成沿至少一个轴线移动的一个载物台上,并且其中该图案序列对应于该结构的层;并且同时且连续控制该图案序列和该载物台移动以通过沿该至少一个轴线逐渐地光聚合该可光聚合基底产生该结构。该图案序列优选地通过从一个计算机控制器传送到该空间光调制器的一组数字掩模产生。
在一些实施例中,该可光聚合基底包括包含在一个容器内的一种预聚合物溶液,并且该方法进一步包括将一种透明窗口定位成与该预聚合物溶液接触以限定聚合平面。在一个实施例中,该载物台朝向该光聚合平面移动,使得该结构的连续层穿过先前聚合的层而突出。在另一个实施例中,该窗口被密封至一个管的一个末端以便浸没在该预聚合物溶液中并且该载物台远离该聚合平面移动使得连续层聚合在先前聚合的层之上。不同的载物台移动方向可以是组合的,其中一些结构由自上而下和自下而上的载物台移动的组合构建。
在一些实施例中,该容器可以是一种多孔板内的一个孔,该多孔板可以包括多个容器,其中该多个容器中的至少一部分含有不同的预聚合物溶液。在其他实施例中,该基底可以是一个电极或一个多电极阵列。该可光聚合基底可以是一种导电聚合物并且该图案序列的至少一部分对应于与一个或多个电极对准的互连结构。
该可光聚合基底可以是选自下组的一种可光交联的水凝胶,该组由以下各项组成:明胶甲基丙烯酸酯[GelMA]、甲基丙烯酸酯化的透明质酸[MeHA]以及聚乙二醇二丙烯酸酯[PEGDA]。
附图的简要说明
图1A是L3PDOP 3D打印系统的一个实施例的一个示意图;图1B是使用一个L3PDOP打印机创建的复杂几何结构的一组SEM图像。
图2示出了用于使用L3PDOP打印方法产生一种载满细胞的3D支架的一种示例性生产流程。
图3是一系列明视场显微照片和共焦荧光显微照片,示出了使用一种L3PDOP打印机制备的支架和与这些支架的细胞相互作用。
图4A-4C是一系列共焦荧光显微照片,示出了于该制造的支架的细胞相互作用。
图5是一组荧光显微照片(A-D),示出了不同的3D支架。
图6A是一种圆木桩支架的一个扫描电子显微照片;图6B是使用本发明打印平台的一种实施方式的血管微结构的一种光学显微照片。
图7是一种大脑芯片平台的一个图,该大脑芯片平台将集成3D非均质神经培养物、光遗传学-激活的高分辨率刺激以及并行的神经活动的电记录和基于图像的记录。
图8A-8C示出了本发明3D打印平台的一个替代实施例,其中图8A利用图解示出在一个多孔板中使用不同预聚合物的聚合物支架的打印,图8B提供了图8A的光学组件的一个详图,并且图8C利用图解示出用于一个3D支架的无分层打印的一种示例性生产流程。
图9A和9B示出使用图8A-8C的替代打印平台的实例,其中图9A是用于设计并且渲染两个不同的3D模型的CAD软件的屏幕截图,并且图9B提供了所得的打印水凝胶的显微照片。
图10A示出了由不同的光暴露子图案产生的一个简单立方体的内在结构的不同放大倍数的理论渲染;图10B示出了一种暴露图案如何可以产生不同的内在形态的实例。
图11提供了应用至复杂形状的不同棋盘格的图案化算法的显微照片。
图12提供了应用至复杂形状的不同棋盘格的图案化算法的显微照片。
图13A–13C分别示出了大鼠大脑的CAD设计和在不同“层”或“片”下的可能的子图案化排布。
图14示出了用于人类下肢模型的可能的子图案化排布。
图15是一个显微照片,示出了具有培养孔、互连路径/通道以及用于与一个MEA对准的电极位点的反向槽的GelMA支架。
图16是一组显微照片,示出了在使用相对于对照的不同GelMA浓度进行支架打印之后的在这些孔内聚集的NPC和延长的神经突。
图17是在本发明支架中的神经细胞培养物的一组显微照片,该本发明支架被标记以在一个月后相对于玻璃对照评估细胞形态、功能和突触连通性。
图18是在本发明支架中培养的神经元的一组显微照片,该本发明支架被标记以相对于玻璃对照评估功能连通性。
图19是在本发明支架中培养的神经元的一组显微照片,该本发明支架被标记以相对于玻璃对照评估突触蛋白表达。
图20A是使用根据本发明的一个实施例的神经簇压印的一个多电极阵列(MEA)的显微照片,其中插图是孔簇的中心的放大图像。图20B是该MEA内的通道12、19和20处测量的波峰活动的一个曲线图。图20C和20D是用于通道20的所选择时间序列的曲线图。
图21A和21B分别是使用标准平板电极相对于使用不同大小的3D打印的导电聚合物电极的一个示例性MEA的图解示图。
图22A-22B示出了使用本发明平台创建的、被构造成用于实现一种与逻辑门的一种示例性生物神经网络;图22C示出了随时间变化的一种示例性训练序列和测试序列;图22D示出了用于一种与逻辑门的一个真值表;图22E示出了一种示例性训练程序。
图23A-23C示出了使用本发明平台创建的、被构造成用于实现一种XOR逻辑门的一种示例性生物神经网络,其中图23A和23B示出了随时间变化的一种示例性训练序列;图23C示出了一种MEA的一个图;图23D示出了用于一种XOR逻辑门的一个真值表;并且图23E是在该神经网孔测试过程中产生的一组理论ROC曲线。
图24A和24B示出了一种示例性神经网络或感知器结构以及使用用于实施根据本发明的一个实施例的该神经网络或感知器结构的载满神经元的水凝胶压印的相应MEA板。
图25A和25B是根据本发明的一个实施例构建的一个神经网络计算系统的图解示图。
图26A和26B利用图解示出了通过本发明3D打印平台实现的定制MEA图案化能力用于平行样品的高通量筛选中的实例。
示例性实施例的详细说明
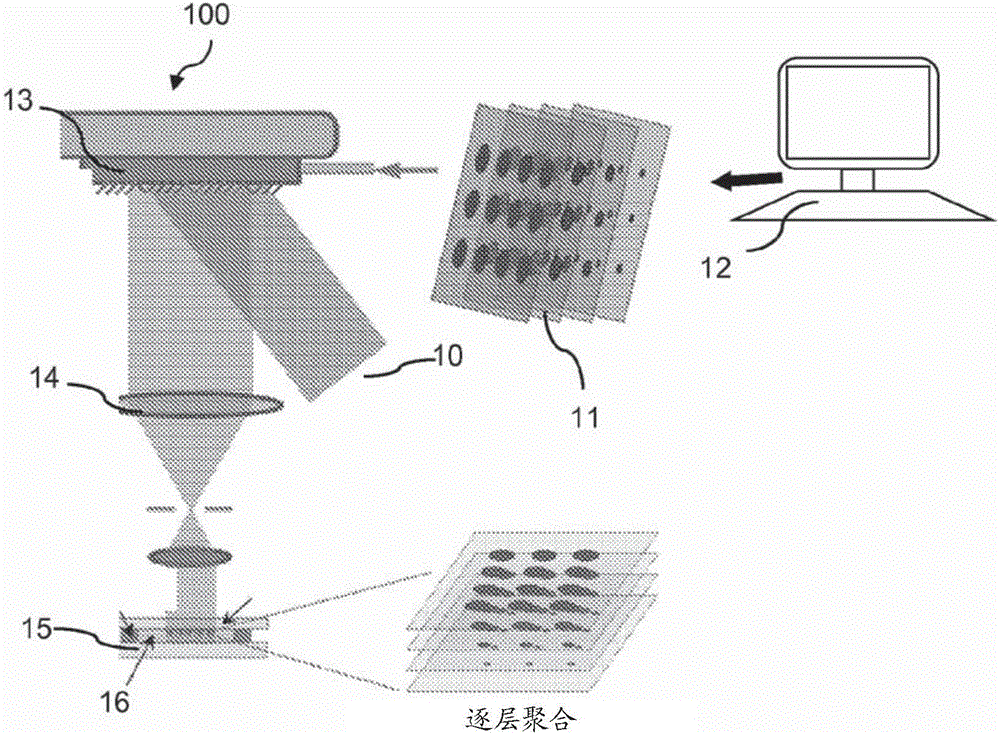
根据本发明的一个示例性实施例的一种L3PDOP 3D打印平台100的基本元件在图1A中示出:一个UV光源10、用于完成片状图像流产生即“虚拟掩模”11和系统同步化的一个计算机控制器/处理器12、用于光学图案产生的一个数字微镜设备(DMD)芯片13、一个投影光学组件14、以及用于样品位置控制的一个多轴线载物台15。由大约一百万个微面镜形成的该DMD芯片13调制该UV光并且将基于专门设计的计算机辅助设计(CAD)模型经由计算机12产生的一种光学图案投影在光聚合物溶液上。该光学图案通过光学透镜14投影出并且投影在光学敏感的生物材料16上以制造一个3D支架。通过使用一个机动化多轴线载物台15而同步控制的一种连续、逐层聚合过程制造复杂的3D结构。
在L3PDOP系统中使用的一个适当UV光源10可以选自不同来源,包括激光(CW或脉冲的)、汞球(弧光灯)、以及LED来源,该LED来源可以包括在一种波长下或跨越一系列UV波长进行发射的一系列LED。在一个示例性实施例中,可以使用一种脉冲锁模的飞秒激光器。该光源10可以包括响应于该计算机控制器/处理器12的可控参数,包括强度、光圈、孔径、暴露时间、快门以及波长。适当的操作参数的选择将取决于使用的材料和所希望的该支架的特性并且将在本领域技术人员的水平之内。
作为DMD芯片的一个代替方案,可以使用一个检流计光学扫描仪或一个多边形扫描镜。这两种技术均是可商购获得的,它们在快速扫描共聚焦显微镜中的应用是已知的。与本发明的系统和方法结合使用的一种适当扫描机制的选择在本领域技术人员的水平之内。
使用本发明打印系统产生的结构的实例示于图1B中,该图1B是具有复杂几何机构的PEG微孔的一系列扫描电子显微镜(SEM)图像,包括(b)分级式、(c)螺旋式、(d)胚胎样以及(e)花样。图1B(a)是(b)-(e)中所示的结构的阵列的一种组合。图1B图像(f)-(i)是(b)-(e)的该微孔的倒置,证明了L3PDOP打印方法的多功能性。
该掩模11在形式上类似于一组“PowerPoint样”幻灯片,并且可以根据CAD模型动态改变的以设计和制造多种多样的3D特征。本发明系统的一个显著优点在于它不需要使用有机溶剂,否则这些有机溶剂可以损害支架材料的生物相容性。本发明的3D打印技术对于高通量制造是理想的并且可易于扩缩,这是产生高体积筛选平台的一个必需要求。
图2A-2C示出了用于使用该L3PDOP打印系统100和该方法制造一个3D支架的一种示例性过程序列。如在图1A中示出的系统中,该系统100的基本元件是一个UV光源110、用于完成片状图像流产生即“虚拟掩模”111的一个计算机控制器/处理器(未示出)、用于光学图案产生的一个数字微镜设备(DMD)芯片113、一个投影光学组件114、以及用于样品位置控制的一个多轴线载物台115。将一种大分子单体溶液124中的细胞放置于由一个透明盖玻片128覆盖的一个腔室126中。在一个示例性实施例中,该盖玻片128是甲基丙烯酸酯化的玻璃。3D支架130a的聚合在该盖玻片表面128处开始,其中对应于来自DMD阵列113的掩模1.0的反射UV图像聚焦在图2A中所示的步骤1中的成像/聚合平面120处。从该支架的基部或底部部分130a开始,该支架与该盖玻片128是交联的,在一个连续过程中制造完整的结构。掩模1.0表示基部部分130a的基本形状,当该结构构建成倾斜边缘或弯曲边缘时,该掩模1.0可以在尺寸上逐渐变化,例如具有多个掩模,高达掩模1.0.n,被投影在DMD上。当伺服控制的平台115向上平移以使该制造的基部部分130a越过该聚合平面120时,DMD 113上的投影掩模转换为掩模2.0–2.0.n(图2B中所示的步骤(2))并且将该腔室126和该大分子单体溶液124的下一部分带进该聚合平面120中以形成该支架的第二部分130b。与基部一样,该掩模的尺寸可以是变化的以创建样品形状中的弯曲边缘和倾斜边缘。在步骤(3)中达到该支架的顶部130c,如通过掩模3.0–3.0.n确定的(图2c)。通过此序列,这些细胞可以被封装在用户限定的3D结构中。图2D利用图解示出了由图2A-2C中所示的步骤产生的示例性3D支架的俯视图(上面的)和侧视图(下面的)。
在本发明的一个实施例中,一个或多个图像采集设备可以包括在光学路径内以使得入射光或投影图像被转化为通过投影光学组件,从而使得该图像的焦平面与所述图像采集设备的焦平面重合。该图像采集设备可以用于捕获该入射光、该投影图像或通过所述基底发射、反射、透射或以其他方式转化的光的图案。适当的图像采集设备包括CMOS照相机、CCD照相机或显微镜,例如荧光显微镜。
构建L3PDOP微光固化快速成型(“μSL”)系统的原型以制造3D支架诸如管、导管、圆木桩和血管状结构。该系统已经用于由不同的生物聚合物来创建结构,这些生物聚合物包括用于3D支架的聚乙二醇二丙烯酸酯(PEGDA,用纤连蛋白功能化以便细胞粘附)、甲基丙烯酸酯化的透明质酸(MeHA)以及明胶甲基丙烯酸酯(GelMA)。这些精确工程化的仿生支架为对细胞与微环境的相互作用的研究提供了一个独特平台。封装的细胞在该支架表面上和在这些结构内部两者的所有几何结构中展示出了良好的细胞活力。在整个较大尺寸的图案上,细胞各个地以及共同地响应于几何提示。
图3提供了对复杂的3D几何提示的细胞响应的实例的显微照片,展示出了与这些支架的动态相互作用以重塑这些结构的位置和形状。上图(a)示出了制造后12小时的具有封装的NIH/3T3细胞的GelMA(明胶甲基丙烯酸酯)支架。第二图(b)揭示出如封装后四天所观察到的这些结构的变形。图(c)是共焦荧光显微照片的一种3D重构,表明了该支架的高度依赖性变形,如通过两种花结构(图(b)的第三幅图像)上的细胞-细胞相互作用介导的。对细胞的F-肌动蛋白(红色)和细胞核(蓝色)进行染色。在图(d)中,如图(c)中所示的同样花结构的单个Z剖面展示出了在从这些结构的底部至顶部向上行进时的高度依赖性变形。所有比例尺为100μm。
图4A-4C提供了仍封装在这些GelMA支架内的细胞的显微照片,表现出3D细胞铺展同时保持活细胞-材料相互作用。3D重构(图4A)和遍布该支架的不同Z平面处观察(图4B)的共焦荧光显微照片揭示出该支架表面上的NIH/3T3成纤维细胞展示出不同于这些结构内部的细胞的形貌。在图4B中,封装后四天仍嵌入该GelMA支架内的细胞表现出优先朝向封装结构的表面的伪足伸出。对细胞的F-肌动蛋白(红色)和细胞核(蓝色)进行染色。在图4C中,封装在GelMA支架内的10T1/2细胞表达出一种平滑肌细胞的表型,如经由对α-SM肌动蛋白的染色示出的,并且封装后8天保持细胞-材料相互作用,如通过3D的伪足突起表明的。所有比例尺为50μm。
特征在于重建天然生理学的细胞组分和生物材料组分的高度复杂的3D仿生结构的微制造可以在临床环境中以及在基础研制工作内产生无数应用。以一种可扩缩和高通量的水平基于患者特异性解剖学提供组织构建体可以应对再生医学中的快速增长市场。复杂的支架几何结构可以用于细胞接种和/或细胞封装以提供导向干细胞分化和/或保持它们多能性的最佳条件。可建立商业服务以提供用于研究复杂3D几何结构和界面内的细胞响应的定制型高通量多细胞支架阵列。商业应用还可以更广泛以使用任何可光聚合的材料在数秒内提供微米分辨率的组分。这对仍在制造时间、特征分辨率和层伪影上存在局限性的目前快速成型系统提供了一种明显改进。
图5是一组荧光显微照片(A-D),示出了使用本发明3D打印平台由透明质酸构建的不同3D支架的实例。图6A是一个圆木桩支架的扫描电子显微照片并且图6B是使用本发明L3PDOP打印平台由GelMA制备的一种血管显微结构的光学显微照片。
用于产生用于该3D支架的L3PDOP打印的掩模的CAD模型通常由一系列数字图像切片组成。这些图像也可以衍生自MRI或CT扫描。使用控制计算机和适当软件,这些图像被自动并连续地逐一加载到该DMD芯片中,并且然后投影到这些可光聚合材料中以通过一种数字、连续的聚合过程形成3D结构。平台的适应性允许复杂3D构建体的不同组件的模块添加和随后的去偶合,从而提供一种用于确定材料类型、共培养物群体、空间细胞排布以及仿生几何结构的单独贡献的手段。因为该微镜阵列的单个像素可以在整个制造过程中进行快速地开启和关闭,聚合物结构在孔隙率或材料刚度方面的高度局部化(例如亚微米)的变化可以通过像素水平的UV暴露的时空控制来实现。
用于本发明系统的仪器(即DMD阵列、UV灯、线性载物台)可以经由使用Visual C++或Go(golang.org)或类似的面向对象的编程语言编写的软件控制。该软件可以提供一种图形用户界面,可以1)在本地执行且受控的独立计算机应用程序中实现,或2)实现为通过连接至该仪器并且经由互联网由远程客户端访问的一个服务器托管的基于Web的应用程序框架,这提供了对每个组件参数的集中控制,从而允许用户指定投影的图像序列、暴露时间/个图像、UV源的强度(光圈设置)、初始的载物台位置以及该结构的总高度。除可作为位图(.BMP)或.PNG(或等同形式)导入的图像序列之外,该软件还可以接受自定义语法格式化的基于文本的数据文件(.DAT文件),针对一个3D结构的每个体元(即x、y、z坐标),该软件指定阵列中每个微镜的镜状态(开启相对于关闭)。因此,3D结构可以不仅经由一种位图图像序列指定并且还经由一种算法/数学函数具体指定。此外,可以包括将一种3D结构的一种形貌位图表示变换为特征在于适当的语法的.DAT文件的能力。此外,该软件可以导入指定3D结构信息的任何其他标准化格式,例如STL文件。最终,该软件将优先沿X和Y轴线控制该载物台,这可以提供高通量、成批制造呈大阵列格式的多种几何结构的能力。
为了匹配生物组织的机械特性,可以使用天然衍生的明胶甲基丙烯酸酯(GelMA)水凝胶作为基体材料。(参见,例如,J.W.尼科尔(Nichol)等人,“满载细胞的微工程化明胶甲基丙烯酸酯水凝胶(Cell-laden microengineered gelatin methacrylate hydrogels)”,生物材料(Biomaterials)31,5536–5544(2010)。)将甲基丙烯酸酯部分添加至天然凝胶的侧基团能够实现该水凝胶的光聚合或光交联,从而允许支持细胞粘附和生长的复杂结构被工程化。
在一个合成GelMA的实验中,猪皮明胶(西格玛·奥德里奇公司(Sigma Aldrich))以10%(w/v)混合到磷酸盐缓冲盐水(PBS;Gibco)中并且在60℃下进行搅拌,直到完全溶解。将甲基丙烯酸的酸酐(MA;西格玛)以0.5ml/min速率添加到溶液中,直到在明胶溶液中获得MA的8%(v/v)浓度。将该溶液在50℃下搅拌1小时,然后用温PBS进行2x稀释并且使用12-14kDa截留透析袋(仕必纯实验室(Spectrum Laboratories))在40℃下在蒸馏水中透析一周以将未反应基团从该溶液中去除。在-80℃下将GelMA溶液冷冻过夜并且在一个冷冻干燥机(Labonco)中冻干一周。将冷冻干燥的GelMA泡沫储存在-80℃下,直到进一步使用。为了制备水凝胶预聚物,将冷冻干燥的GelMA大分子单体以10%或15%浓度混合到PBS中并且在60℃下进行搅拌,直到完全溶解。将光引发剂(1%(w/v),Irgacure 2959,汽巴精化(CIBA Specialty Chemicals))、UV吸收剂(0.1%(w/v),HMBS,(2-羟基-4-甲氧基-苯甲酮(benzphenone)-5-磺酸),西格玛)以及自由基淬灭剂(0.01%(w/v),TEMPO,西格玛)添加到该溶液以允许光聚合并且提供有效的固化深度和最佳的图案分辨率。为了评价固化程度,测量了GelMA大分子单体的FTIR光谱以用于与交联的GelMA比较,从而评估光谱变化的程度。
本发明的生物制造方法可以用于创建一个仿生的三层螺旋线支架。可以对支架结构参数(间距、高度等)进行优化以有利于营养素、氧气以及其他因子的递送。(a)GelMA溶液浓度、(b)UV暴露时间以及(c)UV强度的不同组合可以用于控制这些支架结构参数。也可以结合不同的生物化学因子(药物/生长因子或生物分子)以及3D生物结构排布。此功能支架允许夹带的生物分子的临时释放以有利于延长且依序的信号传导从而最优化细胞功能。3D仿生支架可以制造在一个玻璃载片或一个PDMS基底上。一种可伸缩的PDMS芯片可以用于评价机械应力如何影响该支架和该封装的生物材料的。
为了降低UV损害的可能性,可以使用一种近期发现的光引发剂,苯基-2,4,6-三甲基苯甲酰亚膦酸锂(LAP)。(参见,例如,B.D.费尔班克斯(Fairbanks)等人,“使用苯基-2,4,6-三甲基苯甲酰亚膦酸锂的PEG-二丙烯酸酯的光引发聚合:聚合速率和细胞相容性(Photoinitiated polymerization of PEG-diacrylate with lithium phenyl-2,4,6-trimethylbenzoylphosphinate:polymerization rate and cytocompatibility)”,生物材料30,6702–6707(2009)。)LAP提供更大的水溶性、365nm光源下的更高聚合效率以及最小细胞毒性。此外,LAP在400nm以上具有明显的吸收,这允许使用可见光的有效聚合。在其他实现方式中,可以采用具有跨越可见光谱中的其他波长的吸收的光引发剂。
可以在该3D螺旋式支架上进行张力测试以确定破坏应变、极限抗拉强度以及应变能密度。每个生物支架(2cmx1cmx0.5cm)可以置于配备有夹具和一个50N负荷传感器的一个英斯特朗(Instron)5542机器内。在0.05和0.2的范围内的三个应变循环的机械测试可以以2mm/min的应变速率施加到样品,直到失效。可以选择慢速率以最小化粘弹性效应。这些测量的结果可以与来自文献的天然组织进行比较并且指导这些支架的设计。
因为GelMA衍生自哺乳动物的细胞外基质(ECM),此生物材料应表现出低毒性和良好的生物相容性。然而,如果这些GelMA支架未实现为预期应用所希望的机械特性,则可以将透明质酸(HA)、天然衍生的非硫酸化的糖胺聚糖和细胞外基质的组分与GelMA组合使用。成纤维细胞也可以掺入在同一或替代层中以制造多细胞空间分布的环境。
本发明的打印系统和方法的一个重要目标是提供一个生物制造平台的创建以使用例如小鼠心肌细胞和人类诱导性多能干细胞(hiPSC)衍生的心肌细胞开发具有集成的生物传感器的微组织芯片。本发明的打印平台允许3D、高度指定的仿生结构的快速且可扩缩的制造。此外,该平台的适应性允许复杂3D构建体的不同组件的模块添加和随后的去偶合,从而提供一种用于确定材料类型、空间细胞排布以及针对重演天然组织生理学的仿生几何结构的单独贡献的手段。细胞与它们的微环境-由细胞外基质(ECM)、水性环境、可溶性因子以及相邻细胞组成的相互作用-是细胞过程诸如迁移、分化、谱系特异性以及组织形态发生的基础。集成的感测能力将允许在高精度和这些细胞内部响应于它们的环境提示的分子协调的可视化的情况下对该细胞环境的操纵。
与目前可获得的3D打印机不同,根据本发明的实施例的动态光学投影打印机(即L3PDOP打印机)允许具有在接近纳米级分辨率下的完全限定的复杂3D几何结构的机械上软的生物材料水凝胶的无光栅、一次性、孔内打印。对于大多数材料类型和几何结构(具有3mmx5mmx1mm的总打印支架尺寸),用于单孔的打印过程可以在15至60秒中完成,从而允许在5至15分钟内的一个完整24孔板的打印。此外,该板内的每个孔可以预填充有具有不依赖于待制造的该几何结构的独特材料组成和/或浓度的一种可聚合溶液。通过多路传输在一个培养板内的不同孔上的这些不同参数,用于药物发现、临床诊断学以及基础生命科学研究的高通量3D细胞筛选平台可以使用用户说明书以有效的时间尺度按需制造。
在本发明的打印平台的一个实施例中,创建了一种工具以使用光固化快速成型法研究分离的3D神经网络,该光固化快速成型法允许对3D神经环境的组成和结构的精细控制同时实现高分辨率刺激和记录。此方法的效用对该神经网络的复杂度实现系统性控制并且有利于研究该神经环境与功能支架之间的复杂的相互作用。最终,将3D培养物与2D培养物的神经生理学进行比较的近期工作已显示出3D培养物表现出具有明显减少的同步化活动的复杂放电模式,这类似于体内网络中发现的放电模式并且与由2D培养物表现出的活动相反。这些发现表明在3D环境中可以完全改变分离的神经网络的经典且充分研究的行为。因此,本发明的平台代表对分离的神经网络的神经计算方面和随后它们用于研究神经系统的效用的目前理解上的显著进步。这些优点将基础神经科学研究影响为正常神经状态和病理性神经状态,同时还通过提供加速进展的疾病模型而有利于神经网络模型的临床翻译并且显著降低了用于折磨成千上百的个体的神经变性疾病和精神病学疾病的药物发现的成本。
在3D打印平台的一个实施例中,一种孔内高通量打印方法如图8A-8C中绘示的进行。在此方法中,与图2A-2C中示出的和以上参照图2A-2C描述的“倒置”方法相反,在目标基底内预聚合物溶液并非是完全隔离的。相反,该图像投影成使得它聚焦在光学组件82(在此实施例中,聚焦透镜88、准直透镜89和窗口91)的远端,其中窗口91(由一种透明材料诸如蓝宝石、玻璃、PDMS或其他适当材料形成)形成气密密封,该窗口91可以浸没在含有该预聚合物的多孔板80的一个孔80a(如图所示)内。仅出于说明目的,多孔板80示出为具有孔80a-80x,然而,可以使用任何数量的孔。此外,虽然在该图中标记两种不同的预聚合物(“预聚合物A”和“预聚合物B”)时,可以使用预聚合物的多种不同组合以在该支架内实现所希望的特性,如将在下文进一步描述的。通过相对于该窗口91向上或向下定位该板80,预聚合物的体积和目前打印层的高度是受控制的。重要的是,该窗口91用于消除打印界面90处的弯液面的形成,否则该弯液面可以使该投影图像失真。
参考图8C,该图8C利用图解示出了打印过程中时间t1、t2和t3的“快照(snapshots)”,当基底/载物台92支持的板80及它的孔被拉离该静止窗口91时,新鲜的预聚合物溶液经由毛细管作用引入加宽间隙中。此过程以一种连续方式发生,因为该载物台92平滑地平移越过该支架86的所希望高度并且产生最接近于该打印界面90的最新打印层,因此限定了“聚合平面”。虽然以“层”术语进行描述,该打印过程实际上是连续的,使得这些层也可以被认为是穿过连续结构的“切片”。图8C的左侧部分利用图解示出了在打印“层50”时的时间t1处聚合平面z1的位置。对应于时间t1/层50的插图示出了从DMD 84投影出的目前数字掩模。图8C的中心部分示出了在打印“层100”所处的时间t2处聚合平面z2的位置。对应于时间t2的插图示出了从DMD 84投影出的目前数字掩模。图8C的右侧部分示出了在打印“层161”所处的时间t3处聚合平面z3的位置。对应于时间t3的插图示出了从该DMD投影出的目前数字掩模。
在此打印方案下,投影光未如在以上所述的“倒置”方法中所做的那样透射穿过先前打印层来打印随后的层。除产生具有完全封闭特征的结构之外,此方法允许高很多的结构的打印。这与使用该“倒置”方法打印封闭腔或通道的尝试形成对比,该“倒置”方法常常由于该光必须穿过这些区域来打印随后的层而在这些“空隙”区域中产生不希望的聚合。但是,当与此基于浸没的方法组合时该“倒置”方法可以提供增加的效用,因为一个方法可以用于使用一种材料类型制造完整支架的子组件,而另一方法可以随后用于在同一支架内打印不同的材料。
使用非倒置方法的初始结果示出在图9A和9B中,其中图9A是用于设计和渲染两个不同的3D模型(一个侧边开口的立方体(左边)和一个开窗的圆柱体(右边))的CAD软件的一个屏幕截图。该打印在具有一个PDMS衬垫的一个标准显微载片上进行,该PDMS衬垫放置在该载片之上以限定含有预聚合物溶液的一个孔。最终打印的水凝胶(由PEGDA形成)示出在图9B中,清楚地反映了通过图9A中所示的CAD设计确定的所希望的形貌。
为了确保固化的支架对该基底的优选粘附(与光学窗口相反),目标玻璃基底可以进行化学修饰以促进打印结构与该载片或玻璃底的孔板的交联共价键合。在一个实施例中,使用了甲基丙烯酸酯化。此外,该光学窗口还可以进行表面处理以使它变为疏水的。关于窗口粘附的问题还可以通过自身的连续制造技术来部分地缓解,该连续制造技术具有以下优点:该基底未静止驻留在该打印界面处,在常规的逐层打印情况下发生该静止驻留。
与动态投影机制同步的该载物台的连续运动不仅允许“无分层”打印,而且还提供打印材料的分层式纳米图案化和/或微米图案化的能力。确切地,大尺度结构内的子区域可以使用时空光调制的不同序列进行“子图案化”。作为一个简单实例,如图10A和10B中的平板或立方体结构可以通过由稳态恒定式光强度或由间歇脉冲化光强度产生的相同投影平方的连续暴露进行打印。当该光是脉冲化或闪烁的时,可用于引发一个特定像素位置处的自由基聚合的光子通量可以是可变的。这转化成在相邻体元上的聚合动力学的非线性差异。当该载物台连续移动同时该光以此方式调制时,交联或聚合效率可以随高时空分辨率变化,从而在较大的简单体结构内实现材料特性的微米或亚微米图案化。
图10A示出了由不同的光暴露子图案产生的一个简单立方体的内在结构的理论渲染。在此情况下,该光以棋盘格的方式作为体元离立方体表面的距离的函数进行调制:较大的棋盘格用于该立方体的更内部的部分,而较小的尺寸用于该立方体的较接近该表面的区域。在图10A中,在全视图下面的下方图中的放大图像也展示出光的此子图案化如何可与在材料特性(诸如聚合效率、大分子单体浓度和分子重量等)方面具有不同的特性的预聚合物相互作用。这可以产生更精确详细的结构或可替代地产生更加散开的内部图案化。如图10B所示,相同的暴露图案(上方图像)可理论上产生不同的内部形貌(图10B的中心图像和下方图像所示的),这取决于使用的材料。图11和12提供了相同图案化算法的实例,例如不同的棋盘格,应用到更复杂形状例如圆环形。此子图案化可以应用到复杂的大尺度结构以局部调制孔隙率和扩散性。一个方法可以是增加阻碍低扩散速率的更多较深内部区域的孔径大小,从而“标准化”整个该体结构的扩散性。类似地,机械特性诸如弹性模数的局部差异可以进行图案化以影响封装在这些打印构建体内的细胞的死亡情况和表型。为了提供另一实例,该子图案化技术可如图13A-13C中所呈现的仿生实例中所示的那样应用,示出了大鼠大脑(图13A-CAD设计)和在不同“层”或“切片”处的可能性的子图案化排布(图13B和13C)以及人类下肢模型(图14)。
实例1:大脑芯片
以上所述的L3PDOP平台产生了两种强功能的操作模式,这些操作模式在图7中图解示出。第一模态72提供了经由动态光固化快速成型的生物基底的3D微米级生物打印。第二模态74提供了对具有高时空分辨率的神经元的光遗传学控制。使用参照图1A和图2A-2C所述的打印平台的光固化快速成型的3D生物打印(模型72)提供了多种生物相容性材料(例如PEGDA、MeHA、GelMA)的光聚合并且有利于这些结构内的细胞封装。此外,这些材料-以及它们掺入的细胞类型-可非均质地用于相同支架中以提供3D图案化的共培养基底,从而有利于研究神经元/神经胶质相互作用。
重要的是,本发明的平台不仅能够起到制造和光遗传学刺激模态的作用而且还用于记录多个域上的网络活动:1)多电极阵列(MEA)-在它的上面打印3D神经网络结构-允许与光遗传学刺激同时发生的电活动的正交记录;并且2)电压敏感的染料和蛋白质的荧光成像可以通过使用用于生物打印的相同或类似光源来同时进行,从而提高网络活动的单神经元的分辨率。
在此实例中,目地是产生一种大脑芯片平台,该大脑芯片平台集成3D非均质神经培养物、光遗传学-激活的高分辨率刺激、以及并行的神经活动的电记录和基于图像的记录。此外,本平台中利用的制造方法提供对神经环境的形貌复杂度和细胞及材料组成的控制,从而允许系统控制的复杂度增加的可能性。
研究分离的神经培养物的目标是检验并探查可以代表生理相关模型的简单的体外系统。虽然详述单层神经元的功能的大量神经生理学数据广泛可得,但是用于这些培养物的条件与天然组织中存在的条件是显著不同的。考虑到表明环境对神经功能的影响的大量文献,可以合理地假定2D培养物的行为不是体内神经生理学的复杂系统的良好代表。近期工作证明,与2D培养物中生长的神经网络相比,具有掺入的神经胶质的3D支架中生长的神经元提供了显著的形态学和电生理学差异。这归因于以下事实:3D神经支架更类似于体内存在的复杂神经环境。
实例2:来自iPSC的神经簇
本发明的L3PDOP平台在以下方面中存在无数应用:基础神经科学研究、临床诊断学、新型药物候选物的筛选、以及结合神经形态硬件(例如“大脑芯片”设备)对人工神经网络相对于生物神经网络的对比研究。本发明的打印技术实现支持iPSC衍生的神经元的培养的3D水凝胶的简易快速制造,具有以下能力:1)经由用于高通量支架制造的动态光学光固化快速成型的水凝胶微环境的3D图案化,该动态光学光固化快速成型与MEA以高精度共同配准;2)神经簇的定向排布和经由水凝胶组成、几何形状和尺寸对细胞排列、生长以及连通性的调制;3)对功能连通性的支持,如通过相关生物分子标志物的阳性表达所证明的,以及4)在神经群体的长期培养过程中的自发性电活动,该电活动与这些神经群体在3D打印的水凝胶-MEA基底上的空间排布对应。
在此所述的光固化快速成型的3D生物打印允许多种生物相容性材料的光聚合。例如,但不限制,此类材料包括明胶甲基丙烯酸酯(GelMA)、甲基丙烯酸酯化的透明质酸(MeHA)、聚乙二醇二丙烯酸酯(PEGDA))。该打印方法还有利于这些结构内的细胞封装。专门化的可光交联的聚合物的其他种类可包括导电聚合物,诸如PANI-PAAMPSA[聚苯胺-聚(2-丙烯酰氨基-2-甲基丙烷磺酸)]。(参见,例如,刘(Yoo)J.E.等人,“用于有机电子学的广泛应用的可直接图案化、高度导电的聚合物(Directly patternable,highly conducting polymers for broad applications in organic electronics)”),美国国家科学院院刊(PNAS),(2010)107(13),5712–5717)。此外,这些材料-以及掺入的不同细胞群体-可非均质地用于相同支架中以提供多组分3D图案化的共培养基底,从而有利于研究复杂的细胞-细胞相互作用和细胞-ECM相互作用。
对于神经祖细胞(NPC)的3D图案化,使用在DPBS中的5%至7.5%明胶甲基丙烯酸酯(GelMA)的可光聚合的大分子单体溶液制备水凝胶。经由上述的光固化快速成型技术,打印了具有不同半径(5至300μm)、深度(100至500μm)和通道宽度(5至50μm)的连通的微孔阵列。GelMA水凝胶支架用于培养并图案化iPSC衍生的NPC。UV光介导在图案化暴露的30至60秒内发生的聚合以产生支架5mmx3mmx100至500μm。使用安装在投影平台下方的一个显微照相机,通过平移该线性载物台使透明的MEA与从该DMD投影出的图像对准。具有预限定的培养孔、互连路径/通道以及用于电极位点的反向槽的3D GelMA支架与MEA精确对准以允许水凝胶的直接双面打印,如图15中所示。
当接种时,NPC在这些孔内聚集并且使得神经突沿着这些导向通道以不同程度延长,这取决于材料的含水量。GelMA的百分比浓度(5%相对于7%)对细胞铺展、分化、排列以及连通性具有实质性影响(图16)。在培养一个月后,支架固定在4%低聚甲醛中并且使用针对突触蛋白、VGlut1、MAP2、GFAP和β-III微管蛋白的抗体进行免疫荧光标记以评估细胞形态、功能以及突触连通性。如图17中所示,功能连通性的标志物表现出基于基底类型和图案化尺寸的差异,其中当相比于玻璃对照时,在该GelMA基底上的培养物中观察到较高水平的突触蛋白表达。也观察到VGlut1的稀疏表达,表明一些神经元早期定型为谷氨酸能表型。
为了进一步评估功能连通性,用针对麦胚凝集素(WGA)和绿色荧光蛋白(GFP)报告基因的质粒DNA转染神经元(图18)。神经元染色对WGA呈阳性而对GFP具有阴性表明WGA的突触后摄取通过WGA表达群体与非表达群体之间的功能连通性发生。此外,突触蛋白表达另外经由针对利用突触蛋白表达定位的GFP的共同表达的一种质粒进行评估(图19)。如先前论述的,相比于该玻璃对照(上图),在3D支架条件(下图)中看见更大的表达。
图案化的神经网络还展示出自发性、空间依赖性的电活动。当映射到记录通道时,与水凝胶孔内的这些神经簇的中心对应的MEA电极位置表现出最高的活动。如图20A-20D中所示,通道20(图20A的放大图段中的第3行,第8列)与MEA 200的右上角中大孔簇的中心对应(图20A)并且与附近的但在稀疏分布区域中的其他通道(例如突出显示的通道12和19)相比显示出高的活动(图20B)。以较短的时间尺度示出的波峰活动的子曲线(图20C-D)展示出具有局部场电位特征的波形图。这与放置在该MEA之上的水凝胶的建立是一致的并且反映出孔区域中的集成活动。
实例3:与3D打印的导电聚合物电极的集成
神经网络的高密度3D记录可以通过以下方式实现:使用在此呈现的光固化快速成型技术以精确的空间布置掺入生物导电聚合物(诸如PANI-PAAMPSA)以将神经电信号传输至多电极阵列(MEA)基底。图21A和21B分别示出了一种可能的空间排布和不同的电极长度。图21A示出了MEA 210中的一种简单格栅样阵列,其中具有类似高度的平板电极的行和列均匀间隔开,而图21B示出了从相同格栅延伸不同长度的电极212A-n。如本领域技术人员将容易清楚明白,可以通过选择适当的打印图案、条件以及材料来构建不同的几何布局和不同的电极高度。与MEA上的常规平板电极(仅可以直接获取可在3D神经网络的周边获得的有限网络动态数据)相比,3D打印的导电聚合物电极可以在内部探查在整个满载神经元的支架上的不同空间位置处的网络。此外,该导电聚合物电极可以提供用于一种模态的电神经刺激的一个导管,该模态正交于光遗传学介导的刺激并且因此可以独立地和/或同时地施加。这可能够根据对经由交替的刺激模态的同时发生的激活的网络响应研究神经元亚群体内的长时程增强(LTP)或长时程抑制(LTD)的影响。
实施例4:适应性、可重复编程的生物逻辑门、感知器以及混合的神经网络
与常规的冯·诺伊曼(von Neuman)体系结构相比,神经计算的合成模拟物在任务诸如视觉辨别和语言识别方面表现出高得多的性能。在认知科学和计算科学之内,已开发出神经回路的软件算法(例如,人工神经网络)和硬件实现方式(例如神经形态硬件)以使一种计算基底工程化为具有等效能力。这些技术已广泛应用于解决计算密集型问题,诸如数据挖掘、自动化的医学诊断以及自学的游戏策略,以及应用于揭示人类认知的不同维度之下的潜在机制。然而,这些合成系统的特定计算过程和学习算法真正表示它们的生物对应物的程度大部分仍是未知的。在此所述的集成的神经制造平台可以用于弥合此差距并且用于开发新型的混合人工/生物神经网络设备的技术,这些神经网络设备可以产生尚未通过分离的这些网络的合成或自然版本实现的计算能力。
使用在此所述的本发明创建一种生物神经网络的一个实施例是由两个输入节点221、222、一个输出节点223以及在每个该输入节点与该输出节点之间的两个通道224(即边,每图论)组成的一种逻辑门,如图22A所示。如图22B所示,每个节点含有包含多个(n≥1)不同类型的神经元的一种神经群体,包括下述的神经元:这些神经元在适当时用光响应性离子通道,例如通道视紫红质-2(ChR2)(敏感于蓝光)或盐细菌视紫红质(敏感于绿/黄光)进行光遗传学修饰以分别实现光介导的去极化或超极化。(参见,例如F.张(Zhang)等人,“神经回路的光遗传学询问:用于探查哺乳动物大脑结构的技术(Optogenetic interrogation of neural circuits:technology for probing mammalian brain structures)”,自然实验手册(Nat Protoc)5,439–456(2010)。)在图22B的实例中,使用了ChR2+和野生型ChR2-。每个通道可以导向从一个节点到另一个节点的神经突连接。一旦神经培养物成熟,此简单的神经网络的突触连通性可以用于响应于提供的输入例如一个经典的与逻辑门而输送一个指定输出。用于该与门的相应真值表提供于图22D中。图22C和22E示出了一种示例性训练方案,该训练方案可以根据以下各项进行指定:刺激模态(例如光学或电)、刺激持续时间、输入-输出刺激潜伏期、刺激强度、试验次数、试验中间间隔等,其中一定数量的试验限定了一个训练时期。图22C中的三行不同间隔的竖条表示由在整个一个示例性训练方案上的三个节点产生的尖峰光栅图,其中顶行和底行表示输入节点并且中间行表示输出节点。在竖条的一些子集之上跨越的水平线表示时间段,在该时间段期间针对那个特定节点进行光刺激。从图22C至22E引出的箭头指示不同的训练条件。在若干个训练时期后,该生物神经网络可以经由所声称的赫布型学习原则(Hebbian learning principles)(即突触可塑性)诸如尖峰-时间依赖性塑性改变它的连通性。
随后可以使用一种新的真值表重训练该逻辑门以将该网络变换为一种不同的逻辑门类型,例如将该逻辑门由一个与门变换为一个异或(XOR)门,其中当且仅当一个输入是“1”时输出才将是“1”(图23D)。XOR门训练序列示出在图23A(示出了MEA)并且23B(示出了相应的尖峰光栅图和光刺激的相关时间段)中,使用了蓝光(“B”)和绿/黄光(“G/Y”)。在此实例中,如图23C中所示,MEA 230被打印成在每个节点内以不同比例包括下述神经元,这些神经元用通道视紫红质(ChR2)和盐细菌视紫红质(NpHR)进行修饰以分别响应于不同颜色的光提供去极化/兴奋和超极化/抑制,以及包括野生型(“WT”,即非光激活的)兴奋性神经元和抑制性神经元(例如谷氨酸能(“Glu”)神经元和GABA能(“GABA”)神经元)的群体。实现足够的变换所需的时间或期数可以与该网络的不同特性相关。在一个训练时期结束时,可以测试一个输送的逻辑门以确定它的输出相对于所希望的真值表(图23D)的鲁棒性,并且它的性能可例如使用接收器工作特性(ROC)曲线(图23E)定量地描述。这些性能规格可以与刺激和/或物理节点参数相比较以得出描述这些参数对网络行为的影响的现象学规则。
在较大尺度下,该生物神经网络可以构建成含有多个数目的输入、输出和互连,以及最终将输入层与输出层连接的多个中间层节点。在此实现方式中,该生物神经网络可以类似于人工神经网络模型,例如一种感知器。一种感知器结构240的一个实例以抽象形式示出在图24A中,其中使用在先前实例中使用的相同修饰的神经元构建了输入层242、中间层244和输出层246(由接头248连接):通道视紫红质(ChR2+)和盐细菌视紫红质(NpHR+)加上野生型谷氨酸盐能(Glut)神经元和野生型GABA能(GABA)神经元。图24B利用图解示出了使用本发明的3D打印平台用满载神经元的水凝胶压印了MEA板240a以实现生物感知器240,该MEA板240a具有相应的输入层242a、中间层244a和输出层246a。连接这三层的节点的多分支格栅248表示在该水凝胶内打印的导向通道以有利于如将在图24A中的抽象说明的物理实现方式中实现的互连性。此生物感知器可以与它合成等同物相比较以确定体外实现方式与计算机模拟实现方式之间的对应程度。此外,这些节点的参数可以通过限定支架在制造过程中的几何形状来调整。可以在物理方面调制节点和连接通道,包括但不限于直径、偏心度、节点间距离、通道宽度以及通道的曲率半径。还可以在生物化学方面调制这些节点和这些连接通道,包括但不限于水凝胶组成、浓度、使用生物活性部分的官能化、生物活性分子的局部递送以及生物活性分子的光触发式释放。如通过示意图中的色调和不透明度的差异区分的,光249a-c的激活柱表示在光刺激方面的可能性调制,包括但不限于强度、持续时间、波长、脉冲数以及脉冲宽度。在更复杂的实现方式中,该网络可以含有例如多余的通道或不同形状的节点。与包括作为神经网络模型中的一个定义参数的组成性神经元的相对空间排布的这些神经网络的计算模拟的比较可以进一步解释神经元的空间3D图案化可以如何影响回路行为。
使用所述平台,可以在光学上通过将光投影在光遗传学修饰的神经元上或在电学上经由MEA界面提供神经刺激。在光遗传学激活的情况下,这些神经元可以进行修饰以产生下述群体,这些群体表达引发不同的电响应的不同的光敏感性视蛋白,例如用于去极化/兴奋的通道视紫红质-2(ChR2)相对于用于超极化/抑制的盐细菌视紫红质(NpHR)。通过在每个节点内以不同比例掺入野生型兴奋性和抑制性神经元的非均质群体,例如谷氨酸盐能神经元和GABA能神经元,以及发现于天然组织中或被合成工程化为表现出更多外来的或非天然实现的行为的无数中间神经元种类中的任一种,可以经由兴奋或抑制实现特征在于神经元间调制的网络动态的更多复杂模型。此外,这些神经元可以在掺入到3D支架中之前或之后经受光遗传学修饰。在后者情况下,支架材料可以经由3D图案化而被功能化以允许根据一种限定的空间排布的编码不同视蛋白的质粒的局部转染。最后,这些支架、网络和刺激参数可以结合其他环境变化来调制,诸如神经递质的光激活式解笼和可影响该网络的训练效率、鲁棒性以及总体动态的其他机械、化学和/或生物刺激的给予。
在另一实验范例中,评估该输送的生物神经网络的长期保真性可以提供关于它充当用于记忆的长期生物基底的能力的信息。在经受如先前所述的训练期之后,由若干体外生物神经网络组成的一个多孔MEA板或多分室MEA显微载片可以根据标准细胞培养方案维持培养一个延长的时间段。在限定的时间点例如1至4周之后,该网络的输出响应的保真性可以被量化以确定该输出响应的耐久性或易失性,即嵌入的记忆的持久性。集成的记忆和计算的此非冯·诺伊曼模型提供了用于人类认知的许多理论框架的基础并且近期已经在混合CMOS-忆阻器神经回路的情境下得以实现。
通过将此高通量多孔生物神经网络集成在一个较大的混合人工/生物神经网络系统之内,可以实现分层分布式计算算法以利用两种神经体系结构类型的特征或以将较大的复杂工作有效地分割成感知器特异性的单元任务。在一个实施例中,一个多孔板254的每个孔252a(见于图25B中)可以携带有一个独特的感知器250以响应于不同的刺激例如照射而执行一个特异性子任务。参考图25A,示出了一个单一示例性感知器250,在其中必须计算出颜色和字母符号例如蓝色“A”的一个辨别任务中,图25B中的一个孔252a可以含有一个携带的感知器250a以识别刺激的颜色,同时另一个孔252b包括识别该字母的一个感知器250b。可替代地,多个孔可以携带有相同感知器250以提供一种给定刺激的平行重复计算从而改进该系统的输出的集体精确性。多孔光学刺激可以通过多个DMD 256的同时发生的投影或通过使用在多个孔上快速扫描的一个镜式检流计来实现。总体而言,此方法类似于用于实现并行处理的多核心CPU的新式实现方式。此外,一个集成的计算机处理器258和伴随的算法可以用于实现更复杂的计算能力,包括但不限于1)一种闭路反馈系统,其中通过生物感知器提供的输出可以触发由该DMD 256投影出的照射图案的变化,或2)来自该生物感知器的输出提供了在该计算机内实现的一种人工感知器或神经网络中的输入以产生一种混合生物-人工神经网络。
在另一个实施例中,由于投影设备的高速能力,生物神经网络可以被输送以响应于更多的动态刺激,例如响应于自学习的视频游戏策略,大多是以这样的方式:人工神经网络已被设计成例如使用 DeepMindTM自学习这些任务类型。(参见,例如,V.明(Mnih)等人,“通过深度强化学习的人类水平控制(Human-level control through deep reinforcement learning)”,自然(Nature)518,529–533(2015)。)在一个实现方式中,光遗传学修饰的神经元的密集图案化的神经网络可以通过投影来自一种游戏诸如经典的视频游戏的视频内容(video feed)来输送。该视频游戏的投影帧可以输送该网络以“预测”一个球的轨迹并且因此提供输出以引导板末端处的控制杆的移动。通过在成功返回该球的若干时期内输送该网络,该生物神经网络可以自学习该控制杆的最佳布置以对点进行评分。此输送过程可以通过生物化学(例如多巴胺)或增强在成功的网络响应过程中形成的突触连接的其他刺激的同时给予来增强。这些大尺度的自学习生物神经网络的应用可以用于重现人类视觉系统的交织的记忆和计算机制。
实例5:系统神经科学研究中的典型神经回路的体外模型
分离的神经元群体的体外培养和询问形成了在整个神经科学研究中广泛利用的一种核心平台。正向工程化(即确定性地构建图案化的神经元连接)的能力为经由现有天然神经回路的反向工程化(即,不同尺度下的体外记录和大脑成像)衍生的连接组模型的确证性证据所必需的。贡献于假设性典型回路的解剖特征的真实重现依赖于以适当的相对空间排布系统性图案化非均质神经元群体的能力。在此所述的用于构建这些3D神经网络结构的独特方法具有提供使用常规的分离神经群体难以实现的系统性控制的复杂度增加的可能性。此外,经由导电聚合物电极的集成打印而结合的高密度3D记录实现对适当空间背景下的网络动态学的测量,同时使用了特征在于与体内组织的机械特性更接近的机械特性的软生物相容性水凝胶。使用反映出见于天然神经回路中的组成的神经细胞类型的非均质群体,在此所述的3D打印方法可以应用于创建典型的体内神经系统的区室化和/或系统性上降低的代表。然后这些体外构建体可以用于以一种更易利用的形式评估不同系统组件的功能意义以确定例如神经亚群体在较高水平的认知和行为中的单独贡献和集体贡献。
实施例6:诊断性的和药物筛选的平台
在研究神经病症诸如阿尔茨海默病或帕金森病的一个主要障碍在于在一个台式实验室环境中对它们的病理生理学精确地建模。虽然动物模型提供了对于体外疾病过程的有价值见解,但是伦理和技术的限制常常阻止实验结果完全转化到临床情景中。组织工程方面的新进展-尤其是3D生物打印和诱导性多能干细胞(iPSC)方面-为研究体外神经病理学提供了新方法。iPSC技术能够使研究者使用任何个体独有的成年细胞产生干细胞。这些iPSC可以分化为反映出对这些iPSC所衍生自的患者具有特异性的一种疾病表型的神经元。
在生物材料组成和机械化学特性方面类似于天然环境的3D培养环境可以产生更紧密地与天然系统对应的神经培养物并且因此提供改进的临床相关性。新出现的证据表明当相比于使用常规的细胞培养排布诸如培养皿产生的2D基底时,由生物相容性水凝胶组成的3D微环境有助于处于更精确地描绘患病神经状态的细胞(参见,例如,S.H.蔡(Choi)等人,“阿耳茨海默病的三维人类神经细胞培养模型(A three-dimensional human neural cell culture model of Alzheimer's disease)”,自然515,274–278(2014))。然而,在系统性图案化和探查3D神经培养物方面仍存在解释集体的细胞生理学与发出的电行为之间的关系的挑战。多电极阵列(MEA)和电压敏感性荧光成像,以及用于经由光刺激神经元的光遗传学工具是非常确实的用于记录响应于刺激的神经活动的技术,但是它们对体外3D系统的应用受到限制。
在本发明的一个实施例中,用于3D生物打印、光电刺激/记录以及荧光成像的集成平台应用于体外神经疾病模型的构建和询问。投影打印技术有利于以下两者:满载神经元的水凝胶直接在多孔MEA上的快速3D打印,包括可以购自阿尔法医学科学公司(Alpha MED Scientific,Inc.)(伯克利(Berkeley),加利福尼亚州(CA),美国(US))的MEDTM探针和可购自阿克松生物系统公司(Axion BioSystems)(亚特兰大(Atlanta),佐治亚州(GA),美国)的M768-KAPTM系列,以及随后对在高时空分辨率下的这些构建体的光学刺激,其中刺激图案与先前打印的3D几何结构之间具有精确对准。当相比于基于喷墨的3D生物打印时,使用本发明的光学3D打印技术实现对复杂形貌、复合生物材料/纳米材料、以及非均质细胞群体的具有较高通量的合并,并且具有针对与同时发生的电记录和电压敏感成像多路复用的光遗传学刺激的固有能力。控制3D排布、功能连通性以及动态活动的能力对正常状态和患病状态两者上的神经回路的体外表示提供了系统性评估。这些方法可以有助于解释病理性表型与涉及神经损伤的异常网络动态之间的因果关系。
在此方法的一个简单实施例中,特征在于通过单一通道连接的两个节点的一种连通性模型可以被构建,其中具有一定直径的一个节点含有相应比例数目的神经元的神经簇并且这两个节点之间的距离被调制以影响这两个节点之间的连通性程度。这两个节点之间的连通性水平可以根据形态排布(例如,每神经元的突触数目)和功能活动(例如,相互相关的尖峰/脉冲串活动)进行量化。其他实施例可以包括多个节点、每节点的附加通道、以及节点-通道几何形状和形貌排布的变化。根据这些定量测量的正常神经群体与患病神经群体之间的比较可以为评估疾病预后提供一种诊断性参考标准。用于连通性的标准化规格可以一种高通量方式在多孔MEA中进行评估,这些多孔MEA的特征在于相对于患病神经构建体的相同的正常神经构建体的复制品。具有结合的高度并行化的3D打印神经回路的这些多孔系统可以在用于神经病症的药物治疗的开发中用于筛选药物候选物。图26A和26B示出了供高通量筛选平行样品之用的通过本发明3D打印平台实现的定制MEA图案化能力的实例。此外,可以通过使用患者特异性iPSC-衍生的神经群体对潜在药物的效力和安全性进行评估,该评估具有患者水平的特异性。
实例6:基于云的3D生物打印和神经刺激平台
生物材料支架内的三维细胞培养已演变成结合天然组织微环境的无数方面,诸如形貌图案化、非均质的共同培养群体以及支架特性的动态调制。然而,尽管较新的3D方法提供了研究的新途径,但是更广泛生命科学对它们的使用受到限制。障碍包括用于实现复杂的定制设备所需的知识库和资本投资。研究协作经由资源分享而有助于克服这些困难,但是此类工作常常遇到交流和效率的挑战以及在长距离的样品和试剂转移中的物理瓶颈。团队可以常常很难与外包给一个协作的实验室的项目组成部分的实验细节保持同步。在3D生物打印的情景下,一个实验室的设计要求与另一个实验室的技术能力之间的不相连可以导致修订和返工的无效率循环,同时实验误差、丧失数据完整性以及误释结果的可能性增加。
为了解决这些挑战,可以使用一个Web应用程序框架来扩展在此呈现的集成的生物打印、光学投影以及神经刺激平台的(或一般的其他3D打印平台的)协作能力。此框架通过提供以下来使用用于目前和未来合作者的“基于云的”解决方案:
1)一种Web应用程序,该Web应用程序能够分享创建、说明以及修订3D设计的修订、相关的打印参数,和/或储存在该云上的神经刺激图案,以提高内部协作用户和外部协作用户的重复性和再现性;
2)针对该系统的Web应用程序的包括实验工作流程的扩展,使得关于样品制造过程和/或随后的刺激和/或记录以及任何其他上游制备(例如,试剂合成、细胞的遗传修饰、裸MEA基底的制造)和/或下游实验用途(例如,延长的细胞培养、药物给予、生物化学测定、共焦成像)的所有数据可通过基于云的服务器进行安全、远程和同时的访问;
3)该系统的多用户实时远程监测和控制,以提供该样品的原位视图并且能够实现关于支架的制造和/或刺激的实时评价和反馈以最小化设计修订和实验误差;以及
4)对一种图案化生物和/或混合(生物/人工)神经网络的计算能力的基于云的访问,如先前在实例4中所述的,该访问经由远程控制的输入(经由光学刺激或电刺激)和该神经网络的输出(经由MEA和/或成像)的远程读取,该远程读取作为用于输出该神经网络的学习序列的一部分或作为其中先前输出并最佳化的网络可以用于按需计算的一种分布式计算模型的一部分。
为了研究了解较少的非均质细胞群体之间的细胞-细胞相互作用,上述披露内容提供了在复杂3D生物制造和动态分子生物感测两者方面的新方法。本发明的3D生物打印平台提供了用于创建仿生的功能性组织的一种转化机器。生物传感器和单细胞成像应提供了用于研究活细胞中的空间和时间上的分子协调的强有力工具。高灵敏度/特异性的生物感测技术与3D仿生组织支架的集成将实现对精确工程化的物理/化学微环境中的蛋白质、酶、亚细胞器以及电活性的动态的高分辨率监测。微组织芯片模型的技术影响在于它用于早期药物筛选和个体化医疗的直接应用。对响应于药物的神经群体的神经毒性,或类似地,电活性心脏细胞类型中的心脏毒性的测量可以比当前可能早得多地在药物发现过程中解决苛刻的药物测试要求。此转化的微组织模型将显著降低药物开发的高成本,该高成本目前是持续医疗保健的进展的一个主要经济障碍。
- 还没有人留言评论。精彩留言会获得点赞!