一种间歇式、氨氮流加‑间歇式运行交替的硝化细菌菌群筛选和富集培养方法与流程
本发明属于水处理领域,特别涉及一种间歇式、氨氮流加-间歇式运行交替的硝化细菌菌群筛选和富集培养方法。
背景技术:
氨氮废水的大量排放可引发水体富营养化问题,其主要来源为生活污水、工业废水和农业用水。随着国内外水体富营养化趋势的日益严重以及相关部门对此问题的高度重视,消减外源成为控制水体富营养化的首要措施,为此兴建了大量的污水处理厂通过具体工艺对污水进行有效处理从而减少污染物质输入,且污水处理厂的出水标准越发严格。我国污水处理厂普遍要求严格执行《城镇污水处理厂污染物排放标准》(GB 18918-2002)一级A标准。
传统的生物脱氮过程为自养硝化和异养反硝化。(1)由氨氧化细菌(Ammonia-oxidizing bacteria,AOB)将NH4+氧化为NO2-;(2)由亚硝酸盐氧化细菌(Nitrite-oxidizing bacteria,NOB)将NO2-氧化为NO3-;(3)反硝化细菌将NO3-还原为N2。硝化细菌包括AOB和NOB,是实现生物硝化的核心细菌。相关研究表明,溶解氧(DO)、游离氨(Free ammonia,FA)和游离亚硝酸(Free nitrous acid,FNA)是影响AOB和NOB活性和生长的重要参数。AOB相对于NOB对溶解氧具有更强的亲和力,所以在低溶解氧环境中(0.5mg/L左右),AOB的竞争力强于NOB。DO浓度低于1.0mg/L时,AOB的生长速率比NOB约快2.6倍。而较高DO水平有利于NOB的生长和提高氨氮氧化速率。AOB比NOB承受FA的抑制能力更强,其抑制作用的阈值一般在10~150mg/L和0.1~1.0mg/L。另有研究显示,FA浓度大于6mg/L对NOB产生明显抑制。FNA对NOB的抑制作用比对AOB更加明显,FNA浓度高于0.02mg/L时,抑制NOB的代谢作用,高于0.10mg/L时开始抑制AOB的生长。
污水处理厂目前普遍采用A2/O工艺进行生物脱氮,实际中因运行条件所限,短程硝化难以维持,普遍为全程硝化。现有工艺的硝化反应速率较慢,冬季因水温降低反应速率下降明显,因此对技术进行升级具有极其重要的经济价值。因污水中硝化细菌浓度和硝化反应速率成正比,且反应速率直接影响污水处理工艺的处理效果,为此一些研究人员采用添加载体填料、细胞固定化生物活性填料或生物添加等方式增加反应器内硝化细菌浓度以提高硝化反应速率。此外常采用投加硝化细菌菌剂用于水产养殖业去除氨氮和亚硝酸盐。与纯种细菌相比,复合菌群因具有生物多样性而更易适应实际污水复杂的水质情况。
针对上述问题,开发出一种间歇式、氨氮流加-间歇式运行交替的硝化细菌菌群筛选和富集培养方法,可以获得在总细菌中占有数量优势同时实现高氨氮氧化速率和高亚硝酸盐氧化速率的硝化细菌菌群,为进行工业化硝化细菌菌群培养提供理论指导,在水处理生物硝化领域具有广泛的应用前景。
技术实现要素:
本发明的目的在于开发出一种间歇式、氨氮流加-间歇式运行交替的硝化细菌菌群筛选和富集培养方法,利用该方法筛选和富集培养的硝化细菌菌群,应用于水处理生物硝化领域,可以实现高氨氮氧化速率、高亚硝酸盐氧化速率、硝化细菌菌群在总细菌中占有数量优势等实际应用价值。为了实现上述状态,本发明采用了以下技术方案。
一种间歇式、氨氮流加-间歇式运行交替的硝化细菌菌群筛选和富集培养方法,其特征在于:培养后硝化细菌菌群在总细菌中占有数量优势并且可以实现高氨氮氧化速率和高亚硝酸盐氧化速率。
一种间歇式、氨氮流加-间歇式运行交替的硝化细菌菌群筛选和富集培养方法的具体实施步骤如下:
(1)以含有硝化细菌的活性污泥为接种污泥(本发明优选污水处理厂A2/O工艺回流污泥),白天采用间歇式、晚上采用氨氮流加-间歇式的交替运行方法,白天和晚上各一周期,分别记为A和B;A周期具体实施步骤如下:
1)采用每周期为N个批次的一次性投加基础培养液并反应的间歇式运行模式;在整个周期TA时间内,当天首批次开始向反应器内加入水和基础培养液提供反应底物溶液即为进水,之后各批次只加基础培养液中的氨氮化合物的溶液,每个批次进水后反应液的初始NH4+-N浓度记为[NH4+-N]A0;开启温度控制(本发明优选温度20~30℃)、pH(本发明优选pH7.0~7.5)、搅拌和曝气装置(本发明优选反应初始DO1.0~1.5mg/L)进行本批次反应;反应t时刻NH4+-N 浓度为[NH4+-N]At,使得[NH4+-N]At为[NH4+-N]A0的0.2~0.5倍,计算此反应段的接种污泥的氨氮氧化速率AORA;
2)每批次一次性投加的氨氮底物提供的进水氨氮负荷使得至反应体系内的初始NH4+-N浓度为[NH4+-N]A0(本发明优选[NH4+-N]A0为接种污泥氨氮氧化速率的3~4倍,即投加的氨氮负荷可在3~4h基本反应完全);当氨氮及过程生成的亚硝酸盐最后基本反应完全,即剩余氨氮浓度、亚硝酸盐浓度分别均为[NH4+-N]A0的10%以下,继续以负荷[NH4+-N]A0*(1±10%)投加氨氮下一批次并进行反应;每白天A周期内氨氮投加批次数N视每批反应历时tA确定,即N≈TA/tA;
3)每天选取一个批次取样以考察当天A周期的氨氮氧化速率AORA和亚硝酸盐积累率NARA;该批次刚投加氨氮后以及反应t时刻分别取样测定NH4+-N、NO2--N、NO3--N的浓度,记为[NH4+-N]A0、[NO2--N]A0、[NO3--N]A0、[NH4+-N]At、[NO2--N]At、[NO3--N]At;计算A周期的氨氮氧化速率AORA和亚硝酸盐积累率NARA;
4)随着氨氮氧化速率AORA提高,每隔几天(在每批次该氨氮负荷可以在一定时间(本发明优选时间2~3h)基本反应完全或连续2~3天氨氮氧化速率趋于稳定),提高每天A周期内各批次的氨氮负荷,使得提高后的首批次氨氮负荷为前一个氨氮负荷的1.2~2倍,以通过提高初始氨氮负荷提高氨氮氧化速率;
5)每个A周期结束,进行污泥沉淀、排水至低于当天的初始液位,以避免因各批次加基础培养液导致反应液体积增加对B周期试验的影响;
(2)B周期采用氨氮流加-间歇式运行,进行进水、反应、污泥沉淀、排水的间歇式运行模式,具体实施步骤如下:
1)氨氮投加分为两种方式,即进水时先通过投加氨氮作为反应初始底物,反应开始时再通过流加方式向反应器中连续补充氨氮;每周期开始向反应器内加入水和基础培养液提供反应底物溶液即为进水,进水后反应液的初始NH4+-N浓度记为[NH4+-N]B0(本发明优选浓度20~40mg/L);进行本周期反应、污泥沉淀、排水,每一夜为一周期;
2)氨氮流加即配制氨氮流加液于一储备器中、在每个间歇式运行周期连续不断地滴加供应于反应器内,即随着氨氮氧化的进行连续不断地补充氨氮,以此种方式尽量减小氨氮流加对反应液整体体积变化的影响;其中优选不同周期加入氨氮流加液的体积速率相同(所有周期的体积速率相同),可通过改变储备器中氨氮流加液的浓度(每个周期内的浓度相同),从而改变氨氮流加速率[NH4+-N]add;
3)为维持当天A周期的氨氮氧化速率AORA,另根据A周期的亚硝酸盐积累率NARA,B周期的氨氮流加速率[NH4+-N]add按照[NH4+-N]add=(0.9~1.3)*AORA*(1-NARA)进行计算,以实现通过氨氮流加每小时补充的氨氮量在一小时可以基本全部氧化为硝酸盐,而尽可能少的亚硝酸盐积累;
4)采用氨氮流加-间歇式运行,通过控制B周期氨氮流加速率和当天A周期氨氮氧化速率以及亚硝酸盐积累率的关系,控制整个B反应周期内反应液的NH4+-N、NO2--N浓度,即FA、FNA水平基本未对NOB产生抑制,以保证B周期的低亚硝酸盐积累率(NARB<25%为宜);
5)每个B周期结束后补静置24h以上去除余氯的自来水搅拌后,再重复进行污泥沉淀、排水过程,该过程称为“污泥清洗”,根据亚硝酸盐和硝酸盐积累量确定该“污泥清洗”过程次数,通过“污泥清洗”,剩余NO2--N浓度<30mg/L,NO3--N<200mg/L为宜;
(3)计算公式如下:
1)步骤(1)间歇运行A周期某一批次t时间反应段的氨氮氧化速率,视为A周期的氨氮氧化速率,计算如下:
式中AORA:某一批次氨氮氧化速率,mg/(L·h);
[NH4+-N]A0:某一批次初始NH4+-N浓度,mg/L;
[NH4+-N]At:某一批次反应t时刻NH4+-N浓度,mg/L;
t:反应时间,h;
2)根据步骤(2)氨氮流加-间歇式运行方法,本发明建立计算公式(2)和(3),每个B周期开始和结束时取样进行分析考察B周期的氨氮氧化速率AORB,计算如下:
式中AORB:每个周期氨氮氧化速率,mg/(L·h);
[NH4+-N]B0:每个周期初始NH4+-N浓度,mg/L;
[NH4+-N]add:每个周期氨氮流加速率至反应液,mg/(L·h);
[NH4+-N]Bend:每个周期反应结束NH4+-N浓度,mg/L;
t’:每个周期氨氮流加时间也即反应时间,h;
注:此公式可通用于计算各种反应底物流加-间歇式运行的底物反应速率;
3)根据A周期氨氮氧化速率确定当天B周期预期的氨氮流加速率[NH4+-N]add,B周期开始需要向氨氮流加液储备器中配制氨氮流加液,本发明采用NH4Cl溶液作为氨氮流加液;每个B周期所用NH4Cl的总质量根据以下公式计算:
式中m:每个B周期所用NH4Cl的总质量,g;
[NH4+-N]add:每个周期氨氮流加速率至反应液,mg/(L·h);
t':每个周期氨氮流加时间也即反应时间,h;
V:反应液体积,L;
S:基准值:NH4Cl(g)为1L反应液提供NH4+-N浓度,取100mg/L,计算方法本发明取0.382,即0.382gNH4Cl对应1L反应液的NH4+-N浓度100mg/L;
注:此公式可通用于计算各种反应底物流加-间歇式运行的底物流加液配制,其中计算基准值S视具体反应底物而定;
4)根据A周期某一批次刚投加氨氮后以及反应t时刻NH4+-N、NO2--N、NO3--N的浓度,以NO2--N和NO3--N的生成量计算A周期某一批次t时间反应段的亚硝酸盐积累率,视为A周期的亚硝酸盐积累率,见式(4):
式中NARA:某一批次亚硝酸盐积累率;
[NO2--N]A0:某一批次初始NO2--N浓度,mg/L;
[NO2--N]At:某一批次反应t时刻NO2--N浓度,mg/L;
[NO3--N]A0:某一批次初始NO3--N浓度,mg/L;
[NO3--N]At:某一批次反应t时刻NO3--N浓度,mg/L;
根据氨氮流加-间歇式运行,每天B周期开始和结束时取样进行分析考察B周期的亚硝酸盐积累率,以每周期NO2--N和NO3--N的生成量计算亚硝酸盐积累率,见式(5):
式中NARB:每个周期亚硝酸盐积累率;
[NO2--N]B0:每个周期初始NO2--N浓度,mg/L;
[NO2--N]Bend:每个周期反应结束NO2--N浓度,mg/L;
[NO3--N]B0:每个周期初始NO3--N浓度,mg/L;
[NO3--N]Bend:每个周期反应结束NO3--N浓度,mg/L;
注:若生成量为负值,则按零计算;
(4)每个A和B周期硝化反应消耗碱度,pH下降,反应期间设置加碱装置,根据设定pH值自动调节pH、补充碱度和无机碳源,加碱装置中添加的物质为碳酸钠、碳酸氢钠溶液,即可实现调节pH、补充碱度,同时也能实现无机碳源的补加;
(5)通过运行周期数确定最终需要的活性污泥氨氮氧化速率,结束硝化细菌菌群的筛选和富集培养;
进一步优选:待A周期氨氮氧化速率提高到100mg/(L·h)以上,采用间歇式运行、每批次初始NH4+-N浓度由250~350mg/L降低至50~100mg/L,以通过pH、温度和初始NH4+-N浓度控制反应初始FA浓度未抑制NOB,从而缓解之前试验阶段FA或FNA对NOB的抑制影响,以降低氨氮氧化过程的亚硝酸盐生成峰值(即反应过程中亚硝酸盐生成量的最大值)占初始氨氮浓度的比值、亚硝酸盐积累率;
进一步优选:单独采用B周期,运行和计算方法基本同步骤(2)、(3)、(4)、(5);采用步骤(1)中的1)计算接种污泥的氨氮氧化速率;之后根据步骤(2)、(3)、(4)、(5)进行;其中步骤(2)每周期反应初始NH4+-N浓度[NH4+-N]0,第1个周期的氨氮流加速率近似于接种污泥的氨氮氧化速率;第n个周期的氨氮氧化速率和亚硝酸盐积累率记为AORn和NARn,氨氮流加速率[NH4+-N]add按照[NH4+-N]add=(0.9~1.3)*AORn-1*(1-NARn-1)进行计算,以实现通过氨氮流加每小时补充的氨氮量在一小时可以基本全部氧化为硝酸盐,而尽可能少的亚硝酸盐积累。
将筛选和富集培养的硝化细菌菌群应用于水处理生物硝化领域。
本发明所述的一种间歇式、氨氮流加-间歇式运行交替的硝化细菌菌群筛选和富集培养方法的有益效果主要体现在:
1.间歇运行逐渐提高初始氨氮负荷利于提高氨氮氧化速率;
2.采用氨氮流加-间歇式运行,通过控制B周期氨氮流加速率和A周期氨氮氧化速率以及亚硝酸盐积累率的关系,可以控制反应液NH4+-N、NO2--N浓度,从而控制FA、FNA水平,以实现FA和FNA未对NOB产生抑制,可以维持氨氮氧化速率和实现低亚硝酸盐积累率;
3.采用此方法筛选和富集培养的硝化细菌菌群为主要功能微生物可以实现高氨氮氧化速率和高亚硝酸盐氧化速率;
4.采用此方法培养的硝化细菌菌群在总细菌中占有数量优势;
5.此方法培养的硝化细菌菌群保留了接种污泥(如污水处理厂A2/O工艺回流污泥)硝化细菌的菌群组成,因具有生物多样性而较纯种细菌更具优势;
6.本方法可以用于指导工业化硝化细菌菌群培养,获得的菌种可用于细胞固定化菌源、制作菌剂或生物添加至好氧反应池以提高污水、废水处理的硝化反应速率、制作菌剂用于水产养殖业去除氨氮和亚硝酸盐。
附图说明
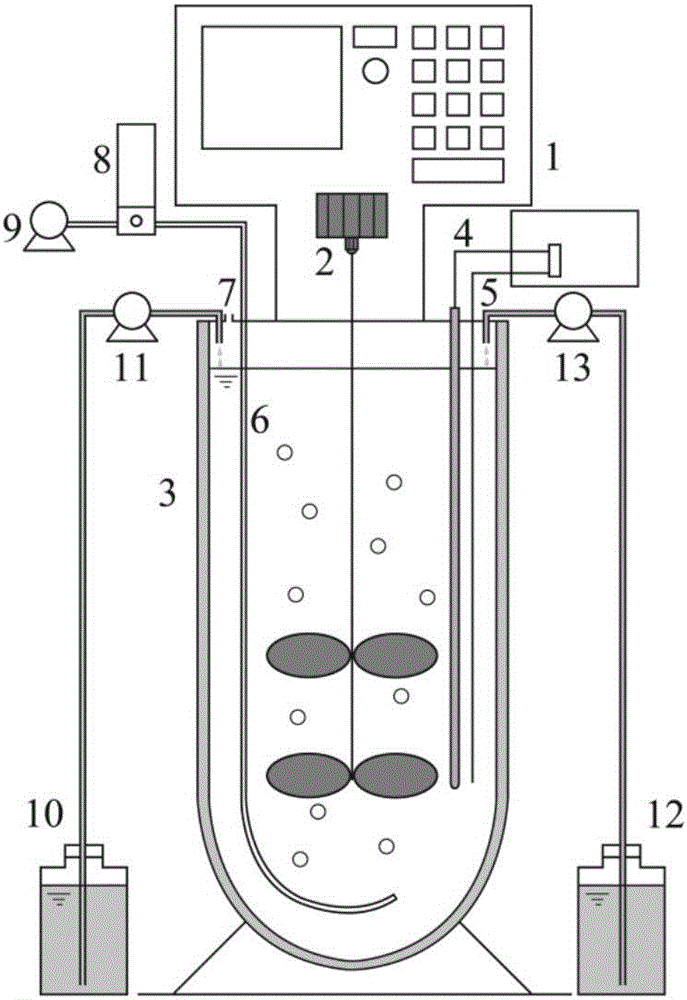
图1为全自动细菌发酵罐示意图;
图中:1.显示屏 2.搅拌器 3.水浴层 4.pH探头 5.温度探头 6.穿孔管曝气装置7.取样口 8.气体流量计 9.空气泵 10.Na2CO3、NaHCO3原液储备器 11.Na2CO3、NaHCO3进液泵 12.NH4Cl流加液储备器 13.NH4Cl进液泵;
图2硝化细菌菌群培养期间白天间歇运行周期(A)某一批次初始和反应t时刻NH4+-N浓度,t时间反应段NO2--N和NO3--N生成量;
图3计算得到的相应天的白天间歇运行周期(A)的氨氮氧化速率和亚硝酸盐积累率;
图4硝化细菌菌群培养期间夜间氨氮流加-间歇式运行周期(B)初始和反应结束NH4+-N、NO2--N、NO3--N浓度;
图5夜间氨氮流加-间歇式运行周期(B)的氨氮流加速率、计算得到的相应天B周期的氨氮氧化速率和亚硝酸盐积累率;
图6硝化细菌菌群培养完成时氨氮氧化和亚硝酸盐积累能力(初始NH4+-N浓度300mg/L);
图7 A周期氨氮氧化速率提高到100mg/(L·h)以上后,采用间歇式运行、降低每批次初始NH4+-N浓度至80mg/L的反应情况;
图8高通量测序结果(属(Genus)水平):yao2为接种污泥样品,yao4为培养第17天污泥样品,yao5为培养第25天污泥样品。
具体实施方式
下面结合实施案例对本发明作进一步具体描述,但本发明的实施方式不限于此。
实施例1
1.白天间歇式运行周期(A)培养硝化细菌菌群
以污水处理厂A2/O工艺回流污泥为接种污泥,以全自动细菌发酵罐为试验装置,有效容积6L,如图1所示。接种污泥的污泥浓度(MLSS)为4573mg/L。温度23±1℃,pH7.2~7.4,反应初始DO1.0~1.5mg/L,搅拌转速100rpm,Na2CO3原液浓度200g/L。采用间歇式、氨氮流加-间歇式运行交替的方法培养硝化细菌菌群,反应器共运行25天,前24天每天间歇式、氨氮流加-间歇式各1周期。基础培养液成分及浓度见表1:
表1基础培养液成分(以下成分不是混合物,是多个单独的溶液)
注:NH4Cl、FeSO4·7H2O溶液分别现用现配;KH2PO4、K2HPO4·3H2O为单独的混合溶液;MgSO4·7H2O、CaCl2为单独的混合溶液;微量元素为单独的混合溶液;此三种溶液为储备液,可供多个周期使用。
A周期开始向反应器内加入去离子水和计算好体积(NH4Cl;KH2PO4、K2HPO4·3H2O;MgSO4·7H2O、CaCl2;FeSO4·7H2O溶液各100mL;微量元素溶液6mL)的基础培养液至6L(反应液体积V),进水后使得体系中水质指标为:50~300mg/LNH4+-N(随运行天数增加,氨氮氧化速率提高,负荷逐渐提高:50、100、150、200、250、300mg/L),30mg/LPO43--P,30mg/LMgSO4·7H2O,15mg/LCaCl2,30mg/LFeSO4·7H2O和1mL/L微量元素(0.5mg/LZnSO4·7H2O,0.5mg/LMnCl2·4H2O,0.4mg/LCoCl2·6H2O,0.4mg/LCuSO4·5H2O,0.2mg/LNiCl2·6H2O,0.05mg/LNa2MoO4·2H2O)。第一天A周期首批次一次性投加氨氮间歇运行测定接种污泥的氨氮氧化速率,初始NH4+-N浓度[NH4+-N]A0为48.32mg/L,反应2h剩余NH4+-N浓度[NH4+-N]A2为14.16mg/L,根据公式(1)计算接种污泥氨氮氧化速率为17.08mg/(L·h)。根据图2每天选定批次初始浓度[NH4+-N]A0、[NO2--N]A0、[NO3--N]A0和反应进行至2h时的浓度[NH4+-N]A2、[NO2--N]A2、[NO3--N]A2,采用公式(1)和(4)计算各天A周期的氨氮氧化速率AORA和亚硝酸盐积累率NARA,考察硝化细菌菌群筛选和富集培养期间A周期反应器运行效果,结果如图3所示。硝化细菌培养结束时,计算得到的A周期氨氮氧化速率由17.08mg/(L·h)逐渐提升至最高109.41mg/(L·h),是接种时的6倍之多。
2.晚上氨氮流加-间歇式运行周期(B)培养硝化细菌菌群
B周期开始向反应器内加入计算好体积的基础培养液至6L,进水后使得体系中水质指标为:30mg/LNH4+-N即[NH4+-N]B0,其他指标同周期A,氨氮流加体积速率20mL/h。根据图4各反应周期初始浓度[NH4+-N]B0、[NO2--N]B0、[NO3--N]B0和反应结束浓度[NH4+-N]Bend、[NO2--N]Bend、[NO3--N]Bend,采用公式(2)和(5)计算各天B周期(即t’为12h)的氨氮氧化速率AORB和亚硝酸盐积累率NARB,考察硝化细菌菌群筛选和富集培养期间B周期反应器运行效果,结果如图5所示。B周期因考虑A周期的亚硝酸盐积累率,氨氮流加速率比A周期氨氮氧化速率有所降低,使得B周期内氨氮流加提供的氨氮和生成的亚硝酸盐在周期末基本反应完全。硝化细菌菌群培养期间,B周期氨氮流加速率由20mg/(L·h)逐渐提升至60mg/(L·h),B周期氨氮氧化速率由18.57mg/(L·h)逐渐提升至61.76mg/(L·h)。培养期间B周期的亚硝酸盐积累率基本维持在25%以下。B周期结束,根据亚硝酸盐和硝酸盐积累量进行“污泥清洗”1~2次,剩余NO2--N浓度<30mg/L,NO3--N<200mg/L。
3.硝化细菌菌群筛选和富集培养效果
第23天以A周期中首批次为例,考察培养后活性污泥的氨氮氧化和亚硝酸盐氧化能力,以评估AOB和NOB的培养效果,结果如图6所示。初始NH4+-N浓度278.39mg/L,FA为3.29mg/L,反应180min时,氨氮氧化完全,此时亚硝酸盐积累率为58.60%。计算得到前2h氨氮氧化平均速率高达109.41mg/(L·h)。180min以后,NOB将前180min生成的亚硝酸盐基本完全氧化为硝酸盐,用时约3h,平均亚硝酸盐氧化速率达到47.91mg/(L·h)。
此后降低初始氨氮负荷,即降低FA浓度,以缓解之前由于氨氮负荷提升导致的FA升高抑制NOB的活性,以降低氨氮氧化过程的亚硝酸盐峰值和亚硝酸盐积累率,考察FA浓度降低后NOB活性的恢复情况,如图7所示。初始NH4+-N浓度74.42mg/L,FA下降至0.88mg/L,反应50min时氨氮反应完全,此时亚硝酸盐积累率为32.12%。与图6初始NH4+-N浓度约300mg/L比较,亚硝酸盐积累率由58.60%降低至32.12%;反应过程中亚硝酸盐生成量峰值占初始氨氮浓度的比值也由65.15%显著降低至51.03%。由此表明撤掉FA对NOB的抑制作用后,NOB的活性恢复较快。此外随着反应进行NH4+-N浓度剩余较少时,DO快速升高易导致菌体内源呼吸而自身氧化分解,因此在DO明显升高后调节溶解氧至3mg/L以下使NO2--N基本反应完全。MLSS在第7、12、19和24天时分别为3836mg/L、2930mg/L、3490mg/L和4064mg/L,MLSS下降而氨氮氧化速率和亚硝酸盐氧化速率显著提高表明硝化细菌得到了有效的筛选和富集,已在总细菌中占有数量优势。根据高通量测序结果,在属(Genus)水平上,见图8,检测到Nitrosomonas(AOB)的比例由接种时的0.24%(yao2序号2)增长至培养后的34.87%(yao5序号2);Nitrospira(NOB)的比例由接种时的2.70%(yao2序号3)增长至培养后的25.79%(yao5序号3),培养后二者在总细菌中的比例达到60.66%,显著高于接种时的2.94%,表明在培养期间AOB和NOB得以大量生长,而其他细菌则通过“污泥清洗”逐渐被淘洗出反应器,与反应器高氨氮氧化速率(约110mg/(L·h))和高亚硝酸盐氧化速率(约50mg/(L·h))的试验结果相符。
上述实例表明,本间歇式、氨氮流加-间歇式运行交替的硝化细菌菌群筛选和富集培养方法可以筛选和富集培养硝化细菌菌群,实现高氨氮氧化速率和高亚硝酸盐氧化速率。本方法可以用于指导工业化硝化细菌菌群培养,获得的菌种可用于细胞固定化菌源、制作菌剂或生物添加至好氧反应池,应用于水处理生物硝化领域,具有极其富有经济价值的应用前景。
- 还没有人留言评论。精彩留言会获得点赞!