流体的分析和分离的制作方法
本发明涉及用于分析组分混合物(诸如多肽混合物)的流动方法(诸如流动扩散法和流动电泳法)以及流动设备。
背景技术:
许多具有基本或技术重要性的体系都作为异类组分的多分散混合物的形式存在。对这种混合物中的各组分的特征性质进行分析是从分析化学领域到生物物理学领域的关键问题。
鉴定复杂混合物的成分在现代生物物理学中变得越来越重要,因为生物体中的大多数过程都依赖于很多不同成分的相互作用。特别地,通过监测人体内的蛋白水平可以很好地促进许多疾病的早期检测。
尽管迫切需要对生物分子的复杂溶液进行分析的方法,但很少有技术提供必要的精度和分辨率。例如,进行2D凝胶电泳或质谱的那些技术要么耗时要么昂贵的,或者即耗时又昂贵。此外,诸如凝胶电泳的技术不提供关于分析物性质的定量信息。
流体流(诸如微流体流)内的组分的分离和检测存在许多挑战。鉴于最近对用于组分的反应、分离和检测的流体技术的兴趣增加,对开发能在连续流动体系中分离和分析组分的方法以及装置是有兴趣的。
本发明人建立了用于对组分(包括多组分混合物中的组分)进行分析的流体方法。
技术实现要素:
本发明提供了一种利用流体技术对组分进行分析的方法。总体来讲,本发明提供了一种方法,所述方法包括以下步骤:使组分横跨流体流分布,分离含所述组分的流体流的一部分,随后使得所述组分横跨另一流体流分布。所述组分在分布步骤中的行为表示该组分固有的化学性质或物理性质,从而每一分布步骤都可用于获得该组分的特征信息。因此,提供两个分布步骤能够使使用者鉴定出该组分的两种性质。
第一组分在分布步骤中的行为可能不同于第二组分的行为,从而产生两种组分横跨流体流的不同分布。收集流体流中含所述第一组分的部分,并且通过这种方式,一种组分可与另一组分至少部分分离。
在第一分布步骤中,所述第二组分的行为可能与所述第一组分相同,例如因为它们具有相同的化学性质或物理性质。因此,分离流体流中含所述第一组分的部分也将收集所述第二组分。
进行第二分布,并且在该第二分布中,所述第一组分的行为可能不同于所述第二组分的行为,从而产生两种组分横跨流体流的不同分布。由于可确定两种不同组分的存在,故此该步骤能够对多组分组合物进行分辨。收集流体流中含所述第一组分的部分,并且通过这种方式,一种组分可与另一组分至少部分分离。因此,本发明的技术可用于:基于另一化学性质或物理性质的不同,分离具有相同化学性质或物理性质的组分。
本发明的方法利用多个分布步骤。多重分布技术的使用允许根据多组分混合物内,组分的相互独立的物理性质和化学性质进行鉴定和分离。通过这种方式,引入第二分布步骤或额外的分布步骤增加了分析方法的分辨率,因为存在额外维度,能够对第一分布步骤中不可分离的组分进行区分。
因此,在本发明的第一方面中,提供了一种用于对组分进行分析的方法,所述方法包括以下步骤:
(iii)提供所述组分横跨接触的第一流体流和第二流体流,诸如层状流体流的分布;
(iv)使所述第一流体流的一部分或该第二流体流的一部分转向,或者使所述第一流体流的一部分和所述第二流体流的一部分转向,其中转向的部分为包括所述组分的第三流体流;
(v)使所述第三流体流与第四流体流接触,从而形成层流;以及
(vi)提供所述组分横跨接触的第三流体流和第四流体流,诸如层状流体流的分布。
在一个实施方式中,所述方法进一步包括以下预备步骤:
(i)提供在第一流体流中的所述组分;以及
(ii)使该流体流与第二流体流接触,从而生成层流。在该实施方式中,所述方法包括生成所述组分分布的预备步骤。
在一个实施方式中,所述方法进一步包括以下后续步骤:
(vii)使所述第三流体流的一部分或所述第四流体流的一部分转向,或者使所述第三流体流的一部分和所述第四流体流的一部分转向;其中,转向的部分为包括所述组分的第五流体流。在该实施方式中,组分可与例如所述第三流体流中存在的另一组分至少部分分离。
在一个实施方式中,步骤(vi)包括使所述组分电泳运动至所述第四流体流中。在此,步骤(iii)可包括使所述组分扩散至所述第二流体流中。在一个实施方式中,步骤(vi)包括使组分扩散至所述第四流体流中。在此,步骤(iii)可包括使所述组分电泳运动至所述第二流体流中。在一个实施方式中,步骤(vi)包括组分响应于等电点测定(也称为等电聚焦)、超速离心或磁分离的运动。
在一个实施方式中,所述方法包括对流体流中的所述组分进行分析的步骤。该流体流可为第三流体流或第五流体流。该流体流可为接触的第一流体流和第二流体流,或接触的第三流体流和第四流体流。
在一个方面,提供一种用于从混合物中分离第一组分的方法,所述混合物进一步包括第二组分和第三组分,所述方法包括以下步骤:
(i)提供在第一流体流中的第一组分、第二组分和第三组分的混合物;
(ii)使所述流体流与第二流体流接触,从而生成层流;
(iii)提供所述第一组分、所述第二组分和所述第三组分横跨接触的第一流体流和第二流体流,诸如层状流体流的分布;
(iv)使所述第一流体流的一部分或所述第二流体流的一部分转向,或者使所述第一流体流的一部分和所述第二流体流的一部分转向;其中,转向的部分为第三流体流,所述第三流体流包括与所述第三组分至少部分分离的所述第一组分和所述第二组分;
(v)使所述第三流体流与第四流体流接触,从而形成层流;以及
(vi)提供所述第一组分和所述第二组分横跨接触的第三流体流和第四流体流的分布,诸如层状流体流。
所述方法允许在两个分布步骤中,使第一组分、第二组分和第三组分彼此至少部分分离,其中两个分布步骤是在连续流体流上进行的。
在一个实施方式中,所述方法进一步包括以下后续步骤:(vii)使所述第三流体流的一部分或所述第四流体流的一部分转向,或者使所述第三流体流的一部分和所述第四流体流的一部分转向;其中,转向的部分为第五流体流,所述第五流体流包括与所述第二组分至少部分分离的所述第一组分。
另一方面提供了一种用于对多组分混合物进行分析的方法,所述多组分混合物包括第一组分和第二组分,所述方法包括以下步骤:
(i)提供在第一流体流中的所述第一组分和所述第二组分的混合物;
(ii)使所述流体流与第二流体流接触,从而生成层流;
提供所述第一组分和所述第二组分横跨接触的第一流体流和第二流体流,诸如层状流体流的分布;
(iv)使所述第一流体流的一部分或所述第二流体流的一部分转向,或者使所述第一流体流的一部分和所述第二流体流的一部分转向;其中,转向的部分为第三流体流,所述第三流体流包括与所述第三组分至少部分分离的所述第一组分;
(v)使所述第三流体流与第四流体流接触,从而形成层流;
(vi)提供所述第一组分横跨接触的第三流体流和第四流体流,诸如层状流体流的分布;
(vii)随后,使所述第一流体流的一部分或所述第二流体流的一部分转向,或者使所述第一流体流的一部分和所述第二流体流的一部分转向;其中,转向的部分为第三流体流,所述第三流体流包括与所述第一组分至少部分分离的所述第二组分;
使所述第三流体流与第四流体流接触,从而形成层流;以及
(ix)提供所述第二组分横跨接触的第三流体流和第四流体流,诸如层状流体流的分布。
上述方法允许在两个连续的分布步骤中分离第一组分,并且可根据在第一分布步骤之后的转向步骤中的变化,在两个连续的分布步骤中分离所述第二组分。通过这种方式,可确定第一组分的多个物理特征和/或化学特征,并且可确定第二组分的多个物理特征和/或化学特征。
在一个实施方式中,步骤(vii)包括改变所述第一组分和所述第二组分横跨接触的第一流体流和第二流体流,诸如层状流体流的分布。在一个实施方式中,所述第一流体流连续通过步骤(iv)和步骤(vii)。
在本发明的另一方面中,提供了一种在本发明的方法中使用的流动设备。所述流动(flow)设备包括:
用于使第一流和第二流接触的第一分离通道,其中,该分离通道适于允许组分在接触的第一流和第二流之间横向运动;第一流动(flow)分离器,所述第一流动分离器与所述第一分离通道流体连通并且在所述第一分离通道的下游,所述第一流动分离器适于使第一流体流的一部分或第二流体流的一部分从所述第一分离通道转向,或者使所述第一流体流的一部分和所述第二流体流的一部分从所述第一分离通道转向,转向的流为第三流;以及
第二分离通道,所述第二分离通道与所述第一流动分离器流体连通并且在所述第一流动分离器的下游,所述第二分离通道用于使第三流和第四流接触,其中,该分离通道适于允许组分在接触的第三流和第四流之间横向运动。以下将对本发明的这些和其他方面,以及实施方式进行进一步地详细描述。
附图说明
图1为根据本发明的一个实施方式的流动设备的示意图,该流动设备用于对组分进行分析和/或分离。比例尺为5000。
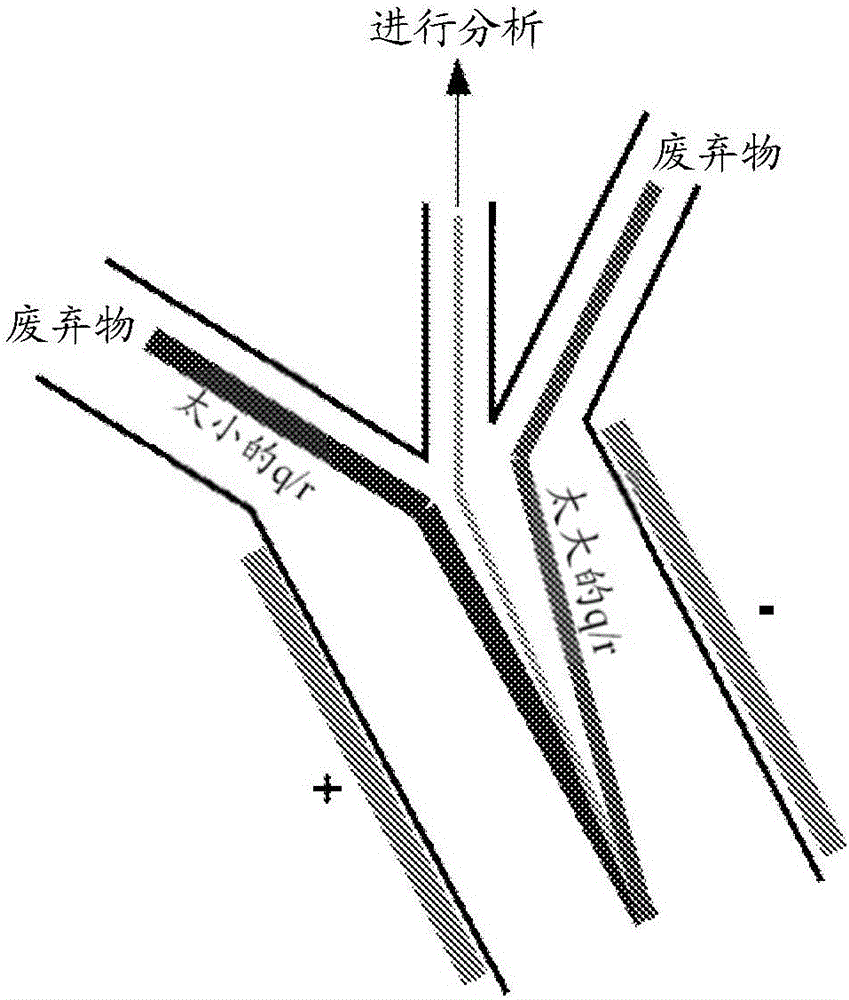
图2是根据本发明的一个实施方式的流动设备的流动分离器的示意图。流动分离器用于在分离通道的下游端部分离流体流的一部分,其中组分在分离通道的下游端部通过电泳进行分布。流动分离器收集流体流中含具有特定质荷比的组分的部分,并且该分离器可供应下游分布通道,如图1的流动设备中所示。具有不同质荷比的组分在其他地方转向。
图3是在具有图1所示设计的装置的扩散分离通道处,拍摄的一系列荧光图像(a)至(c);以及在具有图1所示设计的装置的电泳分离通道的下游端部的流动分离器处,拍摄的一系列荧光图像(d)至(f);其中,图像(a)和图像(d)是在横跨电泳分离通道的1V施加场(applied field)下拍摄的;(b)和(e)是在3V施加场下拍摄的;以及(c)和(f)在5V施加场下拍摄。黄色箭头指示流体流的转向部分,该流体流的转向部分随后被供应至下游的扩散分离通道。所使用的组分是浓度为2mg/mL的13-乳球蛋白。
图4(a)示出了扩散曲线,其通过在具有图1所示设计的装置的扩散分离通道中的4个位置(从左至右,2.5mm、4.7mm、20.7mm和64.7mm)处,记录I3-乳球蛋白的相对荧光强度随通道位置的变化来测量;以及(b)示出了如由来自实验的实验性测得的尺寸和电荷所确定的,随着组分电荷(e)和组分尺寸(nm)的变化,相对荧光强度的变化。
图5(a)至图5(c)是对于标称半径为23.5nm和100nm的荧光胶体的混合物的分布,在具有图1所示设计的装置的电泳分离通道的下游端部,流动分离器处拍摄的一系列荧光图像,其中:图像(a)在横跨电泳分离通道的0V施加场下拍摄;(b)在0.9V施加场下拍摄;和(c)在1.5V施加场下拍摄;(d)示出了扩散曲线,其通过在具有图1所示设计的装置的扩散分离通道中的4个位置(从左至右,2.5mm、4.7mm、20.7mm和64.7mm)处,记录荧光胶体的相对荧光强度随通道位置的变化来测量;以及(e)是分析的组分混合物的分布密度图,示出了对于尺寸r(nm)和电荷9(100e)的特定组合,所测量的组分的相对强度。该相对强度通过明暗法来表示。强度图显示了在组分原始群体中对应于100nm胶体和23.5nm胶体的群体。
具体实施方式
本发明提供了用于对流体内的组分(包括在多组分混合物中的组分)进行分析的方法和设备。
本发明的方法提供了一种替代途径,用于通过依赖于层流的组件化流体策略来分析复杂混合物。即,在通过整体分析以利用另一量来鉴定溶液的内容物之前,根据物理性质在稳态条件下预分离溶液。在本发明中,所述方法例如为,在经扩散光谱法通过尺寸进行后续分离之前,通过微流体自由流动电泳根据分析物的尺寸电荷比对其进行分离。
由于本发明的方法通常在稳态下进行,所以可串联添加几个分离组件以使该技术的分辨率成倍增加,并且可以使用不同的检测组件。
本发明人先前已经描述了使用流体技术对流体流中的组分进行分析和分离。该工作描述于GB 1320146.2(2013年11月14日提交)中,它的内容通过引用整体并入本文中。现在,本发明的工作在于使本工作适于使用串联的分离分布步骤,以允许对组分(例如,多组分混合物中的组分)进行分离和/或分析。利用这些技术,本发明人建立了二维流动的分析和分离方法,其可用于研究含低浓度且小体积的组分的流体,诸如含蛋白的流体。
本发明的方法可以在恒定流体流下,在单个装置中进行。
在第一步骤中,使组分横跨流体流分布。然后使该组分转向,例如同时使该组分与其它组分分离,并且使该组分随后在第二步骤中横跨其它流体流分布。每个分布步骤都能使使用者确定组分的性质,并且每个分布步骤都能使该组分与具有不同性质的组分分离。使用多个分布步骤可允许组分与其它相关组分分离:这些组分可在一个分布步骤中具有相似的行为,但是在第二分布步骤中并不具有相似的行为。通过这种方式,可以分析性地分辨组分的混合物,并且可至少部分分离该混合物,从而允许从另一种组分至少部分纯化一种组分。本发明的方法是顺序(in line)进行,从而分离含横跨流分布的组分的流体,并且该流中含该组分的分离部分进行下游其它分布步骤。
本发明的方法和设备尤其良好地适用于小型化,并且在一个实施方式中,利用微流体技术和微流体设备来分析和/或纯化组分。如上所述,提供具有合适微通道的设备使得能使用小体积的流体来进行本发明的方法,其中利用标准技术来制造该具有合适微通道的设备。
本发明的方法还可用于分析和/或分离多组分混合物中的多种组分。转向步骤可用于收集其它组分,其中转向步骤使一种组分与其它组分至少部分分离。存在两个主要方法来实现这一点。
首先,在第一分离通道的下游端部可设置有多个流动分离器。可设置各流动分离器,以使第一流和第二流的不同部分转向。从而可收集多个流。当在第一分离通道的下游端部收集多个流时,可允许这些流中各自流入分离的第二分离通道中,在其中可进行进一步的分离步骤。任选地,第二(或额外的)分离通道可设置有多个流动分离器,以允许从第三流和第四流的不同部分收集组分。可根据需要对每个转向流进行分析和/或收集。通过这种方式,可在连续流动体系中分离多个组分。
其次,在流动方法期间,可改变分离通道中的条件以改变组分或多组分混合物在分离通道的下游端部的分布曲线。分布曲线的变化使流动分离器收集具有不同成分(例如不同组分或不同的组分量)的第一流体流的一部分和/或第二流体流的一部分。
可以多种方式改变流动流道中的条件。例如,可提高或降低流速以改变下游端部的分布曲线。可改变用于使得上述组分从一个流运动至另一流的条件,以便影响分布曲线。在采用电泳条件的情况下,可改变横跨通道的施加场,从而改变横跨流的组分的偏转程度。组分偏转的变化将导致下游端部的分布曲线改变。可在分析方法期间实现分布曲线的变化,从而能够在单个流上对多种组分进行分析。
如本文所使用的,分布曲线的变化可指曲线形状的变化(即,在横跨流的多个位置处,多种组分的群体的变化)。这包括在横跨通道的一个位置处,多种组分中的一种组分的最大群体的位置改变。
本发明的方法还允许对组分进行定量。本文所述的技术能够分离和收集流体流中的所有组分。这些方法是非破坏性的,因此在输出处收集体系中的所有输入。使一种组分与另一种组分至少部分分离的能力允许绝对量化一种组分的量,或者相对于组分的全部群体来相对量化一种组分的量。使用标准分析技术(诸如荧光光谱)提供检测信号的强度与存在组分的浓度之间的直接关系,因此得到存在组分的量。
下文将进一步详细地描述用于分析和纯化组分的一般方法。
一般方法
本发明第一方面的方法总体上用于分析(诸如表征或量化)溶液中的组分。额外地或可替代地,上述方法可用于使一种组分与多组分混合物中的其它组分至少部分分离。
上述方法涉及组分横跨一系列流体流的分布。组分横跨这些流体流的分布反映出该组分的物理性质和/或化学性质,并且该分布将不同于与该组分的物理性质和/或化学性质不同的其它组分。
组分横跨流体流的分布可响应于所施加的刺激,诸如施加场;或者该分布可利用组分的固有特征,诸如组分的与其尺寸相关的扩散特征。分布步骤在单个流动装置中,利用连续流体流来进行。
使包括一种组分或多种组分的第一流体流在第一分离通道中与第二流体流接触,从而生成层流。使接触的流沿第一分离通道流动,并且使第一流体流中的组分移动至第二流体流中,以提供横跨第一流体流和第二流体流的组分分布。组分进入该第二流体流的运动可为例如扩散运动或电泳运动。
随后,使第一流体流的一部分或第二流体流的一部分转向到第一转向通道中,或者使第一流体流的一部分和第二流体流的一部分转向到第一转向通道中;其中,转向的部分为第三流体流,该第三流体流包括该组分,可选地与其它组分一起。该转向步骤可使该组分与第一流体流和第二流体流中的其它组分至少部分分离。
使包括该组分的第三流体流在第二分离通道中与第四流体流接触,从而生成层流。使接触的流沿第二分离通道流动,并且使第三流体流中的组分移动到第四流体流中,以提供横跨第三流体流和第四流体流的组分分布。组分进入第四流体流的运动可为例如扩散运动或电泳运动。
使组分移动到第四流体流中的条件与用于使组分分布至第二流体流中的条件不同。不同分布技术的使用为使用者提供了附加的分析信息,并提供了从其他组分中纯化该组分的进一步的分离步骤。
可选地,随后使第三流体流的一部分或第四流体流的一部分转向至第二转向通道中,或者使第三流体流的一部分和第四流体流的一部分转向到第二转向通道中;其中,转向的部分为第五流体流,该第五流体流包括该组分,可选地与其它组分一起。上述转向步骤可使组分与第三流体流和第四流体流中的其它组分至少部分分离。
在一个实施方式中,通过使组分电泳运动至第二流体流中,来提供组分横跨接触的第一流体流和第二流体流的分布;以及通过使组分扩散进入第四流体流中,来提供组分横跨接触的第三流体流和第四流体流的分布。在替代实施方式中,通过组分扩散进入第二流体流中,来提供组分横跨接触的第一流体流和第二流体流的分布;以及通过组分电泳运动至第四流体流中,来提供组分横跨接触的第三流体流和第四流体流的分布。
分离通道和转向通道,以及分析通道和试剂通道(当存在时)是流体装置的部件。该流体装置,特别是分析通道适于与组分的检测器一起使用。
在分离步骤和转向步骤的过程中,每一流的流速保持在基本上恒定的水平。可以仅在每个部件的通道中建立稳定流时进行这些分离步骤和转向步骤。
所述组分可以是或包括聚合物,诸如生物聚合物。所述组分可以是多肽、多核苷酸或多糖或包括多肽、多核苷酸或多糖。这些组分中的每一种都可被认为是生物聚合物。在一个实施方式中,所述组分是或包括多肽。在一个实施方式中,所述组分是或包括蛋白质。所述组分可以是多组分混合物的一部分。因此,分离步骤可用于使该组分与其他组分至少部分分离。例如,除其他外,在此描述的技术允许基于尺寸或基于电荷与尺寸之比来进行分离。当所述组分为蛋白时,其他组分可为其它蛋白,或可为处于与所述组分聚集的不同状态的相同蛋白。本发明适用于对分子量为300Da或更高、500Da或更高、1000Da(1kDa)或更高、2kDa或更高的组分(诸如聚合物分子)进行分析。本发明适用于对分子量为5kDa或更低、10kDa或更低、50kDa或更低、100kDa、200KDa、500kDa或1000kDa或更低的组分进行分析。
本发明适用于对流体动力学半径为至少0.05nm、至少0.1nm、至少0.5nm、至少1nm或至少5nm的组分进行分析。本发明适用于对流体动力学半径为至多10nm、至多15nm、至多25nm、至多50nm、至多100nm或至多200nm或至多500nm的组分进行分析。
具体地,本发明尤其适用于对流体动力学半径在0.5nm至500nm(诸如0.5nm至200nm,诸如0.5nm至15nm)范围内的组分进行分析。
组分可具有分析标记物以允许对该组分进行检测。该组分可在用于本发明的方法之前进行标记。可替代地,对组分进行标记可作为本发明的方法的一部分。
在一个实施方式中,提供具有一种或多种发光标记物(诸如荧光标记物)的组分。
在一些实施方式中,无须对组分进行标记,因为组分可能本身具有能使用上述光谱法(如荧光光谱)检测的官能团。例如,当组分具有荧光活性基团时,这些基团可被用于该组分的荧光检测。
组分(该组分是或包括多肽)可具有氨基酸色氨酸、酪氨酸和苯丙氨酸,其侧链具有荧光活性。然而,这些残基的存在可能不足以使该组分被检测到。例如,酪氨酸和苯丙氨酸的荧光活性非常弱,因此难以检测到。在多肽内存在少量色氨酸、酪氨酸和苯丙氨酸的氨基酸残基时,荧光信号可能弱。在这些情况下,优选地是可提供具有更强荧光活性的荧光标记物。OPA衍生的标记物是可以使用的标记物的实例。
在一个实施方式中,所述多组分混合物包括多种组分(包括蛋白,诸如单体、二聚体和三聚体物质)的聚集体,或其他更高级聚集体。因此,在此描述的技术可用于分离和分析蛋白质-蛋白质相互作用。
可选地,可对流体流中的组分进行分析。可对横跨第一流体和第二流体分布的组分(诸如在第一分离通道中)进行分析。诸如在第一流动分离器中,可对第三流体(诸如在第一流动分离器中)内的组分进行分析。可对横跨第三流体和第四流体分布的组分(诸如在第二分离通道中)进行分析。当第五流体流从第三流体流和第四流体流转向时,可对第五流体(诸如在第二流动分离器中)内的组分进行分析。
流体流
本发明提供了对提供在流体流中的组分进行分离和分析的方法。在一个实施方式中,所提及的流体流涉及液体流。
流体流可为水性流。水性流可包括其他溶剂,如DMSO、烷基醇等。
本发明的装置可适于与流体流一起使用,并且可适于与水性流体流一起使用。
在本发明的实施方式中,所述组分初始提供在第一流体流中。所述组分优选溶解在所述第一流体中。
在一个实施方式中,所述第一流体允许一种组分或多种组分保持在其自然状态。当所述组分是生物分子,如蛋白时,所述流体流可为合适的缓冲液。因此,除其他外,可对盐含量和pH值进行选择以使所述组分保持其自然状态。
除了第二流体流不含所述组分之外,第二流体流可与第一流体流相同。相似地,除了第二流体流不含所述组分之外,第四流体流可与第一流体流相同。
第三流体流为第一流体流和/或第二流体流的转向部分。第五流体流(如果收集这样的流)为第三流体流和/或第四流体流的转向部分。
使第一流体流和第二流体流接触,并且允许第一流中的组分移动至第二流中以使该组分横跨第一流体流和第二流体流分布。接触的流可为第一流与第二流的层流。
使第三流体流和第四流体流接触,并且允许第三流中的组分移动至第四流中以使该组分横跨第一流体流和第二流体流分布。接触的流可为第三流与第四流的层流。
在本发明的某些实施方式中,在与第四流体流接触之前,转向的第三流体流可与标记流混合,从而对转向的流体流中的组分进行标记以用于分析。可选地,转向的第三流体流可以与变性流混合,例如在第三流体流接触标记流和第四流体流之前的流。可提供变性流以使组分变性,例如使该组分适于进行标记。
这些标记和可选的变性步骤是较不优选的,转向的第三流体流通常在其从第一流体流和/或第二流体流转向之后直接与第四流体流接触。因此,被转向的组分在其横跨第三流体流和第四流体流分布之前通常不被修饰。
第五流体流(如果收集这样的流)可与标记流混合,从而对转向的流体流中的组分进行标记以用于分析。可选地,转向的第五流体流可与变性流混合,例如在第五流体流接触标记流之前的流。可提供变性流以使组分变性,例如使该组分适合进行标记。
当本发明的方法包含多个侧向分布步骤,例如四个分布步骤中有两个、三个步骤,可仅在这些分布步骤中的最后一个步骤之后,进行任何标记步骤和变性步骤。在其它实施方式中,组分在用于本发明的方法之前进行标记。
所述标记流典型地为液体流,诸如水性流,含有适合于对组分进行标记的试剂。用于流动方法学中的合适标记技术是本领域所熟知的,并且在本文中进行描述。
变性流典型地为液体流,诸如水性流,含有适合于使组分变性的试剂。
下文对标记和变性进一步进行了详细地描述。
分布和分离
本发明的方法包括以下步骤:提供组分横跨第一流体流和第二流体流的分布,随后提供组分横跨第三流体流和第四流体流的分布。该分布典型地是组分横跨第一流体流和第二流体流的非均匀分布,以及组分横跨第三流体流和第四流体流的非均匀分布。
本发明的方法中,分布步骤为这样的步骤:使组分从一个流体流移动至另一流体流。在该情况下,术语分布是指组分横跨流体流的横向分布。这可被认为是正交于流动方向的分布。
如本文中所描述的,分布可包括组分进入第二流体流或第四流体流的扩散,或组分进入第二流体流或第四流体流的电泳运动。可使用其他分布技术。
所述分布是所述组分或包括所述组分的多组分混合物的横向分布。
横向分布可与组分沿流体流的分布不同。例如,本领域已知的是流体方法可基于在流体通道中的物质的泰勒(Talyor)分散,对流体流中的组分进行分离。例如,US 2011/264380描述了用于测定多分散物质的流体动力学半径的方法。将待分析的物质与单分散标准物混合。将得到的混合物添加到沿着毛细管流动的载体流体中,并且在该混合物排出毛细管时记录它的泰勒曲线。US 2011/264380的工作并不包括如下步骤:在组分沿流体流进行第一分布后,进行第二分布步骤。
拉齐姆(Ramsey)小组已经对用于分离蛋白质的电泳方法进行了描述,然而,这些蛋白质是沿着流体流分离的,并不存在组分横跨流的非均匀分布(例如,参见Liu et al.Anal.Chern.2000,72,4608;Jacobson et al.Anal.Chern.1994,66,4127;Jacobson et al.Anal.Chern.1994,66,3472)。这可被认为是时间分布,而不是空间分布。如前文所指出的,相比之下,本发明使组分能够在稳态下进行空间分离,从而允许通过长暴露时间对低浓度样品进行有效检测。
Herling等人以及Kamholz等人分别描述了使用电泳和扩散分级技术使组分横跨流体流横向分布的方法。然而,这些文献没有描述串联使用多种横向分布技术,并且也没有描述流体流的一部分的转向。
在此描述的分离方式很大程度上对于在这些流中使用的溶剂条件的性质是不敏感的。因此,能够在生物分子(诸如蛋白质)的自然条件下,对其进行研究。通过这种方式,组分在分离步骤中的行为是以该组分的自然态为特征。在分析时不需要校准步骤,以组分在外部条件下的行为转换为在自然条件下的预期行为。
当所述组分为混合物(多组分混合物)的一部分时,所述组分和混合物中的其他组分可受到横跨通道的干扰,从而提供所有组分横跨第一流体流和第二流体流以及横跨第三流体流和第四流体流的分布曲线。
第一转向步骤可在组分到达第二流体流的边界(即,通道壁)之前进行。当所述组分为多组分混合物的一部分时,转向步骤可在多组分混合物中的任何组分到达第二流体流的边界之前进行。
类似地,当进行第二转向步骤时,可在所述组分到达第四流体流的边界(即,通道壁)之前进行。当所述组分为多组分混合物的一部分时,转向步骤可在多组分混合物中的任何组分到达第四流体流的边界之前进行。
可通过对分布技术的恰当变化来改变组分横跨接触的流体的分布。
分布曲线取决于用于分布所述组分的技术,以及允许进行分布的时间。典型地,允许进行分布的时间为第一流体流或第三流体流中的组分还未到达第二流体流或第四流体流的边界的时间。例如,可选择第一流和第二流在分离通道中的流动停留时间,以使第一流体流中的组分在所采用的分离条件下没有时间到达边界。
在一个实施方式中,组分的分布可以是从一个流到另一个流的扩散,诸如从第一流到第二流的扩散,或从第三流到第四流的扩散。扩散转移的速率与组分的扩散系数D成正比,并且与流体动力学半径rho成反比。因此,预期较小组分以比较大组分大的速率扩散进入接触的流体流。例如,在转向步骤中,使第二流体流中靠近壁处的第二流体流边界的部分转向,将收集具有较小尺寸的那些组分。使第二流体流中靠近与第一流体流的层流边界的部分转向,将允许收集具有较大尺寸的那些组分。由此得出,使第二流体流中在层流边界与通道边界之间的部分转向,将允许收集具有中等尺寸的那些组分。
转向组分的尺寸将取决于在横跨分离通道的流动分离器中的位置。转向组分的范围将取决于转向部分与第一流体流或第二流体流的总宽度相比的相对尺寸,以及流的转向部分。
转向步骤可收集第一流体流或第三流体流的一部分。使用扩散分离技术,预期在第一流体流或第三流体流中的较小组分比较大组分更迅速地去除,因为较小组分以更大的速率扩散到第二流体流或第四流体流中。
在一个实施方式中,组分的分布可为从第一流到该第二流的电泳运动,或从第三流到第四流的电泳运动。电泳转移的速率与组分的电荷与尺寸之比成正比。因此,将预期与具有较小电荷和/或尺寸的那些组分相比,具有大电荷和/或小尺寸的组分具有更大的电泳运动。
在利用电泳来分离组分时,第二流体流或第四流体流典型地被分别提供在第一流体流和第三流体流的两侧。在电泳过程中,带负电的物质可偏转到第二流体流或第四流体流之一中,而带正电的物质则偏转到第二流体流或第四流体流中的另一流中。
因此,预期电荷与尺寸之比高的组分以比电荷与尺寸之比低的组分大的速率移动(转向)进入第二流体流或第四流体流中。因此,在转向步骤中,使第二流体流或第四流体流中靠近壁处的第二流体流或第四流体流边界的部分转向,将收集电荷与尺寸之比高的那些组分。使第二流体流或第四流体流中靠近与第一流体流或第三流体流层流边界的部分转向,将允许收集电荷与尺寸之比低的那些组分。由此得出,使第二流体流或第四流体流中在层流边界与通道边界之间的部分转向,将允许收集电荷与尺寸之比中等的那些组分。
转向组分的电荷与尺寸之比将取决于在横跨分离通道中的流动分离器的位置。转向组分的范围将取决于转向部分与第一流体流或第二流体流的总宽度相比的相对尺寸,以及流的转向部分。将理解的是,使第二流体流的一部分转向可仅收集带负电或正电的那些物质。
当使用电泳方法时,根据所需的偏转程度,可适当选择横跨通道所施加的电压。在一个实施方式中,施加电压为至多5V、至多10V或至多15V。在一个实施方式中,施加电压为至少0.1V、至少0.5V或至少1.0V。在该方法中,可改变电压以改变偏转程度,进而改变在转向步骤中收集的组分。
以上描述了用于使组分横跨第一流体流和第二流体流分布的扩散方法和电泳方法。可使用用于使组分分布的替代方法。实例包括例如金属蛋白的等电点测定(也被称为等电聚焦)、超速离心和磁分离。
电泳方法可用于分离横跨第一流体流和第二流体流的组分,其中电泳方法包括但不限于介电电泳、等电点测定(也称为等电聚焦)和等速电泳。介电电泳是的常见电泳方法,用于通过将力施加至非均匀电场内的介电颗粒,分离横跨第一流体流和第二流体流的具有中性电荷的组分。除了施加场的强度之外,通过介电电泳来分离组分取决但不限于组分的介电性质和尺寸。
用于分离组分的电泳方法的另一实例是等电点测定(也称为等电聚焦)。根据组分的等电点,分离横跨第一流体流和第二流体流的组分。施加电场并且使组分通过pH梯度迁移。当各组分接近它们的特定等电点,则在pH梯度中固定。
等速电泳方法用于在施加固定电流时,基于分析物的离子迁移率来选择性地分离分析物。
此外,热泳技术用于观察不同组分通过温度梯度横跨第一流体流和第二流体流的运动。可通过红外激光(但不限于)来诱导温度梯度。组分通过温度梯度的扩散速率取决于但不限于其尺寸、电荷、构造和水化壳。
本发明的方法包括以下步骤:使第一流的一部分或第二流的一部分转向,或者使第一流体流的一部分和第二流体流的一部分转向。对流体流的一部分进行分析,能够使使用者确定扩散曲线的一部分中的材料的数量和特性。
在一替代方面中,转向步骤包括使所有的第一流体流或所有的第二流体流转向的步骤。
上述分离步骤不同于组分沿流体流进行分离的色谱分离方法和泰勒(Taylor)分离方法,以及拉姆齐小组的替代电泳技术(毛细管电泳)。这些技术可被认为是在时间上对组分进行分离。相比之下,在本发明中采用的分离方法在空间上对组分进行分离。
在一个实施方式中,第一流体流被提供为在两个层状第二流体流之间的中心流。因此,在该第一流体流中的组分可被分布到这两个第二流体流之一或两者中。
在一个实施方式中,对一种组分或多种组分横跨流的分布进行测量。可沿流体流在多个位置处对一种组分或多种组分的分布进行测量。可在层流转向之前进行测量。当使用扩散分布技术时,例如,每一位置代表特定的扩散时间。仅当组分具有允许它被检测到的固有官能团时,或者当组分在用于本发明的方法中之前提供有例如标记形式时,可进行这样的测量。当组分缺乏这样的官能团时,其可在后续标记步骤中被提供有官能团。
在本发明中,如本文所述,上述步骤不是必要的,因为可由转向流记录与组分分布有关的信息。
转向
本发明的方法包括使第一流体流的一部分和第二流体流的一部分转向的步骤。流体流的转向部分包含与第一流体流和第二流体流的其余部分相分离的组分。该转向部分为第三流体流。
该转向步骤取得第一流体流的一部分或第二流体流的一部分,或者第一流体流的一部分和第二流体流的一部分。该转向步骤可被称为第一转向。在一个实施方式中,该转向步骤取得第二流体流的一部分。
当提及第一流体流的一部分和第二流体流的一部分的转向时,这是指第一流体流的一部分和第二流体流的一部分的转向。层流的这一部分的转向包括第一流体流和第二流体流接触的边界。
在替代方面中,转向步骤取得所有的第一流体流或所有的第二流体流。通常,这是不优选的,因为一个流体流的所有部分的转向使得组分不能充分分离。可在例如一种组分清楚地分布到第二流体流中且另一组分保留在第一流体流时进行该步骤。在此,第一流体流和第二流体流之一的转向具有从另一组分中基本上移除一种组分的效果。而在两种组分都横跨第一流体流和第二流体流分布时,优选使第一流体流和/或第二流体流的一部分转向。
转向步骤分离流体流的一部分,用于后续在第三流体流与第四流体流之间进行进一步分布。所取得的流体流的部分表示在分离步骤中建立的横向分布曲线的部分。转向步骤是分离流体流总宽度的一小部分,或第一流体流或第二流体流的宽度的一小部分。流体流中被转向的一小部分不受特别限制,并且基于用于分析的组分以及多组分混合物中的其他组分(如果存在)进行选择。
转向步骤是指分离流中的一部分,这一部分对应于第一流体流和/或第二流体流的一部分。当第一流体流和第二流体流首次接触时,第一流体流和第二流体流之间存在明显的区别。第一流体流携带多种组分,而第二流体流不携带多种组分。在分离通道的下游端部,第一流体流的组分横向移动进入第二流体流中,以生成组分横跨第一流体流和第二流体流的分布。此时,在第一流体与第二流体之间没有明显的边界。
在本发明中,提及流体流的转向是指接触的第一流体流和第二流体流的特定截面部分,例如通道中的特定区域。如果通道中的该区域对应于通道上游部分处的通道的区域,诸如第一流体流与第二流体流首次接触的接合点,则该区域被称为第一流体流的一部分。
例如,当第一流和第二流首次接触时,可在通道的上游部分处建立接触的流,其中第一流体流占据通道宽度的一半,并且第二流体流占据通道宽度的剩余一半。如果流体流的转向部分取自被第一流体流最初占据的通道宽度的一半,则该流体流的转向部分可以被称为第一流体流的转向部分。在这种情况下,第一流体流和第二流体流之间的分界简单地为通道的中心线。
第一流体和第二流体在接触流的下游端部的位置可由第一流体流中组分的分布来确定。例如,在扩散分布中,非常大的组分扩散进入第二流体流中是可忽略的。在下游端部,非常大的组分将保留在第一流体流中。在电泳分离中,不带电的组分响应于施加场的偏转是可忽略的,因此基本上不会从第一流体流移出。
可选地,本发明的方法包括使第三流体流的一部分和第四流体流的一部分转向的步骤。流体流的转向部分包括从第三流体流和第四流体流的剩余部分中分离出的组分。转向部分为第五流体流。该转向可被称为第二转向步骤。
转向步骤取得第三流体流的一部分或第四流体流的一部分,或者第三流体流的一部分和第四流体流的一部分。在一个实施方式中,转向步骤取得第四流体流的一部分。以下提及第一流和第二流的特定量的转向可分别应用于第三流和第四流的特定量的转向。
在一个实施方式中,所述转向步骤使至少5%、至少10%、至少15%、至少20%、至少25%、至少30%的第一流体流、第二流体流,或者第一和第二流体流转向。在一个实施方式中,所述转向步骤使至多40%、至多50%、至多60%、至多75%、至多85%的第一流体流、第二流体流,或者第一和第二流体流转向。在一个实施方式中,所述转向步骤使一定范围的一定量的第一流体流、第二流体流,或者第一和第二流体流转向,其中该一定范围的下限值和上限值选自以上给定的最小值和最大值。
在一个实施方式中,所述转向步骤使第二流体流的一部分转向。在一个实施方式中,第二流体流中转向的部分可为从第二流体流与第一流体流的边界横跨该第二流体流的宽度至多5%、10%、15%、25%、50%或75%延伸的部分。在一个实施方式中,第二流体流中转向的部分可为从该第二流体流与通道壁的边界横跨该第二流体流的宽度至多5%、10%、15%、25%、50%或75%延伸的部分。在一个实施方式中,第二流体流中转向的部分不包括从第二流体流与第一流体流的边界延伸的部分或从第二流体流与通道壁的边界延伸的部分。因此,该转向的部分是第二流体流的中间部分。该中间部分可为第二流体流的宽度的至多5%、10%、15%、25%、50%或75%。流体流中被导向的部分将取决于待检测的组分的特性。
如上文在分布和分离小节中所提到的,扩散和电泳分离技术可用于获得一种组分或多种组分横跨第一和第二流体流以及第二和第三流体流的分布。可选择流体流中转向的部分,以对具有感兴趣特性的组分(例如特定尺寸或特定电荷与尺寸之比)进行分析。
本发明的方法可用于使与感兴趣特性不同的组分转向。可改变第一或第二流体流的收集部分以使替代组分转向。分离技术也可适用于改变组分在流被转向的点处的分布。例如,扩散分离中的扩散时间可随流速的变化而改变,或者随着分离通道长度的变化而改变(如PCT/GB2013/052757中所述)。在电泳分离中的组分偏转可随着流速的变化而改变,或随着施加场的变化而改变(例如,如Herling等人所述)。无须按照流高度(或深度)的一部分来分离组合流。在本发明的装置中,可以通过将出口通道恰当放置在分离通道的下游端部,来分离流体流。转向通道可被放置在适当的侧向位置,以使来自分离通道的第一流体流或第二流体流(或多个流)的所要求部分的流体转向。
可收集层流中未转向的剩余部分,或可分析这些部分,下文将对此进行进一步的详细描述。
在本发明的一个实施方式中,使多个流体流部分转向。对层状流体流的至少一个转向部分进行分析。在层流的转向部分包括第二流体流的一部分时,对该转向部分进行分析。
每个转向流是第一流体流的一部分、第二流体流的一部分,或者是第一流体流和第二流体流的一部分。转向部分之一包括组分。在第一流体流包括多种组分时,多个流体流部分各自可包括一种组分。
下文描述了对转向流的下游后续分析。
在本发明的一个实施方式中,第一流和第二流的转向部分在分析后与流的其他部分重新组合。因此,可收集在原始第一流体流和第二流体流中的所有组分以用于进一步的分析和使用。
标记
本发明的方法可以包括标记步骤,其中,例如为了便于检测和/或分离,在流动设备内对组分进行标记。
本发明人已经建立了用于在分离装置内的流中对组分(诸如,蛋白)进行标记的方法。合适的标记技术描述于2013年11月14日提交的本发明人的早期申请GB 1320146.2中,该文献的内容通过引用而整体并入本文。
在一个实施方式中,对存在于转向流中的组分进行标记,以用于分析。可在第二分离之前在第三流体流中对组分进行标记;或者可在第二分离之后在第三流体流中对组分进行标记。
在一个实施方式中,在组分用于本发明的方法之前,对其进行标记。因此,不需要另外的标记步骤。在一个实施方式中,在方法结束时已经收集了组分之后,对该组分进行标记。在此,不必在方法进行过程中对组分进行标记。在一个实施方式中,在分析之前,对组分进行标记。可在转向流中对组分进行标记。
在一个实施方式中,使转向流与试剂流接触,并且使试剂流内的一种或多种试剂与转向流中的组分混合,可选地发生反应。在适当的混合和反应后,进行分析。可在流体流内对组分进行分析。试剂可为标记物或在反应时可生成可检测的标记物。
在本发明的一个实施方式中,在分离之后,例如在转向之后,对组分进行标记。标记过程是检测步骤的一部分,用于组分的分析。
在一个实施方式中,标记物是潜在标记物。潜在标记物是只有当它与组分相缔合时才成为光谱活性(如荧光活性)的标记物。否则,该标记物是非光谱活性的。因此,潜在标记物只有当它与组分相缔合时才可检测到,而在未与组分形成缔合的标记物时保持非光谱活性。由此得出,因为没有必要从流体流除去未反应的标记物,或不考虑标记物对所记录的光谱信号的贡献,而简化了对组分的检测。例如,并且如本文所述的,与组分的反应可除去标记物上存在的淬灭其荧光的基团,因此这一反应除去了淬灭。在另一个实例中,标记物(例如荧光基团)在标记反应过程中形成,例如通过形成延伸的共轭体系而形成。
在一个实施方式中,标记物共价键合到组分上。因此,所述标记步骤包括在标记物和组分之间形成一个或多个共价键。该共价键可以通过组分上的氨基、羟基或硫醇基团形成。在该组分是多肽,例如蛋白时,该共价键可通过氨基酸残基的侧链官能团形成。
在其他实施方式中,可使用非共价标记物,其对于所述组分可以是特定的或非特定的。拉姆齐小组描述(参见,例如,Liu et al.Anal.Chem.2000,72,4068)了用于组分的非共价标记物的实例。
在一个实施方式中,标记物与组分的氨基官能团,如伯氨基官能团(-NH2)反应。在组分是或包括多肽(诸如蛋白)时,标记物可以与多肽的赖氨酸残基反应。
在一个实施方式中,标记物衍生自邻苯二醛或含邻苯二醛的化合物。
本发明人已经发现,邻苯二醛(OPA)可用作潜在共价标记物。OPA可与组分的一个或多个氨基反应,以形成可检测的荧光标记物。优选地,在含硫醇试剂,诸如烷基硫醇(诸如乙醇(BME))的存在下,OPA与组分的氨基反应。
在一个实施方式中,标记反应基本上是定量反应。因此,在一个实施方式中,基本上对所有的转向组分进行标记。此外,在组分包含能够与标记物发生反应的多个基团时,基本上所有的基团都与标记物发生反应。因此,所记录的光谱信号可用于直接定量在流中的组分。此外,高度标记(即所有的组分被标记和/或组分具有多重标记)通常改进对流体流中的组分的检测。这在组分以极低浓度存在的流动条件下是特别重要的。
上述标记反应应当适用于流动体系。因此,标记反应在相对短的时间范围内发生很重要,因为流体在装置中的停留时间不长。本发明人已经发现,OPA标记物与组分(诸如蛋白)迅速反应,因此适用于本文所述的流动方法中。
在一个实施方式中,标记反应时间为至多5s、至多2s、至多1.5s或至多1s。标记反应时间可以是指标记至少50摩尔%、至少80摩尔%或至少90摩尔%的组分(优选90摩尔%)所花费的时间。在一个实施方式中,标记反应时间可以是指反应半衰期。
当本发明的方法包括对转向组分进行标记的步骤时,转向流与包括标记物的流体流(标记物流体流)接触,任选地与用于标记反应的相关试剂一起。转向流和标记物流体流在流动分离器下游的接合点汇集在一起。
允许组分和标记物在流体流内混合,从而标记该组分。可以允许标记物流和转向流沿混合通道流动,以确保在装置内有足够的时间来进行标记,例如,以允许在光谱分析之前有足够的时间来进行标记。
在一个一般实施方式中,组分的二级、三级和/或四级结构,诸如二级或三级结构,优选三级结构,在分离步骤之后、分析之前发生改变。使用本文所述的标记方法,本发明人发现不需要破坏组分的二级结构,足以改变三级和/或四级结构(当存在时),以允许进行适当的标记。
在一个实施方式中,该组分在分析之前被变性。变性步骤意于在组分上和组分内提供可利用的官能团,这可有助于该组分的标记和/或检测。例如,当组分是多肽(诸如,蛋白),变性步骤可以暴露出氨基、羟基和硫醇官能团,用于与标记物发生反应。
组分的变性可通过将变性试剂加入到流体流中来实现。例如,当组分是多肽时,可使用SDS作为变性试剂。上述变性步骤不限于使用变性试剂,可使用环境(诸如温度)的改变来实现变性。
可在标记前,使组分变性。可使变性步骤和标记步骤分开以最小化组分的沉淀,在组合的变性和标记步骤中可能发生组分的沉淀。
在变性步骤利用变性试剂时,可将变性试剂提供在与转向流接触的流体流(变性流)中。使转向流和变性流体流在流动分离器下游的接合点汇集在一起。允许组分和变性试剂在流体流内混合,从而使该组分变性。可允许变性流和转向流沿混合通道流动以确保在装置内有足够的时间用于变性,例如,以在与标记流(在使用时)接触之前或在光谱分析之前有足够的时间用于变性。
在所述方法还包括对组分进行标记的步骤时,标记步骤在变性步骤的下游进行。
可替代地,组分可以在一个组合步骤中被变性且被标记。在组分发生沉淀的风险较小时,可使用变性和标记的组合步骤。因此,在一个实施方式中,标记物流体流额外地包括变性试剂。如本文所示,允许转向流和标记流(含有变性剂)接触的接合点可适于处理变性问题。因此,流体通道在接合点处的表面能排斥流体中的组分,例如可使用亲水性表面来防止疏水性组分粘附至通道表面。
在转向流与标记物流或变性流接触时,优选地是允许流的内容物和与其接触的流的内容物快速混合。快速混合确保了组分的快速标记或变性。这与使第一流体流和第二流体流接触的步骤形成对比,其中无须或不期望组分横跨第一流和第二流快速分布。例如,在扩散分离步骤中,不希望在分离通道中过早地建立组分的均匀分布,因为这将使得组分不能被分离。对于扩散分离,需要建立横跨第一流体流和第二流体流的非均匀分布曲线。
分析和检测
本发明的方法可包括对流体流中的组分进行分析(诸如检测)的步骤。流体流可为第三流体流或第五流体流。流体流可为接触的第一流体流和第二流体流,或接触的第三流体流和第四流体流。
组分可具有使其能够在流体流中被分析的官能团。可替代地,如本文所述,可对组分进行标记以允许在流体流中对组分进行检测。如本文所述,荧光方法可用于对组分(可用荧光标记物进行合适的标记)的检测。
分析步骤可包括制备流体流的转向部分(包括制备组分)以用于分析的预备步骤。因此,根据需要,可制备第三流体流或第五流体流(如果存在)中的组分以用于分析。当制备用于分析的组分时,优选地是在其分离前或分离之后,对组分进行标记。
典型地,通过包括UV/vis的光谱法和荧光光谱法对组分进行分析,并且优选通过荧光光谱法对组分进行分析。荧光光谱法由于它的高信噪比而特别具有吸引力。
在对组分进行分析的同时,使其横跨接触的流,诸如接触的第一流和第二流,或者接触的第三流和第四流分布。记录的分布曲线可提供用于分辨分布内组分的足够的分析信息。可无须使流的一部分转向来确定接触流的组成。
因此,本发明的某些方法包括确定一种组分或多种组分横跨流体通道的分布的步骤。测量组分进入流的移动的方式没有特别限制,并且所采用的检测方法可基于待检测组分的性质。
检测器为适用于与流体流通道,特别是微流体通道一起使用的检测器。扩散检测方法是本领域所熟知的,并且例如由Kamholz等人描述的。如上所述,除其它外,实例包括UV-vis光谱法、荧光光谱法或发光光谱法。
可在分布通道中的一个位置处确定一种组分或多种组分的分布。然而,特别是在存在两种或更多种组分的情况下,可在沿通道的两个或更多个(诸如三个、四个或五个)位置处来确定组分的分布。该方法可包括以下步骤:在通道中的多个位置处确定组分的分布曲线。
在组分流中的组分移动到通道边缘(为空白流体流的装置的边界)之前,应当记录至少一个分布测量结果。
对于未知成分的样品,可建立试验流以确定第一组分到达边界边缘的点。因此,可在该点的上游进行第一分布测量。
在沿通道进行多个分布测量时,沿通道的第二测量和后续测量的各自位置并没有特别限制。通常,后续测量在沿通道的足够远的距离处进行,以给出与先前测量具有有用差异的分布曲线。
在本发明的方法中,建立了组分流和空白流的层流,并且该组分流和空白流的层流被设置在小横截面通道中。当流建立时,沿小横截面通道提供扩散梯度。因此,通过对沿小横截面通道的两个或更多个位置处的扩散曲线进行分析,可以同时获得不同扩散时间的数据。
本发明的方法不需要使空白流与组分流相分离。因此,可在组分流与空白流保持接触的同时,测量一种组分或多种组分的扩散曲线。
Kamholz等人描述了在具有组分流(具有单一组分)和空白流的通道的单个测量位置处测量扩散曲线。
在US 2006/263903的流体体系中,在横跨通道区域中接触一定时段后,空白流从组分流转向。在接触点处,组分流中的组分可扩散到空白流中。对分离的空白流进行分析,并且量化组分的量。为了获得组分的扩散系数值,需要获得在空白流和组分流之一或者两者的多个不同流速下,随着时间的若干测量值。
在分析之前,可以对感兴趣的组分进行标记以允许它们在本发明的方法中被检测到。标记物可以采取化学基团的形式,该化学基团能够通过例如标准UV-vis、荧光或发光光谱法来检测。
扩散系数的确定
本发明提供了用于例如在第一分布或第二分布步骤中,确定流体中的一种组分或多种组分的扩散系数的方法。
当组分流体含有单分散组分时,能够使用标准技术确定组分的流体动力学半径。例如Yager组(参见Hatch等人,以及Kamholz等人)所述的那些方法。
当组分流体含有多种组分的多分散混合物时,本发明提供了用于确定混合物中两种或更多种组分或每种组分的扩散系数的方法。这与本领域已知的通常仅提供整体混合物的平均扩散值的方法形成对比。在本发明的第三方面的方法中,随着不同的扩散时间,记录多个扩散测量值。
如本文所述,本发明的方法提供两种层状流体流。该方法在低雷诺数下进行,其中对流和扩散是与质量传递相关的唯一机制。这简化了通道内组分运动的模拟。
通常,相对于一系列的理论扩散曲线对所记录的扩散谱进行去卷积,该一系列的理论扩散曲线是针对具有流体动力学半径(以及因此的扩散系数)的系列组分所确定的,其中流体动力学半径所研究这些组分的半径的可能范围内。去卷积步骤将记录的数据拟合至由可能收集单个理论扩散曲线构成的整体曲线中。上述拟合是与实验误差一致的最简单方案。在上下文中,所提及的最简单方案涉及最小熵正则化。
参照所产生的基函数,对所记录的扩散曲线进行去卷积。基函数是理论扩散曲线的集合,其中每个理论曲线针对具有特定流体动力学半径的组分。该集合由一系列流体动力学半径的曲线组成。对于含多肽的样品,例如,曲线跨越多肽组分的可能半径范围,例如0.5nm至200nm,例如0.5nm至15nm。
在最大熵正则化的情况下,使用最小二乘拟合对记录的数据进行回归分析。结合模拟的基函数,记录的空间曲线可被去卷积为单个扩散曲线谱。
上述去卷积方法是有利的,因为它们提供了包含最少信息的最佳拟合的误差内的方案。进而防止了所谓的数据过拟合。
更详细地,本方法允许精确的数值计算来确定用于给定尺寸的物质的核函数。随后,将在流实验中得到的扩散曲线全局拟合到预测核函数的线性叠加,其中通过约束最小二乘拟合来确定每个核函数的振幅,其中,系数被限制在0到1的区间,以确保它们的物理解释为分数浓度。拟合中的残差提供对测量中误差的估算。然后,在最小熵正则化下进行第二系列的最小二乘拟合。熵在幅度上逐渐增加,直到正则化拟合的残差与随机误差水平的未正则化拟合的残差不同。用于最终拟合的系数是与实验误差一致的最简单(最小熵)解。
如本领域已知的,组分的流体动力学半径可由扩散系数确定。
如本领域已知的,扩散曲线也可用于确定组分流体中的组分浓度。
流动设备
本发明还提供一种用于本发明方法的流动设备。所述流动设备具有合适的流动通道以使组分能横跨流体流分布,并且使流体流的多个部分能转向。
典型地,所述流动设备具有流体连通的两个分离通道。每个分离通道适于使两个流体流在其中流动,例如在分离通道中以层流流动。
如本文中所述,本发明的流动设备包括:用于第一和第二流以及第三和第四流的第一分离通道和第二分离通道。第一分离通道,以及可选地第二分离通道,与下游流动分离器流体连通。每个分离通道适于允许组分在接触的流,诸如接触的第一和第二流,以及接触的第三和第四流之间进行横向移动;以及所述流动分离器适于使接触的流的一部分转向。例如,流动分离器适于使第一流体流的一部分、第二流体流的一部分、或者第一流体流的一部分和第二流体流的一部分从第一分离通道转向。
本发明的流动装置可以是集成装置,诸如整体式装置,具有集成的通道网络。因此,所述装置不具有死体积并且谱带增宽是有限的。
所述流动设备使用小流体通道、特别是微流体通道,因此可以对非常小的样品体积进行分析。因此,可以通过本文所述的方法对提供在小于一微升体积的流体中的组分进行分析。另外,通过适当增加测量次数,还可使用流体流动技术来分析非常稀的样品。
所述分离通道的横截面典型地是在微米范围内,并且因此,用在本发明的第一方面的方法中的流体装置可被称为微流体装置。
本发明还提供在此所述的微流体装置。
使用微流体通道来容纳第一流体流、第二流体流、第三流体流和第四流体流确保了在低雷诺数下发生流动。在本文所描述的扩散分离步骤下,对流和扩散是体系内与质量传递相关的唯一机制。因此,如本文进一步详细描述,这允许对给定尺寸的各组分进行准确的数值计算。在使用电泳方法进行分离时,对流和电泳是体系内与质量传递有关的唯一机制。
分离通道具有合适的大小,用于在其内产生并保持两个(或三个)流束的层流。两个流束的层流指这些流是并排地且是稳定的。因此,典型地,不存在流体再循环的区域,并且湍流最小。典型地,通过小通道,诸如微通道来提供此类条件。
对所述装置中通道的总体大小进行选择,以提供合理的移动速度和分析时间。还可对所述装置的大小进行选择,以减小用于充分分析运行所需要的流体量。
用于使组分横跨流体流扩散的装置,诸如用在分散测量中的装置是本领域所熟知并且例如Kamholz等人(Biophysical Joumal 80(4):1967-1972,2001)所述。
用于使组分横跨流体流电泳的装置是本领域所熟知,并且例如由Herling等人(Applied Physics Letters 102,184102-4(2013))描述。因此,分离通道沿通道长度可设置有电极,用于使横跨通道的带电组分偏转(分布)。这不同于由拉姆齐小组所述的装置,在拉姆齐小组所述的装置中,电极被放置在通道端部,以使组分沿通道长度分布。
分离通道为具有合适大小的通道,以允许产生稳定的流体流并且实现组分横跨流的充分分离。
第一分离通道是使第一流体流与第二流体流在其中进行接触的区域。第二分离通道是使第三流体流与第四流体流在其中进行接触的区域。
在本文中所提及的分离通道是指具有基本上为矩形横截面的通道。因此,分离通道可由基本上平的底部、基本上垂直于该底部延伸的多个壁,以及可选地顶盖构成。典型地,底部和壁由硅酮衬底形成。盖可为玻璃盖,例如为标准玻璃载片或硼硅酸盐晶片。
典型地,装置内的其它通道,诸如供应通道也可基本上为矩形。
第一分离通道与用于供应第一流体的一个或多个储液器流体连通。第一分离通道与用于供应第二流体的一个或多个储液器流体连通。
第二分离通道与用于供应第四流体的一个或多个储液器流体连通。第二分离通道经由用于供应第三流体的第一流动分离器与第一分离通道流体连通。
分离通道具有这样的区域:在其整个长度上都具有基本恒定的宽度。在分离通道中,该区域的宽度可为至多500IJm"、至多700IJm"、至多1000IJm"、至多2000IJm"或至多5000IJm"。该区域的宽度可为至少5、至少10、至少50、至少100或至少200。在一个实施方式中,在分离通道中,该区域的宽度可在选自上述给定的上限值和下限值的范围内。例如,所述宽度可在10至500的范围内。
在一个实施方式中,分离通道具有大截面通道的上游区域和小截面通道的下游区域。上述通道的区域可为通道的小横截面区域。
大截面通道可为使组分溶液流(例如第一流)与空白溶液流(例如第二流)进行接触的区域。然后,上述流由大横截面通道被导向小横截面通道。在小横截面通道中,对一种组分或多种组分进入空白流的横向运动进行监测。大横截面通道与小横截面通道流体连通。
大横截面通道的最大宽度W大于小截面通道的宽度。在一个实施方式中,大横截面通道中不存在宽度小于小横截面通道宽度的截面。在一个实施方式中,大横截面通道的最小宽度与小横截面通道的宽度相同。
大截面通道的最大宽度W可为至多500、至多700、至多1000、至多2000、至多5000或至多10000。通常来讲,大于10000的通道宽度是不实用的,因为制成装置的材料通常为PDMS,很易于发生凹陷。大截面通道的最大宽度W可为至少50、至少100、至少200或至少500。在一个实施方式中,大横截面通道的最大宽度可在选自上述给定的上限值和下限值的范围内。例如,所述宽度可在200至5000的范围内,诸如200至1000的范围内,或诸如1000至5000的范围内。
大横截面通道的长度为至多500、至多700或至多1000。大截面通道的长度为至少10、至少50、至少100或至少200。在一个实施方式中,大横截面通道的长度可在选自上述给定的上限值和下限值的范围内。例如,所述长度可在50至500的范围内,诸如100至500的范围内。
大横截面通道限制了在流体装置中供应通道的接合处的停滞的影响。因此,例如,所计算的扩散系数值和疏水半径可被认为在流体接合处使用大横截面通道时具有更大的精度。
在大横截面通道包括基本恒定的最大宽度的区域和宽度汇聚至小横截面通道的宽度的下游区域时,基本恒定的最大宽度的区域可为大横截面通道总长度的至少50%、至少60%、至少70%、至少80%或至少90%。
具有基本恒定宽度的通道区域的长度足以允许感兴趣的组分以典型流体流速移动到接触的流体流中。1mm长或更长的通道长度通常是足够的。在一个实施方式中,具有基本恒定宽度的通道区域的长度为至少0.5mm、至少1mm、至少2mm或至少5mm。在一个实施方式中,具有基本恒定宽度的通道区域的长度为至多10mm、至多20mm、至多50mm、至多100mm或至多500mm。在一个实施方式中,具有基本恒定宽度的通道区域可在选自上述给定的上限值和下限值的范围内。例如,具有基本恒定宽度的通道区域可在0.5mm至50mm的范围内,诸如1mm至20mm的范围内。
流体沿小横截面通道的纵向轴线流动。组分流中的组分进入空白流的扩散垂直于流动的纵向轴线,横跨通道的宽度。
典型地,所述流动设备包括第一供应通道和第二供应通道,这些通道与下游第一分离通道流体连通。第一供应通道用于容纳第一流体流,第二供应通道用于提供第二流体流。第一供应通道和第二供应通道在接合点处与下游分离通道汇合,该下游分离通道适于容纳层流形式的第一流体流和第二流体流。这些通道提供储液器与分离通道之间的流体连通。
类似地,所述流动设备包括第四供应通道,该通道与下游第二分离通道流体连通。所述第四供应通道用于容纳第四流体流。所述第四供应通道与第三供应通道汇合,在接合点处与下游第二分离通道汇合,该下游第二分离通道适于容纳第三流体流和第四流体流(诸如为层流的形式)。这些通道提供储液器和第二分离通道之间的流体连通。所述第三供应通道是第一流动分离器下游的通道。
在一个实施方式中,分离通道包括第一大横截面通道和第二小横截面通道,该第二小横截面通道在下游且与该大横截面通道流体连通。
本发明人已经发现,在流体(诸如第一和第二流体,或第三和第四流体)首次接触的接合点处使用大横截面通道最大限度地减少了流体滞留。此类通道在PCT/GB2013/052757中进行了描述。
流体沿分离通道的纵向轴流动。一种组分或多种组分从一个流进入另一流的运动(诸如一种组分或多种组分的扩散)垂直于流动的纵向轴线,横跨通道的宽度。
本发明的流动设备可结合本发明人的早期工作,诸如PCT/GB2013/052757中所述的流动装置,该文献的内容通过引用而整体并入本文。
所述流动设备包括:在第一分离通道下游且与其流体连通的第一流动分离器。所述第一流动分离器为横跨分离通道的一部分定位的通道,用于收集层流的一部分,尤其用于收集第一流体流的一部分或第二流体流的一部分,或者收集第一流体流的一部分和第二流体流的一部分。该通道的位置和宽度根据层流的待收集部分以及流的待收集部分来进行选择。
流动分离器使流的一部分从分离通道转向。流动分离器向下游第二分离通道提供转向流并且与下游第二分离通道流体连通。
第一分离通道设置在第二分离通道的上游。第一分离通道与第一供应通道和第二供应通道流体连通。第一通道用于供应含组分的第一流体,第二通道用于供应为空白流体的第二流体。第一流和第二流在第一分离通道下游端部的接合点处汇集在一起。
第一流动分离器设置在第一分离通道的下游端部。第一流动分离器收集来自第一分离通道的流动流的一部分并且使该流,例如经由第三流体供应通道转向至下游第二分离通道,其中第三流体供应通道在第一流动分离器和第二分离通道之间流体连通。来自第一分离通道的收集部分为第三流体流。
第二分离通道与上游第一流动分离器和第四供应通道流体连通。第四供应通道用于供应为空白流体的第四流体。第三流体流和第四流体流在第二分离通道上游端的接合点处汇集在一起。
可选地,第二流动分离器设置在第二分离通道的下游端部。第二流动分离器收集来自第二分离通道的流体流的一部分。从第二分离通道收集的部分为第五流体流。可收集该转向的流。
诸如本文所述,本发明的装置可部分使用标准光刻技术来制造。
流体装置的通道表面可适于防止组分粘附到表面。因此,在一个实施方式中,通道表面限制或防止组分被吸附到表面上。
在一个实施方式中,流体装置内的通道是亲水性的或疏水性的。本发明人已经发现,使用亲水性通道表面(特别是在检测区)防止疏水组分(诸如疏水蛋白)的吸附,从而改进在该装置中对组分的分析。类似地,可以使用疏水性通道以防止亲水性组分的吸附。
本发明人尤其发现,使用亲水性或疏水性通道表面在组分的标记和变性阶段是有益的。使标记步骤中生成的不溶性物质的量最少。
亲水性通道可以使用本领域技术人员熟悉的技术制备。例如,当装置中的通道是由PDMS制造时,可对该材料进行等离子体处理以使表面是亲水性的。在此,等离子体处理在通道的表面上生成亲水性的硅烷醇基团。此类技术如Tan等人(Biomicrofluidics 4,032204(2010))所述。
本发明的流动装置可包括串联布置在第二分离通道下游的额外的分离通道。因此,可使第二分离通道中的流体流的一部分转向,并且该分离的流,即第五流体流可进入第三分离通道,该第五流体流在第三分离通道中与第六流体流接触。可使存在于第五流体流中的组分移动到第三流体流中,以实现横跨第五流体流和第六流体流的非均匀分布。
流动设备的下游端可设置有干质量检测器。
其他偏好设置
在此明确公开了以上所述的各个实施方式以及实施方式的各种可行性组合,如同单独且明确地对各个实施方式以及各种可行性组合进行描述。
鉴于本发明,本领域技术人员将清楚本发明的多个其他方面和实施方式。
在本文中所使用的“和/或”应当理解为明确公开了两个具体特征或组分中的每一个(具有或不具有另外一个)。例如,“A和/或B”应当理解为明确公开了(i)A、(ii)B和(iii)A和B中的每一种情况,就像每一种情况在本文中单独地给出一样。
除非上下文中另外指出,否则上文列出的特征的描述和定义并不限于本发明的任何特定方面或实施方式,并且等同地应用于所描述的所有方面和实施方式。
现在将仅借助于实例并参照以上所述的附图来说明本发明的某些方面和实施方式。
实验
装置制造和操作
使用在3000rpm下旋转的SU8-3025光致抗蚀剂(MicroChem,Newton MA,USA),通过软光刻方法将装置制造成25的通道高度。被照射和显影的抗蚀剂形成负模,在该负模上,倾注未交联的聚二甲基硅氧烷(PDMS,Sylgard 184,Dow Corning,Midland M1,USA)并且进行固化。剥离硬化的PDMS,并且使其等离子体结合到显微镜载玻片上,从而产生密封的微通道,利用穿入至固化的POMS的弹性管状通孔能够达到该密封的微通道。通过将粘合的装置放置在78℃的热板上并将低熔点合金(51%In、32.5%Si、16.5%Sn,Indium Corporation,Utica NY,USA)插入自对准模具来生产电极。半径25且通过25进行分离的系列柱状物由于其表面张力而保留熔融金属,并且在降低温度时,合金凝固并形成固体壁电极。
本装置的设计在图1中示出,并且本装置包括用于电泳分离的第一组件(1)和用于扩散分离的组件(2)。第一组件能够确定组分的尺寸与电荷之比,第二组件能够确定组分的尺寸。
通过用注射泵(neMESYS,Cetoni GmbH,Korbussen,德国)以250IJUh的恒定流速从共用出口抽出液体,并将储液器连接到所有入口(凝胶加样移液管吸头,FisherBrand,Fisher Scientific,Loughborough,UK)来进行流体处理。装置上的流体动力学电阻网络导致约125IJUh的流通过自由流动电泳组件和扩散组件。对于第一组件和第二组件,分析物溶液和辅助流体(缓冲液流)之间的流量比为1:10。
流体装置的说明和应用
图1为根据本发明的一个实施方式的流体装置3的示意图。这种流体装置用在本文所述的示例性方法中。
所述装置包括电泳分离单元1和扩散分离单元2。如上所述,利用标准软光刻技术来制造所述装置。此外,Kamholz等人(Biophysical Joumal 80(4):1967-1972,2001)和Herling等人(Applied Physics Letters 102,184102-4(2013))描述了制造扩散装置和电泳装置的方法,并且本文所述的方法可适于制造本文所述的装置。
装置3包括在电泳分离单元1中的第一分离通道4。电极5沿通道长度被设置在该通道的任一侧。电极5与合适的电源(未示出)相连,该电源用于施加横跨分离通道4的场。提供第一分离通道4用于使组分进行电泳分布。
第一分离通道4通过上游第一供应通道6和上游第二供应通道7来供应。第一供应通道6用于将第一流体流从第一流体储液器8(“样品输入”)供应至第一分离通道4。第一流体流包括在例如多组分混合物中的组分。第二供应通道7用于将第二流体流从第二流体储液器9(“缓冲液输入”)供应至第一分离通道4。在使用中,允许第一流体和第二流体从储液器8和储液器9流经供应通道6和供应通道7,在第一分离通道4上游端部的接合点10处汇合。第二流体流被提供在第一流体流的任一侧。第一分离通道4具有大横截面的上游区域以及小横截面的下游区域。分离通道的上游区域存在大横截面通道与该分离通道中稳定流体流的形成相关。
通过注射泵(未示出)可控制流体穿过装置的运动。注射泵可位于上游端部,以独立地控制来自每个储液器的流体的流动。可替代地,泵可位于下游端部,以通过该设备来抽吸物质。流体也可通过重力加料运动穿过该装置。
接触的第一流体流和第二流体流被允许流过第一分离通道。通过适当施加横跨电极5的电压,来施加横跨第一分离通道4的电场。施加的电场可引起组分基于该组分的电荷与尺寸之比从第一流体流移动至第二流体流之一中。组分响应于施加场的运动可被称为偏转。在第一分离通道4的下游端部,一种组分或多种组分横跨第一流体流和第二流体流非均匀分布。
组分横跨通道的移动方向由该组分的电荷决定。带正电的组分将朝向负极移动,而带负电的组分将朝向正极移动。为此原因,在第一流体流的任一侧设置两个第二流体流:两个第二流体流各自回收带正电的组分或带负电的组分。
偏转的角度将取决于组分的质荷比。具有大电荷和/或较小质量的组分的偏转将大于具有小电荷和/或大质量的那些组分。偏转更多的组分将具有自第一流体流的最大移动,并且将更靠近第二流体流与通道壁的边界。偏转最少的组分将具有自第一流体流的最小移动,并且将更靠近第二流体流与第一流体流的接触区域。
在第一分离通道4的下游端部,提供了第一流动分离器11,用于使流体流的一部分从第一分离通道4转向。第一流动分离器11经设置,以收集接触的第一流体流和第二流体流中含感兴趣组分的横截面的部分。流体流的转向部分为含组分的第三流体流。流动分离器使第一流体流和/或第二流体流的一部分转向至第三供应通道中。
转向步骤能够使具有特定质荷比的一种组分或多种组分与具有其它质荷比的组分相分离。通过这种方式,转向步骤可用于从多组分混合物的其它组分中至少部分地纯化一种组分。图2中示出了原理,其中,中心流动分离器使具有感兴趣的电荷与尺寸之比的组分转向,并且使电荷与尺寸之比过高或过低的那些组分转向别处。
同样,转向步骤可用于对一种组分或多种组分进行分析。只有具有特定质荷比的那些组分将发生转向。因此,第三供应通道(或该通道的下游)中存在的组分表明具有特定质荷比的组分。
还使流体流的剩余部分转向,并且该流随后在装置下游出口处的收集腔12中进行组合。可替代地,这些转向部分也可利用扩散技术(诸如下文所述的用于转向的第三流体流的技术)进行后续分析。
第一流动分离器供应下游第三供应通道13(“样品回路”),进而供应第二分离通道14。
第二分离通道14通过上游第三供应通道13和上游第四供应通道15供应。第四供应通道15用于将第四流体流从第四流体储液器16(“缓冲液输入”)供应至第二分离通道14。在使用中,允许第三流体和第四流体从第一流动分离器11和第四流体储液器16流经供应通道13和供应通道15,在第二分离通道14的上游端部的接合点16处汇合。第四流体流被提供在第三流体流的任一侧。第二分离通道14具有大横截面的上游区域和小横截面的下游区域。在分离通道的上游区域处存在大横截面通道与该分离通道中的稳定流体流的形成相关。
允许接触的第三流体流和第四流体流流经第二分离通道14。随着流沿着第二分离通道14向前流动,允许第三流体流中的组分从第三流扩散至第四流中。移动量与组分的尺寸相关。在第二分离通道14的下游端部,一种组分或多种组分横跨第三流体流和第四流体流非均匀地分布。
移动量将取决于组分的尺寸。具有大尺寸的组分的移动将小于具有小尺寸的组分的移动。小组分将具有自第三流体流的最大移动。大组分将具有自第一流体流的最小移动,并且可基本上保留在第三流体流中。
可在不同扩散时间,对组分的扩散进行测量。在实践中,可在沿通道的不同位置,对组分横跨第二分离通道14的扩散曲线进行测量。在本发明的工作实例中对此进行了描述。
利用通过体系的流速的变化,在第二分离通道14中的单一位置处可得到不同扩散时间下的扩散曲线的测量值。这一方法是不太优选的,因为流速的变化将需要改变第一分离通道4中的分离条件以确保在第一分离通道的端部收集到相同的组分。例如,随着穿过体系的流速的变化,可能需要改变横跨第一分离通道4的施加场。
组分
在5mM,pH 8.0的HEPES缓冲液中,制备浓度2mg/mL的蛋白溶液。通过加入600的潜在荧光物(邻苯二甲醛,P0657,希格玛奥德里奇,Dorset,英格兰)和900的2-巯基乙醇(35602,Thermo Scientific,Cramlington,UK)来完成共价标记。在装置中使用之前,标记的样品在冰上(+4℃)孵育至少5分钟。随后,将20%v/v的二甲亚砜补充到标记的蛋白溶液中以避免蛋白的互相粘附。
补充有20%v/v二甲亚砜的5mM,pH 8.0的HEPES缓冲液用作辅助流体。
从FluoroMax(G50和G200)获得用于使混合物分级的荧光胶体,并且制造商分别将这些胶体的半径确定为23.5nm和100nm。
数据分析
理论上,扩散分级可通过本发明人在PCT/GB2013/052757的专利申请中所述的方法来实现。因此,通过使大量的具有给定尺寸r的各颗粒通过对流和扩散穿过通道进行传播,来生成所谓的基函数Br(y)。然后,将扩散组件的不同位置处的实验曲线拟合成这些基函数的线性组合,以获得量化溶液中具有半径r的颗粒的比例的系数Cr。优化算法本身通过利用至少100次随机移位的盆地跳算法(basin hopping procedure)来实现,以找到包括最小熵项的残差的全局最小值。
包括电泳分离步骤来增加电荷作为自变量。现在,基函数额外地具有对应于分析物的级分的振幅,该分析物的级分为对于给定大小的电场根据尺寸与电荷之比转移至分级组件的那些。这通过使具有半径r的颗粒经电泳组件进行传播,并使所获得的分布的中心位置成比例地转变成迁移速度来进行模拟。然后,通过在分离组件的出口处的相关区域中,对颗粒的级分进行计数来确定由Br;q(y)表示的基函数振幅。
通过对电场进行调整,改变该级分并且可以确定不同电压下的一组完整的扩散测量,可对该完整的扩散测量进行全局分析,即,基函数的线性组合现在必须满足对于所有施加电压所获得的扩散曲线。因为具有类似尺寸的颗粒仍然可根据电荷预分离(当改变电场时,产生不同的振幅特征),从而成倍地增加了上述方法的分辨率。
在本发明人的早期工作PCT/GB2013/052757的全局分析中,组分的全局分析来自于在多个扩散时间点,例如,沿单一分离通道的多个位置处的扩散曲线。扩散曲线均涉及相同的物理参数(流体动力学半径[尺寸]),并且在不同扩散时间下增加测量的扩散曲线的数目可能在某种程度上有助于对组分的复杂混合物的分辨。在本发明中,通过在扩散分离之前增加额外的分离步骤,并且该步骤基于独立于流体动力学半径的参数(例如电荷和等电点),使用于每种组分和每个分离参数(例如,这些参数是独立的)的信息量(例如包含在一组曲线中的信息量)成倍地增加。
装置的应用
图3中示出了扩散通道内和电泳组件端部的一组荧光显微镜图像。施加的电压从1V逐步增加到5V,使分析物束(在此,由标记有潜在荧光团的浓度为2mg/mL的I3-乳球蛋白组成)向分析腔的出口偏转(用黄色箭头标记),从而使扩散组件内的曲线的振幅增加。
从这些图像,可提取出扩散通道的四个位置处(自喷嘴下游2.5mm、4.7mm、20.7mm和64.7mm处)的荧光曲线。图4(a)中通过黑虚线示出了这样的曲线:该曲线在0V至5V范围内的电压下,由溶解在20%DMSO中并且经潜在荧光团(OPA)标记的2mg/mL I3-乳球蛋白来得到。红线是对这些数据的全局拟合,从而获得图4(b)绘制的基函数系数。这组系数表明:我们可以同时确定分析物的尺寸和电荷。获得的约3nm的流体动力学半径很好地对应于我们之前的发现。然而,在该阶段电荷的值还不可靠,因为分离组件的选择性仍然是中等的。
为了证实分离和分析混合物的能力,对半径为23.5nm和100nm的荧光胶体溶液进行了研究。图5(a)至图5(c)显示在0V、0.9V和1.5V的电压下,该混合物在电泳分离组件的端部的荧光显微镜图像。在没有电场的情况下,仅有一小部分的胶体进入到分析通道中。重要地是,只有较小的胶体能够通过扩散到达该通道,其通过红点线和黄虚线来对眼睛进行可视化,这些线分别表示23.5nm和100nm胶体的扩散传播。在非零场下,越来越多的颗粒偏转至分析通道中,并且在1.5V(参见图5(c))下,混合物的两种组分到达分级组件。此外,在该电压下,由于两种胶体具有明显不同的尺寸与电荷之比,使两种胶体流的中心现已彼此偏移。
在图5(d)中,以黑虚线示出了分级组件内测得的扩散曲线,而以红实线描绘了相应的拟合。从图像中可见,在分离组件的端部,对于较高的电压,偏转到分级组件中的颗粒量大大增加。除了在零场(根据模拟,仅有极小的颗粒会达到分析通道)之外,拟合的分布非常好地诠释了上述实验,并且图5(e)示出的所得到的系数表明23.5nm和100nm胶体的存在。另外,该拟合还包括由于在0V下分级组件内的胶体而出现的一系列小颗粒,其中预期扩散不允许颗粒进入分析通道。为了避免这些假象,可以改变装置几何形状以:i)允许在分离组件内扩散相对较小的量(例如通过加宽通道),ii)增加通过左废弃物通道的流量以减少在零场下能够到达分级组件的分析物的量,以及iii)在连接分离通道和分析/废弃物通道的节点处产生更简单的流场,这将允许更准确的模拟。
总之,据证实,在分离电泳步骤之后,在稳态层流下的扩散分级为用于复杂混合物的多维分析的原理证明实验。本发明人已经提出了对单分散溶液以及混合物的精确分级,其中,分离通道内的电场表明能够改变进入分析组件的混合物的组成的相对量。电荷尺寸的受限分辨源自电泳组件的当前几何形状,并且绝对不是该方法的基础。实际上,本发明人先前已经实现了精度优于电子电荷的电荷测量。
参考文献
该说明书中提及的所有文献通过引用而整体并入本文。
GB 1320146.2Hatch et al.Nature Biotechnology,19(5):461-465,2001Herling et al.Applied Physics Letters 102,184102-4(2013)Jacobson et al.Anal.Chern.1994,66,4127Jacobson et al.Anal.Chern.1994,66,3472Kamholz et al.Biophysical Journal 80(4):1967-1972,2001)Kamholz and Yager.Biophysical Journal,80(1):155-160,2001.Kohlheyer et a/.Electrophoresis 29,977(2008)Liu et al.Anal.Chern.2000,72,4608McDonald et a/.Ace.Chern.Res.35,491(2002)PCTfGB2013/052757Tan et a/.Biomicrofluidics 4,032204(2010)US 2006/263903Wales et al.J.Phys.Chern.A 101,5111(1997)。
- 还没有人留言评论。精彩留言会获得点赞!