一种固相萃取材料及其制备方法和应用与流程
本发明属于固相萃取材料
技术领域:
,特别涉及一种纳米硫化铜/聚六亚甲基单胍盐酸盐/硅胶复合材料及制备方法和该复合材料用于固相萃取水中痕量的cr(ⅵ)。
背景技术:
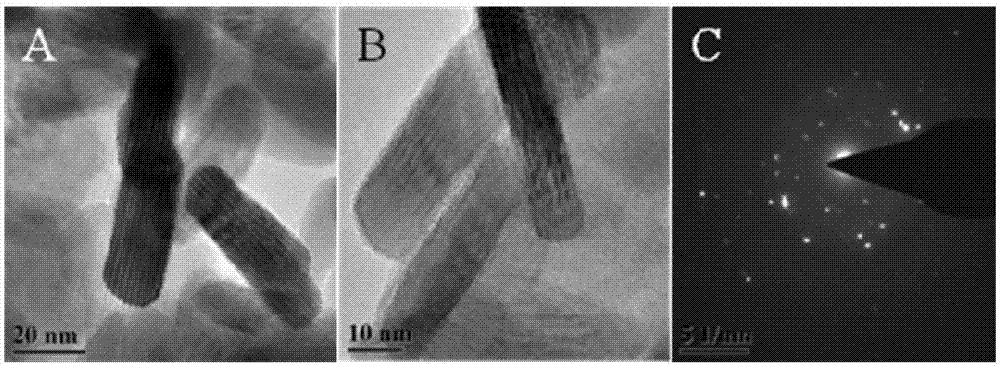
cr(ⅵ)是环境优先监测的五毒重金属元素之一,对人体有毒害作用,具有致癌、致突变等作用。而cr(ⅲ)是维持人体内正常的糖类、脂肪,蛋白质代谢的必需微量元素。因此,在环境水质监测中,准确测定各种价态铬的含量显得尤为重要。由于铬元素在水中含量低,常常需要富集步骤。固相萃取技术,因其具有选择性好、富集倍数高、处理体积样品小、可选择的吸附材料众多等优点,已广泛地应用在环境水样中铬的分离富集中。已有文献报道,将碳纳米管、纳米石墨烯等纳米材料用于固相萃取水中铬,取得很好的分析性能。但纳米材料在使用过程中,存在料粒径小,流动阻力大,易流失、易堵塞管路等问题。因此,有必要对固相萃取铬的材料和技术做进一步研究。技术实现要素:本发明的目的是针对于现有技术中固相萃取铬存在的问题,提供了一种固相萃取材料的制备方法及其应用。该材料为新型纳米硫化铜/聚六亚甲基单胍盐酸盐/硅胶三元复合材料,纳米硫化铜是一种非常重要的纳米材料,具有优良的吸附性能,但是由于纳米硫化铜颗粒较小,直接用于固相萃取很不方便。因此,需要将小颗粒的纳米硫化铜负载在大颗粒的载体表面。首先,利用静电引力将带有大量正电荷的阳离子型高分子聚合物聚六亚甲基单胍盐酸盐自组装在带有负电荷的硅胶表面,然后再将纳米硫化铜负载在其上面,从而制备成纳米硫化铜/聚六亚甲基单胍盐酸盐/硅胶这种复合材料。该复合材料即利用了硅胶的机械性能好,又利用了纳米硫化铜比表面积大的优势,同时又引进了有机官能团胍基和胍基盐,胍基盐的水解使材料表面带有的正电荷,均有利于对重金属cr(ⅵ)离子的吸附。并能够用于固相萃取水中痕量cr(ⅵ),具有良好的分析性能。为了达到上述目的,本发明的技术方案之一为,一种固相萃取材料,由活化硅胶颗粒,吸附在硅胶颗粒表面的聚六亚甲基单胍盐酸盐以及吸附在聚六亚甲基单胍盐酸盐上的纳米硫化铜组成;进一步的,所述聚六亚甲基单胍盐酸盐与活化硅胶颗粒的质量比为0.20-1.0:1,纳米硫化铜与活化硅胶颗粒的质量比为1:5-1:50;所述的活化硅胶颗粒粒径为80-100目;所述的聚六亚甲基单胍盐酸盐的平均分子量为2000-3000。本发明的技术方案之二为,上述固相萃取材料的制备方法:将活化硅胶投入到聚六亚甲基单胍盐酸盐溶液中,分散均匀,然后将纳米硫化铜投入到上述溶液中,分散5-10分钟,离心取沉淀,烘干,既得产品;较好的,所述的聚六亚甲基单胍盐酸盐溶液的质量浓度为0.5-2.0%;聚六亚甲基单胍盐酸盐与活化硅胶颗粒的质量比为0.20-1.0:1;纳米硫化铜与活化硅胶质量比为1:5-1:50;较好的,离心转数为10000-12000转/分钟,离心时间为5-20分钟;较好的,烘干方式为于30-50℃真空干燥箱烘干20-30小时。进一步的,上述方法中纳米硫化铜的制备方法为:在搅拌条件下,将硫代乙酰胺水醇溶液缓慢滴加到硫酸铜水醇溶液中,滴加结束后,将溶液转移至水热合成反应釜中,在120-140℃下反应10-14小时,反应完成后降至室温,取沉淀,干燥,制得长为50±5nm、宽为15±3nm左右的棒状纳米硫化铜;较好的,所述硫酸铜水醇溶液浓度为0.05-0.10mol/l,硫代乙酰胺水醇溶液浓度为0.15-0.30mol/l;较好的,所述硫酸铜水醇溶液与所述硫代乙酰胺水醇溶液的体积比为1:1;较好的,所述硫酸铜水醇溶液和硫代乙酰胺水醇溶液中水与醇的体积比为2:1-4:1;较好的,所述干燥方式为于30-50℃真空干燥箱干燥6-24小时。进一步的,上述方法中硅胶的活化方法为,将粒径为80-100目的硅胶放入1-2mol/l的硝酸溶液中浸泡18-30小时,过滤,用去离子水洗至中性,110-150℃下烘干6-10小时,取出备用,称为活化硅胶。本发明的技术方案之三为,上述制备方法制备的固相萃取材料的应用,用于固相萃取cr(ⅵ)。进一步的,上述制备方法制备的固相萃取材料的应用,所述用于固相萃取cr(ⅵ)包括如下步骤:1)称取适量固相萃取材料,装入萃取柱中,连接蠕动泵;将含cr(ⅵ)的样品溶液调成ph=3.0-5.0,对样品溶液过萃取柱富集cr(ⅵ);2)用硝酸溶液洗脱萃取柱上的cr(ⅵ),将洗脱液用火焰原子吸收分光光度计进行测定,记录吸光度值;3)采用标准曲线法确定该样品中cr(ⅵ)含量,再进一步进行铬的形态分析。较好的,萃取柱的规格为内径内径2.0±0.5mm、长25-45mm的聚四氟乙烯管,固相萃取材料的添加量为20-25mg;较好的,步骤1)中,需富集的样品溶液体积为20-60ml;较好的,样品溶液的过柱流速和硝酸溶液的洗脱流速为0.5-4.0ml/min;较好的,步骤2)中,洗脱液的体积为0.8-1.5ml。本发明具有如下有益效果:(1)本发明以硅胶为载体,利用静电引力将聚六亚甲基单胍盐酸盐和纳米硫化铜依次自组装在硅胶表面上,得到的复合材料对cr(ⅵ)具有良好的吸附性能。(2)本发明为新颖的固相萃取吸附材料,与单一的纳米硫化铜相比,吸附能力提高了5.3倍,吸附效率大大增加。(3)本发明复合材料,对cr(ⅵ)的富集效果理想,在进样体积较少的情况下,检出限低,准确性好,可准确测定环境水样中的cr(ⅵ)含量,还可以用于水样中铬的形态分析。附图说明图1、具体实施方式中制得的纳米硫化铜的透射电子显微镜图(a和b)及电子衍射图(c)。图2、实施例1复合材料的能谱分析图。图3、实施例1复合材料的红外谱图。具体实施方式下面结合具体实施例,进一步阐述本发明。实施例描述的内容仅为便于理解本发明,而非对本发明保护范围的限制。以下实施例中采用的纳米硫化铜的制备方法如下:配制浓度为0.07mol/l的硫酸铜水醇溶液和0.21mol/l的硫代乙酰胺水醇溶液,其中水醇比为3:1。移取上述硫酸铜溶液80ml于250ml烧杯中,取上述硫代乙酰胺溶液80ml,在磁力搅拌下,缓慢滴加到硫酸铜溶液中,滴加结束后,将混合溶液转移至200ml的水热合成反应釜中。将反应釜放入恒温干燥箱中,在120℃下反应12小时。反应完成后降至室温,采用离心的方式分离产物,反应产物用水洗涤数次,最后于30℃真空干燥箱干燥24小时,制得纳米硫化铜。将上述纳米硫化铜做透射电子显微镜及电子衍射分析,如图1所示。图1中a和b为不同放大倍数的纳米硫化铜的透射电子显微镜图,图1中c为纳米硫化铜纳米晶的电子衍射图。从图1中可以看出,样品为分布均匀的长50±5nm,直径15±3nm的棒状硫化铜纳米。从衍射斑点可知,纳米硫化铜为单晶。以下实施例中采用的活化硅胶的制备方法如下:称取20.0g粒径80-100目的硅胶放入250ml烧杯中,加入1.5mol/l的硝酸溶液100ml,搅拌后密封,浸泡10小时,过滤,用去离子水洗至中性,120℃下烘干6小时。以下实施例中采用的聚六亚甲基单胍盐酸盐的平均分子量为2000-3000。实施例1一种固相萃取材料制备方法,其具体作法是:称取活化硅胶100.0mg,放入10ml塑料离心管中,加入1.0%的聚六亚甲基单胍盐酸盐溶液10ml,摇匀、超声震荡10分钟,然后加入20.0mg纳米硫化铜,即纳米硫化铜与硅胶的质量比为1:5,摇匀、再超声震荡10分钟后,离心15分钟、离心转数为10000转/分钟,再用去离子水洗若干次后,放入30℃真空干燥箱,烘干24小时,即得到纳米硫化铜/聚六亚甲基单胍盐酸盐/硅胶三元复合材料。将上述复合材料做能谱分析,如图2所示。从图2中可以看出,该复合材料除含有硅胶中的si和o元素之外,增加了聚六亚甲基单胍盐酸盐中含有的c、n和cl元素,还增加了纳米硫化铜中含有的cu和s元素,证明复合材料已经成功制备。上述复合材料经研磨得粉末,用傅立叶红外光谱仪测量,结果如图3所示。结果显示,在3450-3300cm-1处的多个吸收峰,来自于硅胶分子间氢键-oh伸缩振动和聚六亚甲基单胍盐酸盐中-nh2伸缩振动;在2952cm-1,2881cm-1,2835cm-1处的吸收峰来自于聚六亚甲基单胍盐酸盐中-ch伸缩振动;在1688cm-1处的峰来自于-c=n的伸缩震动;在1539cm-1处的峰来自于聚六亚甲基单胍盐酸盐中-nh3+的吸收峰,1474cm-1和722cm-1处的两个吸收峰来自于-ch的变形振动;1066cm-1的吸收峰来自于硅胶中的si-o伸缩振动。可见,复合材料已经成功制备。实施例2一种固相萃取材料制备方法,其具体作法是:称取活化硅胶200.0mg,放入10ml塑料离心管中,加入1.0%的聚六亚甲基单胍盐酸盐溶液10ml,摇匀、超声震荡8分钟,然后加入20.0mg纳米硫化铜,即纳米硫化铜与硅胶的质量比为1:10,摇匀、再超声震荡10分钟后,离心10分钟、离心转数为12000转/分钟,再用去离子水洗若干次后,放入30℃真空干燥箱,烘干24小时,即得到纳米硫化铜/聚六亚甲基单胍盐酸盐/硅胶复合材料。实施例3一种固相萃取材料制备方法,其具体作法是:称取活化硅胶400.0mg,放入10ml塑料离心管中,加入1.0%的聚六亚甲基单胍盐酸盐溶液10ml,摇匀、超声震荡5分钟,然后加入20.0mg纳米硫化铜,即纳米硫化铜与硅胶的质量比为1:20,摇匀、再超声震荡5分钟,离心5分钟、离心转数为12000转/分钟,再用去离子水洗若干次后,放入40℃真空干燥箱,烘干24小时,即得到纳米硫化铜/聚六亚甲基单胍盐酸盐/硅胶复合材料。实施例4一种固相萃取材料制备方法,其具体作法是:称取活化硅胶300.0mg,放入10ml塑料离心管中,加入1.0%的聚六亚甲基单胍盐酸盐溶液10ml,摇匀、超声震荡5分钟,然后加入10.0mg纳米硫化铜,即纳米硫化铜与硅胶的质量比为1:30,摇匀、再超声震荡8分钟后,离心15分钟、离心转数为10000转/分钟,再用去离子水洗若干次后,放入40℃真空干燥箱,烘干24小时,即得到纳米硫化铜/聚六亚甲基单胍盐酸盐/硅胶复合材料。实施例5一种固相萃取材料制备方法,其具体作法是:称取活化硅胶400.0mg,放入10ml塑料离心管中,加入1.0%的聚六亚甲基单胍盐酸盐溶液10ml,摇匀、超声震荡5分钟,然后加入10.0mg纳米硫化铜,即纳米硫化铜与硅胶的质量比为1:40,摇匀、再超声震荡7分钟后,离心20分钟、离心转数为10000转/分钟,再用去离子水洗若干次后,放入35℃真空干燥箱,烘干24小时,即得到纳米硫化铜/聚六亚甲基单胍盐酸盐/硅胶复合材料。实施例6一种固相萃取材料制备方法,其具体作法是:称取活化硅胶500.0mg,放入10ml塑料离心管中,加入1.0%的聚六亚甲基单胍盐酸盐溶液10ml,摇匀、超声震荡5分钟,然后加入10.0mg纳米硫化铜,即纳米硫化铜与硅胶的质量比为1:50,摇匀、再超声震荡5分钟后,离心15分钟、离心转数为12000转/分钟,再用去离子水洗若干次后,放入50℃真空干燥箱,烘干20小时,即得到纳米硫化铜/聚六亚甲基单胍盐酸盐/硅胶复合材料。实施例7一种固相萃取材料制备方法,其具体作法是:称取活化硅胶200.0mg,放入10ml塑料离心管中,加入0.5%的聚六亚甲基单胍盐酸盐溶液10ml,摇匀、超声震荡5分钟,然后加入20.0mg纳米硫化铜,即纳米硫化铜与硅胶的质量比为1:10,摇匀、再超声震荡5分钟后,离心10分钟、离心转数为12000转/分钟,再用去离子水洗若干次后,放入40℃真空干燥箱,烘干24小时,即得到纳米硫化铜/聚六亚甲基单胍盐酸盐/硅胶复合材料。实施例8一种固相萃取材料制备方法,其具体作法是:称取活化硅胶200.0mg,放入10ml塑料离心管中,加入1.5%的聚六亚甲基单胍盐酸盐溶液10ml,摇匀、超声震荡5分钟,然后加入20.0mg纳米硫化铜,即纳米硫化铜与硅胶的质量比为1:10,摇匀、再超声震荡5分钟后,离心20分钟、离心转数为10000转/分钟,再用去离子水洗若干次后,放入40℃真空干燥箱,烘干24小时,即得到纳米硫化铜/聚六亚甲基单胍盐酸盐/硅胶复合材料。实施例9一种固相萃取材料制备方法,其具体作法是:称取活化硅胶200.0mg,放入10ml塑料离心管中,加入2.0%的聚六亚甲基单胍盐酸盐溶液10ml,摇匀、超声震荡10分钟,然后加入20.0mg纳米硫化铜,即纳米硫化铜与硅胶的质量比为1:10,摇匀、再超声震荡10分钟后,离心20分钟、离心转数为10000转/分钟,再用去离子水洗若干次后,放入40℃真空干燥箱,烘干24小时,即得到纳米硫化铜/聚六亚甲基单胍盐酸盐/硅胶复合材料。应用例1将实施例1~6制得的固相萃取材料各取20mg,装入内径为2.0mm,长30mm的聚四氟乙烯富集柱中,连接蠕动泵,将ph为4.0,浓度为0.2mg/lcr(ⅵ)标准溶液60ml,以3.0ml/min的采样流速,过富集柱进行富集。然后取1.0mol/l硝酸溶液1ml,以3.0ml/min的洗脱流速进行洗脱,将洗脱液用火焰原子吸收分光光度计进行测定,记录吸光度值。并与单一的纳米硫化铜和单一的硅胶进行比较研究,实验结果见表1。表1、纳米硫化铜与硅胶质量配比的影响从表1中可以看出,纳米硫化铜与硅胶质量比在1:5-1:50范围内,复合材料对cr(ⅵ)的富集吸光度明显高于单一使用纳米硫化铜的吸光度,尤其以质量比在1:5-1:30范围内,吸光度最大。与单一纳米硫化铜的吸光度比较,提高了接近5.3倍。说明在此质量比范围内,制备的复合材料显著提高了对cr(ⅵ)的吸附性能。应用例2将实施例7、2、8、9制得的固相萃取材料各取20mg,装入内径为2.0mm,长30mm的聚四氟乙烯富集柱中,连接蠕动泵,将ph为4.0,浓度为0.2mg/lcr(ⅵ)标准溶液50ml,以2.5ml/min的采样流速,过富集柱进行富集。然后用1ml1.0mol/l硝酸溶液以2.5ml/min的洗脱流速进行洗脱,将洗脱液用火焰原子吸收分光光度计进行测定,记录吸光度值,实验结果见表2。从表2中可以看出,聚六亚甲基单胍盐酸盐的浓度为0.5-2.0%范围内,复合材料对cr(ⅵ)的富集吸光度明显高于单一使用纳米硫化铜的吸光度,尤其以聚六亚甲基单胍盐酸盐的浓度为1.0-2.0%范围内,吸光度最大。考虑到聚六亚甲基单胍盐酸盐的浓度越大,粘度越大,离心效果不好。因此最佳聚六亚甲基单胍盐酸盐的浓度为1.0%。表2、聚六亚甲基单胍盐酸盐浓度的影响实施例7实施例2实施例8实施例9单一纳米硫化铜浓度0.5%1.0%1.5%2.0%——吸光度0.1640.2850.2860.2860.054应用例3将实施例3制得的固相萃取材料取20mg,装入内径为2.0mm,长30mm的聚四氟乙烯富集柱中,连接蠕动泵,将样品溶液的ph值调为4.0,以1.5ml/min的采样流速,对30ml水样过富集柱进行富集。然后将1.0mol/l硝酸溶液1ml以1.5ml/min的洗脱流速进行洗脱,将洗脱液用火焰原子吸收分光光度计进行测定,记录吸光度值。采用上述固相萃取水中cr(ⅵ)的方法建立标准曲线,线性范围为0.5-300μg/l;检出限低,可达0.15μg/l;精密度好,相对标准偏差为1.7%。同时用国家标准物质(gsb07-3174-2014)验证了该方法的正确性,测定值为(65.8±1.9)μg/l,与标准值(65.0±3.1)μg/l一致。同时,对实施例3的材料做专一性实验,考查了在不同ph(2-10)值条件下,cr(vi)和cr(iii)在复合材料上的富集效果。实验结果见表3,由表3可见,复合材料对cr(vi)在整个ph范围内都有吸附,尤其在ph=4时,cr(vi)的吸光度最大;而对cr(iii)的吸附能力很小,基本无吸附,可忽略不计。实验结果表明本发明的材料能够专一性的吸附cr(vi)。因此,该复合材料可用于铬的形态分析。表3、ph对cr(vi)和cr(iii)在复合材料上的富集效果的影响元素ph2345678910cr(vi)吸光度0.1050.1620.2860.1830.1140.0910.0810.0680.066cr(iii)吸光度0.0060.0070.0080.0080.0120.0160.0160.0110.007上述的验证实验说明上述建立的方法准确性好,可用于环境水中铬的形态分析。应用例4采用应用例3的方法对来自湖水、河水和雨水的未知水样中的铬进行形态分析,取一份适量水样按应用例3的方法测定水样中cr(vi)的含量,并进行了加标回收实验。另取一份适量水样,加双氧水将水样中cr(iii)氧化为cr(vi),按应用例3的方法测定水样中总铬的含量,然后用差减法算出cr(iii)的含量,实验结果见表4。由表4可见,cr(vi)和cr(iii)的加标回收率分别为102.2%-107.5%和98.3%-108.7%,结果满意。表4、环境水样中铬的形态分析(n=3,置信度95%)当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1