一种大鼠CD4抗体包被磁珠及其制备方法和应用以及含该磁珠的试剂盒与流程
本发明涉及一种大鼠cd4抗体包被磁珠及其制备方法和应用以及含该磁珠的试剂盒。
背景技术:
现有市面上,还没有一种试剂盒,能够用来检测大鼠肾移植后的免疫排斥反应。
技术实现要素:
本发明的目的在于提供一种大鼠cd4抗体包被磁珠及其制备方法和应用以及含该磁珠的试剂盒。
本发明的目的通过如下技术方案实现:
一种大鼠cd4抗体包被磁珠的制备方法,步骤1:将磁珠通过c1试剂洗涤,之后放在磁铁上吸附后去上清液;
步骤2:将步骤1预处理的磁珠中加入抗体、c1试剂、c2试剂后,在室温条件下离心旋转16-24h;
步骤3:将步骤2处理的磁珠通过磁铁沉淀,后通过hb试剂进行清洗;
步骤4:将步骤3处理的磁珠通过磁铁沉淀后去上清,后通过lb试剂进行清洗;
步骤5:将步骤4处理的磁珠通过磁铁沉淀后去上清,后通过sb试剂进行清洗;该过程可根据抗体渗漏情况重复多次;
步骤6:将步骤5处理的磁珠再加入sb试剂,离心处理,之后放置于磁铁吸附后去除上清液,完成大鼠cd4抗体包被磁珠的制备;
其中,c1试剂为60-100%丙烯醛缓冲液,c2试剂为pbs缓冲液。
它还包括步骤7:将步骤6处理的磁珠中加入sb试剂,在2-8℃下储存。
步骤7中还包括防腐剂叠氮化钠。
进一步的,步骤2中,磁珠和抗体、c1试剂、c2试剂的重量体积比为1mg∶20ul∶30ul∶50ul。
进一步的,步骤3中,磁珠和hb试剂的重量体积比为1mg∶40ul。
进一步的,步骤4中,磁珠和lb试剂的重量体积比为1mg∶40ul。
进一步的,步骤5中,磁珠和sb试剂的重量体积比为1mg∶40ul。
所述hb试剂、lb试剂、sb试剂均为0.01%-0.1%tween20。
所述磁珠为环氧树脂磁珠。
所述抗体为兔抗鼠的抗体。
一种通过上述制备方法制得的大鼠cd4抗体包被磁珠。
一种试剂盒,所述试剂盒包括大鼠cd4抗体包被磁珠的制备方法所制得的大鼠cd4抗体包被磁珠。
大鼠cd4抗体包被磁珠在检测大鼠肾移植后的免疫排斥反应中的应用。
较之现有技术而言,本发明的优点在于:大鼠cd4抗体包被磁珠的制备方法,通过上述方法制成的大鼠cd4抗体包被磁珠结合immuknowtm-cylex
附图说明
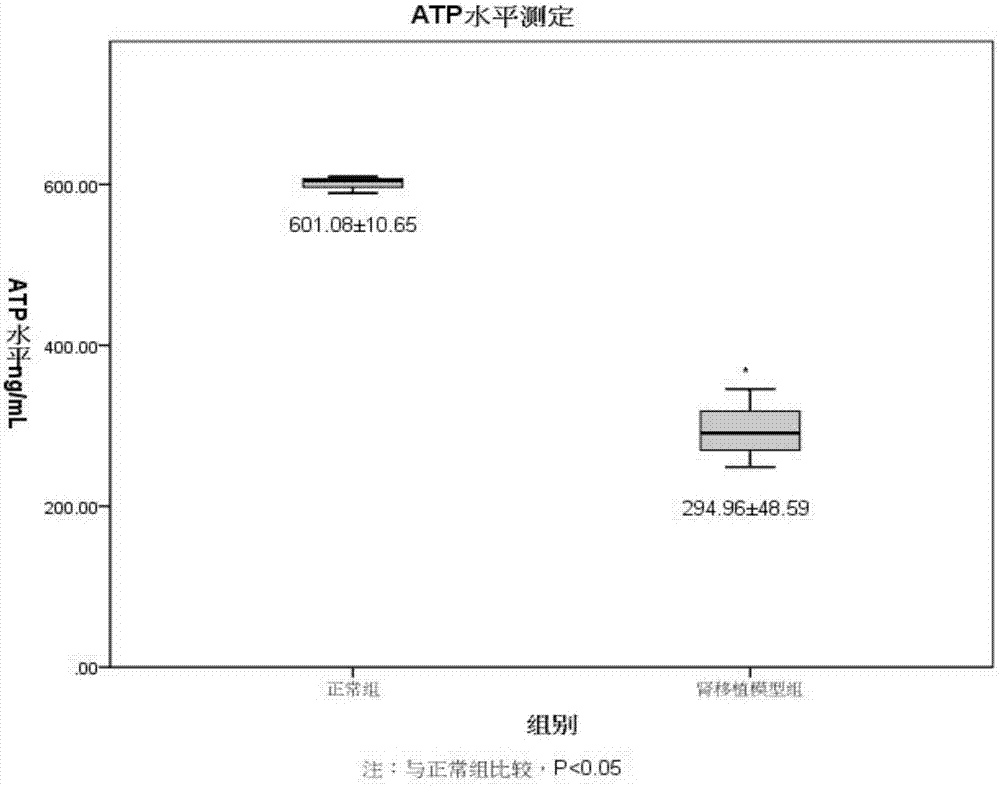
图1正常大鼠和肾移植大鼠atp水平测定对比图。
具体实施方式
下面结合说明书附图和实施例对本发明内容进行详细说明:
实施例1:
一种大鼠cd4抗体包被磁珠的制备方法,所述方法包括以下步骤:
步骤1:用适量75%是丙烯醛缓冲液试剂洗环氧树脂磁珠,涡旋。洗完后放在磁铁上吸附1min,然后去上清。该过程中,只要保证丙烯醛缓冲液的量能够清洗环氧树脂磁珠即可,即便过量也无妨。
步骤2:将步骤1预处理的环氧树脂磁珠中加入丙烯醛缓冲液、pbs缓冲液后,在37℃室温条件下离心旋转16h;其中各组分的占比如下:5mg环氧树脂磁珠、100ul兔抗鼠抗体、150ul丙烯醛缓冲液、250ulpbs缓冲液。
步骤3:将步骤2处理的环氧树脂磁珠通过磁铁沉淀1min,后通过hb试剂进行清洗;5mg的环氧树脂磁珠用200ul0.05%tween20试剂进行清洗。
步骤4:将步骤3处理的环氧树脂磁珠通过磁铁沉淀1min后去上清,后通过lb试剂进行清洗;5mg的环氧树脂磁珠用200ul0.05%tween20进行清洗。
步骤5:将步骤4处理的环氧树脂磁珠通过磁铁沉淀1min后去上清,后通过sb试剂进行清洗;5mg的环氧树脂磁珠用200ul0.05%tween20试剂进行清洗。
步骤6:将步骤5处理的环氧树脂磁珠再加入0.05%tween20试剂,离心处理,之后放置于磁铁吸附后去除上清液,完成大鼠cd4抗体包被磁珠的制备。
步骤7:将步骤6处理的磁珠中加入0.05%tween20试剂,在2-8℃下储存。其中,按100ulsb试剂/mg磁珠的配比关系,添加0.05%tween20试剂。
实施例2
一种试剂盒,所述试剂盒包括实施例1中大鼠cd4抗体包被磁珠的制备方法所制得的大鼠cd4抗体包被磁珠。
实施例3
对发明制得的大鼠cd4抗体包被磁珠进行atp检测,具体实验过程如下:
1.试验第一部分:细胞刺激。
预先从冰箱取出试剂盒中相关组分并平衡至室温。
1.1小心地颠倒混匀质控对照和大鼠cd4全血样本,重复多次以确保血细胞分布均匀。:
1.2用样本稀释液按1:3稀释质控和全血样本(例如:250ul全血+750ul样本稀释液)。
1.3稀释后,每个样本使用一条8孔培养板板条,按照工作表组装培养板。
1.4将25ul样本稀释液加入每个板条的前4个孔中,作为非刺激孔。
1.5将25ul样本稀释液加入每个板条的其余4个孔中,作为刺激孔。
1.6将100ul已稀释的质控样本加入板条1的各孔中。
1.7根据工作表,将100ul已稀释的待测样本加入相应板条的各孔中。
1.8盖上培养板盖,在平板振荡器上震荡30秒。
1.9将带盖的培养板在37℃/5%co2/加湿处理的培养箱中孵育16-18小时。
2.实验第2部分:cd4细胞选择和atp释放。
预先从冰箱取出试剂盒中相关组分并平衡至室温。
2.1从培养相中拿出培养板,置于平板振荡器上震荡3分钟。
2.2小心颠倒cd4磁珠溶液试剂瓶若干次以充分悬浮磁珠;用单通道移液器或连续加样移液器向各孔分别加入50ul磁珠。磁珠在吸取前应充分悬浮以确保各孔加入量一致。
注意:因为磁珠不易在储液槽中充分悬浮,请不要用多通道微量移液器操作这一步骤。
2.3盖上培养板盖,在平板振荡器上震荡30秒,室温下静置(18-28℃)孵育15分钟。震荡培养板30秒,室温(18-28℃)再次静置孵育15分钟。最后,再次震荡培养板30秒以重新悬浮磁珠。
2.4从培养板上取出板条,放在组装好的磁座上,等待1-2分钟使磁珠聚集在孔的一侧;按以下步骤从全血中分离cd4细胞。
2.5用连接到负压抽吸真空泵系统的8通道吸头伸入微孔吸除磁珠以外的的含红细胞培养液。注意轻柔操作,避免吸走磁珠。
2.6洗涤板条三次,以清除残余的未结合的游离细胞和孔中的其他干扰物质。
注意:加入洗涤液时,需垂直提持多通道微量移液器,避免移液器吸头触碰微孔内壁上的磁珠。
洗涤#1:向各孔加入200ul洗涤液,等待一分钟,然后吸走洗涤液。
洗涤#2:向各孔加入200ul洗涤液,检查微孔内壁,若有凝血斑,则用微量移液器吸头将其移除。等待1分钟,然后吸走洗涤液。
洗涤#3:向各孔加入200ul洗涤液,从磁座上移去板条架,将板条放在平板振荡器上振荡1分钟,然后将板条架放在磁座上。等待1分钟,待磁珠聚集在孔的一侧,然后吸走洗涤液。
2.7向各孔加入200ul裂解试剂。
2.8将板条架从磁座上移开,在平板振荡器上振荡5分钟。
2.9将板条架放在磁座上,等待1-2分钟。
2.10继续进行试验第3部分。
注意:如果不能立即(4小时内)进行试验第3部分,应将板条冷冻保存:将板条从磁座板条架上取下来,放在培养板框架上;密封板条,盖上培养板盖,-20℃冷冻保存。冷冻的板条至少在1个月内保持稳定。若要继续进行后续检测试验,从冰箱中取出培养板,将其平衡至室温(18-28℃),把板条放入磁座板条架上,然后重复上述2.8和2.9步骤。
3.试验第3部分:atp测量。
3.1参照试验工作表组装测量板:测量板包括质控测量条,大鼠cd4样本测量条,校准品测量条。
3.2依据工作表,用多道微量移液器从培养板各孔取出50ul裂解产物,加入测量板条相应孔中;将裂解产物加入每一板条之前,需更换新的移液器吸头。
3.3依照工作表,从各浓度水平atp校准品中各取出50ul分别加入测量板的相应孔(通常做2个复孔)
3.4发光试剂:使用前,轻轻颠倒使其充分混匀。用多道微量移液器取150ul发光试剂加至测量板的各孔中;将测量板置于平板振荡器上振荡30秒,以确保充分混合。在加入发光试剂后3-10分钟内读取相对发光强度(rlu)。最终结果参见图1,正常大鼠检测发现atp结果为601.08±10.65ng/ml,而肾移植之后的大鼠atp结果为294.96±48.59ng/ml,与正常对照组相比p<0.05,差异具有统计学意义。本发明制备的大鼠cd4抗体包被磁珠能够用于检测大鼠肾移植后的免疫排斥反应。
- 还没有人留言评论。精彩留言会获得点赞!