一种基于非标记、非固定化的电化学磁性生物传感器检测5-羟甲基胞嘧啶的方法与流程
本发明属于生物技术领域,具体涉及一种非疾病诊断用途的基于非标记、非固定化的电化学磁性生物传感器检测5-羟甲基胞嘧啶的方法。
背景技术:
与5-甲基胞嘧啶(5-mc)测定相比,5-羟甲基胞嘧啶(5-hmc)的准确定量仍然是一个巨大的挑战,因为它具有相对较低的丰度和与更丰富的5-甲基胞嘧啶具有相似性。亚硫酸氢盐测序方法被认为是5-甲基胞嘧啶测定的标准,但它具有无法区别5-甲基胞嘧啶和5-羟甲基胞嘧啶的缺点。目前,已经开发出用于基因组dna中5-羟甲基胞嘧啶测定的各种方法,例如单分子实时(smrt)测序、液相色谱/串联质谱(lc/ms-ms)、高效液相色谱(hplc),薄层色谱(tlc),酶放射性糖基化标记和免疫测定,这些方法可以有效区分5-羟甲基胞嘧啶和5-甲基胞嘧啶。
由于具有低成本,便携性和高灵敏度的优点,基于酶修饰的电化学生物传感器已被用于检测低丰度(pm级别)的5-羟甲基胞嘧啶。然而,基于酶修饰的方法需要昂贵的受dna序列限制的酶、合成酶辅因子/底物的类似物,以及繁琐的碱基修饰步骤。为了克服这些限制,已经开发了一种电致化学发光(ecl)生物传感器,基于kruo4可以将5-羟甲基胞嘧啶特异性氧化至5-甲酰基胞嘧啶(5-fc)来量化5-羟甲基胞嘧啶-dna,然后用电致化学发光(ecl)发光分子n-(4-氨基丁基)-n-乙基异鲁米诺(abei)标记。最近,bayley小组发现了一种替代方法,其中5-羟甲基胞嘧啶是用生物素原位一步化学修饰的,可以富集稀有的含5-羟甲基胞嘧啶的序列并用蛋白质纳米孔进行鉴定。然而,这些方法仅作为概念证明,它们并不适用于检测基因组dna中的5-羟甲基胞嘧啶。
技术实现要素:
针对5-羟甲基胞嘧啶检测存在的问题,本发明提供一种基于非标记、非固定化的电化学磁性生物传感器检测5-羟甲基胞嘧啶的方法。本发明采用末端转移酶(tdt)和ru(iii)氧化还原循环的双信号放大策略,利用非标记、非固定化电化学磁性生物传感器准确定量基因组dna中的5-羟甲基胞嘧啶的电化学方法。
本发明采用以下技术方案:
本发明第一个方面,提供一种非疾病诊断用途的基于电化学磁性生物传感器检测5-羟甲基胞嘧啶的定量分析方法,基于末端转移酶和ru(iii)氧化还原循环的双信号放大策略,利用以丝网印刷碳电极(spce)的电化学磁性生物传感器定量分析5-羟甲基胞嘧啶。
进一步的,所述非疾病诊断用途的基于电化学磁性生物传感器检测5-羟甲基胞嘧啶的定量分析方法具体步骤为:dna链中5-羟甲基胞嘧啶位点的生物素化;具有链霉亲和素包被的磁珠(mb)富集生物素化的5-羟甲基胞嘧啶dna链;末端转移酶催化聚合生物素化5-羟甲基胞嘧啶dna链的延伸;加入ru(nh3)63+/fe(cn)63-体系产生增强的电催化信号;电化学磁性生物传感器定量分析。
进一步的,用半胱氨酸-生物素进行一步亚硫酸氢盐介导的dna链中5-羟甲基胞嘧啶位点的生物素化。
更进一步的,将半胱氨酸-生物素和双链dna混合加入na2s2o5溶液,42~45℃下孵育48~50小时,待溶液冷却至室温,调节ph值,在室温下反应5~10分钟后,将样品通过micro-bio-spinp6柱除去过量的半胱氨酸-生物素和盐,即得。
进一步的,在末端转移酶反应体系中催化聚合生物素化的5-羟甲基胞嘧啶dna链的延伸;所述末端转移酶反应体系包括1×末端转移酶缓冲液、cocl2溶液、dntps和末端转移酶。
进一步的,ru(nh3)63+/fe(cn)63-体系包括1~1.5mmpbs缓冲液,0.1~0.5mnacl,27~30μmru(nh3)63+和2~5mmfe(cn)63-。
进一步的,电化学磁性生物传感器利用0至-500mv,脉冲幅度为50mv,脉冲宽度为50ms的差分脉冲伏安法来记录电化学响应,参比电极为ag/agcl。
本发明第二个方面,提供以上所述的定量分析方法在各种非疾病诊断目的的生物、组织、各种核酸序列中5-羟甲基胞嘧啶分析检测中的应用。
进一步的,5-羟甲基胞嘧啶为基因组dna中5-羟甲基胞嘧啶;所述细胞可为人宫颈癌细胞系(hela细胞)和人胚胎肾细胞系(hek293t)细胞。
本发明第三个方面,提供一种定量分析5-羟甲基胞嘧啶的试剂盒,所述试剂盒包括半胱氨酸-生物素、na2s2o5溶液、链霉亲和素包被的磁珠、洗涤缓冲液、末端转移酶反应液、ru(nh3)63+/fe(cn)63-体系反应液和丝网印刷碳电极;
所述洗涤缓冲液包括:0.5mnacl、20mmtris-hcl和1mmedta,tris-hclph值为7.4;
末端转移酶反应液包括1×末端转移酶缓冲液、0.25mmcocl2溶液、dntps和末端转移酶;
ru(nh3)63+/fe(cn)63-体系反应液包括:1~1.5mmpbs缓冲液,0.1~0.5mnacl,27~30μmru(nh3)63+和2~5mmfe(cn)63-。
本发明取得的有益效果:
(1)原理简单,降低成本:相比于基于酶修饰的电化学生物传感器的方法,本发明方法由于引入末端转移酶,无需昂贵的具有受限识别基序的酶,酶辅因子/底物的类似物的合成,以及碱基修饰的多个步骤,使原理更为清晰易懂;由于丝网印刷碳电极的引入,相比于单分子实时测序,本发明无需复杂且昂贵的的仪器,大大降低了实验的成本。
(2)可做实际样品检测:利用基于丝网印刷碳电极的电化学磁性生物传感器,该生物传感器可灵敏地定量5-羟甲基胞嘧啶,无需将dna固定在电极上。重要的是,该生物传感器可用于人宫颈癌细胞系(hela细胞)和人胚胎肾细胞系(hek293t)细胞中5-羟甲基胞嘧啶的精确定量,并可以很好的区分胞嘧啶(c),5-甲基胞嘧啶和5-羟甲基胞嘧啶。
(3)灵敏度高:本发明利用末端转移酶不需要任何dna模板地催化重复添加dntps,产生更长的dna序列,因此会有更多的ru(nh3)63+可以静电结合到延长的带负电荷的磷酸骨架上,同时,ru(nh3)63+作为一次电子受体发挥作用,fe(cn)63-作为二次电子受体发挥作用。过量的fe(cn)63-可以通过氧化电化学被还原的ru(ii),从而增大ru(nh3)63+的电化学还原电流,导致ru(iii)的再循环和产生放大的电催化电流,实现信号的双放大,因此本发明可以实现对5-羟甲基胞嘧啶的高灵敏度检测。本发明检测限9.06fm,该生物传感器的灵敏度比基于dna甲基转移酶修饰的电化学分析(0.23nm)提高了4个数量级,比基于β-葡萄糖基转移酶修饰的荧光分析(0.167nm)高4个数量级,比基于特异性抗体的光学传感器(0.42pm)高46倍,比基于kruo4的电致化学发光传感器(0.14pm)高25倍。
(4)特异性好:本发明利用5-羟甲基胞嘧啶修饰的化学反应不能在任何其他未羟甲基化的核酸碱基处发生,实现在dna中5-羟甲基胞嘧啶位点进行生物素的一步掺入,而胞嘧啶(c)和5-甲基胞嘧啶在相同反应条件下,不能发生反应,因此本发明方法可以高特异性地检测5-羟甲基胞嘧啶。
附图说明
构成本发明的一部分的说明书附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。
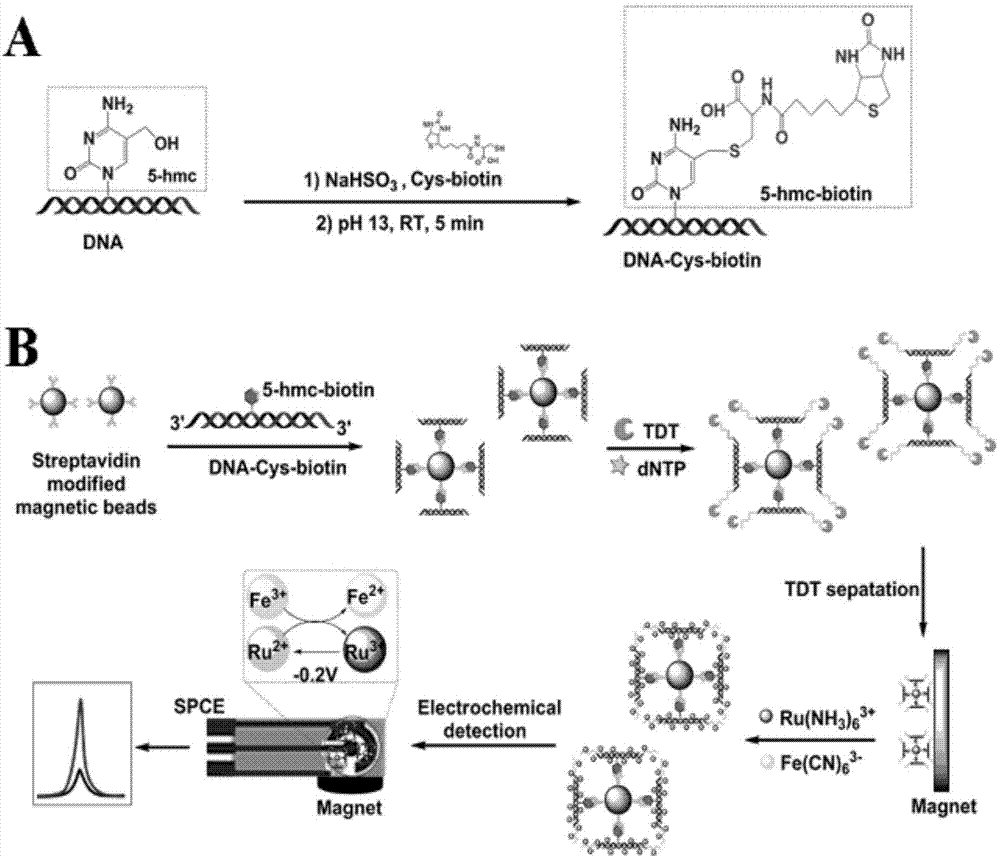
图1.5-羟甲基胞嘧啶测定的非标记、非固定化的电化学磁性生物传感器的示意图。该测定涉及两个连续步骤:(a)一步亚硫酸氢盐法介导的dna中5-羟甲基胞嘧啶位点的生物素化;(b)生物素化的5-羟甲基胞嘧啶dna诱导的末端转移酶催化聚合和随后的ru(iii)氧化还原循环双信号放大策略。
图2.(a)磁珠(a)/丝网印刷碳电极的电化学阻抗谱(eis)的奈奎斯特图,生物素化的5-羟甲基胞嘧啶dna/磁珠/丝网印刷碳电极在添加末端转移酶辅助碱基延伸之前(b)和之后(c)的电化学阻抗谱(eis)的奈奎斯特图,其中阻抗液为含有0.1mkcl的5mmfe(cn)63-/4-溶液。(b)磁珠(a)的zeta电位,生物素化的5-羟甲基胞嘧啶dna/磁珠在添加末端转移酶辅助碱基延伸之前(b)和之后(c)的zeta电位。(c)磁珠/丝网印刷碳电极(a),生物素化的5-羟甲基胞嘧啶dna/mb/spce在添加末端转移酶辅助碱基延伸之前(b)和之后(c)在ru(nh3)63+和fe(cn)63-的混合物中的dpv信号响应。(d)生物素化的5-羟甲基胞嘧啶dna/磁珠/丝网印刷碳电极和末端脱氧核苷酸转移酶(tdt)辅助的碱基延伸在仅存在(a)ru(nh3)63+,(b)ru(nh3)63+和fe(cn)63-中的dpv信号。
图3.(a)电化学磁性生物传感器对不同浓度的5-羟甲基胞嘧啶dna(从a到k,0、0.01、0.1、0.5、1、5、10、50、100、500和1000pm)的dpv响应。(b)dpv峰值增强电流(δi)与5-hmc浓度(在0.01至1000pm的范围内)的对数之间的线性关系。误差棒表示三次重复测量的标准偏差。
图4.(a)在条件1下,5-羟甲基胞嘧啶转化为5-羟甲基胞嘧啶-生物素,并在条件2下用micro-bio-spinp6纯化;然而,胞嘧啶(c)和5-甲基胞嘧啶在条件1下是不发生反应的。(b)仅用反应缓冲液的对照组、正常dna的胞嘧啶(c)、5-甲基胞嘧啶和5-羟甲基胞嘧啶dna的电化学磁性生物传感器的dpv曲线。(c)正常dna的胞嘧啶(c)、5-甲基胞嘧啶和5-羟甲基胞嘧啶dna的电化学磁性生物传感器的dpv信号响应。误差棒代表三次独立实验的标准偏差。
图5.人宫颈癌细胞系(hela细胞)和人胚胎肾细胞系(hek293t细胞)中的5-羟甲基胞嘧啶含量。
具体实施方式
应该指出,以下详细说明都是示例性的,旨在对本发明提供进一步的说明。除非另有指明,本文使用的所有技术和科学术语具有与本发明所属技术领域的普通技术人员通常理解的相同含义。
需要注意的是,这里所使用的术语仅是为了描述具体实施方式,而非意图限制根据本发明的示例性实施方式。如在这里所使用的,除非上下文另外明确指出,否则单数形式也意图包括复数形式,此外,还应当理解的是,当在本说明书中使用术语“包含”和/或“包括”时,其指明存在特征、步骤、操作和/或它们的组合。
为了使得本领域技术人员能够更加清楚地了解本发明的技术方案,以下将结合具体的实施例详细说明本发明的技术方案。
本发明实验原理,如图1所示。含5-羟甲基胞嘧啶单链dna与互补的dna的杂交形成双链dna,随后引入生物素-半胱氨酸衍生物使得能够将生物素一步掺入到含有5-羟甲基胞嘧啶位点的双链dna。在使用micro-bio-spinp6柱除去过量的半胱氨酸-生物素和盐后,利用具有链霉亲和素包被的磁珠通过生物素-链霉亲和素的特异性相互作用来富集生物素化的双链dna。随后,dna的3'-羟基末端可以通过末端转移酶催化重复添加dntps延伸,而不需要任何dna模板,产生更长的dna序列。在该电催化体系中,ru(nh3)63+作为一次电子受体发挥作用,fe(cn)63-作为二次电子受体发挥作用。ru(nh3)63+可以静电吸引到磁珠表面上dna的带负电荷的磷酸骨架上,并借助于磁场固定在丝网印刷碳电极电极上。过量的fe(cn)63-可以通过氧化电化学被还原的ru(ii),从而增大ru(nh3)63+的电化学还原电流,导致ru(iii)的再循环和产生放大的电催化电流。电催化循环遵循由等式(1)和(2)描述的基于电子转移动力学的机制。
ru(nh3)63++e-→ru(nh3)62+(1)
ru(nh3)62++fe(cn)63-→ru(nh3)63++fe(cn)64-(2)
生物素化的5-羟甲基胞嘧啶dna与链霉亲和素标记的磁珠结合后置于丝网印刷碳电极上,该ru(nh3)63+/fe(cn)63-体系可以产生增强的电催化信号。此外,fe(cn)63-带负电,受dna阴离子排斥远离电极表面,消除了它们对假阳性信号的直接反应。由于5-羟甲基胞嘧啶诱导的具有特异性的一步亚硫酸氢盐转化方法和末端转移酶催化的聚合反应与ru(iii)氧化还原循环介导的扩增的高效双信号放大,这种生物传感器能够简单,快速,高灵敏和选择性地检测5-羟甲基胞嘧啶。
本发明所用有关dna序列,如下表1所示。
表1相关dna序列
实施例
所述定量分析方法为:
细胞内总dna的提取:人宫颈癌细胞系(hela细胞)和人胚胎肾细胞系(hek293t)细胞的培养基为含有10%胎牛血清(fbs)和1%青霉素-链霉素的达尔伯克改良伊格尔培养基(dmem),放在37℃、含有5%二氧化碳的培养箱中进行培养。待细胞生长到对数生长期时,使用培养细胞dna提取试剂盒(epigentek)对细胞中的总dna进行抽提与纯化,提取与纯化操作严格按照试剂盒所附的说明书进行,所得总dna使用紫外可见分光光度计测定其浓度。
一步亚硫酸氢盐法介导的dna中5-羟甲基胞嘧啶位点的生物素化:用半胱氨酸-生物素在dna中进行一步亚硫酸氢盐介导的5-羟甲基胞嘧啶生物素化。将半胱氨酸-生物素(120μl,10μm,用10m氢氧化钠调节ph至5.0)和10μl具有不同浓度的双链dna(5-羟甲基胞嘧啶-互补dna)在200μl的离心管中混合。将na2s2o5(5μl,1.0m,ph=5.0)加入到溶液中,然后在42℃下孵育48小时。待溶液冷却至室温,用10m氢氧化钠调节ph至13。在室温下反应5分钟后,将样品通过micro-bio-spinp6柱(biorad)三次以除去过量的半胱氨酸-生物素和盐。
连接5-羟甲基胞嘧啶dna的磁珠的制备:将4μl链霉亲和素包被的磁珠悬浮液转移至上述200μl的离心管中,并用50μl洗涤缓冲液(0.5mnacl,20mmtris-hcl(ph7.4),1mmedta)洗涤两次。使用磁性分离架除去上清液以分离磁珠。在50μl含有1×末端转移酶缓冲液(10mmmg(ac)2,20mmtris-ac,50mmkac,ph=7.9),0.25mmcocl2,1mmdntps,6u末端转移酶的反应体系中进行酶扩增,然后再次用洗涤缓冲液洗涤以形成传感器阵列。
电化学测量:将含有1mmpbs(ph7.4),0.1mnacl,27μmru(nh3)63+和2mmfe(cn)63-的溶液加入到含有分离的生物素化的5-羟甲基胞嘧啶dna/磁珠的离心管中。然后将100μl上述溶液转移到丝网印刷碳电极的表面上。通过在工作电极表面下方施加超级磁体,将生物素化的5-羟甲基胞嘧啶dna/磁珠复合物固定在丝网印刷碳电极上。利用0至-500mv,脉冲幅度为50mv,脉冲宽度为50ms的差分脉冲伏安法(dpv)(参比电极为ag/agcl),来记录电化学响应。
为了验证该方法的可行性,电化学磁性生物传感器的制备通过(图2)的电化学阻抗谱(eis)和zeta电位来表征。电子转移电阻(ret)由[fe(cn)6]3-/4-在修饰的丝网印刷碳电极上的电子转移动力学控制,并且可以通过奈奎斯特图的半圆直径来表征。如图2a所示,非固定丝网印刷碳电极的磁珠的电子转移电阻(ret)为5980ω(图2a,曲线a)。相反,由于负电荷dna和[fe(cn)6]3-/4-之间的静电排斥作用,生物素化的5-羟甲基胞嘧啶dna/磁珠表现出较大的电子转移电阻(ret),为7120ω(图2a,曲线b),表明在磁珠上成功修饰5-羟甲基胞嘧啶dna。将生物素化的5-羟甲基胞嘧啶dna与末端转移酶孵育后,电子转移电阻(ret)增加至9980ω。这可以通过以下事实来解释:在末端转移酶催化聚合后,生物素化的5-羟甲基胞嘧啶dna更带负电荷的磷酸主链可能阻碍[fe(cn)6]3-/4-从溶液到电极表面的电子转移(图2a,曲线c)。
zeta电位用于研究生物素化的5-羟甲基胞嘧啶在磁珠上的连接。如图2b所示,与仅有磁珠的对照组(图2b,曲线a,-2.3±0.5mv)相比,添加生物素化的5-羟甲基胞嘧啶dna(图2b,曲线b,-4.5±0.2mv)诱导zeta电位发生显着变化,表明生物素化的5-羟甲基胞嘧啶dna成功涂覆在磁珠表面上。当5-羟甲基胞嘧啶dna与末端转移酶一起孵育时,由于生物素化的5-羟甲基胞嘧啶诱导的末端转移酶催化聚合,则观察到更高的负zeta电位(-10.2±0.4mv)(图2b,曲线c)。
在ru(nh3)63+和fe(cn)63-的混合物中,在末端转移酶辅助碱基延伸之前和之后,使用包括磁珠/丝网印刷碳电极,生物素化的5-羟甲基胞嘧啶dna/磁珠/丝网印刷碳电极的不同电极记录dpv测量值(图2c)。在dna中没有5-羟甲基胞嘧啶位点的对照组中,电流很小(5.59μa)(图2c,曲线a)。当dna中5-羟甲基胞嘧啶位点生物素化后,信号增加至7.85μa(图2c,曲线b),因为在生物素化的5-羟甲基胞嘧啶dna的带负电的磷酸骨架上吸收了大量的ru(nh3)63+。将生物素化的5-羟甲基胞嘧啶dna/磁珠与末端转移酶孵育后,信号进一步增加至11.5μa(图2c,曲线c),因为更多的ru(nh3)63+静电结合到延长的带负电荷的磷酸骨架上。这些结果证明了该生物传感器对5-羟甲基胞嘧啶检测的可行性。
在最佳实验条件下,本发明评估了磁电化学生物传感器响应不同浓度的5-羟甲基胞嘧啶dna的分析性能。如图3a所示,随着5-hmcdna浓度从0.01到1000pm的增加,dpv信号增强。电流与5-羟甲基胞嘧啶dna浓度的对数在0.01至1000pm范围内获得线性关系(图3b),检测限度计算为9.06fm。该生物传感器的灵敏度比基于dna甲基转移酶修饰的电化学分析(0.23nm)提高了4个数量级,比基于β-葡萄糖基转移酶修饰的荧光分析(0.167nm)高4个数量级,比基于特异性抗体的光学传感器(0.42pm)高46倍,比基于kruo4的电致成化学发光法(0.14pm)的5-羟甲基胞嘧啶选择性化学氧化高25倍,这足以说明本发明的检测灵敏度之高。
为了研究这种生物传感器的特异性,使用具有单5-甲基胞嘧啶位点的5-甲基胞嘧啶和正常dna胞嘧啶(c)作为阴性对照。如图4c所示,在相同的条件下,只有在5-羟甲基胞嘧啶存在的情况下才能检测到较高的峰值电流变化。5-羟甲基胞嘧啶的峰值电流变化(δi)比正常dna胞嘧啶(c)和5-甲基胞嘧啶dna高22及39倍(图4c),表明该生物传感器具有高特异性。本方法的高特异性可归因于5-羟甲基胞嘧啶修饰的化学反应不能在任何其他未羟甲基化的核酸碱基处发生。
为了评估本发明提出的生物传感器在临床诊断中的可行性,使用该生物传感器测量两种不同的癌细胞系,包括。通过q-5000ultramicrouv-vis分光光度计(quawell,usa)测量基因组dna的浓度。如图5所示,人宫颈癌细胞系(hela细胞)和人胚胎肾细胞系(hek293t细胞)中的5-羟甲基胞嘧啶含量分别被确定为总核苷酸的0.00793%和0.00977%,与先前报道的通过基于β-葡萄糖基转移酶修饰的斑点印迹法测定的结果一致(分别为总核苷酸的0.007%和0.009%)。
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
sequencelisting
<110>山东师范大学
<120>一种基于非标记、非固定化的电化学磁性生物传感器检测5-羟甲基胞嘧啶的方法
<130>
<160>4
<170>patentinversion3.3
<210>1
<211>42
<212>dna
<213>人工合成
<400>1
ggtaccatcgatacthmcagatagactacactccagaagctt42
<210>2
<211>41
<212>dna
<213>人工合成
<400>2
ggtaccatcgatactmcagatagactacactccagaagctt41
<210>3
<211>40
<212>dna
<213>人工合成
<400>3
ggtaccatcgatactcagatagactacactccagaagctt40
<210>4
<211>40
<212>dna
<213>人工合成
<400>4
aagcttctggagtgtagtctatctgagtatcgatggtacc40
- 还没有人留言评论。精彩留言会获得点赞!