紫外-可见分光光度法测定食用菌中锌离子含量的方法与流程
本发明属于分析检测领域,具体涉及一种成本低、操作简单、且重复性好,准确性高的紫外-可见分光光度法测定食用菌中锌离子含量的方法。
背景技术:
食用菌是真菌中能形成大型子实体,而且能够提供人们食用或药用的菌类的总称。中国已知的食用菌有350多种,它们分布广泛,品种繁多,营养丰富。食用菌对金属有很强的富集能力,含有丰富的矿质元素、维生素、各种氨基酸及微量元素,如锌、铁、硒等,具有很高的营养价值。而锌是人体必需的微量元素之一,它参与体内多种酶的合成,有“生命之花”、“婚姻和谐素”和“智能之源”的美誉。锌在生物体生长发育、生殖遗传、免疫、内分泌等重要生理过程中起着极其重要的作用。体内缺乏锌元素时,可导致侏儒症、损伤组织愈合困难、生长发育不良、味觉迟钝、食欲减退、性发育异常、免疫功能下降、皮肤病以及心血管疾病等多种疾病。人体缺乏锌对身体不好,但是也不能摄取过多,适量就好。补锌过量的症状有多动症、免疫力功能减退、呕吐、头痛、腹泻、抽搐、贫血、血脂代谢混乱、神经元损伤、记忆力下降等。
当前食用菌中金属元素的检测方法一般有紫外-可见分光光度法、原子吸收光谱法、原子荧光光度法、电子耦合等离子体原子发射光谱法、电子耦合等离子体质谱法、高效液相色谱法、生物分析法、二硫腙比色法等。其中,紫外-可见分光光度法可以作定性定量分析、纯度分析、结构分析,特别在定性定量分析和纯度检测方面,在许多领域更是必备的分析方法。紫外-可见分光光度法是根据物质分子对波长为200~760nm这一范围的电磁波的吸收特性所建立起来的一种定性、定量和结构分析方法。它的优点是找到对的吸收波长时可快速侦测;灵敏度和准确度高仪器结构简单、操作简便、性价比高。但紫外-可见分光光度法的缺点是浓度不能太高,有同吸收峰的物质干扰,且当样品含悬浮物质较多少时,紫外分光对其产生较大偏差。
技术实现要素:
本发明旨在解决上述问题,而提供一种成本低、操作简单、且重复性好,准确性高的紫外-可见分光光度法测定食用菌中锌离子含量的方法。
本发明紫外-可见分光光度法测定食用菌中锌离子含量的方法,该方法包括如下步骤:将待测样品加入浓硝酸中,经过静置,消解后,将样品加入到包含醋酸-醋酸钠缓冲溶液、铬黑t溶液及锌标准工作溶液中,经反应后,通过紫外可见分光光度法测定锌离子的含量。
所述醋酸-醋酸钠缓冲溶液的ph值为5.6,醋酸-醋酸钠缓冲溶液的浓度为20%(v/v)。
所述铬黑t溶液的浓度为6%(v/v)。
所述反应时间为25分钟。
所述各溶液的加入顺序为:锌标准工作溶液、铬黑t溶液、醋酸-醋酸钠缓冲溶液。
所述紫外-可见分光光度法的吸收波长为538nm。
所述静置时间为12小时。
所述消解温度为105℃,消解时间为30min。
所述锌标准工作液的溶度为6%(v/v)。
优选地,本发明的紫外-可见分光光度法测定食用菌中锌离子含量的方法包括如下步骤:将0.5g待测样品溶液加入5ml浓硝酸,静置12h,将溶液移至消解管中于105℃下消解30min,冷却后,取5ml样品,依次加入1.5ml锌标准工作液、1.5ml铬黑t溶液、2.5mlph值为5.6的醋酸-醋酸钠缓冲溶液,定容至25ml,测定所得溶液在波长为538nm处的吸光度,通过作出的标准工作曲线,横坐标是锌离子浓度,纵坐标是吸光度值,根据吸光度值来确定锌离子浓度。
本发明的有益效果为:本发明紫外-可见分光光度法测定食用菌中锌离子含量的方法通过二价锌离子在酸性条件下与铬黑t溶液生成紫色的配合物。本发明的锌离子的检出限是0.0254μg/ml,标准偏差为0.00308,测定食用菌中锌离子含量,所得的回收率在95.54%~102.54%。本发明具有成本较低,操作简单,具有良好的重复性和准确性。
【附图说明】
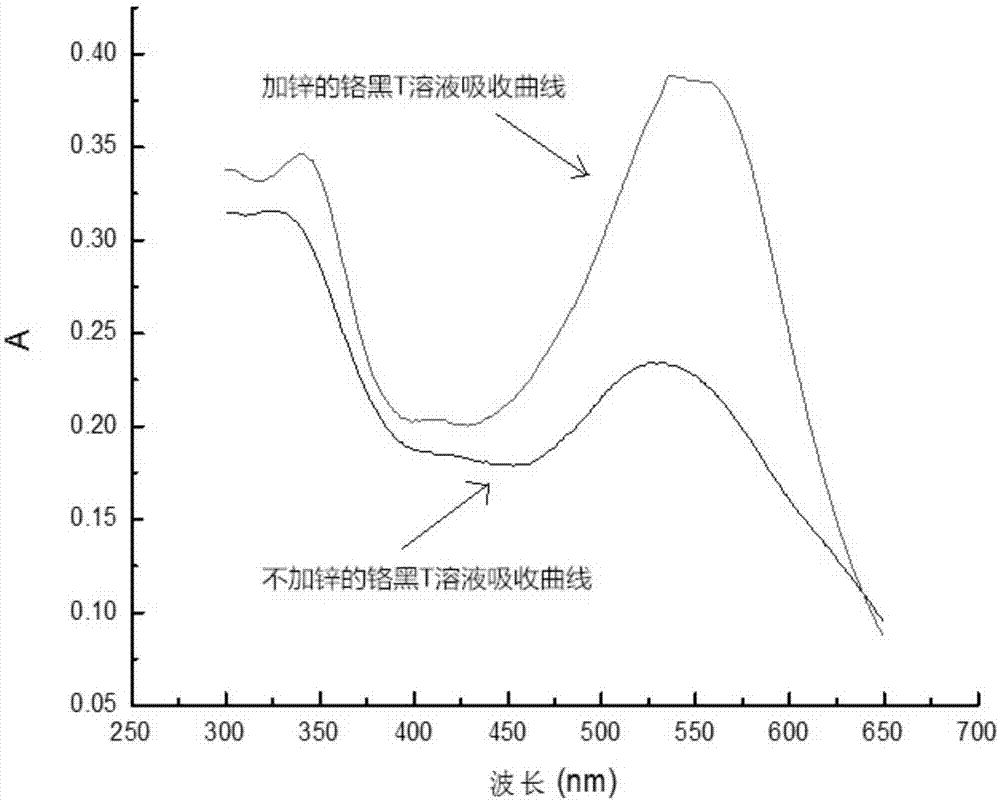
图1是铬黑t溶液的吸收曲线。
图2是ph值对溶液吸光度值的影响。
图3是缓冲溶液用量对溶液吸光度值的影响。
图4是铬黑t用量对溶液吸光度值的影响。
图5是反应时间对溶液吸光度值的影响。
图6是标准工作曲线。
【具体实施方式】
下面结合具体实施例对本发明做进一步详细的描述,对本发明不构成任何限制。
1、仪器、试剂
(1)仪器:ar224cn分析天平(奥豪斯仪器有限公司),evolueion300紫外可见分光光度计(赛默飞世尔科技美国热电公司),phs-3c酸度计(上海仪电科学仪器股份有限公司),wx-8000消解仪(上海屹尧仪器科技发展有限公司)
(2)试剂:七水硫酸锌(分析纯ar,天津市福晨化学试剂厂),铬黑t(成都市科龙化工试剂厂),冰乙酸(分析纯ar成都市科龙化工试剂厂),无水醋酸钠(萨恩化学技术试剂厂)。
2、试验方法和结果
试验方法:
(1)新标准工作溶液的配制:用分析天平准确称取0.4397gznso4·7h2o加水溶解后,移入100ml容量瓶中定容,配成溶液,即为1.0g/l锌标准储备溶液。再移取1ml锌标准储备溶液于100ml容量瓶中,用水稀释至刻度,摇匀,即得10μg/ml锌标准工作溶液。
(2)铬黑t溶液的配制:秤取0.2307g铬黑t(eriochromeblackt:c20h12n3nao7s),用无水乙醇溶解并移入500ml容量瓶中,加无水乙醇稀释至刻度,摇匀,即得1×10-3mol/l铬黑t溶液。
(3)醋酸-醋酸钠缓冲溶液的配制:取醋酸原液11.8ml,加水定容至1000ml,配成溶液a;称取16.28g无水醋酸钠加水溶解,移入1000ml容量瓶中,定容至刻度,为溶液b;最后分别取4.8mla溶液和45.2mlb溶液于同一100ml容量瓶中,再加水稀释至刻度,摇匀,即得ph=5.6醋酸-醋酸钠缓冲溶液。
(4)待测样品的处理:从超市购买新鲜的茶树菇、金针菇、香菇、海鲜菇及蟹味菇,取其可食用部分,洗净,烘干,粉碎。
锌标准溶液的测定方法
将0.5g待测样品溶液加入5ml浓硝酸,静置12h,将溶液移至消解管中于105℃下消解30min,冷却后,取5ml样品,依次加入1.5ml锌标准工作液、1.5ml铬黑t溶液、2.5mlph值为5.6的醋酸-醋酸钠缓冲溶液,定容至25ml,将所得溶液利用紫外-可见分光光度计进行吸收曲线或吸光度的测定。
以此方法为基础,确定铬黑t最大吸收波长,并研究ph值、缓冲液用量、铬黑t用量、反应时间及试剂加入顺序等因素对吸收波长的影响,得出紫外-可见分光光度法测定锌离子的最优条件。
结果与讨论:
(1)铬黑t最大吸收波长的确定
在温度为25℃,反应时间为25min、醋酸-醋酸钠缓冲溶液ph值为5.6用量2.5ml、显色剂为1.5ml的铬黑t溶液的条件下,加入不同体积的锌标准工作溶液。扫300~650nm波长范围内溶液的吸光度值。以不加标的铬黑t溶液作试剂空白测定,测试结果如图1所示。
从图1中可以看出,在300~650nm范围内,波长的总体变化是先减后增,达到最大值后再降下来。不加锌的铬黑t溶液的最大吸光度值在524nm处,它的吸光度值是0.234;加标后的铬黑t溶液最大峰值出现在538nm处,它的吸光度值是0.384。综合上述分析,选择538nm作为测定波长。
(2)ph值对吸收波长的影响
取12支比色试管,分别依次加入5ml10μg/ml的锌标准工作溶液、1.5ml10-3mol/l的ebt溶液,在12支试管中分别加入ph为3.6~5.8的缓冲溶液2.5ml,分别定容至刻度线,室温下放置25min,在538nm处测定。测试结果如表1及图2所示。
表1醋酸-醋酸钠缓冲溶液(0.2mol/l)
从表1及图2可知,在ph为3.6~5.8的缓冲溶液体系中,当ph值增大的时候,溶液的吸光度值总体趋势是增大的。当ph=4.4时,吸光度值出现第一个峰值,随后下降,在ph=5.0时又上升,ph=5.6时到达第二个峰值,也是最大峰值,综合上述分析最佳ph应为5.6。
(3)缓冲液用量对吸收波长的影响
当ph=5.6缓冲溶液用量分别为1.00ml、2.00ml、2.50ml、3.00ml、4.00ml、5.00ml、6.00ml,显色剂用量为1.5ml的铬黑t溶液,反应时间为25min的条件下,在538nm处测定缓冲溶液用量对吸光度值的影响,测试结果如图3所示。
从图3中可以看出,缓冲液的用量对食用菌中锌含量的测定有很大的影响。缓冲液用量从1.00ml到2.50ml时,吸光度值呈上升趋势,且在2.50ml达到最大值,所以选择缓冲液用量为2.50ml。
(4)铬黑t用量对吸收波长的影响
当铬黑t溶液的用量分别为0.50ml、1.00ml、1.50ml、2.00ml、2.50ml、3.00ml10-3mol/l,ph=5.6缓冲溶液用量为2.50ml,反应时间为25min的条件下,在538nm处测定显色剂溶液用量对吸光度值的影响,测试结果如图4所示。
从图4可知,显色剂的用量对食用菌中锌含量的测定有很大的影响。在加入0.50ml~1.50ml显色剂中,溶液曲线呈上升趋势,且在1.50ml处达到最大值,1.50ml以后吸光度值a趋于稳定,所以选择显色剂的加入量为1.50ml。
(5)反应时间对吸收波长的影响
当反应时间为0min、5min、10min、15min、20min、25min、30min、40min、60min、80min、100min、120min时,ph=5.6缓冲溶液用量为2.50ml,显色剂用量为1.5ml的铬黑t溶液的条件下,在538nm处测定反应时间对吸光度值的影响,测试结果见图5所示。
从图5中可以看出,反应时间对食用菌中锌含量的测定也有影响。在0~25min内,溶液曲线呈上升趋势,且在25min处达到最大值,25min以后吸光度值a趋于稳定,且配合物稳定性至少可以达到2h以上.所以选择反应时间为25min。
(6)试剂加入顺序对吸收波长的影响
试剂的加入顺序对食用菌中锌含量的测定也有影响,比较其对生成配合物吸光度值的影响,结果如下图表2所示。从表2可知,该实验方法与试剂加入有很大关系,按zn(ⅱ)→ebt溶液→缓冲溶液的顺序加入时的吸光度值最大。
表2试剂加入与吸光度值之间的关系
(7)正交试验
正交实验依据按zn(ⅱ)→ebt溶液→缓冲溶液的顺序加入,选取酸度的影响、缓冲液用量的影响、显色剂用量的影响和反应时间作为正交因子,作的四因素三水平九组正交试验,得到结果如表3所示。9个实验中,第5个实验中得到的数据最高,即当ph=5.6时的醋酸-醋酸钠缓冲溶液为2.5ml,ebt显色剂为2.00ml,反应时间为30min时,吸光度值为0.473。从极差值中可以看出各因素作用的主次,即酸度的影响>显色剂用量的影响>缓冲液用量的影响>反应时间,说明在考察范围内,当ph=5.6时的醋酸-醋酸钠缓冲溶液与显色剂反应生成的紫罗兰色配合物对其吸光度值的影响最大,其次是显色剂用量及缓冲液用量,而反应时间的影响最小。
表3四因素三水平九组正交实验结果
从表3中的数据得出测定吸光度的最佳因素组合为a2b2c3d3时,在正交试验中效果最好。再用a2b2c3d3方案做三次验证性试验,得到的吸光度值分别为0.475、0.473、0.475,平均值为0.474,比较稳定。所以a2b2c3d3的确是最佳方案。
通过上述内容得出紫外分光光度法测定食用菌中锌离子含量的最佳方法为:将0.5g待测样品溶液加入5ml浓硝酸,静置12h,将溶液移至消解管中于105℃下消解30min,冷却后,取5ml样品,依次加入1.5ml锌标准工作液、1.5ml铬黑t溶液、2.5mlph值为5.6的醋酸-醋酸钠缓冲溶液,定容至25ml,测定所得溶液在波长为538nm处的吸光度,通过作出的标准工作曲线,横坐标是锌离子浓度,纵坐标是吸光度值,根据吸光度值来确定锌离子浓度。
进一步研究该方法的分析性能,取锌标准工作液为0.00ml、1.00ml、2.00ml、3.00ml、4.00ml、5.00ml时,ph=5.6缓冲溶液用量为2.50ml,显色剂用量为1.5ml的铬黑t溶液,反应时间为25min的条件下,在538nm处测定标准工作曲线的吸光度值,测试结果如图6所示。
从图6可知,锌标准工作液浓度在0~2.0μg/ml范围内与吸光度值a呈良好的线性关系。本实验线性方程为a=0.1258c+0.25867,相关系数r2=0.99804,以不加锌的ebt溶液作空白对照测定,计算出它的标准偏差为0.00308,得到检出限为0.0254μg/ml。
(8)样品中锌含量的检测
食用菌中锌含量的检测
新鲜的茶树菇、金针菇、香菇、海鲜菇、蟹味菇购于某超市。取可食用部分,洗净,烘干,粉碎,备用。
称取各固体试样0.5g(精确到0.0001g)于50ml小烧杯中,加入5ml浓硝酸,静置12h。将烧杯中的液体移入消解管中,在消解仪器中以105℃消解30min。冷却后,移取样液5ml至体积为25ml的比色管中,依次加入1.5ml的锌标准工作液(10μg/ml),1.5ml的ebt溶液、2.5mlph=5.6的醋酸-醋酸钠缓冲溶液,定容,摇匀后静置25min,在波长538nm处测定溶液的吸光度值,结果见表4所示。依据标准曲线线性方程a=0.1258c+0.25867,计算得出a=0.157进行加标回收试验,回收率计算公式=(加标试样-原含量)/加标量,回收率在95.54%~102.54%。因此,可用紫外分光光度法测定食用菌中锌离子含量。
表4回收率试验
本发明以铬黑t为显色剂,通过紫外可见分光光度法测定食用菌中锌离子含量。并讨论了ph值、缓冲液用量、铬黑t用量、反应时间及试剂加入顺序等因素对吸收波长的影响,得出最优的紫外可见分光光度法测定食用菌中锌离子含量的方法。在该方法条件下,锌离子的检出限是0.0254μg/ml,标准偏差为0.00308,测定食用菌中锌离子含量,所得的回收率在95.54%~102.54%。
上述实施例只为说明本发明的技术构思及特点,其目的在于让熟悉此项技术的人士能够了解本发明的内容并据以实施,并不能以此限制本发明的保护范围。凡根据本发明精神实质所作的等效变化或修饰,都应涵盖在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!