一种具有多孔膜片的丝网印刷电极的制作方法
本实用新型涉及电化学检测领域,具体地涉及一种具有多孔膜片的丝网印刷电极。
背景技术:
下面的背景技术用于帮助读者理解本实用新型,而不能被认为是现有技术。
以电化学生物传感器为原理的丝网印刷电极在即时检测(POCT)领域应用广泛。生理液体,如血液、尿液、汗液、唾液中含有很多临床实验室感兴趣的检测参数。例如血液中的葡萄糖、胆固醇、糖化血红蛋白、血酮,尿液中的尿酸,汗液中的乳酸等。电极的检测原理大多是将目标分析物所对应的酶修饰到工作电极上,通过检测目标分析物的酶促反应电流实现对目标分析物的快速定量分析。当酶促反应电流信号仅依赖目标分析物的浓度时,能够对目标分析物进行精确的定量分析。但是,在实际检测中,生物体液中存在的其他氧化还原活性物质也会参与电流信号的发生过程,对检测结果造成正干扰或负干扰。因此,为了提高电极的检测精度,提高电极的抗干扰性是关键。
中国专利CN102507670B在工作电极上设置一层抗干扰的试剂层,检测时、待测样品先透过试剂层,试剂层中的抗坏血酸氧化酶与血液中的抗坏血酸反应,以排除抗坏血酸对尿酸信号的干扰。但是这种方法的缺点在于:1、能够排除的干扰物质种类有限,一层试剂层只能用于排除一种干扰物质;2、即使为了排除多种干扰物质、在工作电极上设置多层不同种类的试剂层,一方面试剂层之间的相互干涉、酶层厚度过大均会对酶活性有所影响,酶活性变低会造成干扰物质排除不全,另一方面,待测样品需要透过多层试剂层才能到达底层、使目标分析物产生电信号,一定程度上造成测试时间的延长。另外,大分子物质对样品检测精度的影响也不容忽视,例如在对血液中的物质进行定量分析时、血细胞对检测精度的影响,因此测试中还需要排除大分子物质(如血细胞)对测试的影响。
技术实现要素:
本实用新型的目的在于提供一种能够排除多种干扰物影响、提高检测效率的具有多孔膜片的丝网印刷电极。
一种具有多孔膜片的丝网印刷电极,包括绝缘基板和电极,绝缘基板上设有用于将待测样品导流至电极的导流槽,导流槽具有吸样端口,其特征在于:导流槽内排列有多个微球。多个微球通过物理过滤的方式排除干扰物质。
进一步地,微球由聚苯乙烯或二氧化硅制成。
进一步地,微球的粒径为1~500μm。
进一步地,微球是实心结构或者是多孔结构。
进一步地,电极包括工作电极,微球位于吸样端口至工作电极之间。
生物化学试剂
生物化学试剂能够与干扰物质发生反应,从而将干扰物质从待测样品中去除。
进一步地,微球表面修饰有生物化学试剂,生物化学试剂是与干扰物质对应的酶。优选的,修饰生物化学试剂的方法是吸附、交联、共价结合。
进一步地,所述生物化学试剂是葡萄糖氧化酶、抗坏血酸氧化酶、变旋酶、葡萄糖脱氢酶、乳酸氧化酶、尿酸氧化酶、胆固醇脂酶、胆固醇氧化酶、磷脂酶、氨基酸酶、辣根过氧化物酶、β-羟丁酸脱氢酶等酶中的任一种或几种。
进一步地,每个微球具有一种生物化学试剂,所有微球的生物化学试剂有两种或多种;或者,每个微球具有两种或多种生物化学试剂,所有的微球具有相同的生物化学试剂。
过滤区
过滤区是导流槽内、微球所在的区域。
进一步地,导流槽内设有多个过滤区,过滤区避开电极设置,所有微球均位于过滤区内。优选的,每个过滤区内的微球数量相等,或者,过滤区内的微球数量沿待测样品导流的方向递减。相邻两个过滤区内的微球数量之差可以是10、 20、30、50……每个过滤区可以是直线形或曲线形。
优选的,过滤区为直线形,过滤区的轴线与导流槽中线垂直。
进一步地,过滤区的两端分别与导流槽的两侧壁连接,多个过滤区间隔设置;或者,过滤区的一端与导流槽的侧壁连接、过滤区的另一端是自由端,相邻两过滤区交错分布。优选的,过滤区自由端与相邻两过滤区自由端齐平,或者,过滤区自由端位于相邻两过滤区之间。
优选的,当过滤区具有自由端时,多个过滤区间隔设置。
进一步地,多个过滤区等间距排列;或者,相邻两过滤区之间的距离沿待测样品导流的方向递减。
进一步地,多个过滤区的微球数量相等,或者,多个过滤区的微球数量沿待测样品导流的方向递减。
微球排列
待测样品通过过滤区的速度、待测样品中干扰物质的排除率等很大程度上取决于微球的粒径和排列方式。
进一步地,过滤区由微球区和空留区组成,空留区位于微球区之上,微球区内填满微球。
进一步地,微球有多层,微球的粒径为定值;或者,每层微球具有相同的粒径,上一层微球的粒径小于下一层微球的粒径。上一层微球的粒径小于下一层微球的粒径,也就是说,微球以“上小下大”方式堆垛。
多孔膜片
进一步的,过滤区包括多孔膜片,多孔膜片与导流槽侧壁围成用于容纳微球的过滤区。优选的,多孔膜片上的孔尺寸小于微球的粒径。
进一步的,多孔膜片的两端分别与导流槽两侧壁密封连接,相邻两多孔膜片与导流槽两侧壁围成过滤区。
进一步地,多孔膜片为平板状或曲板状。
进一步地,所有多孔膜片之间平行。
进一步地,多个过滤区之间等间距排列。
进一步地,多孔膜片由Nafion或醋酸纤维素制成。
本实用新型的有益效果:
1、导流槽内具有多个微球,多个微球之间的间隙和微球与导流槽侧壁之间的空隙能够对干扰物质,如血液中的血细胞,进行物理过滤。
2、微球表面修饰有能够与抗干扰物质发生反应、从而消除抗干扰物质的生物化学试剂,对抗干扰物质进行化学过滤;微球具有较大的比表面积能够修饰较多的生物化学试剂;微球表面的生物化学试剂可以有多种,并且多种生物化学试剂之间不会相互干涉,从而能够同时对多种干扰物质进行消除。
3、导流槽内设置多个相互间隔的过滤区,微球均位于过滤区内,防止微球排列过于紧密、造成堵塞,从而提高检测效率;另外,过滤区的多孔膜片能够对待测样品进行第二次物理过滤,还能阻隔微球与电极,同时防止微球被待测样品冲出过滤区。
4、过滤区中的微球采用“上小下大”的堆垛方式能够提高干扰物质的去除效果和检测效率。
附图说明
图1为本实用新型一个实施例的丝网印刷电极片的示意图,其中,图1a) 为平面图,图1b)为立体图。
图2a)为本实用新型一个实施例的过滤区的示意图,图2b)一个实施例的另一种过滤区的示意图。
图3a)为本实用新型一个实施例的微球堆垛的示意图,图3b)一个实施例的另一种微球堆垛的示意图。
图4a)为本实用新型一个实施例的微球堆垛的示意图,图4b)一个实施例的另一种微球堆垛的示意图。
图5a)为本实用新型一个实施例的过滤区的示意图,图5b)一个实施例的另一种过滤区的示意图。
图6为本实用新型一个实施例的多孔膜片示意图。
图7为本实用新型一个实施例的多孔膜片位置的示意图。
图8为本实用新型各实施例1~3测得的血液中尿酸含量和测试时间的曲线图 (血液中尿酸含量为300μmol·L-1)。
图9本实用新型各实施例1、实施例4和实施例5测得的血液中尿酸含量和测试时间的曲线图(血液中尿酸含量为300μmol·L-1)。
具体实施方式
下面结合具体实施例对本实用新型进行一步的详细说明。
实施例1
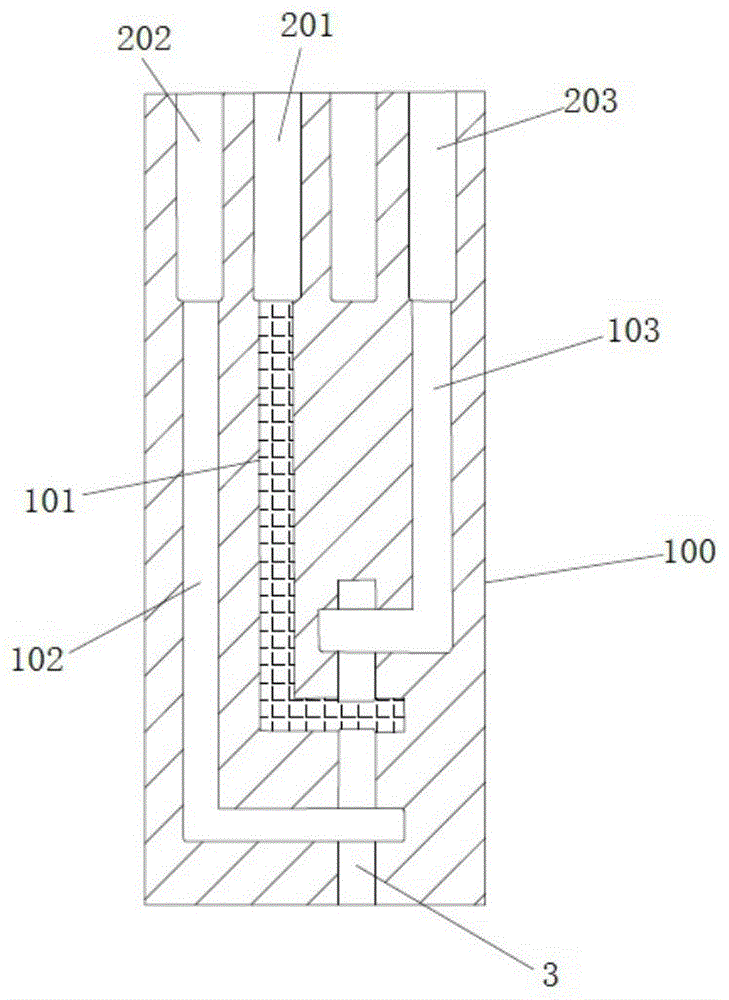
一种具有多孔膜片的丝网印刷电极,如图1a)和图1b)所示,包括绝缘基板100、工作电极101、参比电极102、辅助电极103和盖板4,工作电极101、参比电极102和辅助电极103均设于绝缘基板100上,绝缘基板100上设有用于将待测样品分别导流至工作电极101、参比电极102和辅助电极103的导流槽3。工作电极101一端与工作电极端子201连接、工作电极101的另一端与导流槽3 连接;参比电极102一端与参比电极端子202连接、参比电极102的另一端与导流槽3连接;辅助电极103一端与辅助电极端子203连接、辅助电极103的另一端与导流槽3连接。盖板盖在绝缘基板上,盖板由绝缘材料粘贴覆盖于亲水性薄膜而制成使导流槽形成毛细管。导流槽利用毛细作用将待测样品从吸样端口305 吸入电极试片进行检测。
导流槽3内排列有多个由聚苯乙烯制成的实心微球6。微球的粒径为定值。
在一些实施例中,微球由二氧化硅制成。
在一些实施例中,微球的粒径为1~500μm。
在一些实施例中,微球是多孔结构。多孔结构的微球相对实心结构具有更大的比表面积,从而每个微球能够修饰更多的生物化学试剂。
多个微球之间以及微球与导流槽之间形成间隙。只要待测样品中干扰物质的粒径大于微球之间的间隙、微球与导流槽之间的间隙,待测样品通过导流槽时,干扰物质就能够被微球排除在外。也就是说,导流槽中的多个微球通过物理过滤的方式,排除干扰物质。例如,当待测样品是血液时,多个微球之间的间隙小于血液中血细胞的粒径,即可对血细胞起过滤作用,防止血细胞随待测血液被导流至工作电极和辅助电极、影响检测结果。
微球位于吸样端口303至工作电极101之间。如图1b)所示,工作电极101 与吸样端口303之间的导流槽被参比电极102分为第一段301和第二段302,微球位于第一段301和第二段302。在一些实施例中,微球位于第一段。
生物化学试剂
微球表面修饰有生物化学试剂,生物化学试剂是与干扰物质对应的酶。在本实施例中,修饰生物化学试剂的方法是吸附。在一些实施例中,修饰生物化学试剂的方法可以是交联、共价结合。
举例来说,当丝网印刷电极试片用于检测血液中的尿酸含量时,在工作电极上修饰尿酸氧化酶、在导流槽内微球表面吸附上抗坏血酸氧化酶。当血液流经导流槽时、微球上的抗坏血酸氧化酶使血液中抗坏血酸被氧化破坏以此达到消除干扰的目的。另外,紧密排列的微球可以把血液中血细胞等大分子过滤掉。
另一个例子,普鲁士蓝(PB)对于H2O2的电还原具有高灵敏度,因而被称为“人工过氧化物酶”。但是PB选择性和特异性较差,能够催化血液中如尿酸、抗坏血酸等多种物质。当丝网印刷电极试片用于测试血液中胆固醇的含量时,在工作电极上修饰胆固醇氧化酶,在导流槽内每一个微球表面同时吸附上胆固醇酯酶、抗坏血酸氧化酶、尿酸酶。当血液流经导流槽时,微球上的胆固醇酯酶使血液中胆固醇酯被氧化为游离胆固醇来进行后续的催化,游离胆固醇与胆固醇氧化酶反应生成过氧化氢,普鲁士蓝催化过氧化氢生成媒介体,用来检测信号。微球上的抗坏血酸氧化酶和尿酸酶是来排除血液中的抗坏血酸和尿酸的干扰。另外,紧密排列的微球可以把血液中血细胞等大分子过滤掉。
在一些实施例中,生物化学试剂可以是葡萄糖氧化酶、抗坏血酸氧化酶、变旋酶、葡萄糖脱氢酶、乳酸氧化酶、尿酸氧化酶、胆固醇脂酶、胆固醇氧化酶、磷脂酶、氨基酸酶、辣根过氧化物酶、β-羟丁酸脱氢酶等酶中的任一种或几种。
在一些实施例中,每个微球具有一种生物化学试剂,所有微球的生物化学试剂有两种或多种;或者,每个微球具有两种或多种生物化学试剂,所有的微球具有相同的生物化学试剂。每个微球具有一种生物化学试剂每个微球具有两种或多种生物化学试剂,可以是每种生物化学试剂分别覆盖微球的不同表面,也就是说,微球表面的不同部分覆盖有不同种类的生物化学试剂。如此,微球可以用于排除多种干扰物质,而且不同种类的生物化学试剂之间不会相互干扰,也不会因为涂层太厚而影响酶的活性。
对于目标分析物而言,干扰最大的往往是存在于待测样品中、能够参与电流信号产生的物质。这些干扰物质使电极测得的电信号产生正偏差或负偏差。这些干扰物质尺寸可能小于目标分析物的尺寸,用物理过滤的方法会同时把目标分析物和干扰物同时去除。或者,虽然干扰物质尺寸大于目标分析物的尺寸,但是干扰物质的尺寸依然很小,用物理过滤的方式去除,需要形成的间隙尺寸很小,这样将极大地影响待测样品的导流。因此,这些物质往往难以用物理过滤的方法去除。因此,更可取的方式是,利用生物化学试剂与这些干扰物质发生化学反应,从而去除干扰物质。
过滤区
微球可以在导流槽内紧凑排列,也就是导流槽内充满微球,每个微球都与周围的微球紧密接触。但是,在这种情况下,微球之间形成的间隙太小、太密集,当待测样品通过导流槽时,血细胞容易堵塞微球之间的间隙,导致样品通过速度急剧减缓,影响检测效率。因此,在导流槽内设置过滤区。过滤区是导流槽内、微球所在的区域。
如图2a)所示,导流槽3内设有五个过滤区5,过滤区5避开电极设置,所有微球6均位于过滤区内。
每个过滤区5的两端分别与导流槽3的两侧壁连接,五个过滤区5之间相隔。每个过滤区内填满粒径为8μm的微球,如图5a)所示。盖板、过滤区和导流槽底部依次连接。每个过滤区内的微球数量相等。
多个过滤区平行。多个过滤区等间距排列。过滤区为直线形,过滤区关于导流槽的中线对称。
在一些实施例中,过滤区的微球数量沿待测样品导流的方向递减。待测样品导流的方向指的是待测样品从吸样端口至各电极的方向。随着待测样品经过的过滤区增加,待测样品中的干扰物质减少,所需的生物化学试剂的量减少,因而对应的微球的数量可以减少。相邻两个过滤区内的微球数量之差可以是10、20、 30、50……
在一些实施例中,相邻两过滤区之间的距离沿待测样品导流的方向递减。待测样品刚进入导流槽时,过滤区的分布更加密集,随着待测样品中的干扰物质减少,过滤区的分布密度减小,以加快导流速度。
在一些实施例中,如图2b)所示,每个过滤区5为曲线形。多个过滤区5 之间平行。曲线过滤区能够增加每个过滤区与待测样品的接触面积,从而使每个过滤区能够去除的干扰物质增加。
实施例2
本实施例除过滤区形状外,其余结构和组成均可以与实施例1相同。
如图3所示,过滤区5的一端与导流槽3的侧壁连接、过滤区5的另一端是自由端,相邻两过滤区5交错分布。交错分布指的是,一个过滤区的左端为连接端,与之相邻的两个过滤区的右端为连接端;或者一个过滤区的右端为连接端,与之相邻的两个过滤区的左端为连接端。五个过滤区5间隔设置。
如图3a)所示,过滤区5自由端与相邻两过滤区5自由端齐平。
在一些实施例中,如图3b)所示,过滤区自由端位于相邻两过滤区之间。
过滤区为直线形,过滤区的轴线与导线槽的中线垂直。
在一些实施例中,过滤区为曲线形。
所有的过滤区之间平行。在一些实施例中,与导流槽同一侧壁连接的多个过滤区之间平行,与不同侧壁连接的过滤区之间可以不平行。
多个过滤区5等间距排列。等间距排列指的是,与导流槽同一侧壁连接的多个过滤区连接端等间距排列。
实施例3
本实施例除微球堆垛方式不同外,其余结构和组成均可以与实施例1或实施例2相同。
微球排列
待测样品通过过滤区的速度、待测样品中干扰物质的排除率等很大程度上取决于微球的粒径和排列方式。微球的粒径和排列方式决定了微球之间间隙的大小、微球表面积的大小等。因此,微球的排列方式对检测效果和检测效率而言都至关重要。
如图4a)所示,过滤区501内的微球6有三层,每层微球具有相同的粒径,上一层微球的粒径小于下一层微球的粒径。导流槽靠近盖板的方向为上。
在一些实施例中,过滤区内的微球可以有多层。
能够通过物理过滤的方式被去除的干扰物质往往具有较大的体积和质量,在待测样品的导流过程中沉积在导流槽的底部。过滤区底层的微球粒径较大,粒径较大的微球对干扰物质进行物理过滤,防止微球之间的间隙、微球与导流槽侧壁之间的间隙被体积较大的干扰物质堵塞。而过滤层顶层的微球粒径较小,粒径较小的微球在对干扰物质进行化学过滤上具有优势。因为,微球的粒径越小,相同体积的微球具有的比表面积越大,微球表面能够承载的生物化学试剂量就越多,从而增大了干扰物质与生物化学试剂的接触面积,对干扰物质的消除更加充分。因此,这种“上小下大”的堆垛方式能够提高干扰物质的去除效果和检测效率。
实施例4
本实施例中除过滤区的结构不同外,其他结构和组成可以与实施例1~3相同。
如图4b)和图5b)所示,过滤区5由微球区501和空留区502组成,空留区502位于微球区501之上,微球区501内填满微球6。微球区内的微球对干扰物质进行物理过滤和化学过滤,空留区内待测样品由于没有阻碍、加快了导流速率。
在一些实施例中,微球区的微球有多层,微球的粒径为定值,如图5b)所示;或者,每层微球具有相同的粒径,上一层微球的粒径小于下一层微球的粒径,如图4b)所示。
实施例5
本实施例除过滤区设有多孔膜片外,其余结构和组成均可以与实施例1~4 相同。
多孔膜片
如图6和图7所示,每个过滤区5包括多孔膜片7和微球,多孔膜片与导流槽侧壁围成用于容纳微球的空间。多孔膜片的孔701尺寸小于微球的粒径。
多孔膜片7的两端分别与导流槽两侧壁301连接,相邻两多孔膜片7与导流槽两侧壁301围成过滤区。如图7所示,多孔膜片7为平板状或曲板状。所有多孔膜片7之间平行。多孔膜片由Nafion或醋酸纤维素制成。
待测样品在离开该过滤区之前还能通过多孔膜片进行第二次物理过滤;同时由于多孔膜片上的孔尺寸小于微球粒径,因此该多孔膜片能够防止微球在待测样品被导流的过程中被冲出过滤区。另外,对于靠近电极的过滤区而言,多孔膜片还能够对微球和电极之间进行阻隔。需要进行阻隔的原因在于,在微球表面的生物化学试剂与干扰物质发生反应时,很有可能会产生干扰电流信号,如果这些干扰电流信号被传导至工作电极和辅助电极,反而会加大干扰物质带来的误差。
已知待测血液中尿酸含量为300μmol·L-1,测得的各实施例1~3的尿酸含量的曲线图和测试时间的曲线图如图8所示。各实施例的过滤区中均填满微球。其中①对应导流槽内没有微球的电极试片,②对应实施例1,③对应实施例1过滤区形状和实施例3微球排列的组合,④对应实施例2,⑤对应实施例2过滤区形状和实施例3微球排列的组合。从图8可以看到,实施例2的过滤区形状能够缩短检测时间,实施例3的微球排列能够缩短检测时间并提高检测精度。
已知待测血液中尿酸含量为300μmol·L-1,测得的各实施例1、实施例4和实施例5的尿酸含量的曲线图和测试时间的曲线图如图9所示。实验中,均采用实施例1中的过滤区形状。其中,⑥对应实施例1,⑦对应实施例1过滤区形状和实施例4过滤区结构的组合,⑧对应实施例1过滤区形状和实施例5多孔膜片的组合。从图9可以看到,实施例4的过滤区结构能够缩短检测时间,实施例5 的多孔膜片能够提高检测精度。
本说明书实施例所述的内容仅仅是对实用新型构思的实现形式的列举,本实用新型的保护范围不应当被视为仅限于实施例所陈述的具体形式,本实用新型的保护范围也及于本领域技术人员根据本实用新型构思所能够想到的等同技术手段。
- 还没有人留言评论。精彩留言会获得点赞!