一种虫草头孢菌粉药物制剂中核苷类成分的含量测定方法与流程
本发明具体涉及虫草头孢菌粉药物制剂中核苷类成分的含量测定方法。
背景技术:
虫草头孢菌粉系从新鲜冬虫夏草中分离得到的麦角菌科真菌虫草头孢(cephalosporiumsinensischen.sp.nov)经液体深层发酵所得菌丝体的干燥粉末。虫草头孢菌粉的主要活性成分为多糖和核苷类。现代医学研究表明:虫草中的活性成分虫草多糖具有良好的抗氧化、提高免疫力和抗纤维化的活性。核苷类成分参与调解人体内各种生理过程。腺苷可直接进入心肌经磷酸化生成腺苷酸,参与心肌能量代谢,同时还参与扩张冠脉血管,增加血流量。腺苷对心血管系统和肌体的许多其他系统及组织均有生理作用,常作为虫草类产品的质量控制的标志性物质。
虫草头孢菌粉药物制剂由虫草头孢菌粉、香菇、灵芝、山茱萸、肉苁蓉、玉竹、麦冬7味中药组成,具有补肾培元,滋阴养肺,适用于肺肾气虚型高脂血症,慢性支气管炎恢复期的辅助治疗。其中虫草头孢菌粉是君药,具有增强体质、延缓衰老、保护心脏、改善睡眠、增强食欲、提高人体免疫功能等功效。
以腺苷属虫草头孢菌粉中的主要活性成分,建立虫草头孢菌粉制剂中腺苷的含量测定方法,有利于全面控制产品的质量,但由于虫草头孢菌粉药物制剂中成分复杂,而核苷类成分极性较大,且极性相近,难以分离,照现有报道成分析检测难度大,目前也还没有针对该药物制剂的质量控制方法的研究报道。
技术实现要素:
为解决上述问题,本发明建立了一种虫草头孢菌粉药物制剂中核苷类成分的含量测定方法,它包括如下操作步骤:
1)对照品溶液的制备:取腺苷对照品,加水溶解,即得;
2)供试品溶液的制备:取虫草头孢菌粉制剂,加水或有机溶剂水溶液提取,滤过,取续滤液,即得;
3)分别吸取对照品溶液和供试品溶液注入色谱仪,记录色谱图;色谱条件如下:色谱柱:c18色谱柱;流动相:以磷酸盐溶液为流动相a,以有机溶剂为流动相b;梯度洗脱程序:40min内使流动相a和流动相b比例在(93-60):(5-40)之间梯度变化;
4)根据步骤3)色谱图中峰面积,计算腺苷含量,公式如下:
式中c对为腺苷对照品的浓度,a样为虫草头孢菌粉制剂中腺苷的峰面积,a对为腺苷对照品的峰面积,n为稀释倍数,v样为虫草头孢菌粉制剂的体积。
进一步地,步骤1)所述对照品溶液每1ml含30-60μg腺苷,优选每1ml含42μg腺苷。
进一步地,步骤2)所述虫草头孢菌粉制剂与水或有机溶剂水溶液的体积比为2ml:15-30ml,优选体积比2ml:25ml。
进一步地,步骤2)所述有机溶剂水溶液为10-30%的乙醇或甲醇。
进一步地,步骤2)所述提取为超声或加热回流提取。
更进一步地,所述超声提取10min,所述加热回流提取1-3次,每次10-20min。
进一步地,步骤3)所述流动相a为0.05-0.2mol/l的磷酸二氢钾或磷酸二氢钠,所述流动相b为甲醇或乙腈。
更进一步地,所述流动相a为0.05-0.2mol/l磷酸二氢钾,流动相b为乙腈时,梯度洗脱程序为:
更进一步地,所述流动相a为0.05-0.2mol/l磷酸二氢钾,流动相b为甲醇时,梯度洗脱程序为:
更进一步地,所述流动相a为0.05-0.2mol/l磷酸二氢钠,流动相b为乙腈时,梯度洗脱程序为:
更进一步地,所述流动相a为0.05-0.2mol/l磷酸二氢钠,流动相b为甲醇时,梯度洗脱程序为:
本发明的虫草头孢菌粉药物制剂中核苷类成分的含量测定方法,克服了腺苷类成分呈碱性,易电离,从而导致分离和洗脱效果差的缺点,实现了虫草头孢菌粉药物制剂中腺苷类成分高灵敏度、好稳定性的检测,使虫草头孢菌粉制剂的质量得到客观、全面准确的评价,也保证了其质量和临床疗效,具有重要的意义。
显然,根据本发明的上述内容,按照本领域的普通技术知识和惯用手段,在不脱离本发明上述基本技术思想前提下,还可以做出其它多种形式的修改、替换或变更。
以下通过实施例形式的具体实施方式,对本发明的上述内容再作进一步的详细说明。但不应将此理解为本发明上述主题的范围仅限于以下的实例。凡基于本发明上述内容所实现的技术均属于本发明的范围。
附图说明
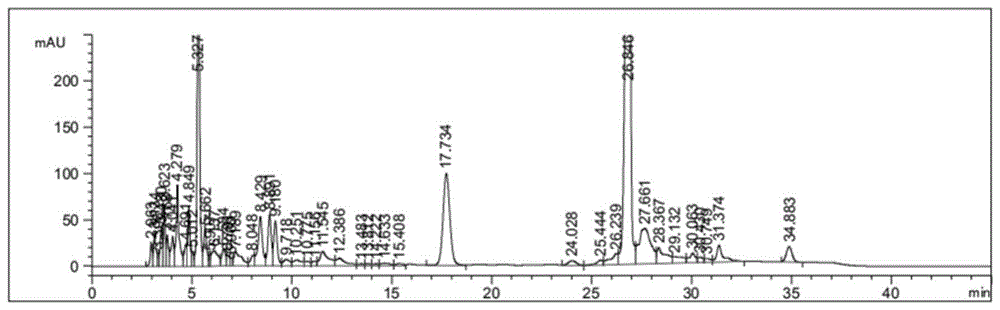
图10.06mol/l磷酸二氢钾(a)-甲醇梯度洗脱液相色谱图
图20.06mol/l磷酸二氢钠(a)-乙腈梯度洗脱液相色图
图30.07mol/l磷酸二氢钾(a)-甲醇梯度洗脱液相色谱图
图40.1mol/l磷酸二氢钠(a)-乙腈梯度洗脱液相色图
图5腺苷标准曲线图
具体实施方式
本发明具体实施方式中使用的原料、试剂、设备均为已知产品,通过购买市售产品获得。
实施例1本发明检测方法
(1)对照品溶液的制备
精密称取腺苷对照品16.91mg,置100ml量瓶中,加水至刻度,摇匀,精密量取5ml,置20ml量瓶中,加水至刻度,摇匀,即得,于4℃保存备用。
(2)供试品溶液的制备
精密量取虫草头孢菌粉制剂2ml置25ml量瓶中,加水20ml,超声提取10min,加水定容置刻度,滤过,取续滤液过0.45μm微孔滤膜,作为样品溶液。
(3)液相色谱图的获取
取对照品溶液和供试品溶液20μl注入高效液相色谱仪,记录色谱图(如图1所示),所用高效液相色谱设置参数如下:
仪器:agilent1200高效液相色谱仪;
色谱柱:comosilpackproc18(4.6*250mm,5μm)色谱柱;
流动相:浓度0.06mol/l磷酸二氢钾(a)-甲醇(b);
流速:1.0ml/min;
进样量:20μl;
检测器:二极管阵列检测器(dad),扫描范围190-400nm;
检测波长:260nm;
流动相的梯度洗脱程序如下:
(4)样品中腺苷活性成分的测定
按如下公式计算有效成分腺苷的含量为18.0mg/瓶
式中c对为腺苷对照品的浓度,a样为虫草头孢菌粉制剂中腺苷的峰面积,a对为腺苷对照品的峰面积,n为稀释倍数,v样为虫草头孢菌粉制剂的体积。
实施例2本发明检测方法
(1)对照品溶液的制备
精密称取腺苷对照品16.91mg,置100ml量瓶中,加10%甲醇至刻度,摇匀,精密量取5ml,置20ml量瓶中,加10%甲醇至刻度,摇匀,即得,于4℃保存备用。
(2)供试品溶液的制备
精密量取虫草头孢菌粉制剂2ml置25ml量瓶中,加10%甲醇20ml,超声提取10min,加10%甲醇定容置刻度,滤过,取续滤液,作为样品溶液。
(3)液相色谱图的获取
取对照品溶液和供试品溶液20μl注入高效液相色谱仪,记录色谱图(如图2所示),所用高效液相色谱设置参数如下:
仪器:agilent1200高效液相色谱仪;
色谱柱:comosilpackproc18(4.6*250mm,5μm)色谱柱;
流动相:浓度0.05mol/l磷酸二氢钠(a)-乙腈(b);
流速:1.0ml/min;
进样量:20μl;
检测器:二极管阵列检测器(dad),扫描范围190-400nm;
检测波长:260nm;
流动相的梯度洗脱程序如下:
(4)样品中腺苷活性成分的测定
按如下公式计算有效成分腺苷的含量为18.0mg/瓶。
式中c对为腺苷对照品的浓度,a样为虫草头孢菌粉制剂中腺苷的峰面积,a对为腺苷对照品的峰面积,n为稀释倍数,v样为虫草头孢菌粉制剂的体积。
实施例3本发明检测方法
(1)对照品溶液的制备
精密称取腺苷对照品16.91mg,置100ml量瓶中,加10%甲醇至刻度,摇匀,精密量取5ml,置20ml量瓶中,加10%甲醇至刻度,摇匀,即得,于4℃保存备用。
(2)供试品溶液的制备
精密量取虫草头孢菌粉制剂2ml置25ml量瓶中,加10%甲醇20ml,超声提取10min,加10%甲醇定容置刻度,滤过,取续滤液,作为样品溶液。
(3)液相色谱图的获取
取对照品溶液和供试品溶液20μl注入高效液相色谱仪,记录色谱图(如图3所示),所用高效液相色谱设置参数如下:
仪器:agilent1200高效液相色谱仪;
色谱柱:comosilpackproc18(4.6*250mm,5μm)色谱柱;
流动相:浓度0.07mol/l磷酸二氢钾(a)-乙腈(b);
流速:1.0ml/min;
进样量:20μl;
检测器:二极管阵列检测器(dad),扫描范围190-400nm;
检测波长:260nm;
流动相的梯度洗脱程序如下:
(4)样品中腺苷活性成分的测定
按如下公式计算有效成分腺苷的含量为18.0mg/瓶。
式中c对为腺苷对照品的浓度,a样为虫草头孢菌粉制剂中腺苷的峰面积,a对为腺苷对照品的峰面积,n为稀释倍数,v样为虫草头孢菌粉制剂的体积。
实施例4本发明检测方法
(1)对照品溶液的制备
精密称取腺苷对照品16.91mg,置100ml量瓶中,加10%甲醇至刻度,摇匀,精密量取5ml,置20ml量瓶中,加10%甲醇至刻度,摇匀,即得,于4℃保存备用。
(2)供试品溶液的制备
精密量取虫草头孢菌粉制剂2ml置25ml量瓶中,加10%甲醇20ml,超声提取10min,加10%甲醇定容置刻度,滤过,取续滤液,作为样品溶液。
(3)液相色谱图的获取
取对照品溶液和供试品溶液20μl注入高效液相色谱仪,记录色谱图(如图4所示),所用高效液相色谱设置参数如下:
仪器:agilent1200高效液相色谱仪;
色谱柱:comosilpackproc18(4.6*250mm,5μm)色谱柱;
流动相:浓度0.1mol/l磷酸二氢钠(a)-甲醇(b);
流速:1.0ml/min;
进样量:20μl;
检测器:二极管阵列检测器(dad),扫描范围190-400nm;
检测波长:260nm;
流动相的梯度洗脱程序如下:
(4)样品中腺苷活性成分的测定
按如下公式计算有效成分腺苷的含量为18.0mg/瓶。
式中c对为腺苷对照品的浓度,a样为虫草头孢菌粉制剂中腺苷的峰面积,a对为腺苷对照品的峰面积,n为稀释倍数,v样为虫草头孢菌粉制剂的体积。
以下通过试验例的方式进一步说明本发明的有益效果:
试验例1方法学验证
1)色谱条件
色谱柱:cosmosilpackedcolumn5c18-paq,4.6*250mm;流动相:0.06mol/l磷酸二氢钾溶液(ph=5)为流动相a,以甲醇为流动相b,按下表进行梯度洗脱;检测波长为260nm;柱温:30℃;进样量:20μl。在以上色谱条件下,规定理论塔板数按腺苷峰计,应不低于3000。
2)系统适用性试验
精密称取腺苷对照品19.61mg,置200ml量瓶中,加水至刻度,摇匀,精密量取10ml,置25ml量瓶中,加水至刻度,摇匀,即得(浓度为39.22μg/ml)。
精密量取腺苷对照品溶液20μl,按上述色谱条件,连续进样测定6次,记录峰面积,结果见表1。
表1系统适用性试验结果
结果表明:rsd<2.0%,系统适用性较好。
3)专属性
溶剂空白溶液的制备:吸取水作为溶剂空白溶液。
对照品溶液的制备:精密称取腺苷对照品适量,加水溶解后制成每1ml含40μg的溶液,即得。
供试品溶液的制备:精密量取本品2ml,置25ml量瓶中,加水20ml,超声提取10分钟,加水至刻度,摇匀,微孔滤膜(0.45μm)滤过,取续滤液作为供试品溶液。
分别精密吸取上述溶液与对照品溶液、溶剂空白溶液各20μl,分别注入液相色谱仪,记录色谱图。结果显示:供试品溶液与对照品溶液中腺苷峰的保留时间一致,主峰与相邻峰分离度为3.79(大于1.5),空白溶液在主峰位置未出峰;供试品图谱中,腺苷主峰的纯度因子为999.334,在计算出的阈值限值以内,表明腺苷主峰检测无其它成分干扰,专属性良好。
4)线性与范围
精密称取腺苷对照品30.37mg,置200ml量瓶中,加水至刻度,摇匀,作为线性溶液母液(浓度为151.85μg/ml),精密量取5ml、6ml、8ml、10ml、12ml、15ml母液置25ml量瓶中,加水至刻度,摇匀,即得。按上述色谱条件测定,记录色谱峰面积,结果见表2。以峰面积(y)对对照品浓度(x)进行回归,计算回归方程,并以峰面积为纵坐标,对照品浓度(μg/ml)为横坐标,绘制标准曲线,见图5。
表2线性关系试验结果
结果表明在30.370~91.110μg/ml范围内,腺苷峰面积与浓度呈良好的线性关系。
5)重复性试验
精密量取样品2ml,6份,置25ml量瓶中,加水20ml,超声提取,放冷,加水至刻度,摇匀,微孔滤膜(0.45μm)滤过,取续滤液作为供试品溶液。按上述色谱条件测定,记录峰面积,采用外标法计算样品中腺苷含量,试验结果见表3。
表3重复性试验结果
结果表明:rsd<2.0%,该方法的重复性较好。
6)稳定性试验
精密量取供试品溶液20μl,按上述色谱条件,分别于0,2,4,8,12h进样,记录峰面积,采用外标法计算样品中腺苷含量,结果见表4。
表4稳定性试验结果
试验结果表明:rsd<2.0%,本品含量测定供试品溶液在室温放置12h内稳定。
7)中间精密度试验
由不同的分析人员,使用不同的仪器在不同的日期进行,按重复性试验项下方法对相同批次样品进行分析,试验结果见表5。
表5中间精密度试验结果
注:rsd*为重复性与中间精密度12份样品含量计算所得rsd值。
结果表明:rsd<2.0%,腺苷含量测定方法重复性良好。
8)准确度试验
精密量取供试品溶液(腺苷含量:0.579mg/ml)1ml,共9份,分别置25ml容量瓶中,依次编号1-9,再分别往容量瓶中加入对照品溶液(0.103mg/ml)3ml、6ml、8.5ml,各三份,加水20ml,超声提取10分钟,放冷,加水至刻度,摇匀,微孔滤膜(0.45μm)滤过,取续滤液作为供试液溶液。按照上述色谱条件,精密量取供试品溶液20μl,记录峰面积,计算供试品中腺苷含量,计算加样回收率,结果见表6。
表6准确度试验结果
结果表明:腺苷含量测定平均回收率均在95%~105%之间,rsd<2.0%,该方法的准确度较好。
9)耐用性试验
精密量取样品(批号16070901)2ml,按供试品溶液的制备方法制备供试品溶液,按上述色谱条件中,其他条件不变情况下,分别改变柱温、检测波长、流速、流动相比例、色谱柱品牌,测定供试品溶液中腺苷含量,记录峰面积,计算腺苷含量,结果见表7、表8。
表7不同色谱条件耐用性试验结果
结果表明:不同的柱温、检测波长、流速、流动相比例的较小变动后,样品中腺苷含量均值为0.579mg/ml,rsd<2.0%,说明该方法耐用性较好。
表8不同色谱柱耐用性试验结果
结果表明:采用不同的品牌的色谱柱,样品中腺苷含量均值为0.532mg/ml,rsd<2.0%,说明该方法耐用性较好。
10)样品含量测定
取三批样品(批号16070901、16070902、16070903),每批2份,分别精密量取2ml,按供试品溶液的制备方法制备供试品溶液。精密量取供试品溶液各20μl,按上述色谱条件测定,记录峰面积,采用外标法计算样品中腺苷含量,结果见表9。
表9三批中试样品含量测定结果
综上,本发明含量测定方法,克服了腺苷类成分呈碱性,易电离,从而导致分离和洗脱效果差的缺点,实现了虫草头孢菌粉药物制剂中腺苷类成分高灵敏度、好稳定性的检测,使虫草头孢菌粉制剂的质量得到客观、全面准确的评价,也保证了其质量和临床疗效,具有重要的意义。
- 还没有人留言评论。精彩留言会获得点赞!