一种磁微粒化学发光法醛固酮测定试剂盒及使用方法与流程
本发明涉及医疗器械生物类免疫体外诊断相关技术领域,特别涉及一种磁微粒化学发光法醛固酮测定试剂盒及使用方法。
背景技术:
醛固酮是是人体内调节血容量的激素,通过调节肾脏对钠的重吸收,维持水平衡。醛固酮是调节细胞外液容量和电解质的激素,醛固酮的分泌,是通过醛固酮一血管紧张素系统实现的。当细胞外液容量下降时,刺激肾小球旁细胞分泌醛固酮,激活醛固酮-血管紧张素-醛固酮系统、醛固酮分泌增加,使肾脏重吸收钠增加,进而引起水重吸收增加,细胞外液容量增多;相反细胞外液容量增多时,通过上述相反的机制,使醛固酮分泌减少,肾重吸收钠水减少,细胞外液容量下降。血钠降低,血钾升高同样刺激肾上腺皮质,使醛固酮分泌增加。
醛固酮增高多见于:原发性醛固酮增多症,假性醛固酮增多症(双侧肾上腺球状带增生),利尿剂、心衰、肝硬变、肾衰、肾病综合征等所致的继发性醛固酮增多症,原发性周期性水肿,bartter氏综合征,肾球旁器增生,手术后,低血容量,各种原因所致的低钾血症,部分恶性高血压及缓进型高血压等。
醛固酮降低多见于:肾上腺皮质功能减退,低醛固酮低醛固酮综合征,18-羟化酶缺乏,糖尿病,turner氏综合征,急性乙醇中毒等。
因此,研发一种操作简便,反应灵敏度高的醛固酮检测产品,对现有技术有着重要的作用。
技术实现要素:
针对现有技术存在的需要一种操作简便,反应灵敏度高的醛固酮检测产品的技术问题,本发明提供一种磁微粒化学发光法醛固酮测定试剂盒及使用方法。
为实现上述目的,本发明的技术方案为:
一种磁微粒化学发光法醛固酮测定试剂盒,包括相互独立包装的磁分离试剂、生物素化醛固酮抗体、碱性磷酸酶标记醛固酮抗原、校准品和质控品;
a、所述生物素化醛固酮抗体通过包括以下步骤的操作制备而成:
sa1:准确称量0.3~0.5mg生物素-nhs并用dmso溶解至终浓度为4.5~5.5mg/ml,制得生物素-nhs的dmso溶液;
sa2:准确称量0.9~1.1mg醛固酮抗体并加入所述生物素-nhs的dmso溶液中,充分混匀后室温反应1.5~2.5h;
sa3:用透析袋对sa2中反应产物进行透析处理;
sa4:用抗试剂缓冲液将sa3制得的混合物稀释至0.45~0.55μg/ml即得;
所述抗试剂缓冲液为ph值为5~6的pbs体系;所述抗试剂缓冲液包括纯化水1l、na2po3h·12h2o10~20g、napo3h2·12h2o1~2g、绵羊血清1~5g、新生牛血清3~10g和马血清1~5g;
b、所述碱性磷酸酶标记醛固酮抗原通过包括以下步骤的操作制备而成:
sb1:将检测醛固酮抗原进行透析处理后用2-it进行活化;
sb2:将碱磷酶用smcc进行活化;
sb3:将活化后的所述检测醛固酮抗原和所述碱磷酶混合后在2~8℃反应16~20h;
sb4:将sb3制备的反应物用层析柱进行纯化,收集i峰ii峰并混合,制得抗原-碱磷酶;
sb5:用抗试剂缓冲液将所述抗原-碱磷酶稀释至0.09~0.11μg/ml即得;
c、所述校准品和所述质控品的成分相同,且均通过包括用醛固酮校准品缓冲液将待检抗原稀释的操作制备而成。
优选的,醛固酮抗体为鼠单克隆抗体。
优选的,所述醛固酮抗体与所述生物素-nhs的摩尔比为1:20;其中,醛固酮抗体的分子量以1500000计,生物素-nhs的分子量以587计。
优选的,sa3中所述透析袋的截留分子量为500。
优选的,sa3中透析处理所用的透析缓冲液为ph为7.5的0.15m的pbs缓冲液。
优选的,sb1中透析处理所用的透析缓冲液为0.1m的pbs缓冲液。
优选的,所述醛固酮校准品缓冲液通过向0.05m的ph为7.4的tris缓冲液中加入牛血清白蛋白和防腐剂制备而成,所述醛固酮校准品缓冲液中所述牛血清白蛋白的体积百分比为0.5%,所述防腐剂的体积百分比为0.2%。
优选的,所述待检抗原稀释的最终浓度为0pg/ml、50pg/ml、250pg/ml、500pg/ml、1000pg/ml和2000pg/ml。
优选的,所述磁分离试剂为链霉亲和素磁珠。
一种上述任一项所述的磁微粒化学发光法醛固酮测定试剂盒的使用方法,包括以下步骤:
sd1:准确称取待检测样本30μl、所述生物素化醛固酮抗体30μl和所述碱性磷酸酶标记醛固酮抗原30μl充分混合并孵育15min;
sd2:向sd1制得的反应物中加入所述磁分离试剂30μl充分混合并孵育5min;
sd3:对sd2制得的反应物磁分离2min,去除上清保留底物;
sd4:对所述底物洗涤3次,每次用300μl洗液;
sd5:用200μl所述醛固酮校准品缓冲液将所述底物稀释后测值。
本发明具有如下优点:
1.整个反应体系避免了放射性污染,延长了试剂效期,简化了实验操作流程;
2.亲和素与生物素间的结合具有极高的亲和力,其反应呈高度专一性,在提高灵敏度的同时,并不增加非特异性干扰;
3.结合特性不会因反应试剂的高度稀释而受影响,使其在实际应用中可最大限度地降低反应试剂的非特异作用。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
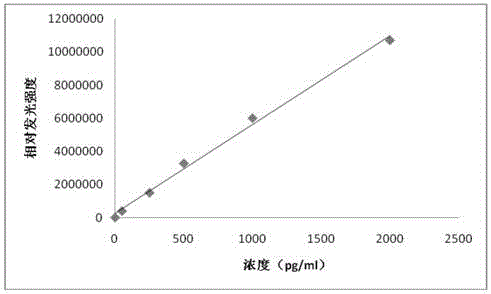
图1为体系1曲线拟合;
图2为体系2曲线拟合。
具体实施方式
下面结合附图对本发明的具体实施方式作进一步说明。在此需要说明的是,对于这些实施方式的说明用于帮助理解本发明,但并不构成对本发明的限定。此外,在以下说明中,省略了对公知结构、技术及操作的描述,以避免不必要地混淆本发明的概念。另外,下面所描述的本发明各个实施方式中所涉及的技术特征只要彼此之间未构成冲突就可以相互组合。
本发明中,未特别注明单位的比例与含量,固体组分为质量比例与含量,液体组分为体积比例与含量。
实施例1
一种磁微粒化学发光法醛固酮测定试剂盒,包括相互独立包装的链霉亲和素磁珠、生物素化醛固酮抗体、碱性磷酸酶标记醛固酮抗原、校准品和质控品;
a、生物素化醛固酮抗体通过包括以下步骤的操作制备而成:
sa1:准确称量0.3mg生物素-nhs并用dmso溶解至终浓度为4.5mg/ml,制得生物素-nhs的dmso溶液;
sa2:准确称量0.9mg鼠单克隆醛固酮抗体并加入生物素-nhs的dmso溶液中,其中,充分混匀后室温反应1.5h;
sa3:用截留分子量为500的透析袋,以及ph为7.5的0.15m的pbs缓冲液充当的透析缓冲液对sa2中反应产物进行透析处理;
sa4:用抗试剂缓冲液将sa3制得的混合物稀释至0.45μg/ml即得;
b、碱性磷酸酶标记醛固酮抗原通过包括以下步骤的操作制备而成:
sb1:用0.1m的pbs缓冲液作为透析缓冲液将检测醛固酮抗原进行透析处理后用2-it进行活化;
sb2:将碱磷酶用smcc进行活化;
sb3:将活化后的检测醛固酮抗原和碱磷酶混合后在2℃反应16h;
sb4:将sb3制备的反应物用层析柱进行纯化,收集i峰ii峰并混合,制得抗原-碱磷酶;
sb5:用抗试剂缓冲液将抗原-碱磷酶稀释至0.09μg/ml即得;
c、校准品和质控品的成分相同,且均通过包括用醛固酮校准品缓冲液将待检抗原稀释最终浓度为0pg/ml、50pg/ml、250pg/ml、500pg/ml、1000pg/ml和2000pg/ml;
其中,醛固酮校准品缓冲液通过向0.05m的ph为7.4的tris缓冲液中加入牛血清白蛋白和防腐剂制备而成,醛固酮校准品缓冲液中牛血清白蛋白的体积百分比为0.5%,防腐剂的体积百分比为0.2%。
实施例2
一种磁微粒化学发光法醛固酮测定试剂盒,包括相互独立包装的链霉亲和素磁珠、生物素化醛固酮抗体、碱性磷酸酶标记醛固酮抗原、校准品和质控品;
a、生物素化醛固酮抗体通过包括以下步骤的操作制备而成:
sa1:准确称量0.4mg生物素-nhs并用dmso溶解至终浓度为5mg/ml,制得生物素-nhs的dmso溶液;
sa2:准确称量1mg鼠单克隆醛固酮抗体并加入生物素-nhs的dmso溶液中,其中,醛固酮抗体与生物素-nhs的摩尔比为1:20,充分混匀后室温反应2h;
sa3:用截留分子量为500的透析袋,以及ph为7.5的0.15m的pbs缓冲液充当的透析缓冲液对sa2中反应产物进行透析处理;
sa4:用抗试剂缓冲液将sa3制得的混合物稀释至0.5μg/ml即得;
b、碱性磷酸酶标记醛固酮抗原通过包括以下步骤的操作制备而成:
sb1:用0.1m的pbs缓冲液作为透析缓冲液将检测醛固酮抗原进行透析处理后用2-it进行活化;
sb2:将碱磷酶用smcc进行活化;
sb3:将活化后的检测醛固酮抗原和碱磷酶混合后在4℃反应18h;
sb4:将sb3制备的反应物用层析柱进行纯化,收集i峰ii峰并混合,制得抗原-碱磷酶;
sb5:用抗试剂缓冲液将抗原-碱磷酶稀释至1μg/ml即得;
c、校准品和质控品的成分相同,且均通过包括用醛固酮校准品缓冲液将待检抗原稀释最终浓度为0pg/ml、50pg/ml、250pg/ml、500pg/ml、1000pg/ml和2000pg/ml;
其中,醛固酮校准品缓冲液通过向0.05m的ph为7.4的tris缓冲液中加入牛血清白蛋白和防腐剂制备而成,醛固酮校准品缓冲液中牛血清白蛋白的体积百分比为0.5%,防腐剂的体积百分比为0.2%。
实施例3
一种磁微粒化学发光法醛固酮测定试剂盒,包括相互独立包装的磁分离试剂、生物素化醛固酮抗体、碱性磷酸酶标记醛固酮抗原、校准品和质控品;
a、生物素化醛固酮抗体通过包括以下步骤的操作制备而成:
sa1:准确称量0.5mg生物素-nhs并用dmso溶解至终浓度为5.5mg/ml,制得生物素-nhs的dmso溶液;
sa2:准确称量1.1mg醛固酮抗体并加入生物素-nhs的dmso溶液中,其中,充分混匀后室温反应2.5h;
sa3:用截留分子量为500的透析袋,以及ph为7.5的0.15m的pbs缓冲液充当的透析缓冲液对sa2中反应产物进行透析处理;
sa4:用抗试剂缓冲液将sa3制得的混合物稀释至0.55μg/ml即得;
b、碱性磷酸酶标记醛固酮抗原通过包括以下步骤的操作制备而成:
sb1:用0.1m的pbs缓冲液作为透析缓冲液将检测醛固酮抗原进行透析处理后用2-it进行活化;
sb2:将碱磷酶用smcc进行活化;
sb3:将活化后的检测醛固酮抗原和碱磷酶混合后在8℃反应20h;
sb4:将sb3制备的反应物用层析柱进行纯化,收集i峰ii峰并混合,制得抗原-碱磷酶;
sb5:用抗试剂缓冲液将抗原-碱磷酶稀释至0.11μg/ml即得;
c、校准品和质控品的成分相同,且均通过包括用醛固酮校准品缓冲液将待检抗原稀释最终浓度为0pg/ml、50pg/ml、250pg/ml、500pg/ml、1000pg/ml和2000pg/ml;
其中,醛固酮校准品缓冲液通过向0.05m的ph为7.4的tris缓冲液中加入牛血清白蛋白和防腐剂制备而成,醛固酮校准品缓冲液中牛血清白蛋白的体积百分比为0.5%,防腐剂的体积百分比为0.2%。
实施例4
磁微粒化学发光法醛固酮测定试剂盒的使用方法(以实施例2制备的产品为例),包括以下步骤:
sd1:准确称取待检测样本30μl、生物素化醛固酮抗体30μl和碱性磷酸酶标记醛固酮抗原30μl充分混合并孵育15min;
sd2:向sd1制得的反应物中加入磁分离试剂30μl充分混合并孵育5min;
sd3:对sd2制得的反应物磁分离2min,去除上清保留底物;
sd4:对底物洗涤3次,每次用300μl洗液;
sd5:用200μl醛固酮校准品缓冲液将底物稀释后测值。
本发明同时用生物素化的醛固酮单克隆抗体-链霉亲和素磁珠(体系1),醛固酮单克隆抗体包被的羧基化的磁微粒(体系2),分别用两个体系对0pg/ml、50pg/ml、250pg/ml、500pg/ml、1000pg/ml和2000pg/ml的醛固酮样品做检测,同时测试同一组样本,并与给值进行比对,数据如下表所示:
表1.不同体系下测值与给值对比以及测值之间对比
体系1和体系2的曲线拟合分别如图1和图2所示。由结果可以看出,不同体系测值与给值相关性都在0.9以上,说明相关性良好,且不同体系之间测值相关性大于0.9,说明2种体系测值一致。
以上结合附图对本发明的实施方式作了详细说明,但本发明不限于所描述的实施方式。对于本领域的技术人员而言,在不脱离本发明原理和精神的情况下,在没有做出创造性劳动前提下,对这些实施方式进行多种变化、修改、替换和变型,仍落入本发明的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种使用磁微粒化学发光定量检测抗SS-B抗体IgG的试剂盒及其制备方法和检测方法
- 一种使用磁微粒化学发光定量检测抗核小体抗体IgG的试剂盒及其制备方法和检测方法
- 一种使用磁微粒化学发光定量检测抗nRNP/Sm抗体IgG的试剂盒及其制备方法和检测方法
- 一种甲状腺球蛋白的磁微粒分离化学发光免疫检测方法
- 一种免疫磁微粒化学发光法HCMVpp65抗原检测试剂盒的制作方法
- 纳米磁微粒化学发光法检测血清总IgE的试剂盒及方法
- 一种使用磁微粒化学发光定量检测抗Scl-70抗体IgG的试剂盒及其制备方法和检测方法
- 基于磁微粒化学发光的多目标物定量检测的微流控芯片的制作方法
- 用于全血样品检测的磁微粒直接化学发光微流控芯片的制作方法
- 定量检测全血中脑钠肽的磁微粒化学发光微流控芯片的制作方法