一种检测新型冠状病毒N蛋白的适配体胶体金试纸及其制备方法与流程
本发明涉及生物医药技术领域,尤其涉及一种用于检测新型冠状病毒n蛋白的适配体胶体金试纸及其制备方法。
背景技术:
冠状病毒是一个大型病毒家族,已知可引起感冒以及中东呼吸综合征(mers)和严重急性呼吸综合征(sars)等较严重疾病。新型冠状病毒是以前从未在人体中发现的冠状病毒新毒株。针对新型冠状病毒的疫苗及特异性治疗药物还没有研发成功,早期的预防和诊断是防控疫情的重要手段。
目前,用于检测新型冠状病毒的试纸采用的是抗体对检测,这个试纸的弊端在于,寻找可匹配检测的抗议对的难度较大,而且用于检测对的抗体对的亲和力可能存在较大差异,生产成本较高。
技术实现要素:
为了解决上述技术问题,本发明提供了一种检测新型冠状病毒n蛋白的适配体胶体金试纸及其制备方法,适配体胶体金试纸用于检测新型冠状病毒的核壳蛋白基因(nucleocapsidprotein,n),以下简称n蛋白。
根据本申请的一个方面,提供了一种检测新型冠状病毒n蛋白的适配体胶体金试纸,适配体胶体金试纸包括:依次相互搭接的样品垫、结合物垫、硝酸纤维素膜和吸水垫;结合物垫上包被有胶体金标记的适配体探针;从样品垫到吸收垫的方向上,硝酸纤维素膜上依次设置有检测线和质控线,检测线包被有新型冠状病毒n蛋白单抗;质控线包被有链霉亲和素蛋白多抗。
可选择地,适配体探针包括核酸适配体48、核酸适配体58、核酸适配体88中的一种或两种以上;核酸适配体48的核苷酸序列如seqidno:1所示;核酸适配体58的核苷酸序列如seqidno:2所示;核酸适配体88的核苷酸序列如seqidno:3所示。
可选择地,适配体探针为生物素化的核酸适配体与链霉亲和素结合,共同形成的链霉亲和素-生物素-核酸适配体结构。
可选择地,核酸适配体包括核酸适配体48、核酸适配体58和核酸适配体88;核酸适配体48、核酸适配体58、核酸适配体88的比例为1:1:1。
可选择地,结合物垫上包被的胶体金标记的适配体探针的工作浓度为1-10pmol/ml;检测线包被的新型冠状病毒n蛋白单抗的工作浓度为1~2mg/ml;质控线包被的链霉亲和素蛋白多抗的工作浓度为1~2mg/ml。
可选择地,新型冠状病毒n蛋白单抗检测的新型冠状病毒n蛋白的序列如seqidno:4所示。
根据本申请的另一个方面,提供了一种检测新型冠状病毒n蛋白的适配体胶体金试纸的制备方法,包括以下步骤:(1)将生物素化的核酸适配体与胶体金标记的链霉亲和素结合,得到链霉亲和素-生物素-核酸适配体;(2)将链霉亲和素-生物素-核酸适配体喷涂到结合物垫上;(3)将新型冠状病毒n蛋白单抗在硝酸纤维素膜上划线;将链霉亲和素蛋白多抗在硝酸纤维素膜上划线;得到包被了检测线和质控线的硝酸纤维素膜;(4)将样品垫结合物垫、硝酸纤维素膜和吸收垫依次固定在底板上,得到用于检测新型冠状病毒n蛋白的适配体胶体金试纸。
可选择地,步骤(1)包括:(1.1)向加热至沸腾的氯金酸水溶液与柠檬酸三钠溶液混合,继续煮沸至溶液呈酒红色后,继续加热预设时长,停止加热,冷却后得到胶体金溶液,其中,氯金酸与柠檬酸三钠的质量比为1:0.9~1.2;其中,胶体金溶液中胶体金的粒径为25~35nm;(1.2)向胶体金溶液中加入碳酸钾,将胶体金溶液的ph值调节到6~6.5;(1.3)将链霉亲和素加入到胶体金溶液中,再向胶体金溶液中加入封闭液,静置第一预定时长,离心分离,向离心分离得到的沉淀物中加入胶体金重悬液使其重新溶解,胶体金重悬液的加入量为胶体金溶液的九分之一到十分之一,得到胶体金标记的链霉亲和素重悬液;(1.4)向胶体金标记的链霉亲和素溶液中加入生物素化的核酸适配体,孵育第二预定时长后,离心得到链霉亲和素-生物素-核酸适配体,向离心分离得到的沉淀物中加入胶体金重悬液使其重新溶解,胶体金重悬液的加入量为胶体金溶液的九分之一到十分之一,得到链霉亲和素-生物素-核酸适配体重悬液。
可选择地,生物素化的核酸适配体包括核酸适配体48、核酸适配体58和核酸适配体88中的一种或多种;核酸适配体48的核苷酸序列如seqidno:1所示;核酸适配体58的核苷酸序列如seqidno:2所示;核酸适配体88的核苷酸序列如seqidno:3所示。
可选择地,步骤(3)包括:(3.1)将新型冠状病毒n蛋白单抗与磷酸盐缓冲液混合,得到新型冠状病毒n蛋白单抗浓度为1~2mg/ml的检测包被溶液,用划膜机构将检测包被溶液在硝酸纤维素膜上划膜,划膜速度为1μl/cm~2μl/cm;(3.2)将链霉亲和素蛋白多抗与磷酸盐缓冲液混合,得到链霉亲和素蛋白多抗浓度为1~2mg/ml的质控包被溶液,用划膜机构将质控包被溶液在硝酸纤维素膜上划膜;质控包被溶液在硝酸纤维素膜上划膜的速度为1μl/cm~2μl/cm;(3.3)将硝酸纤维素膜置于温度30~40℃、湿度低于30%的环境中,干燥6-8小时。
本申请的检测新型冠状病毒n蛋白的适配体胶体金试纸选用适配体和抗体结合检测新型冠状病毒的n蛋白,亲和力更高,反应速度更快,便于操作,易于质控和保存。
附图说明
构成本发明的一部分的附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。在附图中:
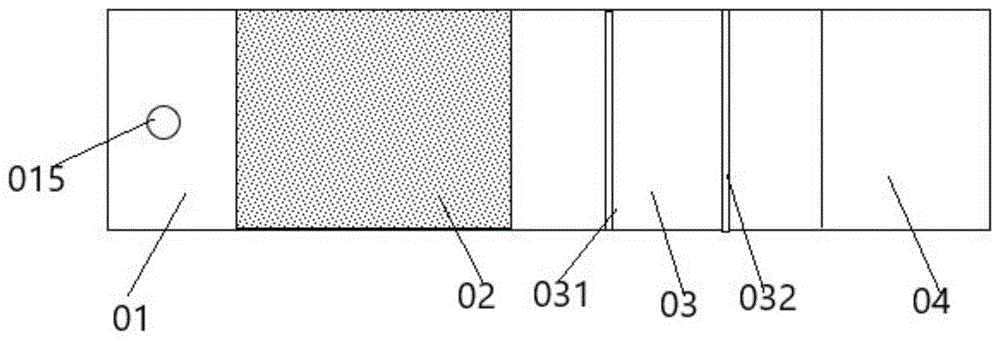
图1是本申请中检测新型冠状病毒n蛋白的适配体胶体金试纸的结构示意图。
具体实施方式
为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。需要说明的是,在不冲突的情况下,本申请中的实施例及实施例中的特征向量可以相互任意组合。
冠状病毒是一个大型病毒家族,已知可引起感冒以及中东呼吸综合征(mers)和严重急性呼吸综合征(sars)等较严重疾病。新型冠状病毒是以前从未在人体中发现的冠状病毒新毒株。
针对新型冠状病毒的疫苗及特异性治疗药物还没有研发成功,早期的预防和诊断是防控疫情的重要手段。目前,新型冠状病毒的诊断通常需要半天到一天才能得到检测结果,而且受检测个体的影响较大,存在假阳性和假阴性的误诊问题,影响防控措施的落实。
本申请提供了一种检测新型冠状病毒n蛋白的适配体胶体金试纸,用于检测新型冠状病毒的n蛋白,其中,新型冠状病毒为covid-19型新型冠状病毒。具体的,适配体胶体金试纸包括:底板、依次相互搭接设置在底板上的样品垫01、结合物垫02、硝酸纤维素膜03和吸收垫04;结合物垫02上包被有胶体金标记的适配体探针;从样品垫到吸收垫的方向上,硝酸纤维素膜03上依次设置有检测线031和质控线032,检测线031包被有新型冠状病毒n蛋白单抗;质控线032包被有链霉亲和素蛋白多抗;适配体探针包括核酸适配体48、核酸适配体58、核酸适配体88中的一种或两种以上;核酸适配体48的核苷酸序列如seqidno:1所示;核酸适配体58的核苷酸序列如seqidno:2所示;核酸适配体88的核苷酸序列如seqidno:3所示。
其中,本申请中用于检测线031包被的新型冠状病毒n蛋白单抗为北京安必奇生物科技有限公司研发的货号为505的新型冠状病毒n蛋白单抗
本申请中用于质控线031包被的链霉亲和素蛋白多抗购自洛阳佰奥通实验材料中心,货号为c020120。
其中,适配体探针为生物素化的核酸适配体与链霉亲和素结合,共同形成的链霉亲和素-生物素-核酸适配体结构。
作为一种示例,硝酸纤维素膜03上还设置有质控区,质控区设置有质控线032;质控线032包被有链霉亲和素蛋白多抗;检测线031设置在硝酸纤维素膜靠近结合物垫02的一侧;质控线032设置在硝酸纤维素膜靠近吸收垫04的一侧。
作为一种示例,核酸适配体包括核酸适配体48、核酸适配体58和核酸适配体88;核酸适配体48、核酸适配体58、核酸适配体58的比例为1:1:1。
作为一种示例,结合物垫02上包被的胶体金标记的适配体探针的工作浓度为1-10pmol/ml:检测线031包被的新型冠状病毒n蛋白单抗的工作浓度为1~2mg/ml;质控线032包被的链霉亲和素蛋白多抗的工作浓度为1~2mg/ml。
作为一种示例,新型冠状病毒n蛋白单抗用于检测的新型冠状病毒n蛋白的序列如seqidno:4所示。
作为一种示例,样品垫01搭接在结合物垫02上,搭接部分长度为0.5~2mm;结合物垫02搭接在硝酸纤维素膜03上,搭接部分长度为0.5~2mm,吸水垫04搭接在硝酸纤维素膜03上,搭接长度为0.5~2mm。
样品垫01、结合物垫02、硝酸纤维素膜03、吸水垫04与底板的两侧边缘对齐,样品垫01和吸水垫04与底板的两端边缘对齐。
作为一种示例,本申请的检测新型冠状病毒n蛋白的适配体胶体金试纸为裁切成宽度均匀的试纸条,试纸条的宽度为2~5mm,检测线031与质控线032相互平行,检测线031、质控线032与搭接在硝酸纤维素膜03上的结合物垫02的侧边平行,且检测线031、质控线032的长度与硝酸纤维素膜03的宽度相同。检测线031、质控线032长度为2~3.5mm,宽度为0.5~1mm。
作为一种示例,硝酸纤维素膜03的长度为2cm至3cm,宽度为2.0mm至5.0mm;质控线032和检测线031间隔3mm~8mm,例如,质控线032和检测线031间隔4mm、5mm、6mm。
作为一种示例,本申请的适配体胶体金试纸还包括外壳,本申请的适配体胶体金试纸设置外壳中,外壳在样品垫01处开设有加样孔015,在硝酸纤维素膜03的检测线031和质控线032处开设有观察窗以便于观察检测线031和质控线032的颜色变化。
本申请检测新型冠状病毒n蛋白的适配体胶体金试纸由如下方法制备得到。
s1将新型冠状病毒n蛋白单抗按在硝酸纤维素膜上划线;将链霉亲和素蛋白多抗按在硝酸纤维素膜上划线。
s2得到包被了检测线和质控线的硝酸纤维素膜。
s3将新型冠状病毒n蛋白单抗与磷酸盐缓冲液混合,得到检测线包被溶液,用检测包被溶液在硝酸纤维素膜上划膜,在硝酸纤维素膜上包被检测线。
s4将样品垫结合物垫、硝酸纤维素膜和吸收垫依次固定在底板上,得到用于检测新型冠状病毒n蛋白的适配体胶体金试纸。
作为一种示例,步骤s1包括:
s1.1将氯金酸水溶液加热至沸腾,向沸腾的氯金酸水溶液中加入柠檬酸三钠溶液,继续煮沸至溶液呈酒红色,继续煮沸预设时长,停止加热,冷却后得到胶体金溶液,其中,氯金酸与柠檬酸三钠的质量比为1:0.9~1.2;溶液呈酒红色,继续煮沸的预设时长为8~15min。作为本申请的一个优选示例,氯金酸与柠檬酸三钠的质量比为1:1;溶液呈酒红色,继续煮沸的预设时长为10~12min。
s1.2向胶体金溶液中加入碳酸钾溶液,碳酸钾溶液的浓度为0.05~2mol/l,将胶体金溶液的ph值调节到6~6.5。
s1.3将链霉亲和素加入到胶体金溶液中,以胶体金溶液的体积分数计,向胶体金溶液中加入8%~15%的封闭液,静置第一预定时长,离心分离,向离心分离得到的沉淀物中加入胶体金重悬液,将沉淀物重新溶解至原胶体金溶液的九分之一到十分之一,得到胶体金标记的链霉亲和素重悬液。其中,封闭液为质量分数为100mg/ml的牛血清蛋白溶液,封闭液中还包括0.2mg/ml的叠氮化钠。
s1.4向胶体金标记的链霉亲和素溶液中加入生物素化的核酸适配体,孵育第二预定时长后,离心分离,向离心分离得到的沉淀物中加入胶体金重悬液,将沉淀物重新溶解至原胶体金溶液的九分之一到十分之一,得到链霉亲和素-生物素-核酸适配重悬液。
s1.5将结合物垫浸入到质量分数为1%~5%的牛血清蛋白溶液,干燥后备用。
其中,步骤s1.1制备得到的胶体金溶液中胶体金的粒径为25~35nm。
基于上述示例,一种可行的实施方式,步骤s1.3中将链霉亲和素加入到胶体金溶液中,链霉亲和素的加入量为30μg/ml~80μg/ml胶体金溶液,例如可以为35μg/ml、40μg/ml、45μg/ml、50μg/ml、55μg/ml、60μg/ml、65μg/ml、70μg/ml、75μg/ml。
基于上述示例,一种可行的实施方式,步骤s1.3中,第一预定时长为45~80min,例如可以为50min、60min、65min、70min、75min。
离心分离的转速为8000~12000rpm,离心分离的时间为15~25min,例如在10000rpm转速下,离心20min。
基于上述示例,一种可行的实施方式,步骤s1.4中,第二预定时长为10~20min,例如可以为11min、13min、15min、18min、19min。
离心分离的转速为8000~12000rpm,离心分离的时间为15~25min,例如在10000rpm转速下,离心20min。
基于上述示例,一种可行的实施方式中,步骤s1.6中,通过划膜机将链霉亲和素-生物素-核酸适配体重悬液在结合物垫上连续划线,以2~5μl/cm的划线速度链霉亲和素-生物素-核酸适配体结合到整个结合物垫上。
作为一种示例,本申请中选用的胶体金重悬液为含有0.7%~1.1%的tris-base、0.2%~0.4%的二水柠檬酸三钠、2.0%~5%的蔗糖、0.3%~0.8%的吐温20的重悬液。
作为一种示例,生物素化的核酸适配体包括核酸适配体48、核酸适配体58和核酸适配体88中的一种或多种。核酸适配体48的核苷酸序列如seqidno:1所示;核酸适配体58的核苷酸序列如seqidno:2所示;核酸适配体88的核苷酸序列如seqidno:3所示。
作为一种示例,步骤(3)具体包括以下步骤:(3.1)将新型冠状病毒n蛋白单抗与磷酸盐缓冲液混合,得到新型冠状病毒n蛋白单抗浓度为1~2mg/m的检测包被溶液,用划膜机构将检测包被溶液在硝酸纤维素膜上划膜,划膜速度为1μμl/cm~2μl/cm;(3.2)将链霉亲和素蛋白多抗与磷酸盐缓冲液混合,得到链霉亲和素蛋白多抗浓度为1~2mg/ml的质控包被溶液,用划膜机构将质控包被溶液在硝酸纤维素膜上划膜;质控包被溶液在硝酸纤维素膜上划膜的速度为1μl/cm~2μl/cm;(3.3)将硝酸纤维素膜置于温度30~40℃、湿度低于30%的环境中,干燥6-8小时。
其中,磷酸盐缓冲液的浓度为0.1~0.3mol/l。
作为一种示例,本申请的适配体胶体金试纸的制备方法,还包括处理样品垫的步骤a):用胶体金重悬液和质量分数为1%~5%的牛血清蛋白血清溶液依次喷涂样品垫,再将样品烘干后备用。
以下对本发明的检测新型冠状病毒n蛋白的适配体胶体金试纸进行举例说明。
实施例1
本申请的检测新型冠状病毒n蛋白的适配体胶体金试纸的制备
s1)胶体金制剂的制备
s1.1量取1000ml纯化水,煮沸后加入氯化金水溶液配制成质量分数为0.04%的氯金酸溶液;待溶液再次沸腾后,加入10ml柠檬酸三钠溶液,柠檬酸三钠溶液的浓度为1mol/l,继续煮沸,观察溶液颜色由黄色变成黑色再变成紫色,最后成稳定的酒红色后,计时继续煮沸10分钟,停止加热,待溶液冷却至室温后,加入纯化水补充至1000ml。制备得到的胶体金溶液中胶体金的粒径约为30nm。其中,氯金酸与柠檬酸三钠的质量比为1:0.9~1.2。
s1.2向胶体金溶液中加入1mol/l的碳酸钾溶液8μl,将胶体金溶液的ph值调节到6。
s1.3将50μg链霉亲和素加入到1ml胶体金溶液中,链霉亲和素的加入量为50μg/ml胶体金溶液,再向胶体金溶液中加入10μl质量分数为100mg/ml的牛血清蛋白溶液,牛血清蛋白溶液中含有0.2mg/ml的叠氮化钠,静置1小时后,10000rpm离心20min,向离心分离得到的沉淀物中加入90μl胶体金重悬液,得到胶体金标记的链霉亲和素重悬液。
s1.4向胶体金标记的链霉亲和素溶液中加入比例为1:1:1的生物素化的核酸适配体48、生物素化的核酸适配体58、生物素化的核酸适配体88,加入量为40μg,孵育20min后,10000rpm离心20min,离心得到链霉亲和素-生物素-核酸适配体沉淀,向离心分离得到的沉淀物中加入90μl胶体金重悬液使其重新溶解,得到胶体金标记的链霉亲和素-生物素-核酸适配体重悬液。
s1.5将准备好的结合物垫浸入到质量分数为1%的牛血清蛋白溶液中,干燥后备用。其中,结合物垫可以为玻璃纤维垫。
s2结合物垫喷金
通过划膜机将链霉亲和素-生物素-核酸适配体在结合物垫上连续划线,以3μl/cm的划线速度链霉亲和素-生物素-核酸适配体结合到整个结合物垫上,烘干后得到结合物垫。
s3硝酸纤维素膜的制备
s3.1将新型冠状病毒n蛋白单抗与0.1mol/l的磷酸盐缓冲液混合,得到检测包被溶液,检测包被溶液中新型冠状病毒n蛋白单抗的浓度为1~2mg/ml;
s3.2将链霉亲和素蛋白多抗与0.1mol/l的磷酸盐缓冲液混合,得到质控包被溶液,质控包被溶液中链霉亲和素蛋白多抗的浓度为1~2mg/ml;
s3.3将检测包被溶液加入连续划膜机的1号杯;将质控线包被溶液加入连续划膜机的2号杯;调试连续划膜机以1μl/cm的速度在硝酸纤维素膜上划线,在硝酸纤维素膜上包被检测线和质控线。
s3.4将硝酸纤维素膜置于温度37℃、湿度低于30%的环境中,干燥6小时。
s4样品垫的处理
将胶体金重悬液喷涂在样品垫上,将样品垫完全浸透后,将样品垫静置3~10min;再用质量分数为2%的牛血清蛋白溶液喷涂样品垫,将样品烘干后备用。其中,样品垫可以为玻璃纤维垫。
s5组装
将样品垫、结合物垫、硝酸纤维素膜和吸收垫依次固定在底板上,吸收垫为吸水纸,得到用于检测新型冠状病毒n蛋白的适配体胶体金试纸。
实施例2
对实施例1制备得到的适配体胶体金试纸进行检测
将待测样品滴加在试纸的样品垫上,将试纸水平静置10~15min,处于试纸另一侧的吸水垫吸取待测样品向结合物垫流动。
如果待测样品中存在新型冠状病毒,则新型冠状病毒中的n蛋白与结合物垫上的胶体金标记的适配体探针反应,并沿着硝酸纤维素膜层析,分别与检测线和质控线反应,然后硝酸纤维素膜层析的检测线和质控线均变色,则待测样品中存在新型冠状病毒,检测结果为阳性。
如果待测样品中不存在新型冠状病毒,则试纸无变色,则待测样品中不存在新型冠状病毒,检测结果为阴性。
实施例3
检测对实施例1制备得到的试纸条进行灵敏度测试
用咽拭子保存液将新型冠状病毒n蛋白(北京安必奇生物科技有限公司生产,货号c010204)以分别稀释成4000ng/ml、800ng/ml、160ng/ml、32ng/ml、6.4ng/ml、1.28ng/ml、0.256ng/ml并分别滴加在本申请权利要求1制备得到的试纸的样品垫上,将试纸静置10~15min,检测结果如表1所示。以质量分数计,咽拭子保存液包括以下组分:hepes0.1m/l、triton-x1001%、酚红0.5%或者tween-201%,脱养胆酸钠0.5%,bsa1%。ph7.0。
表1本申请的检测新型冠状病毒n蛋白的适配体胶体金试纸灵敏度测试
根据表1可以看出,本申请的检测新型冠状病毒n蛋白的适配体胶体金试纸可检测到n蛋白浓度为1.28ng/ml的样品溶液,灵敏度高。
实施例4
用棉签采集待测试样品后,将棉签头折下放入到收集管中,收集管为一端渐缩的锥形管,棉签头放入到收集管中向收集管中滴加数滴咽拭子保存液,静置3~5min以使待测试样品充分裂解,用吹气气球向收集管中吹气,将裂解液吹到试纸的样品垫上。
以质量分数计,咽拭子保存液包括以下组分:hepes0.1m/l、triton-x1001%、酚红0.5%或者tween-201%,脱氧胆酸钠0.5%,bsa1%。ph7.0。
待测试样品为用咽拭子保存液将新型冠状病毒n蛋白(北京安必奇生物科技有限公司生产,货号c010204)以稀释成不同浓度梯度的n蛋白溶液以及采集到的阴性咽拭子样品。检测结果入表2所示。
表2
根据表2可以看出,用本申请的试纸条分别对10组n蛋白溶液和10组阴性咽拭子样品进行检测,10组阴性样品全部检测为阴性,检测结果与实际一致,没有出现错误结果。10组n蛋白溶液的检出率为9组,检出为阳性。
实施例5
交叉反应试验
选择8种常见的咽拭子病毒稀释成菌悬液,分别测试本申请的适配体胶体金试纸,具体检测方法与实施例4相同。测试结果如表3所示:
表3本申请的适配体胶体金试纸条的交叉反应测试
根据表3的测试结果所示,本发明的适配体胶体金试纸对于新型冠状病毒n蛋白的检测特异性好,对于人体常见的病毒没有交叉反应。
实施例6
干扰检测试验
在实际临床检测过程中,病人难免会服用一些小分子药物,而这些药物如果浓度过高则会对检测造成干扰,使其呈现假阳结果。用生活中使用率较高的几种内外科药物,分别检测本申请的试纸,检测结果如表3所示。
表4本申请的检适配体胶体金试纸的干扰反应测试
根据表3可以看出,本申请的试纸条受到多种药物影响的临界值很高,通常人体用药无法达到本本申请试纸条的临界值,本申请的试纸条在临床应用过程中不易受到药物干扰,检测结果准确,能够有效排除假阳性,检测结果更加可靠。
根据本申请实施例可以看出,本申请的适配体胶体金试纸对于新型冠状病毒n蛋白具有较高的灵敏性和优良的特异性,对于人体常见的病毒没有交叉反应,对于人体内可达到的内外科药物浓度无干扰反应。适用于新型冠状病毒的检测。
需要说明的是,在本文中,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种物品或者设备所固有的要素。在没有更多限制的情况下,由语句“包括……”限定的要素,并不排除在包括所述要素的物品或者设备中还存在另外的相同要素。
以上实施例仅用以说明本发明的技术方案而非限制,仅仅参照较佳实施例对本发明进行了详细说明。本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的精神和范围,均应涵盖在本发明的权利要求范围当中。
序列表
<110>北京安必奇生物科技有限公司
<120>一一种检测新型冠状病毒n蛋白的适配体胶体金试纸及其制备方法
<130>012002508
<141>2020-10-28
<160>4
<170>siposequencelisting1.0
<210>1
<211>58
<212>dna
<213>artificialsynthesis
<400>1
gctggatgtcgcttacgacaatattccttaggggcaccgctacattgacacatccagc58
<210>2
<211>58
<212>dna
<213>artificialsynthesis
<400>2
gctggatgtcaccggattgtcggacatcggattgtctgagtcatatgacacatccagc58
<210>3
<211>88
<212>dna
<213>artificialsynthesis
<400>3
gcaatggtacggtacttccggatgcggaaactggctaattggtgaggctggggcggtcgt60
gcagcaaaagtgcacgctactttgctaa88
<210>4
<211>419
<212>prt
<213>artificialsynthesis
<400>4
metseraspasnglyproglnasnglnargasnalaproargilethr
151015
pheglyglyproseraspserthrglyserasnglnasnglygluarg
202530
serglyalaargserlysglnargargproglnglyleuproasnasn
354045
thralasertrpphethralaleuthrglnhisglylysgluaspleu
505560
lyspheproargglyglnglyvalproileasnthrasnserserpro
65707580
aspaspglnileglytyrtyrargargalathrargargilearggly
859095
glyaspglylysmetlysaspleuserproargtrptyrphetyrtyr
100105110
leuglythrglyproglualaglyleuprotyrglyalaasnlysasp
115120125
glyileiletrpvalalathrgluglyalaleuasnthrprolysasp
130135140
hisileglythrargasnproalaasnasnalaalailevalleugln
145150155160
leuproglnglythrthrleuprolysglyphetyralagluglyser
165170175
argglyglyserglnalaserserargserserserargserargasn
180185190
serserargasnserthrproglyserserargglythrserproala
195200205
argmetalaglyasnglyglyaspalaalaleualaleuleuleuleu
210215220
aspargleuasnglnleugluserlysmetserglylysglyglngln
225230235240
glnglnglyglnthrvalthrlyslysseralaalaglualaserlys
245250255
lysproargglnlysargthralathrlysalatyrasnvalthrgln
260265270
alapheglyargargglyprogluglnthrglnglyasnpheglyasp
275280285
glngluleuileargglnglythrasptyrlyshistrpproglnile
290295300
alaglnphealaproseralaseralaphepheglymetserargile
305310315320
glymetgluvalthrproserglythrtrpleuthrtyrthrglyala
325330335
ilelysleuaspasplysaspproasnphelysaspglnvalileleu
340345350
leuasnlyshisileaspalatyrlysthrpheproprothrglupro
355360365
lyslysasplyslyslyslysalaaspgluthrglnalaleuprogln
370375380
argglnlyslysglnglnthrvalthrleuleuproalaalaaspleu
385390395400
aspasppheserlysglnleuglnglnsermetserseralaaspser
405410415
thrglnala
- 还没有人留言评论。精彩留言会获得点赞!