一种痛风动物模型的构建方法及应用与流程
本发明涉及一种动物模型技术领域,具体涉及一种痛风动物模型的构建方法与应用。
背景技术:
痛风(gout)是一种与高尿酸血症相关的炎症性疾病,主要表现为反复发作的痛风性关节炎、尿酸性尿路结石和痛风性肾病等。随着生活方式的改变,我国痛风和高尿酸血症的患病率显着增加,估计高尿酸血症患者可达1.8亿,痛风性关节炎患者在3000万以上。痛风的发作极度痛苦,严重威胁着人们的健康生活。
痛风性关节炎的相关研究需要借助具有痛风类似表现的动物模型进行。然而,目前可供使用的痛风模型还存在许多不足之处。coderre等发明了关节局部注射的方法建立了痛风模型。这种方法主要将单钠尿酸盐(monosodiumurate,msu)悬液直接注射到大鼠的关节腔内造成急性炎症关节炎,类似于痛风发病;近年发现,coderre法建立的关节炎实质上属于非特异性炎症,与局部注射蛋清等异物引起的炎症反应没有本质区别,不同于人类因高尿酸血症所形成的痛风性关节炎。由于兔、鼠等常用模型动物的体内均存在尿酸酶,可以分解尿酸,外周血中没有尿酸存在,这种关节炎发病特点、病理表现均与人体痛风不符;并且关节炎发病与血尿酸无关,割裂了痛风与高尿酸血症的关系,没有真正模拟出痛风的特点。
我国学者分别采用次黄嘌呤或尿酸酶抑制剂氧嗪酸等构建高尿酸血症模型,再在其基础之上,向关节腔内注射msu,建立痛风动物模型。这种改良模型虽然同时具备了高尿酸血症与关节炎等痛风的表现,但高尿酸血症仍不稳定且与关节炎之间非因果关系,尚不能准确评价抗痛风药物的效果和作用机制。有学者发现也存在因为高尿酸血症引起痛风自然发病的禽类。但是关节炎特点与人体不符,并且鸟类与哺乳类动物的尿酸代谢存在种群差异。因此鸟类作为痛风性关节炎的动物模型有其局限性。
高尿酸血症是痛风的发病基础,尿酸的主要致病形式是msu,白细胞介素1β(il-1β)是诱发痛风性关节炎的主要细胞因子。尿酸沉积在关节中形成msu后,在关节滑液蛋白质的协助下可以刺激il-1β分泌,引起痛风发作。在痛风发病过程中,msu需要被膜结合受体(如toll样受体)和细胞内受体(如nod样受体)识别,通过激活不同的信号通路才能刺激il-1β分泌。在nod样受体中,nalp3炎症小体能够通过其富含亮氨酸的重复序列结构域识别并结合msu,在痛风发病中起关键作用,并且nalp3炎症小体可以与toll样受体协同作用,共同促进单核/巨噬细胞分泌il-1β,引起急性痛风性关节炎发病。
痛风必伴有高尿酸血症,复制出可持续的高尿酸血症模型是建立痛风动物模型的前提。近年来,研究者采用大剂量含嘌呤物质、尿酸酶抑制剂、或者加用抑制尿酸排泄药物等不同办法,成功构建了各种高尿酸血症模型,但均未出现自发痛风性关节炎的报道。在敲除尿酸酶基因获得的持续高水平血尿酸的动物模型中,也未见有痛风发病的报道。提示在刺激痛风发病时,仅有msu是不够的,应该还存在其他诱导il-1β分泌的致病信号,它们与msu协同作用,共同刺激痛风性关节炎发病。
除了msu外,il-1β分泌受多种信号通路调控,其中值得关注的是atp-嘌呤受体p2x配体门控的离子通道7(p2x7r)-il-1β信号通路。实验表明,atp不仅是能量的载体,也可作为刺激信号作用于p2x7r,导致k+外流,进而刺激nalp3炎症小体活化和il-1β分泌。急性痛风性关节炎发病的主要诱发因素包括过度劳累、寒冷、饮酒、暴饮暴食等;这些诱发因素引起机体的生理变化中均存在atp剧烈波动,例如剧烈运动可以促进atp释放增加;寒冷时机体出现适应性发热反应,可以使atp增加。因此在msu刺激nalp3炎症小体不足以诱导引起关节炎发病的足量il-1β分泌时,atp的变化可以通过刺激p2x7r信号通路,协同msu刺激nalp3炎症小体,导致il-1β分泌急剧增加,引起急性痛风性关节炎发病。
高尿酸血症患者的msu激活nalp3炎症小体诱导分泌的il-1β不足以引起痛风发病;只有在atp的协同作用下,只有机体对atp刺激分泌il-1β的能力增强时,才能充分激活nalp3炎症小体引起足量il-1β分泌,导致痛风发病;也就是说msu和atp共同参与了痛风性关节炎的发病。
基于这一新机制,我们进行了atp和尿酸协同的动物模型构建。
技术实现要素:
本发明的目的在于基于我们提出的痛风性关节炎发病的新机制,提供一种能够稳定高效的构建具有痛风症状的动物模型的方法,使该动物模型可以应用于痛风的相关研究。
为达到上述目的,本发明第一方面提供一种痛风动物模型构建方法,其包括:
用尿酸酶抑制剂处理实验动物,制备高尿酸动物模型;使用尿酸盐晶体悬液和atp溶液同时处理所述高尿酸动物。
在前述第一方案的一些实施例中,可选用大鼠建立高尿酸动物模型。
优选地,所述尿酸酶抑制剂处理大鼠的时间为每天一次,持续6~9天。
在前述第一方面的一些实施例中,所述尿酸酶抑制剂可选用氧嗪酸溶液。
优选地,所述氧嗪酸以腹腔注射的方式处理大鼠。
优选地,所述氧嗪酸的注射量以大鼠的质量为标准,为每次15.2~36.5mg/100g,持续7天。
在前述第一方面的一些实施例中,所述尿酸盐晶体悬液和atp溶液对大鼠的刺激方式为尾静脉注射。
可选地,所述尿酸盐晶体悬液的浓度为0.1g/ml,注射剂量为31~112μl/只。
可选地,所述atp溶液的浓度为2.4~13.3mm,注射剂量为3.0~12.5ml/只。
在本实施例中,使用尿酸盐晶体悬液和atp溶液以前述的浓度和剂量协同刺激大鼠,可以成功建立稳定的痛风动物模型,此模型可高度模拟人痛风性关节炎的痛风症状和痛风相关炎症机理。
本发明第二方面提供痛风动物模型的构建方法得到的痛风动物模型在相关疾病研究中的应用。
在上述技术方案中,研究内容可以是痛风相关疾病的机制、药物筛选和治疗方法的研究。
有益效果
本发明首次提供了稳定高效接近人类痛风特点的痛风动物模型构建方法,通过对实验动物进行尾静脉atp和尿酸盐晶体的协同刺激,实验大鼠出现了典型的痛风症状:自发出现关节红肿,24小时达高峰,1-2周内左右自行缓解。实验大鼠的发病关节在偏光显微镜下可以观察到大量的尿酸盐晶体沉积,免疫组化检测发现发病组织中有大量的中性粒细胞浸润,证实基于我们提出的新机制成功构建了痛风大鼠模型,该模型可后续用于痛风相关疾病的机制、药物效果评价、治疗方法等研究。
附图说明
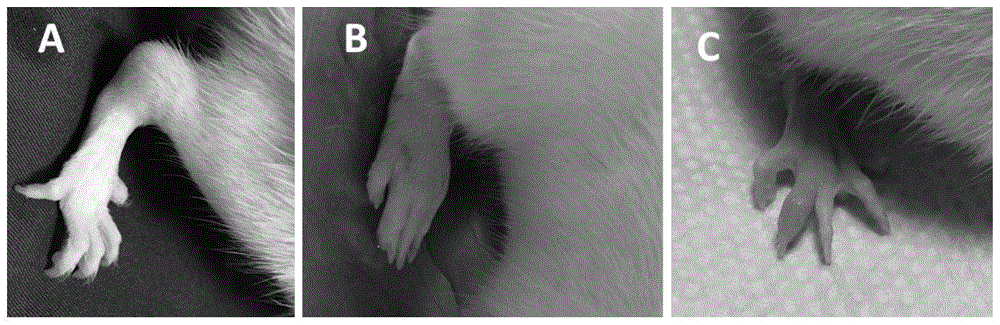
图1是本发明所述实验动物发病前后关节对比,其中图a为正常大鼠关节,图b为coderre法痛风模型的大鼠关节,图c为基于本发明的方法建立的痛风大鼠关节。
图2是本发明痛风模型的部分大鼠关节炎表现(其中包括1-12号大鼠)。
图3是发病实验动物关节切片在偏光显微镜下观察到的尿酸盐结晶。
图4是发病实验动物的关节切片he染色,其中,图k(×100)、图l(×400)为新机制痛风模型的关节组织he染色结果;图m(×100)、图n(×400)为coderre法痛风模型大鼠关节he染色结果。高倍镜下显示,图l中的细胞主要为分叶状细胞核的中性粒细胞,图n中的细胞主要为圆形细胞核的淋巴细胞。
图5是发病实验动物的关节切片荧光染色共聚焦照片,其中dapi为染核,his48标记中性粒细胞,cd3标记t细胞,merge后的结果显示实验动物关节切片中主要为中性粒细胞,少量的t细胞。
具体实施方式
通过解释以下本申请的优选实施方案,本发明的其他目的和优点将变得清楚。
应理解本发明中所述的术语仅仅是为描述特别的实施方式,并非用于限制本发明。另外,对于本发明中的数值范围,应理解为还具体公开了该范围的上限值和下限值之间的每个中间值。在任何陈述值或陈述范围内的中间值以及任何其他陈述值或在所述的范围内的中间值之间的每个较小的范围也包括在本发明内。这些较小范围的上限值和下限值可独立地包括或排除在范围内。
实施例中所使用的试剂主要包括分子生物学实验试剂和试剂盒等,均可通过商业途径获得,具体包括:尿酸酶抑制剂氧嗪酸、尿酸盐晶体和atp均购买于sigma公司,尿酸试纸和尿酸仪均购于北京会好生物科技有限公司,实验大鼠和饲料均购买于合肥庐阳区义东生物用品经营部。本发明实施例中所提供的方法如果没有特殊说明均为常规方法。
实施例1
本实施例提供一种痛风动物模型的构建方法
一、建立痛风大鼠模型
1.将体重为180-220g的雄性大鼠分为三组,包括正常组,coderre法痛风模型组,本发明模型组;每组10只。
2.根据大鼠体重向大鼠腹腔注射尿酸酶抑制剂,注射剂量为30mg/100g体重,固定注射时间,每天一次,持续7天;
3.一周后用尿酸试纸检测大鼠体内尿酸含量,对尿酸值高于180μmol/l的大鼠进行后续试验;
4.确认大鼠体内处于高尿酸状态后,第一天对高尿酸大鼠尾静脉注射浓度为0.1g/ml的尿酸盐晶体悬液,剂量为50μl/只;
5.第二天检测大鼠体内尿酸含量,再次向大鼠尾静脉注射浓度为0.1g/ml的尿酸盐晶体悬液,剂量为50μl/只,尾静脉注射atp溶液10mm,0.5ml/只;
二、检测痛风大鼠模型的造模效果
1.观察大鼠发病情况,纪录病程。
2.对痛风模型大鼠发病关节进行切片,用偏光显微镜检查关节切片中的尿酸盐晶体,用he方法检测切片组织内炎症细胞浸润程度,用荧光染色共聚焦法进一步检测切片组织内炎症细胞类型和浸润程度。
如图1和图2所示的观察结果表明,本发明提供的方法建立的痛风大鼠模型,其关节肿胀程度比coderre法痛风大鼠更符合人类自发性痛风的发病症状,具有明显的优势。
如图3-5所示的检测结果表明,相对于coderre法痛风大鼠模型,本发明提供的方法所建立的痛风模型,关节中浸润着主要为分叶状细胞核的中性粒细胞,而coderre法痛风模型大鼠关节中的细胞主要为圆形细胞核的淋巴细胞。本发明基于新机制建立的痛风动物模型更接近人类痛风发病过程中的炎症信号的发生和发展,是一种更好的痛风药物筛选,相关机制研究的工具。
以上显示和描述了本发明的基本原理、主要特征和本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明精神和范围的前提下,本发明还会有各种变化和改进,本发明要求保护范围由所附的权利要求书、说明书及其等效物界定。
- 还没有人留言评论。精彩留言会获得点赞!