一种新型冠状病毒N蛋白提取保存液及其制备方法和应用与流程
本发明属于体外诊断领域,涉及一种新型冠状病毒n蛋白提取保存液及其制备方法和应用。
背景技术:
为了满足疫情防控需要,提升便捷程度,提高检测准确度,实现疑似患者的快速诊断和密切接触人群的现场筛查,需要快速进行核酸、抗体和抗原的快速检测试剂的开发,同时为提高检测的准确性,样本提取的后处理及保存显得尤为重要。
技术实现要素:
有鉴于此,本发明的主要目的在于提供一种新型冠状病毒n蛋白提取保存液及其制备方法和应用。
为了实现上述目的,本发明提供了一种新型冠状病毒n蛋白提取保存液,1l新型冠状病毒n蛋白提取保存液包括以下各组分:
余量为缓冲液。
在本发明的一个具体方案中,其中所述缓冲液选自tris-hcl缓冲液、pb缓冲液和巴比妥钠-盐酸缓冲液中的一种。
在本发明的一个具体方案中,其中所述缓冲溶液的浓度范围为0.005~0.1m。
在本发明的一个具体方案中,其中所述缓冲溶液的浓度范围为0.01~0.05m,通过该浓度的缓冲溶液处理后,大部分病毒细胞发生破裂,新冠病毒细胞内部n蛋白裸露程度增加。
在本发明的一个具体方案中,其中所述缓冲溶液的浓度为0.02m,通过该浓度的缓冲溶液处理后,病毒细胞发生破裂几乎全部破裂,新冠病毒细胞内部n蛋白裸露程度增加,提高检测结果的准确度。
为了实现上述目的,本发明还提供了一种新型冠状病毒n蛋白提取保存液的制备方法,包括以下步骤:将配方量的酪蛋白、抗生素、牛血清白蛋白、乙基苯基聚乙二醇、抗红细胞单克隆抗体、生物防腐剂和缓冲液混合均匀,即得所述新型冠状病毒n蛋白提取保存液。
为了实现上述目的,本发明还提供了一种新型冠状病毒n蛋白提取保存液的使用方法,包括以下步骤:在塑料软管、样品杯或试剂杯中加入0.2~2ml提取保存液,将采集的样本加入到上述提取保存液中,混合均匀后,将含有样本的提取保存液在2~8℃下保存或者直接取30~100μl用于免疫检测。
在本发明的一个具体方案中,其中所述样本选自鼻拭子、咽拭子、口腔拭子、唾液、痰液或肺泡灌洗液中的一种。
在本发明的一个具体方案中,其中所述免疫检测选自化学发光、酶联免疫、免疫层析、磁微粒化学发光、电化学免疫和质谱免疫中的一种。
本发明的有益效果为:
1、本发明所提供的新型冠状病毒提取保存液,其对鼻拭子、咽拭子、口腔拭子、肺泡灌洗液、痰液、唾液等不同样本具有较好的兼容性,为病毒样本提供了一个合适稳定的缓冲环境,利于样本检测和保存;并且样本加入该提取保存液中,无需将样本洗涤和重新提取,直接可用于检测。
2、本发明所提供的新型冠状病毒提取保存液,其能够降低检测过程中的非特异性吸附,进而提高检测灵敏度和特异性。
3、本发明所提供的新型冠状病毒提取保存液,其通过利用渗透压使新型冠状病毒细胞吸水肿胀破裂,以将新型冠状病毒n蛋白从细胞内充分暴露出来,进而可以通过检测个体样本中新型冠状病毒n蛋白的含量进行新型冠状病毒肺炎诊断,并能进一步提高检测结果的灵敏度和准确性。。
附图说明
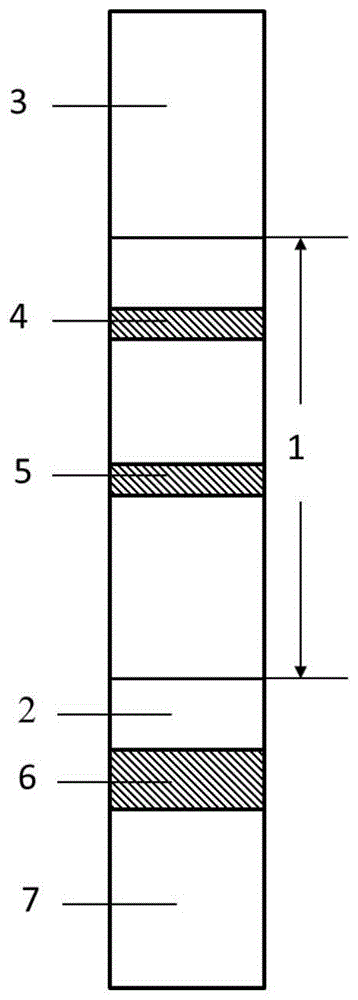
图1为本发明所提供的快速检测新型冠状病毒n蛋白的免疫层析试纸条示意图;
图2a为本发明所提供的快速检测新型冠状病毒n蛋白的免疫层析检测卡中一种上盖的内部结构示意图;
图2b为本发明所提供的快速检测新型冠状病毒n蛋白的免疫层析检测卡中一种底槽的内部结构示意图;
其中,1-包被垫,2-标记物垫,3-吸水垫,4-质控线,5-检测线,6-标记物结合处,7-样品垫,8-上盖,9-底槽,10-加样孔,11-观察窗,12-试纸条放置区域,13-定位柱,14-定位孔,15-第一限定部,16-第二限定部,17-第三限定部。
具体实施方式
下面结合具体实施例对本发明进行进一步说明。
以下材料或试剂,除非特别说明,均为市售。
实施例1新型冠状病毒n蛋白提取保存液的配制
几种1l新型冠状病毒n蛋白提取保存液的配制如表1所示。
牛血清白蛋白
表1
0.2mna2hpo4缓冲溶液和0.2mnah2po4缓冲溶液的配制如下表2所示。
表2
0.01mpb缓冲溶液的配制如下表3所示。
表3
0.02mpb缓冲溶液的配制如下表4所示。
表4
0.05mpb缓冲溶液的配制如下表5所示。
表5
0.1mpb缓冲溶液的配制如下下表6所示。
表6
0.15mpb缓冲溶液配制如下表7所示。
表7
实施例2新型冠状病毒n蛋白免疫层析检测试剂盒的制备
1)采用荧光微球标记另一株鼠抗新型冠状病毒n蛋白单克隆抗体
取0.5ml荧光微球加入1mg碳化二亚胺(edc),1mgn-羟基琥珀酰亚胺(nhs),于室温,120r/min的转速下搅拌3h,然后加入100μl另一株鼠抗新型冠状病毒n蛋白单克隆抗体,于室温,120r/min的转速下搅拌1h,再加入10mgbsa封闭液,继续以120r/min的转速搅拌1h。在2~8℃下,按照12000r/min的转速离心20min,除去上清液。最后,用0.2m的磷酸盐缓冲液(ph=7.4)将离心后获得的固体沉淀物复溶至1ml,再加入1μl的proclin300在4℃下保存待用。
2)采用荧光微球标记兔igg多克隆抗体
取0.5ml荧光微球加入1mg碳化二亚胺(edc),1mgn-羟基琥珀酰亚胺(nhs),于室温,120r/min的转速下搅拌3h,然后加入100μlmg羊兔igg多克隆抗体,于室温,120r/min的转速下搅拌1h,再加入10mgbsa封闭液,继续以120r/min的转速搅拌1h。在2~8℃下,按照11000r/min的转速离心30min,除去上清液。最后,用0.2m的磷酸盐缓冲液(ph=7.4)将固体沉淀物复溶至1ml,再加入1μl的proclin300在4℃下保存待用。
3)包被垫的制备
将一株鼠抗新型冠状病毒n蛋白单克隆抗体和羊抗兔多克隆抗体分别用0.2m的磷酸盐缓冲液(ph=7.4)稀释成1mg/ml,用划膜喷金仪在硝酸纤维素膜(nc膜)上进行划膜。含有一株鼠抗新型冠状病毒n蛋白单克隆抗体的作为检测线(t线)5,含有羊抗兔多克隆抗体的作为质控线(c线)4,然后在37℃,湿度<30%的环境下干燥4h制成包被垫1。
4)标记物垫的制备
①将玻璃纤维素膜在0.2m的磷酸盐缓冲液(ph=7.4)中浸泡6h,然后在35℃下干燥8h,备用。
②将摩尔比为1:1的荧光微球标记的一株鼠抗新型冠状病毒n蛋白单克隆抗体和荧光微球标记的兔igg标记的荧光乳胶微球混合均匀后,按照10μl/cm的速度喷涂在玻璃纤维素膜上,然后放置在45℃下干燥2h制成标记物垫2。标记物垫2上包被有荧光微球标记的一株鼠抗新型冠状病毒n蛋白单克隆抗体和荧光微球标记的兔igg的地方叫做标记物结合处6。
5)免疫层析检测试剂盒的组装
首先在pvc板(图中未示出)上粘接包被垫1,然后在靠近包被垫1上的质控线4的一端搭接吸水垫3,在靠近包被垫1的检测线5的一端搭接标记物垫2及其连接的样品垫7,用切条机切成4mm±0.1mm的试纸条(见图1),将试纸条放入卡壳中制备成新型冠状病毒n蛋白免疫层析检测试剂盒。
所述卡壳选自现有技术,例如,所述卡壳(如图2所示)可以包括:底槽12,其连接于所述pvc板;上盖8,其连接于所述底槽9,所述上盖8上设置有用于向所述样品垫7上加样的加样孔10;观察窗11,其设置于上盖8上,用于检测线5和质控线4的数据采集。
如图2b所示,所述底槽9包括:位于其内表面的对称分布的多个定位孔14,多个所述定位孔14之间设有多个用于限定试纸条横向移动的第一限定部15以及用于限定试纸条纵向移动的第二限定部16;对称设置的所述第一限定部15与所述第二限定部16围设成试纸条放置区域12(虚线区域),用于放置试纸条;
如图2a所示,所述上盖8包括:与多个所述定位孔14相配合的多个定位柱13,这样配合使用以将上盖8和底槽9固定在一起;所述上盖8还包括用于限定试纸条的上下移动的第三限定部17。
所述包被垫1的上方设有用于数据采集的观察窗11,以露出全部所述检测线5和质控线4,用于收集其检测结果;且所述观察窗11开设于所述上盖8上与试纸条放置区域12的中部相对应的位置。所述上盖8在与所述样品垫7相对应的位置处开设有加样孔10,以用于样品垫7上滴加样本。所述检测线5距离加样孔15-25mm。
实施例3检测
收集13例确诊新型冠状病毒肺炎患者的咽拭子样本,分别用实施例1中制备的a、b、c、d、e5种新型冠状病毒n蛋白提取保存液处理样本,具体处理方式为:将采集咽拭子样本后的棉棒浸在提取保存液中并搅拌;用手指挤压塑料软管外侧多次,使提取保存液充分浸透棉棒,然后拔出棉棒,绞出(即将棉棒上采集的样本混合到提取保存液中)的液体即为待测样本。然后取60μl待测样本采用实施例2所述的新型冠状病毒n蛋白免疫层析试剂盒进行检测,将待测样本滴加到试剂盒加样孔处,静置15min,然后插入荧光免疫层析分析仪进行检测,仪器自动计算出样本t/c值,通过与正常值范围判断阴阳性;或者当在紫外灯照射下呈现出两条荧光条带时,即为阳性,检测结果如下表8中所示。
表8
从表8中可以看出,13例新型冠状病毒阳性患者的咽拭子样本经提取保存液a处理后,其中11例检测为阳性,阳性检出率为84.6%;13例新型冠状病毒阳性患者的咽拭子样本经提取保存液b处理后,其中11例检测为阳性,阳性检出率为84.6%;13例新型冠状病毒阳性患者的咽拭子样本经提取保存液c处理后,其中9例检测为阳性,阳性检出率为69.2%;13例新型冠状病毒阳性患者的咽拭子样本经提取保存液d处理后,其中6例检测为阳性,阳性检出率为46.1%;13例新型冠状病毒阳性患者的咽拭子样本经提取保存液e处理后,其中1例检测为阳性,阳性检出率为7.6%。由此可以看出,通过逐渐降低缓冲液的摩尔浓度,使得检测的准确性逐渐提高。这是由于当新型冠状病毒细胞内渗透压大于外界环境时,缓冲溶液中的水会逐渐向细胞内部扩散,当超过细胞膜的最大承受能力时,会使细胞发生破裂,使得新型冠状病毒n蛋白从细胞内充分暴露出来,进而能够提高检测结果的准确性。从表8中测得t/c数据可以看出,当缓冲液浓度为0.15m时,t/c很低,说明此时病毒细胞内外渗透压相当,几乎不发生破裂;当缓冲液浓度为0.1m和0.05m时,t/c值逐渐增大,说明病毒细胞大部分发生破裂;当缓冲液浓度为0.02m和0.01m时,t/c值相当,说明病毒细胞已经完全破裂,新型冠状病毒n蛋白充分暴露出来,进而进一步提高检测结果的准确度准度。
实施例4
1、1l新型冠状病毒n蛋白提取保存液的配制如表9所示。
表9
2、收集9例确诊新型冠状病毒肺炎患者的鼻拭子样本,分别用实施例4步骤1中制备的提取保存液处理样本,具体处理方式为:将采集鼻拭子样本后的棉棒浸在提取保存液中并搅拌;用手指挤压塑料软管外侧多次,使提取保存液充分浸透棉棒,然后拔出棉棒,绞出(即将棉棒上采集的样本混合到提取保存液中)的液体即为待测样本。然后取60μl待测样本采用实施例2所述的新型冠状病毒n蛋白免疫层析试剂盒进行检测,将待测样本滴加到试剂盒加样孔处,静置15min,然后插入荧光免疫层析分析仪进行检测,仪器自动计算出样本t/c值,通过与正常值范围判断阴阳性;或者当在紫外灯照射下呈现出两条荧光条带时,即为阳性,检测结果如下表10中所示。
表10
从表10的临床检测数据可以看出,9例新型冠状病毒阳性样本经样本提取液处理后5例检测为阳性,4例检测为阴性,阳性检出率为55%;9例新型冠状病毒阳性样本经0.05mpb缓冲溶液处理后3例检测为阳性,6例检测为阴性,阳性检出率为33%,表明经样本提取液处理后能够提高检测结果的准确性。
实施例5
1、1l新型冠状病毒n蛋白提取保存液的配制如表11所示。
表11
2、收集9例确诊新型冠状病毒肺炎患者的咽拭子样本,分别用实施例4步骤1中制备的提取保存液处理样本,具体处理方式为:将采集咽拭子样本后的棉棒浸在提取保存液中并搅拌;用手指挤压塑料软管外侧多次,使提取保存液充分浸透棉棒,然后拔出棉棒,绞出(即将棉棒上采集的样本混合到提取保存液中)的液体即为待测样本。然后取60μl待测样本采用实施例2所述的新型冠状病毒n蛋白免疫层析试剂盒进行检测,将待测样本滴加到试剂盒加样孔处,静置15min,然后插入荧光免疫层析分析仪进行检测,仪器自动计算出样本t/c值,通过与正常值范围判断阴阳性;或者当在紫外灯照射下呈现出两条荧光条带时,即为阳性,检测结果如下表12中所示。
表12
从表12的临床检测数据可以看出,9例新型冠状病毒阳性样本经样本提取液处理后6例检测为阳性,3例检测为阴性,阳性检出率为67%;9例新型冠状病毒阳性样本经样本提取液处理后4例检测为阳性,5例检测为阴性,阳性检出率为44%,表明经样本提取液处理后能够提高检测结果的准确性。
以上所述实施例仅是为充分说明本发明而所举的实施例,本发明的保护范围不限于此。本技术领域的技术人员在本发明基础上所作的等同替代或变换,均在本发明的保护范围之内。本发明的保护范围以权利要求书为准。
- 还没有人留言评论。精彩留言会获得点赞!