一种吡虫啉复合载药微球的制备方法与流程
本发明属于农药载体的制备技术领域,具体涉及一种吡虫啉复合载药微球的制备方法。
背景技术:
常规剂型农药成分释放速度快,流失率高,利用率低,且易造成面源污染。缓释剂型是农药发展的一个重要方向,研发一种可降解、缓释效果良好的载药微球成为当前的关注热点。
纤维素因其无毒、低成本、可生物降解、良好的生物相容性等特点在医药和农药缓释领域受到广泛关注。但纤维素微球结构较疏松,药物释放易爆释。通过共混改性能改变纤维素微球的微相结构,增强微球的致密度和凝胶强度,从而实现有效调节复合微球的缓释性能的目的。
纤维素基载药微球处理技术中,利用无机矿物质材料进行共混是一种有效便捷的方法,可以利用现有的设备开展研究。该技术的关键是合成高效载药性、微球骨架结构紧密的载药材料。目前已有许多专利涉及复合载药微球缓释研究。例如,公开号103446624a公开了一种载药微球/壳聚糖/海藻酸钠可注射水凝胶的制备方法;公开号106668870a公开了一种载药聚吡咯/海藻酸钠凝胶的制备方法;从已有的专利来看,现有的载药材料进行简单的有机改性处理,如偶联剂或表面活性剂处理,一般未考虑微球的结构紧密问题,存在易爆释的缺点。因此,开展可降解、流失率低、利用率高、不易造成二次污染的载药材料的研究极有必要。
技术实现要素:
为解决目前农药施放流失率高、利用率低的问题,本发明提出了一种吡虫啉复合载药微球的制备方法,具有良好的缓释效果、可生物降解、生产成本低、环保的特性。
本发明是通过以下技术方案实现的,包括以下步骤:
(1)酰氯改性的mwcnt的制备
原材料羧基-碳纳米管(mwcnt-cooh)和亚硫酰氯(socl2)在30~50℃回流24~36h,合成酰氯改性的mwcnt(mwcnt-cocl)。产物用n’n-二甲基甲酰胺洗涤3~5次,干燥。
其制备路线为:
所述的羧基-碳纳米管(mwcnt-cooh)、亚硫酰氯(socl2)的质量比为5~7:1mg。
作为优选,作为优选,产物的干燥温度为60~80℃。
(2)壳聚糖改性mwcnt聚合物(cs/mwcnt)的制备
壳聚糖(cs)在n,n-二甲基甲酰胺(dmf)中溶胀18~28h,然后添加步骤(1)制备的mwcnt-cocl在90~110℃的温度下反应18~24h。产物cs/mwcnt用乙酸溶液洗涤,干燥。
其制备路线为:
所述的壳聚糖、mwcnt-cocl、n,n-二甲基甲酰胺的质量体积比为2.0~3.0g:1.0g:80~120ml。
所述的采用乙酸溶液洗涤产物,其目的在于去除多余的壳聚糖。
所述的乙酸溶液的质量分数为1~2%。
作为优选,产物的干燥温度为60~80℃。
(3)吡虫啉复合载药微球(cmc@cs/mwcnt)的制备
将步骤(2)制备的cs/mwcnt与吡虫啉混合溶液在无水乙醇中搅拌30~60min;再将羧甲基纤维素(cmc)溶于蒸馏水。将上述两种溶液混合均匀,逐滴加入到ca2+溶液中交联1~2h后过滤,洗涤,干燥。得到吡虫啉复合载药微球。
其制备路线为:
所述的cs/mwcnt、吡虫啉、无水乙醇的质量体积比为1~1.5g:1g:10~20ml。
所述的羧甲基纤维素(cmc)、蒸馏水的质量比为1:40~60g。
所述的混合溶液中cs/mwcnt、吡虫啉、羧甲基纤维素(cmc)、ca2+离子溶液的质量体积比为1~1.5g:1g:1g:50~100ml。
所述的ca2+溶液可以为氯化钙、溴化钙中的一种。
所述的ca2+离子溶液的质量分数为2~5%。
作为优选,混合溶液逐滴加入ca2+离子溶液时采用的仪器为皮下注射器。
作为优选,产物的干燥温度为60~80℃。
本发明提供了一种吡虫啉复合载药微球的制备方法,可以合理调控吡虫啉药物的释放速率,延长其有效期,提高吡虫啉的利用率,起到减施增效的效果。并且易于生物降解,可应用于农药可控缓释体系,具有良好的发展前景。
与现有技术相比,本发明的有益效果是:具有生物可降解性、农药释放速度缓慢,流失率低,利用率高,且不会造成面源污染的特性;同时本发明的思路,可对农药缓释剂型的研究提供指导。
附图说明
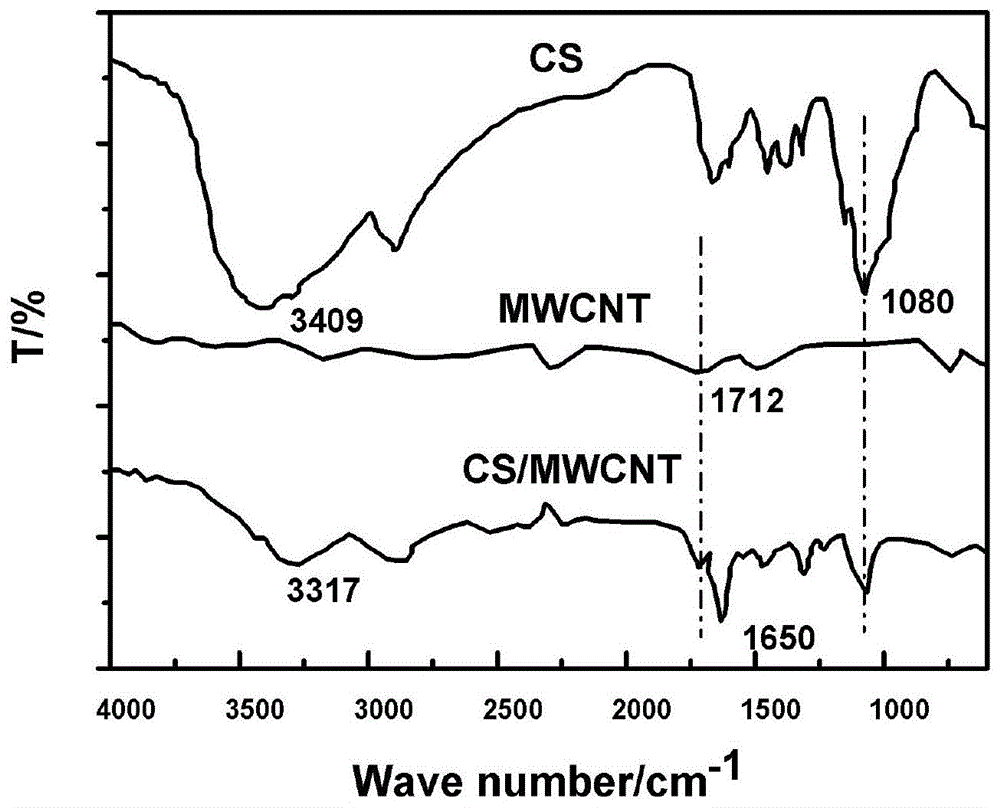
图1为实施例1中原料壳聚糖cs、碳纳米管mwcnt、壳聚糖改性mwcnt聚合物(cs/mwcnt)的红外谱图;
图2为实施例1所制备的吡虫啉复合载药微球(cmc@cs/mwcnt)的外观图;
图3实施例1所制备的吡虫啉复合载药微球(cmc@cs/mwcnt)的缓释效果图;
具体实施方式
以下结合具体实施方式和附图对本发明的技术方案作进一步详细描述:
实施例1:
吡虫啉复合载药微球(cmc@cs/mwcnt)的制备,包括以下步骤:
(1)酰氯改性的mwcnt的制备
将150mg的mwcnt-cooh分散在30ml亚硫酰氯(socl2)中,30℃剧烈搅拌下回流24h,过滤分离残余物,用100mln’n-二甲基酰胺洗涤3次,并在80℃下真空干燥,合成酰氯改性的mwcnt(mwcnt-cocl)。
(2)壳聚糖改性mwcnt聚合物(cs/mwcnt)的制备
将2.5g壳聚糖悬浮于100mldmf中,并使其溶胀24h,然后添加1.0gmwcnt-cocl。在90℃下进行接枝反应24h。用1%乙酸溶液洗涤3次(以除去游离的壳聚糖),并将cs/mwcnt接枝聚合物在65℃下真空干燥至恒重。
(3)吡虫啉复合载药微球(cmc@cs/mwcnt)的制备
先称取1.5g羧甲基纤维素加入60ml蒸馏水中,搅拌溶解;再称取一定2gcs/mwcnt和1.2g吡虫啉加入30ml无水乙醇中,搅拌30min,使cs/mwcnt充分吸附吡虫啉。将上述2种溶液混合并搅拌均匀,超声分散40min,另配制5%的cacl2溶液50ml,再将上述混合液用10ml皮下注射器逐滴加入到cacl2溶液中并恒速搅拌,交联30min后过滤,反复用蒸馏水冲洗5次,最后在60℃下真空干燥至恒重。
实施例2:
吡虫啉复合载药微球(cmc@cs/mwcnt)的制备,包括以下步骤:
(1)酰氯改性的mwcnt的制备
将200mg的mwcnt-cooh分散在50ml亚硫酰氯(socl2)中,30℃剧烈搅拌下回流26h,过滤分离残余物,用100mln’n-二甲基酰胺洗涤5次,并在60℃下真空干燥,合成酰氯改性的mwcnt(mwcnt-cocl)。
(2)壳聚糖改性mwcnt聚合物(cs/mwcnt)的制备
将2g壳聚糖悬浮于80mldmf中,并使其溶胀24h,然后添加1.8gmwcnt-cocl。在90℃下进行接枝反应24h。用2%乙酸溶液洗涤3次(以除去游离的壳聚糖),并将cs/mwcnt接枝聚合物在60℃下真空干燥至恒重。
(3)吡虫啉复合载药微球(cmc@cs/mwcnt)的制备
先称取1g羧甲基纤维素加入50ml蒸馏水中,搅拌溶解;再称取一定1.5gcs/mwcnt和1g吡虫啉加入20ml无水乙醇中,搅拌30min,使cs/mwcnt充分吸附吡虫啉。将上述2种溶液混合并搅拌均匀,超声分散30min,另配制2%的cacl2溶液100ml,再将上述混合液用10ml皮下注射器逐滴加入到cacl2溶液中并恒速搅拌,交联30min后过滤,反复用蒸馏水冲洗5次,最后在60℃下真空干燥至恒重。
实施例3:
吡虫啉复合载药微球(cmc@cs/mwcnt)的制备,包括以下步骤:
(1)酰氯改性的mwcnt的制备
将100mg的mwcnt-cooh分散在20ml亚硫酰氯(socl2)中,30℃剧烈搅拌下回流24h,过滤分离残余物,用80mln’n-二甲基酰胺洗涤3次,并在80℃下真空干燥,合成酰氯改性的mwcnt(mwcnt-cocl)。
(2)壳聚糖改性mwcnt聚合物(cs/mwcnt)的制备
将2.3g壳聚糖悬浮于80mldmf中,并使其溶胀24h,然后添加0.9gmwcnt-cocl。在90℃下进行接枝反应24h。用1%乙酸溶液洗涤3次(以除去游离的壳聚糖),并将cs/mwcnt接枝聚合物在65℃下真空干燥至恒重。
(3)吡虫啉复合载药微球(cmc@cs/mwcnt)的制备
先称取1.2g羧甲基纤维素加入60ml蒸馏水中,搅拌溶解;再称取一定2gcs/mwcnt和1.2g吡虫啉加入350ml无水乙醇中,搅拌30min,使cs/mwcnt充分吸附吡虫啉。将上述2种溶液混合并搅拌均匀,超声分散40min,另配制5%的cacl2溶液40ml,再将上述混合液用10ml皮下注射器逐滴加入到cacl2溶液中并恒速搅拌,交联30min后过滤,反复用蒸馏水冲洗5次,最后在60℃下真空干燥至恒重。
试验例1:
吡虫啉复合载药微球(cmc@cs/mwcnt)的结构和性能测试。
试验样品:实施例1所制备的cs/mwcnt、吡虫啉复合载药微球(cmc@cs/mwcnt)。
1、红外(ftir)分析:采用傅立叶变换红外光谱仪进行测定反应物cs、mwcnt、中间产物cs/mwcnt的ir谱,设置仪器扫描波数为4000~600cm-1。得出的谱图如图1所示。对于原料,谱图中3409cm-1的宽峰来自于-oh的拉伸;在1712cm-1处有一个羧基峰,表明羧基官能团在碳纳米管表面;合成cs/mwcnt后,在1650cm-1处出现了一个新的吸收峰。这表明cs的共价接枝mwcnt中酰胺键的c-o拉伸振动,表明了酰胺键的接枝,证明cs/mwcnt的成功制备。
2、形貌分析:吡虫啉复合载药微球(cmc@cs/mwcnt)的外观形貌照片如图2所示。外观形态表明载药微球呈乳白色凝胶球型,表面光滑而且具有一定的弹性,大小均匀,直径约为0.5mm,意味着吡虫啉复合载药微球(cmc@cs/mwcnt)的成功制备。
试验例2:
吡虫啉复合载药微球(cmc@cs/mwcnt)的载药性能测试。
试验样品:实施例1、实施例2、实施例3所制备的吡虫啉复合载药微球。
取0.1g载药微球放入50ml50%的乙醇溶液中,充分溶胀后将微球破坏,再超声1h破坏微球结构,完全浸提出模型药物,取样,测定吸光度,根据公式求得微球的载药率(lc)和包封率(ee)。实验数据表明实施例中载药微球的载药率(lc)和包封率(ee)最佳,分别为52.7%、92.4%。
lc=(微球中含药量/微球质量)×100%
ee=(微球中含药量/投药量)×100%
试验例3:
吡虫啉复合载药微球(cmc@cs/mwcnt)的缓释性能测试
分别称取10mg吡虫啉原药和复合载药微球(cmc@cs/mwcnt)放置在透析袋中并置于30℃下的50ml50%乙醇水溶液的锥形瓶中,间隔一定时间(t),移取1ml样品液,同时向锥形瓶补加原缓释介质,用uv扫描测量其吸光度,吡虫啉随时间的累积释放率为r,绘制t-r曲线作为吡虫啉的缓释动力学曲线。如图3所示。结果表明复合载药微球有着良好的缓释效果,这是因为cs/mwcnt通过静电或氢键与cmc作用,起到交联与增强凝胶强度的作用,使微球结构变得致密,阻碍了药物分子从微球向释放介质的扩散;同时,cs/mwcnt通过对农药的吸附,延长了药物分子在载体中的扩散路径,对药物扩散起滞留作用,这些综合作用导致释放速率与累计释放率降低。
- 还没有人留言评论。精彩留言会获得点赞!