一元稳定复合过氧乙酸消毒剂及其制备方法与流程
1.本发明涉及消毒技术领域,具体涉及一种一元稳定复合过氧乙酸消毒剂及其制备方法。
背景技术:
2.过氧乙酸是高效消毒液,属过氧化物类消毒液,具有快速、高效、分解后无残留有害物质等优点。过氧化氢俗称双氧水,是一种重要的无机化工产品,在纺织、造纸、化工、轻工、医药、电子、食品、环保和军工等领域应用广泛。以过氧乙酸和过氧化氢为主要成分的混合型消毒液作为一种具有高效、灭菌范围广、无毒、无二次污染等特点的消毒液于已经广泛用于设备、工具、管道、包装容器等领域的消毒。作为强氧化性物质,过氧化氢和过氧乙酸均不能长期稳定保存,为了克服过氧乙酸和过氧化氢的不稳定性,近几年市售产品多为二元包装,即产品分为a、b两液,平时分瓶存放,使用前一天等量混匀,然后再稀释成所需浓度使用,使用不便。现有技术中,也有过氧乙酸与双氧水的一元消毒液,则通常需要在其中加入稳定剂。
3.如申请号为cn201610400921.6的专利公开了一种消毒液,该消毒液由以下重量百分比的组分组成:过氧化氢 20-28%;过氧乙酸 3-6%;乙酸 1-2.5%;硫酸 0.001-0.02%;稳定剂 0.01-3.5%;表面活性剂 0.01-0.2%;余量为去离子水或蒸馏水;所述的稳定剂为焦磷酸钠、吡啶二羧钠、羟基乙叉二膦酸四钠、乙二胺四甲叉膦酸钠、羟基甲苯叉二磷酸、多乙烯多胺多亚烷基膦酸、肌醇六磷酸、多聚磷酸钾、焦磷酸钾的一种或几种的混合物。该消毒液存在以下问题:过氧化氢含量过高且未考虑过氧化氢的稳定性;含有硫酸,消毒液中通常对硫酸根离子有最高限量要求,其的存在容易腐蚀医疗器械,限制了其在医疗器械上的使用;其中添加表面活性剂,由于表面活性剂剂会增大消毒剂的表面张力,这容易堵塞透气孔,导致过氧乙酸、过氧化氢分解产生的气体排出受阻,易发生危险。
4.如申请号为cn201811567035.8的专利公开了一元型过氧乙酸消毒剂,所述一元型过氧乙酸消毒剂原料活性成分由25-40%w/w过氧化氢、27-40%w/w冰乙酸、0.5-3%w/w硫酸或磷酸、0.005-0.1%w/w吡啶二羧酸、0.045-0.09%w/w hedp、0.035-0.6%w/w焦磷酸钠、0.01-0.05%w/w edta组成。该消毒液存在以下问题:过氧化氢含量过高且未考虑过氧化氢的稳定性;含有硫酸,消毒液中通常对硫酸根离子有最高限量要求,其的存在容易腐蚀医疗器械,限制了其在医疗器械上的使用;hedp具有刺激性且损伤眼睛,焦磷酸钠具有刺激性且损伤眼睛,吡啶二羧酸具有一定毒性且较贵。另外,该专利的消毒剂主要在畜禽养殖场所环境、物体表面的消毒方面的应用,应用场景特殊,与常规应用场景的要求不一样。
技术实现要素:
5.为了解决前述问题,本发明实施例提供了一种一元稳定复合过氧乙酸消毒剂,该消毒剂中,过氧乙酸和过氧化氢的稳定性均非常好,保质期2年以上;对碳钢和铜中度腐蚀,对铝轻度腐蚀,对不锈钢无腐蚀;杀菌效果好。所述技术方案如下:
一方面,本发明实施例提供了一种一元稳定复合过氧乙酸消毒剂,由以下重量百分比的组分组成:过氧乙酸0.1-0.3%,过氧化氢4.0-8.0%,乙酸1-10%,对甲苯磺酸0.05-0.2%,乙二胺四乙酸0.05-0.2%,硅酸钠0.01-0.05%和余量去离子水。其中,本实施例中,过氧乙酸、过氧化氢和乙酸能形成平衡体系,对甲苯磺酸作为反应的催化剂,不会增加消毒剂的腐蚀性和刺激性,反而还会提升杀菌效果,也能提升过氧乙酸和过氧化氢的稳定性。乙二胺四乙酸能提升过氧乙酸和过氧化氢的稳定性,硅酸钠能降低反应液的腐蚀性。
6.优选地,本发明实施例提供的一元稳定复合过氧乙酸消毒剂由以下重量百分比的组分组成:过氧乙酸0.15%,过氧化氢4.38%,乙酸4%,对甲苯磺酸0.10%,乙二胺四乙酸0.08%,硅酸钠0.02%和余量去离子水。
7.优选地,本发明实施例提供的一元稳定复合过氧乙酸消毒剂由以下重量百分比的组分组成:过氧乙酸0.26%,过氧化氢7.21%,乙酸5%,对甲苯磺酸0.15%,乙二胺四乙酸0.1%,硅酸钠0.05%和余量去离子水。
8.另一方面,本发明实施例还提供了前述一元稳定复合过氧乙酸消毒剂的制备方法,该方法包括以下步骤:(1)将过氧化氢、乙酸和对甲苯磺酸混合均匀后在室温下静置一定时间,再搅拌,再静置至反应完全(根据需要也可补充过氧乙酸,以使过氧乙酸的含量符合要求),即得到复合消毒剂。(2)将乙二胺四乙酸加入部分去离子水中,在室温下搅拌至溶解,得到含乙二胺四乙酸的稳定剂溶液。(3)将步骤(2)的稳定剂溶液加入到步骤(1)的复合消毒剂中,再依次加入硅酸钠和剩余的水,在室温下搅拌10h以上得到产品。
9.其中,过氧化氢和乙酸反应生成过氧乙酸,此反应为平衡反应,制得的消毒剂中过氧化氢、过氧乙酸和乙酸的重量百分比为过氧化氢:过氧乙酸0.1-0.3%,过氧化氢4.0-8.0%,乙酸1-10%。相应地,步骤(1)中的过氧化氢和乙酸根据实际需求进行添加,保证制备后的产品满足配比要求。
10.其中,在步骤(1)中,将过氧化氢、乙酸和对甲苯磺酸混合均匀后在室温下静置1-3h,再搅拌,再静置至少5h至反应完全,即得到复合消毒剂。
11.其中,在步骤(2)中,将乙二胺四乙酸加入5-10wt%的去离子水中。
12.本发明提供的消毒剂具有如下有益效果:(1)过氧乙酸和过氧化氢的稳定性均非常好,保质期2年以上,两年后,过氧乙酸的含量下降在8%以下,过氧化氢的含量下降在5%以下。
13.(2)对碳钢和铜中度腐蚀,对铝轻度腐蚀,对不锈钢无腐蚀。
14.(3)杀菌效果好,对大肠杆菌、金黄色葡萄球菌和铜绿假单胞菌的平均杀灭对数值均>5.00;符合gb27952-2011《普通物体表面消毒剂的卫生要求》中的规定。对木质物体表面自然菌的平均杀灭对数值为1.52,且各次试验的杀灭对数值均>1.00;符合gb27952-2011《普通物体表面消毒剂的卫生要求》中的规定。对染在不锈钢水管内壁的大肠杆菌的平均杀灭对数值为5.12,且对每样本的杀灭对数值均>3.00;符合gb27952-2011《普通物体表面消毒剂的卫生要求》中的规定。
[0015] (4)3个剂量组的样品小鼠骨髓嗜多染红细胞微核试验结果为阴性。根据《消毒技术规范》(2002年版)的小鼠骨髓嗜多染红细胞微核试验中所述,样品对昆明种小鼠不具有体内染色体损伤作用;符合gb27952-2011《普通物体表面消毒剂的卫生要求》中的规定。所
送样品制备的受试物急性经口毒性ld
50
>5000mg/kg体重,符合gb27952-2011《普通物体表面消毒剂的卫生要求》中的规定。
具体实施方式
[0016]
为使本发明的目的、技术方案和优点更加清楚,下面对本发明实施方式作进一步地详细描述。
[0017]
实施例一实施例一公开了一种一元稳定复合过氧乙酸消毒剂,由以下重量百分比的组分组成:过氧乙酸0.15%,过氧化氢4.38%,乙酸4%,对甲苯磺酸0.10%,乙二胺四乙酸0.08%,硅酸钠0.02%和余量去离子水。ph值为3.12。
[0018]
实施例二实施例二公开了一种一元稳定复合过氧乙酸消毒剂,其特征在于,由以下重量百分比的组分组成:过氧乙酸0.26%,过氧化氢7.21%,乙酸5%,对甲苯磺酸0.15%,乙二胺四乙酸0.1%,硅酸钠0.05%和余量去离子水。
[0019]
验证例,试验均采用实施例1提供的消毒剂。
[0020]
一、金属腐蚀试验1.1.金属片:碳钢(规格见gb700-65),铜(规格见gb2060-80),铝(规格见gb1173-74),不锈钢(规格见gb1220-75),均由金坛市振兴实验器材厂提供。
[0021]
1.2.分析天平:sartorius天平。
[0022]
1.3.砂纸:120号粒度水砂纸,gb2477。
[0023]
1.4.根据《消毒技术规范》(2002年版)2.2.4条进行试验。
[0024]
1.5.对碳钢、铜、铝和不锈钢的腐蚀速率为0.8943mm/a、0.8870mm/a、0.0773mm/a和0.0000 mm/a。结果如表1所示:表1从表1可以看出,本专利的消毒剂对碳钢和铜中度腐蚀,对铝轻度腐蚀,对不锈钢无腐蚀。
[0025]
二、灭菌试验2.1. 试验菌株:大肠杆菌atc 6538、金黄色葡萄球菌8099和铜绿假单胞菌atcc15442,均由中国普通微生物菌种保藏中心提供。以上菌株代数为第7代,用tps配置菌悬浮液。
[0026]
2.2.中和剂:含1%硫代硫酸钠的tps溶液。
[0027]
2.3.菌悬液的制备:根据《消毒技术规范》(2002年版)2.1.1.2.3条,含菌量为1*10
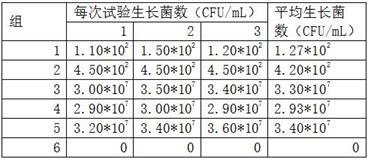
8-5*108cfu/ml。中和剂鉴定试验:根据《消毒技术规范》(2002年版)2.1.1.5条,试验菌为大肠杆菌。试验分组为:(1)消毒剂+菌悬液,(2)(消毒剂+菌悬液)+中和剂,(3)中和剂+菌悬液,(4)(消毒剂+中和剂)+菌悬液,(5)tps+菌悬液,(6)试验所用同批次tps、中和剂和培养
基。作用时间1min,试验温度20
±
1℃,试验重复3次。
[0028]
2.4.悬液定量杀菌试验:根据《消毒技术规范》(2002年版)2.1.1.7条,作用时间4min、8min和12min,试验温度20
±
1℃,试验重复3次。
[0029]
2.5.结果:中和剂鉴定试验:第(1)组平均生长菌数为1.27*102cfu/ml;第(2)组平均生长菌数为3.40*102cfu/ml;第(3)、(4)和(5)组平均生长菌数接近,三组间误差率为5.82%;第(6)组无菌生长。结果如表2和表3所示:表2表3从表2和表3可以看出,对大肠杆菌、金黄色葡萄球菌和铜绿假单胞菌的灭杀效果:在20
±
1℃条件下,作用8min,对大肠杆菌、金黄色葡萄球菌和铜绿假单胞菌的平均杀灭对数值均>5.00。
[0030]
三、对物体表面消毒现场试验3.1.采样液:含1%硫代硫酸钠的tps溶液。
[0031]
3.2.规格板(5cm*5cm)、无菌棉拭子。
[0032]
3.3. 根据《消毒技术规范》(2002年版)2.1.2.10条,把5cm*5cm规格板放在物体表面,用浸润了采样液的棉拭子涂抹采样,横竖往返各8次,剪断拭子棉花端置5ml采样液中作为对照组。用本实施例的消毒剂对物体表面进行擦拭后,作用8min,在对照格附近按对照组方法取样,剪断拭子棉花端置5ml采样液中,进行活菌培养计数。试验重复30次,试验温度20
±
1℃。结果如表4所示:表4
从表4可以看出:对木质物体表面自然菌的平均杀灭对数值为1.52,且各次试验的杀灭对数值均>1.00。
[0033]
四、对管道消毒模拟现场试验(不锈钢)4.1.试验菌株:大肠杆菌8099。
[0034]
4.2.采样液:含1%硫代硫酸钠的tps溶液。
[0035]
4.3.消毒对象:30根不锈钢水管。
[0036]
4.4.菌悬液的制备:根据《消毒技术规范》(2002年版)2.1.1.2条,染菌量为5*10
5-5*10
6 cfu/m2。
[0037]
4.5.对管道模拟现场试验:根据《消毒技术规范》(2002年版)2.1.2.9条,于规格板中央空格内用无菌棉拭以菌悬液均匀涂抹试表面的60个区块(各为25cm2)。待自然干燥后进行试验。30个区块作为阳性对照区(用无菌纯水,对管道内壁表面染菌部位进行冲洗),30个区块为试验区(用消毒剂,对管道内壁表面染菌部位进行冲洗)。试验组消毒作用8min,然后用浸润了采样液的棉拭子涂抹采样,横竖往返各8次,剪断拭子棉花端置5ml采样液中。在对照格用浸润了采样液的棉拭子涂抹采样,横竖往返各8次,剪断拭子棉花端置5ml采样液中作为对照组,剪断拭子棉花端置5ml采样液中,进行活菌培养计数,试验重复3次,试验温度20
±
1℃。结果如表5所示:表5
从表5可以看出:对染在不锈钢水管内壁的大肠杆菌的平均杀灭对数值为5.12,且对每样本的杀灭对数值均>3.00。
[0038]
五、过氧乙酸稳定性检测5.1.标准溶液:硫代硫酸钠标准滴定液0.1096mol/l。
[0039]
5.2.检测依据:根据《消毒技术规范》(2002年版)2.2.1.2.3条。
[0040]
5.3.检测条件:试验环境温度20-22℃,相对湿度40-50%。
[0041]
5.4.检测方法:在5ml消毒剂中加入2mol/l硫酸5ml,100g/l硫酸锰3滴,摇匀并用0.02mol/l高锰酸钾溶液滴定至溶液呈粉红色。随即加100g/l碘化钾溶液10ml与30g/l钼酸铵3滴,摇匀并用0.1096mol/l硫代硫酸钠滴定液滴定至淡黄色。加入5g/l淀粉溶液3滴(溶液立即变蓝色),继续用硫代硫酸钠滴定至蓝色消失,记录硫代硫酸钠滴定液的总用量。
[0042]
5.5.序号1为实施例1提供的消毒剂,序号2为实施例2提供的消毒剂。
[0043]
5.6.稳定性试验:经35℃3三个月和2年保存后。结果如表6所示:表6六、皮肤刺激试验6.1.测试方法:根据《消毒技术规范》(2002年版)2.2.1.2.3条。
[0044]
6.2.测试环境:普通级动物房;环境温度21-23℃,相对湿度55-65%。
[0045]
6.3.动物试验:采用普通级新西兰白色家兔,由广东省医学实验动物中心(三水基地)提供,实验动物体重2.3-2.5kg,试验动物数量/性别:4只/公:母=2:2。
[0046]
6.4.消除受试物后的1h、24h和48h观察给予受试物部位的皮肤反应。
[0047]
6.5.试验步骤:(1)选4只健康成年新西兰兔。试验前24h,将试验动物背部脊柱两侧毛剃掉,准备2块去毛区域(每一去毛范围各3cm*3cm),确认动物皮肤完好无损后进行试验。(2)取受试物0.5ml均匀涂抹于试验动物左侧去毛皮肤约2.5cm*2.5cm区域上。然后用斑贴覆盖,再用无刺激性胶布和绷带加以固定。另一侧去毛区域皮肤斑贴覆盖作为对照。贴敷1h后用温水清除残留受试物。于清除受试物后的1h、24h和48h贯穿受试部位皮肤反应并按
《消毒技术规范》中表2-11“皮肤刺激反应的评分标准”进行皮肤刺激反应评分,记录每一观察时点的皮肤反应分值,按方法2.3.3.4评价规定中相应的内容对反应分值进行计算,按方法表2-12“皮肤刺激强度分级”评定该受试物对动物皮肤刺激强度的级别。其结果如表7所示:表7从表7可以看出:在各观察时点均未观察到该受试物对家兔完整皮肤造成红斑、水肿刺激反应,最高积分均值(刺激指数)为0。根据皮肤刺激强度分级标准,该受试物对家兔急性皮肤刺激性为无刺激性反应。
[0048]
七、小鼠骨髓嗜多染红细胞微核试验7.1.标准:根据《消毒技术规范》(2002年版)。
[0049]
7.2.检测环境:spf级动物房,室温22
±
1℃,湿度60
±
5%。
[0050]
7.3.试验动物:50只spf级昆明种小鼠,雌雄各半,体重25.4-29.0克,实验动物和饲料购自广东省医学实验动物中心。
[0051]
7.4.样品处理:计量:该样品小鼠急性经口毒性ld
50
>5000mg/kg体重,确定本次测试三个剂量组,分别为:5000mg/kg体重、2500mg/kg体重和1250mg/kg体重。对照组:阳性对照组选用环磷酰胺,受试计量为40mg/kg体重,配制方法为称取40mg环磷酰胺用纯净水稀释至20ml供试;阴性对照组给予蒸馏水。
[0052]
7.5.试验步骤:试验组,按0.2ml/10g体重的灌胃量分两次染毒,间隔24h;末次染毒后6h处死动物,取肱骨,挤出骨髓液于小牛血清中,常规涂片,待晾干后使用姬姆萨快速染液进行染色8-10min,随后使用pbs缓冲液(ph6.8)冲洗,晾干。每鼠观察1000个完整骨髓嗜多染红细胞(pce),记录有微核的细胞数,计算细胞微核率,用波松分布u检验进行统计学处理:同时计数200个pce所见到的nce(成熟红细胞)数,计算pce/nce比例。其结果如表8所示:表8从表8可以看出:经波松分布u检验结果表明,样品各计量组与阴性对照组比较差
异均无显著性意义(p>0.05),阳性对照组与阴性对照组比较差异有显著性意义(p<0.05),故试验结果为阴性。即样品对昆明种小鼠不具有体内染色体损伤作用。
[0053]
八、急性毒性试验8.1.标准:根据《消毒技术规范》(2002年版)。
[0054]
8.2.检测环境:spf级动物房,室温22
±
1℃,湿度60
±
5%。
[0055]
8.3.试验动物:20只spf级昆明种小鼠,雌雄各半,体重18.2-19.8克,实验动物和饲料购自广东省医学实验动物中心。
[0056]
8.4.试验步骤:预试时,未发现所送样品制备液在5000mg/kg体重剂量出现死亡,故正式试验采用一次最大限度试验,实验设计受试物计量为5000mg/kg体重。按0.2ml/10g体重的量经口灌胃给予试验用液,灌胃前动物禁食4h,自由饮水。灌胃1h后给予正常饮食。实验观察14天,每天记录中毒症状及死亡情况,计算ld
50
。结果如表9所示:表9从表9可以看出:14天观察期内所有受试动物未见明显中毒症状及死亡。故小鼠急性经口毒性ld
50
>5000mg/kg体重。
[0057]
对比例1对比例1公开了一种消毒剂,由以下重量百分比的组分组成:过氧乙酸0.15%,过氧化氢4.38%。
[0058]
对比例2对比例2公开了一种消毒剂,由以下重量百分比的组分组成:过氧乙酸0.15%,过氧化氢4.38%,乙酸4%,硫酸适量使体系的ph值为3.12,乙二胺四乙酸0.08%,硅酸钠0.02%和余量去离子水。
[0059]
对比例3对比例3公开了一种消毒剂,由以下重量百分比的组分组成:过氧乙酸0.15%,过氧化氢4.38%,乙酸4%,乙二胺四乙酸0.08%,硅酸钠0.02%和余量去离子水。
[0060]
稳定性试验的条件为54℃,时间为1个月,3个月,6个月和12个月,稳定性试验的结果如表10所示:表10从表10可以看出,仅过氧乙酸和过氧化氢,过氧乙酸的衰减速度非常快,过氧化氢的衰减速度中等;以硫酸替代对甲苯磺酸,过氧乙酸的衰减速度中等,过氧化氢的衰减速度较快;去除对甲苯磺酸,过氧乙酸的衰减速度较快,过氧化氢的衰减速度中等。从表10可以
看出,加入对甲苯磺酸能减缓过氧乙酸和过氧化氢的衰减。
[0061]
对金属的腐蚀性试验,过程见前述金属腐蚀试验的过程,结果如表11所示:表11从表11可以看出,过氧乙酸和过氧化氢的混合液本身具有较高的腐蚀性,加入硫酸(同时加入其他缓蚀剂)会提升腐蚀性,加入乙二胺四乙酸和硅酸钠等能降低腐蚀性,加入对甲苯磺酸(同时加入乙二胺四乙酸和硅酸钠等)不会增加腐蚀性。
[0062]
对管道消毒模拟现场试验(不锈钢),50℃放置7天后进行试验,结果如表12所示:表12从表12可以看出,放置一段时间后,本实施例提供的消毒剂具有更好的杀菌效果。
[0063]
对管道消毒模拟现场试验(不锈钢),制备完成后3天内使用,结果如表13所示:表13从表13可以看出,对甲苯磺酸还能提升过氧乙酸和过氧化氢的混合液的杀菌效果。
[0064]
以上所述仅为本发明的较佳实施例,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1