用于牙齿的再矿化和增白的经表面反应的碳酸钙的制作方法
牙釉质是人体中最硬的物质且含有约96%的矿物质,其中其余部分由水和有机物构成。牙釉质的主要矿物质为羟基磷灰石,其为结晶磷酸钙。在牙齿萌出进入口中之前,在其在牙龈内发育的同时,在牙齿上形成釉质。
然而,其高矿物质含量使釉质极易遭受去矿化过程,所述去矿化过程尤其通过摄取酸性饮料和甜食而触发。牙齿的再矿化可在一定程度上修复对牙齿造成的损伤,但超出该程度的损伤无法由身体修复,且最终持续的去矿化过程导致牙齿腐蚀和龋齿。因此,对人类牙釉质的维持和修复是牙科学主要关注的问题之一。
使用含有羟基磷灰石和一氟磷酸钠的牙膏的再矿化研究公开于Hornby等人的International Dental Journal 2009,59,325-331中。US 2007/0183984 A1涉及一种用于牙齿矿化或再矿化的口腔组合物,其包含磷酸钙盐和在口腔中具有不同溶解度的酸的组合。
牙釉质的典型颜色在淡黄色至灰白色或青白色变化。由于牙釉质为半透明的,所以牙本质和牙釉质下面的任何物质的颜色强烈地影响牙齿的外观。乳牙上的牙釉质具有更不透明的晶型且因此显得比恒牙白。在放射照片上,可注意到牙齿和周围牙周组织的不同部分中矿化的差异;牙釉质呈现出比牙本质或牙髓更浅,因为其比所述二者更致密且更不透射线(参见“Tooth enamel”,Wikipedia,The Free Encyclopedia,2014年3月6日)。
随着人年龄变大,由于牙齿矿物质结构的变化,恒牙通常变得更深。此外,牙齿会被富含类胡萝卜素或氧杂蒽酮类化合物的细菌色素、食品和蔬菜染色。某些抗菌药物(如四环素)可造成牙齿染色或釉质的亮度降低,且摄取有色液体(如咖啡、茶和红酒)或抽烟会使牙齿变色(“Tooth bleaching”,Wikipedia,The Free Encyclopedia,2014年2月5日)。
用于增白牙齿的方法通常涉及使用如过氧化物的侵蚀性氧化剂的漂白过程,且可能需要全部固体组合物保持与牙齿接触较长的时间段。作为替代方案,已建议采用钙盐提供牙齿的再矿化和增白的牙粉组合物。
WO 2012/143220 A1描述了一种适用于牙齿的再矿化和增白的组合物,其包含钙源和再生源钙盐。包含不溶于水和/或微溶于水的钙源和有机酸,或其生理学上可接受的盐的牙粉组合物描述于WO 2013/034421 A2中。WO 2012/031786 A2涉及具有复合颗粒活性剂(具有核和包衣)的口腔护理组合物,由此包衣与磷酸根离子相互作用产生钙和磷酸盐反应产物,所述反应产物适于粘附于牙釉质和/或牙本质以提高牙齿特性。
鉴于前文,存在对适用于牙齿再矿化和/或牙齿增白的药剂的持续需求。
因此,本发明的一个目标为提供适于牙齿再矿化和增白且与常规口腔护理组合物相容的药剂。还期望提供使用温和且容易施用的再矿化剂和/或增白剂。还期望提供再矿化剂和/或增白剂,其不一定需要诊室内处理而可例如每天在家使用。
本发明的一个目标还为提供更耐酸攻击的再矿化剂和/或增白剂。还期望提供再矿化剂和/或增白剂,其不一定需要具有在纳米尺寸范围内的粒度。还期望提供再矿化剂和/或增白剂,其提供作为用于活性剂的载体材料的额外益处。
通过如本文独立权利要求中界定的内容实现前述和其他目标。
根据本发明的一个方面,提供用于牙齿再矿化和/或增白的经表面反应的碳酸钙(surface-reacted calcium carbonate),其中所述经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和至少一种酸的反应产物。
根据本发明的另一方面,提供用于牙齿再矿化和/或增白的口腔护理组合物,其包含经表面反应的碳酸钙,其中所述经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和至少一种酸的反应产物。
根据本发明的又一方面,提供用于牙齿再矿化的经表面反应的碳酸钙,其中所述经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和至少一种酸的反应产物。
根据本发明的又一方面,提供用于牙釉质增白的经表面反应的碳酸钙,其中所述经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和至少一种酸的反应产物。
本发明的有利实施方案界定于相应的从属权利要求。
根据一个实施方案,所述至少一种酸选自:盐酸、硫酸、亚硫酸、磷酸、柠檬酸、草酸、乙酸、甲酸及其混合物,所述至少一种酸优选选自:盐酸、硫酸、亚硫酸、磷酸、草酸及其混合物,且所述至少一种酸更优选为磷酸。
根据一个实施方案,经表面反应的碳酸钙呈颗粒形式,所述颗粒具有等于或小于15μm、优选1μm至10μm、更优选2μm至8μm、且最优选3μm至7μm的体积中值粒径(d50)和/或等于或小于25μm、优选7μm至22μm、更优选10μm至20μm且最优选15μm至18μm的体积限定顶切粒度(d98)。根据另一个实施方案,经表面反应的碳酸钙呈颗粒形式,所述颗粒具有使用氮气和根据ISO 9277的BET方法所测量的5m2/g至200m2/g、更优选20m2/g至80m2/g、且甚至更优选30m2/g至60m2/g的比表面积。
根据一个实施方案,经表面反应的碳酸钙与氟化物化合物组合使用,所述氟化物化合物优选选自:氟化钠、氟化亚锡、一氟磷酸钠、氟化钾、氟化钾亚锡、氟锡酸钠、氯氟化亚锡、氟化胺、及其混合物,且所述氟化物化合物更优选为一氟磷酸钠和/或氟化钠。
根据另一个实施方案,至少一种活性剂与经表面反应的碳酸钙结合,所述活性剂优选为至少一种额外脱敏剂,且所述至少一种额外脱敏剂更优选选自:硝酸钾、戊二醛、硝酸银、氯化锌、六水合氯化锶、氟化钠、氟化亚锡、氯化锶、乙酸锶、精氨酸、羟基磷灰石、磷硅酸钙钠、草酸钾、磷酸钙、碳酸钙、生物活性玻璃及其混合物。
根据一个实施方案,通过包括以下步骤的方法获得经表面反应的碳酸钙:(a)提供天然或合成碳酸钙的悬浮体;(b)向步骤(a)的悬浮体添加至少一种在20℃下具有0或更小的pKa值或在20℃下具有0至2.5的pKa值的酸,以及(c)在步骤(b)之前、期间或之后用二氧化碳处理步骤(a)的悬浮体。根据另一个实施方案,通过包括以下步骤的方法获得经表面反应的碳酸钙:(A)提供天然或合成碳酸钙;(B)提供至少一种水溶性酸;(C)提供气态CO2;(D)使步骤(A)的所述天然或合成碳酸钙接触步骤(B)的至少一种酸和步骤(C)的CO2,所述方法的特征在于:(i)步骤B)的至少一种酸在20℃下具有大于2.5且小于或等于7的与其第一可用氢的电离相关的pKa,且在失去此第一可用氢时形成能够形成水溶性钙盐的对应的阴离子,以及(ii)在使所述至少一种酸与天然或合成碳酸钙接触之后,额外提供至少一种水溶性盐,其在含氢盐的情况下在20℃下具有大于7的与第一可用氢的电离相关的pKa,且其盐阴离子能够形成水不溶性钙盐。
根据一个实施方案,口腔护理组合物包含以所述组合物的总重量计1wt%至40wt%、优选1.5wt%至35wt%,更优选2wt%至30wt%的经表面反应的碳酸钙。根据另一个实施方案,口腔护理组合物为牙膏、牙粉或漱口剂,且其中经表面反应的碳酸钙优选为天然或合成碳酸钙与二氧化碳和磷酸的反应产物。
根据一个实施方案,口腔组合物还包含氟化物化合物,所述氟化物化合物优选选自:氟化钠、氟化亚锡、一氟磷酸钠、氟化钾、氟化钾亚锡、氟锡酸钠、氯氟化亚锡、氟化胺、及其混合物,且所述氟化物化合物更优选为一氟磷酸钠和/或氟化钠。
根据另一个实施方案,口腔护理组合物还包含额外的再矿化剂和/或增白剂,其优选选自:羟基磷灰石(例如纳米羟基磷灰石)、碳酸钙(例如非晶碳酸钙)及其与酪蛋白磷脂的组合、过氧化氢、过氧化脲、氟化物化合物,及其混合物。根据又一个实施方案,口腔护理组合物的pH为7.5至10,优选为8至9。
应当理解,出于本发明的目的,以下术语具有以下含义。
出于本发明的目的,“酸”定义为酸,即,其为H3O+离子提供者。“酸盐”定义为H3O+离子提供者,例如含氢盐,其被正电性元素部分中和。“盐”定义为由阴离子和阳离子形成的电中性离子化合物。“部分结晶盐”定义为在XRD分析时显示基本上离散的衍射图案的盐。
根据本发明,pKa为表示与给定酸中的给定可电离氢相关的酸解离常数的符号,且表示该氢在给定温度下在水中的平衡下从该酸的自然解离程度。可在例如Harris,D.C.“Quantitative Chemical Analysis:第3版”,1991,W.H.Freeman&Co.(USA),ISBN 0-7167-2170-8的参考教材中发现所述pKa值。
“研磨碳酸钙”(GCC)在本发明的含义中为从天然来源(例如石灰石、大理石、白云石或白垩)且通过例如旋风机或分类器通过湿处理和/或干处理(例如研磨、筛分和/或分级)加工的碳酸钙。
“沉淀碳酸钙”(PCC)在本发明的含义中为通过二氧化碳和石灰在水性、半干燥或潮湿环境中的反应之后的沉淀或通过钙离子源和碳酸根离子源在水中的沉淀获得的合成材料。PCC可呈球霰石、方解石或文石晶型。
为了本发明的目的,“经表面反应的碳酸钙”为包含碳酸钙和不溶、至少部分结晶的非碳酸钙盐(优选从至少部分碳酸钙的表面延伸)的材料。形成所述至少部分结晶的非碳酸钙盐的钙离子主要源自还用以形成经表面反应的碳酸钙核心的起始碳酸钙材料。所述盐可包括OH-阴离子和/或结晶水。
在本发明的含义中,“水不溶性”材料定义为当与去离子水混合且在20℃下在具有0.2μm孔径的过滤器上过滤以回收液体滤液时,100g所述液体滤液在95℃至100℃下蒸发之后提供小于或等于0.1g回收固体材料的材料。“水溶性”材料定义为使得100g所述液体滤液在95℃至100℃下蒸发之后回收大于0.1g回收固体材料的材料。
在整个本发明文件中,碳酸钙和其他材料的“粒度”由其粒度分布描述。值dx表示直径,相对于所述直径x重量%的颗粒具有小于dx的直径。这意味着d20值为20wt%的所有颗粒小于其的粒度,且d75值为75wt%的所有颗粒小于其的粒度。因此d50值为重量中值粒度,即50wt%的所有颗粒大于或小于此粒度。为了本发明的目的,除非另外指明,否则粒度规定为重量中值粒度d50。为测定重量中值粒度d50值,可使用沉降图(Sedigraph)。为了本发明的目的,经表面反应的钙的“粒度”描述为体积限定粒度分布。为测定经表面反应的碳酸钙的体积限定粒度分布,例如体积中值粒径(d50)或体积限定顶切粒度(d98),可使用Malvern Mastersizer 2000。如果所有颗粒的密度相等,则重量确定粒度分布可相当于体积限定粒度。
在本发明的含义中,碳酸钙的“比表面积(SSA)”定义为碳酸钙的表面积除以其质量。如本文中所用,使用BET等温线(ISO 9277:2010)通过氮气吸附测量比表面积且以m2/g规定。
在本发明的含义中,“口腔护理组合物”指的是适合于用在口腔且适用于兽医和/或人类应用但特别适用于人类口腔应用的组合物。
为了本发明的目的,术语“粘度”或“布氏粘度(Brookfield viscosity)”指的是布氏粘度。为此,通过布氏(RVT型)粘度计在20℃±2℃下以100rpm使用适当轴测量布氏粘度且以mPa·s规定。
在本发明的含义中,“悬浮体”或“浆料”包含不溶性固体和水,以及任选的其它添加剂,且通常含有大量固体,且因此比形成其的液体更粘且可具有更高的密度。
当术语“包含”用于本发明说明书和权利要求时,其不排除其它要素。为了本发明的目,术语“由……组成”视为术语“包含”的优选实施方案。如果下文中将组界定为包含至少某一数目的实施方案,则还应理解为公开优选仅由这些实施方案组成的组。
除非另外明确规定,否则当提及单数名词不使用数量词时,这包括所述名词的复数。
如“可获得”或“可界定”和“获得的”或“界定的”的术语可互换使用。此例如意味着除非上下文另作明确规定,否则术语“获得的”不指例如必须通过例如术语“获得的”之后的步骤顺序获得的实施方案,即使术语“获得的”或“界定的”始终包括所述受到限制的理解作为优选实施方案。
根据本发明,经表面反应的碳酸钙用于牙齿的再矿化和/或增白。经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和至少一种酸的反应产物。
在下文中,将更详述本发明经表面反应的碳酸钙的细节和优选实施方案。应当理解,这些技术细节和实施方案还适用于用于产生经表面反应的碳酸钙的本发明方法以及包含经表面反应的碳酸钙的本发明组合物。
经表面反应的碳酸钙
根据本发明,经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和至少一种酸的反应产物。
天然(或经研磨)碳酸钙(GCC)理解为碳酸钙的天然存在形式,其开采自例如石灰石或白垩的沉积岩或变质大理岩。已知碳酸钙主要以三种类型的晶体多晶型物存在:方解石、文石和球霰石。最常见的晶体多晶型物方解石被视为碳酸钙的最稳定晶型。文石较为少见,其具有离散或丛集的针状斜方晶系晶体结构。球霰石为最罕见的碳酸钙多晶型物,且通常不稳定。天然碳酸钙几乎完全为方解石型多晶型物,其称为三方菱面体且表示最稳定的碳酸钙多晶型物。在本发明的含义中,术语碳酸钙的“源”指的是从其获得碳酸钙的天然存在的矿物材料。碳酸钙的源可包含其它天然存在的组分,例如碳酸镁、硅酸铝等。
根据本发明的一个实施方案,天然碳酸钙选自:大理石、白垩、白云石、石灰石及其混合物。
根据本发明的一个实施方案,通过干磨获得GCC。根据本发明的另一个实施方案,GCC通过湿磨和任选的后续干燥获得。
通常,可用任何常规研磨装置例如在使得主要由与副体撞击造成粉碎的条件下进行研磨步骤,所述研磨装置即以下中的一种或更多种:球磨机、棒磨机、振动磨机、辊碎机、离心冲击磨机、垂直珠磨机、磨碎机、针磨机、锤磨机、磨粉机、撕碎机、碎料机、刀切割机或技术人员已知的其它此类设备。在含碳酸钙矿物材料包含含湿磨碳酸钙矿物材料的情况下,可在使发生自磨的条件下和/或通过水平球磨研磨和/或技术人员已知的其它此类方法进行研磨步骤。由此获得的湿加工含研磨碳酸钙矿物材料可通过熟知方法,例如通过絮凝、过滤或强制蒸发,先于干燥进行洗涤和脱水。后续干燥步骤可以单一步骤(例如喷雾干燥)进行或以至少两个步骤进行。还常见该矿物材料经历选矿步骤(例如浮选、漂白或磁性分离步骤)以移除杂质。
在本发明的含义中,“沉淀碳酸钙”(PCC)为合成材料,其通常通过二氧化碳与石灰在水环境中的反应之后沉淀或通过钙离子源和碳酸根离子源在水中沉淀或通过钙离子和碳酸根离子(例如,CaCl2和Na2CO3)沉淀出溶液获得。产生PCC的其它可能方式为石灰碱法,或Solvay法,其中PCC为合成氨的副产物。沉淀碳酸钙以三种主要晶型存在:方解石、文石和球霰石,且对于这些晶型中的每一者存在许多不同多晶型物(晶体惯态)。方解石具有三方结构,其典型晶体惯态例如偏三角面体(S-PCC)、菱面体(R-PCC)、六方棱柱形、轴面、胶状(C-PCC)、立方和棱柱形(P-PCC)。文石为斜方晶结构,其典型晶体惯态为孪生六方棱柱形晶体,以及不同类别的细长棱柱形、弯曲叶片状、陡锥状、凿状晶体、分枝树状和珊瑚或蠕虫状形式。球霰石属于六方晶系。所获得的PCC浆料可进行机械脱水和干燥。
根据本发明的一个实施方案,合成碳酸钙为沉淀碳酸钙,优选包含文石、球霰石或方解石矿物晶型或其混合物。
根据本发明的一个实施方案,天然或合成碳酸钙在用二氧化碳和至少一种酸处理之前经研磨。可用技术人员已知的任何常规研磨装置(例如研磨机)进行研磨步骤。
根据本发明的一个实施方案,天然或合成碳酸钙呈颗粒形式,所述颗粒具有等于或小于15μm、优选1μm至10μm、更优选2μm至8μm、且最优选3μm至7μm的重量中值粒度d50。根据本发明的另一个实施方案,天然或合成碳酸钙呈颗粒形式,所述颗粒具有等于或小于25μm、优选7μm至22μm、更优选10μm至20μm、且最优选15μm至18μm的顶切粒度d98。
优选地,待用于本发明中的经表面反应的碳酸钙制备为具有大于6.0,优选大于6.5,更优选大于7.0,甚至更优选大于7.5的在20℃下测量的pH的水性悬浮体。
在用于制备经表面反应的碳酸钙的水性悬浮体的一个优选方法中,精细粉碎的(例如通过研磨)或未经精细粉碎的天然或合成碳酸钙悬浮于水中。优选地,浆料具有以浆料的重量计1wt%至90wt%,更优选3wt%至60wt%,且甚至更优选5wt%至40wt%范围内的含量的天然或合成碳酸钙。
在下一步骤中,将至少一种酸添加至含有天然或合成碳酸钙的水性悬浮体中。所述至少一种酸可为在制备条件下产生H3O+离子的任何强酸、中强酸或弱酸,或其混合物。根据本发明,所述至少一种酸还可为在制备条件下产生H3O+离子的酸式盐。
根据一个实施方案,所述至少一种酸为在20℃下具有0或更小的pKa的强酸。根据另一个实施方案,所述至少一种酸为在20℃下具有0至2.5的pKa值的中强酸。若20℃下的pKa为0或更小,则所述酸优选选自硫酸、盐酸或其混合物。若20℃下的pKa为0至2.5,则所述酸优选选自H2SO3、H3PO4、草酸或其混合物。所述至少一种酸还可为酸式盐,例如HSO4-或H2PO4-(被例如Li+、Na+或K+的相应阳离子至少部分中和),或HPO42-(被例如Li+、Na+、K+、Mg2+或Ca2+的相应阳离子至少部分中和)。所述至少一种酸还可为一种或更多种酸和一种或更多种酸式盐的混合物。
根据又一个实施方案,所述至少一种酸为弱酸,所述弱酸当在20℃下测量时具有大于2.5且小于或等于7的与第一可用氢的电离相关的pKa值,且具有在此第一可用氢损失时形成的能够形成水溶性钙盐的相应阴离子。根据优选实施方案,弱酸在20℃下具有2.6至5的pKa值,且更优选所述弱酸选自:乙酸、甲酸、丙酸及其混合物。
在使用弱酸的情况下,在将所述酸添加至含有天然或合成碳酸钙的水性悬浮体中之后,另外添加至少一种水溶性盐,其在含氢盐的情况下,当在20℃下测量时,具有大于7的与第一可用氢的电离相关的pKa,且其盐阴离子能够形成水不溶性钙盐。所述水溶性盐的阳离子优选选自钾、钠、锂及其混合物。在一个更优选实施方案中,所述阳离子为钠。应当注意,根据阴离子电荷,可存在一种以上所述阳离子以提供电中性离子化合物。所述水溶性盐的阴离子优选选自磷酸盐、磷酸二氢盐、磷酸一氢盐、草酸盐、硅酸盐、其混合物和其水合物。在一个更优选实施方案中,所述阴离子选自磷酸盐、磷酸二氢盐、磷酸一氢盐、其混合物和其水合物。在一个最优选实施方案中,所述阴离子选自磷酸二氢盐、磷酸一氢盐、其混合物和其水合物。水溶性盐可逐滴或一步添加。在逐滴添加的情况下,此添加优选发生在10分钟的时间段内。更优选在一步中添加所述盐。
根据本发明的一个实施方案,所述至少一种酸选自:盐酸、硫酸、亚硫酸、磷酸、柠檬酸、草酸、乙酸、甲酸及其混合物。所述至少一种酸优选选自:盐酸、硫酸、亚硫酸、磷酸、草酸、H2PO4-(用例如Li+、Na+或K+的相应阳离子至少部分中和)、HPO42-(用例如Li+、Na+、K+、Mg2+或Ca2+的相应阳离子至少部分中和)、及其混合物,所述至少一种酸更优选选自:盐酸、硫酸、亚硫酸、磷酸、草酸或其混合物,且所述至少一种酸最优选为磷酸。不受任何理论束缚,本发明者相信使用磷酸可有益于牙齿的再矿化和/或增白。
所述至少一种酸可作为浓溶液或更稀释的溶液添加至悬浮体中。优选地,所述至少一种酸与天然或合成碳酸钙的摩尔比为0.05至4,更优选0.1至2。
作为一个替代方案,还有可能在悬浮天然或合成碳酸钙之前将所述至少一种酸添加至水中。
根据本发明,经表面反应的碳酸钙为用二氧化碳处理天然或合成碳酸钙获得。二氧化碳可通过酸处理原位形成和/或可来自外部源供应。如果例如硫酸或盐酸的强酸或例如磷酸的中强酸用于天然或合成碳酸钙的酸处理,则自动形成二氧化碳。或者或另外,二氧化碳可来自外部源供应。
根据一个实施方案,经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和至少一种酸的反应产物,其中二氧化碳为由于使至少一种酸与天然或合成碳酸钙接触而原位形成的和/或来自外部源供应的。
酸处理和用二氧化碳处理可同时进行,当使用强酸或中强酸时情况如此。还有可能例如用在20℃下具有0至2.5范围内的pKa的中强酸首先进行酸处理,其中原位形成二氧化碳,且因此,二氧化碳处理将自动与酸处理同时进行,接着进行用来自外部源供应的二氧化碳的额外处理。
优选地,悬浮体中气态二氧化碳的浓度以体积计为使得比率(悬浮体体积):(气态CO2体积)为1:0.05至1:20,甚至更优选1:0.05至1:5。
在一个优选实施方案中,酸处理步骤和/或二氧化碳处理步骤重复至少一次,更优选多次。根据一个实施方案,经过至少30分钟,优选至少45分钟且更优选至少1小时的时间段添加所述至少一种酸。
在酸处理和二氧化碳处理之后,在20℃下测量的水性悬浮体的pH自然地达到大于6.0、优选大于6.5、更优选大于7.0、甚至更优选大于7.5的值,从而将经表面反应的碳酸钙制备成具有大于6.0、优选大于6.5、更优选大于7.0、甚至更优选大于7.5的pH的水性悬浮体。如果允许水性悬浮体达到平衡,则pH大于7。当持续搅拌水性悬浮体足够时间段(优选1小时至10小时、更优选1小时至5小时)时,可在不添加碱的情况下调节到大于6.0的pH。
或者,在达到平衡(其在大于7的pH下发生)之前,可通过在二氧化碳处理之后添加碱来将水性悬浮体的pH增加至大于6的值。可使用任何常规碱,例如氢氧化钠或氢氧化钾。
关于制备经表面反应的天然碳酸钙的进一步细节公开于WO 00/39222 A1和US 2004/0020410 A1中,其中经表面反应的天然碳酸钙描述为用于造纸的填料。用弱酸制备经表面反应的碳酸钙公开于EP 2 264 108 A1中。制备经表面反应的碳酸钙及其在提纯工艺中的用途公开于EP 1 974 806 A1、EP 1 982 759 A1和EP 1 974 807 A1中。经表面反应的碳酸钙作为载体用于活性剂的受控释放的用途描述于WO 2010/037753 A1中。
类似地,获得经表面反应的沉淀碳酸钙。如可从EP 2 070 991 A1详细获知,通过在水性介质中使沉淀碳酸钙与H3O+离子接触且与溶解于水性介质中并能够形成水不溶性钙盐的阴离子接触以形成经表面反应的沉淀碳酸钙的浆料获得经表面反应的沉淀碳酸钙,其中所述经表面反应的沉淀碳酸钙包含形成于至少部分沉淀碳酸钙的表面上的所述阴离子的不溶的、至少部分结晶的钙盐。
所述溶解钙离子相当于相对于沉淀碳酸钙被H3O+离子溶解而自然产生的溶解钙离子的过量溶解钙离子,其中所述H3O+离子仅提供为阴离子的平衡离子形式,即通过添加呈酸或非钙酸盐形式的阴离子,且不存在任何其它钙离子或钙离子产生源。
所述过量溶解钙离子优选为通过添加可溶中性或酸性钙盐或通过添加酸或原位产生可溶中性或酸性钙盐的中性或酸性非钙盐来提供。
所述H3O+离子可通过添加酸或所述阴离子的酸式盐,或添加同时用以提供所有或部分所述过量溶解钙离子的酸或酸式盐来提供。
根据本发明的一个实施方案,通过包括以下步骤的方法获得经表面反应的碳酸钙:
a)提供天然或合成碳酸钙的悬浮体,
b)向步骤a)的悬浮体中添加至少一种在20℃下具有0或更小的pKa值或在20℃下具有0至2.5的pKa值的酸,以及
c)在步骤b)之前、期间或之后通过二氧化碳处理步骤a)的悬浮体。
根据一个实施方案,在步骤b)中将在20℃下具有0或更小的pKa值的至少一种酸添加至步骤a)的悬浮体中。根据另一个实施方案,在步骤b)中将在20℃下具有0至2.5的pKa值的至少一种酸添加至步骤a)的悬浮体中。
用于步骤c)中的二氧化碳可通过步骤b)的酸处理原位形成和/或可来自外部源供应。
根据本发明的一个实施方案,通过包括以下步骤的方法获得经表面反应的碳酸钙:
A)提供天然或合成碳酸钙,
B)提供至少一种水溶性酸,
C)提供气态CO2,
D)使步骤A)的所述天然或合成碳酸钙与步骤B)的至少一种酸和步骤C)的CO2接触,
其特征在于:
i)步骤B)的所述至少一种酸在20℃下具有大于2.5且小于或等于7的与其第一可用氢的电离相关的pKa,且在此第一可用氢损失时形成能够形成水溶性钙盐的相应阴离子,以及
ii)在使所述至少一种酸与天然或合成碳酸钙接触之后,另外提供至少一种水溶性盐,其在含氢盐的情况下在20℃下具有大于7的与第一可用氢的电离相关的pKa,且其盐阴离子能够形成水不溶性钙盐。
经表面反应的碳酸钙可保持在悬浮体中,任选地通过分散剂进一步稳定。可使用技术人员已知的常规分散剂。优选分散剂为聚丙烯酸和/或羧甲基纤维素。
或者,可干燥上述水性悬浮体,从而获得呈颗粒或粉末形式的固体(即干燥的或含有使其不呈流体形式的极少水)经表面反应的天然或合成碳酸钙。
根据本发明的一个实施方案,经表面反应的碳酸钙具有5m2/g至200m2/g,更优选20m2/g至80m2/g且甚至更优选30m2/g至60m2/g的比表面积,所述比表面积为使用氮气和根据ISO 9277的BET法测量。
根据本发明的一个实施方案,经表面反应的碳酸钙呈颗粒形式,所述颗粒具有等于或小于15μm、优选1μm至10μm、更优选2μm至8μm且最优选3μm至7μm的体积中值粒径(d50)。根据本发明的另一个实施方案,经表面反应的碳酸钙呈颗粒形式,所述颗粒具有等于或小于25μm、优选7μm至22μm、更优选10μm至20μm且最优选15μm至18μm的体积限定顶切粒度(d98)。根据本发明的一个优选实施方案,经表面反应的碳酸钙呈颗粒形式,所述颗粒具有等于或小于15μm、优选1μm至10μm、更优选2μm至8μm且最优选3μm至7μm的体积中值粒径(d50),且具有等于或小于25μm、优选7μm至22μm、更优选10μm至20μm且最优选15μm至18μm的体积限定顶切粒度(d98)。体积中值粒径(d50)和体积限定顶切粒度(d98)可通过激光衍射测量(例如通过使用Malvern Mastersizer 2000)测定。
根据本发明的一个实施方案,经表面反应的碳酸钙包含至少一种酸的阴离子的不溶的、至少部分结晶的钙盐,其形成于天然或合成碳酸钙的表面上。根据一个实施方案,至少一种酸的阴离子的不溶的、至少部分结晶的盐至少部分地、优选完全地覆盖天然或合成碳酸钙的表面。根据所采用的至少一种酸,阴离子可为硫酸根、亚硫酸根、磷酸根、柠檬酸根、草酸根、乙酸根、甲酸根和/或氯离子。
根据一个优选实施方案,经表面反应的碳酸钙为天然碳酸钙与至少一种酸(优选磷酸)的反应产物。
经表面反应的碳酸钙具有好的负载容量且在口腔护理中可用作载体。例如,经表面反应的碳酸钙能够结合和运输活性剂。结合优选为吸收至经表面反应的碳酸钙颗粒的表面上,所述表面为颗粒的外表面或内表面,或吸收至颗粒中,由于颗粒的多孔性这是可能的。
在这方面,普遍认为由于表面反应碳酸钙的孔隙内和孔隙间结构,此材料相对于具有相似比表面积的常用材料为随时间推移而递送预先吸附/吸收的材料的优良试剂。
经表面反应的碳酸钙可具有从水银孔隙度计测量计算出的5vol%至50vol%,优选20vol%至50vol%、且更优选30vol%至50vol%的颗粒内孔隙度。从双峰衍生孔径分布曲线,峰之间的最低点表明可分隔颗粒内和颗粒间孔隙体积的直径。直径大于此直径的孔隙体积为与颗粒间孔隙有关的孔隙体积。总孔隙体积减去此颗粒间孔隙体积得到颗粒内孔隙体积,由颗粒内孔隙体积可计算出颗粒内孔隙度,优选为固体材料体积分数形式,如Transport in Porous Media(2006)63:239-259中所描述。
关于经表面反应的碳酸钙的孔隙度和其作为试剂用于传递材料的用途的进一步细节可在WO 2010/037753 A1中找到。
因此,通常,适合经表面反应的碳酸钙载体的颗粒内和/或颗粒间孔隙的任何药剂皆适合于通过本发明的经表面反应的碳酸钙载体来运输。例如,可使用例如选自医药活性剂、生物活性剂、消毒剂、防腐剂(如三氯生)、调味剂、表面活性剂(如消泡剂)或额外的脱敏剂的活性剂。根据一个实施方案,至少一种活性剂与经表面反应的碳酸钙结合。根据一个优选实施方案,活性剂为至少一种额外脱敏剂,其优选选自:硝酸钾、戊二醛、硝酸银、氯化锌、六水合氯化锶、氟化钠、氟化亚锡、氯化锶、乙酸锶、精氨酸、羟基磷灰石、磷硅酸钙钠、草酸钾、磷酸钙、碳酸钙、生物活性玻璃、及其混合物。羟基磷灰石(还称为羟磷灰石)为天然存在的具有式Ca5(PO4)3(OH)的钙磷灰石的矿物形式。根据一个示例性实施方案,羟基磷灰石为纳米尺寸羟基磷灰石,还称为纳米羟基磷灰石。
口腔护理组合物
用于根据本发明用途的口腔护理组合物包含经表面反应的碳酸钙,其中所述经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和至少一种酸的反应产物。
根据本发明的一个实施方案,以组合物的总重量计,所述组合物包含1wt%至40wt%、优选1.5wt%至35wt%、更优选2wt%至30wt%的经表面反应的碳酸钙。
经表面反应的碳酸钙可仅由一种类型的经表面反应的碳酸钙组成或可为两种或两种以上类型的经表面反应的碳酸钙的混合物。本发明的口腔护理组合物可含有经表面反应的碳酸钙作为唯一的再矿化剂和/或增白剂。或者,本发明的口腔护理组合物可含有与至少一种额外的再矿化剂和/或增白剂组合的经表面反应的碳酸钙。
根据一个实施方案,口腔护理组合物包含至少一种额外再矿化剂。额外再矿化剂优选选自:羟基磷灰石(例如纳米羟基磷灰石)、碳酸钙(例如非晶碳酸钙)及其与酪蛋白磷脂的组合、及其混合物。非晶碳酸钙为碳酸钙的非晶且最不稳定的多晶型物,且除几个特殊生物体外未在天然情况下发现所述非晶碳酸钙。
根据另一个实施方案,口腔护理组合物包含至少一种额外增白剂。所述额外增白剂可为漂白剂、研磨剂、再矿化剂,且优选选自:过氧化氢、过氧化脲、羟基磷灰石、碳酸钙、氟化物化合物、及其混合物。
根据本发明的一个实施方案,所述至少一种额外再矿化剂和/或增白剂选自:羟基磷灰石(例如纳米羟基磷灰石)、碳酸钙(例如非晶碳酸钙)及其与酪蛋白磷脂的组合、过氧化氢、过氧化脲、氟化物化合物、及其混合物。
根据一个实施方案,所述额外再矿化剂和/或增白剂的重量中值粒度d50为10nm至100μm,优选为0.1μm至50μm,更优选为1μm至20μm,且最优选为2μm至10μm。
以组合物的总重量计,所述至少一种额外再矿化剂和/或增白剂可以1wt%至20wt%,优选1.5wt%至15wt%,更优选2wt%至10wt%的量存在于口腔护理组合物中。
根据一个实施方案,本发明的口腔护理组合物包含以组合物的总重量计1wt%至40wt%的经表面反应的碳酸钙和1wt%至20wt%的额外的再矿化剂和/或增白剂。
本发明的口腔护理组合物可为例如牙膏、牙粉、清漆、粘合凝胶、粘接剂、树脂、喷雾、泡沫、香膏、口腔带或口腔粘合贴片上带有的组合物、咀嚼片、咀嚼锭剂、咀嚼胶、含片、饮料或漱口剂。根据本发明的一个实施方案,口腔护理组合物为牙膏、牙粉或漱口剂,且优选为牙膏。
根据一个优选实施方案,口腔护理组合物为牙膏、牙粉或漱口剂,且经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和磷酸的反应产物。根据另一个优选实施方案,口腔护理组合物为牙膏、牙粉或漱口剂且经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和磷酸的反应产物,其中所述经表面反应的碳酸钙呈颗粒形式,所述颗粒具有等于或小于15μm、优选1μm至10μm、更优选2μm至8μm且最优选3μm至7μm的体积中值粒径(d50),和/或等于或小于25μm、优选7μm至22μm、更优选10μm至20μm且最优选15μm至18μm的体积限定顶切粒度(d98)。
根据本发明的一个实施方案,口腔护理组合物具有7.5至10,优选8至9的pH。
经表面反应的碳酸钙可与氟化物化合物组合使用。本发明者惊讶地发现经表面反应的碳酸钙与氟化物化合物的组合引起改善的牙齿的再矿化和/或增白。
根据一个优选实施方案,口腔组合物还包含氟化物化合物。所述氟化物化合物可选自:氟化钠、氟化亚锡、一氟磷酸钠、氟化钾、氟化钾亚锡、氟锡酸钠、氯氟化亚锡、氟化胺,及其混合物。氟化物化合物优选为一氟磷酸钠和/或氟化钠。可通过使用一定量的氟化物化合物以在口腔护理组合物中得到在300ppm至2000ppm范围内(优选约1450ppm)的可用氟离子来获得良好的结果。
根据一个实施方案,提供一种用于牙齿的再矿化和/或增白的口腔护理组合物,其优选为牙膏、牙粉或漱口剂,其包含经表面反应的碳酸钙,其中所述经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和至少一种酸(优选磷酸)的反应产物,且其中所述口腔组合物还包含氟化物化合物,所述氟化物化合物优选选自:氟化钠、氟化亚锡、一氟磷酸钠、氟化钾、氟化钾亚锡、氟锡酸钠、氯氟化亚锡、氟化胺,及其混合物,且更优选选自一氟磷酸钠和/或氟化钠。
除经表面反应的碳酸钙、任选的额外再矿化剂和/或增白剂和任选的氟化物化合物外,口腔护理组合物还可包含生物粘合聚合物、表面活性剂、粘合剂、保湿剂、脱敏剂、调味剂、甜味剂和/或水。
根据本发明的一个实施方案,口腔护理组合物包含生物粘合聚合物。生物粘合聚合物可包括促进经表面反应的碳酸钙粘合于牙齿或牙齿表面且保持在牙齿或牙齿表面上持续例如1小时、3小时、5小时、10小时、24小时的较长时间段的任何聚合物。在某些实施方案中,生物粘合聚合物在口腔护理组合物用例如水或唾液湿润时可变得粘合性更高。在另一些实施方案中,生物粘合聚合物为增强活性成分在施用组合物的牙齿或牙齿表面上的保持力的材料或材料组合。所述生物粘合聚合物包括例如亲水性有机聚合物、疏水性有机聚合物、有机硅胶、二氧化硅、及其组合。根据一个实施方案,生物粘合聚合物选自:甲基丙烯酸羟乙酯、PEG/PPG共聚物、聚乙烯甲基醚/马来酸酐共聚物、聚乙烯吡咯烷酮(PVP)、交联PVP、虫胶、聚氧化乙烯、甲基丙烯酸酯、丙烯酸酯共聚物、甲基丙烯酸类共聚物、乙烯吡咯烷酮/乙酸乙烯酯共聚物、聚乙烯己内酰胺、聚交酯、有机硅树脂、有机硅粘合剂、壳聚糖、乳蛋白(酪蛋白)、牙釉质蛋白基因、酯胶、及其组合。
适合的表面活性剂在整个宽pH范围内通常为阴离子性有机合成表面活性剂。以口腔护理组合物的总重量计,在约0.5wt%至5wt%的范围内使用的所述表面活性剂的代表为以下的水溶性盐:C10-C18烷基硫酸盐(如月桂基硫酸钠)、脂肪酸的磺化单甘油酯(如单甘油磺酸钠)、牛磺酸的脂肪酸酰胺(如N-甲基-N-棕榈酰基牛磺酸钠)和羟乙基磺酸的脂肪酸酯和脂族丙烯酰胺(如N-十二酰基肌氨酸钠)。然而,还可使用从天然来源获得的表面活性剂,如椰油酰胺基丙基甜菜碱。
提供所需稠度的适合的粘合剂或增稠剂为例如羟乙基纤维素、羧基甲基纤维素钠、天然胶(如刺梧桐胶、阿拉伯胶、黄蓍胶、黄原胶或纤维素胶)、胶体硅酸盐或经精细粉碎的二氧化硅。通常,可使用以口腔护理组合物的总重量计的0.5wt%至5wt%。
脱敏剂可选自:硝酸钾、戊二醛、硝酸银、氯化锌、六水合氯化锶、氟化钠、氟化亚锡、氯化锶、乙酸锶、精氨酸、羟基磷灰石、磷硅酸钙钠、草酸钾、磷酸钙、碳酸钙、生物活性玻璃、及其混合物。
可例如基于口腔护理组合物的总重量以20wt%至40wt%的量使用普通技术人员已知的多种保湿剂,如丙三醇、山梨糖醇和其它多元醇。适合的调味剂的实例包括冬青油、绿薄荷油、薄荷油、丁香油、黄樟油等。可例如基于口腔护理组合物的总重量以0.01wt%至1wt%的量将糖精、阿斯巴甜、右旋糖或果糖用作甜味剂。如苯甲酸钠的防腐剂可基于口腔护理组合物的总重量以0.01wt%至1wt%的量存在。还可例如基于口腔护理组合物的总重量以0.01wt%至1.5wt%的量将如二氧化钛的着色剂添加至口腔护理组合物中。
本发明的口腔护理组合物还可含有选自以下的材料:二氧化硅、沉淀二氧化硅、氧化铝、铝硅酸盐、偏磷酸盐、磷酸三钙、焦磷酸钙、研磨碳酸钙、沉淀碳酸钙、碳酸氢钠、膨润土、高岭土、氢氧化铝、磷酸氢钙、羟基磷灰石、及其混合物。所述材料可根据口腔护理组合物的总重量以1wt%至40wt%的量存在。根据一个实施方案,口腔护理组合物含有选自研磨碳酸钙和/或沉淀二氧化硅的材料。根据另一个实施方案,口腔护理组合物含有选自以下的材料:研磨碳酸钙、沉淀碳酸钙、氢氧化铝、磷酸氢钙、二氧化硅、羟基磷灰石、及其混合物。根据本发明的一个优选实施方案,口腔护理组合物包含经表面反应的碳酸钙,其中所述经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和至少一种酸的反应产物,且碳酸钙优选为研磨碳酸钙和/或沉淀碳酸钙。
根据本发明的一个实施方案,口腔护理组合物为牙膏。牙膏可通过包括以下步骤的方法制造:
I)提供水和保湿剂和任选的增稠剂、防腐剂、氟化物和甜味剂中的至少一者的混合物,
II)将经表面反应的碳酸钙和任选的着色剂添加至步骤I)的混合物中,其中所述经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和至少一种酸的反应产物,
III)将表面活性剂添加至步骤II)的混合物中,以及
IV)任选地添加调味剂至步骤III)的混合物中。
然而,本发明的牙膏还可通过普通技术人员已知的任何其它方法产生。
治疗和美容用途
发现经表面反应的碳酸钙可用于牙齿的再矿化和/或增白。根据本发明的一个实施方案,提供一种用于牙齿再矿化的经表面反应的碳酸钙,其中所述经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和至少一种酸的反应产物。根据本发明的另一个实施方案,提供一种用于牙釉质增白的经表面反应的碳酸钙,其中所述经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和至少一种酸的反应产物。根据本发明的又一个实施方案,提供一种用于再矿化和牙齿增白的经表面反应的碳酸钙,其中所述经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和至少一种酸的反应产物。
根据本发明的另一方面,提供一种用于牙齿的再矿化和/或增白的口腔护理组合物,其包含经表面反应的碳酸钙,其中所述经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和至少一种酸的反应产物。根据一个实施方案,提供一种用于牙齿再矿化的口腔护理组合物,其包含经表面反应的碳酸钙,其中所述经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和至少一种酸的反应产物。根据另一个实施方案,提供一种用于牙齿增白的口腔护理组合物,其包含经表面反应的碳酸钙,其中所述经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和至少一种酸的反应产物。根据又一个实施方案,提供一种用于再矿化和牙齿增白的口腔护理组合物,其包含经表面反应的碳酸钙,其中所述经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和至少一种酸的反应产物。
本发明的发明人惊讶地发现经表面反应的碳酸钙可用于牙齿的再矿化和/或增白。经表面反应的碳酸钙在多个方面中不同于常规碳酸钙。例如,不同于常规碳酸钙,经表面反应的碳酸钙包含多孔、板状或薄层状表面结构。不受任何理论束缚,普遍认为在将经表面反应的碳酸钙施用于例如患者牙齿上期间,经表面反应的碳酸钙断裂成片,从而使多孔板状或薄层状表面结构要素从所述经表面反应的碳酸钙的表面裂开。所述裂开的多孔板状或薄层状表面结构要素可提供对牙釉质的粘合性改善。
此外,表面处理使得经表面反应的碳酸钙对酸更具抗性。因此,经表面反应的碳酸钙在酸性条件下,例如在摄取酸性饮料(如软饮料)或酸式菜肴(如具有醋类调料的色拉)期间更稳定。本发明的经表面反应的碳酸钙的另一优点为其可在微米粒度范围内使用,且由此可避免使用纳米尺寸化颗粒。
本发明人还惊讶地发现经表面反应的碳酸钙适于使牙齿表面变平滑。不受任何理论束缚,普遍认为由经表面反应的碳酸钙的断裂而生成的裂开的多孔板状或薄层状表面结构要素粘附于釉质表面且密封表面缺陷,且由此使得釉质表面更光滑。此外,普遍认为更光滑的表面可防止或降低细菌和染色剂的附着性,其进行可降低不良口气和龋齿的风险。
根据另一个方面,提供一种用于使牙齿表面平滑的经表面反应的碳酸钙,其中所述经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和至少一种酸的反应产物。根据又一个方面,提供一种用于使牙齿表面平滑的口腔护理组合物,其包含经表面反应的碳酸钙,其中所述经表面反应的碳酸钙为天然或合成碳酸钙与二氧化碳和至少一种酸的反应产物。
本发明的经表面反应的碳酸钙和/或包含其的口腔组合物可用于专业、诊室内治疗或在家治疗。
根据一个实施方案,用于牙齿的再矿化和/或增白的经表面反应的碳酸钙用于包含以下步骤的方法:向患者的至少一颗牙齿施用治疗有效量的经表面反应的碳酸钙至少一天一次,优选一天两次且更优选一天三次。经表面反应的碳酸钙的“治疗有效”量为当以本发明的方式使用时足以在施用活性剂的人类受试者中起到期望的治疗或预防作用而无不当的不良副作用(如毒性、刺激或过敏反应)、与合理的效益/风险比相匹配的量。特定有效量将随例如以下的因素变化:治疗的具体状况、受试者的身体状况、同步疗法(如果有的话)的性质、特定剂型、所采用的口腔护理组合物和期望的给药方案。
根据一个实施方案,用于牙齿的再矿化和/或增白的口腔组合物用于包括以下步骤的方法:向患者的至少一颗牙齿施用所述组合物有效量的时间,所述组合物优选在至少一颗牙齿上保持至少1分钟,至少15分钟,至少30分钟,至少1小时,至少2小时,至少12小时或至少24小时。
本发明的经表面反应的碳酸钙或包含本发明的经表面反应的碳酸钙的口腔组合物甚至在无任何氧化增白化合物存在下也可有效用于牙齿增白。根据本发明的一个优选实施方案,口腔护理组合物不含氧化增白化合物。
根据一个实施方案,本发明的经表面反应的碳酸钙或包含本发明的经表面反应的碳酸钙的口腔组合物在用于增白牙齿的美容方法中使用,其包括向个体的至少一颗牙齿施用所述组合物有效量时间的步骤,所述组合物优选在至少一颗牙齿上保持至少1分钟,至少15分钟,至少30分钟,至少1小时,至少2小时,至少12小时或至少24小时。
基于下列图和实施例将更好地理解本发明的范围和关注点,所述图和实施例旨在说明本发明的某些实施方案且为非限制性的。
附图说明
图1示出实施例1制备的牙膏样品的表面显微硬度(surface micro hardness,SMH)测量结果的曲线图。
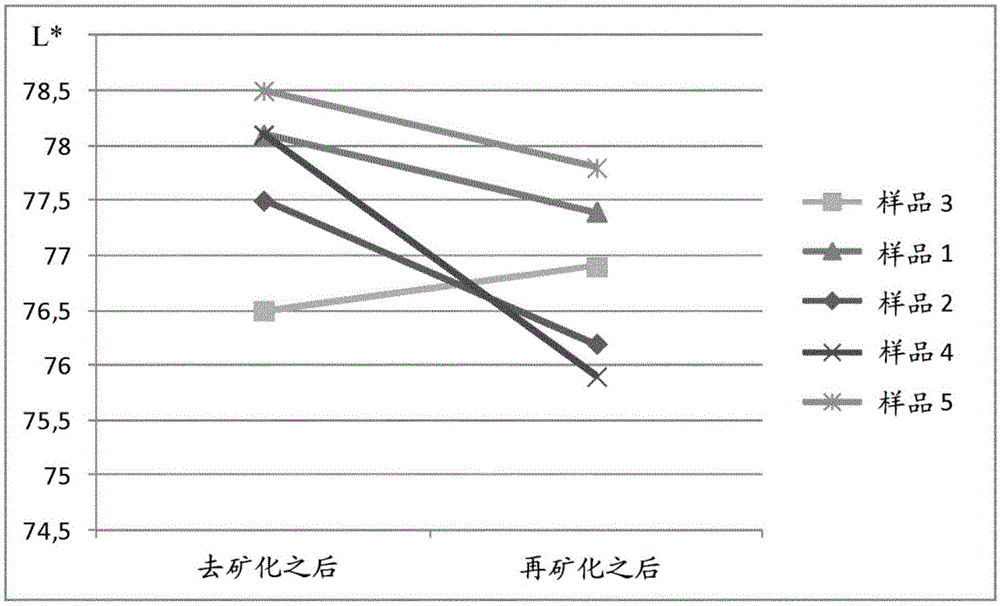
图2示出对实施例1制备的牙膏样品确定的CIELAB L*坐标值的图。
图3示出对实施例1制备的牙膏样品确定的CIELAB b*坐标值的图。
图4示出去矿化的牛牙釉质样品的扫描电子显微镜(SEM)显微图。
图5示出去矿化的牛牙釉质样品的扫描电子显微镜(SEM)显微图。
图6示出用实施例1的本发明牙膏样品1处理的再矿化牛牙釉质样品的扫描电子显微镜(SEM)显微图。
图7示出用实施例1的本发明牙膏样品1处理的再矿化牛牙釉质样品的扫描电子显微镜(SEM)显微图。
实施例
1.测量方法
在下文中,描述了在实施例中实施的测量方法。
粒度分布
使用来自美国Micromeritics公司的Sedigraph 5100测量非经表面反应的碳酸钙颗粒,例如研磨碳酸钙的粒度分布。方法和仪器为技术人员已知且通常用于测定填料和颜料的粒径。测量在包含0.1wt%Na4P2O7的水溶液中进行。使用高速搅拌器和超声分散样品。对于分散样品的测量,不添加其它分散剂。
使用Malvern Mastersizer 2000激光衍射系统(英国,Malvern Instruments Plc.,)测定经表面反应的碳酸钙的体积中值粒径(d50)。
比表面积(SSA)
通过在250℃下加热30分钟的时间段调整样品条件之后,通过使用氮气根据ISO 9277的BET法测量比表面积。在这些测量之前,在Büchner漏斗内过滤样品、用去离子水冲洗且在烘箱中在90-100℃下干燥过夜。随后在研钵中彻底研磨干滤饼,且所得粉末置于130℃下的水分天平中直至达到恒重。
扫描电子显微镜(SEM)显微图
通过Sigma VP场发射扫描电子显微镜(Carl Zeiss AG,德国)和具有约50Pa的腔室压力的变压二次电子探测器(VPSE)检测所制备的牛牙釉质样品。
2.材料
MCC:基于研磨碳酸钙和磷酸的经表面反应的碳酸钙(d50=6.54μm,d98=16.8μm,SSA=25.1m2/g)。所述研磨碳酸钙(d50=3μm,d98=12μm)从法国Orgon获得,且其可购自瑞士Omya AG。
GCC:从意大利Avenza-Carrara获得的天然研磨碳酸钙(d50=5μm,d98=30μm),其可购自瑞士Omya AG。
3.实施例
实施例1-牙膏组合物
牙膏样品1至4根据以下过程使用汇编于下表1中的成分和量制造。
步骤A:在烧杯中混合水和山梨糖醇。混合黄原胶、苯甲酸钠、一氟磷酸钠(phoskadent Na 211,BK Giulini,德国)和糖精钠并将所获得的混合物添加至烧杯中。
步骤B:分别用水润湿MCC或GCC和二氧化钛,且随后添加至步骤A的混合物中。均质化所述混合物直至获得均匀的混合物。
步骤C:在均质化条件下将二氧化硅Sorbosil TC 15(PQ公司,美国)添加至步骤B的混合物中,由此混合物剧烈变热。搅拌混合物直至其冷却至室温。
步骤D:在缓慢搅动下以25%的溶液形式将表面活性剂月桂基硫酸钠添加至步骤C的混合物中。
步骤E:将0.8wt%(2.4g)的绿薄荷调味剂添加至步骤D的混合物中。
表1:牙膏样品1至4的成分和量。百分比指以组合物的总重量计的重量百分比。
实施例2-再矿化研究
牛牙釉质样品如下制备:
切割出牛牙釉质块(4mm×4mm),将其平面平行地重叠并对其手工抛光。使用具有Knoop压头和MicroMet MHT软件的MicroMet 5103硬度测试机(Buehler Ltd.,美国)以50g负载、10s压进时间和每块5个压痕测定平均基线表面显微硬度(SMH)值。
在37℃和pH 4.6下,使牛牙釉质样品在1:1 8%甲基纤维素/乳酸凝胶系统中去矿化14天。在去矿化之后,测量各样品的SMH。样品分层进入10个块的槽内,其中向实施例1的四种牙膏样品中的每一者提供一个槽。此外,市售的无氟二氧化硅牙膏样品(Boots Smile无氟薄荷牙膏,可购自Boots UK Ltd.,英国)在另一槽上作为样品5测试且再使用三个槽以弥补损耗。
使样品经受以下处理:用含有5UI/ml磷酸酶的3:1水:牙膏浆料处理5分钟;用酸性缓冲剂(50mM乙酸、1.50mM二水合氯化钙、0.90mM正磷酸二氢钾、130mM氯化钾,pH 5.0)处理30分钟;且用中性缓冲剂(20mM HEPES、1.50mM二水合氯化钙、0.90mM正磷酸二氢钾、130mM氯化钾,pH 7.0)处理10分钟。每天重复此循环6次,持续8天。
完成该循环之后,将样品留在中性缓冲剂中过夜。在pH循环之前和之后通过对样品的SMH分析来评估功效。每个样品取10个读数且再矿化表示为SMH的改变。在去矿化之后和再矿化之后,使用CR321 Konika Minolta色度计(Konica Minolta,Inc.,日本)记录在SMH基线测量下所有块的CIELAB坐标L*a*b*。此外,通过Sigma VP场发射扫描电子显微镜(Carl Zeiss AG,德国)和具有约50Pa的腔室压力的变压二次电子侦测器(VPSE)检测样品的表面结构。
再矿化研究的结果展示于图1至图7中。
从图1中示出的表面显微硬度(SMH)测量结果可推测氟化牙膏样品二者(样品1和样品3)促进再矿化至显著大于无氟对照制剂的程度。
CIELAB坐标的测量显示去矿化之后所有经测试的样品的L*值增加(post demin:去矿化之后;post remin:再矿化之后)。这由牙釉质的去钙化造成,其中产生所谓的白斑病灶。除牙膏样品4(不含氟化物的GCC)外,所有经测试的样品的L*值(亮度的立方)在再矿化之后降低(参见图2),其为再矿化的证据。
在图3中示出的b*坐标的测量显示所有牙釉质样品具有负的b*值(post demin:去矿化之后;post remin:再矿化之后)。负的b*值意为所记录的图像具有蓝色色调,其意为所有牙釉质样品呈蓝白色,其通常被感知为极明亮的白色。由含有经表面反应的碳酸钙且不含氟化物的牙膏(样品2)再矿化的牙釉质样品显示最负的b*值,且因此显示最好的增白效果。
图4和图5示出去矿化之后牙釉质样品的扫描电子显微镜(SEM)显微图,且图6和图7示出经牙膏样品1处理的牙釉质样品的SEM显微图。图4和图5中清晰可见牙釉质表面的裂缝和不均匀性,而图6和图7证明牙釉质表面在经本发明的牙膏再矿化之后看起来更光滑且更均匀。
- 还没有人留言评论。精彩留言会获得点赞!