制剂的制作方法
在最广泛的方面,本发明涉及控制鱼类疾病的领域。更具体而言,本发明涉及用于控制寄生虫侵袭例如由海虱的侵袭的可注射制剂。
背景技术:
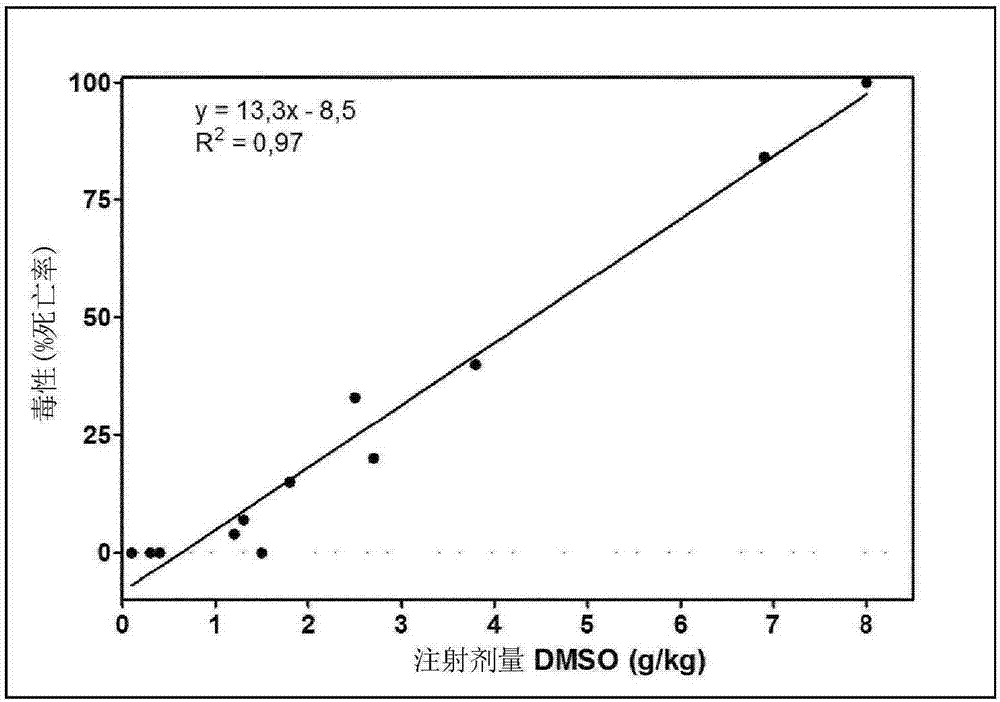
:寄生虫侵袭在鱼类养殖业中构成相当大的问题。特别是由海虱(例如鲑疮痂鱼虱(lepeophtheirussalmonis)、细长鱼虱(caliguselongatus)和智利鱼虱(caligusrogercresseyi))的侵袭视为鲑科养殖中,尤其是在大西洋鲑鱼(盐湖鲑鱼(salmosalar))和虹鳟鱼(虹鳟(oncorhynchusmykiss))中最重要的疾病问题之一。寄生虫针对目前可获得的产品发展抗性呈现了鱼业的主要问题。商业鱼类养殖中的寄生虫控制在很大程度上涉及用诸如有机磷酸酯、拟除虫菊酯和过氧化氢的物质的浴处理。可替代地,例如几丁质合成抑制剂或大环内酯的物质可经口施用,例如与饲料混合,并且可有效针对鱼类的寄生虫病。也可借助于腹膜内注射对鱼施用治疗,然而这需要鱼的广泛处理,引起应激和潜在的死亡,因为鱼必须在容纳罐和含有麻醉剂的罐之间泵送。由于现代水产养殖的大规模,这种处理方案是劳动密集和昂贵的。然而,先前已描述了适合于腹膜内注射的几丁质合成抑制剂的水性制剂。wo99/063824公开了包括氟铃脲的抑制剂的水性制剂,然而该制剂仅提供相对低的生物利用度。wo2014/016252公开了包含纳米颗粒氟铃脲或虱螨脲的水性悬浮液的可注射制剂。需要用于治疗鱼类寄生虫侵袭的改进制剂,其中所述制剂递送高的生物利用度,随着时间过去是生理化学稳定的,并且可以工业上方便的方式施用。目前已惊讶地发现可生产非水性可注射制剂,其包含在均相非水性溶液中的杀寄生虫剂。此外,这些制剂是抗寄生虫有效的,对鱼无毒,证明良好的抑制剂稳定性和生物利用度,并且在施用后延长的时间段提供针对寄生虫的有力保护。技术实现要素:根据本发明的第一个方面,提供了杀寄生虫剂制剂。当通过腹膜内注射施用时,该制剂对鱼无毒。该制剂是均相非水性杀寄生虫剂溶液,并且该制剂包含:(a)亲水性聚合物;和/或,(b)以按重量计5-40%的量存在的非水极性溶剂,和增溶剂。在一些实施例中,制剂包含亲水性聚合物。在一些实施例中,制剂包含亲水性聚合物和以按重量计5-40%的量存在的非水极性溶剂。在一些实施例中,制剂包含亲水性聚合物、以按重量计5-40%的量存在的非水极性溶剂、和增溶剂。在一些实施例中,制剂包含以按重量计5-40%的量存在的非水极性溶剂、和增溶剂。当在约17℃的水温下通过腹膜内注射施用于大西洋鲑鱼(24-26克)时,该制剂诱导:(a)当以0.05ml的量施用时,无死亡率增加;和,(b)当以0.2ml的量施用时,死亡率的至多40%的增加。相对于对照处理组,换言之,相对于通过以0.05ml或适当时0.2ml的量的腹膜内注射施用对照制剂例如pbs的相同鱼群,在7天后测定增加的死亡率。在一些实施例中,当通过腹膜内注射施用时,制剂对鲑科无毒。在一些实施例中,制剂适合于通过宿主鱼的腹膜内注射来治疗海虱。在制剂的制备期间不添加水。然而,如技术人员将了解的,在一些情况下,由于例如组成成分试剂中的一种或多种的吸湿性质,少量的水可存在于制剂中。因此,制剂是非水性溶液,并且含有至多4%、3%或2%,且优选至多1.5%、1%或0.5%的水。该制剂是均相的,并且由单一的均匀非水相组成。该制剂不包含悬浮液、分散体或乳液,并且是非胶束或基本上非胶束溶液。杀寄生虫剂可不溶于水。杀寄生虫剂可具有小于0.1mg/ml的在水中的溶解度。杀寄生虫剂可包含几丁质合成抑制剂。几丁质合成抑制剂可由下述之一或组合组成或包含下述之一或组合:氟铃脲、除虫脲、虱螨脲、溴氰菊酯、伊维菌素或依马菌素。优选地,杀寄生虫剂是氟铃脲、除虫脲或虱螨脲之一或组合,并且最优选地,杀寄生虫剂包含氟铃脲。在一些实施例中,制剂包含在亲水性聚合物中的溶液中的杀寄生虫剂。在这些实施例中,杀寄生虫剂可以10-150mg/ml,例如15-120、20-100、90-100、25-90或30-80mg/ml的量存在于制剂中。在一些实施例中,制剂包含在亲水性聚合物(例如peg400)和非水极性溶剂(例如dmso)的组合中的溶液中的杀寄生虫剂。非水极性溶剂可以按重量计5-40%,例如按重量计约15%的量存在于制剂中。在这些实施例中,杀寄生虫剂可以10-300mg/ml,例如50-260、60-200、70-180、75-140、80-130、85-120、或90-100mg/ml的量存在于制剂中。优选地,杀寄生虫剂以约90mg/ml的量存在于制剂中。在其中制剂包含在亲水性聚合物中的溶液中的杀寄生虫剂的实施例中,制剂还可包含增溶剂。在一些实施例中,制剂包含在非水极性溶剂中的溶液中的杀寄生虫剂。非水极性溶剂以按重量计5-40%的量存在,并且制剂还包含增溶剂。在这些实施例中,杀寄生虫剂可以10-300mg/ml,例如50-260、60-230、70-190、75-170、80-150、85-120、或90-100mg/ml的量存在于制剂中。当非水极性溶剂以较低的量,例如小于35%,小于30%,小于25%,例如或10-20%的量存在于制剂中时,杀寄生虫剂可以10-300mg/ml,例如50-230、70-190、75-170、80-150、85-120,最优选90-100mg/ml的量存在。在一些实施例中,制剂包含在非水极性溶剂中的溶液中的杀寄生虫剂。非水极性溶剂以按重量计5-40%的量存在,并且制剂还包含增溶剂和亲水性聚合物。在这些实施例中,杀寄生虫剂以10-300mg/ml,例如50-260、60-230、70-190、75-170、80-150、85-120、或90-100mg/ml的量存在。当制剂包含亲水性聚合物时,亲水性聚合物可具有在50-2000的范围内,例如100-1800的分子量。亲水性聚合物可由下述之一或组合组成或包含下述之一或组合:peg、peg衍生物、ppg或ppg衍生物。优选地,亲水性聚合物包含单功能peg、同双功能peg、异双功能peg、多臂peg、星形peg、聚醚、同型双功能ppg或单功能ppg。更优选地,亲水性聚合物包含peg,并且亲水性聚合物可为具有200至1000g/mol的分子量的peg。优选地,亲水性聚合物包括peg300、peg400或peg600。亲水性聚合物可以按重量计5-100%,例如10-99%、15-98%、20-97%、25-96%、30-95%、35-94%、40-93%、45-92%、50-91%、55-90%、60-89%、65-88%、70-87%、75-86%、80-85%的量存在于制剂中。优选地,亲水性聚合物以按重量计约70-90%,最优选约85%的量存在于制剂中。当制剂包含一种或多种亲水性聚合物和一种或多种非水极性溶剂的组合时,亲水性聚合物可以按重量计5-97%,例如25-95%、或50-90%,例如75-87%的总量存在。在这些实施例中,非水极性溶剂可以按重量计5-35%,例如按重量计7-20%或10-15%的总量存在于制剂中。优选地,当制剂包含一种或多种亲水性聚合物和一种或多种非水极性溶剂的组合时,亲水性聚合物以按重量计约85%的总量存在于制剂中,并且非水极性溶剂以按重量计约15%的总量存在于制剂中。当制剂包含非水极性溶剂时,非水极性溶剂可由下述之一或组合组成或包含下述之一或组合:dmso、nmp、四甘醇、丙酮或dmf。优选地,非水极性溶剂包含dmso。非水极性溶剂可以按重量计5-35%的量存在于制剂中,并且优选地,可以按重量计5-30%、7-25%、10-20%或12-15%的量存在。优选地,非水极性溶剂以按重量计约15%的量存在于制剂中。当制剂包含增溶剂时,增溶剂可由下述之一或组合组成或包含下述之一或组合:cremophorel、tween、brijc10、kolliphorhs15、或cremophorrh40。优选地,增溶剂包含cremophorel和/或tween80。增溶剂可以按重量计5-60%,例如至少约7、10、15、20或25%的量存在于制剂中,并且优选地,可以按重量计30-55%、35-50%或40-45%的量存在。在一些实施例中,制剂还包含赋形剂。赋形剂可由下述之一或组合组成或包含下述之一或组合:丙二醇、乙醇、异丙醇、碳酸丙烯酯、丁二醇、正丁醇和/或极性油(其可为肉豆蔻酸异丙酯)。赋形剂可以按重量计1-60%的量存在于制剂中,并且优选地,可以按重量计20-55%、25-50%、30-45%或35-40%的量存在。在一些实施例中,制剂还包含稳定剂。稳定剂可由ph控制剂组成或包含ph控制剂。ph控制剂可包含有机酸,其可为柠檬酸、乙酸、己二酸、盐酸、n-羟基琥珀酸、乳酸、苹果酸、草酸、丙酸、蓖麻油酸、琥珀酸和酒石酸。稳定剂可以按重量计高达约3%的量存在于制剂中,并且优选地,可以按重量计0.05-2.0%、0.1-1.0%、0.2-0.4%,例如约0.3%的量存在。优选地,制剂包含以约0.3%的量的柠檬酸。在一些实施例中,杀寄生虫剂的沉淀在腹膜内注射后一周在鱼的内部器官上可见。在一些实施例中,在腹膜内注射后三周,沉淀物也是可见的。在一些实施例中,杀寄生虫剂的治疗有效浓度在制剂的腹膜内注射后至少2个月(60天)在鱼的组织中是可检测的。优选地,杀寄生虫剂的治疗有效浓度在腹膜内注射后至少3个月(90、100或110天)、4个月(120、130或140天)、5个月(150、160或170天)、6个月(180、200、220天)、8个月(220、240或260天)、10个月(300、320或340天)在鱼的组织中是可检测的,并且优选地,在腹膜内注射后至少12个月(360天)是可检测的。最优选地,杀寄生虫剂的治疗有效浓度在制剂的腹膜内注射后至少400天、500天、600天、700天或750天在鱼的组织中是可检测的。在一些实施例中,制剂不包含1-取代的氮杂环烷-2-酮。在一些实施例中,制剂可包含:杀寄生虫剂,其可为氟铃脲;非水极性溶剂,其可为以按重量计5-25%或10-20%,最优选15%的量的dmso;增溶剂,其可为以按重量计20-80%、30-70%、40-60%、45-55%,最优选50%的量的cremophorel;和赋形剂,其可为以按重量计20-50%、25-45%、30-40%,最优选35%的量的丙二醇。制剂优选还包括稳定剂,其可为以0.1-0.5%、0.2-0.4%,最优选0.3%的量的柠檬酸。在这些实施例中,杀寄生虫剂可以10-300mg/ml,例如50-260、60-230、70-190、75-170、80-150、85-120,最优选90-100mg/ml的量存在。在一些实施例中,制剂可包含:杀寄生虫剂,其可为氟铃脲;非水极性溶剂,其可为以按重量计5-25%或10-20%,最优选约15%的量的dmso;增溶剂,其可为以按重量计20-80%、30-70%、40-60%、45-55%,最优选约50%的量的cremophorel;和亲水性聚合物,其可为以按重量计20-50%、25-45%、30-40%,最优选约35%的量的peg或peg衍生物,例如peg300或优选peg400。制剂优选还包括稳定剂,其可为以0.1-0.5%、或0.2-0.4%,最优选约0.3%的量的柠檬酸。在这些实施例中,杀寄生虫剂可以10-300mg/ml,例如50-260、60-230、70-190、75-170、80-150、85-120,最优选约90-100mg/ml的量存在。例如,制剂可包含按重量计约15%的dmso、按重量计约50%的cr.el、按重量计约35%的peg400、约0.3%柠檬酸和约90-100mg/ml氟铃脲。在一些实施例中,制剂可包含:杀寄生虫剂,其可为氟铃脲;非水极性溶剂,其可为以按重量计5-25%或10-20%,最优选约15%的量的dmso;和亲水性聚合物,其可为以按重量计50-95%、或70-90%,最优选约85%的量的peg或peg衍生物,例如peg300或优选peg400。制剂优选还包括稳定剂,其可为以0.1-0.5%、或0.2-0.4%,最优选约0.3%的量的柠檬酸。在这些实施例中,杀寄生虫剂可以10-300mg/ml,例如50-260、60-200、70-180、75-140、80-130、85-120,最优选约90-100mg/ml的量存在。例如,制剂可包含按重量计约15%的dmso、按重量计约85%的peg400、约0.3%柠檬酸和约90-100mg/ml氟铃脲。在一些实施例中,制剂可包含:杀寄生虫剂,其可为氟铃脲;和亲水性聚合物,其可为以按重量计高达50%、60%、70%、80%、90%或100%的量的peg或peg衍生物,例如peg300或peg400。制剂优选还包括稳定剂,其可为以0.1-0.5%、或0.2-0.4%,最优选约0.3%的量的柠檬酸。在这些实施例中,杀寄生虫剂可以10-150mg/ml,例如15-120、20-100、25-90或30-80mg/ml的量存在。在一些实施例中,制剂可包含:(a)以按重量计约80-90%的量的亲水性聚合物;(b)以按重量计约12-18%的量的非水极性溶剂;(c)以约0.2-0.4%的量的稳定剂;和,(d)以约85-100mg/ml的量的几丁质合成抑制剂。在这些实施例中的一些中:(a)亲水性聚合物可包含以按重量计约85%的量的peg400;(b)非水极性溶剂可包含以按重量计约15%的量的dmso;(c)稳定剂可包含柠檬酸;和,(d)几丁质合成抑制剂可包含以约90mg/ml的量的氟铃脲。根据本发明的第二个方面,提供了治疗鱼的寄生虫侵袭的方法。该方法包括通过腹膜内注射将根据第一个方面的制剂施用于鱼。根据本发明的第三个方面,提供了用于通过腹膜内注射治疗鱼的寄生虫侵袭的根据第一个方面的制剂。根据本发明的第四个方面,提供了根据第一个方面的制剂作为鱼的抗寄生虫治疗的用途。该用途包括制剂的腹膜内注射。具体实施方式包含杀寄生虫剂的非水性均相溶液用于鱼的可注射制剂先前未描述过。请求保护的非水性制剂可借助于腹膜内注射施用于鱼,用于针对寄生虫治疗鱼。在本文上下文中,术语“寄生虫”预期指生活在鱼上或鱼中或以宿主鱼为代价获益的任何生物,例如,从鱼获得其一些或全部营养需要的任何生物。寄生虫包括生活在鱼的外表面上或以鱼的外表面为食的体外寄生虫和生活在鱼体内的体内寄生虫两者。术语“杀寄生虫剂”指能够消耗寄生虫群体的任何物质,例如通过杀死寄生虫或者预防寄生虫的生长或繁殖,或以其他方式引起来自宿主鱼的寄主虫损失或去除。该物质可靶向广泛范围的寄生虫,或者可对于小群寄生虫例如个别类型的寄生虫特异性。术语“治疗鱼的寄生虫侵袭”、“鱼的寄生虫侵袭的治疗”、“鱼的治疗”、“针对寄生虫治疗鱼”、“控制寄生虫”、“治疗寄生虫”和类似术语预期指预防性或反应性治疗,例如控制、消除、保护和/或预防鱼由寄生虫的侵袭。寄生虫侵袭的治疗包括减少感染鱼群中每条鱼的寄生虫的平均数目。寄生虫侵袭的控制包括预防感染鱼群中每条鱼的寄生虫的平均数目的增加。鱼该制剂可用于治疗各种不同类型的鱼,包括在淡水、海水和微咸水中存在的所有年龄的食物鱼、怀卵鱼、观赏鱼、池塘鱼、河鱼、水库鱼。例如,鲈鱼、鲷鱼、鲤鱼、鲶鱼、鲑鱼、鲢鱼、丽鱼、军曹鱼、鳕鱼、鳗鱼、牙鲆、丝足鱼、茴鱼、石斑鱼、庸鲽、鲻鱼、鲶鱼、鲽鱼、鲳鱼、斜齿鳊、红眼鱼、鲑鱼、鳎鱼、罗非鱼、鳟鱼、金枪鱼、白鲑、黄尾鰤、大菱鲆、蓝鳍金枪鱼、丁鲷、琥珀鱼、金龙鱼、乌鳢、河豚、黄花鱼、岩鱼、尖吻鲈、白姑鱼、鲟鱼、圆鳍鱼、濑鱼。特别值得注意的是,该制剂适合于治疗下述目的鱼:鲑形目(samoniformes)、鲶形目(siluriformes)、鲈形目(perciformes)、鲤形目(cypriniformes)、鲀形目(tetraodontiformes)、骨舌鱼目(osteoglossiformes)、鲟形目(acipenseriformes)和鲉形目(scorpaeniformes)。例如,请求保护的制剂可用于治疗鲑鱼例如大西洋鲑鱼和太平洋鲑鱼,以及鳟鱼例如虹鳟鱼和海鳟以及花鲈、真鲷、罗非鱼、鲶鱼、大菱鲆和金枪鱼。寄生虫该制剂可用于针对寄生虫治疗鱼。特别地,这包括下述的寄生虫:管口水蚤目(siphonostomatoida)(lus)、指环虫目(dactylogyridea)(鳞盘虫属(diplectanum))、铗钩虫目(mazocraeidea)(例如sparycotyle和异沟盘虫属(heterobothrium))、膜口目(hymenostomatida)(淡水白斑)、分室科(capsalidae)(本尼登虫属(benedenia))、胭蚧科(dactylopodida)(p.perurans)、剑水蚤目(cyclopoida)、parabodonida(隐鞭虫属物种(cryptobiaspp.))、盾纤目(scuticocilitida)(纤毛虫)、gluegeida(l.salmonae)、双壳目(bivalvulida)(例如粘液丸虫属(myxobolus)、角形虫属(ceratomyxa)和h.ictaluri)、单后盘目(monopisthocotylea)(三代虫)、有壁目(strigeatida)(血吸虫)、botriocephalidea(绦虫)、旋尾目(spirurida)(线虫)、鲺目(arguloida)(淡水中的鱼虱)和蛔目(ascaridida)(异尖线虫属(anisakis)),以及隐核虫属(cryptocaryon)(海水中的白斑)、双穴吸虫属(diplostomum)(淡水中的眼吸虫)和enteromyxum(e.leei)。这包括下述科:鱼虱科(caligidae)、王鱼虱科(cecropidae)、双螯鱼虱科(dichelesthiidae)、颚虱科(lernaeopodidae)、将鱼虱科(pandaridae)、羽肢鱼虱科(pennellidae)、锤虱科(sphyriidae)、锚头鳋科(lernaeidae)、盗鱼蚤科(bomolochidae)、软刺鱼蚤科(chondracanthidae)、鳋科(ergasilidae)、嗜爱鱼虱科(philichthyidae)和鲺科(argulidae)。特别有利的是对鱼虱属(dissonus)、鱼虱属(caligus)(特别包括短鱼虱(c.curtus)、细长鱼虱、c.clemensi、智利鱼虱)和lepeophtheirus(包括鲑疮痂鱼虱)的寄生虫。在鱼内的寄生虫的可能局部位置是皮肤、鳃、肠和其他内部器官以及其他位置,例如眼和/或口。杀寄生虫剂请求保护的制剂包括杀寄生虫剂作为用于针对这些寄生虫治疗鱼的活性物质。杀寄生虫剂一般是不溶于水的杀寄生虫剂。例如,杀寄生虫剂可为具有小于10、1或0.1mg/ml的在水中的溶解度的杀寄生虫剂。杀寄生虫剂可溶于非水极性溶剂,例如杀寄生虫剂可为具有大于5、10或25mg/ml的在dmso中的溶解度的杀寄生虫剂。杀寄生虫剂可为具有小于0.1mg/ml的在水中的溶解度和大于25mg/ml的在dmso中的溶解度的任何杀寄生虫剂。杀寄生虫剂可在下述组内:乙酰胆碱酯酶(ache)抑制剂、gaba门控氯化物通道拮抗剂、gaba门控氯化物通道抑制剂、钠通道调节剂、烟碱乙酰胆碱受体(nachr)激动剂、烟碱乙酰胆碱受体(aachr)变构激活剂、氯化物通道激活剂、保幼激素模拟物、弦音感觉器官调节剂、线粒体atp合酶抑制剂、经由质子梯度破坏的氧化磷酸化解偶联剂、烟碱乙酰胆碱受体(nachr)通道阻滞剂、几丁质生物合成的抑制剂、0型和1型、蜕皮干扰剂、蜕皮激素受体激动剂、章鱼胺受体激动剂、线粒体复合物iii电子传递抑制剂、线粒体复合物i电子传递抑制剂、电压依赖性钠通道阻滞剂、乙酰辅酶a羧化酶抑制剂、线粒体复合物ii电子传递抑制剂、兰尼碱受体调节剂、微管蛋白结合剂、乙酰胆碱酯酶(ache)模拟物、氧化磷酸化的解偶联剂。杀寄生虫剂可为适用于控制鱼中的寄生虫侵袭,换言之,对鱼无毒并且能够针对寄生虫治疗鱼,例如由上文列出的寄生虫的侵袭的任何杀寄生虫剂。例如,杀寄生虫剂可为:钠通道调节剂,其可为拟除虫菊酯,例如溴氰菊酯;或噁二嗪,例如茚虫威;氯化物通道调节剂,其可为阿维菌素,例如依马菌素或伊维菌素,或者可为大环内酯如莫昔克丁、或米尔倍霉素例如米尔倍霉素肟;神经毒素,其可为新烟碱例如烯啶虫胺、或三嗪例如灭蝇胺;吡啶,例如吡蚜酮;或苯甲酰脲,其可为几丁质合成抑制剂。在一些实施例中,制剂不包含驱虫剂,并且特别地,在一些实施例中,制剂不包含苯并咪唑,例如甲苯达唑、阿苯达唑、芬苯达唑或奥芬哒唑。几丁质合成抑制剂杀寄生虫剂可为苯甲酰脲,其可为几丁质合成抑制剂。几丁质合成抑制剂通过抑制几丁质的产生而起作用,所述几丁质是昆虫和甲壳类动物角质层的重要部分。在每次蜕壳或蜕皮时,需要几丁质的新合成用于发育。如果几丁质的合成被抑制,则将防止昆虫或甲壳类动物的发育,并且发育不全的动物将死亡。这就是例如在每次蜕壳之间依赖于几丁质合成的海虱的情况。此外,几丁质合成抑制剂还可影响雌性海虱卵的质量,使得它们异常地孵化或发育异常,伴有幼虫畸形和缺乏完成正常发育周期的能力。在经处理的鱼中,几丁质合成抑制剂优选分布于所有组织和器官,包括粘液、皮肤、鳃和肠。受抑制剂影响并且位于具有抗寄生虫有效浓度的几丁质合成抑制剂的鱼组织中的寄生虫将在其进一步发育中被抑制且死亡。在鱼内的寄生虫的可能局部位置是皮肤、鳃、肠和其他内脏。可用于请求保护的制剂中的几丁质合成抑制剂一般是苯甲酰脲化合物,并且可为例如双三氟虫脲、氟啶脲、氟环脲、氟虫脲、氟铃脲、敌草胺、多氟脲、噻嗪酮、除虫脲、啶蜱脲、虱螨脲和氟苯脲。抑制剂可以游离形式或以任何活性形式,例如以任何兽医学上可接受的盐的形式存在于抗寄生虫制剂中。用于制剂的优选的几丁质合成抑制剂包括除虫脲、虱螨脲和氟铃脲。杀寄生虫剂浓度杀寄生虫剂可以任何合适的浓度或量使用。例如,当抑制剂是几丁质合成抑制剂例如氟铃脲时,抑制剂可以5-300mg/ml的量使用。在一个例子中,制剂可包含:杀寄生虫剂;非水极性溶剂,其可为dmso;增溶剂,其可为cremophorel;和赋形剂,其可为丙二醇。在这些制剂中,杀寄生虫剂可以10-300mg/ml,例如20-250、30-200、40-150、50-120、70-115、80-110、85-105,最优选90-100mg/ml,例如约90mg/ml或约100mg/ml的量存在。在另一个例子中,制剂可包含:杀寄生虫剂,其可为氟铃脲;和亲水性聚合物,其可为以按重量计高达50%、60%、70%、80%、90%或100%的量的peg或peg衍生物,例如peg300或peg400。制剂优选还包括稳定剂,其可为以0.1-0.5%、或0.2-0.4%,最优选约0.3%的量的柠檬酸。在这些制剂中,杀寄生虫剂可以10-150mg/ml,例如15-120、20-100、25-90或30-80mg/ml的量存在。在另一个例子中,制剂可包含:杀寄生虫剂;非水极性溶剂,其可为dmso;增溶剂,其可为cremophorel;和亲水性聚合物,其可为peg或peg衍生物,例如peg300或peg400。在这些制剂中,杀寄生虫剂可以10-300mg/ml,例如20-250、30-200、40-150、50-120、70-115、80-110、85-105,最优选90-100mg/ml,例如约90mg/ml或约100mg/ml的量存在。在又一个例子中,制剂可包含:杀寄生虫剂;非水极性溶剂,其可为dmso;和亲水性聚合物,其可为peg或peg衍生物,例如peg300或peg400。在这些制剂中,杀寄生虫剂可以10-300mg/ml,例如20-250、30-200、40-150、50-120、70-115、80-110、85-105,最优选90-100mg/ml,例如约90mg/ml或约100mg/ml的量存在。制剂可包含两种或更多种杀寄生虫剂,例如具有不同作用模式的两种或更多种杀寄生虫剂的组合。当制剂包含两种或更多种杀寄生虫剂时,可使用抑制剂,使得总组合的抑制剂浓度在范围5-300mg/ml内。例如,总组合的抑制剂浓度可优选在10-250mg/ml的范围内,且最优选在20-225mg/ml或25-200mg/ml的范围内,且最优选在50-175mg/ml或75-150mg/ml的范围内,例如约80、90、100、110或120mg/ml。最优选地,总组合的抑制剂浓度可为约90-100mg/ml。在经处理的鱼中,杀寄生虫剂优选以药理学有效浓度分布于所有组织和器官,包括粘液、皮肤、鳃和肠。腹膜内注射先前已将杀寄生虫剂例如几丁质合成抑制剂经口施用于鱼。例如,已将几丁质合成抑制剂例如氟铃脲加入预先制造的鱼饲料或丸剂中,或者在制备丸剂之前与鱼饲料中的其他组分混合。几丁质合成抑制剂先前也已借助于加入其中含有鱼的水中进行施用。这种施用方法是非常简单和劳动效率高的,并且具有附加的优点,即抑制剂可能够直接作用于可从外部接近的任何寄生虫。然而,本文制剂适合于借助于腹膜内注射施用于鱼。这种施用途径比其他施用方法更具技术挑战性,劳动密集和昂贵,并且因此将不是用杀虫剂处理鱼的最直接和明显的方法。制剂腹膜内注射涉及将制剂注射到鱼的内部器官的表面上。因此,注射制剂的效应且特别是毒性难以预测,并且与通过其他方式施用相比较,当通过腹膜内注射将组合物递送至鱼时可能不同。当注射到鱼的腹腔内时,溶剂的效应特别地先前未在大规模研究中充分调查。例如,溶剂可能损害内脏器官的表面或引起对鱼的其他内部损伤。出于这个原因,用于腹膜内注射的先前制剂一般仅以水性制剂的形式生产。例如,wo99/063824公开了几丁质合成抑制剂的水性制剂。然而,一些杀寄生虫剂包括几丁质合成抑制剂的水溶性非常低。例如,发现氟铃脲的水溶性为约2.7x10-5mg/ml。因此,如果氟铃脲以水性溶液的形式制备,它递送差的性能,因为氟铃脲的浓度非常低,这是由于氟铃脲在水中的溶解度低。为了解决这个问题,wo2014/016252公开了包含以悬浮液形式的杀寄生虫剂氟铃脲或虱螨脲的纳米颗粒的水性制剂的生产。然而,目前已发现包含悬浮液或乳液的制剂存在缺点。例如,在其中颗粒氟铃脲分散在连续油相中的油包水乳液中,氟铃脲颗粒可能在生产、贮存和使用期间沉降,导致非均相产物。此外,乳液的不透明度隐藏了沉降的程度。请求保护的制剂是均相的,并且不包含悬浮液或多个液相,例如乳液。因此,已发现它们经过延长的时间段以及在各种不同的贮存条件和温度下是物理上稳定的。这提供了超过悬浮液和多相制剂的显著和重要的优点,所述悬浮液和多相制剂已知是本质上不稳定的,并且因此对于延长的时间的贮存是挑战性的。该制剂包含在均相非水性溶液中的杀寄生虫剂,其中杀寄生虫剂完全溶解于溶剂中,得到均相的热力学稳定的液体制剂。杀寄生虫剂不以例如包含悬浮液的颗粒形式存在。制剂优选是非胶束或基本上非胶束溶液,并且杀寄生虫剂不包含在分散体内。该制剂包含单一非水相,并且不包含乳液。已发现一些杀寄生虫剂,包括几丁质合成抑制剂,例如氟铃脲,基本上不溶于水和非极性溶剂如庚烷两者。另外,在许多溶剂中,且特别是有机溶剂中,已发现氟铃脲在化学上不稳定。然而,令人惊讶的是,目前已发现杀寄生虫剂在某些极性溶剂中具有一定程度的溶解度,所述某些极性溶剂包括二甲基亚砜(dmso)、二甲基甲酰胺(dmf)、二甲基乙酰胺(dma)、四甘醇、n-甲基-2-吡咯烷酮(nmp)、丙酮和乙酸乙酯。特别地,已发现能够以这样的方式配制杀寄生虫剂,包括几丁质合成抑制剂如氟铃脲,使得它们在这些极性溶剂中具有足够的溶解度和稳定性以适合于腹膜内注射。极性溶剂如果溶剂分子具有正电荷和负电荷的永久分离,或者正电荷和负电荷的中心不重合,则溶剂视为极性溶剂。极性溶剂具有高介电常数,例如,介电常数在约15.0以上的溶剂一般视为极性溶剂。在一些实施例中,制剂包含在极性溶剂中的溶液中的杀寄生虫剂。为了避免疑问,关于请求保护的制剂,术语“极性溶剂”不包括使用水作为溶剂,并且为了清楚起见,极性溶剂因此可被称为“非水极性溶剂”。在实践中,在制剂制备期间不添加水,但是如技术人员将了解的,然而可能的是例如由于从大气中吸附,不可避免地可存在少量的水。因此,本文制剂是非水性制剂,并且含有至多4%、3%或2%,优选至多1.5%、1%或0.5%的水。在本文上下文中,术语“非水性”指至多仅包括非常少量的水的制剂,所述水并非加入制剂中,而是可例如源自大气。例如,已知一些非水极性溶剂,例如dmso,在某些条件下是吸湿性的,并且因此可引起少量的水积聚在制剂中或在制剂生产之前的溶剂中。为了清楚的目的,制剂不包含除由于吸附可能存在于组成成分试剂中的水之外的水。在请求保护的制剂的一些实施例中可单独或组合使用的极性溶剂的例子包括丙酮、四甘醇、乙酸乙酯、dmf、dma、dmso、nmp、乙醇、异丙醇、甘油、乙二醇、二甘醇、1-丙醇、1-丁醇、2-丁醇、乙腈和甲醇。极性溶剂可为极性非质子溶剂,例如dmf、dma或dmso。例如,已发现杀寄生虫剂,包括几丁质合成抑制剂如氟铃脲,可充分溶于极性非质子溶剂中,以允许产生用于腹膜内注射的合适制剂。例如,已惊讶地发现氟铃脲在dmso中的溶解度大于300mg/ml。因此,优选的非水极性溶剂是dmso。在一些实施例中,非水极性溶剂不包含nmp、四甘醇和/或丙酮。丙二醇不视为非水极性溶剂,并且因为它是用于杀寄生虫剂如氟铃脲的弱溶剂,所以丙二醇不能用作本文制剂中的溶剂。然而,如下所述,丙二醇可与非水极性溶剂如dmso和/或亲水性聚合物如peg组合用作赋形剂。毒性请求保护的制剂适合于通过腹膜内注射使用,并且因此当以这种方式施用于鱼时不诱导死亡。难以预测通过腹膜内注射施用于鱼的制剂的效应且特别是毒性,并且这些效应可能不同于当通过其他方式施用相同制剂或相同制剂施用于不同动物时观察到的效应。例如,尽管先前已显示,当经口施用于各种不同类型的鱼包括鲑科时,dmso具有低毒性(benville等人,toxicologyandappliedpharmacology12,156-178(1968)),但先前未知如果借助于腹膜内注射连同杀寄生虫剂例如几丁质合成抑制剂一起施用,极性溶剂对鱼是否有毒。目前已惊讶地发现这样的制剂对鱼有毒,并且该毒性是由于极性溶剂而不是杀寄生虫剂。这种先前未认识到的问题的发现是显著的和不幸的,因为目前已发现包含非水极性溶剂的制剂证明比等价乳液或水性悬浮液制剂显著优越的杀寄生虫剂的摄取和生物利用度。已发现毒性与鱼的大小和重量有关,因此取决于要处理的鱼群,可使用而不会诱导过高死亡率的极性溶剂的水平可不同。例如,较大的鱼可能能够耐受比较小的鱼更大量和更大浓度的极性溶剂。请求保护的制剂是无毒的,并且不产生死亡。毒性可通过任何适用的方法进行测量,并且合适的方法是技术人员已知的。例如,对鱼无毒的制剂可在已处理的鱼群中诱导至多2%的死亡率。更优选地,与安慰剂处理的对照组相比较,死亡率水平小于1%,例如小于0.5%。如技术人员将知道的,制剂的毒性可以多种方式进行测定。一些方法可能涉及牵涉大量鱼类的试验。因此,为了避免测试大量鱼的需要,可使用涉及数量小得多的制剂毒性的模型测试。模型测试例如下文所述的那种的使用提供了进一步的优点,它去除了诸如所测试的鱼的大小和敏感性的复杂因素,因为与较大的鱼相比较,小鱼通常更容易受到给定的处理剂量和腹膜内注射的影响。以这种方式,模型测试允许获得不同制剂的毒性的标准化比较。在模型测试中,在约17℃的水温下处理少量大小为24-26克的大西洋鲑鱼,例如每组30条鱼。用大剂量体积(0.2ml)的主题制剂(通过腹膜内注射)处理一组鱼,并且第二组以相同方式用常规剂量体积(0.05ml)的主题制剂进行处理。另外,两个对照组以与主题组相同的方式进行处理,但使用对照制剂例如pbs代替主题制剂。监测鱼并记录经过七天的累积死亡率。如果满足两个条件,则认为主题制剂是无毒的。第一个条件是当制剂以0.05ml的量施用时,相对于相关对照组,在主题组中不存在增加的死亡率。第二个条件是当制剂以0.2ml的量施用时,相对于相关对照组,在主题组中存在死亡率的至多40%的增加。一般地,当极性溶剂是极性非质子溶剂例如dmso时,制剂包含5-40%(w/w)的极性溶剂。优选地,制剂包含小于35%、小于30%、小于25%或小于20%(w/w)的极性溶剂,例如7-35%、10-30%、12-25%或15-20%(w/w)的极性溶剂,例如约5%、10%、15%、20%或25%(w/w)的极性溶剂。增溶剂增溶是其中通过在加入增溶剂后形成胶束结构来增加化合物的溶解度的过程。术语增溶几乎唯一地用于水性体系。在水性药物制剂中,例如,增溶剂通常用于促进难溶性化合物的溶解。另一方面,在非水性制剂中,增溶剂加入是主要为了在水性介质中,而不是在制剂本身中的产品使用期间具有功能。例如,增溶剂是自乳化药物递送系统sedds中的必需组分(singhb.等人critrevtherdrugcarriersyst.2014;31(2):121-185)。sedds是非水溶剂、增溶剂和共溶剂的各向同性混合物,当引入水性介质中时形成精细的水包油乳液。虽然增溶过程在水性体系中得到充分描述,但是均相完全非水性体系本身中的增溶了解较少。基本上,除非增溶剂在如上所述的水性介质中的使用期间具有功能,否则不存在向非水性制剂中加入增溶剂的明确合理的理由。因此,在非水性制剂例如本发明中描述的那些中,将不考虑增溶剂的使用。请求保护的制剂优选是非胶束或基本上非胶束溶液,并且杀寄生虫剂优选基本上不与胶束结合或包含在胶束内。为了清楚起见,不包含增溶剂的本专利申请的制剂是非胶束的。现在已惊讶地并且有利地发现能够产生包含非水极性溶剂的制剂,并且如果还包括增溶剂,则制剂中所需的非水极性溶剂的水平可降低至毒性水平以下。因此,目前已发现对于先前未认识到的腹膜内注射的非水极性溶剂的毒性问题,令人惊讶的解决方案是配制非水极性溶剂连同增溶剂。在本文上下文中,术语“增溶剂”指能够增加杀寄生虫剂在极性溶剂中或在极性溶剂和赋形剂或极性溶剂和亲水性聚合物的混合物中的溶解度的任何物质。增溶剂可为两亲分子或表面活性剂,并且可为阳离子、阴离子或非离子的,非聚合或聚合的。不同的增溶剂可与非水极性溶剂和/或亲水性聚合物组合用于制剂中,并且例如,增溶剂可选自handbookofpharmaceuticaladditives,m.ash和i.ash,gowerpublishinglimited,1996,第900-903或874-880页中分别给出的增溶剂或乳化剂列表。增溶剂可包含两种或更多种不同增溶剂的混合物。合适的增溶剂包括例如:聚氧乙烯脱水山梨糖醇脂肪酸酯,例如聚山梨醇酯20(tween20)、聚山梨醇酯21、聚山梨醇酯40、聚山梨醇酯60、聚山梨醇酯61、聚山梨醇酯65、聚山梨醇酯80(tween80)、聚山梨醇酯81、聚山梨醇酯85和聚山梨醇酯120;聚氧乙烯蓖麻油衍生物,例如聚氧乙烯5蓖麻油、聚氧乙烯9蓖麻油、聚氧乙烯15蓖麻油、聚氧乙烯35蓖麻油(cremophoreel)、聚氧乙烯40蓖麻油、聚氧乙烯40氢化蓖麻油、聚氧乙烯60蓖麻油、聚氧乙烯60氢化蓖麻油、聚氧乙烯100蓖麻油、聚氧乙烯100氢化蓖麻油、聚氧乙烯200蓖麻油和聚氧乙烯200氢化蓖麻油;泊洛沙姆(聚氧乙烯-聚氧丙烯共聚物),例如泊洛沙姆124、泊洛沙姆188、泊洛沙姆237、泊洛沙姆338和泊洛沙姆407;聚氧乙烯烷基醚,例如聚西托醇1000、聚氧乙烯6鲸蜡硬脂醚、聚氧乙烯20鲸蜡硬脂醚、聚氧乙烯25鲸蜡硬脂醚、聚氧乙烯2鲸蜡醚、聚氧乙烯10鲸蜡醚、聚氧乙烯20鲸蜡醚、聚氧乙烯4月桂醚、聚氧乙烯9月桂醚、聚氧乙烯23月桂醚、聚氧乙烯2油基醚、聚氧乙烯10油基醚、聚氧乙烯20油基醚、聚氧乙烯2硬脂醚、聚氧乙烯10硬脂醚、聚氧乙烯21硬脂醚和聚氧乙烯100硬脂醚;聚氧甘油酯,例如辛酰己酰聚氧甘油酯、月桂酰聚氧甘油酯、亚油酰聚氧甘油酯、油酰聚氧甘油酯和硬脂酰聚氧甘油酯;和脱水山梨糖醇脂肪酸酯,如脱水山梨糖醇二异硬脂酸酯、脱水山梨糖醇二油酸酯、脱水山梨糖醇单异硬脂酸酯、脱水山梨糖醇单月桂酸酯、脱水山梨糖醇单油酸酯(span80)、脱水山梨糖醇单棕榈酸酯、脱水山梨糖醇单硬脂酸酯、脱水山梨糖醇倍半异硬脂酸酯、脱水山梨糖醇倍半油酸酯、脱水山梨糖醇倍半硬脂酸酯、脱水山梨糖醇三异硬脂酸酯、脱水山梨糖醇三油酸酯和脱水山梨糖醇三硬脂酸酯;聚乙二醇15羟基硬脂酸酯;鲸蜡硬脂醇和鲸蜡醇。已发现特别适用于一些实施例中的增溶剂包括例如tween、brijc10、kolliphorhs15或cremophorrh40。尤其优选的增溶剂包括tween80和cremophorel。当制剂包含增溶剂时,增溶剂一般以5-60%(w/w)的量使用。优选地,制剂包含10-55%(w/w)的增溶剂,更优选15-50%(w/w)的增溶剂,例如约20、25、30、35、40、45、50或55%(w/w)增溶剂。当制剂包含cremophorel作为增溶剂时,它优选以至少约5、7、10、12、15、18、20或25%,例如30-60%,例如约35、40、45、50或55%的量存在于制剂中。亲水性聚合物作为对于在制剂中使用增溶剂的替代或补充,还惊讶地且有利地发现,如果极性溶剂连同亲水性聚合物一起配制,则可克服腹膜内注射的非水极性溶剂的毒性效应。因此,已惊讶地且有利地发现,能够产生包含非水极性溶剂的适合于鱼的腹膜内注射的杀寄生虫剂制剂,并且如果还包括亲水性聚合物的话,则制剂中所需的极性溶剂的水平可降低至毒性水平以下。此外,已惊讶地且有利地发现,杀寄生虫剂(包括几丁质合成抑制剂,例如氟铃脲)在亲水性聚合物中的溶解度足够高,使得可令人惊讶地产生适合于腹膜内注射的制剂,而无需任何另外的试剂,例如极性溶剂和/或增溶剂。这提供至少重要的优点,即可任选地完全避免非水极性溶剂的任何毒性作用的可能性。此外,已惊讶地发现使用亲水性聚合物可产生对鱼无毒的制剂,并且制剂证明具有显著的和非常有利的储库效应。已发现这种贮库效应由于杀寄生虫剂在腹腔中沉淀而出现。以给使用者提供非常有利的新工具的非常出乎意料的方式,已发现包含增溶剂的制剂不导致杀寄生虫剂在腹腔中沉淀,而在制剂的腹膜内注射后观察到沉淀物,所述制剂包含亲水性聚合物,并且不包含增溶剂。已发现提供储库效应,包含亲水性聚合物连同很少的增溶剂或不含增溶剂的这些制剂显示杀寄生虫剂在经处理的鱼的组织中有利增加的半衰期。相比之下,在腹膜内注射至鱼时,包含增溶剂的制剂具有较短的杀寄生虫剂半衰期,但具有较高的峰值组织浓度。因此,通过调节制剂的组成,并且具体地通过控制可注射制剂的增溶剂和/或亲水性聚合物含量,使用者可容易地控制杀寄生虫剂的半衰期和峰值浓度。这种长效的功效持续时间是主要的优点,因为它降低了必须对鱼施用杀寄生虫剂的频率。实际上,在一些情况下,对于一次0.05ml施用,半衰期可能足以在整个海洋生长期保护鱼。亲水性聚合物含有极性或荷电官能团,使得它们溶于水和/或极性溶剂。在制剂中可使用不同的亲水性聚合物,任选与非水极性溶剂和/或增溶剂组合,或在不存在任何其他溶剂或增溶剂的情况下。亲水性聚合物可为能够氢键合的聚合物。优选地,亲水性聚合物具有50-2000,例如100-1800、或150-1600的平均分子量。亲水性聚合物可为聚烷氧基化醇,或聚烷氧基化醇的衍生物。优选地,亲水性聚合物是聚烷氧基化二醇或聚烷氧基化二醇的衍生物。例如,亲水性聚合物可为聚亚烷基二醇或聚亚烷基二醇的衍生物。合适的亲水性聚合物特别包括peg和peg衍生物以及ppg和ppg衍生物。可使用的peg衍生物的例子包括:单功能peg,例如聚(乙二醇)甲基醚;同双功能peg,例如聚(乙二醇)二甲醚、聚(乙二醇)二缩水甘油醚、或聚(乙二醇)双(羧甲基)醚;异双功能peg,例如聚(乙二醇)四氢糠基醚;多臂peg或星形peg,例如三羟甲基丙烷乙氧基化物或甘油乙氧基化物。可使用的ppg衍生物的例子包括:单功能ppg,例如聚(丙二醇)单丁醚;和同双功能ppg,例如聚(丙二醇)二缩水甘油醚。亲水性聚合物可为聚醚,例如甘油丙氧基化物。优选地,亲水性聚合物是peg或peg衍生物。例如,亲水性聚合物可为具有200至1000的分子量的peg。优选地,亲水性聚合物是peg300、peg400或peg600。亲水性聚合物可包含两种或更多种亲水性聚合物的组合。优选地,当通过腹膜内注射施用时,亲水性聚合物对鱼无毒。亲水性聚合物可作为唯一的溶剂存在于制剂中。在一些实施例中,亲水性聚合物可以按重量计5-100%的量存在于制剂中。亲水性聚合物可与另一种溶剂(例如非水极性溶剂)组合存在于制剂中。在这种情况下,亲水性聚合物可以按重量计10-99%、15-98%、20-97%、25-96%、30-95%、35-94%、40-93%、45-92%、50-91%、55-90%、60-89%、65-88%、70-87%、75-86%,优选约80-85%的量存在于制剂中。赋形剂制剂可包含赋形剂。在本文上下文中,术语“赋形剂”用于指加入制剂中的任何惰性无毒物质,例如作为稀释剂,以允许将制剂制备成所需的稠度、形式或浓度。任何合适的赋形剂均可用于制剂中,并且制剂可包含一种赋形剂或赋形剂的组合。例如,赋形剂或赋形剂混合物可选自但不限于handbookofpharmaceuticaladditives,m.ash和i.ash,gowerpublishinglimited,1996,第862-863或903-904页中分别给出的载体/媒介物或溶剂的列表。合适的赋形剂包括例如极性的低分子量物质如丙二醇、丁二醇、碳酸丙烯酯、乙醇、异丙醇、甘油、丁醇和乳酸乙酯。用于制剂中的赋形剂可包括一种或多种极性油。极性油含有给予分子偶极矩的杂原子,并且当与非极性油例如矿物油相比较时,这提供了具有独特溶解性的物质。可适用于制剂的极性油包括例如:脂肪醇,例如肉豆蔻醇、油醇和硬脂醇;酯,例如肉豆蔻酸异丙酯、棕榈酸异丙酯和油酸乙酯;甘油三酯,例如三辛酸甘油酯、中链甘油三酯和三油酸甘油酯;以及椰子油。一般地,制剂可包含约5-70%(w/w)的赋形剂。优选地,赋形剂中的一种或组合以10-60%(w/w)、20-55%(w/w)或30-50%(w/w),例如约35、37.5、40、42.5或45%(w/w)的总量包括在制剂中。稳定剂目前已惊讶地发现,在本文非水性制剂中的氟铃脲的化学稳定性可通过包括稳定剂而急剧增加。稳定剂可为ph控制剂,例如柠檬酸。因此,在一些情况下,可能有利的是在制剂中包括稳定剂,例如ph控制剂。如技术人员将知道的,术语“ph”仅对水性介质有意义,而不对于非水性溶液例如本文制剂有意义。因此,在本文上下文中,术语“ph控制剂”、“ph调节剂”和类似术语用于指任何物质,当在水性溶液中使用时,所述物质潜在地能够控制ph,例如缓冲和/或调节ph。已惊讶地发现这些试剂增加了氟铃脲在本文非水性制剂中的化学稳定性。ph控制剂可以高达约3体积%,例如0.05-2.0体积%、或0.1-1.0体积%的量包括在制剂中。优选地,ph控制剂可以约0.1、0.2、0.3、0.4或0.5体积%的量包括在制剂中,并且最优选可以0.3体积%的量包括在制剂中。其可为ph控制剂的不同稳定剂可用于制剂中。例如,用于制剂中的ph控制剂可选自但不限于在handbookofpharmaceuticaladditives,m.ash和i.ash,gowerpublishinglimited,1996,第896页中给出的ph控制剂的列表。具体地,已发现用于制剂中的合适的ph控制剂包括例如有机酸如柠檬酸、乙酸、己二酸、盐酸、n-羟基琥珀酸、乳酸、苹果酸、草酸、丙酸、蓖麻油酸、琥珀酸和酒石酸。其他试剂根据需要,可在制剂中包括另外的试剂。制剂可包括冰点降低剂。合适的冰点降低剂包括例如丙二醇和乙醇。本发明的制剂还可包含防腐剂。可使用任何合适的防腐剂或防腐剂的组合,包括例如氯丁醇、苯甲醇、对羟基苯甲酸酯(例如对羟基苯甲酸甲酯或对羟基苯甲酸丙酯)、山梨酸、苯氧基乙醇或硫柳汞。防腐剂可以0.001%至2.5%(w/v),例如0.002至1.5%(w/v)的量包含于制剂中。本发明的制剂还可包含晶体生长抑制剂。可使用任何合适的晶体生长抑制剂或晶体生长抑制剂的组合,包括例如单糖或二糖、糖醇、二醇、甘油、至少部分水溶性盐及其混合物。例子是葡萄糖、蔗糖、果糖、甘露糖、乳糖、海藻糖;甘露醇、山梨糖醇、木糖醇;乙二醇、丙二醇;甘油;氯化钠、氯化钾、氯化镁。优选的晶体生长抑制剂包括甘露醇、山梨糖醇、葡萄糖、乳糖、蔗糖、海藻糖、丙二醇、甘油和氯化钠。本发明的制剂中的晶体生长抑制剂的量可为例如0.1-20%(w/v),优选0.25-15%(w/v),且特别是0.5-10%(w/v)。本发明的制剂优选不包含1-取代的氮杂环烷-2-酮。制剂的用途已惊讶地发现请求保护的抗寄生虫制剂在针对寄生虫治疗鱼方面明显比以前的杀寄生虫剂制剂(包括通过注射、在饲料中或借助于浴处理施用的制剂)更有效。特别地,当制剂包含几丁质合成抑制剂时,已发现它们相对于几丁质合成抑制剂的先前制剂证明具有增加的生物利用度。因此,可减少剂量/鱼以及要注射的体积。这改善了产品的安全性。另外,由于组织浓度增加,治疗效应可延长。具有改善的安全性和延长的效应的产品对养鱼者具有明显的经济利益。它也可为环境有益的,因为较少的活性药物成分释放到环境中。此外,因为活性化合物在溶液中,所以它具有比悬浮液例如wo2014/016252中所述的那种好得多的长期物理化学稳定性。请求保护的制剂适合于以任何合适的方式对鱼的腹膜内注射。例如,在鲑科的情况下,一种处理方案包括在转移到海洋之前的初始淡水阶段期间处理鱼。另外或可替代地,可在鱼已在海中时执行处理。一般地,注射到鱼内的抗寄生虫制剂的总体积为约0.01-2ml,例如0.05ml或0.1ml。注射到鱼内的杀寄生虫剂的总量优选为0.00010至250mg/kg鱼生物量,更优选0.0015至150mg/kg鱼生物量,甚至更优选0.2至120mg/kg鱼生物量。例如,当杀寄生虫剂是几丁质合成抑制剂如氟铃脲时,可施用的抑制剂的量可为1至75mg/kg鱼生物量,例如5-50或10-30mg/kg鱼生物量。请求保护的抗寄生虫制剂还具有许多其他优点。特别地,已惊讶地发现在本文制剂中,几丁质合成抑制剂可为高度化学稳定的,从而提供长保质期。鱼吸收杀寄生虫剂,并且杀寄生虫剂的浓度优选在鱼的血液、肉片和皮肤内以治疗有效浓度维持和可检测延长的时间段。因此,除直接治疗效应之外,制剂一般还在施用后延长的时间段保护鱼免受寄生虫的新攻击。杀寄生虫剂的消耗速率以及因此的保护期在很大程度上取决于制剂的性质。如上所述,本文制剂出乎意料地且有利地发现提供可控制的储库效应,从而为技术人员提供了用于控制鱼组织中的杀寄生虫剂的峰值浓度和由杀寄生虫剂提供的保护持续时间两者的有价值的工具。当施用请求保护的制剂时,杀寄生虫剂的治疗有效浓度在施用后至少2个月(60天)可在鱼的组织中检测到,因此指示在延长的时间段针对寄生虫的鱼的有效保护。优选地,请求保护的制剂提供保护鱼免受寄生虫的新侵袭至少3个月(90天)的时期,并且最优选地,在施用后鱼被保护至少5个月(150天)、至少6个月(180天)、至少8个月(240天)、至少10个月(300天)、至少12个月(360天)、至少15个月(450天)、至少18个月(540天)、至少20个月(600天)、至少24个月(720天)或至少25个月(750天)。已显示针对寄生虫的鱼保护期与鱼肉片、皮肤或血液中观察到的几丁质合成抑制剂水平非常相符。目前已惊讶地发现在用请求保护的抗寄生虫制剂,特别是包含亲水性聚合物的制剂,以及包含低浓度的增溶剂或无增溶剂的制剂注射后,可在内脏腔中观察到沉淀的杀寄生虫剂。已发现沉淀的杀寄生虫剂的存在与非常有利的贮库效应相关联,其中杀寄生虫剂在鱼组织中的半衰期相对于其中未观察到沉淀物的制剂显著增加。在这种情况下,在制剂的腹膜内注射后至少6个月(180天)、至少8个月(240天)、至少10个月(300天)、至少12个月(360天)、至少15个月(450天)、至少18个月(540天)、至少20个月(600天)、至少24个月(720天)或至少25个月(750天),治疗有效浓度的杀寄生虫剂可在鱼的组织中检测到。由请求保护的制剂提供的延长的处理后保护期是特别有利的,因为显著降低了重复处理的需要。这减少了环境被治疗物质的污染,并且对于养鱼者也是成本有效和节省劳动的。此外,通过调节可注射制剂的组成,可有利地容易地控制储库效应。在一些情况下,可能期望使用请求保护的抗寄生虫制剂与另外的抗寄生虫剂,例如另外的杀虫剂。可与请求保护的抗寄生虫制剂组合使用的合适的进一步杀虫剂是例如过氧化氢;甲醛;有机磷酸酯例如敌百虫、马拉硫磷、敌敌畏或甲基吡恶磷;大环内酯例如伊维菌素或苯甲酸依马菌素;拟除虫菊酯例如氯氰菊酯;或多杀菌素例如多杀霉素。药物试剂盒本发明还提供了包含填充有本发明制剂的一个或多个容器的药物包装或试剂盒。在试剂盒中另外提供的是由管理药物的制造、使用或销售的政府机构规定形式的通知,以及药物的使用说明书。实例现在将在下述实例中更详细地解释本发明,所述实例证明了用于鱼的腹膜内注射的请求保护的抗寄生虫制剂的开发。实例1氟铃脲作为不溶于水的杀寄生虫剂的例子进行研究。先前已调查了氟铃脲在常规溶剂甲醇、水和二甲苯中的溶解度,并且结果显示于表1中。对于产生适合于腹膜内注射的稳定溶液的目的,氟铃脲在这些溶剂中未充分溶解。表1溶剂氟铃脲溶解度(mg/ml)水2.7x10-5甲醇11.3二甲苯5.20tomlin,c.d.s.(编辑)thepesticidemanual-worldcompendium,第11版,britishcropprotectioncouncil,surrey,england1997,第676页。为了产生其中氟铃脲存在于稳定溶液中的制剂,调查了氟铃脲在各种其他溶剂中的溶解度。通过将每种溶剂逐渐加入特定质量的氟铃脲中直至观察到完全溶解来测定溶解度。所得到的溶解度在表2中给出。表2溶剂氟铃脲溶解度(mg/ml)丙酮>130四甘醇>75.0乙酸乙酯>75.0肉豆蔻酸异丙酯<1.0正庚烷<0.5丙二醇(pg)<0.5液体石蜡<0.10dmso>300nmp>300dmf>300dma>300发现氟铃脲在非极性溶剂例如庚烷中的溶解度非常低。然而,发现氟铃脲在一些极性溶剂例如dmso、nmp、dmf和dma中的溶解度令人惊讶地高。实例2测试在极性溶剂中制备的杀寄生虫剂的制剂用于腹膜内注射到大西洋鲑鱼内的安全性。用10种制剂之一注射保持在淡水(17℃)中的大西洋鲑鱼幼鱼(平均大小:35.5g),所述10种制剂含有作为示例极性溶剂的dmso、包含丙二醇(pg)的赋形剂和从0到100mg/ml不等的一定量的氟铃脲(参见表3)。10组各自含有30条鱼。表3图1.用表3中所示的制剂注射大西洋鲑鱼幼鱼后的死亡率。记录注射组中的死亡率。在用0.05ml的体积注射的所有组中均观察到低至中等的死亡率,与氟铃脲浓度无关。死亡率随着注射体积急剧增加,当注射体积为0.2ml时达到>90%。该死亡率不依赖于制剂中氟铃脲的存在。结果证明基于dmso的制剂在腹膜内注射后对鱼高度毒性。具体地,即使当用最小体积的0.05mldmso注射鱼时,观察到的死亡率水平(一般为约5%)对于要用于大群养殖鱼的产品也是完全无法接受的。此外,不可能增加注射体积而不显著进一步增加死亡率的水平。为了进一步调查极性溶剂的毒性,如表4中详述的制备包含不同量的dmso的制剂。将制剂以单一剂量腹膜内注射到保持在淡水(8–17℃)中的大西洋鲑鱼(19–38g)内。通过连续登记死亡直到注射后3个月来评价通过每种制剂诱导的最终毒性,并且显示于表4中。表4图2显示了在dmso的注射剂量(g/kg鱼)和毒性(%死亡率)之间的关联性。图2显示了毒性(%死亡率)随着dmso的注射剂量(g/kg鱼)线性增加(r2=0.97)。发现dmso在大约1g/kg以上的剂量下对大西洋鲑鱼有毒。据报道对于鲑科的ld50在12-17g/kg之间(benville等人,toxicologyandappliedpharmacology12,156-178(1968)),并且据报道7.05g/kg的剂量未产生鲑科中的任何死亡。因此,非常惊讶地发现低至约1g/kg的剂量引起大西洋鲑鱼中的死亡。考虑到用包含dmso的制剂观察到的令人惊讶和出乎意料的毒性,产生包含其他极性溶剂的制剂,并且测试这些制剂用于鱼的腹膜内注射的安全性。将保持在淡水(17℃)中的大西洋鲑鱼(平均大小:37.8g)分成5或25条鱼/组的11组。每组接受表5中所示的制剂之一的注射(0.2ml)。制剂基于如表5中所示的不同溶剂。然后记录经过3周时期的死亡率。结果证明除了对照组(其为安全的pg和pbs)之外,测试的所有溶剂在腹膜内注射时对鱼有高度毒性(参见表5)。表5实例3在实例2中,证明由基于溶液的制剂诱导的无法接受的毒性是由于制剂中的极性溶剂(dmso),而不是杀寄生虫剂的含量。用其他极性溶剂代替dmso并未解决毒性挑战(参见表5)。鉴于此,为了尝试产生具有降低的毒性的制剂,产生了其中制剂中极性溶剂的比例降低,同时增加赋形剂pg的比例的制剂。先前已发现在大西洋鲑鱼中的腹膜内注射后pg是安全的(参见表5)。然而,如表2中所示,已发现氟铃脲在pg中的溶解度非常低。因此发现不可能充分地调节pg和dmso的相对比例,以获得其中杀寄生虫剂是可溶的,并且在鱼中不诱导无法接受水平的毒性的制剂。通过在制剂中另外包括增溶剂例如cremophorel(cr.el)令人惊讶地解决了该问题。表6显示了包含dmso、cr.el和pg的杀寄生虫剂(在这种情况下为氟铃脲)的不同制剂的组成。制剂可通过多种不同的方法产生,并且技术人员将熟悉合适的方法。在本实例中,杀寄生虫剂的制剂通过在极性溶剂、增溶剂和/或赋形剂(如指示的)的预混物中在环境温度下在搅拌下溶解杀寄生虫剂(和当指定时的有机酸)进行制备。可替代地,杀寄生虫剂可首先在环境温度下在搅拌下溶解在极性溶剂中,随后在搅拌和环境温度下相继加入增溶剂和/或赋形剂(如指示的)。发现杀寄生虫剂在所有制剂中具有良好的溶解性。因此,通过该方法,惊讶地发现能够制备具有少至5质量%的极性溶剂的杀寄生虫剂的25mg/ml溶液。鉴于此,调查了极性溶剂、增溶剂和赋形剂的组合是否可用于制备包含浓度高得多的杀寄生虫剂的制剂。表6表7显示了已成功制备的包括以高浓度存在于稳定溶液中的杀寄生虫剂(在这种情况下为氟铃脲)的多种制剂的组成。使用极性溶剂、增溶剂和赋形剂的组合,已发现能够制备具有小于40质量%dmso的包含高浓度杀寄生虫剂的制剂。表7以这种方式产生杀寄生虫剂制剂是特别有利的,因为这意味着可减少需要注射到鱼内的制剂体积。这在大型鱼的情况下是有利的,因为这意味着无需注射大体积的制剂。以小体积施用制剂的能力对于与易受腹膜内注射影响的鱼例如小型轻量的鱼一起使用也是特别重要的。进行大规模实验以调查具有低含量的极性溶剂的新型制剂对于腹膜内注射是否是完全安全的。将保持在淡水(8℃)中的总共3000条大西洋鲑鱼幼鱼(在实验开始时的平均体重:19g)分成6组(n=500/组),并且用杀寄生虫剂(在这种情况下为氟铃脲)的制剂或对照制剂腹膜内注射(0.05ml/鱼)。使用的对照制剂是具有或不具有杀寄生虫剂的商购可得的疫苗alphajectmicro6(pharmaqas,norway)和pbs。每个制剂的确切含量在表8中给出。在3个月的研究期间自始至终记录死亡率。表8在所有组中均观察到非常低水平的死亡率,并且包含极性溶剂和增溶剂的新型制剂未引起超过三个对照组中观察到的背景水平的显著水平的死亡率(参见表8)。在分开的实验中,用在dmso/pg(85/15)(n=210)、dmso/cr.el/pg(15/45/40)(n=499)、或pbs(n=500)中配制的0.05ml的25mg/ml氟铃脲注射大西洋鲑鱼(约19-35g)。死亡率在用dmso/pg(85/15)注射的组中记录6天,并且在两个剩余组中记录3个月。观察到的%死亡率为约3.3%(dmso/pg)、约0.6%(dmso/cr.el/pg)和约0.8%(pbs)。包含极性溶剂和增溶剂的新型杀寄生虫剂制剂因此可视为对于腹膜内注射到大西洋鲑鱼内是安全的。实例4已证明适合于腹膜内注射的制剂可使用dmso作为示例极性溶剂进行制备,调查是否也可使用其他极性溶剂产生合适的制剂。将保持在17℃淡水中的大西洋鲑鱼(大约18g)用0.1ml由不同极性溶剂配制为溶液的杀寄生虫剂(在这种情况下,氟铃脲)腹膜内注射。在每种制剂中,发现氟铃脲存在于稳定溶液中。对于每种制剂,极性溶剂的性质以及极性溶剂、增溶剂和赋形剂的相对数量在表9中给出。将pbs注射到一组内作为对照。观察所有组(n=5/组)共一周,并且记录死亡率(参见表9)。表9制剂的内容物比率(质量%)注射的鱼(n)死亡的鱼(n)pbs10050dmso/cr.el/pg10/50/4050dmso/cr.el/pg40/45/1550nmp/crel/pg10/50/4050四甘醇/crel/pg30/50/2050丙酮/crel/pg20/50/3050dmf/crel/pg10/50/4050dmf/crel/pg40/45/1550结果提示杀寄生虫剂制剂可使用各种不同的极性溶剂进行生产,并且制剂可使用对于腹膜内注射到鱼内安全的不同的极性溶剂各自进行生产。实例5在实例3中,证明了可使用极性溶剂(dmso)、增溶剂(cr.el)和赋形剂(pg)的组合来制备适合于腹膜内注射的氟铃脲制剂。在本实验中,调查是否也可以这种方式配制其他杀寄生虫剂。如表10中详述的,将不同杀寄生虫剂配制为在极性溶剂(20或40质量%dmso)、增溶剂(40质量%cr.el)和赋形剂(20或40质量%pg)中的25mg/ml溶液。制备用于比较的包含氟铃脲的制剂。在每种制剂中,发现杀寄生虫剂存在于稳定溶液中。表10在另一个实验中,测试了在相同产品中制备包含氟铃脲和第二杀寄生虫剂的组合产品的可行性。如表11中详述的,在极性溶剂(20或30质量%dmso)、增溶剂(40质量%cr.el)和赋形剂(30或40质量%pg)中制备包含氟铃脲(12.5mg/ml)和7种其他杀寄生虫剂(各自为12.5mg/ml)之一的制剂。表11在每种制剂中,发现杀寄生虫剂存在于稳定溶液中。实例6用在3种不同制剂中配制的杀寄生虫剂(氟铃脲)注射大西洋鲑鱼:在极性溶剂(85质量%dmso和15质量%pg)中的25mg/ml溶液、具有在连续油相中分散的25mg/ml氟铃脲的油包水乳液、以及作为50mg/ml水性悬浮液。在乳液制剂中,通过标准高剪切混合,将氟铃脲精细地分散在连续油相中。相同的方法用于乳化过程。在水性悬浮液中,通过标准高剪切混合,使氟铃脲精细分散,使用0.1%tween80辅助分散过程和0.4%羟乙基纤维素稳定悬浮液。将注射体积调节以适应鱼的大小,使得所有鱼均接受25mg/kg的注射,除了接受125mg/kg的用水性悬浮液注射的组之外。研究结果显示于图3中。在注射后一周在肌肉和皮肤的一部分中测量氟铃脲的浓度。误差条指示平均值的标准误。图3中所示的结果令人惊讶地证明基于极性溶剂的制剂(dmso/pg)的显著优越摄取。该出乎意料的结果证明与先前可获得的组合物相比较,包含极性溶剂的制剂提供显著改善的杀寄生虫剂的生物利用度。用0.05ml表12中所示的制剂之一注射保持在淡水(17℃)中的大西洋鲑鱼(平均大小:25.6g)。在注射后6天从每组10条鱼中取样骨骼肌与皮肤的一部分。测定每种组织样品中的氟铃脲浓度。实验结果显示于表12中。指示了每种制剂的含量,并且显示了注射后6天在肌肉和皮肤中检测到的氟铃脲的平均浓度(n=10)。表12结果令人惊讶地和出乎意料地证明,当制剂中增溶剂(cr.el)的相对量从0增加到35%时,肌肉和皮肤中的氟铃脲浓度显著增加。实例7已证明适合于腹膜内注射的制剂可使用cr.el作为增溶剂进行制备,调查了是否也可使用替代增溶剂产生合适的制剂。在实验中,使用cr.el或各种其他增溶剂来配制杀寄生虫剂(在这种情况下,氟铃脲)。对于每种制剂,增溶剂的性质以及极性溶剂、增溶剂和赋形剂的相对量在表13中给出。表13在每种制剂中,发现氟铃脲是可溶的。结果提示可使用不同的增溶剂产生合适的杀寄生虫制剂。实例8在该实验中,调查是否可使用不同的赋形剂产生合适的制剂。如表14中所示产生制剂。在每种制剂中,发现杀寄生虫剂(氟铃脲)存在于稳定溶液中。结果提示可使用不同的赋形剂产生合适的杀寄生虫剂制剂。表14执行实验以便测试是否可使用包含极性油的赋形剂配制杀寄生虫剂溶液。肉豆蔻酸异丙酯(ipm)用作示例极性油,并且产生包含ipm作为赋形剂的制剂。表15显示了制备的不同制剂。表15所有制剂均为澄清溶液,其中氟铃脲在稳定溶液中,指示极性油例如ipm可用作包含杀寄生虫剂的制剂生产中的赋形剂。实例9在该实验中,调查了添加稳定剂(在这种情况下为ph调节剂)对溶液制剂中的氟铃脲的化学稳定性的影响。柠檬酸用作示例ph调节剂。如表16中所示产生制剂。表16将制剂在胁迫条件下在40℃和75%相对湿度下温育8周。在实验开始时以及在2、4和8周后取出样品用于氟铃脲分析。通过hplc方法与uv检测来测定氟铃脲含量。图4中所示的结果证明包含稳定剂的氟铃脲素制剂在实验期间是化学稳定的。相比之下,在不存在稳定剂的情况下,氟铃脲相当快地分解。这证明在某些情况下向氟铃脲制剂中加入稳定剂可能是有利的。实例10调查是否可生产包含亲水性聚合物的合适制剂。亲水性聚合物用于替换在较早实例中使用的赋形剂。如表17中所示产生制剂。制剂可通过多种不同的方法产生,并且技术人员将熟悉合适的方法。在本实例中,杀寄生虫剂的制剂通过在极性溶剂和亲水性聚合物(如指示的)的预混物中在环境温度下在搅拌下溶解杀寄生虫剂(和当指定时的有机酸)进行制备。可替代地,杀寄生虫剂可首先在环境温度下在搅拌下溶解在极性溶剂中,随后在搅拌和环境温度下加入亲水性聚合物(如指示的)。表17在每种制剂中,发现杀寄生虫剂(氟铃脲)存在于稳定溶液中。结果提示可产生包含亲水性聚合物的合适的杀寄生虫制剂。为了进一步调查亲水性聚合物的用途,执行实验以调查根据亲水性聚合物(在这种情况下,peg)的分子量的杀寄生虫剂(氟铃脲)的溶解度。所研究的制剂包含dmso(15质量%)、cr.el(50质量%)、peg(35质量%)和稳定剂柠檬酸(ca)(0.3体积%)。增加量的氟铃脲溶解于包含具有范围为200至700的分子量的peg的不同形式的制剂中。图5指示了根据peg分子量的氟铃脲的最大溶解度(mg/ml)。由图5显而易见的是氟铃脲的溶解度随着peg分子量的增加而显著增加。考虑到这一发现,执行实验以调查杀寄生虫剂(氟铃脲)在包含dmso、cr.el和peg400的制剂中的溶解度。如表18中所示产生制剂。通过在极性溶剂、增溶剂和peg400(如指示的)的预混物中在环境温度下在搅拌下溶解增加量的氟铃脲直至饱和来制备制剂。表18在每种制剂中,所有这些均为澄清溶液,发现杀寄生虫剂(氟铃脲)存在于稳定溶液中。结果提示可使用不同比率的增溶剂和亲水性聚合物产生合适的杀寄生虫剂制剂。此外,以这种方式,可产生具有有利地高浓度的氟铃脲的氟铃脲制剂。然后执行实验以便调查是否可使用与极性溶剂组合的不同亲水性聚合物来制备合适的制剂。如表19中所示产生制剂。表19发现所有制剂均为澄清的均相溶液,其中氟铃脲在稳定溶液中,证明包含极性溶剂、增溶剂和亲水性聚合物的杀寄生虫剂制剂可使用各种不同的亲水性聚合物进行制备。考虑到这些发现,调查了是否可使用替代增溶剂产生包含亲水性聚合物的合适的杀寄生虫制剂。在实验中,如表20中所示,使用亲水性聚合物(peg300)和不同的增溶剂配制杀寄生虫剂(在这种情况下,氟铃脲)。表20在每种制剂中,发现氟铃脲是可溶的,并且形成稳定的均相溶液。结果提示可使用极性溶剂、亲水性聚合物和各种不同的增溶剂来产生合适的杀寄生虫剂制剂。有利地,可产生具有至少12.5-100mg/ml的广泛范围的杀寄生虫剂浓度的制剂。实例11考虑到杀寄生虫剂例如氟铃脲在亲水性聚合物中的令人惊讶地高溶解度,假设能够产生包含极性溶剂和亲水性聚合物的制剂,而无需增溶剂。为了调查这一点,如表21中所示制备制剂。通过在极性溶剂、增溶剂和peg400(如指示的)的预混物中在环境温度下在搅拌下溶解增加量的氟铃脲直至饱和来制备制剂。表21所有制剂均为澄清溶液。发现氟铃脲是可溶的,并且在包含极性溶剂和亲水性聚合物的制剂中形成稳定的均相溶液,而无需增溶剂。此外,以这种方式,可生产具有有利地高浓度的氟铃脲的氟铃脲制剂。执行实验以便调查根据peg分子量在包含peg(85质量%)、dmso(15质量%)和ca(0.3体积%)的制剂中的杀寄生虫剂(氟铃脲)溶解度。增加量的氟铃脲溶解在具有范围为200-600的peg分子量的peg/dmso/ca(85/15/0.3)的不同混合物中。图6显示了根据peg分子量的氟铃脲的最大溶解度(mg/ml)。由图6显而易见的是氟铃脲的溶解度随着peg分子量而显著增加。在包含按重量计85%peg600和按重量计15%dmso的制剂中,氟铃脲的最大溶解度为约130mg/ml。执行实验以便调查是否能够使用不同的亲水性聚合物制备包含极性溶剂的类似农药制剂。如表22中所示制备制剂。表22所有制剂均为澄清溶液,其中氟铃脲在稳定溶液中,证明包含极性溶剂和亲水性聚合物的农药制剂可使用各种不同的亲水性聚合物进行制备。执行实验以调查通过包含亲水性聚合物和极性溶剂但不含增溶剂的制剂的腹膜内注射对鱼组织的杀寄生虫剂递送。用表22中所示的杀寄生虫剂(氟铃脲)制剂之一腹膜内注射平均重量35克的大西洋鲑鱼(平均25条鱼/组)。制剂还含有0.3%柠檬酸。注射体积为0.05ml。将鱼保持在12℃下的淡水中。在注射后6周,在肌肉和皮肤的一部分中测量氟铃脲的浓度。研究结果显示于表23中。表23制剂增溶剂存在氟铃脲浓度1(dmso/cr.el/peg400)是218892(dmso/peg400)否18841结果证明两种制剂在注射后六周在经处理的鱼的组织中均生成大量和显著浓度的杀寄生虫剂。显然,可使用与增溶剂或亲水性聚合物(例如peg)之一或两者组合的极性溶剂来产生合适的杀寄生虫制剂。实例12鉴于上述发现,进一步调查了亲水性聚合物例如peg在生产合适的杀寄生虫剂制剂中的潜力。产生包含亲水性聚合物(peg300),任选连同极性溶剂和/或增溶剂的制剂,如表24中所示。表24在其中存在杀寄生虫剂的每种制剂中,发现杀寄生虫剂存在于稳定的均相溶液中。特别令人惊讶的是,可产生包含亲水性聚合物但不含极性溶剂或增溶剂的包含在均相溶液中的杀寄生虫剂的合适制剂。因此执行实验以便调查根据peg分子量在包含peg(100质量%)和ca(0.3体积%)的制剂中的杀寄生虫剂(氟铃脲)溶解度。增加量的氟铃脲溶解在具有范围为200-600的peg分子量的peg/ca(100/0.3)的不同混合物中。图7显示了根据peg分子量的氟铃脲的最大溶解度(mg/ml)。由图7显而易见的是氟铃脲在亲水性聚合物例如peg中具有显著的溶解度,并且溶解度随着peg分子量而显著增加。考虑到这些发现,调查了是否可用其他杀寄生虫剂产生包含亲水性聚合物的合适制剂。不同的杀寄生虫剂被配制为在peg400中的25–50mg/ml溶液,如表25中详述的。通过在环境温度下在搅拌下使杀寄生虫剂(和当指定时的有机酸)溶解在亲水性聚合物(如指示的)中来制备制剂。表25杀寄生虫剂杀寄生虫剂浓度(mg/ml)peg400(质量%)溴氰菊酯25100伊维菌素50100虱螨脲50100依马菌素25100氟铃脲40100在每种制剂中,发现杀寄生虫剂存在于稳定溶液中。然后测试制备包含氟铃脲和第二杀寄生虫剂的组合产品的可能性。如表26中详述的,在peg400中制备含有氟铃脲(12.5或20mg/ml)和4种其他杀寄生虫剂(各自为12.5或20mg/ml)之一的制剂。表26在每种制剂中,发现杀寄生虫剂存在于稳定溶液中。考虑到发现适合于腹膜内注射的制剂可使用具有不同链长的不同peg制备,调查了是否可使用替代的亲水性聚合物制备合适的制剂。如表27中所示产生制剂。表27亲水性聚合物分子量氟铃脲浓度(mg/ml)聚(丙二醇)42510聚(丙二醇)42520甲氧基聚(乙二醇)35010甲氧基聚(乙二醇)35080甲氧基聚(乙二醇)55010甲氧基聚(乙二醇)55070聚(乙二醇)甲醚35080聚(乙二醇)甲醚55075聚(乙二醇)四氢糠基醚20080聚(乙二醇)四氢糠基醚200100甘油丙氧基化物150010聚(乙二醇)二甲醚25080聚(乙二醇)二甲醚250140聚(乙二醇)二甲醚50080聚(乙二醇)二甲醚50010聚(乙二醇)二缩水甘油醚50030聚(乙二醇)二缩水甘油醚50042三羟甲基丙烷乙氧基化物17024三羟甲基丙烷乙氧基化物45012聚(丙二醇)42520聚(丙二醇)72510聚(丙二醇)单丁醚34010聚(丙二醇)二缩水甘油醚38020在每种制剂中,发现杀寄生虫剂存在于稳定溶液中。结果提示可使用各自具有小于2000的分子量的不同亲水性聚合物生产合适的杀寄生虫制剂。此外,以这种方式,可生产具有一定浓度的氟铃脲的制剂。实例13执行实验以调查包含亲水性聚合物的制剂的毒性。将具有28.7g的平均大小的大西洋鲑鱼保持在淡水(17℃)中的500l槽中。每组接受表24中所示的制剂之一的腹膜内注射(0.2ml)。稳定剂(ca)以0.3体积%的量包括在制剂中。在注射后每天监测鱼行为和死亡率,并且结果显示于表28中。表28制剂内容物注射体积(ml)注射的鱼死亡的鱼(n)1peg3000.21002admso/cr.el/pg/ca0.22012bdmso/cr.el/pg/ca0.051003dmso/cr.el/ipm/ca0.051004dmso/cr.el/peg300/ca0.22015cr.el/peg300/ca0.22006tween80/peg300/ca0.22027ipm0.21008pg0.21009pbs0.2200结果明确地显示包含peg300的制剂的安全性类似于dmso/cr.el制剂的安全性。特别地,惊讶地且有利地发现包含在均相溶液中的杀寄生虫剂的制剂在腹膜内注射时对鱼无毒,所述均相溶液包含亲水性聚合物,但不含极性溶剂或增溶剂。即使当制剂以大体积(0.2ml)注射时也是如此。测试包含亲水性聚合物的制剂对杀寄生虫剂递送的作用。用制剂1、2b或3腹膜内注射后一周测量皮肤中的氟铃脲浓度(表28)。结果显示于图8中。结果显示所有测试的制剂在注射后一周在鱼组织中导致显著水平的氟铃脲的累积。该结果与制剂无毒的发现组合指示,在不存在极性溶剂或增溶剂的情况下,包含在亲水性聚合物中的溶液中的杀寄生虫剂的制剂适用于通过腹膜内注射将杀寄生虫剂递送到鱼。出乎意料地观察到在注射后,在内脏腔中可见沉淀的氟铃脲。因此执行实验以更详细地调查该观察。实例14根据表29将保持在淡水(12℃)中的大西洋鲑鱼(平均体重:30.0g)分成30条鱼/组的6组。每组接受如表29中所示的制剂的腹膜内注射(0.05ml)。在水/油乳液中配制的氟铃脲用作对照组(制剂6)。表29未观察到由于任何注射在死亡率或行为的明显变化。在注射后1、3和8周取样来自每组的10条鱼的全肉片的皮肤,并且测量氟铃脲的浓度。结果显示于图9中。误差条表示95%置信区间,而线指示平均值。由图9明确的是在每个时间点的平均氟铃脲组织浓度在组之间相当不同。两组,制剂1和2,在注射后一周显示非常高的组织浓度,随后快速消耗。其他组在注射后一周具有较低的峰值测量,但较慢的消耗(图9)。在注射后一周和三周检查腹腔的局部反应。在一些组中一致地观察到内部器官上的白色沉淀物(参见表30)。表30*可能不是沉淀的氟铃脲,而是油滴图9中的消耗动力学提示氟铃脲在鱼组织中的半衰期强烈依赖于制剂。消耗更慢的制剂也在腹腔中形成白色沉淀物(表30),指示该沉淀物可充当储库。表31显示了从第1到8周的氟铃脲的组织浓度。根据该信息,对于每种制剂计算在皮肤中的氟铃脲半衰期。估计的平均半衰期从制剂1的最少17.35天到制剂3的最多95.57天不等。使用代表性半衰期,对于每种制剂直接估计功效的理论持续时间(假定大约100μg/kg的功效阈值)。还进行保守估计,假定在第8周后17.35天的最小半衰期。这是因为可预期储库效应在一段时间后将降低。基于该分析,当用0.05ml剂量注射30g鱼时,估计制剂3有效至少179天,并且在12℃下最多大约765天。表31当在注射后高达8周时比较不同注射制剂的消耗动力学时,观察到显著差异。在注射后一周提供最大组织浓度的制剂不一定提供最长的保护持续时间。特别地,已发现不包含增溶剂的制剂在腹膜内注射后导致氟铃脲在腹腔中的沉淀。还已发现这些制剂提供储库效应。如本文制剂中可见的,由于相对高的组织水平和缓慢的消耗,长效的功效持续时间的提供是主要的优点,因为它降低了必须对鱼施用杀寄生虫剂的频率。实际上,在一些情况下,对于一次0.05ml施用,半衰期可能足以在整个海洋生长期保护鱼。此外,还有利的是通过调节可注射制剂的组成,可容易地控制储库效应。实例15执行实验以调查杀寄生虫剂的组织浓度和对虱子数目的作用之间的关系。大西洋鲑鱼(总数n=180)保持在完全海水(3.5%盐度,12℃)中。在第0天用杀寄生虫剂(在这种情况下为氟铃脲)处理一半的群体(n=90)。从每组随机收集经处理和未经处理的鱼(n=10/组),并且在12周期间在共同的攻击槽中用鲑疮痂鱼虱的桡足幼体攻击。这在处理后在处理后的第1、3、6、8、10和12周中进行6次。在攻击后2周,对每条鱼记录达到附着幼体(chalimus)阶段的虱子数目。在虱子计数时,在每条鱼中还测量肌肉与皮肤的一部分中的氟铃脲浓度。表32显示了在处理后的不同时间点的处理组和未经处理的组中的平均虱子数目(附着幼体阶段)。表32将在每个时间点的处理效应与在该时间点的鱼组织中氟铃脲的平均浓度进行比较。图10显示了在处理后的指示时间点,抵抗附着幼体阶段海虱发育的功效与氟铃脲的平均组织水平(在肌肉和皮肤的一部分中)的比较。功效以百分比(虚线)给出和组织浓度以ug/kg(实线)给出。显示了基于测量数据的趋势线。每条个别鱼的虱子数目也与在同一鱼中测量的氟铃脲浓度相关联。图11显示了整个实验中个别鱼的氟铃脲的组织浓度和虱子数目之间的明确关联性。为了呈现,省略了100ug/kg以上的组织浓度。完全数据集的关联性是统计学显著的(p<0.0001)。这些分析证明氟铃脲的组织浓度和海虱数目之间非常强的关联性(p<0.0001)。因此,氟铃脲的组织浓度可视为给定制剂在针对寄生虫治疗鱼中的潜在功效的强指示剂。为了解决各种问题并且推进现有技术,本公开内容的整体通过举例说明性的不同实施例显示,在所述实施例中可实践请求保护的本发明,并且提供用于鱼的腹膜内注射的改良抗寄生虫制剂。本公开内容的优点和特征仅是实施例的代表性示例,并且不是详尽的和/或排他的。它们仅被呈现以帮助理解和教导请求保护的特征。应理解本公开内容的优点、实施例、实例、功能、特征和/或其他方面不应视为对由权利要求限定的本公开内容的限制或对权利要求的等价物的限制,并且可利用其他实施例并且可作出修改而不脱离本公开内容的范围和/或精神。不同实施例可适当地包含下述、由下述组成、或基本上由下述组成:所公开的元素、组分、特征、部分、步骤、手段等的不同组合。另外,本公开内容包括当前未请求保护的但在未来可请求保护的其他发明。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1