治疗银屑病中成药在制备防治1型糖尿病药物中的应用的制作方法
本发明涉及医用的配制品,具体涉及含有来源于植物的未确定结构的药物制剂。
背景技术:
1型糖尿病是一种由T淋巴细胞介导对自身胰岛β细胞产生免疫应答导致胰岛损伤,胰岛素绝对缺乏的急发性慢性病,需胰岛素终身治疗。国外资料表明,全世界不同地区的1型糖尿病发病率有数十倍差异,最高的是芬兰白人,达36.0/10万人年,而东南亚地区则较低,报告的结果为2.0/10万人年左右,而我国0~14岁人群中该病发病率达0.6/10万。由此看来,虽然我国1型糖尿病发病率较低,但是人口的众多决定了患者并不在少数,是危害人类健康的疾病之一。有研究资料显示我国青少年1型糖尿病患者呈现出逐年上升的趋势,发病率也随年龄的增长而增加,民族间的发病率差异达12倍,且发病率在不同地区之间呈现明显的南低北高现象。因此寻找有效治疗和改善该病的药物已成为一项迫在眉睫的任务。
在1型糖尿病(即胰岛素依赖型,IDDM)患者中,胰腺常有明显的病理改变,β细胞数量仅在正常的10%以下,多伴有胰小岛炎。主要病理改变有:1.胰小岛萎缩:此为1型糖尿病最常见的病理改变,表现为细胞皱缩,呈条束状而变窄。萎缩的小岛细胞形态较小,核致密,胞浆少。此类皱缩细胞尚能分泌胰高血糖素、生长抑素和胰多肽激素,但很少分泌胰岛素。2.胰小岛增生肥在:此系另一种较少见的重要改变,多见于病程短或新发病的患者。胰小岛细胞增生,甚至肥大,直径超过300~400μm。细胞较大,外形规则清晰,核较大。颗粒染色后观察,小岛主要含有具有流行性的β细胞,颗粒几乎全脱去,也含有α细胞。为“蜜月期”病情缓解的表现,数年后病情加重时β细胞可几乎完全消失。3.β细胞空泡变性:主要见于本病的急性型,特点为细胞浆变空,光镜下未见颗粒或其他细胞器。主要由于糖原子核沉着所致,并不造成β细胞永久性损伤,属可逆性改变。4.胰小岛炎:50%~70%的1型糖尿病患者,尤其是得病不久后死亡的儿童,常可见有胰小岛及其周围有淋巴细胞和单核细胞的浸润,为胰岛炎(insulitis)。由此提示自身免疫反应系1型糖尿病的发病机理。
西医虽然还无法治愈1型糖尿病,但临床中已取得了重大的进展,治疗手段日趋多样化,不同程度地延缓了疾病的发生,减轻疾病的症状,提高1型糖尿病患者的生活质量。近几年,1型糖尿病的治疗取得了许多新的突破,如胰岛移植,胰岛素类似物及给药途径,基因,免疫干预,干细胞治疗等方面的研究为1型糖尿病的治疗提供了新的思路和方法。但是纯西医制剂副作用较大,血糖波动明显,胰岛素注射治疗患者依从性较差,而中药煎服口感又较差,所以急需研制用于治疗1型糖尿病的中成药。
目前国内关于中药治疗1型糖尿病的研究多局限在中药单体或活性成分,而中药组合物治疗1型糖尿病的研究很少。陈蔚等研究发现,早期应用黄芪多糖(Astragalus Polysacharin,APS)预免疫可以纠正NOD小鼠Ts细胞的缺陷,恢复其细胞功能,使免疫抑制作用加强,纠正Thl型细胞/细胞因子的免疫失衡状态,从而预防或延缓NOD小鼠糖尿病发病。Kobayashi等发现人参提取物可降低NOD鼠的IFN-γ含量,增高IL-4含量从而预防糖尿病的发生发展。葱酸类成分大黄酸具有明显治疗NOD小鼠糖尿病及其肾病的作用,还可以明显改善db/db小鼠糖尿病肾病的损害,延缓肾功能减退。研究发现桑叶水提物对链脲佐菌素(Streptozotocin,STZ)诱导的1型糖尿病小鼠胰岛的治疗作用和对肾脏以及肝脏的保健功效。康敏等研究结果显示黑苦荞粉对四氧嘧啶致糖尿病小鼠有一定的降糖作用。施念玮等研究发现雷公藤多苷通过下调NOD鼠胰腺中的Th1表达来预防糖尿病的发生。曹莉等发现葛根素可显著改善实验性糖尿病小鼠的胰岛索抵抗。王莉英等发现早期应用茶多糖预免疫可以预防或延缓NOD小鼠1型糖尿病的发生。关于防治1型糖尿病的中药,国知局的专利文献中先后公开了各种中药复方。其中,CN104042928专利申请公开了由石斛40-60份,葫芦巴5-15份制备的复方;CN103816438专利申请公开了由葛根50g;苦瓜50g;玉米须50g;番石榴叶25g;麦冬20g;海带20g;枸杞子15g;麦芽10g;生地9g;赤芍6g;二甲双胍0.03g制备的复方;CN103316101专利申请公开了由葫芦巴6-15份、黄芪6-15份、淫羊藿3-8份、补骨脂3-8份、山茱萸3-8份、大黄1-5份、肉桂3-8份、黄连2-6份制备的复方;CN103005446专利申请公开了由玉米须、蛹虫草合成的纯天然复方片剂,为降血糖功能食品;CN103585431专利申请公开了由土木香3-9份,艾叶3-9份,覆盆子6-12份,瓜子金15-30份,红景天3-6份,酸枣仁10-15份,知母6-12份,芡实9-15份,菟丝子6-12份制备的复方。
公开号为CN105233150的专利申请公开了一种中药组合物,该组合物可治疗银屑病、银屑病性关节炎、类风湿性关节炎和恶性肿瘤,该组合物为含有如下重量份原料制成的制剂:莪术5~30重量份,肿节风5~30重量份,紫草5~30重量份,赤芍5~30重量份,土茯苓5~60重量份,乌梅5~30重量份,甘草3~25重量份、当归3~25重量份、川芎3~25重量份、生地5~60重量份。上述银屑灵片具有养血润燥、凉血解毒、化瘀通络之功效,临床用于治疗血虚风燥型的银屑病疗效确切。
现代药理研究表明,银屑灵片及其中药组分具有多种药理活性,概况起来讲,目前已公开的文献报道的药理作用如下:
(1)方中含有的芍药苷和甘草酸等指标成分,具有抗炎、免疫抑制等作用,肿节风中含有绿原酸、迷迭香酸、落新妇苷等化合物,也具有抗炎、免疫抑制等作用(冯丽敏,赵瑞芝,王银洁,韩凌,卢传坚.正交设计法优选银屑灵片中肿节风有效成分的提取工艺[J].时珍国医国药,2011,08:1860-1861.)。
(2)紫草中的紫草素对角质形成细胞株增殖有抑制及凋亡的作用(吴晓霞,周武庆.紫草素对角质形成细胞细胞株增殖的抑制及凋亡的作用[J].中国麻风皮肤病学杂志,2003,19(6):563-565.)。
(3)莪术能使天然角化不全表皮细胞转化为正常细胞,并能抑制上皮细胞有丝分裂而起到抑制表皮增生过快的作用(徐厚谦,李应东.莪术研究概况[J].甘肃中医学院学报,1995,12(1):46.)。
(4)莪术、肿节风、赤勺等活血化瘀诸药对于皮肤病微循环障碍的病理有明显的改善作用(黄咏菁,吴元胜,廖列辉,王蕾.阿维A胶囊联合银屑灵片治疗寻常性银屑病的临床观察[J].中国皮肤性病学杂志,2007,10:643-644.)。
(5)中药提取液对于TNF-α刺激产生的IL-8的具有抑制作用(卢传坚,刘凤年.“银屑灵片”中药提取液对肿瘤坏死因子-α刺激后角朊细胞分泌细胞因子IL-8的影响[J].辽宁中医杂志,2009,11:1862-1863.)。
(6)全方对于上皮细胞有丝分裂的抑制作用(卢传坚,刘凤年.银屑灵片对上皮细胞有丝分裂的影响[J].中医药临床杂志,2007,01:25-26.)。
(7)全方具有止痒作用(卢传坚,闫玉红.银屑灵片止痒作用的研究[J].中国药房,2008,06:409-411.)。
以上研究提示,银屑灵片具有一定的抗炎、免疫抑制作用。目前,银屑灵片作为治疗银屑病的药物在临床上应用,尚未见有将其应用于防治1型糖尿病(胰岛素依赖性糖尿病,insulin-dependent diabetes mellitus,简称IDDM)的研究报道。
技术实现要素:
本发明要解决的技术问题是提供治疗银屑病中成药在制药中的新用途。
所述治疗银屑病中成药在制药中的新用途具体是:治疗银屑病中成药在制备防治1型糖尿病药物中的应用。其中,所述防治1型糖尿病药物是公开号为CN105233150专利申请权利要求3所公开的一种中药组合物,该药物的有效成分由以下重量份原料药制得:
莪术10份,肿节风20份,紫草20份,赤芍15份,土茯苓20份,乌梅20份,甘草10份,当归10份,川芎10份,生地20份。
上述应用中的所述的防治1型糖尿病药物为片剂,该片剂由以下方法制成:
(1)取土茯苓粉碎过80目筛,得土茯苓粉;
(2)取莪术、肿节风、紫草、赤芍、乌梅、甘草、当归,川芎、生地,以水提取煎煮三次,第一次加11倍量水,提取两小时;第二、三次分别加9倍量水,提取1小时,过滤,合并提取液,弃去残渣;
(3)将提取液浓缩提取液得稠膏,冷却至室温,加入重量为稠膏70%的乙醇,放置24h,过滤,回收乙醇,浓缩得稠膏;
(4)取乳糖、淀粉和糊精与步骤(3)的稠膏混合均匀,干燥,粉碎过80目筛,加入步骤(1)的土茯苓粉和硬脂酸镁,混合均匀,按照常规方法制备成片剂;其中,所述乳糖、淀粉和糊精的加入量为稠膏重量的32.67%,乳糖、淀粉与糊精之间的重量比为乳糖∶淀粉∶糊精=1∶2∶6,所述硬脂酸镁的加入量为稠膏重量的0.67%。
将本发明所述防治1型糖尿病药物制成片剂的的用法如下:成人每次5片,一日3次,7天一个疗程;儿童每次2-3片,一日3次,7天一个疗程。
本发明所述防治1型糖尿病药物能够减轻小鼠胰腺组织内炎症的浸润,保护胰岛细胞,显著提高IDDM模型鼠胰腺内胰岛细胞的存活率,延缓小鼠发病,降低小鼠IDDM的发病程度,延长IDDM小鼠的生存期,预防和治疗1型糖尿病的效果显著。
为了公众能更好地理解本发明的有益效果,下面将通过动物实验进一步阐明。
附图说明
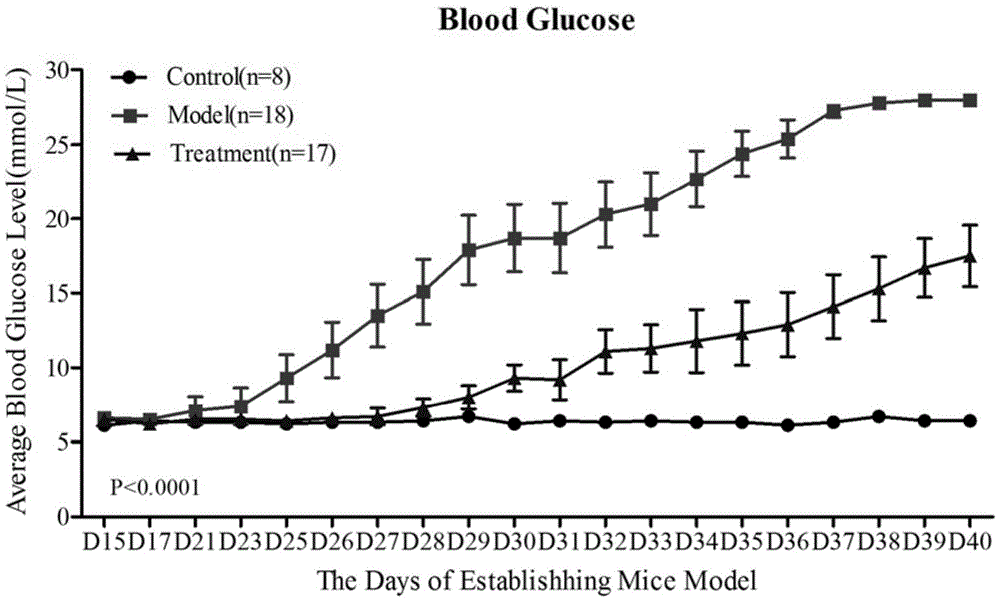
图1为造模后小鼠的血糖变化趋势曲线图。
图2为造模后小鼠的发病率曲线图。
图3为观察期40天内小鼠血糖未达到规定的IDDM发病标准16.7mmol/L的累积天数的生存分析图。
图4为胰腺炎轻重程度得分分布图。
图5为目的基因的Q-PCR的结果柱状图,其中,A图是关于InsulinⅡ基因的检测,图中***表示正常组与模型组比较,模型组与治疗组比较,正常组与治疗组比较,P<0.001,统计学差异极显著。B图是关于CD3ε基因的检测,图中***表示正常组与模型组比较,P<0.001,统计学差异极显著;**表示模型组与治疗组比较,正常组与治疗组比较,P<0.01,统计学差异显著。C图是关于IL-4基因的检测,图中模型组与治疗组比较,P=0.0007<0.001,统计学差异显著。D图是关于IL-10基因的检测,图中模型组与治疗组比较,P<0.0001,统计学差异极显著。E图是关于IL-1β基因的检测,图中模型组与治疗组比较,P=0.0107<0.05,差异有统计学意义。F图是关于IFN-γ基因的检测,图中模型组与治疗组比较,P=0.0387<0.05,差异有统计学意义。G图是关于IL-17A基因的检测,图中模型组与治疗组比较,P=0.0409<0.05,差异有统计学意义。
具体实施方式
动物实验
1.1 1型糖尿病小鼠模型的建立
1.1.1 仪器
解剖器械若干套-剪刀和镊子,2mL注射器针柄,细胞培养皿(35mm×10mm),45mL离心管,15mL离心管,滤网,载物台,擦手纸,乳胶手套,1mL注射器,冰盒,细胞计数板,倒置显微镜,超净工作台,管式低速常温离心机(德国Eppendorf公司),1mL/200μL/10μL移液枪(德国Eppendorf公司)和枪头,废物缸,10mL移液管,管架等。
1.1.2 试剂
红细胞裂解液(1×,ACK Lysis Buffer),PBS(1×)溶液,0.2%的台盼蓝,消毒酒精。
1.1.3 动物
NOD(shi/Ltj)小鼠由上海斯莱克实验动物有限公司提供,6-8周,20~22g,雌性,SPF级,实验动物质量合格证号:2007000559394,实验单位使用许可证号:60062456。NOD-SCID小鼠,6-8周,20~22g,雌性,SPF级,实验动物质量合格证号:11400700069152,实验单位使用许可证号:00100146。实验室温22℃±2℃,相对湿度40%±5%。
1.1.4 自发1型糖尿病NOD(shi/Ltj)雌性小鼠筛选
饲养NOD(shi/Ltj)雌性小鼠﹥4个月时,通过观测小鼠垫料的湿润、粘连程度和饮水量初步判定小鼠是否发病,开始检测血糖,将血糖≥11.1mmol/L的小鼠进行标记并与未发病小鼠分开放置,造模备用。
1.1.5 自发1型糖尿病NOD(shi/Ltj)雌性小鼠脾淋巴细胞的分离与移植
1.准备解剖小鼠、分离组织所用的器械、用品,把碎冰盒装上冰。
2.颈椎脱臼处死小鼠,腹部喷洒75%乙醇消毒置于超净工作台中载物台上,打开细胞培养皿,倒入一定量预冷的PBS溶液。
3.解剖小鼠,接触内脏前注意更换器械,分离脾脏,置于PBS中,用镊子分离白色筋膜组织,放入新的PBS溶液中,剪碎,研磨,用滤网在45mL离心管中过一遍后移入新的15mL离心管中,放入碎冰盒中,然后用管式低速常温离心机离心,1300转/分钟或300g,6分钟,4℃。提前将红细胞裂解液放入37℃水浴锅中复温,拿出冷的PBS置于超净台中管架上。
4.离心结束后,倒出上清,先加入1mL的ACK,吹打均匀,再加入适量的ACK,上下颠倒两下,从加入开始5分钟计时,静置到30秒时,把上清倒入新管中,再静置4分30秒后直接加入冷的PBS溶液停止反应,同条件离心。
5.离心结束后,倒出上清,先加入1mLPBS吹打均匀,再加满到15mL的PBS清洗,上下颠倒,同条件离心。
6.离心结束后倒出上清,加入1mLPBS吹打,打散细胞,再加入9mL的PBS,盖紧离心管盖子,上下颠倒晃动,使细胞均匀悬浮在PBS溶液中,取出50μL,然后同条件离心,离完心放入冰盒中。
7.在50μL的细胞悬液中加入一定的PBS稀释n倍,吹打均匀,再取出50μL,加入50μL的浓度为0.2%的台盼蓝,混合均匀,取出10μL用来计数(稀释了2*n倍)。
8.在准备细胞计数的同时注意离心后将细胞悬液存放在冰盒中。细胞计数结果eg:假设使用计数板计数,平均每一大格细胞数为A(50-150cell),稀释倍数为a=2*n,则细胞总数S=A×104×a×10,1只小鼠回输细胞浓度P=0.5×107cell/0.2mL,即移植细胞终浓度为P=0.25×108cells/mL,则稀释体积V=S/P=A*a/250ml,即V=A*n/125mL。
9.从冰盒中取出离完心的细胞,倒出上清,加入的V(=A*n/125)mL的PBS,吹打均匀,用若干支1mL的注射针吸走细胞悬液,用锡箔纸包裹装有细胞的注射器,放置冰盒中带入动物房。将处理好的脾淋巴细胞悬液注射到6-8周龄的雌性NOD-SCID小鼠体内,注射量0.2mL,然后统计造模小鼠数量。
10.把已造模的NOD-SCID小鼠用苦味酸标记,根据随机数字表进行分组,分笼,做好动物挂牌。
1.1.6 结果
最后统计,我们将11只已发IDDM(血糖≥11.1mmol/L)的NOD(shi/Ltj)小鼠的脾淋巴细胞成功移植到39只NOD-SCID小鼠体内,每只小鼠植入脾淋巴细胞量约0.5×107个。已造模小鼠随机分为2组,模型组19只,只灌胃水溶液,用于疗效对照;治疗组20只,用于银屑灵水溶液干预处理。正常NOD-SCID小鼠8只作为正常对照组,用于模型对照。
1.2 实验药液的配制
实验药物为广东省中医医院药剂科按公开号为CN105233150专利申请的实施例1的处方按下述方法制成片剂(银屑灵片),该银屑灵片临床成人剂量为一日3次,一次5片,每片0.5g,即成人一日用药量为3×5×0.5=7.5g,成人体重为60kg,则成人每千克体重用药量为0.125g,根据《中药药理实验方法学》规定小鼠的用药剂量是成人的12倍,则小鼠的每千克用药量为0.125g×12=1.5g,小鼠每10g体重用药量为0.015g,若每10g体重灌胃量为0.1mL,则需配制的药物浓度为0.015g/0.1mL=0.15g/mL,现配制10片药片即5g,需加入的双蒸水的量为5g/0.15g/mL≈33.33mL,为方便配制,取银屑灵片10片研磨成粉末后加入到33mL双蒸水中,再用涡旋振荡器震荡直至药物粉末溶于水中。
银屑灵片的制备方法:
(1)取土茯苓粉碎过80目筛,得土茯苓粉;
(2)取莪术、肿节风、紫草、赤芍、乌梅、甘草、当归,川芎、生地,以水提取煎煮三次,第一次加11倍量水,提取两小时;第二、三次分别加9倍量水,提取1小时,过滤,合并提取液,弃去残渣;
(3)将提取液浓缩提取液得稠膏,冷却至室温,加入重量为稠膏70%的乙醇,放置24h,过滤,回收乙醇,浓缩得稠膏;
(4)取乳糖、淀粉和糊精与步骤(3)的稠膏混合均匀,干燥,粉碎过80目筛,加入步骤(1)的土茯苓粉和硬脂酸镁,混合均匀,按照常规方法制备成片剂;其中,所述乳糖、淀粉和糊精的加入量为稠膏重量的32.67%,乳糖、淀粉与糊精之间的重量比为乳糖∶淀粉∶糊精=1∶2∶6,所述硬脂酸镁的加入量为稠膏重量的0.67%。
1.3 灌胃与血糖监测
造模后第三天开始灌胃,正常对照组无需任何处理,模型组只灌胃双蒸水,治疗组只灌胃银屑灵水溶液,两组灌胃容量一致,均按照0.1mL/10g计算,灌胃前均进行小鼠体重称重,做好记录,灌胃30天后停止灌胃。从造模后第15天开始通过小鼠尾静脉采血检测所有小鼠的随机血糖,使用雅培安妥血糖仪及试纸快速检测。血糖监测点设置在第15天,第17天,第21天,第23天,第25天,第26天,第27天,一直到第40天,做好小鼠血糖记录。
1.4 实验结果
1.4.1 各组小鼠一般状况、体重、血糖在实验前后的变化
正常组小鼠活动频繁,动作敏捷,反应迅速,垫料干燥;模型组小鼠精神萎靡,反应迟钝,动作迟缓,毛发枯槁无光泽,弓背蜷体,尿量增多,饮水、进食量与正常组比较增加明显;治疗组精神状况、反应、毛色活动较模型组明显增多,而垫料湿度较小。正常组(n=8)、模型组(n=18)和治疗组(n=17)三组的小鼠血糖采用重复测量的方差分析进行总体间的比较,差异有统计学意义(P<0.0001)。组间比较,由于方差不齐,采用Dunnett’s T3检验法,正常组与模型组比较,P<0.0001,提示造模成功;模型组与治疗组比较,P<0.0001,说明药物治疗有效;治疗组与正常组比较,P=0.003<0.01。可见,与正常组比较,治疗组有差异,但远没有模型组差异显著。测定各组小鼠造模后血糖变化情况见表1及图1。
表1 NOD-SCID小鼠及造模后小鼠血糖(mmol/L)变化
注:采用重复测量的方差分析进行总体间的比较,④P<0.0001。组间比较,由于方差不齐,采用Dunnett’s T3检验法,正常组与模型组比较,①P<0.0001;模型组与治疗组比较,②P<0.0001;治疗组与正常组比较,③P=0.003<0.01。小鼠后期血糖很高,血糖仪无法检测,显示“HI”,统计数据时用“28”表示。
1.4.2 各组小鼠发病率在造模后的变化
以小鼠血糖≥11.1mmol/L为标准,判定造模的NOD-SCID小鼠是否发病。造模后3周内,小鼠发病率三组间进行两两比较,由于两组间的总样本量小于40,采用卡方检验中的确切概率法进行比较,差异均无统计学意义(P>0.05),但模型组(n=18)有明显发病趋势,与正常组比较,第28天后有差异有统计学意义(P<0.05),说明1型糖尿病造模成功,而治疗组(n=17)发病缓慢,到3周以后才有发病趋势,与正常组比较,到第38天时,差异有统计学意义(P<0.05),与模型组比较,27天以后,差异有统计学意义,说明药物治疗有效。计算各组小鼠造模后发病率情况见表2及图2。
表2 造模后NOD-SCID小鼠IDDM发病率(%)
注:三组间进行两两比较,由于两组间的总样本量小于40,采用卡方检验中的确切概率法进行比较,模型组、治疗组与正常组比较,△P<0.05,*P<0.01,**P<0.001,***P<0.0001。
1.4.3 各组小鼠40天观察期内血糖未达到16.7mmol/L的天数
以血糖≥16.7mmol/L为标准,将小鼠定义为典型的1型糖尿病血糖,通过计算比较治疗组与模型组小鼠发1型糖尿病的天数,可见模型组平均发病时间明显大于模型组1周,两组数据经过正态性检验和方差齐性检验得出两组资料均服从正态分布,两组方差齐,所以采用两样本均数比较的假设检验t检验,比较造模后40天观察期内两组小鼠血糖未达到16.7mmol/L的天数,得出P<0.0001,差异有统计学意义,说明银屑灵片水溶液治疗效果明显,见表3。因个体差异,病理结果提示模型组1只小鼠未发病,治疗组3只小鼠未发病,因此未纳入统计结果,用“0”表示,发病的小鼠用“1”表示,根据两组天数绘制生存曲线图,横坐标为观察时间,纵坐标为生存率,采用Log-rank时序检验法进行比较,得出χ2=8.5750,P=0.0034<0.01,差异有统计学意义,见图3。
表3 造模后40天观察期内两组小鼠血糖未达到16.7mmol/L的天数比较
注:两组数据经过正态性检验和方差齐性检验得出两组资料均服从正态分布,两组方差齐,所以采用两样本均数比较的t检验,比较造模后40天观察期内两组小鼠血糖未达到16.7mmol/L的天数,得出P<0.0001,差异有统计学意义。
2.1 取材与组织病理学实验
2.1.1 仪器
研究级电动显微镜成像系统日本Olympus,BX61+DP720
全自动密封式组织脱水机德国Thermo Scientific,Pathcentre
组织包埋机德国Thermo Scientific,Histostar
石蜡切片机德国Leica,RM2245
摊片机德国Leica,HI1210
全自动染色封片一体化工作站德国Leica,ST5020+CV5030+TS5025
2.1.2 试剂
苏木素 中国广州化学试剂厂
伊红 中国广州化学试剂厂
硫酸铝钾 中国广州化学试剂厂
碘酸钠 中国广州化学试剂厂
冰乙酸 中国广州化学试剂厂
甘油 中国广州化学试剂厂
RNAlater 美国,life,AM7020
中性树胶 国药,10004160
2.1.3 取材
所有组小鼠在造模后第40天取材,颈椎脱臼处死,取胰腺组织,分三部分保存。一部分置于10%的中性甲醛中固定18小时,然后组织脱水,进行石蜡包埋;一部分置于冰冻包埋液(OCT)中迅速放于液氮中冷却,-80℃保存备用;一部分置于RNAlater(RNA Stabilization Solution,RNA稳定剂,购于life公司)中保存,以提取RNA检测组织样品中基因的表达。
2.1.4 苏木素-伊红(Hematoxylin-eosin,HE)染色。
用石蜡切片机进行石蜡样本的切片,厚度3μm,连续切片,一部分普通载玻片捞片用作HE染色,一部分粘附载玻片捞片用作免疫组织化学染色。石蜡切片放于切片架上室温过夜,次日用HE染色-封片一体机(ST5020-CV5030,Leica,Nussloch,Germany)进行染色,染色程序见表4,结束染色后直接封片机封片。
表4 HE机染程序
2.1.5 各组小鼠胰腺组织病理变化
光镜下观察:分别在光镜下放大100倍、200倍、400倍观察。先在光镜下放大100倍观察,寻找胰腺组织中的胰岛并拍照,然后在200倍和400倍镜下拍照。低倍镜下,可见标本外围有一不太完整的结缔组织被膜。被膜伸入实质形成小叶间隔,将腺实质分隔成许多小叶。小叶间结缔组织内可见胰腺导管与血管的断面。小叶内大部分染色较深的是浆液性腺泡(外分泌部),腺泡之间可见一些染色较浅、大小不等的细胞团,此即为胰岛(内分泌部)。胰岛为染色较浅淡的细胞团,大小不等,外包薄层结缔组织,位于外分泌部的腺泡之间。胰岛内细胞排列成团或索状,细胞间有丰富的毛细血管。HE染色图片中正常组胰腺组织中胰岛包膜完整,胰岛β细胞排列整齐,细胞核染色清亮,着色均匀,核膜完整;模型组胰腺组织中胰岛β细胞减少、颗粒脱失、空泡变性、坏死、消失,纤维组织增生、玻璃样变,胰岛α细胞明显增多,β细胞代偿性肥大,胰岛内部和周边有大量的炎性细胞浸润;治疗组胰腺组织中胰岛靠近导管一侧有炎性细胞浸润且有胰岛α细胞增殖,另一侧存留的胰岛β细胞较多,形态完整,排列分布整齐。
2.1.6 结果与分析
从整体上看,正常组(n=8)无胰岛炎;治疗组(n=15)胰腺组织中胰岛β细胞明显比模型组(n=15)多,炎症浸润的范围和程度明显比模型组要小,要轻。从病理学图片可以看出银屑灵片水溶液治疗1型糖尿病模型小鼠效果明显。以有无胰岛炎为判断标准,将胰腺病理进行分级,见表5。病理评分结果见表6及图4。采用秩和检验中的Kruskal Wallis H检验法进行三组间的比较,P<0.0001,差异有统计学意义。表6可见,模型组胰腺炎的病理例多分布在“4分”这个阶段,而治疗组病理例多分布在“1分”和“2分”这两个阶段,而正常组为NOD-SCID小鼠,联合免疫缺陷小鼠,胰岛中没有炎症浸润,对比之下,治疗组效果明显,胰岛炎症浸润程度远没有模型组。
表5 病理评分标准
表6各组小鼠治疗后胰腺病理得分分布及胰腺炎轻重程度分布百分率(百分比=各得分分布例数/各组总例数,5例/样本)
注:等级资料,采用秩和检验中的Kruskal Wallis H检验法进行三组间的比较,P<0.0001,差异有统计学意义。
2.2 免疫组织化学染色
2.2.1 仪器
冰冻切片机 德国,Thermo SCIENTIFIC,HM560
双蒸水机 德国,Millipore
2.2.2 试剂
rabbit anti-mouse insulin IgG美国,abcam,ab181547
rabbit anti-mouse CD3 IgG美国,abcam,ab5690
冰冻包埋液 美国,SAKURA
加强型DAB Plus Kit 中国福州迈新生物技术,DAB-2031
即用型酶标抗兔二抗 中国福州迈新生物技术,KIT-5004
动物非免疫血清(羊) 中国福州迈新生物技术,SP KIT-B3
抗体稀释液 中国福州迈新生物技术,ABD-0030
柠檬酸组织抗原修复液 中国福州迈新生物技术,MVS-0100
二甲苯 中国广州化学试剂厂
无水乙醇 中国广州化学试剂厂
2.2.3 Insulin抗体的免疫组织化学染色
2.2.3.1 染色方法
1.切片、烤片:胰腺组织石蜡切片3μm,37℃过夜,次日4℃保存,如需染色,则放入65℃烘箱烤片2小时,以防脱片。
2.脱蜡:二甲苯1次×10分钟,1次×5分钟。
3.复水:二甲苯与无水乙醇1:1混匀1次×5分钟,无水乙醇2次×5分钟,95%乙醇1次×5分钟,70%乙醇1次×5分钟,50%乙醇1次×5分钟。
4.修复:1×柠檬酸修复液(福州迈新,100×),修复前置自来水中1分钟,待水沸腾计高压锅冒顶起时计时,修复3分钟,然后室温自然冷却40分钟至1小时。
5.PBS清洗3次×3分钟。
6.消酶:用3%H2O2消除内源性过氧化物酶,室温孵育15分钟。
7.PBS清洗3次×3分钟。
8.用二抗同来源血清(动物非免疫羊血清,福州迈新)封闭,室温孵育30分钟。
9.孵一抗:抗体稀释液稀释(福州迈新)insulin抗体(rabbit anti-mouse insulin IgG,clone EPR17359,abcam,U.K.),稀释比例1:64000,放入保湿盒中4℃冰箱过夜,16小时,需设PBS阴性对照,样品阳性对照和样品阴性对照,批量做之前需做抗体浓度梯度,寻找最佳条件。
10.复温:次日,取出样本,室温复温30分钟。
11.PBS清洗3次×5分钟。
12.孵二抗:因为一抗为兔来源抗鼠抗体,所以二抗选用羊抗兔二抗,即用型,室温孵育15分钟。
13.PBS清洗3次×5分钟。
14.DAB显色:开始时镜下观察,记下显色时间,3分钟,后可同时显色,DAB的配制和显色观察都需避光操作。
15.自来水冲洗,苏木素复染1分钟,自来水冲洗,0.5%盐酸酒精分化10秒,PBS返蓝。
16.脱水:70%乙醇1次×3分钟,95%乙醇1次×3分钟,无水乙醇1次×3分钟,二甲苯透明1次×3分钟。
17.中性树胶封片,待日后观察与拍照。
2.2.3.2 胰腺组织中胰岛素免疫组织化学染色变化
光镜下观察:分别在光镜下放大100倍、200倍、400倍观察。先在光镜下放大100倍观察,寻找胰腺组织中的胰岛并拍照,然后在200倍和400倍镜下拍照。然后通过photoshop软件手动计数胰岛β细胞,观察可见,正常对照组insulin抗体阳性的区域弥漫整个胰岛,只有胰岛周边α细胞未被染上;模型组染上的只有零星的几个胰岛β细胞,治疗组胰岛中insulin阳性的胰岛β细胞较多。用Image-Pro Plus 6.0软件统计出各组的阳性区域的积分光密度值,再计算出平均光密度值,平均光密度=积分光密度/观察区域胰岛的面积。
2.2.3.3 结果与分析
正常组胰岛细胞正常;治疗组胰腺组织中胰岛素阳性的胰岛β细胞明显比模型组多,三组资料均进行正态性检验得出均服从正态分布,方差齐性检验得出,χ2=2.3223,P=0.3131>0.05,方差齐,故采用单因素方差分析法进行三组间的比较,P=0.0002<0.001,三组Insulin(胰岛素抗体)免疫组织化学染色阳性细胞总数比较,差异有统计学意义。两两比较采用q检验(Newman-Keuls法),模型组与正常组比较,P<0.01,差异有统计学意义,说明造模成功;治疗组与模型组,P<0.05,差异有统计学意义,说明药物治疗有效。结果见表7。三组Insulin(胰岛素抗体)免疫组织化学染色阳性区域平均光密度资料均进行正态性检验得出正常组不服从正态分布,方差齐性检验得出,χ2=12.9221,P=0.0016<0.05,三组资料方差不齐,故采用秩和检验(Kruskal-Wallis法)进行三组间的比较,P<0.05,差异有统计学意义。组间比较采用两两比较的秩和检验(Nemenyi法),模型组与正常组比较,P<0.05,差异有统计学意义,说明正常组的胰岛素的表达量明显多于模型组,1型糖尿病模型建立成功。结果见表8。
表7 三组Insulin(胰岛素抗体)免疫组织化学染色阳性细胞总数比较
注:三组资料均进行正态性检验得出均服从正态分布,方差齐性检验得出,χ2=2.3223,P=0.3131>0.05,方差齐,故采用单因素方差分析法进行三组间的比较,P=0.0002<0.001,三组Insulin(胰岛素抗体)免疫组织化学染色阳性细胞总数比较,差异有统计学意义。
表8 三组Insulin(胰岛素抗体)免疫组织化学染色阳性区域平均光密度比较
注:三组资料均进行正态性检验得出正常组不服从正态分布,方差齐性检验得出,χ2=12.9221,P=0.0016<0.05,三组资料方差不齐,故采用秩和检验(Kruskal-Wallis法)进行三组间的比较,P<0.05,三组Insulin(胰岛素抗体)免疫组织化学染色阳性区域平均光密度比较,差异有统计学意义。
2.2.4 CD3抗体的免疫组织化学染色
2.2.4.1 染色方法
1.切片、固定:使用冰冻切片机(HM560,Microm,Germany)将胰腺组织进行冰冻切片,厚度为5μm,-80℃保存,如需染色,则放入丙酮中4℃冰箱固定10分钟。
2.PBS清洗3次×3分钟。
3.消酶:用3%H2O2/甲醇消除内源性过氧化物酶,室温孵育10分钟。
4.PBS清洗3次×3分钟。
5.用二抗同来源血清(动物非免疫羊血清,福州迈新)封闭,室温孵育30分钟。
6.孵一抗:抗体稀释液稀释(福州迈新)稀释CD3抗体(rabbit anti-mouse CD3IgG,polyclonal,abcam,U.K.),稀释比例1:200,放入保湿盒中4℃冰箱过夜,16小时,需设PBS阴性对照,样品阳性对照和样品阴性对照,批量做之前需做抗体浓度梯度,寻找最佳条件。
7.复温:次日,取出样本,室温复温30分钟。
8.PBS清洗3次×5分钟。
9.孵二抗:因为一抗为兔来源抗鼠抗体,所以二抗选用羊抗兔二抗,即用型,室温孵育15分钟。
10.PBS清洗3次×5分钟。
11.DAB显色:开始时镜下观察,记下显色时间,3分钟,后可同时显色,DAB的配制和显色观察都需避光操作。
12.自来水冲洗,苏木素复染30秒,自来水冲洗,0.5%盐酸酒精分化10秒,PBS返蓝。
13.脱水:70%乙醇1次×3分钟,95%乙醇1次×3分钟,无水乙醇1次×3分钟,二甲苯透明1次×3分钟。
14.中性树胶封片,待日后观察与拍照。
2.2.4.2 胰腺组织中CD3T淋巴细胞免疫组织化学染色变化
光镜下观察:分别在光镜下放大100倍、200倍、400倍观察。先在光镜下放大100倍观察,寻找胰腺组织中的胰岛并拍照,然后在200倍和400倍镜下拍照。然后通过photoshop软件手动计数CD3阳性的T淋巴细胞,观察可见,正常组CD3抗体阴性;模型组染上CD3阳性的T细胞很多,治疗组胰岛中CD3阳性的T细胞较少。用Image-Pro Plus 6.0软件统计出各组的阳性区域的积分光密度值,再计算出平均光密度值,平均光密度=积分光密度/观察区域胰岛的面积。
2.2.4.3 结果与分析
从免疫组化图片中可见正常组CD3抗体免疫组织化学染色为阴性,所以不纳入统计比较范围,只将模型组与治疗组进行比较。两组T细胞计数资料进行正态性检验,P>0.05,均服从正态分布,方差齐性检验,F=1.0814,P=0.9413>0.05,两组资料方差齐,采用两样本均数比较的假设检验,t检验进行比较,P=0.0002<0.001,说明两组CD3抗体免疫组织化学染色阳性细胞总数比较,差异有统计学意义,结果见表9。两组CD3抗体免疫组织化学染色阳性区域平均光密度资料进行正态性检验,P>0.05,均服从正态分布,方差齐性检验,F=8.2075,P=0.0656>0.05,两组资料方差齐,采用两样本均数比较的假设检验,t检验进行比较,P=0.0153<0.05,说明两组CD3抗体免疫组织化学染色阳性区域平均光密度比较,差异有统计学意义,结果见表10。
表9 两组CD3抗体免疫组织化学染色阳性细胞总数比较
注:两组资料进行正态性检验,P>0.05,均服从正态分布,方差齐性检验,F=1.0814,P=0.9413>0.05,两组资料方差齐,采用两样本均数比较的假设检验,t检验进行比较,P=0.0002<0.001,两组CD3抗体免疫组织化学染色阳性细胞总数比较,差异有统计学意义。
表10 两组CD3抗体免疫组织化学染色阳性区域平均光密度比较
注:两组资料进行正态性检验,P>0.05,均服从正态分布,方差齐性检验,F=8.2075,P=0.0656>0.05,两组资料方差齐,采用两样本均数比较的假设检验,t检验进行比较,P=0.0153<0.05,两组CD3抗体免疫组织化学染色阳性区域平均光密度比较,差异有统计学意义。
2.3 从微观上探索银屑灵片水溶液对于1型糖尿病小鼠模型的治疗作用
2.3.1 仪器
荧光定量PCR仪 美国Bio-Rad,CFX96
梯度热循环仪 美国Bio-Rad
化学成像系统 美国Biorad,ChemiDoc RS+
多功能酶标仪 美国Rayto,RT2100C
微量紫外分光光度计 美国Thermo scitific,Nanodrop2000
台式高速冷冻离心机 美国Eppendorf,5804R
2.3.2 试剂
RNeasy Micro Kit 德国,QIAGEN
逆转录试剂盒 美国,Promega
2.3.3 组织总RNA提取
胰腺组织总RNA提取过程,使用Micro Kit提取:
1.实验前准备:试剂配制
组织裂解液:1mL RLT缓冲液中加入10μLβ-巯基乙醇,
DNA酶缓冲液:70μL RDD缓冲液加入10μL DNA酶Ⅰ原液,
70%乙醇:7mL的无水乙醇中加入3mL的无RNA酶水,
80%乙醇:8mL的无水乙醇中加入2mL的无RNA酶水;
2.用0.1%DEPC水浸泡过夜,180℃高温烘烤8小时的剪刀在1.5mL无RNA酶的连盖尖底离心管中剪碎组织;
3.加入350μL预先配制好的裂解液,吹匀,静置5分钟,然后在高速离心机中全速离心3分钟;
4.取上清350μL移入新的1.5mL连盖尖底离心管中,加入等体积350μL的70%乙醇,混匀;
5.将混合物转移到装有2mL收集管的RNeasy纯化柱子中,盖好盖子,做上标记,以大于8000g的离心力离心15秒,弃废液;
6.加入350μL RW1缓冲液,以大于8000g的离心力离心15秒,弃废液;
7.加入80μL DNA酶缓冲液,从柱子膜中间缓慢加入,室温放置15分钟;
8.加入350μL RW1缓冲液清洗以大于8000g的离心力离心15秒,弃收集管;
9.将柱子放入新的收集管中,加入500μL RPE缓冲液,以大于8000g的离心力离心15秒,弃废液;
10.加入500μL 80%乙醇,以大于8000g的离心力离心15秒,弃收集管,将柱子放入新的收集管中,打开盖子,全速离心5分钟以干燥RNA,弃管;
11.将柱子放入新的1.5mL无RNA酶的连盖尖底离心管中,从柱子膜中间缓慢加入14μL无RNA酶水,全速离心1分钟,弃柱子;
12.测RNA样品的浓度,调整至合适浓度。
2.3.4 RNA逆转录
按以下比例配制预反应体系:
RNA template 5μg(按实际浓度取相应体积,体积<9.5μL)
Oligo(dT)15Primer 1μL
Nuclease-Free Water 加至10.5μL
瞬时离心30秒,放入热循环仪中,70℃加热5分钟。然后立即将样品冷藏于冰上至少5分钟,微型离心机离心10秒,放在冰上直到加入逆转录混合液9.5μL。逆转录反应体系:
加入逆转录混合物9.5μL后,瞬时离心10秒,放入Bio-Rad PCR仪进行逆转录,反应条件如下:25℃退火5分钟,42℃延伸1小时,冷却至4℃后取出,-20℃保存。
2.3.5 Real Time-qPCR
按以下比例配置反应体系:
使用Bio-Rad CFX96PCR仪进行PCR扩增,采用两步法,扩增程序如下:95℃预变性3分钟,95℃变性10秒,55℃退火及延伸30秒,40个循环,每个循环在55℃延伸时收集荧光值,测定达到荧光阈值(400dT)最小循环次数(Ct),完成后进行熔解曲线测定。以β-actin为内参基因,计算相对表达量2-△ΔCt,其中△ΔCt=(Ct目的基因-Ctβ-actin)处理组-(Ct目的基因-Ctβ-actin)正常组或者△ΔCt=(Ct目的基因-CtCD3ε)处理组-(Ct目的基因-CtCD3ε)模型组。基因序列见表11。
表11 基因序列
2.3.6 结果与分析
InsulinⅡ是胰腺中胰岛细胞的特征基因,其含量的多少反映组织中胰岛的功能状况。正常组(n=8)小鼠胰岛功能正常,模型组(n=15)和治疗组(n=15)基因的相对表达量明显低于正常组,治疗组保留胰岛一半的功能,模型组几乎完全丧失胰岛功能,采用单因素方差分析进行总体比较,差异极显著(P<0.0001),结果见表12及图5-A。
CD3ε是T淋巴细胞的特征基因,其含量的多少反映组织中炎症浸润的程度。正常NOD-SCID小鼠胰岛组织中不表达CD3ε,模型组(n=15)CD3ε基因的相对表达量远高于治疗组(n=15)和正常组(n=8),说明模型组炎症浸润相当严重,采用单因素方差分析进行总体比较,差异极显著(P<0.0001),结果见表12及图5-B。
IL-4是Th2细胞的特征因子,治疗组(n=15)IL-4基因的相对表达量远高于模型组(n=15),采用两独立样本t检验法进行比较,差异显著(P=0.001<0.01),结果见表12及图5-C。
IL-10是一种重要的抗炎因子。治疗组(n=15)IL-10基因的相对表达量明显高于模型组(n=15),说明药物治疗可能调节胰腺组织病变部分T细胞向Th2细胞分化,采用两独立样本t检验法进行比较,差异极显著(P<0.0001),结果见表12及图5-D。
IL-1β是一种与抗原协同作用,促使CD4+T细胞活化的炎性细胞因子。模型组(n=15)IL-1β基因的相对表达量高于治疗组(n=15),采用两独立样本t检验法进行比较,差异有统计学意义(P=0.011,P<0.05),结果见表12及图5-E。
IFN-γ是Th1细胞的特征因子,模型组(n=15)IFN-γ基因的相对表达量高于治疗组(n=15),采用两独立样本t检验法进行比较,差异有统计学意义(P=0.041,P<0.05),结果见表12及图5-F。
IL-17A是Th中与1型糖尿病发展密切相关Th-17细胞的特征因子,为促炎因子。模型组(n=10)IL-17A基因的相对表达量远高于治疗组(n=9),说明模型组炎症浸润的严重程度,采用两独立样本t检验法进行比较,差异有统计学意义(P=0.03,P<0.05),结果见表12及图5-G。
表12 胰腺组织内特定基因相对表达量
注:insulinⅡ和CD3ε是以β-actin为内参基因,以正常组为对照组;IL-4,IL-10,IL-1β,IFN-γ,IL-17A是以CD3ε为内参基因,以模型组为对照组。insulinⅡ和CD3ε三组的数据采用单因素方差分析进行三组间总体比较,先进行方差齐性检验,P<0.05,说明方差不齐,采用均值相等性的键壮性检验(Welch/Brown-Forsythe),P<0.0001,组间多重比较采用Tamhane's T2检验法,正常组与模型组,模型组与治疗组,治疗组与正常组比较,***P<0.001,**P<0.01。IL-4,IL-10,IL-1β,IFN-γ,IL-17A的模型组与治疗组两组独立样本采用t检验,先进行数据的正态性检验及方差齐性检验,IL-4,IL-10,IL-1β,IFN-γ,IL-17A的数据虽有符合正态性分布,但方差不齐,采用非参数检验法中Wilcoxon检验法,P值分别为0.0007,<0.0001,0.0107,0.0387,0.0409。
2.4 统计学分析
所有的定量资料以(SEM)表示,样本数量根据实验需要而定,用Graphpad Prism 5软件作图,统计学分析使用Graphpad Prism 5软件、SPSS 20.0软件,重复测量的数据采用重复测量设计方差分析法,方差不齐时使用Dunnett’s T3检验法。定量资料三组间的比较采用单因素方差分析法;方差齐时,组间多重比较采用Tukey HSD检验法,方差不齐时,采用均值相等性的键壮性检验(Welch/Brown-Forsythe),组间多重比较采用Tamhane's T2检验法。定量资料两组间的比较采用两独立样本t检验,不符合正态性分布且方差不齐的两组数据采用非参数检验法中Wilcoxon检验法。分类资料使用Fisher's Exact检验法,而1型糖尿病小鼠的生存评价资料采用Log-rank时序检验法。等级资料的比较采用秩和检验中的Kruskal Wallis H检验法。P<0.05认为差异有统计学意义。
2.5 结论
1型糖尿病动物模型经过银屑灵片干预处理,起到了很大延缓病情和治疗的作用。银屑灵片能够减轻小鼠胰腺组织内炎症的浸润,保护胰岛细胞的功能。总之,如今的研究表明中药复合物银屑灵片能够显著提高T1D模型鼠胰腺内胰岛细胞的存活率,减少胰岛内炎性细胞如T细胞的浸润,延缓小鼠发病,降低小鼠T1D的发病率,延长小鼠的生存期,提示银屑灵片对模拟人自发1型糖尿病建立的T1D模型小鼠胰腺内胰岛细胞损伤具有良好的保护作用,减少炎症细胞的浸润,预示着银屑灵片在防治1型糖尿病方面有很大的开发应用前景,拓展了银屑灵片的适应证范围。
SEQUENCE LISTING
<110> 广东省中医院
<120> 治疗银屑病中成药在制备防治1型糖尿病药物中的应用
<160> 16
<170> PatentIn version 3.3
<210> 1
<211> 20
<212> DNA
<213> 人工序列
<400> 1
cacccaggct tttgtcaagc 20
<210> 2
<211> 20
<212> DNA
<213> 人工序列
<400> 2
ggtctgaagg tcacctgctc 20
<210> 3
<211> 20
<212> DNA
<213> 人工序列
<400> 3
gcctcagaag catgataagc 20
<210> 4
<211> 20
<212> DNA
<213> 人工序列
<400> 4
cccagagtga tacagatgtc 20
<210> 5
<211> 20
<212> DNA
<213> 人工序列
<400> 5
ccaaggtgct tcgcatattt 20
<210> 6
<211> 20
<212> DNA
<213> 人工序列
<400> 6
atcgaaaagc ccgaaagagt 20
<210> 7
<211> 20
<212> DNA
<213> 人工序列
<400> 7
aggcgctgtc atcgatttct 20
<210> 8
<211> 21
<212> DNA
<213> 人工序列
<400> 8
atggccttgt agacaccttg g 21
<210> 9
<211> 21
<212> DNA
<213> 人工序列
<400> 9
tgccaccttt tgacagtgat g 21
<210> 10
<211> 20
<212> DNA
<213> 人工序列
<400> 10
atgtgctgct gcgagatttg 20
<210> 11
<211> 20
<212> DNA
<213> 人工序列
<400> 11
gaggtcaaca acccacaggt 20
<210> 12
<211> 20
<212> DNA
<213> 人工序列
<400> 12
gggacaatct cttccccacc 20
<210> 13
<211> 20
<212> DNA
<213> 人工序列
<400> 13
actacctcaa ccgttccacg 20
<210> 14
<211> 20
<212> DNA
<213> 人工序列
<400> 14
ttccctccgc attgacacag 20
<210> 15
<211> 20
<212> DNA
<213> 人工序列
<400> 15
aaggccaacc gtgaaaagat 20
<210> 16
<211> 21
<212> DNA
<213> 人工序列
<400> 16
gtggtacgac cagaggcata c 21
- 还没有人留言评论。精彩留言会获得点赞!