用于改善皮肤外观的组合物和方法与流程
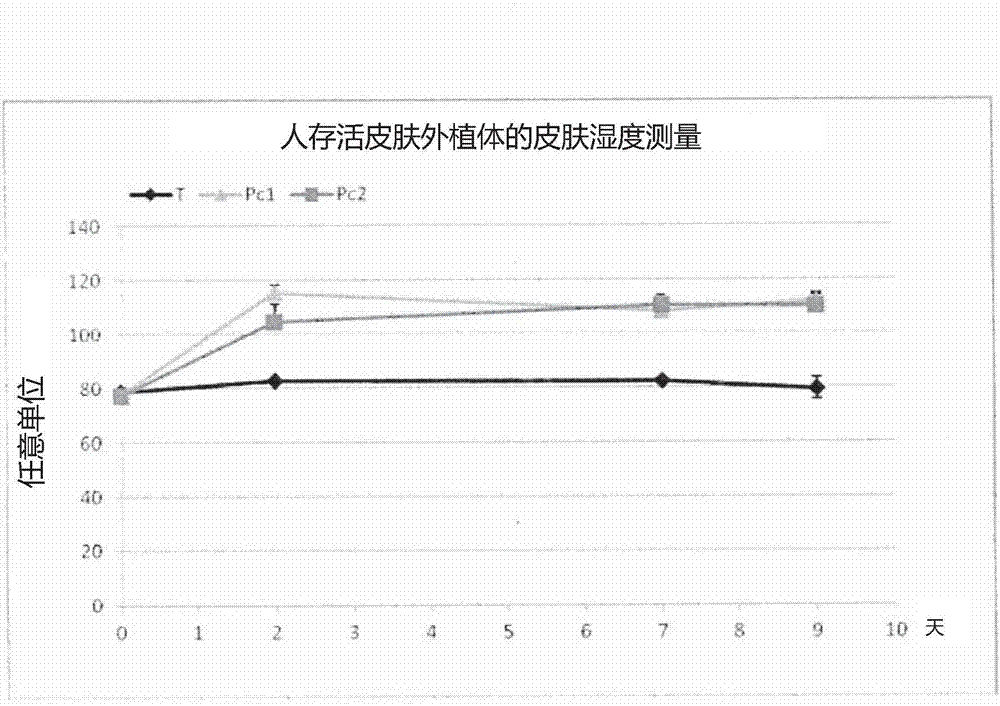
本发明主要涉及可注射组合物,更具体地,涉及用于处理皮肤细纹的基于透明质酸的组合物。目前,用于改善全脸或其他重要皮肤表面区域的皮肤质量的可注射处理选项需要多个处理疗程(通常3-4次处理,每次3至4周),并且具有较短的效果持续时间。皮肤由表皮和真皮构成。最外面的表皮由具有下层基膜的复层扁平上皮组成。表皮不含血管,通过真皮的扩散获得营养。构成表皮的主要细胞类型是角化细胞,也存在黑素细胞和朗格汉斯细胞。这层皮肤负责维持身体内的水分,并阻挡有害化学物质和病原体。真皮位于表皮下方并且包含许多结构,包括血管、神经、毛囊、平滑肌、腺体和淋巴组织。真皮(dermis或corium)的厚度通常为3-5mm,是人皮肤的主要组成部分。真皮由结缔组织网络组成,主要是提供支撑的胶原纤维和提供弹性的弹性组织。主要细胞类型是成纤维原细胞、脂肪细胞(储存脂肪)和巨噬细胞。透明质酸(ha)是真皮组分的一部分,并且是细胞外基质的主要成分。面部老化的发生是多种因素的结果:皮肤内的固有变化、重力效应、面部肌肉对皮肤的作用(动力性皱纹(dynamiclines))、软组织损失或移位以及骨损失和组织弹性损失。当表皮开始变薄时,皮肤老化,导致与真皮的结合处变平。随着人变老,胶原减少,并且胶原束(其使皮肤充盈)变得松散并丧失强度。当皮肤失去弹性时,其较少能够耐受拉伸。加上重力、肌肉拉力和组织改变,皮肤开始起皱纹。水分流失和细胞之间的键的断裂也降低皮肤的屏障功能,这会导致皮肤的孔径增大。众所周知,眼睛通常是第一个显示老化迹象的面部特征。因为眼睛周围的皮肤较薄,所以眼睛周围的皮肤变化比脸的其余部分更早发生。眼睛周围的皮肤含有较少的腺体,并经受不断的眨眼、眯眼、摩擦和拉动。当脸颊开始下垂时面中部老化,引起鼻唇沟皱褶。鼻唇沟皱褶是从鼻子的两侧到嘴角的皱纹。随着面部老化,在面部较低区域,面部组织下降。这导致所谓的“笑纹”。这些以及其他皱褶和皱纹目前通常用皮下和真皮注射面部美容填充剂来处理,面部美容填充剂增加皮肤所失去的体积,从而减少皱褶和皱纹外观。透明质酸(ha)(hyaluronicacid,也称为hyaluronan),目前是真皮填充剂中最常使用的组分之一。透明质酸是天然存在的水溶性多糖,特别是糖胺聚糖(glycosaminoglycan),其为细胞外基质的主要成分,广泛分布在动物组织中。透明质酸在所有物种和组织中的结构相同,这使得该多糖成为用作健康和医药中的生物材料的理想物质。ha具有优异的生物相容性,并且与胶原蛋白不同,其在植入前不需要任何皮肤测试。此外,ha具有结合大量水的能力,使其成为优异的软组织丰盈剂(volumizer)。为了提高ha在体内的寿命,真皮填充剂中的ha通常是交联的。化学交联ha通过在合适的反应条件下将未交联ha与交联剂进行反应而形成。通常认为粘度高的基于ha的真皮填充剂——例如高度交联和/或由高分子量ha制成和/或具有高ha浓度的填充剂——倾向于在体内持续更长时间。相反地,通常认为粘度低的基于ha的真皮填充剂——例如较轻度交联和/或由低分子量ha制成和/或具有低ha浓度的基于ha的真皮填充剂——可能具有较短的体内持续时间。自然地,通过针注射高粘度材料相对更加困难,通常比注射较低粘度的材料需要更低规格(gauge)的针(例如,相比于27g或30g,需要21g或23g的)。已经证明难以开发一种既容易通过高规格针(即细针)注射又具有延长的体内持续时间的基于ha的组合物。技术实现要素:本发明涉及可注射组合物,更具体而言,涉及用于皮内注射到皮肤中的可注射组合物。该组合物和方法通过填充浅表皮肤凹陷、和/或改善皮肤质量和外观而提供改善的皮肤外观和质量。一方面,该组合物和方法提供改善的皮肤纹理、增加的皮肤水合和增加的弹性中的至少一种。一方面,本发明的组合物是基于透明质酸(ha)和ha的药学上可接受的盐,例如透明质酸钠(naha)。许多长效、高度可注射的本发明组合物包含由较低分子量ha制成的交联ha基质。在一些实施方案中,组合物具有较低的ha浓度。有利地,本文中提供的许多组合物具有延长的效果持续时间。例如,本文中提供的许多本发明组合物和方法具有三个月、四个月、六个月、至一年或以上的效果持续时间,而不需要每三至四个星期进行多次重复处理(如采取常规皮内注射处理方法所常见地)。在本发明的宽的方面,提供一种组合物,所述组合物主要包含ha凝胶,所述ha凝胶包含低分子量ha材料或基本上由低分子量ha材料组成。ha组分包含多于50重量%(例如至少70重量%,例如约90重量%)的低分子量ha。低分子量ha材料的重均分子量不超过约0.20mda和约0.99mda,例如为约0.4mda至约0.8mda。在一些实施方案中,ha凝胶可以还包含高分子量ha,即分子量为至少约1.0mda至约4.0mda的ha材料。一般而言,在包含高分子量ha材料的本发明实施方案中,高分子量ha材料的重均分子量是低分子量ha材料的重均分子量的至少两倍。ha凝胶的ha可以交联。例如,ha可通过合适的交联剂化学交联。在一些实施方案中,交联剂选自:1,4-丁二醇二缩水甘油醚(bdde)、或1,4-双(2,3-环氧丙氧基)丁烷、或1,4-双缩水甘油基氧基丁烷(它们全部通常称为bdde),1,2-双(2,3-环氧丙氧基)乙烯和1-(2,3-环氧丙基)-2,3-环氧环己烷。在一些实施方案中,组合物具有约10.0mg/g至最高达约17.0mg/g的ha浓度。在一些实施方案中,ha浓度小于约17.0mg/g,例如小于约15.0mg/g。在一些实施方案中,ha浓度为约10.0mg/g至约14.0mg/g。在一些实施方案中,ha浓度为约10.0mg/g、约11.0mg/g、约12.0mg/g、约13.0mg/g或约14.0mg/g。在本发明的另一方面,提供使用本发明组合物处理皮肤的方法。例如,提供改善皮肤的一种或多种特性或改善皮肤外观或纹理的方法。一方面,提供处理皮肤干燥、纹理或粗糙和/或弹性的方法。所述方法一般包括通过向皮肤区域引入组合物的多次间隔隔开的注射来处理皮肤区域,所述组合物包含含有交联ha的透明质酸(ha)凝胶,其中经处理的皮肤因处理带来的改善的水合、更光滑的纹理或增加的弹性维持延长的持续时间,例如,至少约3个月至约一年或以上。在一个特别有利的实施方案中,引入步骤仅以单次处理疗程(session)进行,从而消除对重复处理以维持效果持久的需要。在一些实施方案中,引入步骤包括以约2mm至约30mm距离间隔隔开的注射而引入组合物。例如,引入步骤包括以约5mm至约20mm、或约10mm至约15mm距离间隔隔开的注射而引入组合物。在一些实施方案中,组合物以约500微米至约2000微米的注射深度引入,例如约1000微米的深度。在优选实施方案中,组合物以约0.5mm至约5.0mm,优选约1.0mm至约4.0mm,更优选约1.5mm至约3.0mm的注射深度引入。一般而言,较深的注射提供改善的水合结果。另一方面,本发明提供一种处理皮肤粗糙的方法,包括通过向皮肤区域引入组合物的多次间隔隔开的注射来处理皮肤区域,所述组合物包含含有交联ha的透明质酸(ha)凝胶,其中经处理的皮肤因处理带来的更光滑的纹理维持至少约3个月、至少约4个月、至少约6个月或至少约12个月。具体实施方式在数值的上下文中,术语“约”将是本领域技术人员容易理解的,优选意为那个特定值可以调整+/-10%。关于范围的端点,修饰词“约”优选意为较低的端点可减小10%,较高的端点增加10%。还可想到,在本申请中公开的各数值或范围可以是绝对的,即可以删除修饰词“约”。在本文中,表示ha的“分子量”的所有数值都应被理解作指示以道尔顿为单位的重均分子量(mw)。ha的分子量使用以下markhouwink关系由特性粘度测量值来计算:特性粘度(m3/kg)=9.78×10-5×mw0.690特性粘度根据europeanpharmacopoeia(ha专论n°1472,01/2009)规定的程序来测量。如本文中所使用的高分子量ha描述的是具有至少约1百万道尔顿(mw≥106da或1mda)至约5.0mda分子量的ha材料。例如,在本发明组合物中的高分子量ha可具有约1.5mda至约3.0mda范围内的分子量,或该高分子量ha可具有约2.0mda的重均分子量。在另一实例中,高分子量ha可具有约3.0mda的分子量。在另一实例中,高分子量ha的分子量可为约1mda(根据如上所述的markhouwink关系计算时,其对应于1.35m3/kg的特性粘度)、1.5mda(1.35m3/kg)、2mda(2.18m3/kg)、3mda(2.88m3/kg)、5mda(4.10m3/kg)、0.2mda(0.44m3/kg)、0.4mda(0.72m3/kg)、0.8mda(1.1m3/kg)、0.99mda(1.34m3/kg)。如本文中所使用的低分子量ha描述的是具有小于约1.0mda的分子量的ha材料。低分子量ha可具有约200000da(0.2mda)至小于1.0mda的分子量,例如,约400000da至约800000da,例如约386000da(0.386mda)至约740000da(0.74mda)。在一些实施方案中,用于制备交联ha基质的低分子量ha不超过0.99mda。优选地,低分子量ha和高分子量ha的混合物具有双峰分子量分布(bimodalmolecularweightdistribution)。混合物也可具有多峰分布。在本发明的一个方面,组合物包含具有高分子量组分和低分子量组分的ha,并且高分子量组分的重均分子量是低分子量组分的重均分子量的至少两倍。例如,根据本发明的该方面的组合物可包含具有约500000da的重均分子量的低分子量组分,和具有约或至少约1.0mda的重均分子量的高分子量组分。在另一实例中,根据本发明的组合物可包含具有约800000da的重均分子量的低分子量组分,和具有约或至少约1.6mda的重均分子量的高分子量组分。交联度由交联剂与ha二糖单元的最终重量比来度量。如本文中所使用的未交联ha,其意指彼此未交联的单个ha聚合物分子。未交联ha通常仍然可溶于水。在本文中提供了用于处理皮肤的组合物——例如可经皮内引入的可注射组合物——以改善皮肤外观或皮肤质量,例如改善水合、纹理和/或弹性。该组合物也可有效地处理皮肤细纹并减少浅表皮肤凹陷。还提供了制备这些组合物的方法,以及使用这些组合物的处理方法。该组合物是基于透明质酸(ha)和ha的药学上可接受的盐,例如透明质酸钠(naha)。如本文中所用,透明质酸(ha)可以意指任何其透明质酸盐,包括但不限于:透明质酸钠(naha)、透明质酸钾、透明质酸镁、透明质酸钙及其组合物。ha及其药学上可接受的盐均可被用于本发明中。一般而言,在一些本发明组合物中,ha的浓度为约10.0mg/g至最高达约17.0mg/g。在一些实施方案中,ha浓度小于约17.0mg/g,例如小于约15.0mg/g。在一些实施方案中,ha浓度为约10.0mg/g至约14.0mg/g。在一些实施方案中,ha浓度为约10.0mg/g、约11.0mg/g、约12.0mg/g、约13.0mg/g或约14.0mg/g。本发明的一些组合物包含额外的试剂,例如,有效量的缓解注射组合物所经受疼痛的麻醉剂。麻醉剂可选自氨布卡因、阿莫拉酮、阿米卡因、丁氧普鲁卡因(benoxinate)、苯佐卡因、贝托卡因、苯柳胺酯(biphenamine)、布比卡因、布他卡因、氨苯丁酯、布坦卡因、丁胺卡因、丁托西卡因(butoxycaine)、卡替卡因(carticaine)、氯普鲁卡因、可卡乙碱(cocaethylene)、可卡因、环美卡因、辛可卡因、二甲异喹(dimethisoquin)、二甲卡因、地哌冬、双环胺(dicyclomine)、去水芽子碱(ecgonidine)、芽子碱(ecgonine)、氯乙烷、依替卡因、β-优卡因、尤普罗辛、非那可明、福莫卡因(formocaine)、海克卡因、羟丁卡因、对氨苯酸异丁酯、甲磺酸亮氨卡因、左沙屈尔、利多卡因、马比佛卡因、美普卡因、美布卡因、氯甲烷、麦替卡因、纳依卡因、奥妥卡因(octocaine)、奥索卡因、奥昔卡因(oxethazaine)、对乙氧卡因、芬那卡因、苯酚、皮珀罗卡因、哌啶卡因、聚多卡醇、普莫卡因、丙胺卡因、普鲁卡因、丙泮卡因、丙美卡因、丙哌卡因、丙氧卡因、假可卡因、吡咯卡因、罗哌卡因、水杨醇、丁卡因、托利卡因、三甲卡因、佐拉敏以及它们的盐。在一个实施方案中,至少一种麻醉剂是利多卡因,例如为盐酸利多卡因的形式。本文所述的组合物的利多卡因浓度可为组合物的约0.1重量%至约5重量%,例如,组合物的约0.2重量%至约1.0重量%。在一个实施方案中,组合物的利多卡因浓度为组合物的约0.3重量%(w/w%)。在一些实施方案中,组合物还包含有益添加剂,例如抗氧化剂。在一些实施方案中,组合物包含例如甘露醇。甘露醇的存在量可为约0.1%w/w至约2.0%w/w,或约0.3%至约0.9%w/w。在一些实施方案中,甘露醇的存在量小于、不大于或约1.0%w/w。在一些实施方案中,甘露醇的存在量为约0.9%w/w。在其它实施方案中,甘露醇的存在量为约0.1%w/w,或约0.2%w/w,或约0.3%w/w,或约0.4%w/w,或约0.5%w/w,或约0.6%w/w,或约0.7%w/w,或约0.8%w/w,或约0.9%w/w,或约1.0%w/w。在其它实施方案中,甘露醇的存在量大于约1.0%w/w。在一些实施方案中,甘露醇的存在量为约1.0%w/w至约5.0%w/w。在一些实施方案中,组合物还包含维生素,例如,维生素c。在一个更优选的实施方案中,该维生素是维生素c的衍生物或维生素c的稳定形式,例如抗坏血酸2-葡糖苷。维生素的存在量可为约0.1%至约2.0%w/w,或约0.2%至约1.0%w/w,或约0.3%至约0.6%w/w。在一些实施方案中,维生素c的存在量为约0.6%w/w。在其它实施方案中,维生素c衍生物的存在量为约0.1%w/w,或约0.2%w/w,或约0.3%w/w,或约0.4%w/w,或约0.5%w/w,或约0.6%w/w,或约0.7%w/w,或约0.8%w/w,或约0.9%w/w,或约1.0%w/w。在其它实施方案中,维生素c衍生物的存在量大于1.0%。在一些实施方案中,维生素c衍生物的存在量为约1.0%w/w至约5.0%w/w。在一些实施方案中,组合物还包含甘露醇和抗坏血酸2-葡糖苷的混合物。在这些实施方案的一些中,甘露醇的存在量不大于1.0%w/w,例如为0.9%w/w,并且抗坏血酸2-葡糖苷的存在量为约0.6%w/w。在一些实施方案中,组合物不包含抗氧化剂或维生素。例如,在一些实施方案中,组合物包含经交联剂交联的透明质酸及水、或基本上由经交联剂交联的透明质酸及水组成。这些组合物可包含或可不包含麻醉剂如利多卡因。本发明的产品和组合物优选以无菌形式提供。组合物可采用常规方法灭菌,例如高压灭菌。例如,可通过将组合物暴露于至少约120℃至约130℃的温度和/或至少约12磅/平方英寸(psi)至约20psi的压力至少约1分钟至约15分钟的时间而将组合物灭菌。制备组合物的方法包括提供干燥ha纤维或粉末形式的原料ha材料的步骤。原料ha材料可以是ha,其盐和/或它们的混合物。在一个优选实施方案中,该ha材料包括naha的纤维或粉末,例如细菌来源的naha纤维。在本说明书的一些方面,该ha材料可以是动物来源的。该ha材料可以是包括ha和至少一种其它多糖如糖胺聚糖(gag)的原料材料的混合物。在本发明的广义方面,组合物的ha材料可包含交联的ha基质,其由约5%至约95%低分子量ha及其余的包含高分子量ha的ha材料制成。在本发明的一些实施方案中,用于制备本发明组合物的ha材料几乎完全包含低分子量ha或由低分子量ha组成。在一些实施方案中,几乎100%的用于制备本发明组合物的ha材料都可以是如上文定义的低分子量ha。在其它实施方案中,用于制备组合物的ha材料包含较高分子量ha和较低分子量ha的混合物,如上文定义的。在某些实施方案中,组合物中至少约50%w/w,例如至少约70%w/w,例如至少约90%w/w或更多的ha材料是如上文定义的低分子量ha,其余部分的ha是高分子量ha。在一个实施方案中,组合物是使用90:10比例的低分子量ha和高分子量ha制成。也就是说,这些实施方案的组合物是由高分子量ha和低分子量ha的混合物制成,其中约90%w/w的ha是低分子量ha。在一个实施方案中,使纯的干燥naha纤维在碱性溶液中与水化合以生成未交联的naha凝胶。在该步骤中可使用任何合适的碱性溶液使naha与水化合,例如,但不限于含有以下物质的水溶液:氢氧化钠(naoh)、氢氧化钾(koh)、碳酸氢钠(nahco3)、氢氧化锂(lioh)等。在另一实施方案中,合适的碱性溶液是含有naoh的水溶液。所得碱性凝胶将具有高于7.5的ph。所得碱性凝胶的ph可为大于9的ph,或大于10的ph,或大于11的ph,或大于12的ph,或大于13的ph。制备方法的下一步包括用合适的交联剂交联该水合的碱性naha凝胶的步骤。交联剂可为已知适于使多糖及其衍生物通过它们的羟基进行交联的任何试剂。适合的交联剂包括但不限于1,4-丁二醇二缩水甘油醚(或1,4-双(2,3-环氧丙氧基)丁烷、或1,4-双缩水甘油基氧基丁烷,其全部通常称为bdde)、1,2-双(2,3-环氧丙氧基)乙烯和1-(2,3-环氧丙基)-2,3-环氧环己烷。本公开内容的范围不排除使用多于一种交联剂或使用不同的交联剂。在一个实施方案中,本文中所述的ha凝胶是使用bdde进行交联。交联步骤可采取本领域普通技术人员已知的任何手段进行。本领域技术人员了解如何根据ha的性质来优化交联条件,以及如何使交联进行至最佳程度。在另一实施方案中,ha的交联在ha纤维的水合过程中完成,其通过使混合的高分子量和低分子量纤维在含有交联剂如bdde的碱性溶液中与水化合而进行。本发明组合物的ha组分的交联度为至少约1%bdde/ha至最高达约20%bdde/ha(w/w),例如约4%至约12%w/w,例如约10%w/w,例如约8%w/w,例如约6%w/w,例如约5%w/w,例如约4%w/w。可以使水合交联的ha凝胶溶胀,以获得所需的ha浓度。该步骤可通过中和交联的水合ha凝胶,例如通过加入含有酸如hcl的水溶液来完成。然后使凝胶在磷酸盐缓冲盐水(pbs)溶液中溶胀。可通过常规方式如对磷酸盐缓冲液透析、或醇沉淀而将凝胶纯化,以回收交联材料、稳定材料的ph并除去任何未反应的交联剂。将组合物混合以达到均匀。优选地,均化步骤包括用可控的剪切力混合、搅拌或拍打凝胶,获得基本均匀的混合物。在一些实施方案中,在混合期间或之后,加入磷酸盐缓冲液,以使在最终的组合物中达到所需的ha浓度。在一些实施方案中,向组合物中加入利多卡因(例如以盐酸利多卡因的形式)或另一合适的麻醉剂。例如,将经纯化的基本上ph中性的凝胶的ph调节至使凝胶变成微碱性,使得凝胶的ph值大于约7.2,例如,约7.5至约8.0。或者,将凝胶调节至使凝胶变成碱性,使得凝胶的ph大于约9,例如约10.0至约11.0。该步骤可通过任何合适的手段来完成,例如通过向凝胶中加入适量的稀的naoh、koh、nahco3或lioh,或本领域技术人员已知的任何其它碱性分子、溶液和/或缓冲组合物。例如,在一些实施方案中,提供粉末形式的盐酸利多卡因,将其用注射用水(wfi)溶解。然后将该利多卡因加入到(微)碱性凝胶中。如果需要,然后可向含利多卡因的凝胶中加入未交联的ha。例如,在一个实施方案中,期望的ha浓度为约12.0mg/g。包含利多卡因的组合物的利多卡因浓度可为组合物的约0.1%至约5重量%,例如约0.3重量%(或w/w),基于组合物的总重量计。包含未交联ha的组合物的未交联ha的浓度可小于10%w/w或小于5%w/w,例如优选为组合物的约0.5重量%至约1.5重量%,例如约0.9至1.0%,基于组合物的总重量计。未交联ha优选具有高分子量。将组合物引入递送装置,例如注射器中。根据本说明书,有用的注射器包括能够递送粘性真皮填充组合物的本领域已知的任何注射器。注射器的内体积可为约0.4ml至约3ml,约0.5ml至约1.5ml或约0.8ml至约1.0ml。在其它实施方案中,将组合物引入适于递送该组合物的注射装置中,采取多次微滴注射进入到较浅的浅表皮肤表面。用于递送本发明组合物的针的规格包括约18g至约40g的规格。在一些实施方案中,用于递送组合物的针为约25g至约33g,例如约31g至约33g,或约32g至约33g。在一些实施方案中,使用28g、29g、30g、32g或33g的规格的针递送组合物。在本发明的另一方面,提供使用本发明组合物处理皮肤的方法。例如,提供改善皮肤的一种或多种质量或改善皮肤外观或纹理的方法。在一个方面,提供处理皮肤干燥、纹理或粗糙、和/或弹性的方法。所述方法一般包括通过向皮肤区域引入组合物的多次间隔隔开的注射来处理皮肤区域,所述组合物包含含有交联ha的透明质酸(ha)凝胶,其中经处理的皮肤因处理带来的改善的水合、更光滑的纹理或增加的弹性维持延长的持续时间,例如至少约3个月至约一年或以上。在一个特别有利的实施方案中,引入步骤仅以单次处理疗程进行,从而消除对重复处理以维持效果持久的需要。在本发明的一个方面,所提供的皮肤处理方法包括在一次处理疗程期间将组合物引入到皮肤中,所述一次处理疗程包括向皮肤区域中多次注射组合物。在一个实施方案中,一次处理疗程包括病人单次到访医师。在该处理疗程期间,可向皮肤,例如向特定皮肤区域中给予多次注射。单次处理疗程的多次注射可包括,例如,2至约500次注射,约50至约200次注射。在一些实施方案中,一次处理疗程包括向皮肤区域中的例如至少2次注射、至少10次注射、至少20次注射、至少40次注射、至少60次注射、至少80次注射、至少100次注射、至少140次注射、至少180次注射、至少200次注射、至少300次注射、至少400次注射、至少500次注射或更多次。在一些实施方案中,处理疗程不超过约45分钟、不超过约30分钟、不超过约15分钟、或不超过约10分钟/每个处理区域。处理区域定义为被本发明组合物和方法处理的皮肤区域。处理区域可包括面部、颈部或胸部(décolletage)中的至少一个皮肤区域,或由面部、颈部或胸部中的至少一个皮肤区域组成。处理区域也可包括除了面部、颈部或胸部之外的皮肤区域,或由除了面部、颈部或胸部之外的皮肤区域组成,例如手、膝盖、肘部、前臂、小腿、大腿、背部的顶部的皮肤区域或任何其它皮肤区域,所述任何其它皮肤区域是可使用本发明组合物和方法处理并从而受益或改善的皮肤区域。在一些实施方案中,引入步骤包括以约2mm至约30mm的距离间隔隔开的注射而引入组合物。例如,引入步骤包括以约5mm至约20mm的距离间隔隔开的注射而引入组合物。在一些实施方案中,引入步骤包括以约10mm至约15mm的距离间隔隔开的注射而引入组合物。在一些实施方案中,在皮肤中的非常浅的深度处提供注射。例如,在一些实施方案中,在不大于约2000微米的深度处引入组合物。例如,在约500微米至约2000微米,约800微米至约1600微米,约1000微米至约1200微米的深度处提供注射。在优选实施方案中,在约0.5mm至约5.0mm、优选约1.0mm至约4.0mm、更优选约1.5mm至约3.0mm的注射深度处引入组合物。在一个实施方案中,以约1μl至约200μl例如约5μl至约100μl每次注射、例如约20μl至约80μl、例如约40μl至约60μl每次注射的量引入注射。在一些实施方案中,以约5μl至约500μl每次注射、约10μl至约400μl、约50μl至约200μl、或约100μl每次注射的量引入注射。在一些实施方案中,注射通过至少27g,例如28g、30g或32g的规格的针递送。有利地,处理方法可包括持续较短时间量的单次处理疗程或由持续较短时间量的单次处理疗程组成。在一些实施方案中,处理疗程覆盖被处理的皮肤区域,包括向皮肤区域中多次皮内注射,并且进行不超过约45分钟。在一些实施方案中,处理疗程不超过约30分钟。在又一些实施方案中,处理疗程不超过约20分钟,或不超过约15分钟,或不超过约10分钟。还提供一种处理皮肤粗糙的方法,其中所述方法包括通过向皮肤区域引入组合物的多次间隔隔开的注射来处理皮肤区域,所述组合物包含含有交联ha的透明质酸(ha)凝胶,其中经处理的皮肤因处理带来的更光滑的纹理维持至少约3个月、至少约4个月、至少约6个月、至少约9个月、或至少约12个月。在一个特定的实施方案中,本发明的组合物包含用1,4-丁二醇二缩水甘油醚(bdde)交联的非动物来源的透明质酸(ha)凝胶的无菌生理溶液,浓度为12mg/ml。该组合物可用于处理浅表皮肤凹陷,以与未经处理的浅表皮肤凹陷相比在皮肤纹理上的改善和皮肤质量如光滑度、水合和弹性的改善作为量度。在一个特定的实施方案中,处理方法包括使用32g的针穿过目标组织区域向真皮内注射,例如积存注射(depotinjection)。目标组织区域包括面部皮肤区域和颈部皮肤区域。病人可以明显注意到与未经处理的皮肤相比皮肤外观的改善,如减少的凹陷、细纹和不均匀或粗糙纹理的外观,并且在仅持续45分钟、或仅30分钟、或仅20分钟、或仅15分钟或更短的单次处理疗程之后,改善可持续至少4个月、6个月、9个月或甚至12个月的时间。皮肤纹理的改善可以使用适当的尺度(scale)来评估。水合和弹性的皮肤质量测量可使用适当的仪器进行,并与基线(即未经处理的皮肤)比较。其他评估方法,例如,faceq和gais可分别用于评定受试者和调查者的满意度。在一个特定的实施方案中,在处理之后产品作用的持续时间为至少约4个月,例如约6个月。在一些实施方案中,在组合物中添加利多卡因可减轻处理区域的疼痛。然而,在一些实施方案中,组合物不包含利多卡因,以解决病人关于利多卡因过敏及疼痛敏感的需要。另一实施方案提供增加皮肤光滑度、水合和弹性中的至少一种的方法,包括在单次处理疗程中,向皮肤区域约500微米至约5000微米深度处引入组合物的多次间隔隔开的注射,所述组合物包含含有经bdde交联的ha和未交联ha的透明质酸(ha)凝胶,其中以约5μl至约100μl每次注射的量引入注射,其中注射通过28g至33g的规格的针递送,其中注射以约5mm至约20mm的距离间隔隔开。在一些实施方案中,皮肤区域因处理带来的增加的光滑度、水合和/或弹性维持至少约3个月、约4个月、约5个月、约6个月、9个月、12个月或更长。在另一实施方案中,提供用于增加皮肤光滑度、水合和弹性中的至少一种的组合物,其包含透明质酸(ha)凝胶,所述透明质酸(ha)凝胶包含由重均分子量约400000da至约800000da的低分子量ha材料制成的交联ha基质;其中组合物的ha浓度为约10.0mg/g至约14.0mg/g;并且其中从以包括组合物的多次间隔隔开的注射的单次处理疗程被引入到皮肤中起,组合物使因处理带来的增加的光滑度、水合和/或弹性维持至少约6个月,其中以约5μl至约100μl每次注射的量引入注射,通过28g至33g的规格的针递送,并且以约5mm至约20mm的距离间隔隔开。皮肤区域因处理带来的增加的光滑度、水合和/或弹性可维持至少约3个月、约4个月、约5个月、约6个月、9个月、12个月或更长。组合物还可包含甘露醇和维生素c中的至少一种。在一些实施方案中,在组合物中既存在甘露醇和又存在维生素c衍生物。如果在0.1hz下测量,组合物具有约50至200pa,例如100-150pa或120pa的凝胶硬度g',如果在5hz下测量,约100至300pa,例如150至200pa或175pa。测量凝胶硬度的方法是本领域已知的。凝胶硬度是真皮填充剂柔软度的指示。此外,如果在0.1hz下测量,组合物具有约10至100pa,例如15-40pa或20pa的凝胶粘度g”,或者如果在5hz下测量,约10至100pa,例如20-40pa或30pa。测量粘度的方法是本领域已知的。组合物还具有约5至20n,例如10-15n或12n的压缩性(compression)。测量压缩性的方法是本领域已知的。压缩性是真皮填充剂的抗变形性的指示。一般而言,压缩性越低,填充剂的可提升展开性(liftspreadibility)越低,即与更适合于较深注射和体积复原的具有较高压缩性的填充剂相比,所述填充剂更适合于处理面部或颈部的浅表细纹和褶皱。实施例1自由基降解测试使得可以评估凝胶样品对ha链被自由基降解(ha的主要降解途径之一)的耐受性。对3个不同批次的本发明组合物进行自由基降解测试。所得结果显示在表1中。发现所有的测量值都是一致的(cvr<10%)。表1本发明组合物的自由基降解结果3个不同批次的批次间差异为约3%,且降解时间平均值为4985s(表2)。表2本发明组合物降解时间的批次间差异实施例2一名37岁的女性在其生命过程中因老化、暴露于干燥的气候和/或太阳/风而表现出粗糙、干燥的面部皮肤。医师通过皮内微-积存注射(micro-depotinjection)给予本文所述的组合物。处理由每个皮肤区域10至约100次浅表注射构成,用32g/4mm的针进行。所处理的皮肤区域为面部、颈部和胸部。从最初注射至最后注射,对患者所有皮肤区域的全部的处理疗程持续约40分钟。各处理区域以间隔隔开的注射接受合适量的组合物。例如,面部区域接受约2ml至约3ml的组合物,通过约每10mm至约15mm的间隔隔开的浅表单次注射而给予。颈部用约1ml至2ml的组合物处理,约每15mm至约20mm间隔隔开地注射。处理之后,通过视觉、触觉和压力感来检验经处理的皮肤区域。处理开始时和结束时进行照相评估。患者向医师报告:处理仅引起极小的不适。处理之后患者立即回到其日常活动中。在其经处理的右手皮肤的一小块区域中,发现了瘀斑,但是这在施用抗炎霜后几天就消散了。在处理之后4个月,病人返回医师处进行随访评价。在随访评价访问之前,患者没有进行进一步的填充剂注射或美索疗法处理(mesotherapytreatments)。在随访访问时的客观检查中,处理已引起表皮纹理改善、干燥度降低并且皮肤亮度提高。通过照片资料部分地证明了这些改善。轻轻触摸经处理的皮肤区域,似乎在水合、柔软度、弹性和色调方面有所增进。通过完成自我评估调查表,患者对处理表示高度满意。患者声称经处理的区域已经改善,并且她对结果非常满意。有趣的是,这些良好的结果基于仅单次处理疗程而实现,在处理疗程和随访访问之间的时间内没有重复注射、“增补(top-up)”或进一步注射处理。实施例3可注射组合物对人存活皮肤外植体的表皮和真皮结构的水合作用通过皮肤湿度(corneometry)测量来评价:使用cm825(courage&khazaka),对角质层最外皮肤层的湿度水平进行测定。的作用原理是基于以冷凝器形式设计的检测器电容的改变。与皮肤接触的测量头的表面,根据皮肤湿度水平,其电容发生改变。在d0(=第0天),以au(任意单位)表示的表皮电容是皮肤水合的指标。测定了根据本公开内容的以下组合物:表3在研究期间,产品是在室温下储存着的。外植体制备:在45岁白种女性的腹部整形术中,制备了9个外植体。在bem培养基(bio-ec’sexplantsmedium)中,在37℃下,在潮湿的5%-co2气氛中使外植体保持存活。将外植体分成3个批次(nb=数目):表4产品应用:用于皮肤湿度测量的c1批次的外植体是用4×10μl的可注射产品进行处理(方形注射),各注射点间隔0.5cm(参见图1)。用于皮肤湿度测量的c2批次的外植体是用4×10μl的可注射产品进行处理(方形注射),各注射点间隔1cm(参见图1)。未经处理的对照未接受任何处理。皮肤湿度:在d0、d2、d7和d9,使用cm825(courage&khazaka)在外植体上进行皮肤水合指标、表皮电容评价。测量是使用1厘米直径的探针,在方形外植体的中心进行的。进行十次测量,并通过皮肤湿度测定仪(corneometer)计算平均值。采样:在d0,收集t0批次的3个外植体,并切成2个部分,一半在-80℃冷冻,一半固定在甲醛中。在d2、d7和d9,收集每批次的3个外植体并以相同的方式处理。统计分析:根据studentt检验进行统计分析。studentt检验给出了两个批次显著不同的概率“p”。如果p<0.05(*)两个批次之间差异显著,那么两个批次95%概率地显著不同;或者如果p<0.01(**),那么两个批次99%概率地显著不同。结果:各批次的皮肤湿度的测量值(也参见图2和3):表5:皮肤湿度数据皮肤湿度测量显示,使用产品pc1,在d2,皮肤表面测量值比t高44.0%**,在d7比t高34.9%**,在d9比t高43.6%**。使用产品pc2,在d2皮肤湿度测量值比t高30.7%*,在d7比t高38.6%**,在d9比t高41.9%**。(studentt检验:*显著性为p<0.05(95%);**显著性为p<0.01(99%))。无论测试条件如何,本公开内容的组合物都显示出良好的水合活性(pc1和pc2分别注射4次,每间隔0.5cm或1cm注射10μl),其诱导表皮电容值极大的增长,这提高了皮肤水合。实施例3本公开内容的可注射组合物对人存活皮肤外植体的表皮和真皮结构的皮肤水合作用是通过额外的皮肤湿度测量而评价的。测定了以下组合物:表6在研究期间,产品是在室温下储存的。外植体制备:对于第一个供体,从一个59岁的白种女性,在腹部整形术中制备9个1.5cm×2cm尺寸的外植体。对于第二个供体,从一个42岁的白种女性,在腹部整形术中制备9个1.5cm×2cm尺寸的外植体。对于第三个供体,从一个52岁的白种女性,在腹部整形术中制备9个1.5cm×2cm尺寸的外植体。对于每个供体,将9个外植体分为如下3个批次:表7产品应用:在d0,用针将3×50μl的产品p1或p2注射到矩形(1.5×2cm)外植体的真皮中。未经处理的对照未接受任何处理。在d1、d2、d5和d7更新一半培养基(1ml)。皮肤湿度:在d0、d1、d2和d8,使用cm825(courage&khazaka)在外植体上进行皮肤水合指标、表皮电容评估。结果:得出三个供体的皮肤湿度测量结果,并表示为三个值的平均值(也参见图4和5):au(皮肤湿度的任意单位)表8对于3个供体,皮肤湿度测量显示,产品p1导致在d1皮肤湿度测量值比在d0增加15%,在d2继续增加到18%,在d8增加到22%。产品p2导致从d0至d1迅速增加37%,并从d2至d8继续增加达49%。根据这些实验条件,并在d8(tj8)与空白批次相比,可以得出以下结论:vstj8p1p2皮肤湿度d8+22%+49%表9总体而言,在本研究的实验条件下,结果表明,在第8天(d8),与产品p1和未经处理的对照t相比,本公开内容的产品(p2)在角质层(stratumcorneum)中显示出增加的皮肤水合作用。虽然已经以一定具体的程度对本发明进行了描述和说明,但应理解,本公开内容仅以示例的方式进行了公开,本领域技术人员可以采取部分、步骤和元素的组合和排列的许多变化,而不背离本发明的范围,如下文所要求保护的。本发明还可由以下实施方案说明:1.一种用于减少皮肤浅表凹陷外观的可注射组合物,所述组合物包含:透明质酸(ha)凝胶,其含有由重均分子量约0.20mda至约0.99mda的低分子量ha材料制成的交联ha基质;其中组合物的ha浓度小于约17.0mg/g;其中组合物从被引入到皮肤中起,维持皮肤浅表凹陷外观的减少至少约3个月。2.第1项的组合物,其中组合物从被引入到皮肤中起,维持皮肤浅表凹陷外观的减少至少约6个月。3.第1项的组合物,其中组合物从被引入到皮肤中起,维持皮肤浅表凹陷外观的减少至少约9个月。4.第1项的组合物,其还包含甘露醇和维生素c衍生物中的至少一种。5.第4项的组合物,其中甘露醇以约0.3%至约0.9%w/w的量存在。6.第4项的组合物,其中维生素c衍生物为抗坏血酸2-葡糖苷。7.第6项的组合物,其中抗坏血酸2-葡糖苷以约0.3%至约0.6%w/w的量存在。8.第1项的组合物,其还包含约0.9%w/w的甘露醇和约0.6%w/w的抗坏血酸2-葡糖苷。9.第1项的组合物,其中低分子量ha材料的重均分子量为约400000da至约800000da。10.第1项的组合物,其中交联ha基质用选自以下的交联剂交联:1,4-丁二醇二缩水甘油醚(bdde)、1,4-双(2,3-环氧丙氧基)丁烷、1,4-双缩水甘油基氧基丁烷、1,2-双(2,3-环氧丙氧基)乙烯和1-(2,3-环氧丙基)-2,3-环氧环己烷。11.第1项的组合物,其中ha浓度为约10.0mg/g至约14.0mg/g。12.第1项的组合物,其中ha浓度为约12.0mg/g。13.一种用于减少皮肤浅表凹陷外观或用于改善皮肤质量的可注射组合物,所述组合物包含:含有交联ha基质的透明质酸(ha)凝胶;甘露醇和维生素c衍生物中的至少一种;其中所述组合物的ha浓度小于约17.0mg/g;其中所述组合物从被引入到皮肤中起,维持皮肤浅表凹陷外观的减少或皮肤质量的改善至少约3个月。14.第13项的组合物,其中组合物从被引入到皮肤中起,维持皮肤浅表凹陷外观的减少或皮肤质量的改善至少约6个月。15.第13项的组合物,其中组合物从被引入到皮肤中起,维持皮肤浅表凹陷外观的减少或皮肤质量的改善至少约9个月。16.第13项的组合物,其中甘露醇以约0.3%至约0.9%w/w的量存在。17.第13项的组合物,其中维生素c衍生物为抗坏血酸2-葡糖苷。18.第17项的组合物,其中抗坏血酸2-葡糖苷以约0.3%至约0.6%w/w的量存在。19.第13项的组合物,其中甘露醇和维生素c衍生物的至少一种包含以约0.9%w/w存在的甘露醇和以约0.6%w/w存在的维生素c衍生物。20.第19项的组合物,其中维生素c衍生物为抗坏血酸2-葡糖苷。21.第13项的组合物,其中ha浓度为约10.0mg/g至约14.0mg/g。22.第13项的组合物,其中ha浓度为约12.0mg/g。23.一种改善皮肤纹理、水合和弹性中的至少一种的方法,所述方法包括:通过在单次处理疗程中向皮肤区域引入组合物的多次间隔隔开的注射来处理皮肤区域,所述组合物包含含有交联ha的透明质酸(ha)凝胶;其中组合物的ha浓度小于约17.0mg/g;其中经处理的皮肤因处理带来的改善的纹理、水合和弹性中的至少一种维持至少约3个月。24.第23项的方法,其中经处理的皮肤因处理带来的改善的纹理、水合和弹性中的至少一种维持至少约6个月。25.第23项的方法,其中经处理的皮肤因处理带来的改善的纹理、水合和弹性中的至少一种维持至少约12个月。26.第23项的方法,其中ha浓度为约10.0mg/g至约14.0mg/g。27.第23项的方法,其中ha浓度为约12.0mg/g。28.第23项的方法,其中注射以约5mm至约20mm的距离间隔隔开。29.第23项的方法,其中注射以约5μl至约100μl每次注射的量引入。30.第23项的方法,其中处理不超过约45分钟。31.第23项的方法,其中注射通过28g至33g的规格的针递送。32.第23项的方法,其中组合物还包含甘露醇和维生素c衍生物中的至少一种。33.第23项的方法,其中甘露醇以约0.3%至约0.9%w/w的量存在。34.第23项的方法,其中维生素c衍生物为抗坏血酸2-葡糖苷。35.第34项的方法,其中抗坏血酸2-葡糖苷以约0.3%至约0.6%w/w的量存在。36.一种增加皮肤光滑性、水合和弹性中的至少一种的方法,包括:在单次处理疗程中向皮肤区域约0.5至约4.0mm或约0.5至约5.0mm深度处引入组合物的多次间隔隔开的注射,所述组合物包含含有bdde-交联ha和未交联ha的透明质酸(ha)凝胶;其中注射以约5μl至约100μl每次注射的量引入;其中注射通过28g至33g的规格的针递送;其中注射以约5mm至约20mm的距离间隔隔开;并且其中皮肤区域因处理带来的增加的光滑性、水合和弹性维持至少约6个月。37.第36项的方法,其中组合物还包含甘露醇和维生素c衍生物中的至少一种。38.一种用于增加皮肤光滑性、水合和弹性中的至少一种的组合物,其包含:透明质酸(ha)凝胶,所述透明质酸(ha)凝胶含有由低分子量ha材料制成的交联ha基质,所述低分子量ha材料的重均分子量为约400000da至约800000da;其中组合物的ha浓度为约10.0mg/g至约14.0mg/g;并且其中从以单次处理疗程向皮肤引入组合物起,组合物因处理带来的增加的光滑性、水合和/或弹性维持至少约6个月,所述单次处理疗程包括组合物的多次间隔隔开的注射,其中注射以约5μl至约100μl每次注射的量引入,通过28g至33g的规格的针递送,并且以约5mm至约20mm的距离间隔隔开。39.第38项的组合物,其中组合物还包含甘露醇和维生素c衍生物中的至少一种。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1